Реактивный артрит патогенез кратко
Обновлено: 04.07.2024
03.11.2014
Клиническая картина реактивного артрита. Этиология и патогенез
Реактивный артрит (РеА) — иммуновоспалительное заболевание суставов, которое возникает одновременно с инфекционным процессом или вскоре после него и является системным клиническим проявлением этой инфекции.
Реактивный артрит (РеА) — иммуновоспалительное заболевание суставов, которое возникает одновременно с инфекционным процессом или вскоре после него и является системным клиническим проявлением этой инфекции.
Заболевание наиболее часто встречается у лиц молодого возраста (20-40 лет), при этом мужчины страдают реактивным артритом значительно чаще, чем женщины. Свыше 85 % больных являются носителями HLA-В27-антигена.
Клинически реактивный артрит проявляется воспалительным процессом в мелких суставах нижних конечностей, который сочетается в некоторых случаях с типичными для спондилоартропатии признаками — энтезопатиями и болями в нижних отделах спины. У некоторых больных наблюдается характерная триада — артрит, конъюнктивит и уретрит, что составляет симптомокомплекс болезни Рейтера. При реактивном артрите могут наблюдаться и системные проявления заболевания — в частности, ирит, изъязвления слизистой оболочки полости рта, кератодермия (keratodermia blenorragica), поражения сердца и нервной системы.
Этиология реактивного артрита.
В отличие от большинства других артритов, этиология которых не установлена, при реактивном артрите существует четкая хронологическая связь с экзогенным провоцирующим фактором, известны генетические маркеры и хорошо изучен клеточный и гуморальный иммунный ответ, развивающийся на причинный антиген.
По этиологическому фактору реактивные артриты подразделяются на две группы: постэнтероколитические и урогенитальные. Среди кишечных патогенов, способных вызвать заболевание, следует выделить иерсинии, сальмонеллы, кампилобактер и шигеллы. Ведущим возбудителем урогенитальных реактивных артритов является Chlamidia trachomatis, которая выявляется у 50-65 % больных. Роль данного микроорганизма при урогенитальных реактивных артритах подтверждается обнаружением его в соскобах эпителия уретры и цервикального канала, выявлением хламидийных антигенов в синовиальной жидкости больных, а также обнаружением ДНК и РНК хламидий в синовиальной оболочке пораженных суставов. При этом Chlamidia trachomatis практически единственный из триггеров реактивного артрита, который выявляется в пораженных суставах больных теми методами исследования, которые подтверждают жизнеспособность микроорганизма, — культуральными и молекулярно-биологическими.
Следует отметить, что за последние десятилетия произошли существенные изменения в составе провоцирующих микроорганизмов. Так, в спорадических случаях реактивного артрита частота инициации болезни хламидией осталась постоянной, в то время как частота возникновения артритов, связанных с перенесенной иерсиниозной инфекцией, снизилась в соответствии со снижением частоты возникновения кишечных инфекций в целом.
Патогенез реактивного артрита.
На сегодняшний день имеется много доказательств, что хламидии и иерсинии способны инициировать цитотоксический Т-клеточный ответ, при этом активация и пролиферация CD8+ Т-лимфоцитов, ответственных за элиминацию причинных микроорганизмов, осуществляемую при участии антигена HLA-B27 и цитокинов, приводит к повреждению синовиальной оболочки. Образующиеся в большом количестве иммунные комплексы фиксируются в суставных тканях, вызывая гиперпродукцию провоспалительных цитокинов (простагландина Е2, интерлейкина-1β, фактора некроза опухолей-α и др.), что приводит к индукции и поддержанию воспалительного процесса в суставах.
О значении генетических факторов в патогенезе реактивного артрита свидетельствует тесная ассоциация с антигеном HLA-B27 (на сегодняшний день известно уже 25 субтипов антигенов — от HLA-B2701 до В2725), который выявляется при урогенитальных РеА в 80-90 % случаев и в 70 % — при постэнтероколитических артритах. Согласно гипотезе антигенной мимикрии, рецепторное сходство между антигеном HLA-B27 и бактериальными пептидами способствует их длительной персистенции в организме пациента и стимуляции выработки антител, направленных против собственных тканей организма, в частности синовиальной оболочки и хрящевой ткани суставов. У пациентов-носителей HLA-B27 антигена определяется низкий уровень элиминации S. typhymurium, при этом он еще более низкий у HLA-B27+ больных реактивным артритом. Некоторые исследователи объясняют этот феномен способностью липополисахаридных компонентов клеточной стенки микроорганизма стимулировать гиперпродукцию ИЛ-10 Т-лимфоцитами, что может способствовать персистенции иммуновоспалительных изменений.
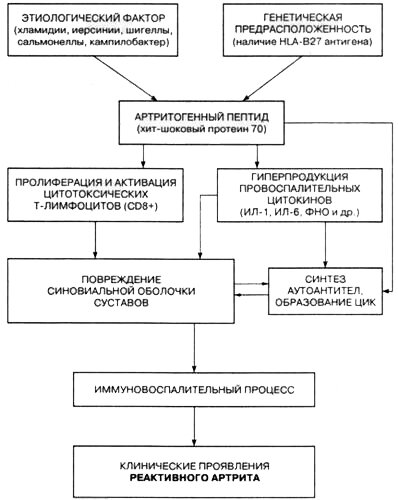
Патогенез реактивного артрита
С практической точки зрения патогенез реактивного артрита можно условно подразделить на три фазы: инициации, острого реактивного артрита и хронического реактивного артрита. В фазе инициации пациент подвергается воздействию патогенных микроорганизмов, что клинически проявляется инфекционным процессом (энтероколит или уретрит) с характерной клинической симптоматикой. У большинства больных происходит полное излечение без каких-либо последствий, однако у некоторых развивается реактивный артрит. Для фазы острого реактивного артрита характерно развитие синовита, а признаки спондилоартропатии развиваются в основном у носителей HLA-В27-антигена. В случае хронического реактивного артрита также возможны клинические различия между пациентами с HLA-B27+ и HLA-B27-, при этом у больных с HLA-B27+ большая вероятность развития рецидивирующих форм заболевания.
Болезни суставов
В.И. Мазуров
Теги:
234567 Начало активности (дата): 03.11.2014 22:09:00
234567 Кем создан (ID): 1
234567 Ключевые слова: артрит
12354567899
Для цитирования: Лила А.М., Гапонова Т.В. Реактивные артриты: особенности патогенеза и терапевтическая тактика. РМЖ. 2010;27:1663.
Литература
1. Лила А.М., Мазуров В.И., Гапонова Т.В. Реактивные артриты / Учебное пособие. – СПб.: издательство СПбМАПО, 2008. – 36 с.
2. Мазуров В.И., Лила А.М., Блохин М.П. Случай группового заболевания синдромом Рейтера у больных, перенесших острую кишечную инфекцию // Терапевт. арх. — 1990. — Т.62, N 12. — C.117–119.
3. Насонов Е.Л. Нестероидные противовоспалительные препараты: новые аспекты применения в ревматологии и кардиологии // Русский медицинский журнал. – 2003. – Т.11, №23. – С.1280–1284.
4. Насонова В.А. Ацеклофенак – безопасность и эффективность // Русский медицинский журнал. – 2003. – Т.11, №5. – С. 3–6.
5. Ahvonen P., Sievers K., Aho K. Arthritis associated with Yersinia enterocolitica infection. Acta Rheum Scand 1969;15:232–253.
6. Bas S., Scieux C., Vischer T.L. Male sex predominance in Chlamydia trachomatis sexually acquired reactive arthritis: are women more protected by anti–chlamydia antibodies? Ann Rheum Dis 2001;60:605–611.
7. Carter J.D., Valeriano J., Vasey F.B. Doxycycline versus doxycycline and rifampin in undifferentiated spondyloarthropathy, with special reference to Chlamydia–induced arthritis. A prospective, randomized 9–month comparison // J. Rheumatol. – 2004. – Vol. 31, № 10. – Р. 1973–1980.
8. Cohen Susanne E., Bodmer Hellen C. Cytotoxic T lymphocytes recognize and lyse chondrocytes under inflammatory, but not non–inflammatory conditions. Immunology 2003;109:8–14.
9. Colbert R.A. HLA–B27 misfolding: a solution to the spondyloarthropathy conudrum? Mol Med Today 2000;6:224–230.
10. El–Shabrawi Y., Mangge H, Hermann J. Anti–tumour necrosis factor and treatment in chronic recurrent inflammation of the anterior segment of the eye in patients resistant to standard immunomodulatory treatment. Ann Rheum Dis 2003;62:1243–1244.
11. Gordon F.B., Quan A.L., Steinman T.I., Philip R.N. Chlamydia isolates from Reiter’s syndrome. Br J Venereal Dis 1973;49:376–379.
12. Hammer M., Nettelnbreker E., Hopf S., Schmitz E., Porshke K., Zeidler H. Chlamidial rRNA in the joints of patients with Chlamydia–induced arthritis and undifferentiated arthritis. Clin Exp Rheumatol 1992;10:63–66.
13. Hannu T., Mattila L., Siitonen A., Leirisalo–Repo M. reactive arthritis attributable to Shigella infection: a clinical and epidemiological nationwide study. Ann Rheum Dis 2005;64:594–598.
14. Henrotin Y., De Leval Х, Mathy–Hartet M et al. In vitro effects of aceclofenac and its metabolites on the production by chondrocytes of inflammatory mediators // Inflamm.Res. – 2001. – Vol. 50. – P. 391–399.
15. Kohnke Susan J. Reactive Arthritis. A Clinical Approach. Orthopaedic Nursing 2004;23:274–280.
16. Kruithof E., F. van den Bosch. Repeated infusions of infliximab, chimeric anti– TNF a monoclonal antibody in patients with active spondyloarthropathy, one year follow up. Ann Rheum Dis 2002;61:207–212.
17. Kvein T.K., Gaston J.S.N., Bardin T., et al. Three month treatment of reactive arthritis with azithromycin: a EULAR double blind, placebo controlled study. Ann Rheum Dis, 2004;63:1113–1119.
18. Laasila K, Laasonen L, Leirisalo–Repo M. Antibiotic treatment and long term prognosis of reactive arthritis. Ann Rheum Dis, 2003;62:655–658.
19. Leirisalo–Repo M. Reactive arthritis // Scand. J. Rheumatol. – 2005. – Vol. 34, № 4. – Р. 251–259.
20. Lidburg P.s., Vojnovic J., Warner T.D. “COX2/COX1 selectivity of aceclofenac in comparison with celecoxib and rofecoxob in the human whole blood assay / Fith world Congress og the OARS, Barselona, Spain, 4–6 October, 2000. – Suppl B, Th053.
21. Mertz Andreas K.N., Wu Peihua, Sturniolo Tiziana, et al. Multispecific CD4+T Cell Response to a Single 12–mer Epitope of the Immunodominant Heat–Shock Protein 60 of Yersinia enterocolitica in Yersinia–Triggered Reactive Arthritis: Overlap with the B27– Restricted CD8 Epitope, Functional Properties, and Epitope Presentation by Multiple DR Alleles. J Immunol 2000;164:1529–1537.
22. Rihl M., Kohler L., Kloss A., Zeidler H. Persistent infection of Chlamydia in reactive arthritis. Ann Rheum Dis 2006;65:281–284.
23. Schumaher H.R. Jr, Arayssi T., Crane M., et al. Chlamydia trachomatis nucleic acids can be found in the synovium of some asymptomatic subjects. Arthritis Rheum 1999;42:1281–1284.
24. Sibilia J., Libmach F–X. Reactive arthritis or chronic infectious arthritis? Ann Rheum Dis 2002;61:580–587.
25. Sieper J. Pathogenesis of reactive arthritis. Curr Rheumatol Rep 2001;3:412–418.
26. Sieper J., Fendler C., Eggens U. et al. Long term antibiotic treatment in reactive arthritis and undifferentiated oligoarthritis: results of a double–blinded placebo–controlled randomized study. Arthritis Rheum 1997;40:S227.
27. Smieja M., MacPherson D.W. et al. Randomised, blinded, placebo–controlled trial of doxycycline for chronic seronegative arthritis. Ann Rheum Dis 2001;60: 1088–1094.
28. Sobao Y., Tsuchiya N., Takiguchi M., et al. Overlapping peptide– binding specificities of HLA–B27 and B39. Arthritis Rheum 1999;42:175–181. Toivanen A. Managing reactive arthritis. Rheumatology 2000;39:117–121.
29. Toivanen A. Managing reactive arthritis. Rheumatology 2000;39:117–121.
30. Yanagawa A., Endo T., Kusakari K. et al. Endoscopie evaluation of aceclofenac–induced gastroduodenal mucosal damage: a double–blind comparison with sodium diclofenac and placebo // J.J.Rheumaco L. – 1998 – Vol. 18. – P. 249–259.
31. Yli–Kerttula T. et al. Effect of a three month course of ciprofloxacin on the late prognosis of reactive arthritis // Ann. Rheum. Dis. – 2003. – Vol. 62, № 9. – Р. 880–884.
Реактивный артрит - воспалительное негнойные заболевание суставов, которое развивается одновременно или после инфекции (не в суставе, а в другом участке тела). Инфекция, вызывающая развитие реактивного артрита, обычно поражает носоглотку, мочевыводящие пути и половые органы, желудочно-кишечного тракт. Обычно артрит развивается через 2-4 недель после возникновения инфекции.
Чаще всего болезнь поражает людей в возрасте от 20 до 40 лет. Мужчины в девять раз чаще женщин заболевают реактивным артритом, связанным с инфекциями, передающимися половым путем (хламидиоз или гонорея), в то время как при пищевых отравлениях реактивный артрит одинаково часто встречается у мужчин и у женщин.
- инфекции мочеполовой системы
- инфекции желудочно-кишечного тракта.
Чаще всего реактивный артрит связан с микроорганизмами, называемыми хламидиями. Обычно хладимии передаются при половых контактах. Часто инфекция не имеет никаких симптомов, а самые частые симптомы (если они присутствуют) - боли или неприятные ощущения при мочеиспускании и выделения из полового члена или влагалища.
Кроме этого, реактивный артрит могут вызывать бактерии, поражающие желудочно-кишечный тракт: сальмонеллы, шигеллы, иерсинии и кампилобактерии. Симптомами поражения желудочно-кишечного тракта являются нарушение стула (жидкий стул). Инфицирование происходит из-за приёма неправильно приготовленной пищи, при контакте с инфицированными людьми или фекалиями (микроорганизма должен попасть в желудочно-кишечный тракт).
Реактивный артрит развивается далеко не у всех людей после перенесённой инфекции. Причины такой избирательности неясны. Показано, что чаще болезнь развивается у людей, имеющих ген - HLA B 27.
Симптомы реактивного артрита
Проявления реактивного артрита могут быть разнообразными. Как правило за 1-4 недели до появления суставных изменений перенес ОРЗ, кишечное расстройство или было учащенное и болезненное мочеиспускание.
Три классических симптома реактивного артрита: воспаление суставов (артрит - боли в суставах, их покраснение, отёк, суставы горячие, подвижность ограничены), воспаление глаз (конъюнктивит - покраснение глаз, чувство жжения в глазах, слезотечение) и воспаление мочевыводящих путей (уретрит - боль, жжение или рези при мочеиспускании; простатит - боли или неприятные ощущения в промежности, неприятные ощущения при мочеиспускании и при дефекации, во время которой могут отмечаться незначительные выделения из мочеиспускательного канала, цистит - частое мочеиспускание, непреодолимые позывы и ощущение жжения или болезненность в нижней части живота во время мочеиспускания, частое мочеиспускание ночью).
Кроме того, на коже ладоней рук и/или подошв ног могут образовываться крошечные, заполненные жидкостью пузырьки, которые иногда наполняются кровью. Пораженная кожа может шелушиться и напоминать псориаз.
В ротовой полости могут образоваться изъязвления на твердом, мягком небе, языке. Они могут быть не замечены пациентом, так как часто безболезненны.
В большинстве случаев симптомы конъюнктивита и уретрита выражены очень слабо и воспалены лишь 1-2 сустава. У некоторых пациентов, однако, реактивным артрит может быть острым и тяжёлым, ограничивать их физическую активность.
- развитие заболевания у лиц молодого возраста (до 30-40 лет), преимущественно мужчин
- хронологическая связь с урогенитальной или кишечной инфекцией (во время или спустя 2-6 нед)
- негнойный артрит с выраженной асимметрией и предпочтительной локализацией в суставах нижних конечностей с частым вовлечением в процесс сухожильно-связочного аппарата и бурс (ахиллобурсит, подпяточный бурсит и т. д.)
- внесуставные проявления (поражение кожи, ротовой полости, половых органов)
- серонегативность (отсутствие в сыворотке крови ревматоидного фактора);
- частая ассоциация артрита с наличием у больных антигена НLА-В27;
- частое вовлечение в воспалительный процесс крестцово-подвздошных сочленений и позвоночника;
- выявление бактериологическими, серологическими и иммунологическими методами микроорганизмов, ответственных за развитие реактивного артрита или их антигенов.
Лечение реактивного артрита должно быть индивидуальным и в условиях стационара, так как развитие его может быть связано с различными инфекциями. Целью терапии является устранение инфекции, излечение или устранение прогрессирования болезни.
Если сохраняются признаки активной инфекции, то оправдано назначение антибиотиков (выбор антибактериальных средств определяется возбудителем инфекции), чтобы устранить бактерии и убрать первопричину воспаления.
Нестероидные противовоспалительные препараты уменьшают боль и воспаление суставов.
При тяжёлом воспалении суставов иногда выполняют инъекции глюкокортикостероидов непосредственно в воспаленный сустав.
Во время активного воспаления сустав следует избегать нагрузок. Однако после купирования воспаления рекомендовано постепенное восстановление физической активности.
Прогноз
В большинстве случаев прогноз реактивного артрита благоприятен, полное выздоровление в течение 6-12 месяцев наблюдается у 80 % пациентов. Лишь у небольшого процента пациентов симптомы могут вернуться или состояние может носить хронический характер.
-
— круглосуточно. — понедельник-пятница, с 08:00 до 21:00; суббота, с 09:00 до 18:00; воскресенье, с 09:00 до 18:00.
В летний период: понедельник-пятница, с 08:00 до 21:00; суббота, с 09:00 до 18:00; воскресенье, с 09:00 до 15:00.
В летний период: понедельник-пятница, с 08:00 до 21:00; суббота, с 09:00 до 18:00; воскресенье, с 09:00 до 15:00.
Информационно-образовательнный портал
для врачей при поддержке ведущих
медицинских вузов Санкт-Петербурга
Информационно-
образовательнный
портал для врачей
Реактивные артриты: особенности патогенеза и терапевтическая тактика
Санкт–Петербургская медицинская академия последипломного образования, Клиническая ревматологическая больница № 25, Санкт–Петербург
Профессор А.М. Лила, Т.В. Гапонова
Вместе с тем уже в 70–80–х годах XX века в биоптатах синовиальной оболочки методами световой и электронной микроскопии с применением иммуноцитохимии были обнаружены микроскопи-ческие внутриклеточные включения Chlamidia trachomatis, впоследствии признанной наиболее значимым артритогенным микроорганизмом при РеА [11]. С внедрением в клиническую практику в начале 90–х годов метода обратной транскриптазо–полимеразной цепной реакции (ОТ–ПЦР) в полости сустава были обнаружены небольшие количества ДНК и РНК Ch.trachomatis. Наличие этих нуклеиновых кислот, которые имеют очень непродолжительное время жизни в тканях (несколько минут), свидетельствовало о возможности транскрипции и, следовательно, активного размножения бактерий в полости сустава[12].
Позднее было обнаружено, что сустав и в норме не является стерильной средой [23]. Так, ДНК различных микроорганизмов была обнаружена в биоптатах синовиальной оболочки здоровых людей и больных остеоартрозом (у 9 и 20% соответственно).
Активно изучаются генетические факторы в патогенезе РеА. В частности, доказана тесная ассоци-ация заболевания с антигеном HLA–B27. Существует несколько точек зрения о его роли в развитии РеА. Согласно одной из них антиген HLA–B27 является антигенпрезентирующей молекулой, способной представлять артритогенные пептиды цитотоксическим CD8 Т–лимфоцитам [24]. Объектом лизиса при этом, вероятно, являются хондроциты, локализующиеся как в хрящевой ткани, так и в энтезисах, где также развивается воспалительный процесс [8]. По мнению Y. Sobao исоавт. (1999), для некоторых бактерий (Yersinia, Salmonella) наличие HLA–B27 является фактором, существенно облегчающим их инвазию в клетки синовиальной оболочки [28].
Известно, что важную роль в эрадикации инфекционных агентов, особенно в случае с внутри-клеточными бактериями, играют провоспалительные цитокины Th1 типа, такие как интерферон гамма (ИФ–γ) и фактор некроза опухоли–альфа (ФНО–α). В многочисленных исследованиях было показано, что при РеА антибактериальный Тh1–иммунный ответ (продукция ИФ–γ, ФНО–α, ИЛ–2 и ИЛ–12) снижен в пользу Th2–иммунного ответа (синтез ИЛ–4 и ИЛ–10) [21]. Так возникла наибо-лее распространенная в настоящее время гипотеза патогенеза РеА, предложенная J. Sieper (2001), в основе которой лежит дисбаланс цитокинов [25]. По мнению автора, активные мононуклеарныеклетки синовиальной жидкости больных РеА переключаются на Th2–иммунный ответ с низкой продукцией ИФ–γ и ФНО–α и гиперпродукцией ИЛ–4, что способствует длительной персистенции бактерий в синовиальной оболочке и полости сустава. В частности, S. Bas и соавт. (1999) подтвердили низкую продукцию антител у мужчин, больных РеА, что, по их мнению, указывало на провоспалительный Th1 тип иммунного ответа и могло способствовать индукцииартрита [6].
Вместе с тем, несмотря на большое количество проведенных исследований, посвященных изучению механизмов развития реактивного артрита, окончательный ответ на этот вопрос до настоящего времени не сформулирован, что, естественно, отражается и на эффективности терапии данного заболевания.
Клинические проявления РеА
Продолжительность первичных случаев РеА составляет в среднем 3–6 месяцев, однако часто клинические симптомы заболевания сохраняются до 12 месяцев и более. При урогенитальном РеА, особенно у пациентов с синдромом Рейтера, отмечается склонность к более частому рецидивированию заболевания, что объясняется как возможностью реинфицирования, так и персистирующей хламидийной инфекцией. Рецидивы, как правило, протекают с суставным синдромом, поражением глаз, кожи, слизистых оболочек и уретритом. Характер течения заболевания отличается большим разнообразием, у многих пациентов развивается стойкая ремиссия, вместе с тем в 12–15% случаев РеА приобретает хроническое течение [15].
Лечение РеА
Комплексная терапия РеА включает применение нестероидных противовоспалительных препаратов (НПВП), глюкокортикоидов (в некоторых случаях), медленно действующих болезнь–модифицирующих препаратов (базисных средств) при затяжных и хронических вариантах течения заболевания, а также биологических агентов. Отдельное место в лечении РеА занимает антибактериальная терапия.
Одним из серьезных побочных эффектов НПВП, ограничивающих их применение, является развитие НПВП–индуцированных гастропатий, проявляющихся эрозиями (часто множественными) и язвами антрального отдела желудка. Основными факторами риска развития НПВП–гастропатии являются пожилой возраст больных, наличие в анамнезе язвенной болезни, желудочно–кишечного кровотечения или мелены, длительный прием высоких доз НПВП, прием одновременно НПВП и препаратов других фармакологических групп (антикоагулянтов и др.) [3]. Данные многочисленных клинических исследований свидетельствуют о том, что частота возникновения неблагоприятных явлений со стороны органов ЖКТ при приеме подавляющего большинства неселективных НПВП достигает 30%, а госпитализация пациентов пожилого возраста из–за развития пептической язвы в 4 раза выше по сравнению с лицами той же возрастной группы, не принимающих НПВП.
В этой связи представляет интерес исследование А. Yanagawa и соавт. (1998), в котором изучалось возможное побочное действие ацеклофенака и диклофенака на слизистую оболочку 12–перстной кишки [30]. Было установлено, что эндоскопические изменения после 2–недельного приема ацеклофенака, диклофенака и плацебо достоверно чаще наблюдались в группе диклофенака. При этом у пациентов, получавших диклофенак, содержание гексозамина (фактора, оказывающего цитопротективное действие) и локальный кровоток в слизистой оболочке желудка и 12–перстной кишки были значимо снижены, в то время как при лечении ацеклофенаком эти показатели достоверно не отличались от группы плацебо.
В последние годы с появлением генно–инженерных биологических препаратов они начали активно назначаться больным с серонегативными спондилоартропатиями. В немногочисленных публикациях приведены сведения об эффективности инфликсимаба и у больных РеА, назначаемого при низком эффекте традиционных иммуносупрессантов [10,16].
В настоящее время антибактериальная терапия назначается больным РеА с доказанной хламидийной инфекцией с учетом чувствительности причинных микроорганизмов. Применяются антибиотики тетрациклинового ряда – доксициклин по 0,3 г/сут., фторхинолоны – ципрофлоксацин – 0,5 г/сут., ломе флоксацин – 0,8 г/сут., из группы макролидов эффективен кларитромицин – 0,5 г/сут. [7]. Применение антибиотиков из группы пенициллинов при РеА хламидийной этиологии противопоказано, так как они могут способствовать переводу хламидий в L–формы, весьма устойчивые к антибактериальной терапии. При лечении урогенитальных РеАбольшинство исследователей отдают предпочтение длительной антибактериальной терапии (до 28 дней и более) [17,18,22,27].
Результаты многоцентровых исследований свидетельствуют о вероятной неэффективности антибактериальной терапии у больных постэнтероколитическими РеА, хотя этот вопрос нельзя считать окончательно решенным [26,29].
Таким образом, существующее многообразие предлагаемых к лечению антибактериальных препаратов, а также попытки разработать новые схемы терапии свидетельствуют об отсутствии в настоящее время единой стратегии в этом вопросе и требуют дальнейшего изучения.
Читайте также:

