Переваривание жиров кратко и понятно
Обновлено: 05.07.2024
Расщепление триглицеридов в желудке взрослого человека невелико, но оно в определенной степени облегчает последующее переваривание их в кишечнике. Даже незначительное по объему расщепление триглицеридов в желудке приводит к появлению свободных жирных кислот, которые, не подвергаясь всасыванию в желудке, поступают в кишечник и способствуют там эмульгированию жиров, облегчая таким образом воздействие на них липазы панкреатического сока.
После того как химус попадает в двенадцатиперстную кишку, прежде всего происходит нейтрализация попавшей в кишечник с пищей соляной кислоты желудочного сока бикарбонатами, содержащимися в панкреатическом и кишечном соках. Выделяющиеся при разложении бикарбонатов пузырьки углекислого газа способствуют хорошему перемешиванию пищевой кашицы с пищеварительными соками. Одновременно начинается эмульгирование жира. Наиболее мощное эмульгирующее действие на жиры оказывают соли желчных кислот, попадающие в двенадцатиперстную кишку с желчью в виде натриевых солей. Большая часть желчных кислот конъюгирована с глицином или таурином. По химической природе желчные кислоты являются производными холановой кислоты:
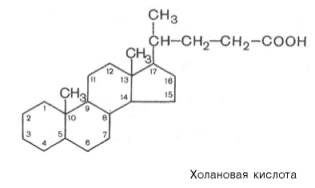
Желчные кислоты представляют собой основной конечный продукт метаболизма холестерина.
В желчи человека в основном содержатся холевая (3,7,12-триоксихола-новая), дезоксихолевая (3,12-диоксихолановая) и хенодезоксихолевая (3,7-диоксихолановая) кислоты (все гидроксильные группы имеют α-конфи-гурацию и поэтому обозначены пунктирной линией):
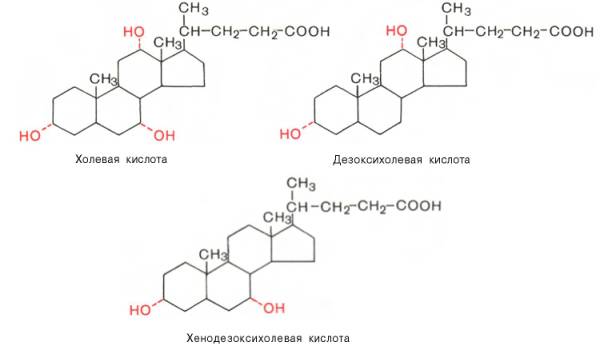
Кроме того, в желчи человека в малых количествах содержатся лито-холевая (3α-оксихолановая) кислота, а также аллохолевая и уреодезокси-холевая кислоты – стереоизомеры холевой и хенодезоксихолевой кислот.
Как отмечалось, желчные кислоты присутствуют в желчи в конъюги-рованной форме, т.е. в виде гликохолевой, гликодезоксихолевой, гли-кохенодезоксихолевой (около 2 /3 – 4 /5 всех желчных кислот) или таурохо-левой, тауродезоксихолевой и таурохенодезоксихолевой (около 1 /5 – 1 /3 всех желчных кислот) кислот. Эти соединения иногда называют парными желчными кислотами, так как они состоят из двух компонентов – желчной кислоты и глицина или таурина. Соотношения между конъюгатами обоих видов могут меняться в зависимости от характера пищи: в случае преобладания в ней углеводов увеличивается относительное содержание глициновых конъюгатов, а при высокобелковой диете – тауриновых конъюгатов. Строение парных желчных кислот может быть представлено в следующем виде:

Считают, что только комбинация соль желчной кислоты + ненасыщенная жирная кислота + моноглицерид придает необходимую степень эмульгирования жира. Соли желчных кислот резко уменьшают поверхностное натяжение на поверхности раздела жир/вода, благодаря чему они не только облегчают эмульгирование, но и стабилизируют уже образовавшуюся эмульсию.
Известно, что основная масса пищевых глицеридов подвергается расщеплению в верхних отделах тонкой кишки при действии липазы панкреатического сока. Этот фермент был впервые обнаружен известным французским физиологом С. Bernard в середине прошлого века.
Панкреатическая липаза (КФ 3.1.1.3) является гликопротеидом, имеющим мол. массу 48000 (у человека) и оптимум рН 8–9. Данный фермент расщепляет триглицериды, находящиеся в эмульгированном состоянии (действие фермента на растворенные субстраты значительно слабее). Как и другие пищеварительные ферменты (пепсин, трипсин, химотрипсин), панкреатическая липаза поступает в верхний отдел тонкой кишки в виде неактивной пролипазы.
Превращение пролипазы в активную липазу происходит при участии желчных кислот и еще одного белка панкреатического сока – колипазы (мол. масса 10000). Последняя присоединяется к пролипазе в молекулярном соотношении 2:1. Это приводит к тому, что липаза становится активной и устойчивой к действию трипсина.
Установлено, что основными продуктами расщепления триглицеридов при действии панкреатической липазы являются β(2)-моноглицерид и жирные кислоты. Фермент катализирует гидролиз эфирных связей в α(1), α'(3)-положениях, в результате чего и образуются β(2)-моноглицерид и две частицы (молекулы) жирной кислоты. На скорость катализируемого липазой гидролиза триглицеридов не оказывает существенного влияния ни степень ненасыщенности жирных кислот, ни длина ее цепи (от С12 до С18).
Гидролиз триглицеридов при участии панкреатической липазы можно изобразить в виде следующей схемы:
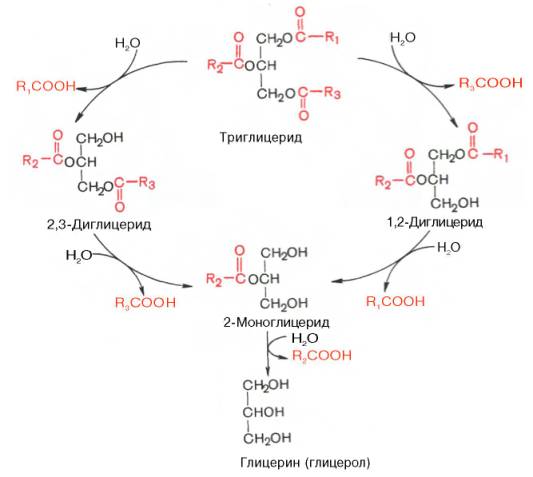
В панкреатическом соке наряду с липазой содержится моноглицеридная изомераза – фермент, катализирующий внутримолекулярный перенос ацила из β(2)-положения моноглицерида в α(1)-положение. В процессе переваривания пищевых жиров при участии этого фермента примерно треть β-моноглицерида превращается в α-моноглицерид. Поскольку эфирная связь в α-положении чувствительна к действию панкреатической липазы, последняя расщепляет большую часть α-моноглицеридов до конечных продуктов – глицерина и жирной кислоты. Меньшая часть α-моноглице-ридов успевает всосаться в стенку тонкой кишки, минуя воздействие липазы.
Всасывание триглицеридов и продуктов их расщепления. Всасывание происходит в проксимальной части тонкой кишки. Тонкоэмульгированные жиры (величина жировых капель эмульсии не должна превышать 0,5 мкм) частично могут всасываться через стенки кишечника без предварительного гидролиза. Основная часть жира всасывается лишь после расщепления его панкреатической липазой на жирные кислоты, моноглицериды и глицерин. Жирные кислоты с короткой углеродной цепью (менее 10 атомов углерода) и глицерин, будучи хорошо растворимыми в воде, свободно всасываются в кишечнике и поступают в кровь воротной вены, оттуда в печень, минуя какие-либо превращения в кишечной стенке.
Более сложно происходит всасывание жирных кислот с длинной углеродной цепью и моноглицеридов. Этот процесс осуществляется при участии желчи и главным образом желчных кислот, входящих в ее состав. В желчи соли желчных кислот, фосфолипиды и холестерин содержатся в соотношении 12,5:2,5:1,0. Жирные кислоты с длинной цепью и моноглицериды в просвете кишечника образуют с этими соединениями устойчивые в водной среде мицеллы. Структура мицелл такова, что их гидрофобное ядро (жирные кислоты, моноглицериды и др.) оказывается окруженным снаружи гидрофильной оболочкой из желчных кислот и фосфолипидов. Мицеллы примерно в 100 раз меньше самых мелких эмульгированных жировых капель. В составе мицелл высшие жирные кислоты и моноглицериды переносятся от места гидролиза жиров к всасывающей поверхности кишечного эпителия. Относительно механизма всасывания жировых мицелл единого мнения нет. Одни исследователи считают, что в результате так называемой мицеллярной диффузии, а возможно, и пиноцитоза мицеллы целиком проникают в эпителиальные клетки ворсинок, где происходит распад жировых мицелл. При этом желчные кислоты сразу поступают в ток крови и через систему воротной вены попадают сначала в печень, а оттуда вновь в желчь. Другие исследователи допускают возможность перехода в клетки ворсинок только липидного компонента жировых мицелл. Соли желчных кислот, выполнив свою физиологическую роль, остаются в просвете кишечника; позже основная масса их всасывается в кровь (в подвздошной кишке), попадает в печень и затем выделяется с желчью. Таким образом, все исследователи признают, что происходит постоянная циркуляция желчных кислот между печенью и кишечником. Этот процесс получил название печеночно-кишечной (гепатоэнтеральной) циркуляции.
С помощью метода меченых атомов было показано, что в желчи содержится лишь небольшая часть желчных кислот (10–15% от общего количества), вновь синтезированных печенью. Таким образом, основная масса желчных кислот (85–90%) – это желчные кислоты, реабсорбирован-ные в кишечнике и повторно секретируемые в составе желчи. Установлено, что у человека общий пул желчных кислот составляет примерно 2,8–3,5 г, при этом они совершают 6–8 оборотов в сутки.
Расщепление и всасывание фосфолипидов и холестерина. Подавляющая часть фосфолипидов содержимого тонкой кишки приходится на фосфати-дилхолин (лецитин), основная масса которого поступает в кишечник с желчью (11–12 г/сут) и меньшая часть (1–2 г/сут) – с пищей.
Существует две точки зрения относительно судьбы поступивших в тонкую кишку экзогенных и эндогенных фосфолипидов. Согласно одной из них, и те, и другие фосфолипиды подвергаются в кишечнике атаке со стороны фосфолипазы А2, катализирующей гидролиз сложноэфирной связи в β-положении. В результате катализируемой фосфолипазой А2 реакции глицерофосфолипиды расщепляются с образованием лизофосфолипида и жирной кислоты. Лизофосфолипид может подвергаться расщеплению при действии другого фермента панкреатического сока – лизофосфолипазы. В результате из лизолецитина освобождается последняя частица жирной кислоты и образуется глицерофосфохолин, который хорошо растворяется в водной среде и всасывается из кишечника в кровь.
В зависимости от пищи организм взрослого человека получает ежедневно 300–500 мг холестерина, содержащегося в пищевых продуктах частично в свободном (неэстерицифицированном) виде, частично в виде эфиров с жирными кислотами. Эфиры холестерина расщепляются на холестерин и жирные кислоты особым ферментом панкреатического и кишечного соков – гидролазой эфиров холестерина, или холестеролэстеразой (КФ 3.1.1.13). В тонкой кишке происходит всасывание холестерина, источником которого являются:
– холестерин пищи (0,3–0,5 г/сут; у вегетарианцев значительно меньше); – холестерин желчи (ежедневно с желчью выделяется 1–2 г эндогенного неэстерифицированного холестерина);
– холестерин, содержащийся в слущенном эпителии пищеварительного тракта и в кишечных соках (до 0,5 г/сут).
В общей сложности в кишечник поступает 1,8–2,5 г эндогенного и экзогенного холестерина. Из этого количества около 0,5 г холестерина выделяется с фекалиями в виде восстановленного продукта – копростерина и очень небольшая часть в виде окисленных продуктов – холестенона и др. И восстановление, и окисление холестерина происходят в толстой кишке под воздействием ферментов микробной флоры. Основная часть холестерина в неэстерифицированной форме подвергается всасыванию в тонкой кишке в составе смешанных жировых мицелл, состоящих из желчных кислот, жирных кислот, моноглицеридов, фосфолипидов и лизофосфо-липидов.
Ресинтез липидов в кишечной стенке. Триглицериды. По современным представлениям, ресинтез триглицеридов происходит в эпителиальных
клетках (энтероцитах слизистой оболочки ворсинок тонкой кишки) двумя путями. Первый путь – β-моноглицеридный. Долгое время этот путь считался единственным. Суть его состоит в том, что β-моноглицериды и жирные кислоты, проникающие в процессе всасывания в эпителиальные клетки кишечной стенки, задерживаются в гладком эндоплазматическом рети-кулуме клеток. Здесь из жирных кислот образуется их активная форма – ацил-КоА и затем происходит ацилирование β-моноглицеридов с образованием сначала диглицеридов, а затем триглицеридов:
β-Моноглицерид + R—СО—S-KoA –> Диглицерид + HS-KoA ;
Диглицерид + R1—СО—S-KoA –> Триглицерид + HS-KoA.
Все реакции катализируются ферментным комплексом – триглицерид-синтетазой, включающим в себя ацил-КоА-синтетазу, моноглицеридацил-трансферазу и диглицеридацилтрансферазу.
Второй путь ресинтеза триглицеридов протекает в шероховатом эндо-плазматическом ретикулуме эпителиальных клеток и включает следующие реакции:
1) образование активной формы жирной кислоты – ацил-КоА при участии ацил-КоА-синтетазы;
2) образование α-глицерофосфата при участии глицеролкиназы;
3) превращение α-глицерофосфата в фосфатидную кислоту при участии глицерофосфат-ацилтрансферазы;
4) превращение фосфатидной кислоты в диглицерид при участии фос-фатидат-фосфогидролазы;
5) ацилирование диглицерида с образованием триглицерида при участии диглицеридацилтрансферазы.
Как видно, первая и последняя реакции повторяют аналогичные реакции β-моноглицеридного пути. Установлено, что α-глицерофосфатный путь ресинтеза жиров (триглицеридов) приобретает значение, если в эпителиальные клетки слизистой оболочки тонкой кишки поступили преимущественно жирные кислоты. В случае, если в стенку кишки поступили жирные кислоты вместе с β-моноглицеридами, запускается β-моногли-церидный путь. Как правило, наличие в эпителиальных клетках избытка β-моноглицеридов тормозит протекание α-глицерофосфатного пути.
Ресинтез фосфолипидов в кишечной стенке. В энтероцитах наряду с ре-синтезом триглицеридов происходит также и ресинтез фосфолипидов. В образовании фосфатидилхолинов и фосфатидилэтаноламинов участвует ресинтезированный диглицерид, а в образовании фосфатидилинозитолов – ресинтезированная фосфатидная кислота. Участие этих субстратов в образовании фосфолипидов в стенке кишечника происходит по тем же закономерностям, что и в других тканях (см. с. 396, 397).
Необходимо подчеркнуть, что в стенке кишечника синтезируются жиры, в значительной степени специфичные для данного вида животного и отличающиеся по своему строению от пищевого жира. В известной мере это обеспечивается тем, что в синтезе триглицеридов (а также фосфолипидов) в кишечной стенке принимают участие наряду с экзогенными и эндогенные жирные кислоты. Однако способность к осуществлению в стенке кишечника синтеза жира, специфичного для данного вида животного, все же ограничена. Показано, что при скармливании животному (например, собаке), особенно предварительно голодавшему, больших количеств чужеродного жира (например, льняного масла или верблюжьего жира) часть его обнаруживается в жировых тканях животного в неизмененном виде. Жировая ткань скорее всего является единственной тканью, где могут откладываться чужеродные жиры. Липиды, входящие в состав протоплазмы клеток других органов и тканей, отличаются высокой специфичностью, их состав и свойства мало зависят от пищевых жиров.
Образование хиломикронов и транспорт липидов. Ресинтезированные в эпителиальных клетках кишечника триглицериды и фосфолипиды, а также поступивший в эти клетки из полости кишечника холестерин (здесь он может частично эстерифицироваться) соединяются с небольшим количеством белка и образуют относительно стабильные комплексные частицы – хиломикроны (ХМ). Последние содержат около 2% белка, 7% фосфолипидов, 8% холестерина и его эфиров и более 80% триглицеридов. Диаметр ХМ колеблется от 0,1 до 5 мкм. Благодаря большим размерам частиц ХМ не способны проникать из эндотелиальных клеток кишечника в кровеносные капилляры и диффундируют в лимфатическую систему кишечника, а из нее – в грудной лимфатический проток. Затем из грудного лимфатического протока ХМ попадают в кровяное русло, т.е. с их помощью осуществляется транспорт экзогенных триглицеридов, холестерина и частично фосфолипидов из кишечника через лимфатическую систему в кровь. Уже через 1–2 ч после приема пищи, содержащей жиры, наблюдается алиментарная гиперлипемия. Это физиологическое явление, характеризующееся в первую очередь повышением концентрации триглицеридов в крови и появлением в ней ХМ. Пик алиментарной гиперлипемии наблюдается через 4–6 ч после приема жирной пищи. Обычно через 10–12 ч после приема пищи содержание триглицеридов возвращается к нормальным величинам, а ХМ полностью исчезают из кровяного русла.
Известно, что печень и жировая ткань играют наиболее существенную роль в дальнейшей судьбе ХМ. Последние свободно диффундируют из плазмы крови в межклеточные пространства печени (синусоиды). Допускается, что гидролиз триглицеридов ХМ происходит как внутри печеночных клеток, так и на поверхности. ХМ не способны (из-за своих размеров) проникать в клетки жировой ткани. В связи с этим триглицериды ХМ подвергаются гидролизу на поверхности эндотелия капилляров жировой ткани при участии фермента липопротеидлипазы.

Среднее потребление жиров(масло животное и растительное, маргарин, молоко, мясо, сосиски, яйца, орехи и т. д.) составляет примерно 60-100 г в сутки, но существуют большие индивидуальные вариации (10-250 г в сутки). Большинство жиров в пище (90%) - это нейтральные жиры, или триацилглицериды (триглицериды). Остальные жиры -это фосфолипиды, эфиры холестерина и жирорастворимые витамины (витамин A, D, Е и К). Более 95% липидов обычно всасываются в тонком кишечнике.
Переваривание жиров (А). Липиды плохо растворяются в воде, и поэтому для их переваривания в водной среде желудочно-кишечного тракта и для последующего всасывания и транспорта в плазму крови требуются специальные механизмы. Хотя недеградированные триацилглицериды могут всасываться в небольших количествах, жиры пищи должны быть гидролизованы ферментами перед тем, как они смогут эффективно всосаться. Для оптимальной ферментативной активности требуется предварительная механическая эмульгация жиров (в основном в дистальной части желудка), поскольку липидные капли в эмульсии (1-2 мкм; Б1) имеют гораздо большую (относительную к массе жиров) поверхность для работы липаз.

Липазы - ферменты, растворяющие жиры, вырабатываются железами языка, дна желудка (главные клетки и слизистые клетки шейки) и поджелудочной железы (А). Примерно 10-30% пищевых жиров гидролизуется в желудке, а остальные 70-90% расщепляется в двенадцатиперстной кишке и верхней части тощей кишки. Липазы из языка и желудка имеют кислый оптимум pH, а липазы поджелудочной железы - pH 7-8. Липазы становятся активными в области контакта жира (масла) с водой (Б). Панкреатическая липаза (триацилглицеролгидролаза) проявляет липолитическую активность (максимальная скорость липолиза 140 г жира/мин) в присутствии колипаз и Са 2+ . Проколипазы из сока поджелудочной железы, будучи активированы трипсином, образуют липазы. В большинстве случаев панкреатические липазы расщепляют триацилглицериды (ТГ) по первой и третьей сложноэфирной связи. Этот процесс требует присутствия воды и приводит к образованию свободных жирных кислот (СЖК) и 2-моно-ацилглицерида.
При этом вокруг фермента формируется вязко-однородная фаза с водной и гидрофобной зонами (Б2). Избыток Са 2+ или дефицит моноацилглицерида приводит к превращению жирных кислот в кальциевые мыла, которые потом выводятся.
Фосфолипаза А2 (образуется из профосфолипазы А3 панкреатического сока при активации трипсином) расщепляет вторую сложноэфирную связь фосфолипидов (в основном фосфатидилхолина = лектина), содержащихся в мицеллах. Для этой реакции требуется присутствие желчных солей и Са 2+ .
Неспецифичная карбоксилэстераза (= неспецифичная липаза = гидролаза эфиров холестерина) из панкреатического секрета воздействует на эфиры холестерина в мицеллах, а также на все три эфирные связи ТГ и эфирные связи витаминов A, D, Е.
Эта липаза также присутствует в женском грудном молоке (но не в коровьем), и поэтому вскормленные грудью младенцы получают пищеварительные ферменты, требующиеся для расщепления молочного жира вместе с молоком матери. Поскольку ферменты чувствительны к теплу, пастеризация грудного молока значительно уменьшает способность младенцев переваривать молочные жиры.
2-Моноацилглицериды, длинноцепочечные свободные жирные кислоты и другие липиды агрегируют с желчными кислотами и спонтанно формируют мицеллы в тонком кишечнике (БЗ). (Поскольку короткоцепочечные жирные кислоты более полярны, они могут всасываться непосредственно и не нуждаются в желчных кислотах или мицеллах.) Диаметр мицелл составляет всего 20-50 нм, отношение поверхность/объем у них примерно в 50 раз больше, чем у липидных капель в эмульсии. Они облегчают плотный контакт между продуктами расщепления жиров и стенкой тонкого кишечника и, следовательно, важны для всасывания липидов. Полярный конец участвующих в процессе веществ (в основном конъюгированных желчных кислот, 2-моноацилглицерида и фосфолипидов) обращен в водную среду, а неполярная - внутрь мицелл. Полностью неполярные липиды (например, эфиры холестерина, жирорастворимые витамины и липофильные яды) находятся внутри мицелл. Таким образом, неполярные липиды во время всех этих процессов остаются в липофильном окружении до тех пор, пока не достигают липофильной щеточной каймы (микроворсинок) мембран эпителия. Там они абсорбируются клетками слизистой путем либо растворения в мембране, либо пассивного транспорта (например, в случае свободных жирных кислот при помощи переносчиков). Хотя всасывание жиров завершается к тому моменту, когда химус достигает конца тощей кишки, желчные кислоты, высвобождающиеся из мицелл, абсорбируются только в конце подвздошной кишки и затем рециркулируют (внутрипеченочная циркуляции).

Липиды в крови транспортируются в виде липопротеинов, ЛП (А), представляющих собой агрегаты молекул (микроэмульсии) с центральной частью из сильногидрофобных липидов, таких как триацилглицерид (ТГ) и сложные эфиры холестерина (СНО-эфиры), окруженных слоем амфипатических липидов (фосфолипиды, холестерин). Липопротеины содержат также некоторые типы белков, называемых аполипопротеинами. Липопротеины различны по размеру молекул, плотности, липидному составу, а также участкам синтеза и составу аполипопротеинов. Аполипопротеины (Аро) функционируют в качестве структурных элементов липопротеинов (например, АроАII и АроВ48), лигандов рецепторов липопротеинов (АроВ100, АроЕ и т. д.) на мембране клеток-мишеней липопротеинов и активаторов ферментов (например, ApoAI и АроСII).
Хиломикроны транспортируют липиды (в основном триацилглицериды, ТГ) из кишечника на периферию (при помощи кишечной лимфы и большого круга кровообращения; Г), где их АроСII активируют эндотелиальную липазу липопротеинов (ЛЯП), которая отщепляет свободные жирные кислоты (СЖК) от ТГ. В основном СЖК абсорбируется миоцитами и жировыми клетками (Г). При помощи АроЕ хиломикронные остатки доставляют остальные триацилглицериды, холестерин и сложные эфиры холестерина в гепатоциты при помощи рецептор-опосредованного эндоцитоза (Б, Г).
Холестерин и ТГ, импортируемые из кишечника, а также синтезированные в печени, экспортируются как фракция ЛПОНП (липопротеины очень низкой плотности) из печени на периферию, где они при помощи АроСII также активируют ЛПСП, приводя к высвобождению СЖК (Г). Это приводит к потерям АроСН и экспозиции АроЕ. Остатки ЛПОНП или ЛПСП (липиды средней, или промежуточной плотности) остаются. Примерно 50% ЛПСП возвращается в печень (в основном в связанном виде - с АроЕ на рецепторах ЛПНП; см. далее), где ЛПСП репроцессируются и экспортируются из печени в виде ЛПОНП (Б).

Другие 50% ЛПСП превращаются в ЛПНП (липопротеины низкой плотности) после контакта с липазой печени (что приводит к потерям АроЕ и экспозиции АроВ100). Две трети ЛПНП доставляют холестерин и эфиры холестерина в печень, а другая треть - во внепеченочные ткани (Б). Связывание АроВ100 с рецепторами ЛПНП необходимо для обоих процессов.
Липопротеины высокой плотности (ЛПВП) обменивают некоторые апопротеины на хиломикроны и ЛПОНП и абсорбируют излишний холестерин из внепеченочных клеток и крови (Б). Вместе с АроА1 они активируют плазматические лецитин-холестеролацилтрансферазы (ЛХАТ), которые ответственны за частичную этерификацию холестерина. ЛПВП также доставляют холестерин и его эфиры в печень и железы, продуцирующие стероидные гормоны и имеющие рецепторы ЛПВП (яичники, семенники, кора надпочечников).

Триацилглицерины, поступающие с пищей, расщепляются на свободные жирные кислоты (СЖК) и 2-моноацилглицерид (МГ) в желудочно-кишечном тракте (В). Поскольку короткоцепочечные свободные жирные кислоты растворимы в воде, они могут быть абсорбированы и транспортированы в печень по воротной вене. Длинноцепочечные жирные кислоты и 2-моноацилглицерин нерастворимы в воде. Они в клетках слизистой оболочки вновь превращаются в ТГ (В). (СЖК, необходимые для синтеза ТГ, переносятся СЖК-связывающими белками от клеточной мембраны к участкам синтеза, т. е. к гладкому эндоплазматическому ретикулуму.) Поскольку ТГ нерастворимы в воде, вслед за этим они включаются в хиломикроны, которые, в свою очередь, экзоцитируются во внеклеточную жидкость, затем проходят в кишечную лимфу (снова проходя через печень), откуда, в итоге, попадают в большой круг кровообращения (В, Г). (Плазма крови становится мутной примерно через 20-30 мин после принятия жирной пищи из-за присутствия в ней хило-микронов.) Печень также синтезирует ТГ, забирая необходимые СЖК из плазмы или синтезируя их из глюкозы. ТГ с ЛПОНП (см. ранее) после этого сек-ретируются в плазму (Г).

Поскольку экспортная емкость этого механизма ограничена, избыток СЖК или глюкозы (Г) может привести к аккумуляции ТГ в печени (жирная печень).
Свободные жирные кислоты (СЖК) представляют собой высокоэнергетические субстраты, используемые для энергетического метаболизма. Жирные кислоты, циркулирующие в крови, существуют в основном в форме ТГ (в составе липопротеинов), а СЖК плазмы образуют комплексы с альбумином. Жирные кислоты удаляются из ТГ хиломикронов и ЛПОНП липазой липопротеинов (ЛЛП) на стороне просвета эндотелия капилляров многих органов (в основном в жировой ткани и мышцах) (Г). АроСН на поверхности ТГ и ЛПОНП активируют ЛЛП. Инсулин, секретируемый после еды, индуцирует ЛЛП (Г), что способствует быстрой деградации реабсорбированых пищевых ТГ. ЛЛП также активируются гепарином (из эндотелиальной ткани, из тучных клеток и т. д.), что позволяет удалить хиломикроны из мутной плазмы; и поэтому он также называется фактором просветления плазмы. СЖК в составе комплексов с альбумином в плазме в основном транспортируются в мишени (Г).
- В сердечную мышцу, скелетную мышцу, почки и другие органы, где они окисляются до СО2 и Н2О в митохондриях (β-окисление) и используются как источник энергии.
- В жировые клетки (Г), которые либо хранят СЖК, либо используют их для синтеза ТГ. При возрастании энергетических потребностей либо снижении поставки СЖК в жировых клетках они отщепляются из триацилглицеридов (липолиз) и транспортируются в те участки, где необходимы (Г). Липолиз стимулируется адреналином, глюкагоном и кортизолом и ингибируется инсулином.
- В печень, где СЖК окисляются или используются для синтеза ТГ.
Сложные эфиры холестерина (СНО-эфиры), как и триацилглицериды (ТГ), представляют собой неполярные молекулы. В водной среде организма они могут транспортироваться лишь в составе липопротеинов (или связанными с белками) и могут быть использованы в обмене веществ только после превращения в холестерин, который более полярен (Б). СНО-эфиры служат запасными веществами и в некоторых случаях как транспортная форма СНО. СНО-эфиры присутствуют во всех липопротеинах, но наиболее распространены в ЛПНП (42%) (А).
Холестерин - важный компонент клеточной мембраны. Более того, он предшественник желчных солей (Б), витамина D и стероидных гормонов. В сутки примерно 0,6 г холестерина теряется с фекалиями (в виде копростерина) и выводится через кожу. Количество желчных кислот, теряемых за сутки, составляет около 0,5 г. Эти потери (без учета потребления холестерина с пищей) должны компенсироваться путем постоянного ресинтеза холестерина в желудочно-кишечном тракте и печени (Б). Холестерин, поступающий с пищей, частично усваивается сам по себе, а частично - в этерифицированной форме (Б, справа внизу). До того как он реабсорбируется, эфиры холестерина расщепляются неспецифической панкреатической карбоксилэстеразой до холестерина, который всасывается в верхней части тонкого кишечника (Б, внизу). Клетки слизистой желудка содержат ацил-КоА-холестеринацилтрансферазу (АХАТ) - фермент, реэтерифицирующий всасываемый холестерин, так что и холестерин, и его эфиры могут быть интегрированы в хил омикроны (А). Холестерин и его эфиры СНО в остатках хиломикронов (см. ранее) транспортируются в печень, где ли-зосомальные кислые липазы снова расщепляют эфиры до холестерина. Этот холестерин, а также холестерин из других источников (ЛПНП, ЛПВП) покидают печень (Б) различными способами: 1) путем экскреции в желчь; 2) путем превращения в желчные соли, которые также потом поступают в желчь; 3) путем включения в ЛПОНП — липопротеины печени, экспортирующие липиды в другие ткани. Под действием ЛЛП (см. далее) ЛПОНП преобразуются в ЛПСП и позже в ЛПНП (Б, слева). ЛПНП транспортируют холестерин и его эфиры в клетки с рецепторами ЛПНП (печеночные и внепеченочные клетки; Б, вверху). Плотность рецепторов на поверхности клеток колеблется в соответствии с потребностями в холестерине. Как и печеночные клетки (см. выше), внепеченочные клетки поглощают ЛПНП посредством рецептор-опосредованного эндоцитоза, и лизосомальные кислые липазы переводят эфиры холестерина в холестерин (Б, справа вверху). Затем клетки могут встраивать холестерин в клеточные мембраны или использовать его для синтеза стероидов. Избыток холестерина вызывает (а) ингибирование синтеза холестерина в клетках (З-НМG-СоА-редуктаза) и (б) активацию АХАТ - фермента, зтерифицирующего и запасающего холестерин в форме его эфиров.
Избыток липидов в крови может отражать увеличение уровня триацилглицеридов и/или холестерина (> 2,0-2,2 г/л сыворотки, этот показатель обнаруживается у примерно каждого пятого жителя западных стран). В наиболее серьезной форме семейная гиперлипопротеинемия (генетический дефект) вызывает увеличенную концентрацию холестерина в крови с самого рождения, что может привести к инфаркту миокарда в юношеском возрасте. Болезнь вызывается генетическим дефектом высокоаффинных рецепторов ЛПНП. Уровень холестерина в сыворотке повышается, поскольку клетки поглощают небольшие количества богатых холестерином липопротеинов низкой плотности (ЛПНП). Внепеченочные ткани синтезируют большие количества холестерина, поскольку З-НМG-СоА-редуктаза не может ингибировать синтез холестерина по причине пониженного всасывания ЛПНП. В результате все больше ЛПНП связывается с низкоаффинными рецепторами, опосредующими всасывание и запасание холестерина в макрофагах, кожных покровах и кровеносных сосудах. Таким образом, гиперхолестеринемия увеличивает риск атеросклероза и коронарной болезни сердца.
Сегодня мы поговорим о том, что происходит с пищей в тонком и толстом кишечнике.
Все, что случилось с пищей в ротовой полости и желудке, являлось подготовкой к дальнейшим превращениям. Усвоения и всасывания питательных веществ там практически не было. Настоящая алхимия пищеварения происходит в тонком кишечнике, точнее, в ее начальной части — двенадцатиперстной кишке, названной так, потому что длина ее измеряется 12-ю сложенными вместе пальцами — перстами.
Обработанная желудочными секретами пища, уже совсем непохожая на то, что мы съели, продвигается к выходу из желудка, к пилорической ее части. Здесь находится сфинктер (клапан), отделяющий желудок от кишечника, который порциями выпускает химус в дуоденум (другое название двенадцатиперстной кишки), где среда уже не кислая, как в желудке, а щелочная. Регуляция клапана — это очень сложный механизм, зависящий, в том числе, и от сигналов, поступающих от рецепторов, реагирующих на кислотность, состав, консистенцию и степень обработки пищи, и на давление в желудке. В норме, на выходе из желудка, пища должна иметь уже слабокислую реакцию среды, в которой продолжают работать иные протеолитические (расщепляющие белок) ферменты. Кроме того, в желудке всегда должно оставаться свободное пространство для газов, которые образуются в результате ферментации и брожения. Давление газов особенно способствует открытию сфинктера. Именно поэтому рекомендуется есть такое количество пищи, чтобы в желудке 1/3 была заполнена твердой пищей, 1/3 жидкой и 1/3 пространства сохранялась бы свободной, что поможет избежать многих неприятных последствий (отрыжки, формирования рефлюксов, преждевременного прохождения в кишечник недообработанной пищи и формирования стойких, ставших хроническими нарушений). Иначе говоря, лучше не переедать, а для этого необходимо есть не торопясь, так как сигналы о насыщении начинают поступать в мозг только через 20 минут.
Пищеварение в тонком кишечнике
В тонком кишечнике должна быть щелочная среда, а из желудка приходит кислый химус, что происходит? Обильное выделение в просвет двенадцатиперстной кишки кишечных соков, секрета поджелудочной железы и желчи, содержащих бикарбонаты, способно быстро нейтрализовать поступающую кислоту всего за 16 сек (в течение суток каждого из секретов выделяется от 1,5 до 2,5 л). Таким образом в кишечнике создается необходимая слабощелочная среда, в которой активируются ферменты поджелудочной железы.
Поджелудочная железа — жизненно важный орган. Она не только выполняет секреторную пищеварительную функцию, но также продуцирует гормоны инсулин и глюкагон, которые не выделяются в просвет кишечника, а сразу поступают в кровь и играют наиважнейшую роль в регуляции сахара в организме.
Панкреатический сок богат ферментами, осуществляющими гидролиз (расщепление) белков, жиров и углеводов. Протеолитические ферменты (трипсин, химотрипсин, эластаза и др.) расщепляют внутренние связи белковой молекулы с образованием аминокислот и низкомолекулярных пептидов, способных пройти через ворсинчатый слой тонкого кишечника в кровь. Ферментативный гидролиз жиров осуществляют панкреатическая липаза, фосфолипаза, холестеролэстераза. Но эти ферменты могут работать только с эмульгированными жирами (эмульгация — осуществляемое желчью расщепление крупных молекул жиров на более мелкие, подготовка к обработке липазами). Конечный продукт гидролиза липидов — жирные кислоты, которые далее в закишечном пространстве попадают в лимфатические сосуды.
Расщепление пищевых углеводов (крахмалы, сахароза, лактоза), начавшееся в ротовой полости, продолжается в тонком кишечнике под действием ферментов поджелудочной железы в слабощелочной среде до конечных моносахаридов (глюкозы, фруктозы, галактозы).
Уделим немного больше внимания роли желчи. Желчь продуцируется печенью, этот процесс идет непрерывно и днем, и ночью (за сутки вырабатывается 1–2 л), но усиливается во время еды и стимулируется определенными химическими соединениями (медиаторами) и гормонами. Упомяну только одно вещество — холецистокинин-панкреозимин — важный стимулятор желчевыделения, продуцируемый клетками тонкого кишечника и с током крови поступающий в печень. При воспалительных изменениях в кишечнике этот гормон может не вырабатываться. Из продуктов основными стимуляторами желчевыделения являются: масла (жиры), яичные желтки (содержат желчные кислоты), молоко, мясо, хлеб, сульфат магния. По желчным протокам печени желчь попадает в общий желчный проток, где на пути может накапливаться в желчном пузыре (до 50 мл), в котором происходит обратное всасывание воды, приводящее к сгущению желчи (еще один повод пить воду в достаточном количестве). Если желчь густая, да еще существуют анатомические особенности расположения желчного пузыря (перегибы, перекруты), то движение ее затрудняется, что может приводить к застою и образованию камней.
Что входит в состав желчи? Желчные кислоты; желчные пигменты (билирубин); холестерин и лицетин; слизь; метаболиты лекарств (если принимаются таковые, то печень очищает организм и выводит их с желчью). Желчь должна быть стерильной и иметь рH 7,8–8,2 (щелочная среда позволяет оказывать бактерицидный эффект).
Функции желчи: эмульгация жиров (подготовка для дальнейшего гидролиза ферментами поджелудочной железы); растворение продуктов гидролиза (что обеспечивает их всасывание в тонком кишечнике); повышение активности кишечных и панкреатических ферментов; обеспечение всасывания жирорастворимых витаминов (А,D,E), холестерина, солей кальция; бактерицидное действие на гнилостную флору; стимуляция процессов желчеобразования и желчевыделения, моторной и секреторной деятельности; участие в запрограммированной гибели и обновлении эритроцитов (апоптоз и пролиферация эритроцитов); вывод токсинов.
Пищеварение в толстом кишечнике
Далее все, что не усвоилось в тонком кишечнике, переходит в толстый кишечник, где на протяжении длительного времени происходит всасывание воды и формирование фекальных масс. В толстом кишечнике проживают дружественные и недружественные нам микроорганизмы, которые разделяют с нами оставшуюся трапезу, воюя между собой за среду обитания, а иногда и с нашим организмом. А вы думаете, что в нас никто не живет? Это целый мир и война миров… Их разнообразие не поддается точному исчислению. Только в кишечнике обитает несколько сотен видов микроорганизмов. Одни из них нам дружественны и приносят пользу, другие — доставляют нам неприятности. Ученые доказали, что бактерии могут передавать друг другу информацию, и что именно таким образом быстро нарастает резистентность (устойчивость) к антибиотикам и другим медикаментозным препаратам. Они могут прятаться от иммунных клеток нашего организма, выделяя определенные вещества и становясь невидимыми для них. Они мутируют и приспосабливаются.
Патогенные микроорганизмы растут и размножаются, используя в качестве пищи продукты распада белка. А это значит, что чем больше в рационе белковых, трудно перевариваемых продуктов (мясо, яйца, молочное) и рафинированных сахаров, тем активнее будут развиваться процессы гниения в кишечнике. В результате произойдет закисление, что сделает среду еще более благоприятной для развития условно патогенной микрофлоры. Наши друзья — симбиоты предпочитают пищу, богатую растительной клетчаткой. Поэтому рацион с низким содержанием белка и обилием овощей, фруктов и цельнозерновых углеводов благоприятно сказывается на состоянии здоровой микрофлоры человека, которая в процессе своей жизнедеятельности продуцирует витамины и расщепляет клетчатку и другие сложные углеводы до простейших веществ, которые могут использоваться в качестве энергетического ресурса для кишечного эпителия. Кроме того, пища богатая клетчаткой, способствует перистальтическим движениям в желудочно-кишечном тракте, тем самым предотвращая нежелательные застои пищевых масс.
Как гниение пищи отражается на здоровье человека? Продукты гниения белка являются токсинами, которые легко проходят через слизистые кишечника и попадают в кровеносное русло, и далее в печень, где происходит их нейтрализация. Но помимо токсинов, в кровь могут попасть и продуцирующие их патогенные микроорганизмы, что становится нагрузкой не только для печени, но и для иммунной системы. Если поток токсинов очень стремителен, печень не успевает их нейтрализовать, в результате яды разносятся по всему организму, отравляя каждую его клетку. Все это не проходит для человека бесследно, и вследствие хронического отравления, человек чувствует хроническую усталость. На высокобелковом рационе, вследствие повышенной активности иммунных клеток, может усиливаться проницаемость капилляров и мелких кровеносных сосудов, через которые могут пройти вредоносные бактерии и продукты распада, что постепенно ведет к развитию очагов воспаления во внутренних органах. И далее воспаленные ткани отекают, кровоснабжение и обменные процессы в них нарушаются, что в конечном итоге способствует развитию самых разнообразных патологических состояний и заболеваний.
Застой каловых масс при нарушении перистальтики и нерегулярном опорожнении кишечника также способствует поддержанию гнилостных процессов, высвобождению токсинов и формированию воспалительных процессов, как в самом кишечнике, так и в органах, расположенных рядом. Так, например, провисающий, перерастянутый от каловых масс толстый кишечник может давить на репродуктивные органы женщин и мужчин, вызывая в них воспалительные изменения. Состояние нашего физического и психоэмоционального здоровья напрямую зависит от состояния процессов в толстом кишечнике и регулярного его опорожнения.
Что я хочу, чтобы вы запомнили
Наши органы пищеварения работают строго по законам. В каждом отделе желудочно-кишечного тракта происходят свои процессы. Очень важно помогать своему организму быть здоровым. Очень важно обратить внимание на то, как и что вы едите, раз нам необходимо есть, чтобы жить. Действительно важно и физиологично поддерживать правильный кислотно-щелочной баланс, который в норме у нас слабощелочной, за исключением желудка. Обработка еды — это очень сложный, энергозатратный процесс, которому помогает не подсчет калорий и полезных составляющих в изначальном продукте, а простые действия.
К ним относятся:
Важно следить, чтобы опорожнение кишечника было регулярным. И очень важно пить достаточное количество воды, которая нужна не только для запуска ферментных систем, выработки слизи, но и для очищения организма в целом.
Пишем статьи о питании, тренировках и здоровом образе жизни на основе научных исследований
Некоторые полагают, что углеводы, жиры и белки всегда полностью усваиваются организмом. Многие думают, что абсолютно все присутствующие на их тарелке (и, конечно, подсчитанные) калории поступят в кровь и оставят свой след в организме. На самом деле все обстоит иначе. Давайте рассмотрим усвоение каждого из макронутриентов по отдельности.
Переваривание (усвоение) – это совокупность механических и биохимических процессов, благодаря которым поглощаемая человеком пища преобразуется в вещества, необходимые для функционирования организма.
Процесс переваривания обычно начинается уже во рту, после чего пережеванная пища попадает в желудок, где подвергается различным биохимическим обработкам (в основном на данном этапе обрабатывается белок). Продолжается процесс в тонком кишечнике, где под воздействием различных пищевых ферментов происходит превращение углеводов в глюкозу, расщепление липидов на жирные кислоты и моноглицериды, а белков – на аминокислоты. Все эти вещества, всасываясь через стенки кишечника, попадают в кровь и разносятся по всему организму.
Всасывание макронутриентов не длится часами и не растягивается на все 6,5 метров тонкой кишки. Усвоение углеводов и липидов на 80%, а белков – на 50% осуществляется на протяжении первых 70 сантиметров тонкого кишечника.
Усвоение углеводов
Усвоение различных типов углеводов происходит по-разному, так как они имеют различную химическую структуру . Для визуализации этой разницы и принципов переваривания основные этапы для простых и сложных углеводов представлены в инфографике ниже.
Высокий гликемический индекс продукта означает, что в результате его переваривания подъём уровня глюкозы в крови будет значительным. Низкий гликемический индекс продукта указывает, что его усвоение организмом изменит содержание глюкозы в крови незначительно.
Результаты замеров позволяют воспроизвести график (см. картинку), на котором вся площадь под полученной кривой отражает общий рост уровня сахара в крови. Эта величина делится на число, полученное от стандарта (глюкоза или белый хлеб), и умножается на 100 для получения процентной величины.
На графике вы можете видеть, как продукты с различным значением ГИ изменяют уровень глюкозы (гликемию) в крови после употребления. У завтрака с высокий гликемическим индексом – высокий пик подъема уровня глюкозы, у завтрака с низким ГИ – кривая более пологая.
Важно отметить, что пик гликемии наступает примерно в одно и то же время для всех видов углеводов, вне зависимости от того, сложен или прост состав их молекулы.
За последние три десятилетия исследователи измерили гликемический индекс нескольких тысяч продуктов.
Важно понимать, что гликемический индекс не является постоянной величиной . Его значение зависит от ряда параметров: происхождение, сорт и разновидность продукта (для злаковых, фруктов), степень созревания (для фруктов), термическая и гидротермическая обработка, вид переработки продукта (дробление, измельчение до муки), а также индивидуальные особенности организма каждого человека и другие факторы.
Гликемический индекс определенных продуктов может также зависеть от того, с чем эти продукты употребляются . Оливковое масло или что-то кислое, например, уксус или лимонный сок, могут замедлить превращение крахмала в сахар и таким образом снизить гликемический индекс.
Гликемическая нагрузка
Помимо ГИ для регуляции уровня глюкозы в крови диетологами было предложено также учитывать и гликемическую нагрузку продуктов (ГН) .
Гликемическая нагрузка (ГН) принимает в расчет и ГИ продукта, и количество углеводов в нём. Нередко у продуктов с высоким ГИ будет маленькая ГН. Формула подсчета ГН:
- Кабачки готовые (ГИ=75). ГН = 75*4,9/100 = 3,68.
- Бублик пшеничный (ГИ=72). ГН = 72*58,5/100=42,12.
Шкала уровней ГН:
- ГН≤10 — минимальный уровень;
- ГН = 11-19 — умеренный уровень;
- ГН ≥20 — повышенный.
В последние годы в научной среде появилось мнение о необходимости пересмотра оценки ГИ.
Исследования показывают, что ГИ и ГН не являются достаточно надежными критериями для выбора углеводосодержащих продуктов, так как не позволяют с высокой точностью оптимизировать уровень глюкозы при составлении рациона.
Гликемический индекс продуктов и похудение
Есть достаточное количество научных данных о том, что системы питания, основанные на употреблении продуктов с низким ГИ, могут положительно влиять на снижение веса. Биохимических механизмов, которые в этом участвуют, множество, но назовем наиболее актуальные для нас:
- Продукты с низким ГИ вызывают большее чувство сытости, нежели продукты с высоким ГИ.
- После употребления продуктов с высоким ГИ поднимается уровень инсулина, который стимулирует всасывание глюкозы и липидов в мышцы, жировые клетки и печень, параллельно приостанавливая расщепление жиров. Как следствие, уровень глюкозы и жирных кислот в крови падает, и это стимулирует голод и новый прием пищи.
- Продукты с разными ГИ по-разному влияют на расщепление жиров во время отдыха и во время спортивных тренировок. Глюкоза из продуктов с низким ГИ не так активно откладывается в гликоген, но зато во время тренировок гликоген не так активно сжигается, что указывает на повышенное использование жиров для этой цели.
- Чем продукт более измельчен (в основном относится к зерновым), тем выше ГИ продукта.
- Чем больше в продукте содержится клетчатки, тем ниже его ГИ.
Различия между пшеничной мукой (ГИ 85) и зерном пшеницы (ГИ 15) попадают под оба этих критерия. Это значит, что уровень глюкозы в крови после употребления муки вырастает более резко, чем после употребления цельного зерна, например, булгура или полбы.
Свекла – это источник углеводов с более высоким содержанием клетчатки, чем мука. Несмотря на то что у нее высокий гликемический индекс, у нее низкое содержание углеводов, т. е. более низкая гликемическая нагрузка. В данном случае , несмотря на то, что ГИ у нее такой же, как и у зернового продукта, количество глюкозы, поступившее в кровь, будет намного меньше. Когда мы сравниваем цельные культуры с переработанными, важно не забывать обо всех микро- и фитонутриентах, которые присутствуют в натуральных продуктах и которых нет в полученных промышленным способом.
Это правило касается не только моркови, но и всех овощей с высоким содержанием крахмала, таких как батат, картошка, свекла и т. д. В процессе тепловой обработки существенная часть крахмала превращается в мальтозу (дисахарид), который очень быстро усваивается.
Следовательно, даже вареные овощи лучше не разваривать, а следить, чтобы они оставались целыми и твердыми. Однако, если у вас такие заболевания, как гастрит или язва желудка, все же лучше употреблять в пищу овощи в приготовленном виде.
Овощи содержат пищевые волокна и сложные углеводы, которые не усваиваются организмом, но очень важны для эффективного пищеварения. Кроме того, добавление белка к любому виду углеводов снизит общий ГИ блюда .
Натуральные продукты, в отличие от соков, содержат клетчатку и тем самым понижают ГИ. Более того, желательно есть фрукты и овощи с кожурой не только потому, что кожура – это клетчатка, но и потому, что большая часть витаминов прилегает непосредственно к кожуре.
Усвоение белков
Процесс переваривания белков требует повышенной кислотности в желудке. Желудочный сок с повышенной кислотностью необходим для активизации ферментов, ответственных за расщепление белков на пептиды, а также за первичное расформировывание пищевых белков в желудке. Из желудка пептиды и аминокислоты попадают в тонкую кишку, где часть из них всасывается через стенки кишечника в кровь, а часть расщепляется далее на отдельные аминокислоты.
Для оптимизации этого процесса нужно нейтрализовать кислотность желудочного раствора, и за это отвечает поджелудочная железа, а также желчь, вырабатываемая печенью и необходимая для абсорбции жирных кислот.
Белки из пищи делятся на две категории: полноценные и неполноценные.
Полноценные белки – это белки, которые содержат все необходимые (незаменимые) для нашего организма аминокислоты. Источником этих белков в основном являются животные белки, т. е. мясо, молочные продукты, рыба и яйца. Исключением является соевый белок, который по аминокислотному составу схож с мясным. Среди круп лидером по содержанию незаменимых аминокислот является киноа.
Неполноценные белки содержат только часть незаменимых аминокислот. Считается, что бобовые и злаковые сами по себе содержат неполноценные белки, однако их сочетание позволяет нам получить все незаменимые аминокислоты.
Во многих национальных кухнях правильные сочетания, приводящие к полноценному потреблению белков, возникли естественным путем. Так, на Ближнем Востоке распространена пита с хумусом или фалафелем (пшеница с нутом) или рис с чечевицей, в Мексике и Южной Америке нередко сочетают рис с фасолью или кукурузой.
Одним из параметров, определяющих качество белка, является наличие незаменимых аминокислот. В соответствии с этим параметром существует система индексации продуктов.
Так, например, аминокислота лизин находится в малых количествах в злаках, и поэтому они получают низкую оценку (хлопья – 59; цельная пшеница – 42), а в бобовых содержится небольшое количество незаменимых метионина и цистеина (нут – 78; фасоль – 74; бобовые – 70). Животные белки и соя получают высокую оценку по этой шкале, так как содержат необходимые пропорции всех незаменимых аминокислот (казеин (молоко) – 100; яичный белок – 100; соевый белок – 100; говядина – 92).
Кроме того, необходимо учитывать белковый состав, их усвояемость из данного продукта, а также пищевую ценность всего продукта (наличие витаминов, жиров, минералов и калорийность). Например, гамбургер будет содержать много белка, но также много насыщенных жирных кислот, соответственно, его пищевая ценность будет ниже, чем у куриной грудки.
Белки из разных источников и даже разные белки из одного источника (казеин и белок из молочной сыворотки) утилизируются организмом с разной скоростью [5].
Питательные вещества, поступающие с пищей, не обладают стопроцентной усвояемостью. Степень их всасывания может существенно меняться в зависимости от физико-химического состава самого продукта и поглощаемых одновременно с ним продуктов, особенностей организма и состава кишечной микрофлоры.
Усвоение жиров
Жир, попадая в организм, проходит через желудок почти нетронутым и попадает в тонкую кишку, где есть большое количество ферментов, перерабатывающих жиры в жирные кислоты. Эти ферменты называются липазы. Они функционируют в присутствии воды, но для переработки жиров это проблематично, т. к. жиры не растворяются в воде.
Для того чтобы иметь возможность утилизировать жиры , организм производит желчь. Желчь разъединяет комки жира и позволяет ферментам, находящимся на поверхности тонкой кишки, расщепить триглицериды на глицерол и жирные кислоты.
Транспортеры для жирных кислот в организме называются липопротеины. Это специальные белки, способные упаковывать и транспортировать жирные кислоты и холестерин по кровеносной системе. Далее жирные кислоты упаковываются в жировых клетках в довольно компактном виде, т. к. для их комплектации (в отличие от полисахаридов и белков) не требуется вода [9].
Доля всасывания жирной кислоты зависит от того, какую позицию она занимает относительно глицерина. Те жирные кислоты, которые занимают позицию Р2, всасываются лучше. Это связано с тем, что липазы имеют разную степень воздействия на жирные кислоты в зависимости от расположения последних.
Не все поступившие с пищей жирные кислоты полностью всасываются в организме, как ошибочно полагают многие диетологи. Они могут частично или полностью не усвоиться в тонком кишечнике и быть выведены из организма.
Например, в сливочном масле 80% жирных кислот (насыщенных) находятся в позиции Р2, то есть они практически полностью всасываемы. Это же относится к жирам, входящим в состав молока и всех не проходящих процесс ферментации молочных продуктов.
Жирные кислоты, присутствующие в зрелых сырах (особенно сырах длительной выдержки), хоть и являются насыщенными, находятся все же в позициях Р1 и Р3, что делает их менее абсорбируемыми.
Более подробно о типах жиров и их особенностях мы пишем в статье “Жиры” .
Авторы: Дегтярь Елена, PhD; Кардакова Мария, MSc
Литература
1. Mann (2007) FAO/WHO Scientific Update on carbohydrates in human nutrition: conclusions. European Journal of Clinical Nutrition 61 (Suppl 1), S132–S137
2. FAO/WHO. (1998). Carbohydrates in human nutrition. Report of a Joint FAO/WHO Expert Consultation (Rome, 14–18 April 1997). FAO Food and Nutrition Paper 66
3. Holt, S. H., & Brand Miller, J. (1994). Particle size, satiety and the glycaemic response. European Journal of Clinical Nutrition, 48 (7), 496–502.
4. Jenkins DJ (1987) Starchy foods and fiber: reduced rate of digestion and improved carbohydrate metabolismScand J Gastroenterol Suppl.129:132-41.
5. Boirie Y. (1997) Slow and fast dietary proteins differently modulate postprandial protein accretion. Proc Natl Acad Sci U S A. 94 (26):14930-5.
6. Popkin, BM (2012) Global nutrition transition and the pandemic of obesity in developing countries. Nutrition reviews 70 (1): pp. 3 -21.
7. Your Meta Body’s bolism
8. About Glycemic Index
9. International table of glycemic index and glycemic load values: 2002
10.Jenkins, D. J., Wolever, T. M., Taylor, R. H., Barker, H., Fielden, H., Baldwin, J. M., … & Goff, D. V. (1981). Glycemic index of foods: a physiological basis for carbohydrate exchange. The American journal of clinical nutrition, 34(3), 362-366.
11. Как пользоваться таблицей ГИ, составляя меню для диабетиков.
Читайте также:

