Патогенез аортального стеноза кратко
Обновлено: 30.06.2024
Изолированный аортальный стеноз встречается весьма редко, однако в сочетании с другими клапанными поражениями он наблюдается довольно часто (например, приблизительно у половины больных с аортальной недостаточностью). У мужчин он обнаруживается чаще, чем у женщин.
В отличие от врожденного аортального стеноза, который может быть подклапанным, клапанным или надклапанным, приобретенный аортальный стеноз всегда клапанный.
Наиболее частой причиной приобретенного аортального стеноза является ревматизм. Редко стеноз аортального клапана обусловлен образованием сращений между клапанными заслонками после излечения бактериального эндокардита. Не вполне ясна этиология идиопатического аортального стеноза, для которого характерны изолированное поражение аортального клапана и кальциноз его заслонок (порок Менкеберга). Предполагают, что в генезе этого порока у молодых людей этиологическую роль играет ревматизм, а у пожилых атеросклероз, хотя есть данные о кальцинозе аортального клапана преимущественно при врожденном сужении устья аорты или при другой врожденной аномалии — двустворчатом аортальном клапане.
Так называемый относительный стеноз аорты характеризуется возникновением систолического шума в проекции аортального клапана обычно вследствие расширения полости аорты над клапаном и полости левого желудочка под клапаном, сужения клапанного отверстия при этом нет.
Нарушения внутрисердечной и системной гемодинамики определяются высоким сопротивлением кровотоку в суженном устье аорты, преодоление которого достигается созданием более высокого, чем в норме, систолического градиента давления между камерой левого желудочка и аортой за счет повышенного систолического напряжения стенок желудочка, ведущего к ранней его гипертрофии. Значительное повышение градиента давления необходимо при уменьшении площади аортального отверстия до 1 /3— 1 /4нормальной величины. При выраженном аортальном стенозе градиент давления может превышать 100 и даже 150 мм рт. ст., однако и он не обеспечивает должной объемной скорости изгнания крови, которая замедляется, а фаза изгнания удлиняется. При этом линейная скорость кровотока в зоне суженного и деформированного устья аорты возрастает, что порождает турбулентные потоки, с которыми связано возникновение характерных для аортального стеноза систолического шума изгнания и систолического дрожания. Удлинение фазы изгнания крови из левого желудочка приводит к тому, что эта фаза становится более продолжительной, чем фаза изгнания из правого желудочка (в физиологических условиях это соотношение носит обратный характер). В результате аортальный компонент II тона не предшествует легочному, а следует за ним, причем интервал между ними не увеличивается при задержке дыхания на высоте вдоха, как обычно, а уменьшается (парадоксальное расщепление II тона).
Степень гипертрофии миокарда зависит от тяжести стеноза и длительности его существования. Выраженная гипертрофия левого желудочка сопровождается уменьшением диастолической растяжимости его стенок и повышением диастолического давления в его полости, что требует увеличения силы сокращения левого предсердия для заполнения левого желудочка.
Тем не менее в связи с небольшой продолжительностью систолы левого предсердия среднее давление в его полости и соответственно венозное давление в легких практически не повышаются до момента декомпенсации порока. Начало декомпенсации порока характеризуется некоторой дилатацией полости левого желудочка, дополнительным повышением диастолического давления в ней и снижением сердечного выброса. В дальнейшем возникает относительная митральная недостаточность, повышается давление в полости левого предсердия и легочных венах, что в итоге ведет к развитию артериальной легочной гипертензии, перегрузке правого желудочка и правожелудочковой недостаточности. Возможности увеличения сердечного выброса в ответ на нагрузку при выраженном сужении устья аорты ограничены. Учащение сердечных сокращений при нагрузке скорее препятствует этому увеличению, т.к. может привести к снижению фракции выброса из-за укорочения при тахикардии фазы изгнания. Поэтому перераспределение крови в скелетные мышцы при физической нагрузке сопряжено при выраженном стенозе с недостаточным кровоснабжением миокарда и головного мозга, что проявляется стенокардией и обморочными состояниями.
Симптомы Аортального стеноза:
При небольшом сужении устья аорты, приобретенном в молодом возрасте, субъективные признаки порока отсутствуют иногда в течение десятилетий, причем отдельные больные выполняют тяжелую физическую работу и даже способны заниматься спортом. При более выраженном аортальном стенозе относительно рано возникает ощущение сердцебиений (как сильных ударов, а не как возрастания их частоты), связанное с мощными сокращениями гипертрофированного левого желудочка сердца. По мере снижения сердечного выброса появляются жалобы, указывающие на формирование централизации кровообращения: повышенная утомляемость, мышечная слабость, бледность кожи. Недостаточность этого компенсаторного механизма проявляется характерными для аортального стеноза жалобами на боли в области сердца (стенокардия отмечается у 40—50% больных), головокружения и обмороки. Впоследствии больные жалуются на одышку при физической нагрузке, переносимость которой постепенно снижается. В ряде случаев появившаяся стенокардия быстро прогрессирует, наблюдается как при физической нагрузке, так и в покое, иногда ангинозные приступы протекают в виде многочасового ангинозного статуса, рефракторного к терапии нитратами. Возникновение предобморочных состояний также связано с физической нагрузкой, которая может провоцировать иногда глубокий обморок с медленным восстановлением сознания. При декомпенсации порока одышка постепенно нарастает, затем появляются приступы сердечной астмы, эпизоды отека легких.
Объективные признаки порока выявляются преимущественно при исследовании сердца (внешний вид больных чаще не изменяется). Смещение верхушечного толчка сердца влево и вниз (в шестом межреберье) при аортальном стенозе, в отличие от аортальной недостаточности, отмечается лишь в стадии декомпенсации порока в связи с дилатацией в этот период левого желудочка. Однако пальпаторно рано обнаруживаются усиление верхушечного толчка (признак гипертрофии желудочка) и важный симптом стеноза устья аорты — систолическое дрожание. Последнее лучше определяется в области абсолютной сердечной тупости и во втором межреберье справа от грудины, а при резко выраженном стенозе нередко также в яремной ямке и по ходу сонных артерий, II тон над аортой ослаблен, иногда расщеплен (парадоксальное расщепление). Основной аускультативный признак порока — систолический шум (как правило, грубого тембра) во втором межреберье справа от грудины (иногда лучше слышен слева от нее или в точке Боткина — Эрба), он проводится в тех же направлениях, что и систолическое дрожание (особенно хорошо на сонные артерии).
Систолическое и пульсовое АД при аортальном стенозе чаще снижены. Пульс малый и медленный. Выраженность этих симптомов прямо пропорциональна степени сужения устья аорты.
Трудоспособность больных, особенно выполняющих ограниченную физическую нагрузку, сохраняется многие годы, а при умеренном и маловыраженном стенозе — десятилетия. Она рано нарушается при резко выраженном стенозе устья аорты. Сочетание частых приступов стенокардии с синкопальными состояниями и особенно появление сердечной астмы прогностически неблагоприятны, т.к. консервативное лечение в этой фазе течения порока мало эффективно, а развитие сердечной недостаточности и других осложнений носит прогрессирующий характер.
К осложнениям, угрожающим жизни больных с выраженным аортальным стенозом, относятся отек легких и инфаркт миокарда . Последний иногда развивается при еще достаточно компенсированной общей гемодинамике, но в этих случаях его развитие обычно ведет к возникновению и быстрому прогрессированию левожелудочковой сердечной недостаточности.
По некоторым данным, от 14 до 18% больных с тяжелым аортальным стенозом погибают внезапно, причем иногда внезапная смерть — первое проявление болезни. Среди возможных причин внезапной смерти предполагают фибрилляцию желудочков сердца . Однако нарушение ритма сердца у больных с аортальным стенозом наблюдается сравнительно редко и обычно протекает в форме желудочковой экстрасистолии . Иногда при аортальном стенозе глубокий обморок завершается смертью.
Диагностика Аортального стеноза:
Этиологическая диагностика затруднена в случаях, когда отсутствуют указания на ревматизм в анамнезе. Ревматическая природа порока несомненна при сочетании аортального стеноза с пороком митрального клапана. Об атеросклеротической этиологии следует думать при первом выявлении незначительного изолированного аортального стеноза у пожилых больных.
Дифференциальный диагноз проводят с пороками и другими заболеваниями сердца, при которых определяются систолический шум и гипертрофия левого желудочка сердца. При неясной этиологии порока, особенно у детей, прежде всего исключают врожденный аортальный стеноз, для которого характерны выявление признаков порока в раннем детском возрасте и нередко сочетание с другими врожденными аномалиями развития сердечно-сосудистой системы (незаращение артериального протока, коарктация аорты). Это же относится и к дефекту межжелудочковой перегородки, для различения которого с аортальным стенозом иногда приходится прибегать к зондированию сердца и вентрикулографии, что необходимо также для определения показаний к оперативному вмешательству. У взрослых дифференциальный диагноз чаще проводят с идиопатическим гипертрофическим субаортальным стенозом (см. Кардиомиопатии ), стенозом устья легочного ствола, реже с митральной недостаточностью. Во всех этих случаях существенное значение для правильного диагноза имеет эхокардиографическое исследование.
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Аортального стеноза, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Стеноз устья аорты : патогенез.
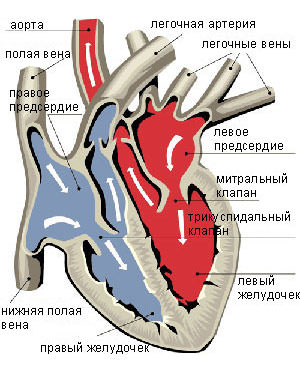
Первичным в нарушении гемодинамики является обструкция оттоку крови из левого желудочка, что ведет к возникновению градиента систолического давления между левым желудочком и аортой. На вызванную в эксперименте внезапную обструкцию левый желудочек отвечает дилатацией и уменьшением ударного объема. Однако у больных со стенозом устья аорты, несмотря на имеющуюся с рождения или постепенно нарастающую в течение многих лет обструкцию, сердечный выброс поддерживается за счет развивающейся гипертрофии левого желудочка. Последняя служит компенсаторным механизмом, поскольку уменьшает до нормального уровня систолическое напряжение, развивающееся в каждом сегменте миокарда. Значительный трансаортальный клапанный градиент давления может существовать в течение многих лет, не приводя к уменьшению сердечного выброса, дилатации левого желудочка и появлению жалоб. По мере прогрессирования степени стеноза устья аорты систолическое давление в левом желудочке продолжает повышаться, однако редко превышает 300 мм рт. ст.
Считается, что максимальный градиент систолического давления, превышающий 50 мм рт. ст. в условиях нормального сердечного выброса или при эффективной площади устья аорты менее чем 0,5 см2 на 1 м2 площади тела, т. е. составляющей примерно менее 33 % от нормальной площади, представляет собой критическое препятствие для оттока крови из левого желудочка. По мере того как сокращение левого желудочка становится все более умеренным, вершина кривой давления в левом желудочке приобретает закругленную форму. Увеличенное конечно-диастолическое давление в левом желудочке, регистрирующееся у многих больных с выраженным стенозом устья аорты, не обязательно свидетельствует о дилатации левого желудочка или о его недостаточности: оно может отражать лишь сниженную податливость гипертрофированной стенки левого желудочка.
При выраженном стенозе устья аорты на кривой давления в левом предсердии обычно регистрируется большой амплитуды волна а, отражающая усиленную сократимость левого предсердия и сниженную податливость левого желудочка. Сокращение предсердия ведет к повышению конечно-диастолического давления в левом желудочке, при этом не наблюдается аналогичного увеличения среднего давления в левом предсердии. Такое функционирование левого предсердия в качестве вспомогательного насоса препятствует повышению давления в легочных венах и легочных капиллярах до уровня, который может вызвать застойные явления в легких и поддерживает в то же время конечно-диастолическое давление в левом желудочке на повышенном уровне, необходимом для его эффективного сокращения. Прекращение регулярных и сильных сокращений левого предсердия при мерцании предсердий или атриовентрикулярной диссоциации может вызвать резкое усиление симптомов болезни.
Несмотря на то что в покое сердечный выброс у большинства больных со стенозом устья аорты поддерживается на нормальном уровне, он не может адекватно возрастать в ответ на физическую нагрузку. В поздних стадиях болезни сердечный выброс и градиент давления между левым желудочком и аортой уменьшаются, среднее давление в левом предсердии, давление заклинивания легочного ствола, давление в легочном стволе и давление в правом желудочке повышаются.
Гипертрофия мышечной массы левого желудочка приводит к увеличению потребности миокарда в кислороде. Кроме того, даже при обструкции в венечных артериях коронарный кровоток может страдать вследствие того, что давление, сжимающее венечные артерии, превышает перфузионное давление в них. Метаболические проявления ишемии миокарда, т. е. увеличение выброса лактата в ответ на введение изопротеренола больным со стенозом устья аорты, могут наблюдаться как при сужении венечных артерий, так и при отсутствии его.
У значительной части больных со стенозом устья аорты ревматической этиологии наблюдается сопутствующее поражение левого предсердно-желудочкового клапана. Стеноз устья аорты усиливает выраженность недостаточность данного клапана за счет увеличения давления, способствующего продвижению крови из левого желудочка в левое предсердие.
Стеноз устья аорты : Клинические признаки ( клиника стеноза устья аорты ).
Стеноз устья аорты редко сопровождается гемодинамическими или клиническими проявлениями до тех пор, пока клапанное кольцо не сужается до величины, составляющей около 30 % от нормы. В противоположность стенозу левого атриовентрикулярного отверстия, клинические проявления которого нарастают быстро, как только обструкция становится достаточно выраженной (так как камера, расположенная непосредственно над суженным клапаном, т. е. левое предсердие, обладает слабыми компенсаторными возможностями), стеноз устья аорты может существовать годам" без каких-либо клинических проявлений. Это объясняется способностью гипертрофированного левого желудочка поддерживать внутрижелудочковое давление на повышенном уровне, а также наличием нормально функционирующего левого предсердно-желудочкового клапана.
У большинства больных с чистым или преобладающим стенозом устья аорты степень обструкции с годами постепенно увеличивается, однако клинически порок у них не проявляется до возраста 50-70 лет. Основные симптомы стеноза устья аорты - одышка при физической нагрузке, стенокардия, синкопе. Течение болезни часто характеризуется подспудно нарастающими одышкой и утомляемостью, которые постепенно ограничивают работоспособность больных. Одышка является в первую очередь следствием повышенного давления в легочных капиллярах, которое в свою очередь вызвано повышением давления в левом предсердии и конечно-диастолического давления в левом желудочке. Стенокардия обычно развивается несколько позже, она отражает дисбаланс между увеличенной потребностью миокарда в кислороде и сниженной его доставкой. Первое является следствием увеличения массы миокарда и внутрижелудочкового давления, в то время как последнее может быть результатом сопутствующей ишемической болезни сердца, нередко встречающейся у больных со стенозом устья аорты, либо результатом компрессии венечных артерий гипертрофированным миокардом. Следовательно, стенокардия при выраженном стенозе может возникать и без наличия обструкции венечных артерий, однако отсутствие стенокардии обычно свидетельствует о малой вероятности значительных изменений в венечных артериях. Синкопе при физической нагрузке может быть следствием понижения артериального давления, вызванного вазодилатацией в работающих мышцах и неадекватной вазоконстрикцией в нефункционирующих мышцах в условиях фиксированного сердечного выброса, либо следствием внезапного снижения сердечного выброса, вызванного нарушениями ритма.
Поскольку в состоянии покоя нормальный сердечный выброс обычно поддерживается достаточно долгое время, такие симптомы сниженного сердечного выброса, как выраженная утомляемость, слабость, периферический цианоз, появляются лишь в далеко зашедших стадиях болезни. Ортопноэ, пароксизмальная одышка в ночное время, отек легких - проявления левожелудочковой недостаточности - также развиваются в выраженных стадиях болезни. Значительная легочная гипертензия приводит к развитию правожелудочковой недостаточности и системной венозной гипертензии, гепатомегалии, мерцательной аритмии и недостаточности правого предсердно-желудочкового клапана. Появление всех этих симптомов, как правило, свидетельствует о вступлении болезни в предтерминальную стадию.
При одновременном существовании стеноза устья аорты и стеноза левого атриовентрикулярного отверстия последний маскирует многие клинические проявления первого. Уменьшение сердечного выброса, наблюдающееся при стенозе левого атриовентрикулярного отверстия, приводит к снижению градиента давления по обе стороны клапана аорты, более резкому развитию приступов стенокардии, задерживает появление выраженной гипертрофии левого желудочка. С другой стороны, при таком сочетании могут наблюдаться симптомы, считающиеся более характерными для стеноза левого атриовентрикулярного отверстия, такие как застой в легких и кровохарканье. Физикальное, электрокардиографическое, радиологическое и эхокардиографическое исследования у больных со стенозом устья аорты и стенозом левого атриовентрикулярного отверстия выявляют более выраженные- признаки увеличения левого желудочка, чем при чистом стенозе левого атриовентрикулярного отверстия. Катетеризация левых отделов сердца помогает выявить преимущественное поражение того или иного клапана.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Аортальный стеноз – это сужение отверстия аорты в области клапана, затрудняющее отток крови из левого желудочка. Аортальный стеноз в стадии декомпенсации проявляется головокружением, обмороками, быстрой утомляемостью, одышкой, приступами стенокардии и удушья. В процессе диагностики аортального стеноза учитываются данные ЭКГ, эхокардиографии, рентгенографии, вентрикулографии, аортографии, катетеризации сердца. При аортальном стенозе прибегают к баллонной вальвулопластике, протезированию аортального клапана; возможности консервативного лечения при данном пороке весьма ограничены.
МКБ-10


Общие сведения
Аортальный стеноз или стеноз устья аорты характеризуется сужением выносящего тракта в области полулунного клапана аорты, в связи с чем затрудняется систолическое опорожнение левого желудочка и резко возрастает градиент давления между его камерой и аортой. На долю аортального стеноза в структуре других пороков сердца приходится 20–25%. Стеноз устья аорты в 3–4 раза чаще выявляется у мужчин, чем у женщин. Изолированный аортальный стеноз в кардиохирургии встречается редко – в 1,5-2% наблюдений; в большинстве случаев данный порок сочетается с другими клапанными дефектами - митральным стенозом, аортальной недостаточностью и др.

Причины
Приобретенный аортальный стеноз чаще всего обусловлен ревматическим поражением створок клапанов. При этом заслонки клапана деформируются, сращиваются между собой, становятся плотными и ригидными, приводя к сужению клапанного кольца. Причинами приобретенного стеноза устья аорты также могут служить:
- атеросклероз аорты;
- кальциноз (обызвествление) аортального клапана;
- инфекционный эндокардит;
- болезнь Педжета;
- системная красная волчанка;
- ревматоидный артрит;
- терминальная почечная недостаточность.
Врожденный аортальный стеноз наблюдается при врожденном сужении устья аорты или аномалии развития - двустворчатом аортальном клапане. Врожденный порок аортального клапана обычно проявляется в возрасте до 30 лет; приобретенный – в более старшем возрасте (обычно после 60 лет). Ускоряют процесс формирования аортального стеноза курение, гиперхолестеринемия, артериальная гипертензия.
Патогенез
При аортальном стенозе развиваются грубые нарушения внутрисердечной, а затем и общей гемодинамики. Это связано с затрудненным опорожнением полости левого желудочка, ввиду чего происходит значительное увеличение градиента систолического давления между левым желудочком и аортой, который может достигать от 20 до 100 и более мм рт. ст.
Функционирование левого желудочка в условиях повышенной нагрузки сопровождается его гипертрофией, степень которой, в свою очередь, зависит от выраженности сужения аортального отверстия и времени существования порока. Компенсаторная гипертрофия обеспечивает длительное сохранение нормального сердечного выброса, сдерживающего развитие сердечной декомпенсации.
Однако при аортальном стенозе достаточно рано наступает нарушение коронарной перфузии, связанное с повышением конечного диастолического давления в левом желудочке и сдавлением гипертрофированным миокардом субэндокардиальных сосудов. Именно поэтому у пациентов с аортальным стенозом признаки коронарной недостаточности появляются задолго до наступления сердечной декомпенсации.
По мере снижения сократительной способности гипертрофированного левого желудочка, уменьшается величина ударного объема и фракции выброса, что сопровождается миогенной левожелудочковой дилатацией, повышением конечного диастолического давления и развитием систолической дисфункции левого желудочка. На этом фоне повышается давление в левом предсердии и малом круге кровообращения, т. е. развивается артериальная легочная гипертензия.

Классификация
По происхождению различают врожденный (3-5,5%) и приобретенный стеноз устья аорты. С учетом локализации патологического сужения аортальный стеноз может быть подклапанным (25-30%), надклапанным (6-10%) и клапанным (около 60%).
Степень выраженности аортального стеноза определяется по градиенту систолического давления между аортой и левым желудочком, а также площади клапанного отверстия.
- При незначительном аортальном стенозе I степени площадь отверстия составляет от 1,6 до 1,2 см² (при норме 2,5—3,5 см²); градиент систолического давления находится в пределах 10–35 мм рт. ст.
- Об умеренном аортальном стенозе II степени говорят при площади клапанного отверстия от 1,2 до 0,75 см² и градиенте давления 36–65 мм рт. ст.
- Тяжелый аортальный стеноз III степени отмечается при сужении площади клапанного отверстия менее 0,74 см² и увеличении градиента давления свыше 65 мм рт. ст.
В зависимости от степени гемодинамических нарушений аортальный стеноз может протекать по компенсированному или декомпенсированному (критическому) клиническому варианту, в связи с чем выделяется 5 стадий.
- I стадия (полная компенсация). Аортальный стеноз может быть выявлен только аускультативно, степень сужения устья аорты незначительна. Больным необходимо динамическое наблюдение кардиолога; хирургическое лечение не показано.
- II стадия (скрытая сердечная недостаточность). Предъявляются жалобы на быструю утомляемость, одышку при умеренной физической нагрузке, головокружение. Признаки аортального стеноза определяются по данным ЭКГ и рентгенографии, градиент давления в диапазоне 36–65 мм рт. ст., что служит показанием к хирургической коррекции порока.
- III стадия (относительная коронарная недостаточность). Типично усиление одышки, возникновение стенокардии, обмороков. Градиент систолического давления превышает 65 мм рт. ст. Хирургическое лечение аортального стеноза на данной стадии возможно и необходимо.
- IV стадия (выраженная сердечная недостаточность). Беспокоит одышка в покое, ночные приступы сердечной астмы. Хирургическая коррекция порока в большинстве случаев уже исключена; у некоторых больных кардиохирургическое лечение потенциально возможно, но с меньшим эффектом.
- V стадия (терминальная). Неуклонно прогрессирует сердечная недостаточность, выражены одышка и отечный синдром. Медикаментозное лечение позволяет добиться лишь кратковременного улучшения; хирургическая коррекция аортального стеноза противопоказана.
Симптомы аортального стеноза
На стадии полной компенсации аортального стеноза больные длительное время не ощущают заметного дискомфорта. Первые проявления связаны с сужением устья аорты приблизительно до 50% ее просвета и характеризуются одышкой при физической нагрузке, быстрой утомляемостью, мышечной слабостью, ощущением сердцебиений.
На этапе коронарной недостаточности присоединяются головокружение, обмороки при быстрой смене положения тела, приступы стенокардии, пароксизмальная (ночная) одышка, в тяжелых случаях - приступы сердечной астмы и отек легких. Прогностически неблагоприятно сочетание стенокардии с синкопальными состояниями и особенно – присоединение сердечной астмы. При развитии правожелудочковой недостаточности отмечаются отеки, ощущение тяжести в правом подреберье.
Осложнения
Внезапная сердечная смерть при аортальном стенозе наступает в 5–10% случаев, главным образом, у лиц пожилого возраста с выраженным сужением клапанного отверстия. Осложнениями аортального стеноза могут являться инфекционный эндокардит, ишемические нарушения мозгового кровообращения, аритмии, АВ-блокады, инфаркт миокарда, желудочно-кишечные кровотечения из нижних отделов пищеварительного тракта.
Диагностика
- ЭФИ сердца. Изменение тона и патологические шумы также регистрируются при фонокардиографии. По данным ЭКГ определяются признаки гипертрофии левого желудочка, аритмии, иногда – блокады.
- Рентген. В период декомпенсации на рентгенограммах выявляется расширение тени левого желудочка в виде удлинения дуги левого контура сердца, характерная аортальная конфигурация сердца, постстенотическая дилатация аорты, признаки легочной гипертензии. Вентрикулография необходима для выявления сопутствующей митральной недостаточности. Аортография и коронарография применяются для дифференциальной диагностики аортального стеноза с аневризмой восходящего отдела аорты и ИБС.
- УЗИ сердца. На эхокардиографии определяется утолщение заслонок аортального клапана, ограничение амплитуды движения створок клапана в систолу, гипертрофия стенок левого желудочка.
- Катетеризация сердца. С целью измерения градиента давления между левым желудочком и аортой выполняется зондирование полостей сердца, которое позволяет косвенно судить о степени аортального стеноза.

Лечение аортального стеноза
Консервативная тактика
Все пациенты, в т.ч. с бессимптомным, полностью компенсированным аортальным стенозом, должны находиться под тщательным наблюдением кардиолога. Им рекомендуются проведение ЭхоКГ каждые 6-12 месяцев. Данному контингенту больных с целью профилактики инфекционного эндокардита необходим превентивный прием антибиотиков перед стоматологическими (лечение кариеса, удаление зубов и т. д.) и другими инвазивными процедурами.
Ведение беременности у женщин с аортальным стенозом требует тщательного контроля показателей гемодинамики. Показанием к прерыванию беременности служит тяжелая степень аортального стеноза или нарастание признаков сердечной недостаточности. Медикаментозная терапия при аортальном стенозе направлена на устранение аритмий, профилактику ИБС, нормализацию АД, замедление прогрессирования сердечной недостаточности.
Хирургическое лечение
Радикальная хирургическая коррекция аортального стеноза показана при первых клинических проявлениях порока – появлении одышки, ангинозных болей, синкопальных состояний. С этой целью может применяться баллонная вальвулопластика - эндоваскулярная балонная дилатация аортального стеноза. Однако зачастую данная процедура бывает малоэффективна и сопровождается последующим рецидивом стеноза. При негрубых изменениях створок аортального клапана (чаще у детей с врожденным пороком) используется открытая хирургическая пластика аортального клапана (вальвулопластика). В детской кардиохирургии нередко выполняется операция Росса, предполагающая пересадку клапана легочной артерии в аортальную позицию.
При соответствующих показаниях прибегают к проведению пластики надклапанного или подклапанного аортального стеноза. Основным методом лечения аортального стеноза на сегодняшний день остается протезирование аортального клапана, при котором пораженный клапан полностью удаляется и заменяется на механический аналог или ксеногенный биопротез. Пациентам с искусственным клапаном требуется пожизненный прием антикоагулянтов. В последние годы практикуется перкутанная замена аортального клапана.
Прогноз и профилактика
Аортальный стеноз может протекать бессимптомно в течение многих лет. Появление клинических симптомов существенно увеличивает риск осложнений и летальности. Основными, прогностически значимыми симптомами служат стенокардия, обмороки, левожелудочковая недостаточность – в этом случае средняя продолжительность жизни не превышает 2-5 лет. При своевременном оперативном лечении аортального стеноза 5-летняя выживаемость составляет около 85%, 10-летняя — порядка 70%.
Меры профилактики аортального стеноза сводятся к предупреждению ревматизма, атеросклероза, инфекционного эндокардита и др. способствующих факторов. Больные с аортальным стенозом подлежат диспансеризации и наблюдению кардиолога и ревматолога.
3. Современные подходы к диагностике аортального стеноза/ Синькво А.В.// Сибирский медицинский журнал (Иркутск). - 2017.
Для цитирования: Карпова Н.Ю., Рашид М.А., Казакова Т.В., Шостак Н.А. Аортальный стеноз. РМЖ. 2014;2:162.
Распространенность аортального стеноза (АС), по данным разных авторов, колеблется от 3–4 до 7%. С возрастом частота выявления данного порока возрастает, составляя 15–20% у лиц старше 80 лет. Причем с увеличением продолжительности жизни встречаемость АС в популяции также будет увеличиваться. Он чаще наблюдается у представителей мужского пола (2,4:1), однако в старшей возрастной подгруппе преобладают женщины. За последние 30 лет этиология аортальных клапанных пороков изменилась. В то время как распространенность постревматических поражений аортального клапана (АК) снизилась с 30 до 18%, частота оперативной коррекции двухстворчатых АК – с 37 до 33%, отмечено увеличение частоты кальцинированного аортального стеноза (КАС) с 30 до 46%, в особенности у лиц старше 65 лет. Указанное обстоятельство обусловливает трудности в диагностике, заключающиеся в стертости клинических симптомов (вследствие наличия ассоциированных заболеваний, особенно у лиц пожилого возраста) и затруднениях в интерпретации результатов инструментальных исследований. В то же время своевременное выявление симптомов заболевания является краеугольным камнем ведения больных с АС, поскольку их появление резко ускоряет прогрессирование порока, утяжеляет состояние больных и значимо снижает среднюю продолжительность и качество жизни. Также появление симптомов АС является абсолютным показанием к проведению кардиохирургической коррекции порока.
Классификация аортального стеноза
АС подразделяется по происхождению на врожденный и приобретенный, по объему поражения – на изолированный и сочетанный, по локализации – на клапанный, надклапанный, подклапанный или же вызванный гипертрофической кардиомиопатией.
Врожденными пороками развития АК могут быть одностворчатые, двухстворчатые или трехстворчатые клапаны или наличие куполообразной диафрагмы.
- Одностворчатый клапан вызывает выраженную обструкцию уже в грудном возрасте и является причиной смерти детей до 1 года.
- Стеноз врожденного двухстворчатого клапана приводит к появлению турбулентного тока крови, травмирующего створки клапана, что в последующем ведет к фиброзированию, увеличению жесткости и кальцификации створок и сужению аортального отверстия у взрослых.
- Врожденно-измененный трехстворчатый клапан характеризуется наличием неравномерных по размеру створок с признаками сращения по комиссурам. При этом турбулентный ток крови, вызванный умеренным врожденным дефектом, может приводить к фиброзу и, в конечном счете, – к кальцификации и АС.
Среди приобретенных форм АС выделяют:
Патофизиология
В ответ на возникновение механической обструкции изгнанию крови и повышение систолического напряжения стенки ЛЖ развивается его концентрическая гипертрофия, которая позволяет создавать дополнительный градиент давления на АК без уменьшения сердечного выброса, расширения полости ЛЖ, не сопровождающаяся клиническими симптомами. С течением времени, учитывая неоднородный характер гипертрофированных миоцитов и увеличение выраженности механической обструкции, присоединяется левожелудочковая недостаточность, обусловленная расширением камер левых отделов сердца и развитием венозного полнокровия в малом круге кровообращения. На поздних стадиях заболевания происходит снижение сердечного выброса, ударного объема и, соответственно, градиента давления.
Наряду с увеличением содержания коллагена в миокарде, характерным для многих кардиальных заболеваний, при АС происходит изменение его поперечной исчерченности, что ведет к увеличению массы миокарда, нарастанию диастолической жесткости и нарушению диастолической функции, в результате которой для полноценного заполнения камер ЛЖ требуется большее внутриполостное давление. Клинически это ассоциируется с внезапным развитием эпизодов отека легких у больных с АС без явных провоцирующих факторов.
Дальнейшее прогрессирование ГЛЖ может приводить к нарушению оксигенации миокарда у пациентов с критическим АС даже при отсутствии выраженных изменений в коронарных артериях. Основным субстратом ишемии миокарда при АС, как и при других заболеваниях сердца, является дисбаланс между потреблением кислорода и возможностью его доставки.
Повышение потребности миокарда в кислороде обусловлено:
- увеличением массы миокарда за счет гипертрофии ЛЖ;
- повышением систолического напряжения стенки ЛЖ;
- удлинением времени изгнания крови из полости ЛЖ.
Нарушение доставки кислорода по коронарным артериям вызывается:
- превышением давления, сжимающего коронарные артерии извне, над перфузионным давлением внутри коронарных сосудов;
- укорочением диастолы.
Дополнительными факторами, снижающими перфузию миокарда ЛЖ, являются:
- относительное уменьшение плотности капилляров;
- увеличение конечного диастолического давления в полости ЛЖ, приводящее к уменьшению перфузионного давления в коронарных артериях.
Клинические проявления АС
В течении АС у взрослых существует длительный латентный период, во время которого происходит постепенное увеличение обструкции и перегрузки давлением миокарда ЛЖ при полном отсутствии каких-либо симптомов. Кардиальные проявления приобретенного АС появляются обычно на пятой или шестой декаде жизни и представлены в виде стенокардии, обмороков, одышки и, в конечном счете, сердечной недостаточности.
Стенокардия наблюдается приблизительно у 2/3 пациентов с критическим АС (около половины из которых имеют выраженную обструкцию коронарных сосудов). Клиническая картина сходна с проявлениями стенокардии в рамках ИБС. Приступы возникают при физической нагрузке и прекращаются в состоянии покоя.
В отсутствие стенозирующего коронаросклероза стенокардия у больных АС возникает при определенном сочетании трех факторов:
- уменьшение продолжительности диастолы;
- увеличение частоты сердечных сокращений;
- снижение просвета коронарных сосудов.
Убедительным доказательством указанного феномена является факт исчезновения стенокардии непосредственно после проведения протезирования аортального клапана (ПАК).
Синкопальные состояния (обмороки) являются вторым классическим признаком выраженного АС. При этом под синкопальным состоянием подразумевают преходящую потерю сознания, вызванную неадекватной перфузией головного мозга кровью, обогащенной достаточным количеством кислорода. Нередко у больных АС эквивалентом синкопальных состояний являются головокружения или приступы необъяснимой слабости. Выделяют несколько причин развития обморочных состояний (головокружений) при АС:
- обструкция выходного тракта ЛЖ;
- нарушения ритма и проводимости;
- снижение вазомоторного тонуса;
- синдром гиперчувствительности каротидного синуса;
- гиперактивация механорецепторов ЛЖ;
- возрастное снижение количества пейсмейкерных клеток (КАС).
Редким ассоциированным симптомом АС являются желудочно-кишечные кровотечения, как идиопатические, так и вследствие ангиодисплазии сосудов подслизистой оболочки кишечника, описанные Heyde в 1958 г. Наиболее часто источником кровотечения является восходящий отдел ободочной кишки. Особенностью данных кровотечений является их исчезновение после хирургической коррекции порока.
Диагностика
Объективными признаками тяжелого АС являются: разлитой верхушечный толчок, замедление и уменьшение пульса на сонных артериях, уменьшение интенсивности аортального компонента в формировании 2-го тона сердца с возможным его парадоксальным расщеплением, систолический шум изгнания над аортой.
Систолический шум при АС характеризуется грубым характером, возникновением вскоре после первого тона, увеличением по интенсивности и достижением пика к середине систолы с последующим ослаблением и исчезновением непосредственно перед 2-м тоном. Шум лучше всего выслушивается на основании сердца. Он хорошо проводится на сосуды шеи.
Особенностями систолического шума при кальцинированном АС у пожилых лиц являются:
- снижение его интенсивности;
- изменением тембра с грубого на мягкий;
- смещение аускультативного максимума на верхушку сердца (симптом Галавердена).
Последнее обстоятельство приводит врача общей практики к ошибочной трактовке аускультативной картины как проявления относительной митральной регургитации в рамках ХСН.
Электрокардиография. Основным ЭКГ-признаком АС является гипертрофия миокарда ЛЖ. В то же время ее отсутствие не исключает наличия даже критического АС, в особенности у лиц пожилого возраста. Часто отмечаются инверсия волны Т и депрессия сегмента ST в отведениях с вертикальным положением желудочкового комплекса (причина которых описана выше). Нередко выявляется депрессия сегмента ST больше, чем на 0,2 mV, что является косвенным признаком сопутствующей ГЛЖ. Изредка могут отмечаться инфарктоподобные изменения ЭКГ, заключающиеся в уменьшении амплитуды зубца R в правых грудных отведениях, что также служит причиной гипердиагностики ИБС.
Фибрилляция предсердий и/или различные варианты внутрижелудочковых блокад свидетельствуют в пользу сопутствующего кальциноза митрального клапана.
При проведении рентгенографии органов грудной клетки обычно выявляют аортальную конфигурацию сердца, кальциноз АК и постстенотическую дилатацию аорты, больше характерную для бикуспидального АС. На поздних стадиях отмечаются дилатация полости ЛЖ и признаки застоя в легких. При сопутствующем поражении митрального клапана отмечается расширение левого предсердия.
Базовым методом диагностики АС является дуплексное эхокардиографическое исследование (2ДЭхоКГ), целями проведения которого являются (класс I):
- диагностика и оценка тяжести АС (уровень доказательности В);
- оценка выраженности ГЛЖ, размеров камер и функции ЛЖ (уровень доказательности В);
- динамическое обследование пациентов с установленным АС при изменении выраженности клинических признаков или симптомов (уровень доказательности В);
- оценка тяжести порока и функции ЛЖ у пациенток с установленным АС во время беременности (уровень доказательности В);
- динамическое наблюдение за бессимптомными пациентами: ежегодно при тяжелом АС; каждые 1–2 года – при среднетяжелом и каждые 3–5 лет – при легком АС (уровень доказательности В).
Тяжесть АС оценивается по критериям, представленным в таблице 1.
Естественное течение
Лечение
- профилактика внезапной смерти и сердечной недостаточности;
- облегчение симптомов заболевания и улучшение качества жизни.
Медикаментозное лечение
Назначают неоперабельным пациентам вследствие сопутствующей патологии. Выбор консервативной тактики у больных КАС ограничен и направлен на уменьшение выраженности клинических симптомов. Применяют препараты следующих классов:
- b-блокаторы (при площади отверстия аортального клапана >0,8 см2) и нитраты (с осторожностью) – при стенокардии. Наиболее предпочтительными препаратами являются бисопролол, карведилол и метопролол;
- дигоксин (при мерцательной тахиаритмии и/или фракции выброса 25–30% и ниже);
- диуретики (с осторожностью при ХСН);
- ингибиторы АПФ (тщательное титрование дозы).
При возникновении отека легких показано введение в условиях блока интенсивной терапии нитропруссида натрия для уменьшения застойных явлений и улучшения функции ЛЖ. Антиаритмические препараты III класса назначаются при возникновении фибрилляции предсердий после неэффективной кардиоверсии для контроля частоты сокращений желудочков сердца.
Показания к хирургическому лечению
Ведущим методом оперативной коррекции АС является ПАК.
Абсолютным показанием к проведению ПАК является наличие доказанного тяжелого АС по данным 2ДЭхоКГ в сочетании с клиническими симптомами и/или систолической дисфункцией ЛЖ, планируемым проведением АКШ или иных оперативных вмешательств на аорте и/или других клапанах сердца (класс I).
В остальных случаях к определению показаний подходят индивидуально, с учетом не только тяжести порока и клинической картины, но и выраженности кальциноза клапанов, наличия факторов быстрого прогрессирования заболевания (возраст, ассоциированные состояния, включая ИБС), а также доступности высокотехнологичной кардиохирургической помощи (класс II).
К сожалению, большинство врачей общей практики считают, что левожелудочковая недостаточность, пожилой возраст, ассоциированные состояния, а также улучшение соматического статуса после начала консервативной терапии являются противопоказаниями для проведения ПАК. Такой подход нельзя считать оправданным, поскольку своевременное проведение оперативного вмешательства вне зависимости от возраста существенно увеличивает продолжительность жизни и улучшает ее качество.
Антитромботическая терапия у больных КАС
Все пациенты с механическими протезами нуждаются в назначении пожизненной терапии варфарином (табл. 2). Ацетилсалициловая кислота (АСК) рекомендована всем больным с искусственными клапанами сердца, в т. ч. в виде монотерапии – у пациентов с биологическими клапанами без факторов риска и в сочетании с варфарином – у больных с механическими клапанами, а также у больных с биологическими протезами при наличии факторов риска. При наличии высокого риска и невозможности приема АСК рекомендовано добавление клопидогрела (75 мг/сут) к варфарину. Однако даже на фоне приема антикоагулянтов у оперированных больных пожизненный риск развития тромбоэмболий сохраняется в пределах от 1 до 2% в год, что существенно ниже, чем при отсутствии терапии варфарином. При биологических протезах тромбогенный риск составляет в среднем 0,7% в год.
Таким образом, назначение антитромботической терапии требует соответствующего обучения пациента и должно быть индивидуальным в каждом конкретном случае (табл. 2).
При АС профилактика инфекционного эндокардита проводится по стандартным схемам исключительно 2-м категориям пациентов: после проведения ПАК с имплантацией искусственного клапана сердца и ранее перенесшим инфекционный эндокардит.
Ведение послеоперационных пациентов
А. Первый врачебный осмотр
Наряду со сбором анамнеза и объективным исследованием включает в себя: ЭКГ, рентгенографию органов грудной клетки, 2ДЭхоКГ, клинический анализ крови, азот мочевины/креатинин, ЛДГ и МНО (если необходимо). Цель обследования – оценка функции искусственного клапана, выявление инфекции, инфаркта миокарда, нарушений проводимости или клапанных нарушений.
Б. Последующее ведение пациентов с неосложненным течением послеоперационного периода
Интервалы осмотра определяются потребностями пациента. При неосложненном течении они составляют 1 раз в год и включают в себя сбор жалоб, объективное исследование, а также в определенных случаях – проведение ЭКГ и рентгенологического исследования грудной клетки. Дополнительные тесты включают в себя концентрацию гемоглобина, гематокрит и ЛДГ. При отсутствии признаков дисфункции ЛЖ, дисфункции искусственного или других клапанов сердца проведение 2ДЭхоКГ не показано. Однако, как только возникает подозрение на появление нового шума в сердце или изменяется клинический статус пациента, 2ДЭхоКГ проводится каждые 3–6 мес.
В. Последующее ведение пациентов с осложненным течением послеоперационного периода
Пациенты с систолической дисфункцией ЛЖ после проведения хирургического вмешательства на клапанах сердца должны получать соответствующую стандартную терапию. Лечение должно быть продолжено даже в случае нивелирования или уменьшения симптомов систолической дисфункции ЛЖ.
Дисфункция ЛЖ или явные признаки сердечной недостаточности после протезирования клапанов сердца могут быть следствием:
- существовавшей до операции дисфункции ЛЖ, проявления которой могут оставаться неизменными или уменьшаться лишь частично в последующем;
- периоперационного повреждения миокарда;
- прогрессирования заболеваний других клапанов сердца;
- осложнений, связанных с искусственными клапанами сердца;
- сопутствующих заболеваний сердца, таких как ИБС и АГ.
Пациентам, у которых не наблюдается улучшения или отмечается ухудшение функционального статуса после оперативного вмешательства, для выявления причины показано проведение соответствующих тестов, включающих ДЭхоКГ, и, если необходимо, – трансэзофагеальное ЭхоКГ и катетеризацию сердца с ангиографией. Пациенты с послеоперационной систолической дисфункцией ЛЖ, даже при отсутствии симптомов, должны получать стандартную терапию, проведение которой не следует прекращать после улучшения функционального статуса. В этом случае пациентам должен проводиться весь комплекс мер первичной и вторичной профилактики для уменьшения риска сердечно-сосудистых событий в будущем.
Учитывая затруднения, возникающие у практикующих врачей и особенности МКБ Х пересмотра, ниже мы приводим примеры формулировки клинического диагноза различных вариантов АС.
I 35.0 Кальцинированный аортальный (клапанный) стеноз легкой (средней, тяжелой) степени, бессимптомная (декомпенсированная) форма. НК IIА, ФК III (NYHA).
I 06.2 Ревматическая болезнь сердца: сочетанный аортальный порок с преобладанием стеноза (или недостаточности) АК. НК I, ФК II (NYHA).
Q 23.1 Врожденный двухстворчатый АК со стенозом (и/или недостаточностью), стеноз легкой (средней, тяжелой) степени, бессимптомная (декомпенсированная) форма. НК IIА, ФК III (NYHA).
Читайте также:

