Общие сведения о воде кратко
Обновлено: 05.07.2024

Интересные факты о воде
Вода — самая удивительная и загадочная из всех жидкостей, существующих на Земле.
Учёные на протяжении многих столетий продолжают проводить исследования, находя новые интересные факты. Каждый человек знает, что без воды жизнь невозможна.
Вода участвует в формировании климата, для многих живых организмов является средой обитания. Её важность сложно недооценить. Не случайно, нашу планету называют голубой, именно вода покрывает 71 % поверхности земного шара.
В статье мы собрали самую важную и интересную информацию про воду: гипотезы её появления на нашей планете, особенности строения молекулы, агрегатные состояния, уникальные и необычные свойства.
Что такое вода, химические названия
Вода — это бинарное неорганическое соединение, химическая формула H2O.
При нормальных условиях представляет собой прозрачную, бесцветную жидкость, которая не имеет вкуса и запаха, текуча (принимает форму сосуда).
Молекула воды состоит из одного атома кислорода и двух атомов водорода, которые соединены между собой ковалентной связью. Никакие другие элементы таблицы Менделеева при соединении не образуют жидкости. Рассмотрим строение молекулы H2O на изображении.

Вода имеет несколько химических названий:
- оксид водорода;
- гидроксид водорода;
- монооксид дигидрогена;
- дигидромонооксид;
- гидроксильная кислота.
Агрегатные состояния
Из всех веществ, существующих на Земле, только вода может иметь три принципиально разных агрегатных состояния: жидкое, газообразное и твердое. Благодаря трём агрегатным состояниям происходит круговорот воды в природе и жизнь на Земле. Рассмотрим подробнее каждое агрегатное состояние.
- Жидкое (вода). В нормальных условиях вода является жидкостью. Образует мировой океан, реки, ручьи и т.д.
- Газообразное (водяной пар) — это бесцветный газ, не имеет вкуса и запаха. Испаряется с поверхности океанов, рек, болот, почвы, растений и поступает в воздух или образуется путём кипения жидкой воды или сублимации из льда. Сублимация — переход вещества из твёрдого состояния сразу в газообразное, минуя стадию плавления (перехода в жидкое состояние).
- Твердое (лёд). При температуре от нуля и ниже вода превращается в лёд. В холодное время года он сковывает реки и лужи, выпадает в виде осадков: снежинок, града, инея, образует ледяные облака. Встречается в виде ледников и айсбергов.
Строение в различных агрегатных состояниях
Жидкая вода, лёд и водяной пар имеют один и тот же состав, но разные состояния.
Рассмотрим строение молекулы на изображении.

Многочисленные исследования ученых подтверждают, что по структуре вода и лед близки друг к другу. Структура льда – это решетчатый каркас. Структура воды зависит от содержания разных веществ, которые в ней растворяются, а также от нерастворимых соединений и некоторых других факторов.
При температуре близкой к точке замерзания, молекулы жидкой воды собираются в небольшие группы, практически так, как в кристаллах. При температуре близкой к точке кипения они располагаются более свободно.
Свойства
Вода — уникальный природный компонент, который обладает рядом свойств. Рассмотрим основные:
- не имеет цвета, запаха и вкуса;
- распространенный растворитель;
- обладает высоким поверхностным натяжением, уступая в этом только ртути;
- имеет большую теплоту испарения (используется для терморегуляции);
- чистая вода — хороший изолятор;
- обладает большой теплоёмкостью (увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение ее температуры);
- плотность в разных диапазонах температур меняется неодинаково.
Существуют необычные свойства. Например, в твердом виде вода легче, чем в жидком. Лёд не тонет в воде. В твёрдом состоянии частички воды располагаются по порядку, между ними остается много свободного пространства. Когда лёд тает, активность частичек повышается, свободное пространство заполняется. Жидкая форма становится более тяжелой, нежели твердая.
Такая уникальная способность даёт возможность любому водоёму не замерзать по всей глубине. Даже при самом сильном морозе температура воды у дна не опускается ниже +4 ᵒС. Все живые существа (рыбы и другие) могут спокойно пережить самую суровую зиму подо льдом.
Когда лёд тает, плотность увеличивается, и становится максимальной при температуре +4 ᵒС. В диапазоне от +4 ᵒС до +40 ᵒС плотность снижается, потом снова увеличивается. При понижении температуры ниже +4 ᵒС плотность уменьшается, т.е. при замерзании вода расширяется.
Горячая вода замерзает быстрее, чем холодная. Это связано с большей скоростью испарения и излучения тепла.
Теплоемкость и некоторые другие физические свойства воды тоже зависят от температуры неодинаково. Другие виды жидкостей не имеют таких особенностей – чтобы какой-то один параметр менялся по-разному на разных порогах температуры.
Круговорот воды в природе
Вода образует водную оболочку нашей планеты – гидросферу.
Её делят на Мировой океан, континентальные поверхностные воды и ледники, а также подземные водоёмы. Переходы H2O из одних частей гидросферы в другие составляют сложный круговорот воды на Земле
Круговорот воды в природе — это непрерывное движение воды в гидросфере Земли. В процессе этого обмена водная масса меняет агрегатное состояние: из жидкой или твердой превращается в газообразную и обратно.
Рассмотрим на примере.
- С поверхности океанов, морей, рек и суши вода в виде пара поднимается вверх.
- Высоко над землей он охлаждается и образует множество водяных капелек и льдинок. Из них образуются облака.
- В виде осадков вода возвращается на Землю.
Происхождение воды на планете
Возникновение воды на нашей планете является предметом научных споров. Существует 2 основные гипотезы:
- Космическое происхождение. Часть учёных считают, что вода появилась вследствие падающих метеоритов, астероидов, которые содержали воду.
- Земное происхождение. Другие учёные считают, что вода образовалась на Земле во время формирования, а не занесена с космоса.
Наука о воде
Изучением природных вод, явлений и процессов занимается наука Гидрология.
Первые упоминания о гидрологии появились на заре истории человечества около 6000 лет назад.
Начало гидрологических наблюдений в России относится к XV–XVI вв.: в записях русских летописцев сохранились сведения о свойствах воды, наводнениях, паводках, замерзании.
Значение на Земле
Без воздуха человек может прожить несколько секунд, без еды – несколько месяцев, без воды – максимум несколько суток. Снижение содержания воды в организме всего лишь на 2% может вызвать сильную слабость. При нехватке 8% уже может возникнуть серьезное недомогание, а при 12% – смерть.
Каждая клетка живого организма состоит из жидкости и нуждается в регулярном пополнении. Без воды не проживут ни люди, ни растения, ни животные.
Вода формирует климат, участвует в круговороте воды в природе, для многих живых организмов является средой обитания.
Применение
Все люди на планете прекрасно знают, что жизнь без воды невозможна. Любое начало жизни изначально зарождается в воде.
Человек применяет воду:
- для поддержании жизни (приготовления пищи, обеспечения организма водой);
- для бытовых нужд (гигиены, уборки и т. д);
- в сельском хозяйстве и животноводстве;
- промышленности (используется при производстве продуктов питания, чугуна, стали, резины и т. д);
- медицине;
- химии (в качестве реагента для химических реакций, опытов, исследований);
- рыболовстве;
- для транспортировки людей и грузов;
- для спорта;
- в земледелии;
- для пожаротушения;
- служит источником энергии (электростанции).
Сколько жидкости в теле человека

Эмбрион человека состоит из жидкости не менее, чем на 97%. Когда ребенок рождается, вода составляет около 80% его тела. В первые несколько суток после рождения этот показатель существенно снижается.
В дальнейшем содержание воды в организме человека постоянно уменьшается. В пожилом возрасте в теле человека доля воды не превышает 50-60%.
Как определить, сколько воды в теле человека?
Массу тела необходимо разделить на 3 и умножить на 2.
Стоит отметить, что расчет считается приблизительным (может отличаться на 5-10%) Так как количество воды зависит от возраста, пола, физической активности, состояния здоровья.
Основные функции
Вода необходима каждому живому существу. Каждый живой организм состоит из клеток. Ключевую роль выполняет вода. Она составляет около 70 процентов от её массы. Рассмотрим кратко основные функции.
- Растворитель. Большинство химических реакций протекают только в водной среде.
- Транспортная функция. Переносит питательные вещества из одной части в другую.
- Функция регенерации. С помощью воды удаляются ненужные продукты жизнедеятельности.
- Регулирует терморегуляцию. Защищает организм от перегрева и обеспечивает равномерное распределение тепла по организму.
- Все обменные процессы в организме регулируются водой.
Польза чистой питьевой воды
Врачи, диетологи и другие специалисты часто совершают ошибку, когда слишком много внимания уделяют разным продуктам питания и забывают про воду. Любые вещества, даже самые питательные и полезные, могут оказаться совершенно неэффективными, если нет растворителя, способного доставить их в нужные части тела. На Земле есть только один простой, надежный и распространенный растворитель – вода.
Вода участвует абсолютно во всех обменных процессах. И чтобы они протекали нормально, необходимо пить достаточное количество чистой воды. Именно воды, не чая, не напитков. Содержание разных примесей, консервантов и прочих веществ существенно меняют структуру, нормальное молекулярное состояние воды.
Изначально природой заложено употреблять чистую воду. Когда в организм вносится некая смесь, то пищеварительной системе приходится прикладывать много усилий, растрачивать много энергии, чтобы отделить все лишнее и получить воду. Кроме этого, высокое содержание сахара неизбежно провоцирует нарушение нормального обмена веществ.
Сколько нужно пить воды в день
Рекомендуется употреблять чистую воду без примесей 30-40 мл на 1 кг веса.
Средние показатели:
для женщины: 1,5 – 2 литра ежедневно;
для мужчины: 2,5 – 5 литров ежедневно.
Количество рекомендуемой нормы зависит от физической активности, климата и веса.
Процентное содержание в органах
Вода в теле человека находится в разных субстанциях и никогда не смешивается в единое целое.
Жидкости больше в тех клетках, в которых обмен веществ протекает более интенсивно. Рассмотрим таблицу № 1.
Таблица № 1. Процент содержания в органах человека
| Органы | Процент содержания |
| Мозг | 90 |
| Лёгкие | 86 |
| Печень | 86 |
| Кровь | 83 |
| Яйцеклетки | 90 |
| Кости | 72 |
| Кожа | 72 |
| Сердце | 75 |
| Желудок | 75 |
| Селезёнка | 77 |
| Почки | 83 |
| Мышцы | 75 |
Признаки обезвоживания
Если содержание воды резко меняется в одну или другую сторону, то это сразу сказывается на общем состоянии здоровья. Чрезмерное количество воды организм переносит намного легче, чем ее нехватку. Рассмотрим основные симптомы проявления нехватки воды в организме человека.
- Жажда – первый сигнал нехватки жидкости в организме.
- У человека возникают твердые каловые массы и запоры.
- Появляется усталость и слабость.
- Возникают головные боли и головокружения.
- Кожа становится сухой.
- Состояние может сопровождаться сильным упадком настроения (вплоть до тяжелой депрессии).
При длительном сохранении такого состояния могут возникнуть проблемы:
- с артериальным давлением;
- нарушением пищеварения;
- заболеваниями органов ЖКТ;
- может появиться диабет, ожирение (или наоборот – истощение, дистрофия);
- появляются зрительные и слуховые галлюцинации (при потери воды 10%);
- сильное обезвоживание может привести к смерти.
Проходя гидрологический цикл, вода может дополняться химическими элементами: ионами, растворенными газами, микроэлементами и т.д.
Воду квалифицируют по следующим признакам:
- по наличию и составу изотопов в молекуле;
- по степени растворения частиц солей и других примесей;
- по источнику;
- по взаимодействию с другими элементами и компонентами;
- по воздействию человека;
- по индивидуальным параметрам.
Рассмотрим некоторые виды на рисунке.

Запасы пресной воды
Несмотря на то, что Земля более, чем на 70% покрыта водой, лишь 1% является пресной (её солёность не превышает 0,5 ‰).
Более 2/3 запасов пресной воды на Земле хранится в ледниках. Крупнейшим водоёмом пресной воды считается озеро Байкал в России.
Показатели качества
Современные нормы очистки водопроводной питьевой воды предполагают использование хлорсодержащих реагентов, которые избавляют воду от инфекций. В дополнение рекомендуется использовать дополнительные методы очистки. Например, фильтры.
Большой популярностью в развитых странах пользуется бутилированная питьевая вода. Она является экологически чистым продуктом. Реализуется в гигиенически чистой ёмкости и соответствует всем установленным требованиям.
25 интересных фактов
Ученые постоянно исследуют оксид водорода, находя интересные факты.
- Лёд не тонет в воде. Дело в том, что плотность льда меньше чем, воды в жидком состоянии. Поэтому морские обитатели продолжают жизнедеятельность. Другие вещества увеличивают плотность при замерзании.
- Большинство загрязнений вымораживаются при образовании льда.
- Более 2/3 запасов пресной воды на Земле хранится в ледниках.
- Вёдра для воды изготавливают в форме конуса для того, чтобы их не разорвало при случайном замерзании воды.
- Теплоёмкость и некоторые другие физические свойства воды зависят от температуры не одинаково.
- Жидкая вода регулирует температуру Земли, водяной пар — влажность воздуха.
- Снег способен отражать лучи света на 75%, а вода только на 5%, поэтому снежные ночи такие светлые.
- В Антарктиде есть озеро с водой, в 11 раз солёнее морской. В нем настолько соленая вода, что не замерзает даже при — 50 С.
- Горячая вода имеет способность замерзать быстрее, чем холодная. Этот факт легко проверить самостоятельно.
- Лёд встречается на полюсах Луны, а также на полюсах Марса и Меркурия.
- В Антарктике находится самый холодный лёд, а вот самым теплым льдом считается Альпийский, так как его температура составляет 0 градусов по Цельсию.
- Температура кипения воды не всегда составляет 100 градусов по Цельсию. Показатель зависит от атмосферного давления. Например, на Эльбрусе — самой высокой вершине Европы (5642 м), — вода закипит при 80,8 °С.
- Примерно на каждые 100 метров вглубь к центру Земли температура кипения увеличивается на 3°C.
- Озеро Байкал — самое большое пресное озеро в мире.
- Для производства 1 тонны стали требуется 300 тонн воды.
- Учёные считают, что мировой океан изучен только на 2-7%.
- На 1 кг тела коровы приходится 600 грамм жидкости.
- В теле рыбы 70-80 процентов.
- В медузе больше 95 процентов.
- Растения на 50-90 процентов состоят из жидкости.
- Вода участвует в фотосинтезе растений.
- Бегемот употребляет около 250 литров воды в сутки.
- Древесное растение Эвкалипт в сутки поглощает из почвы и испаряет 320 л влаги.
- Верблюд способен выпить больше 100 литров воды менее, чем за 15 минут.
- Скалистая белка может жить без воды до 100 дней.
Заключение
Вода – удивительное вещество, обладающее химическими и физическими свойствами. Она формирует климат на планете, для многих живых организмов является средой обитания, необходима для фотосинтеза растений и жизнедеятельности всех живых организмов.


Является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы).
Вода имеет ключевое значение в создании и поддержании жизни на Земле, в химическом строении живых организмов, в формировании климата и погоды. Является важнейшим веществом для всех живых существ на планете Земля.
Содержание
Виды воды
По особенностям происхождения, состава или применения, выделяют, в числе прочего:
-
и жёсткая вода — по содержанию катионов кальция и магния
- По изотопам молекулы:
-
(по составу почти соответствует обычной) (дейтериевая)
- Сверхтяжёлая вода (тритиевая)
-
, Водопроводная вода и деионизированная вода
Химические названия воды
С формальной точки зрения вода имеет несколько различных корректных химических названий:
- Оксид водорода
- Гидроксид водорода
- Гидроксильная кислота
- Оксидан
- Дигидромонооксид
Свойства
Физические свойства
Вода в нормальных атмосферных условиях сохраняет жидкое агрегатное состояние, тогда как аналогичные водородные соединения являются газами. Это объясняется особыми характеристиками слагающих молекулы атомов и присутствием связей между ними. Атомы водорода присоединены к атому кислорода, образуя угол 104,45°, и эта конфигурация строго сохраняется. Из-за большой разности электроотрицательностей атомов водорода и кислорода электронные облака сильно смещены в сторону кислорода. По этой причине молекула воды является активным диполем, где кислородная сторона отрицательна, а водородная положительна. В результате молекулы воды притягиваются своими противоположными полюсами, и образуют полярные связи, на разрыв которых требуется много энергии [2] . В составе каждой молекулы Ион водорода (протон) не имеет внутренних электронных слоев и обладает малыми размерами, в результате чего он может проникать в электронную оболочку отрицательно поляризованного атома кислорода соседней молекулы, образуя водородную связь с другой молекулой. Каждая молекула связана с четырьмя другими посредством водородных связей — две из них образует атом кислорода и две атомы водорода [2] . Комбинация этих связей между молекулами воды — полярной и водородной и определяет очень высокую температуру её кипения и удельную теплоты парообразования [2] . В результате этих связей в водной среде возникает давление в 15-20 тыс. атмосфер, которое и объясняет причину трудносжимаемости воды, так при увеличении атмосферного давления на 1 бар, вода сжимается на 0,00005 доли её начального объёма [2] [В каких пределах изменения давления корректна эта оценка?] .
Структуры воды и льда между собой очень похожи [2] . В воде, как и во льду, молекулы стараются расположиться в определённом порядке — образовать структуру, однако тепловое движение этому препятствует. При температуре перехода в твёрдое состояние тепловое движение молекул более не препятствует образованию структуры, и молекулы воды упорядочиваются, в процессе этого объёмы пустот между молекулами увеличиваются и общая плотность воды падает, что и объясняет причину меньшей плотности воды в фазе льда. При испарении, напротив, рвутся все связи. Разрыв связей требует много энергии, отчего у воды самая большая удельная теплоёмкость среди прочих жидкостей и твёрдых веществ. Для того чтобы нагреть один литр воды на один градус, требуется затратить 4,1868 кДж энергии. Благодаря этому свойству вода нередко используется как теплоноситель. Однако удельная теплоёмкость воды, в отличие от других веществ непостоянна: при нагреве от 0 до 35 градусов Цельсия её удельная теплоёмкость падает, в то время как у других веществ она постоянна при изменении температуры. Помимо большой удельной теплоёмкости, вода также имеет большие значения удельной теплоты плавления (0 °C и 333,55 кДж/кг) и парообразования (2250 кДж/кг).
| Температура °С | Удельная теплоёмкость воды кДж/(кг*К) |
|---|---|
| -60 (лёд) | 1,64 |
| -20 (лёд) | 2,01 |
| -10 (лёд) | 2,22 |
| 0 (лёд) | 2,11 |
| 0 (чистая вода) | 4,218 |
| 10 | 4,192 |
| 20 | 4,182 |
| 40 | 4,178 |
| 60 | 4,184 |
| 80 | 4,196 |
| 100 | 4,216 |
Вода обладает также высоким поверхностным натяжением среди жидкостей, уступая в этом только ртути [3] [4] [5] [6] . Относительно высокая вязкость воды обусловлена тем, что водородные связи мешают молекулам воды двигаться с разными скоростями.
По сходным причинам вода является хорошим растворителем полярных веществ. Каждая молекула растворяемого вещества окружается молекулами воды, причём положительно заряженные участки молекулы растворяемого вещества притягивают атомы кислорода, а отрицательно заряженные — атомы водорода. Поскольку молекула воды мала по размерам, много молекул воды могут окружить каждую молекулу растворяемого вещества.
Это свойство воды используется живыми существами. В живой клетке и в межклеточном пространстве вступают во взаимодействие растворы различных веществ в воде [7] . Вода необходима для жизни всех без исключения одноклеточных и многоклеточных живых существ на Земле.


Чистая вода — хороший изолятор. При нормальных условиях вода слабо диссоциирована и концентрация протонов (точнее, ионов гидроксония H3O + ) и гидроксильных ионов HO − составляет 0,1 мкмоль/л. Но поскольку вода — хороший растворитель, в ней практически всегда растворены те или иные соли, то есть в воде присутствуют положительные и отрицательные ионы. Благодаря этому вода проводит электричество. По электропроводности воды можно определить её чистоту.
Вода имеет показатель преломления n=1,33 в оптическом диапазоне. Однако она сильно поглощает инфракрасное излучение, и поэтому водяной пар является основным естественным парниковым газом, отвечающим более чем за 60 % парникового эффекта. Благодаря большому дипольному моменту молекул, вода также поглощает микроволновое излучение, на чём основан принцип действия микроволновой печи.
Агрегатные состояния

Фазовая диаграмма воды: по вертикальной оси — давление в Па, по горизонтальной — температура в Кельвинах. Отмечены критическая (647,3 K; 22,1 МПа) и тройная (273,16 K; 610 Па) точки. Римскими цифрами отмечены различные структурные модификации льда

Оглавление
- Введение
- Глава 1. Здоровье в условиях современного мира. Связь между экологическими реалиями, здоровьем человека и водой
- Глава 2. Что такое вода? Общие сведения о воде, ее химический состав. Историческое значение воды. Место воды в жизни человека.
Приведённый ознакомительный фрагмент книги Легкая вода – cредство от 100 недугов! предоставлен нашим книжным партнёром — компанией ЛитРес.
Глава 2. Что такое вода? Общие сведения о воде, ее химический состав. Историческое значение воды. Место воды в жизни человека: от первобытного времени до наших дней
Вода, у тебя нет ни вкуса, ни цвета, ни запаха, тебя невозможно описать, тобой наслаждаются, не ведая, что ты такое. Нельзя сказать, что ты необходима для жизни: ты — сама жизнь. Ты наполняешь нас радостью, которую не объяснить нашими чувствами.
Антуан де Сент-Экзюпери
Вода окружает нас. Мы и не задумываемся, насколько разнообразным может быть вещество, которое мы обозначаем одним словом. Океаны, моря, реки, озера, ледники, айсберги, болота, дождь, туман, снег, роса — все это вода, и она всегда разная.
Кстати, из всех известных нам веществ, только вода может пребывать одновременно в трех агрегатных состояниях — газообразном, жидком и твердом.
Большая часть запасов воды на нашей планете — это соленые воды, непригодные для использования человеком без предварительной очень сложной очистки. Таким образом, пресная вода, которая так необходима нам, составляет всего 2,5 % от общей массы. Но и этим небольшим количеством мы не можем воспользоваться в полной мере. 75 % пресной воды пребывает в твердом состоянии, например в ледниках, 24 % располагается под землей в виде грунтовых вод, а еще 0,5 % находится в почве в виде влаги. А на наиболее доступные и дешевые источники воды — реки, озера и прочие наземные водоемы приходится чуть больше 0,01 % мировых запасов воды.
Помня о значении, которое вода имеет для жизнедеятельности человека и всего живого на Земле, можно безапелляционно утверждать, что водные ресурсы — самые ценные.
На школьных уроках химии мы изучали формулу воды: Н2О. Но, оказывается, и здесь все не так просто. Действительно, молекула воды состоит из двух атомов водорода и одного атома кислорода. Но полностью соответствует такой формуле лишь вода, находящаяся в парообразном состоянии. И объяснение здесь достаточно простое.
В молекуле воды ядра атомов водорода и кислорода образуют равнобедренный треугольник. В вершине его — сравнительно крупное кислородное ядро, в углах — по одному ядру водорода. В соответствии с электронным строением атомов водорода и кислорода молекула воды располагает пятью электронными парами, которые образуют электронное облако. Оно неоднородно. У кислородного ядра создается избыток электронной плотности. Внутренняя электронная пара кислорода равномерно обрамляет ядро: схематически она представлена окружностью с центром — ядром O 2- . Четыре внешних электрона группируются в две электронные пары, тяготеющие к ядру, но частично не скомпенсированные.

Схематически суммарные электронные орбитали этих пар показаны в виде эллипсов, вытянутых от общего центра — ядра O 2- . Каждый из оставшихся двух электронов кислорода образует пару с одним электроном водорода. Эти па́ры также тяготеют к кислородному ядру. Поэтому водородные ядра — протоны — оказываются несколько оголенными, и здесь наблюдается недостаток электронной плотности.
Таким образом, в молекуле воды есть два отрицательных заряда (избыток электронной плотности в области кислородного ядра) и два положительных (недостаток электронной плотности у двух водородных ядер). Так как электрические заряды расположены асимметрично, то молекула воды имеет заметно выраженную полярность, и, соответственно, высокую диэлектрическую проницаемость, самую высокую из всех известных нам соединений.
Благодаря этому вода является прекрасным растворителем. И всегда представляет собой раствор сложного состава. Даже из дождевой воды, считающейся наиболее чистой, можно выделить различные минеральные и органические вещества, захваченные водой из атмосферы.
Из пресных и морских вод можно выделить органические компоненты — растворимые соединения белков, сахаров, спиртов, углеводородов и подобных веществ, являющихся продуктами жизнедеятельности животных и растений, обитающих на берегах водоемов и в них самих, а также отходы промышленности и сельского хозяйства. А в одном литре океанской воды растворено около 35 г солей. При этом солевой состав отличается не только количественно, но и качественно. На 89 % морские соли состоят из хлоридов (преимущественно — натрия и кальция), на 10 % — из сульфатов (натрия, калия и магния), на 1 % — из карбонатов (натрия и кальция). В пресных водах больше всего карбонатов (натрия и кальция) — до 80 %. Сульфатов (натрия, кальция и магния) — около 13 %. Остальные 7 % приходятся на хлориды (натрия и кальция) и другие соли.
Газ в воде также присутствует, и наиболее часто встречается кислород, азот, углекислый газ, сероводород. В истоках горных рек содержание кислорода может достигать 6 мг/л. В глубинных слоях Черного моря высока концентрация сероводорода — до 100 мг/л. Этот ядовитый газ присутствует и в нижних слоях некоторых озер.
Таким образом, несмотря на свой простой химический состав, вода является одним из самых загадочных и странных веществ на нашей планете.
Согласно наиболее распространенной теории, все живое на Земле зародилось в ее бескрайних доисторических морях примерно 3,8 миллиардов лет назад, когда при особых, существовавших именно тогда условиях, образовались вещества с кристаллическими формами. И при помощи солнечного света и электрических зарядов в качестве источники энергии из них зародились первые обитатели Земли — прокариоты, организмы без оформленного ядра, похожие на бактерий. Они существовали в тонкой пленке на дне водоемов и во влажных местах. И уже впоследствии из них (а возможно, и совершенно независимым путем) возникли и крошечные одноклеточные организмы — древнейшие простейшие животные.
Но как на Земле появилась вода?
Для того чтобы узнать ответ на этот вопрос, обратимся еще к одной распространенной теории и вернемся на 4,5–5 миллиардов лет назад, когда частицы гигантского облака космической пыли спрессовались в раскаленный шар. Эта пыль состояла из всех известных в природе химических элементов, и горячий водяной пар вырывался с поверхности этого раскаленного докрасна шара и обволакивал его плотным облаком. В ледяной атмосфере пар охлаждался и превращался в воду, которая выпадала обратно на Землю в виде сплошных дождей. Но Земля еще не остыла, и на ее поверхности вода снова превращалась в пар, который опять поднимался в атмосферу.
Согласно пониманию человека древнейшей эпохи, наводнения или засуха были результатом доброжелательного или враждебного отношения к человеку духа, живущего в воде. И люди старались уважить его различными способами. Способы эти варьировались от абсолютно безобидных, таких, как обычай выпить глоток воды, зачерпнутый руками на берегу реки, до таких, как жертвоприношение.
Как и все важное и необъяснимое, вода приобретала в глазах людей мистические свойства. Так, например, поражаясь способности ее растворять физическую грязь, воде стали приписывать свойства очищать душу, что впоследствии также отразилось во всех религиях мира.
И если в первобытные времена люди поклонялись общему Духу Воды, то уже в греческой античности каждая река, каждый ручеек имели свое божество — нимфу, не говоря уже о более крупных водоемах, и главного повелителя этой стихии — бога Посейдона, брата Зевса.
С развитием цивилизации человечество все больше использовало воду не только в бытовых целях, но и в медицине и производсте. А для обеспечения ее непрерывного присутствия в нужном количестве изобретатели решали проблемы создания, а потом и усовершенствования специальных приспособлений и сооружений, позволяющих доставлять воду от водоемов к месту обитания человека.
Вода — одно из самых распространенных веществ в природе и главная составная часть всех живых организмов. Она покрывает около 2/3 поверхности нашей планеты. Без воды жизнь на Земле была бы невозможна.

Вода — основа жизни
Все живые существа на 75 % состоят из воды. Это самый необходимый элемент живой природы. Вода постоянно совершает круговорот между морями, атмосферой и сушей, создавая условия, в которых может существовать и развиваться жизнь.
Вода — на первый взгляд простейшее химическое соединение — является основой жизни на Земле. Вода транспортирует тепло, растворяет и переносит колоссальные массы химических веществ и элементов, разрушает и перераспределяет горные породы, образует формы рельефа и даже участвует в образовании полезных ископаемых. Кроме того, вода задействована в ряде метеорологических явлений, таких как осадки, туманы, облака. Она участвует в создании течений, волнений, перемещении русел рек и формировании водоемов. А еще она является средой жизни для множества организмов.
Человек может прожить без воды всего несколько суток. Для нормальной работы всех органов человеку необходимо как минимум 1,5 л воды в день. Вода доставляет в клетки организма питательные вещества и уносит отходы жизнедеятельности. Кроме того, вода участвует в процессах терморегуляции и дыхания человека.
Под лучами Солнца вода испаряется из водоемов и поднимается в воздух. Там капельки воды собираются в облака и тучи и выпадают на землю в виде дождя или снега, который превращается в воду. Она впитывается в землю и снова возвращается в моря, реки и озера. И все начинается сначала. Так происходит круговорот воды в природе.
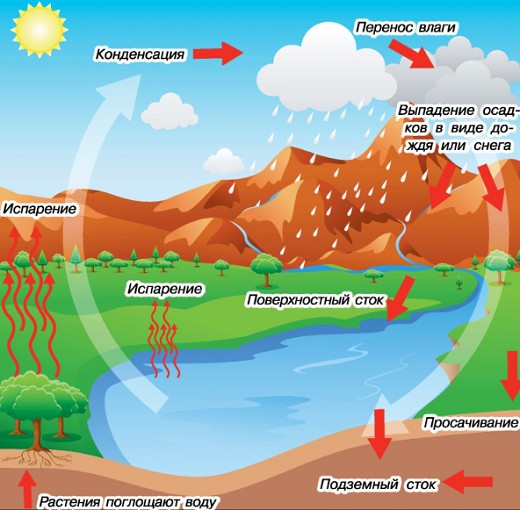
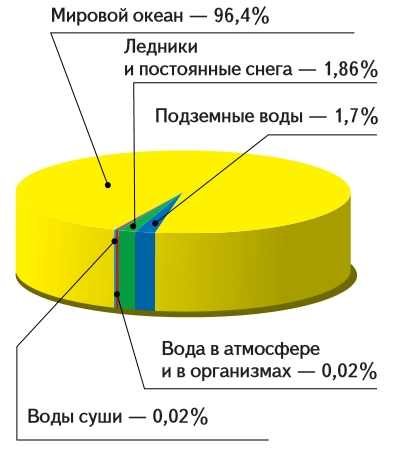
Сколько и где?
Всего на земном шаре 1390 млн км 3 воды, больше всего её в морях и океанах — 96,4%. На суше вода спрятана в ледниках и постоянных снегах — около 1,86%. Вечным льдом покрыты Антарктида, остров Гренландия и многие другие острова в высоких широтах. В горах на больших высотах образуются горные ледники. Под землёй воды немного — всего около 1,7% от общего объёма, а на воды суши (реки, озёра, болота, водохранилища) приходится примерно 0,02%. В живых организмах и в атмосфере тоже есть вода. А вот пресной воды, так необходимой нам для жизни, на планете мало — только 2,64%.
Три состояния воды
Вещества в зависимости от температуры замерзания, плавления и кипения могут встречаться в природе в трех агрегатных состояниях — твердом, жидком и газообразном. Вода замерзает при О °С, а кипит при 100 °С.
В повседневной жизни мы можем встретить воду в любом из ее трех состояний, причем ее форма постоянно меняется. Жидкая вода испаряется и переходит в газообразное состояние — водяной пар. Он конденсируется и превращается в жидкость. При минусовых температурах вода замерзает и превращается в твердый лед.
Если в сосуд с водой мы поместим кристаллы поваренной соли, то сможем наблюдать, как количество твердого вещества постепенно уменьшается. Вода при этом приобретает новые свойства: у нее появляется соленый вкус, изменяются плотность и температура замерзания. Полученную жидкость уже нельзя назвать водой, это раствор. Между молекулами соли и воды возникают межмолекулярные связи, благодаря которым молекулы соли отрываются от поверхности кристалла.
Артезианская вода
Согласитесь, несколько необычно называть воду полезным ископаемым: она вокруг нас, течет в ручейках и реках, плещется в морях и океанах, даже с неба льется. И тем не менее такое название верное. Вспомните о колодцах и артезианских скважинах. Разве в этих случаях не приходится добывать воду в буквальном смысле слова из-под земли? Артезианская вода — это вода, находящаяся на глубине 50—200 м и заключенная между водоупорными слоями. Такая вода надежно защищена от внешнего загрязнения.
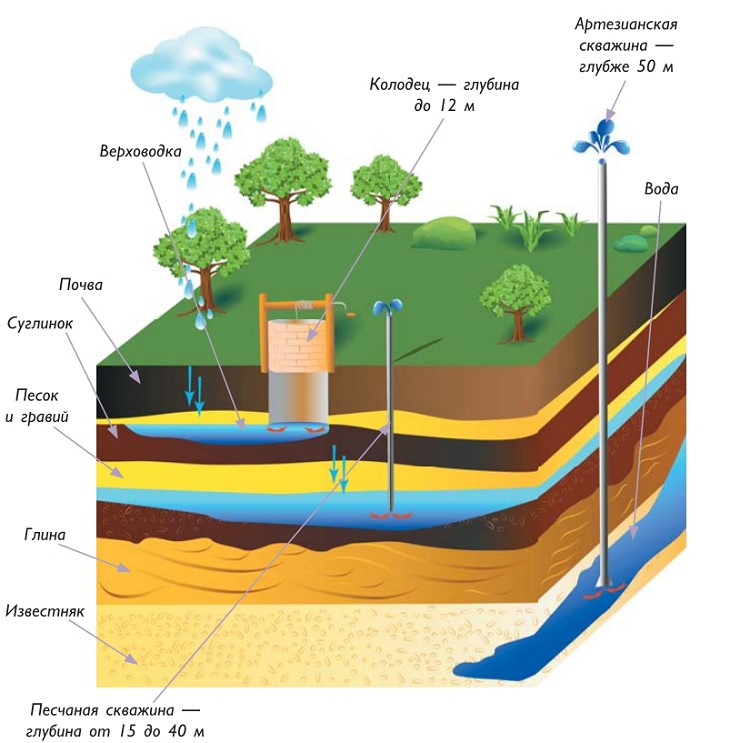
Источник энергии
Вода — важный источник энергии. Мощность движущейся воды очень велика, поэтому ее используют для получения электричества. Гидроэлектростанции строятся там, где вода движется с большой скоростью, например на реках. Кроме того, могут возводиться и искусственные сооружения, такие как плотины, которые создают движение воды.
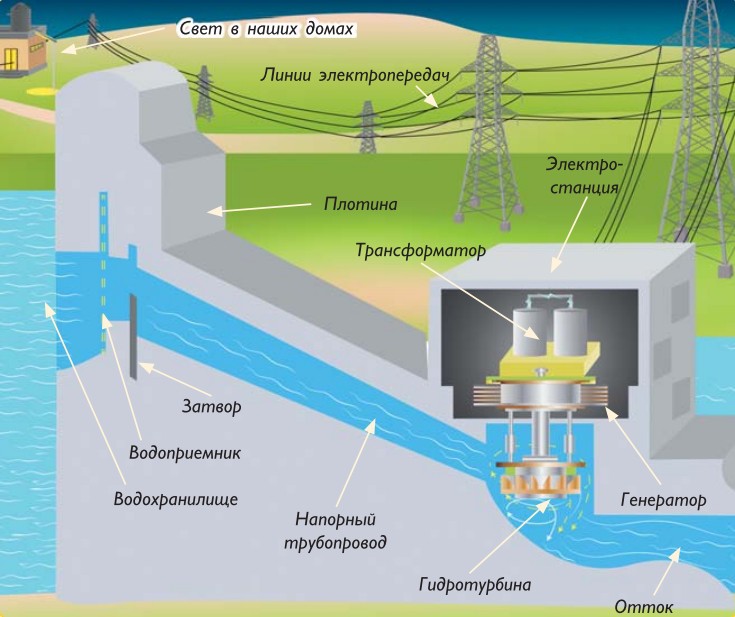
Вода, перетекая с верхнего уровня на нижний по специальным турбинным трубопроводам, приобретает большую скорость. Струя воды поступает далее на лопасти гидротурбины и вращает их. Так энергия превращается в механическую. Соединенный с турбиной генератор вращается, и механическая энергия становится электрической. Трансформаторы преобразуют электричество в напряжение нужной величины. Электричество через передающие линии пересылается на распределительные станции.
Читайте также:

