Нарушение инсулинообразования в организме кратко
Обновлено: 04.07.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сахарный диабет: причины появления, симптомы, диагностика и способы лечения.
Определение
Сахарный диабет (СД) – группа хронических эндокринных патологий, связанных с нарушением усвоения глюкозы, возникающих в результате абсолютной или относительной инсулиновой недостаточности.
Основное его клиническое проявление – длительная гипергликемия вследствие нарушения метаболизма глюкозы в организме.
Причины появления сахарного диабета
Этиологию или патогенез большинства типов СД упрощенно можно описать как нарушение чувствительности к инсулину или как нарушение секреции инсулина.
Инсулин — это гормон, регулирующий уровень содержания сахара в крови и синтезирующийся β-клетками поджелудочной железы - последовательно, в несколько этапов. При диабете поджелудочная железа не вырабатывает достаточно инсулина или организм не может эффективно использовать вырабатываемый ею инсулин. Физиологическим и наиболее важным стимулятором секреции инсулина является глюкоза. Практически во всех тканях организма инсулин влияет на обмен углеводов, жиров, белков и электролитов, увеличивая транспорт глюкозы, белка и других веществ через мембрану клетки. Эндогенный инсулин сначала поступает в печень и лишь затем, меньшая его часть, - в большой круг кровообращения и почки.
К инсулинозависимым тканям относится печень, мышцы и жировая ткань. В клетки этих тканей глюкоза может попасть только с помощью инсулина. Если в организме мало инсулина или клетки невосприимчивы к нему, то глюкоза остается в крови. К инсулиннезависимым тканям относится эндотелий сосудов, нервная ткань и хрусталик глаза.
Хроническая гипергликемия при сахарном диабете сопровождается повреждением, дисфункцией и недостаточностью различных органов, особенно глаз, почек, нервов, сердца и кровеносных сосудов.
Классификация заболевания
По МКБ-10 сахарный диабет имеет кодировки Е10-Е14, однако классификация включает в себя еще 5 уточняющих диагнозов:
- E10 - сахарный диабет I типа.
- E11 - сахарный диабет II типа.
- E12 - сахарный диабет, связанный с недостаточностью питания.
- E13 - другие уточненные формы сахарного диабета.
- E14 - сахарный диабет неуточненный.
- с кетоацидозом (кетоацидотическая) или без него;
- гиперосмолярная;
- гипогликемическая.
- кетоацидоза (ацидоза без упоминания о коме, кетоацидоза без упоминания о коме);
- поражения почек (диабетическая нефропатия, интракапиллярный гломерулонефроз, синдром Киммельстила-Уилсона);
- поражений глаз (диабетическая: катаракта, ретинопатия);
- неврологических осложнений (амиотрофии, автономной невропатии, мононевропатии, полиневропатии);
- нарушений периферического кровообращения (гангрена, язва);
- других уточненных осложнений (диабетической артропатии и т.д.);
- множественными осложнениями;
- неуточненными осложнениями.
- для определения тактики лечения;
- для стимулирования исследования причин и механизмов развития заболевания;
- для обеспечения основы для эпидемиологических исследований.
Наиболее распространенный тип, который определяется различной степенью дисфункции β-клеток и инсулинорезистентностью. СД II типа развивается у людей старшего возраста. Среди основных факторов риска его развития – несбалансированное питание, гиподинамия, избыточный вес, отягощенная наследственность.
- Медленно латентно развивающийся иммуноопосредованный СД у взрослых, при котором дольше сохраняется функция β-клеток.
- СД II типа со склонностью к кетозу и дефициту инсулина (не иммуноопосредованный). Абсолютная потребность в заместительной инсулинотерапии у этих больных может появляться и исчезать.
- Моногенный СД связан с определенными мутациями гена, имеет несколько клинических проявлений, требующих различного лечения. Встречается в детском и молодом возрасте, имеет признаки тяжелой инсулинорезистентности без ожирения.
- СД, связанный с заболеваниями и травмами экзокринной части поджелудочной железы.
- СД, ассоциированный с эндокринопатиями (акромегалия, синдром Кушинга, глюкагонома, гипертиреоз и другие).
- СД, индуцированный лекарственными препаратами или химическими веществами.
- СД, развивающийся в исходе вирусных и бактериальных инфекций.
- Необычные специфические формы иммуноопосредованного СД связаны с редкими иммунными заболеваниями. СД, диагностированный в первые 6 месяцев жизни, в большинстве случаев не является типичным аутоиммунным СД, а относится к так называемому неонатальному СД.
- Другие генетические синдромы, иногда связанные с СД.
- Неклассифицированный СД - должен использоваться временно, когда нет четкой диагностической категории в дебюте заболевания.
- СД I типа или СД II типа, выявленные при беременности.
- Гестационный СД - гипергликемия ниже диагностического порога СД.
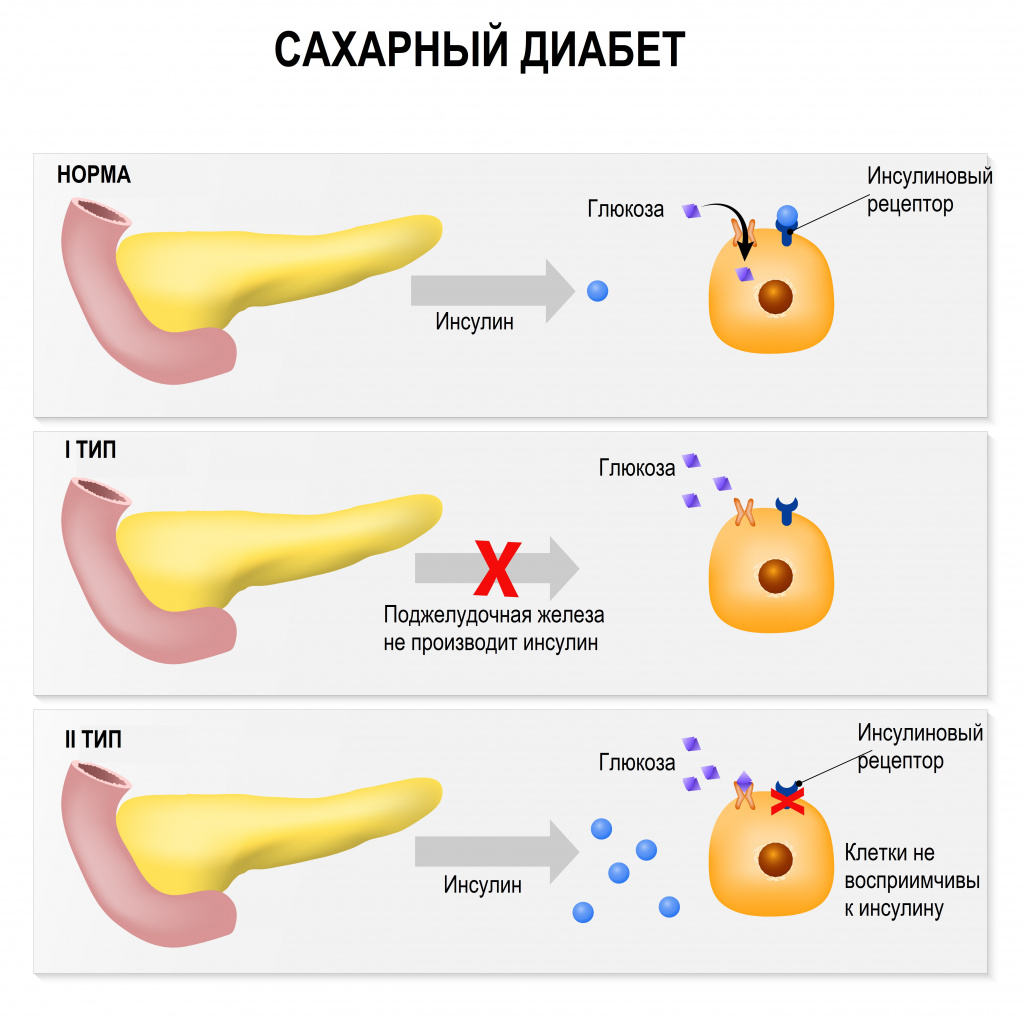
Диабет I типа – инсулинозависимый. Заболевание является следствием тотальной инсулиновой недостаточности в организме и чаще всего обнаруживается у лиц молодого возраста. Инсулиновая недостаточность развивается стремительно и имеет классические клинические проявления:
- частые обильные мочеиспускания;
- постоянное чувство жажды;
- потеря веса;
- повышенный аппетит;
- слабость;
- частые головокружения;
- помутнение зрения;
- плохая заживляемость ран, гнойнички на коже.
Диагностика сахарного диабета
Диагностика включает в себя установление формы заболевания, оценку общего состояния организма пациента, выявление сопутствующих патологий.
При наличии оснований подозревать у пациента впервые выявленный сахарный диабет назначаются лабораторные методы обследования.
-
Вначале проводится оценка уровня гликированного гемоглобина и/или уровня глюкозы натощак.
Синонимы: Анализ крови на гликированный гемоглобин. Glycohemoglobin; HbA1c; Hemoglobin A1c; A1c; HgbA1c; Hb1c. Краткая характеристика определяемого вещества Гликированный гемоглобин Образуется в результате медленного неферментативного присоединения глюкозы к гемоглобину А, со.
Инсулин - гормон, который регулирует уровень глюкозы в крови. Глюкоза - моносахарид, то есть простой углевод. После принятия пищи сложные углеводы расщепляются в ЖКТ до простых и всасываются в кровоток.
Инсулин регулирует обмен углеводов, принимает участие в белковом и углеводном обмене. Благодаря этому гормону происходит усваивание глюкозы из крови клетками органов и тканей. Ее остатки откладываются в клетках печени и мышцах в форме гликогена. Он представляет собой полисахарид, состоящий из молекул глюкозы. Это - накапливаемый резерв углеводов, который является первичным источником энергии для нашего тела. Она высвобождается и превращается в глюкозу, когда организм испытывает повышенную потребность в энергии. Это происходит при физических нагрузках, стрессах, при снижении уровня глюкозы в крови из-за пропуска приема пищи, дефиците калорий.
Участие инсулина в белковом обмене заключается в том, что этот гормон усиливает синтез нуклеиновых кислот, тормозит распад белковых соединений. При обмене жиров инсулин активизирует энергетические процессы в жировых клетках, участвует в синтезе жирных кислот.
Как действует инсулин
Именно этот гормон регулирует распределение энергии в виде глюкозы. По этому критерию все органы и ткани подразделяются на инсулинозависимые и инсулиннезависимые. Инсулинозависимыми являются печень, мышечная и жировая ткань. В них глюкоза попадает только тогда, когда инсулин "даст разрешение" на создание энергетических депо. При нехватке калорий, когда энергии недостаточно, жировая ткань и мышцы остаются без глюкозы, которую инсулин не пропускает в клетки. Она направляется головному мозгу и другим жизненно важным органам, которые являются инсулиннезависимыми.
Открытие инсулина и его роли в организме
За выработку этого гормона отвечает поджелудочная железа. Гормон вырабатывается специальными ß-клетками островков Лангерганса. Инсулин является жизненно важным гормоном, нарушение секреции которого приводит к серьезным сбоям обмена веществ. Самым известным заболеванием, которое связано с нарушением инсулинарной функции поджелудочной железы, является сахарный диабет (СД).
Самое первое описание симптомов сахарного диабета было сделано египтянином Имхотепом в 2980 году до н.э. Информация о СД была обнаружена и в древнегреческих папирусах, датируемых 1500 году до н.э.
Исследования, касающиеся природы "сахарной болезни", велись на протяжении многих лет. Открытие гормона, который регулирует уровень глюкозы в крови, принадлежит ученому Паулю Лангергансу. В 1869 году он обнаружил группу клеток в поджелудочной железе, которые отвечают за секрецию инсулина. Специалист смог доказать, что именно поджелудочной железе принадлежит функция регулировки уровня сахара в крови.
В 1900 году ученый Л. В. Соболев продолжил исследования этого органа и обнаружил, что патологические изменения островков Лангерганса приводят к сахарному диабету, а при их сохранении СД не возникает даже в случае атрофии железистой ткани.
Выделение гормона и открытие инсулинотерапии принадлежит канадскому врачу Фредерику Бантингу. Он первым в мире смог выделить так называемый "экстракт поджелудочной железы" из ее клеток, чтобы использовать его в лечении сахарного диабета. Это произошло только в 1921 году. Первоначально инсулин назвали айлетином, но потом его переименовали.
До появления инсулинотерапии люди с сахарным диабетом были обречены на быструю смерть. В 1922 году был получен препарат на основе очищенного инсулина животного происхождения. В 1923 году началось массовое производство этого лекарства. Он позволил людям с СД искусственно регулировать уровень глюкозы в крови и тем самым избежать смертельно опасных осложнений диабета.
В настоящее время инсулин для диабетиков получают методом генной инженерии. Такой препарат называют рекомбинантным. Его создают из вещества, которое вырабатывается штаммами дрожжей, помещенными в питательную среду. Этот способ позволил отказаться от сырья животного происхождения и получить препарат, действие которое идентично натуральному инсулину.
Секреция инсулина и ее нарушения
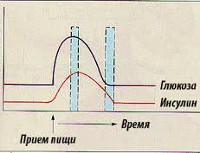
Для нормального течения обменных процессов важно, чтобы инсулин вырабатывался в нужном объеме. Минимальное количество этого гормона продуцируется всегда. Речь идет о базальной секреции инсулина. После еды и поступления глюкозы в кровь происходит активный выброс гормона – так называемый прандиальный пик. Это необходимо, чтобы глюкоза могла поступить в клетки органов и тканей.
При нормальной работе поджелудочной железы выработка инсулина после приема пищи происходит в две фазы. Быстрая фаза длится 1-3 минуты, медленная - до получаса.
Уровень инсулина в крови здоровых людей колеблется в широком диапазоне. Он зависит от возраста и физиологического состояния. У детей это значение составляет от 3 до 20 мкЕд/мл, у взрослых верхний порог достигает 25 мкЕд/мл.
У женщин во время беременности и после менопаузы происходят существенные изменения гормонального фона. Нормальные показатели инсулина в этом случае составляют от 6 до 27/36 мкЕд/мл.
Нарушением считается не только пониженная секреция гормона, но и повышенная. Существует несколько факторов, из-за которых поджелудочная железа не может вырабатывать инсулин в нужном количестве:
- СД первого типа. Патологический процесс обусловлен аутоиммунной реакцией. У людей с таким заболеванием ß-клетки островков Лангерганса разрушены и не могут покрыть потребность организма в гормоне. . Воспаление поджелудочной железы приводит к нарушению секреторной функции и нехватке инсулина из-за фиброза тканей. Сахарный диабет, который развивается при панкреатите, называют панкреатогенным или СД 3 типа.
- Травмы, операции на поджелудочной железе. Они вызывают повреждение островкового аппарата, который продуцирует инсулин.
- Злоупотребление быстрыми углеводами. Избыточное поступление глюкозы с пищей заставляет орган работать в усиленном режиме. Со временем это приводит к нарушению инсулинарной функции из-за износа поджелудочной железы.
- Интоксикация. Алкоголь, сильнодействующие лекарства, химические и природные яды, радиоактивные вещества повреждают клетки поджелудочной железы.
- Инсулинома. Опухоль β-клеток островков поджелудочной железы приводит к избыточной секреции инсулина.
Повышенное содержание гормона опасно из-за постоянной гипогликемии. Клетки органов и тканей не могут получать достаточное количество энергии из-за низкого уровня глюкозы. Гипогликемический приступ, при котором содержание глюкозы в крови падает ниже 2,5 ммоль/л, приводит к потере сознания, локальным поражениям нервной системы, может стать причиной инфаркта миокарда. В тяжелых случаях у пациента наступает гипогликемическая кома - смертельно опасное состояние.
Инсулин для диабетиков
При нарушении или отсутствии выработки инсулина глюкоза из пищи поступает в кровь, но не может попасть в клетки инсулинозависимых тканей, то есть мышц и жира. В то же время инсулиннезависимые органы получают глюкозу в избытке, что приводит к патологическим изменениям. При сахарном диабете в первую очередь страдают органы-мишени: сосуды, нервы, почки.

Инсулинотерапия используется в лечении диабета первого и второго типа. При СД 1 типа клетки поджелудочной повреждены, поэтому инъекции препарата становятся единственным способом контроля уровня глюкозы.
При СД второго типа нарушения возникают из-за снижения восприимчивости чувствительных к инсулину тканей. Он может вырабатываться в достаточном количестве или даже избытке, однако печень, жировая и мышечная ткань перестают воспринимать действие этого гормона. Возникает хроническая гипергликемия - повышенное содержание глюкозы в крови.
Основополагающую роль в лечении СД 2 типа играет диета с пониженным содержанием углеводов, прием препаратов для снижения уровня сахара, повышения чувствительности клеток к инсулину. Инъекции инсулина при диабете второго типа назначаются пациентам с прогрессирующим заболеванием. Как правило, это происходит, когда бета-клетки поджелудочной железы не могут справляться с выработкой эндогенного гормона, а сахаропонижающие препараты перестают давать эффект.
Диабет становится декомпенсируемым, то есть неконтролируемым, что чревато серьезными осложнениями. В этом случае на помощь приходит экзогенный инсулин - тот, который поступает извне.
Препараты для инсулинотерапии

Глюкоза раствор
- Показана при гипогликемии, недостаточности углеводного питания;
- При заболеваниях печении, коллапсе, шоке;
- Для коррекции дегидратации.
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ПЕРЕД ПРИМЕНЕНИЕМ ВНИМАТЕЛЬНО ПРОЧИТАЙТЕ ИНСТРУКЦИЮ ИЛИ ПРОКОНСУЛЬТИРУЙТЕСЬ С ВРАЧОМ
При лечении диабета используют инсулиновые препараты разных типов. У них одинаковый эффект, но они отличаются по быстродействию и продолжительности воздействия. Это необходимо, чтобы сделать лечение более физиологичным, ведь у здоровых людей уровень инсулина естественным способом повышается и понижается в течение дня.
При диабете используют инсулин четырех типов:
- Препарат быстрого действия вводят до принятия пищи. Он подействует через 15 минут и сохраняет эффект в течение 3-4 часов.
- Короткий инсулин также используют перед едой. Он сработает через 30-60 минут. Эффект сохраняется в течение 5-8 часов.
- Промежуточный инсулин срабатывает через 1-2 часа после укола. Эффект сохраняется в течение 14-16 часов.
- Длинный инсулин срабатывает через два часа после укола. Его эффект сохраняется до суток и более.
Режим терапии и дозировку препарата подбирает лечащий врач исходя из клинического случая. При СД 1 типа обычно используется базально-болюсная инсулинотерапия. Она включает препараты короткого и быстрого действия, чтобы использовать сахар из каждого приема пищи и поддерживать уровень глюкозы в норме в течение суток.
Диабет сахарный - заболевание, обусловленное абсолютной или относительной недостаточностью инсулина и характеризующееся грубым нарушением обмена углеводов с гипергликемией и глюкозурией, а также другими нарушениями обмена веществ.
Имеют значение наследственное предрасположение, аутоиммунные, сосудистые нарушения, ожирение, психические и физические травмы, вирусные инфекции.
При абсолютной недостаточности инсулина снижается уровень инсулина в крови вследствие нарушения его синтеза или секреций бета-клетками островков Лангерганса. Относительная инсулиновая недостаточность может являться результатом снижения активности инсулина вследствие его повышенного связывания с белком, усиленного разрушения ферментами печени, преобладания эффектов гормональных и негормональных антагонистов инсулина (глюкагона, гормонов коры надпочечников, щитовидной железы, гормона роста, неэстерифицированных жирных кислот), изменения чувствительности инсулинзависимых тканей к инсулину.
Недостаточность инсулина приводит к нарушению углеводного, жирового и белкового обмена. Снижается проницаемость для глюкозы клеточных мембран в жировой и мышечной ткани, усиливаются гликогенолиз и глюконеогенез, возникают гипергликемия, глюкозурия, которые сопровождаются полиурией и полидипсией. Снижается образование и усиливается распад жиров, что приводит к повышению в крови уровня кетоновых тел (ацетоуксусной, бета-оксимасляной и продукта конденсации ацетоуксусной кислоты - ацетона). Это вызывает сдвиг кислотно-щелочного состояния в сторону ацидоза, способствует повышенной экскреции ионов калия, натрия, магния с мочой, нарушает функцию почек.
Значительная потеря жидкости вследствие полиурин приводит к обезвоживанию организма. Усиливается выделение из организма калия, хлоридов, азота, фосфора, кальция.
Симптомы
- инсулинзависимый сахарный диабет (ИЗСД);
- инсулиннезависимый сахарный диабет (ИНСД) у лиц с нормальной массой тела и у лиц с ожирением; сахарный диабет, связанный с недостаточностью питания (СДНП);
- другие типы сахарного диабета, связанные с определенными состояниями и синдромами:
- заболеваниями поджелудочной железы,
- болезнями гормональной природы,
- состояниями, вызванными лекарственными средствами или воздействием химических веществ,
- изменениями инсулина и его рецепторов,
- определенными генетическими синдромами,
- смешанными состояниями; нарушенная толерантность к глюкозе (НТГ) у лиц с нормальной массой тела и улиц с ожирением, нарушенная толерантность к глюкозе, связанная с другими состояниями и синдромами; сахарный диабет беременных.
Статистически достоверные классы риска (лица с нормальной толерантностью к глюкозе, но со значительно увеличенным риском развития сахарного диабета). Предшествовавшие нарушения толерантности к глюкозе. Потенциальные нарушения толерантности к глюкозе.
В клинической практике наиболее часто встречаются больные с НТГ, у которых содержание глюкозы в крови натощак и в течение суток не превышает нормы, но при введении легкоусвояемых углеводов уровень гликемии превышает значения, характерные для здоровых лиц, и истинный сахарный диабет: ИЗСД тип I и ИНСД тип II у лиц с нормальной массой тела или улиц с ожирением, характерными клиническими и биохимическими симптомами заболевания.
ИЗСД чаще развивается у молодых людей до 25 лет, имеет выраженную клиническую симптоматику, часто лабильное течение со склонностью к кетоацидозу и гипогликемиям, в большинстве случаев начинается остро, иногда с возникновения диабетической комы. Содержание инсулина и С-пептида в крови ниже нормы или не определяется.
Основные жалобы больных: сухость во рту, жажда, полиурия, похудание, слабость, снижение трудоспособности, повышенный аппетит, кожный зуд и зуд в промежности, пиодермия, фурункулез. Часто наблюдаются головная боль, нарушение сна, раздражительность, боль в области сердца, в икроножных мышцах. В связи со снижением резистентиости у больных сахарным диабетом часто развивается туберкулез, воспалительные заболевания почек и мочевыводящих путей (пиелит, пиелонефрит). В крови определяется повышенный уровень глюкозы, в моче - глюкозурия.
ИНСД II типа возникает обычно в зрелом возрастет часто у лиц с избыточной массой тела, характеризуется спокойным, медленным началом. Уровень инсулина и С-пептида в крови в пределах нормы или может превышать ее. В некоторых случаях сахарный диабет диагностируется лишь при развитии осложнений или при случайном обследовании.
В зависимости от уровня гликемии, чувствительности к лечебным воздействиям и наличия или отсутствия осложнений выделяют три степени тяжести сахарного диабета. Легкой степени относят случаи заболевания, когда компенсация достигается диетой, кетоацидоз отсутствует. Возможно наличие ретинопатии 1 степени. Обычно это больные с сахарным диабетом II типа.
Тяжелая степень сахарного диабета характеризуется лабильным течением (выраженные колебания уровня сахара крови в течение суток, склонность к гипогликемии, кетоацидозу), имеются выраженные осложнения: ретинопатия III-IV степени, нефропатия с нарушением функции почек, периферическая нейропатия; трудоспособность нарушена.
Осложнения сахарного диабета
Характерны сосудистые осложнения: специфические поражения мелких сосудов- микроангиопатии (ангиоретинопатия, нефропатия и другие висцеропатии), нейропатия, ангиопатия сосудов кожи, мышц и ускоренное развитие атеросклеротических изменений в крупных сосудах (аорта, коронарные церебральные артерии и т. д. ). Ведущую роль в развитии микроангиопатий играют метаболические и аутоиммунные нарушения.
Поражение сосудов сетчатки глаз (диабетическая ретинопатия) характеризуется дилатацией вен сетчатки, образованием капиллярных микроаневризм, экссудацией и точечными кровоизлияниями в сетчатку (I стадия, непролиферативная); выраженными венозными изменениями, тромбозом капилляров, выраженной экссудацией и кровоизлияниями в сетчатку (II стадия, препролиферативная); при III стадии - пролиферативной-имеются вышеперечисленные изменения, а также прогрессирующая неоваскуляризация и пролиферация, представляющие главную угрозу для зрения и приводящие к отслойке сетчатки, атрофии зрительного нерва. Часто у больных сахарным диабетом возникают и другие поражения глаз: блефарит, нарушения рефракции и аккомодации, катаракта, глаукома.
Хотя почки при сахарном диабете часто подвергаются инфицированию, главная причина ухудшения их функции состоит в нарушений микрососудистого русла, проявляющемся гломерулосклерозом и склерозом афферентных артериол (диабетическая нефропатия).
Диабетическая нейропатия - частое осложнение при длительно текущем СД; поражаются как центральная, так и периферическая нервная система. Наиболее характерна периферическая нейропатия: больных беспокоят онемение, чувство ползания мурашек, судороги в конечностях, боли в ногах, усиливающиеся в покое, ночью и уменьшающиеся при ходьбе. Отмечается снижение или полное отсутствие коленных и ахилловых рефлексов, снижение тактильной, болевой чувствительности. Иногда развивается атрофия мышц в проксимальных отделах ног. Возникают расстройства функции мочевого пузыря, у мужчин нарушается потенция.
Диабетический кетоацидоз развивается вследствие выраженной недостаточности инсулина при неправильном лечении СД, нарушении диеты, присоединении инфекции, психической и физической травме или служит начальным проявлением заболевания. Характеризуется усиленным образованием кетоновых тел в печени и увеличением их содержания в крови, уменьшением щелочных резервов крови; увеличение глюкозурии сопровождается усилением диуреза, что вызывает дегидратацию клеток, усиление экскреции с мочой электролитов; развиваются гемодинамические нарушения.
Диабетическая (кетоацидотическая) кома развивается постепенно. Для диабетической прекомы характерна симптоматика быстро прогрессирующей декомпенсации сахарного диабета: сильная жажда, полиурия, слабость, вялость, сонливость, головная боль, отсутствие аппетита, тошнота, запах ацетона в выдыхаемом воздухе, сухость кожных покровов, гипотензия, тахикардия. Если своевременно не оказана помощь, развивается диабетическая кома: спутанность и затем потеря сознания, многократная рвота, глубокое шумное дыхание.
Лактацидотическая (молочнокислая) кома возникает обычно на фоне почечной недостаточности и гипоксии, наиболее часто встречается у больных, получающих бигуаниды, в частности фенформин.
Диагноз сахарного диабета
- наличие классических симптомов диабета: полиурии, полидипсии, кетонурии, снижения массы тела, гипергликемии;
- повышение уровня глюкозы натощак (при неоднократном определении) не менее чем 6,7 ммоль/л либо
- гликемия натощак менее 6,7 ммоль/л, но при высокой гликемии в течение суток либо на фоне проведения глюкозотолерантного теста (более 11,1 ммоль/л).
-
— круглосуточно. — понедельник-пятница, с 08:00 до 21:00; суббота, с 09:00 до 18:00; воскресенье, с 09:00 до 18:00.
В летний период: понедельник-пятница, с 08:00 до 21:00; суббота, с 09:00 до 18:00; воскресенье, с 09:00 до 15:00.
В летний период: понедельник-пятница, с 08:00 до 21:00; суббота, с 09:00 до 18:00; воскресенье, с 09:00 до 15:00.
Гиперинсулинизм — клинический синдром, характеризующийся повышением уровня инсулина и снижением сахара в крови. Гипогликемия приводит к слабости, головокружению, повышению аппетита, тремору, психомоторному возбуждению. При отсутствии своевременного лечения развивается гипогликемическая кома. Диагностика причин состояния основывается на особенностях клинической картины, данных функциональных проб, динамическом исследовании глюкозы, ультразвуковом или томографическом сканировании поджелудочной железы. Лечение панкреатических новообразований – хирургическое. При внепанкреатическом варианте синдрома проводят терапию основного заболевания, назначают специальную диету.
![Гиперинсулинизм]()
Общие сведения
Гиперинсулинизм (гипогликемическая болезнь) - врожденное или приобретенное патологическое состояние, при котором развивается абсолютная или относительная эндогенная гиперинсулинемия. Признаки болезни впервые были описаны в начале ХХ века американским врачом Харрисом и отечественным хирургом Оппелем. Врожденный гиперинсулинизм встречается достаточно редко - 1 случай на 50 тыс. новорожденных. Приобретенная форма заболевания развивается в возрасте 35-50 лет и чаще поражает лиц женского пола. Гипогликемическая болезнь протекает с периодами отсутствия выраженной симптоматики (ремиссия) и с периодами развернутой клинической картины (приступы гипогликемии).
![Гиперинсулинизм]()
Причины гиперинсулинизма
Врожденная патология возникает вследствие внутриутробных аномалий развития, задержки роста плода, мутаций в геноме. Причины возникновения приобретенной гипогликемической болезни разделяют на панкреатические, приводящие к развитию абсолютной гиперинсулинемии, и непанкреатические, вызывающие относительное повышение уровня инсулина. Панкреатическая форма болезни встречается при злокачественных или доброкачественных новообразованиях, а также гиперплазии бета-клеток поджелудочной железы. Непанкреатическая форма развивается при следующих состояниях:
- Нарушения в режиме питания. Длительное голодание, повышенная потеря жидкости и глюкозы (поносы, рвота, период лактации), интенсивные физические нагрузки без потребления углеводной пищи вызывают резкое снижение уровня сахара в крови. Чрезмерное употребление в пищу рафинированных углеводов увеличивает уровень сахара крови, что стимулирует активную выработку инсулина.
- Поражение печени различной этиологии (рак, жировой гепатоз, цирроз) приводит к снижению уровня гликогена, нарушению обменных процессов и возникновению гипогликемии.
- Бесконтрольный прием сахароснижающих препаратов при сахарном диабете (производных инсулина, сульфанилмочевины) вызывает медикаментозную гипогликемию.
- Эндокринные заболевания, приводящие к снижению уровня контринсулиновых гормонов (АКТГ, кортизол): гипофизарный нанизм, микседема, болезнь Аддисона.
- Недостаток ферментов, участвующих в процессах обмена глюкозы (печеночная фосфорилаза, почечная инсулиназа, глюкозо-6-фосфатаза) вызывает относительный гиперинсулинизм.
Патогенез
Глюкоза является главным питательным субстратом центральной нервной системы и необходима для нормального функционирования головного мозга. Повышенный уровень инсулина, накопление гликогена в печени и торможение гликогенолиза приводит к снижению уровня глюкозы в крови. Гипогликемия вызывает торможение метаболических и энергетических процессов в клетках головного мозга. Происходит стимуляция симпатоадреналовой системы, увеличивается выработка катехоламинов, развивается приступ гиперинсулинизма (тахикардия, раздражительность, чувство страха). Нарушение окислительно-восстановительных процессов в организме приводит к снижению потребления кислорода клетками коры головного мозга и развитию гипоксии (сонливость, заторможенность, апатия). Дальнейший дефицит глюкозы вызывает нарушение всех обменных процессов в организме, увеличение притока крови к мозговым структурам и спазм периферических сосудов, что может привести к инфаркту. При вовлечении в патологический процесс древних структур мозга (продолговатый и средний мозг, варолиев мост) развиваются судорожные состояния, диплопия, а также нарушение дыхательной и сердечной деятельности.
Классификация
В клинической эндокринологии наиболее часто используется классификация гиперинсулинемии в зависимости от причин возникновения заболевания:
- Первичный гиперинсулинизм (панкреатический, органический, абсолютный) является следствием опухолевого процесса или гиперплазии бета-клеток островкового аппарата поджелудочной железы. Повышению уровня инсулина в 90% способствуют доброкачественные новообразования (инсулинома), реже – злокачественные (карцинома). Органическая гиперинсулинемия протекает в тяжелой форме с выраженной клинической картиной и частыми приступами гипогликемии. Резкое понижение уровня сахара в крови возникает утром, связано с пропуском приема пищи. Для данной формы заболевания характерна триада Уиппла: симптомы гипогликемии, резкое снижение сахара в крови и купирование приступов введением глюкозы.
- Вторичный гиперинсулинизм (функциональный, относительный, внепанкреатический) связан с дефицитом контринсулярных гормонов, поражением нервной системы и печени. Приступ гипогликемии возникает по внешним причинам: голодание, передозировка гипогликемических препаратов, интенсивная физическая нагрузка, психоэмоциональное потрясение. Обострения болезни возникают нерегулярно, практически не связаны с приемом пищи. Суточное голодание не вызывает развернутой симптоматики.
Симптомы гиперинсулинизма
Клиническая картина гипогликемической болезни обусловлена понижением уровня глюкозы в крови. Развитие приступа начинается с повышения аппетита, потливости, слабости, тахикардии и ощущения голода. Позже присоединяются панические состояния: чувство страха, тревога, раздражительность, дрожь в конечностях. При дальнейшем развитии приступа отмечается дезориентация в пространстве, диплопия, парестезии (онемение, покалывание) в конечностях, вплоть до возникновения судорог. При отсутствии лечения наступает потеря сознания и гипогликемическая кома. Межприступный период проявляется снижением памяти, эмоциональной лабильностью, апатией, нарушением чувствительности и онемением в конечностях. Частый прием пищи, богатой легкоусвояемыми углеводами, провоцирует увеличение массы тела и развитие ожирения.
В современной практике выделяют 3 степени гиперинсулинизма в зависимости от тяжести течения болезни: легкую, среднюю и тяжелую. Легкая степень проявляется отсутствием симптоматики межприступного периода и органического поражения коры головного мозга. Обострения болезни проявляются реже 1 раза в месяц и быстро купируются медикаментозными препаратами или сладкой пищей. При средней степени тяжести приступы возникают чаще 1 раза в месяц, возможна потеря сознания и развитие коматозного состояния. Межприступный период характеризуется легкими нарушениями поведенческого характера (забывчивость, снижение мышления). Тяжелая степень развивается при необратимых изменениях коры головного мозга. При этом приступы случаются часто и заканчиваются потерей сознания. В межприступном периоде пациент дезориентирован, память резко снижена, отмечается тремор конечностей, характерна резкая смена настроения и повышенная раздражительность.
Осложнения гиперинсулинизма
Осложнения можно условно разделить на ранние и поздние. К ранним осложнениям, возникающим в ближайшие часы после приступа, относят инсульт, инфаркт миокарда вследствие резкого снижения метаболизма сердечной мышцы и головного мозга. В тяжелых ситуациях развивается гипогликемическая кома. Поздние осложнения проявляются спустя несколько месяцев или лет от начала болезни и характеризуются нарушением памяти и речи, паркинсонизмом, энцефалопатией. Отсутствие своевременного диагностики и лечения заболевания приводит к истощению эндокринной функции поджелудочной железы и развитию сахарного диабета, метаболического синдрома, ожирения. Врожденный гиперинсулинизм в 30% случаев приводит к хронической гипоксии головного мозга и снижению полноценного умственного развития ребенка.
Диагностика гиперинсулинизма
Диагностика основывается на клинической картине (потеря сознания, тремор, психомоторное возбуждение), данных анамнеза заболевания (время начала приступа, его связь с приемом пищи). Эндокринолог уточняет наличие сопутствующих и наследственных заболеваний (жировой гепатоз, сахарный диабет, синдром Иценко-Кушинга), после чего назначает лабораторные и инструментальные исследования. Пациенту проводится суточное измерение уровня глюкозы крови (гликемический профиль). При выявлении отклонений выполняют функциональные пробы. Проба с голоданием используется для дифференциальной диагностики первичного и вторичного гиперинсулинизма. Во время теста измеряют С-пептид, иммунореактивный инсулин (ИРИ) и глюкозу в крови. Повышение данных показателей свидетельствует об органическом характере болезни.
Для подтверждения панкреатической этиологии заболевания проводят тесты на чувствительность к толбутамиду и лейцину. При положительных результатах функциональных проб показано УЗИ, сцинтиграфия и МРТ поджелудочной железы. При вторичном гиперинсулинизме для исключения новообразований других органов выполняют УЗИ брюшной полости, МРТ головного мозга. Дифференциальная диагностика гипогликемической болезни проводится с синдромом Золлингера-Эллисона, началом развития сахарного диабета 2 типа, неврологическими (эпилепсия, новообразования головного мозга) и психическими (неврозоподобные состояния, психоз) заболеваниями.
Лечение гиперинсулинизма
Тактика лечения зависит от причины возникновения гиперинсулинемии. При органическом генезе показано хирургическое лечение: частичная резекция поджелудочной железы или тотальная панкреатэктомия, энуклеация новообразования. Объем оперативного вмешательства определяется местоположением и размерами опухоли. После операции обычно отмечается транзиторная гипергликемия, требующая медикаментозной коррекции и диеты с пониженным содержанием углеводов. Нормализация показателей наступает через месяц после вмешательства. При неоперабельных опухолях проводят паллиативную терапию, направленную на профилактику гипогликемии. При злокачественных новообразованиях дополнительно показана химиотерапия.
Функциональный гиперинсулинизм в первую очередь требует лечения основного заболевания, вызвавшего повышенную продукцию инсулина. Всем больным назначается сбалансированная диета с умеренным снижением потребления углеводов (100-150 гр. в сутки). Отдается предпочтение сложным углеводам (ржаные хлебцы, макароны из твердых сортов пшеницы, цельнозерновые крупы, орехи). Питание должно быть дробным, 5-6 раз в день. В связи с тем, что периодические приступы вызывают у пациентов развитие панических состояний, рекомендована консультация психолога. При развитии гипогликемического приступа показано употребление легкоусвояемых углеводов (сладкий чай, конфета, белый хлеб). При отсутствии сознания необходимо внутривенное введение 40 % раствора глюкозы. При судорогах и выраженном психомоторном возбуждении показаны инъекции транквилизаторов и седативных препаратов. Лечение тяжелых приступов гиперинсулинизма с развитием комы осуществляют в условиях реанимационного отделения с проведением дезинтоксикационной инфузионной терапии, введением глюкокортикоидов и адреналина.
Прогноз и профилактика
Профилактика гипогликемической болезни включает в себя сбалансированное питание с интервалом в 2-3 часа, употребление достаточного количества питьевой воды, отказ от вредных привычек, а также контроль уровня глюкозы. Для поддержания и улучшения обменных процессов в организме рекомендованы умеренные физические нагрузки с соблюдением режима питания. Прогноз при гиперинсулинизме зависит от стадии заболевания и причин, вызывавших инсулинемию. Удаление доброкачественных новообразований в 90% случаев обеспечивают выздоровление. Неоперабельные и злокачественные опухоли вызывают необратимые неврологические изменения и требуют постоянного контроля за состоянием пациента. Лечение основного заболевания при функциональном характере гиперинсулинемии приводит к регрессии симптомов и последующему выздоровлению.
Читайте также: