Коррозия это в материаловедении кратко
Обновлено: 02.07.2024
Свидетельство и скидка на обучение каждому участнику
Зарегистрироваться 15–17 марта 2022 г.
3. Классификация коррозионных процессов по типу разрушений . 7
4.2 Методы защита от коррозии………………………………………. 10
Коррозия — это самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды.
Коррозия металлов — разрушение металлов вследствие физико-химического воздействия внешней среды, при котором металл переходит в окисленное (ионное) состояние и теряет присущие ему свойства.
В тех случаях, когда окисление металла необходимо для осуществления какого-либо технологического процесса, термин “коррозия” употреблять не следует. Например, нельзя говорить о коррозии растворимого анода в гальванической ванне, поскольку анод должен окислятся, посылая свои ионы в раствор, чтобы протекал нужный процесс. Нельзя также говорить о коррозии алюминия при осуществлении аллюмотермического процесса. Но физико-химическая сущность изменений, происходящих с металлом во всех подобных случаях, одинакова: металл окисляется.
Типы коррозии
Различают 4 основных вида коррозии, например: электрохимическая коррозия, водородная, кислородная коррозия и химическая.
Электрохимическая коррозии
Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов-называют электрохимической коррозией. Не следует путать с электрохимической коррозией коррозию однородного материала, например, ржавление железа или т. п. При электрохимической коррозии всегда требуется наличие электролита, с которым соприкасаются электроды — либо различные элементы структуры материала, либо два различных соприкасающихся материала с различающимися окислительно-восстановительными потенциалами. Если в воде растворены ионы солей, кислот, или т. п., электропроводность её повышается, и скорость процесса увеличивается.
Водородная коррозия - повреждение стали и ее страновление более хрупкой под влиянием длительного воздействия водородной среды при повышенных (gt; 200 °С) температурах эксплуатации в результате физико-химического взаимодействия водорода с отдельными компонентами и/или фазами сплава.
Водородное повреждение при повышенных температурах связано с образованием продуктов реакции между водородом и углеродом по типу: В углеродистой стали суммарная химическая реакция между углеродом, связанным в карбидах железа, и водородом может быть представлена в виде
образующийся в результате реакции метан покидает металл и/или образует внутренние полости и трещины, наполненные газообразным метаном под высоким давлением. В поверхностных слоях металла формируются обезуглероженные зоны. Водородная коррозия может протекать во всех сталях, если они содержат углерод в доступной для реакции форме и он достаточно подвижен, чтобы вступать в реакцию с водородом.
Восприимчивость стали к водородной коррозии зависит от легирующих элементов, которые воздействуют на активность углерода. Скорость водородной коррозии зависит от давления водорода и температуры, а также от размера зерен, состава их границ, степени наклепа стали и других факторов.
Кислородная коррозия возникает при питании парогенератора водой, содержащей кислород. Проявляется эта коррозия в виде язвин и питтингов на трубах. Причиной питтинговой коррозии является двойственное влияние кислорода на коррозионный процесс. С одной стороны, кислород является активным деполяризатором и ускоряет катодный процесс и коррозию в целом. С другой стороны, окисляя металл и образуя окислы, кислород играет роль пассиватора, снижающего скорость коррозии. В результате в присутствии кислорода уменьшается число анодных участков и возрастает площадь катодных участков. Коррозия становится местной, интенсивность её возрастает, разрушения идут, вглубь образуя язвы. Язвенный характер кислородной коррозии делает её особенно опасной.Наблюдается кислородная коррозия главным образом в экономайзерах. При значительном содержании кислорода в питательной воде (более 0,3 мг/кг) кислородная коррозия может протекать в пароводяном коллекторе и отпускных трубах парогенераторов с естественной циркуляцией.
Величина кислородной коррозии пропорциональна содержанию кислорода в питательной воде.
Подъёмные парообразующие трубы также могут разрушаться вследствие кислородной коррозии. Однако коррозионный процесс в них протекает менее интенсивно и практически мало зависит от содержания кислорода. Это обстоятельство связано с деаэрирующией способностью пара при кипении воды в подъёмных трубах.
Повышение давления и температуры при неизменном содержании кислорода приводит к усилению коррозии. Это связано с возрастанием скорости диффузии кислорода к катодным участкам.
Скорость кислородной коррозии зависит от плотности теплового потока, скорости циркуляции, наличия в воде солей. Если в питательной воде наряду с О 2 содержаться хлориды, то коррозия усиливается Химическая коррозия
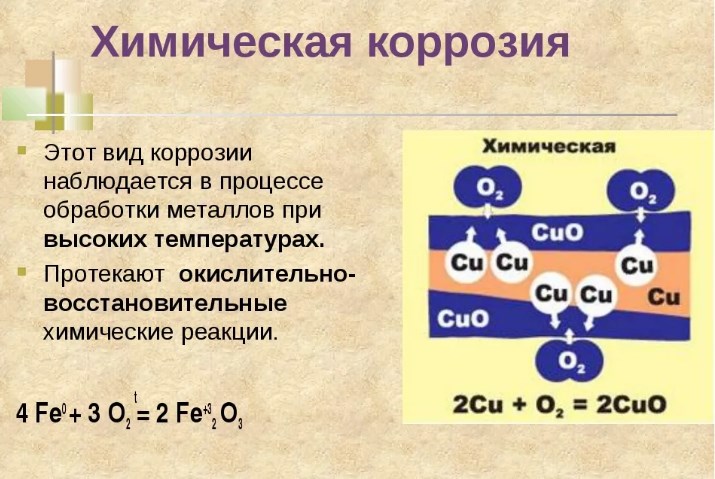
Химическая коррозия — самопроизвольное взаимодействие металла с коррозионной средой, при котором окисление металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Как и любая химическая реакция, этот вид коррозии носит временной характер. Окислителями (корродирующими агентами) могут быть сухие газы (О 2 , СО 2 , SО 2 , HC1, оксиды азота и др.), перегретый водяной пар, жидкости, не являющиеся электролитами, а также расплавы органических и неорганических веществ, в том числе металлов. Наиболее часто химической коррозии подвергается металлургическое оборудование, сопла реактивных двигателей, детали газовых турбин и двигателей внутреннего сгорания, оболочки ракет и космических кораблей, т. е. изделия, работающие при высоких температурах.
Скорость коррозии
Скорость коррозии металлов и металлических покрытий в атмосферных условиях определяется комплексным воздействием ряда факторов: наличием на поверхности фазовых и адсорбционных пленок влаги, загрязненностью воздуха коррозионно-агрессивными веществами, изменением температуры воздуха и металла, образованием продуктов коррозии и так далее.
Оценка и расчет скорости коррозии должны основываться на учете продолжительности и материальном коррозионном эффекте действия на металл наиболее агрессивных факторов.
В зависимости от факторов, влияющих на скорость коррозии, целесообразно следующее подразделение условий эксплуатации металлов, подвергаемых атмосферной коррозии:
Закрытые помещения с внутренними источниками тепла и влаги (отапливаемые помещения);
Закрытые помещения без внутренних источников тепла и влаги (неотапливаемые помещения);
Открытая атмосфера.
Классификация коррозионных процессов по типу разрушений
Наиболее часто встречаются следующие виды коррозии металлов :
Равномерная – охватывает всю поверхность равномерно
Местная пятнами – корродируют отдельные участки поверхности
Язвенная (или питтинг)
Межкристаллитная – распространяется вдоль границ кристалла металла
Защита от коррозии
Для защиты металлов от коррозии применяются различные способы, которые условно можно разделить на следующие основные направления: легирование металлов; защитные покрытия; электрохимическая защита; изменение свойств коррозионной среды; рациональное конструирование изделий.
Легирование металлов. Это эффективный метод повышения коррозионной стойкости металлов. При легировании в состав сплава или металла вводят легирующие элементы (хром, никель, молибден и др.), вызывающие пассивность металла. Пассивацией называют процесс перехода металла или сплава в состояние его повышенной коррозионной устойчивости, вызванное торможением анодного процесса. Пассивное состояние металла объясняется образованием на его поверхности совершенной по структуре оксидной пленки (оксидная пленка обладает защитными свойствами при условии максимального сходства кристаллических решеток металла и образующегося оксида).
Широкое применение нашло легирование для защиты от газовой коррозии. Легированию подвергаются железо, алюминий, медь, магний, цинк, а также сплавы на их основе. В результате чего получаются сплавы с более высокой коррозионной стойкостью, чем сами металлы. Эти сплавы обладают одновременно жаростойкостью и жаропрочностью .
Жаростойкость – стойкость по отношению к газовой коррозии при высоких температурах. Жаропрочность – свойства конструкционного материала сохранять высокую механическую прочность при значительном повышении температуры. Жаростойкость обычно обеспечивается легированием металлов и сплавов, например, стали хромом, алюминием и кремнием. Эти элементы при высоких температурах окисляются энергичнее, чем железо, и образуют при этом плотные защитные пленки оксидов.
Легирование также используется с целью снижения скорости электрохимической коррозии, особенно коррозии с выделением водорода. К коррозионностойким сплавам, например, относятся нержавеющие стали, в которых легирующими компонентами служат хром, никель и другие металлы.
Защитные покрытия. Слои, искусственно создаваемые на поверхности металлических изделий для защиты их коррозии, называются защитными покрытиями. Нанесение защитных покрытий – самый распространенный метод борьбы с коррозией. Защитные покрытия не только предохраняют изделия от коррозии, но и придают поверхностям ряд ценных физико-химических свойств. Они подразделяются на металлические и неметаллические. Общими требованиями для всех видов защитных покрытий являются высокая адгезионная способность, сплошность и стойкость в агрессивной среде.
Металлические покрытия. Металлические покрытия занимают особое положение, так как их действие имеет двойственный характер. До тех пор, пока целостность слоя покрытия не нарушена, его защитное действие сводится к изоляции поверхности защищаемого металла от окружающей среды. Это не отличается от действия любого механического защитного слоя (окраска, оксидная пленка и т.д.). Металлические покрытия должны быть непроницаемы для коррозионных агентов.
При повреждении покрытия образуется гальванический элемент. Характер коррозионного разрушения основного металла определяется электрохимическими характеристиками обоих металлов. Защитные антикоррозионные покрытия могут быть катодными и анодными . К катодным покрытиям относятся покрытия, потенциалы которых в данной среде имеют более положительное значение, чем потенциал основного металла. Анодные покрытия имеют наиболее отрицательный потенциал, чем потенциал основного металла.
При повреждении никелевого покрытия на анодных участках происходит процесс окисления железа вследствие возникновения микрокоррозионных гальванических элементов. На катодных участках - восстановление водорода. Следовательно, катодные покрытия могут защищать металл от коррозии лишь при отсутствии пор и повреждения покрытия.
Местное повреждение защитного цинкового слоя ведет к дальнейшему его разрушению, при этом поверхность железа защищена от коррозии. На анодных участках происходит процесс окисления цинка. На катодных участках - восстановление водорода.
Электродные потенциалы металлов зависят от состава растворов, поэтому при изменении состава раствора может меняться и характер покрытия.
Для получения металлических защитных покрытий применяются различные способы: электрохимический (гальванические покрытия); погружение в расплавленный металл (горячее цинкование, лужение); металлизация (нанесение расплавленного металла на защищаемую поверхность с помощью струи сжатого воздуха); химический (получение металлических покрытий с помощью восстановителей, например гидразина).
Методы защита от коррозии
На скорость коррозии влияют как внутренние факторы (наличие дефектов кристаллической решетки металла, механические напряжения и др.), так и внешние: температура, природа и состав электролита. С повышением температуры скорость коррозии, как и большинства химических реакций, возрастает. Усиливают коррозию содержащаяся в атмосфере промышленных городов пыль, SO 2 , СO 2 и другие газы. Поэтому в городах коррозия протекает в 5-10 раз быстрее, чем в сельской местности. Ионы присутствующие в морской воде, являются катализаторами коррозии железа и его сплавов, так как адсорбируясь на поверхности металла, разрушают или препятствуют образованию на нем защитных слоев. Кроме того, скорость коррозии двух контактирующих металлов будет тем больше, чем больше разность потенциалов этих металлов. Полностью предотвратить процессы коррозии металлов практически не удается, однако существуют способы защиты металлов от коррозии.
1. Изменение коррозионной среды - этот метод пригоден для тех случаев, когда защищаемые изделия эксплуатируются в небольшом объеме. Суть метода состоит в удалении из электролита растворенного кислорода или добавлении к этому раствору веществ, замедляющих коррозию - ингибиторов.
2. Легирование металлов. Это введение в состав сплавов компонентов, повышающих химическую стойкость. Наибольшее применение находят нержавеющие стали, в состав которых входит хром , до 15 % и никель, до 10 %. Кроме того, в качестве легирующих компонентов используют марганец, кремний, вольфрам, молибден, титан и другие металлы.
3. Неметаллические покрытия . Механически защищают металлы от коррозии, изолируя их от влияния внешней среды. Неметаллические покрытия делятся на неорганические и органические. Из неорганических покрытий наиболее распространены оксидные и фосфатные пленки. Так, при кипячении железа в растворе солей фосфорной кислоты получают фосфатные пленки, хорошо защищающие от коррозии в атмосфере. Среди органических, покрытий наиболее распространенными являются масляные краски, лаки, полимерные пленки. Лакокрасочные покрытия - самый дешевый метод защиты от коррозии.
4. Металлические покрытия. По характеру защитного действия различают анодные и катодные покрытия. Анодным является покрытие металлом, электродный потенциал которого меньше, чем у защищаемого металла. Покрытие из металла менее активного (с большим электродным потенциалом), чем защищаемый металл, называется катодным. Если покрытие не нарушено и полностью изолирует основной металл от воздействия окружающей среды, принципиального различия между анодными и катодными покрытиями нет. При нарушении слоя защищающего металла возникают коррозионные гальванические элементы, в которых защищаемый металл может играть роль или инертного катода, или активного анода.
5. Электрохимическая защита:
а) катодная защита. Защищаемую конструкцию присоединяют к катоду внешнего источника тока, в результате она становится катодом, не окисляется, на ней идет восстановление компонентов среды. В качестве анода применяют любой металлический лом, который присоединяют к аноду внешнего источника тока. Таким способом защищают, например, подземные трубопроводы;
б) протекторная защита. Защищаемый металл соединяют с более активным металлом, имеющим меньший электродный потенциал. Последний служит анодом, растворяется и защищает основной металл.
Для более активной защиты металлических конструкций можно совмещать несколько способов защиты от коррозии, например, покрытие и катодную электрозащиту.
Материалы из металлов под химическим или электрохимическим воздействием окружающей среды подвергаются разрушению, которое называется коррозией.
Коррозия металлов вызывается окислительно-восстановительными реакциями, в результате которых металлы переходят в окисленную форму и теряют свои свойства, что приводит в негодность металлические материалы.
Можно выделить 3 признака, характеризующих коррозию:
- Коррозия – это с химической точки зрения процесс окислительно-восстановительный.
- Коррозия – это самопроизвольный процесс, возникающий по причине неустойчивости термодинамической системы металл – компоненты окружающей среды.
- Коррозия – это процесс, который развивается в основном на поверхности металла. Однако, не исключено, что коррозия может проникнуть и вглубь металла.
Виды коррозии металлов
Наиболее часто встречаются следующие виды коррозии металлов:
- Равномерная – охватывает всю поверхность равномерно
- Неравномерная
- Избирательная
- Местная пятнами – корродируют отдельные участки поверхности
- Язвенная (или питтинг)
- Точечная
- Межкристаллитная – распространяется вдоль границ кристалла металла
- Растрескивающая
- Подповерхностная

Основные виды коррозии металлов
С точки зрения механизма коррозионного процесса можно выделить два основных типа коррозии: химическую и электрохимическую.
Химическая коррозия металлов
Химическая коррозия металлов — это результат протекания таких химических реакций, в которых после разрушения металлической связи, атомы металла и атомы, входящие в состав окислителей, образуют химическую связь.
Электрический ток между отдельными участками поверхности металла в этом случае не возникает. Такой тип коррозии присущ средам, которые не способны проводить электрический ток – это газы, жидкие неэлектролиты.
Виды химической коррозии
Химическая коррозия металлов бывает газовой и жидкостной.
Газовая коррозия металлов – это результат действия агрессивных газовых или паровых сред на металл при высоких температурах, при отсутствии конденсации влаги на поверхности металла. Это, например, кислород, диоксид серы, сероводород, пары воды, галогены. Такая коррозия в одних случаях может привести к полному разрушению металла (если металл активный), а в других случаях на его поверхности может образоваться защитная пленка (например, алюминий, хром, цирконий).
Жидкостная коррозия металлов– может протекать в таких неэлектролитах, как нефть, смазочные масла, керосин и др. Этот тип коррозии при наличии даже небольшого количества влаги, может легко приобрести электрохимический характер.
При химической коррозии скорость разрушения металла пропорциональна скорости химической реакции и той скорости с которой окислитель проникает сквозь пленку оксида металла, покрывающую его поверхность. Оксидные пленки металлов могут проявлять или не проявлять защитные свойства, что определяется сплошностью.
Фактор Пиллинга-Бэдворса
Сплошность такой пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе) по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла
где Vок — объем образовавшегося оксида
VМе — объем металла, израсходованный на образование оксида
Мок – молярная масса образовавшегося оксида
ρМе – плотность металла
n – число атомов металла
AMe — атомная масса металла
ρок — плотность образовавшегося оксида
Оксидные пленки, у которых α 2,5 условие сплошности уже не соблюдается, вследствие чего такие пленки не защищают металл от разрушения.
Ниже представлены значения сплошности α для некоторых оксидов металлов
| Металл | Оксид | α | Металл | Оксид | α |
| K | K2O | 0,45 | Zn | ZnO | 1,55 |
| Na | Na2O | 0,55 | Ag | Ag2O | 1,58 |
| Li | Li2O | 0,59 | Zr | ZrO2 | 1.60 |
| Ca | CaO | 0,63 | Ni | NiO | 1,65 |
| Sr | SrO | 0,66 | Be | BeO | 1,67 |
| Ba | BaO | 0,73 | Cu | Cu2O | 1,67 |
| Mg | MgO | 0,79 | Cu | CuO | 1,74 |
| Pb | PbO | 1,15 | Ti | Ti2O3 | 1,76 |
| Cd | CdO | 1,21 | Cr | Cr2O3 | 2,07 |
| Al | Al2O2 | 1,28 | Fe | Fe2O3 | 2,14 |
| Sn | SnO2 | 1,33 | W | WO3 | 3,35 |
| Ni | NiO | 1,52 |
Электрохимическая коррозия металлов
Электрохимическая коррозия металлов – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
При таком типе коррозии атом удаляется из кристаллической решетки результате двух сопряженных процессов:
- Анодного – металл в виде ионов переходит в раствор.
- Катодного – образовавшиеся при анодном процессе электроны, связываются деполяризатором (вещество — окислитель).
Сам процесс отвода электронов с катодных участков называется деполяризацией, а вещества способствующие отводу – деполяризаторами.
Наибольшее распространение имеет коррозия металлов с водородной и кислородной деполяризацией.
Водородная деполяризация
Водородная деполяризация осуществляется на катоде при электрохимической коррозии в кислой среде:
2H + +2e — = H2 разряд водородных ионов
Кислородная деполяризация
Кислородная деполяризация осуществляется на катоде при электрохимической коррозии в нейтральной среде:
O2 + 4H + +4e — = H2O восстановление растворенного кислорода
Все металлы, по их отношению к электрохимической коррозии, можно разбить на 4 группы, которые определяются величинами их стандартных электродных потенциалов:
- Активные металлы (высокая термодинамическая нестабильность) – это все металлы, находящиеся в интервале щелочные металлы — кадмий (Е 0 = -0,4 В). Их коррозия возможна даже в нейтральных водных средах, в которых отсутствуют кислород или другие окислители.
- Металлы средней активности (термодинамическая нестабильность) – располагаются между кадмием и водородом (Е 0 = 0,0 В). В нейтральных средах, в отсутствии кислорода, не корродируют, но подвергаются коррозии в кислых средах.
- Малоактивные металлы (промежуточная термодинамическая стабильность) – находятся между водородом и родием (Е 0 = +0,8 В). Они устойчивы к коррозии в нейтральных и кислых средах, в которых отсутствует кислород или другие окислители.
- Благородные металлы (высокая термодинамическая стабильность) – золото, платина, иридий, палладий. Могут подвергаться коррозии лишь в кислых средах при наличии в них сильных окислителей.
Виды электрохимической коррозии
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
- Коррозия в растворах электролитов — в растворах кислот, оснований, солей, в природной воде.
- Атмосферная коррозия – в атмосферных условиях и в среде любого влажного газа. Это самый распространенный вид коррозии.
Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
А: Fe – 2e — = Fe 2+
K: O2 + 4H + + 4e — = 2H2O
Катодом является та поверхность, где больше приток кислорода.
- Почвенная коррозия – в зависимости от состава почв, а также ее аэрации, коррозия может протекать более или менее интенсивно. Кислые почвы наиболее агрессивны, а песчаные – наименее.
- Аэрационная коррозия — возникает при неравномерном доступе воздуха к различным частям материала.
- Морская коррозия – протекает в морской воде, в связи с наличием в ней растворенных солей, газов и органических веществ.
- Биокоррозия – возникает в результате жизнедеятельности бактерий и других организмов, вырабатывающих такие газы как CO2, H2S и др., способствующие коррозии металла.
- Электрокоррозия – происходит под действием блуждающих токов на подземных сооружениях, в результате работ электрических железных дорог, трамвайных линий и других агрегатов.
Методы защиты от коррозии металла
Основной способ защиты от коррозии металла – это создание защитных покрытий – металлических, неметаллических или химических.
Металлические покрытия
Металлическое покрытие наносится на металл, который нужно защитить от коррозии, слоем другого металла, устойчивого к коррозии в тех же условиях. Если металлическое покрытие изготовлено из металла с более отрицательным потенциалом (более активный) , чем защищаемый, то оно называется анодным покрытием. Если металлическое покрытие изготовлено из металла с более положительным потенциалом (менее активный), чем защищаемый, то оно называется катодным покрытием.
Например, при нанесении слоя цинка на железо, при нарушении целостности покрытия, цинк выступает в качестве анода и будет разрушаться, а железо защищено до тех пор, пока не израсходуется весь цинк. Цинковое покрытие является в данном случае анодным.
Катодным покрытием для защиты железа, может, например, быть медь или никель. При нарушении целостности такого покрытия, разрушается защищаемый металл.
Неметаллические покрытия
Такие покрытия могут быть неорганические (цементный раствор, стекловидная масса) и органические (высокомолекулярные соединения, лаки, краски, битум).
Химические покрытия
В этом случае защищаемый металл подвергают химической обработке с целью образования на поверхности пленки его соединения, устойчивой к коррозии. Сюда относятся:
оксидирование – получение устойчивых оксидных пленок (Al2O3, ZnO и др.);
азотирование – поверхность металла (стали) насыщают азотом;
воронение стали – поверхность металла взаимодействует с органическими веществами;
цементация – получение на поверхности металла его соединения с углеродом.
Изменение состава технического металла и коррозионной среды
Изменение состава технического металла также способствует повышению стойкости металла к коррозии. В этом случае в металл вводят такие соединения, которые увеличивают его коррозионную стойкость.
Изменение состава коррозионной среды (введение ингибиторов коррозии или удаление примесей из окружающей среды) тоже является средством защиты металла от коррозии.
Электрохимическая защита
Электрохимическая защита основывается на присоединении защищаемого сооружения катоду внешнего источника постоянного тока, в результате чего оно становится катодом. Анодом служит металлический лом, который разрушаясь, защищает сооружение от коррозии.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором. Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
Примеры задач с решениями на определение защитных свойств оксидных пленок, определение коррозионной стойкости металлов, а также уравнения реакций, протекающих при электрохимической коррозии металлов приведены в разделе Задачи к разделу Коррозия металлов
- Определение коррозии
- Виды коррозии металлов
- Химическая
- Методы защиты от коррозии
- Металлические покрытия
- Неметаллические покрытия
- Химические покрытия
- Изменение состава технического металла и коррозионной среды
- Электрохимическая защита
Теория коррозии предполагает, что для начала разрушения металла необходимо наличие четырёх основных компонентов:
Электрического соединения, которое существует между катодом и анодом.
Электролита или любой другой токопроводящей среды, облегчающей направленное перемещение ионов.
Обычное образование ржавчины на стали можно рассматривать как электрическую батарейку. Когда атомы металлов подвергаются воздействию окружающей среды, которая содержит кислород, металл производит электроны. Это действие можно локально ограничить, чтобы создать трещину или микроуглубление. С развитием процесса коррозия распространяется на прилегающую территорию, что приведет к общему ухудшению состояния поверхности. Ограниченная (точечная) коррозия способна вызвать усталость металла – снижение его прочностных характеристик, а имеющиеся коррозионные агенты, например, морская вода, могут привести к прогрессирующему росту трещины.

Теория коррозии утверждает также, что интенсификации поверхностного разрушения металла способствуют микроструктурные изменения, возникающие при повышенных температурах, в частности, при сварке. Это объясняется повышенными значениями энергии активации, из-за чего количество ионов, проводящих электрический ток, лавинообразно возрастает.
Определение коррозии
Коррозия - это постепенное разрушение объектов, обычно металлов, вызванное активной окружающей средой-электролитом и химической реакцией окисления.
Суть коррозионного процесса – наличие постоянно действующей анодной реакции. Она вызывается за счёт растворения металла, который генерирует электроны. Часть энергии активации дополнительно расходуется на другой процесс, называемый катодной реакцией. Эти два процесса уравновешивают произведенные заряды. Зоны, вызывающие эти процессы, могут быть расположены близко или далеко друг от друга, в зависимости от ситуации.
Электроны, генерируемые в процессе, должны потребляться посредством катодной реакции. Ионы водорода и электроны вступают в реакцию с образованием атомарного, а затем и газообразного водорода. Однако водород является сильнейшим восстановителем, поэтому дальнейшую коррозию можно предотвратить, создав на поверхности металла тонкую газовую плёнку. Она служит поляризатором, уменьшающим контакт металла с водой и уменьшающим коррозию. Таким образом, всё, что разрушает барьерную плёнку, увеличивает скорость коррозии.
Основными факторами, определяющими интенсивность процесса, являются:
Уровень возникающих механических и термических напряжений;
Характер протекающих химических реакций.
Коррозия сдерживает внедрение в производство новых металлических материалов и причиняет значительный ущерб экономике.
Виды коррозии металлов
Классификация всех коррозионных явлений может быть произведена по следующим параметрам:
По степени равномерности. Различают поверхностную коррозию, которая равномерно уменьшает толщину поверхности, и неравномерную коррозию – точечную или язвенную;
При межкристаллитной коррозии разрушение происходит по границам зёрен и распространяется вглубь металла.
Фреттинг-коррозия, когда два контактирующих между собой тела совершают относительно друг друга колебательные движения малой амплитуды (не более 100 мкм).
При одновременном воздействии растягивающих напряжений и агрессивной среды наблюдается коррозионное растрескивание межкристаллитного или транскристаллитного характера, а при наложении знакопеременных напряжений начинается коррозионно-усталостное разрушение. Защита металлов от коррозии, таким образом, предполагает также и одновременное уменьшение износа деталей.

Далее рассматриваются основные явления, которые происходят в повреждающихся зонах при различных видах коррозии.
Химическая
Химическая коррозия относится к постепенному разрушению поверхности металла из-за реакции поверхности с веществами во внешней среде. Она происходит в результате окисления металла кислотами с образованием оксидов.
Высокотемпературный вариант заключается в воздействии на металл сухих газов. Все металлы в сухом воздухе покрыты очень тонким (2…10 мкм) слоем оксидов. Этот слой образуется при очень высоких температурах, когда реакция с кислородом воздуха идёт без каких-либо ограничений. При комнатной температуре реакция останавливается, поскольку оксидная плёнка становится слишком тонкой. В случае, например, с алюминием, такая плёнка, состоящая из оксида Al2O3, эффективно защищает поверхность алюминиевой посуды, поскольку коррозионная стойкость чистого алюминия невысока.
Химическая коррозия начинается в месте, где металл находится под давлением и изолирован от циркуляции воздуха. Это побуждает ионы металлов растворяться во влажной среде, что в конечном итоге ускоряет реакцию между ними и водой. В результате реакции образуются водные оксиды (известные при взаимодействии с железом как ржавчина) и свободные ионы.
Электрохимическая
Для моделирования процесса необходимо рассмотреть железную пластину, покрытую любым электропроводящим покрытием, например, оксидной окалиной, которая образовалась во время высокотемпературной обработки. При погружении пластины в раствор хлорида натрия, обнаруживается, что, если повредить целостность окалины, в этом месте ржавление железа пойдёт значительно быстрее. Электрохимическая коррозия наиболее достоверно объясняет ржавление железа в аэробных условиях.
Теория электрохимической коррозии предполагает наличие дополнительных химических реакций:
Fe → Fe ++ + 2e−, - анодная реакция;
2e− + O + H2O → 2OH− - катодная реакция.
Когда ионы металла растворяются, их заряд уравновешивается ионами хлорида, которые мигрируют в область атаки, притягиваясь образующимися ионами положительного заряда. Хлорид железа растворяется в воде, но это не создаёт препятствий для дальнейшей коррозии, поскольку раствор хлорида железа вследствие гидролиза очень кислый. По мере того, как ионы Fe ++ удаляются из этого места, они сталкиваются с гидроксильными ионами, которые либо присутствуют в воде естественным образом, либо образуются в результате катодной реакции. Результатом является образование и осаждение гидроксида железа Fe (OH)2. Далее, в присутствии растворённого кислорода, он быстро окисляется до оксигидроксида железа FeOOH.
Таким образом, при электрохимической коррозии происходят три реакции, причём в трёх разных местах. Анодная происходит в зонах потери металла, катодная – там, где растворённый в воде кислород может принимать электроны, а сама твёрдая окалина формируется в местах механических повреждений на поверхности изделия.
В последнее время выделяют ещё один вид коррозии – механохимическую, которая происходит в результате динамического взаимодействия контактирующих элементов окружающей среды в условиях высоких контактных давлений.
Методы защиты от коррозии
Ржавчина и другие коррозионные проявления могут приводить к проблемам с безопасностью, нарушать целостность производственного оборудования и расходных материалов. Даже плановое техническое обслуживание по удалению и устранению ржавчины увеличивает эксплуатационные затрат. Отработано ряд способов, используя которые, можно минимизировать коррозию.
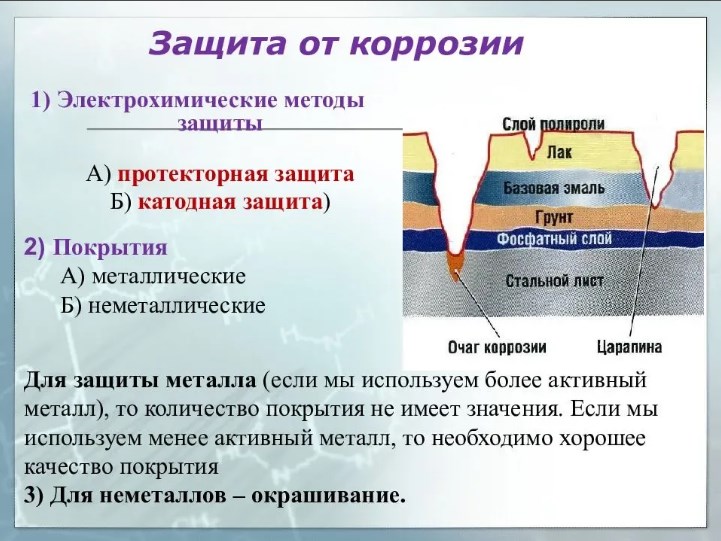
Металлические покрытия
Эти методы предотвращения коррозии заключаются в погружении стали в расплав металла, электрический потенциал которого меньше, чем железа (чем больше разница, тем эффективнее покрытие).
Практическое применение находят гальванические покрытия цинком или оловом, а также диффузионные покрытия никелем, хромом, кремнием или алюминием. По сравнению с другими методами защиты от коррозии гальванизация известна более низкими начальными затратами, устойчивостью и универсальностью.
Поскольку расход металла-протектора довольно велик, преимущество получают технологии, отличающиеся экономичностью используемых компонентов и прочностью создаваемых покрытий. Первым в этом списке находится цинкование. Железо в стали вступает в реакцию с цинком, образуя прочное покрытие из сплава, которое служит защитой.
Неметаллические покрытия
Один из самых простых способов предотвратить коррозию - использовать защитные покрытия из неметаллов - краски, пластика, воска или порошка. Порошки, включая эпоксидную смолу, нейлон и уретан, наносятся на металлическую поверхность и нагреваются до стадии расплавления, образуя тонкую плёнку.
Краска действует как покрытие, защищающее металлическую поверхность от электрохимического заряда, который исходит от коррозионно опасных соединений. Обычно используют комбинацию различных слоёв краски, которые выполняют разные функции. Грунтовка действует как ингибитор, промежуточный слой увеличивает общую толщину краски, а финишный слой обеспечивает устойчивость к факторам окружающей среды.
Химические покрытия
Относятся к методам временной антикоррозионной защиты стали, например, во время пластического деформирования при повышенных температурах. Наибольшее распространение получили технологии фосфатирования и оксалатирования.
При фосфатировании поверхность покрывают сплошным слоем фосфатных солей железа и марганца, а при оксалатировании – водорастворимыми солями щавелевой кислоты. Фосфатирование используется для обработки нелегированных сталей, оксалатирование – легированных. Покрытие прочно сцепляется с поверхностью, способствуя снижению трения и уменьшению износа инструмента. После окончания штамповки покрытие удаляют.
Изменение состава технического металла и коррозионной среды
Заключается в специальном легировании стали элементами, повышающими её коррозионную стойкость. Если это возможно, то в механическую систему, которая работает в условиях повышенной температуры и влажности, вводят смазку, содержащую противокоррозионные компоненты (восстановители).
Элементом, который положительно влияет на коррозионную стойкость стали, является хром. Для реализации этого эффекта сталь должна содержать не менее 13% хрома. Каждые дополнительные 5% хрома обеспечивают еще лучшую коррозионную стойкость.

Никель - второй важный элемент для улучшения коррозионной стойкости стали, причём добавка никеля приводит также к стабилизации аустенита. Третьим важным элементом повышения коррозионной стойкости является молибден. Однако его добавки повышают коррозионную стойкость только нержавеющих сталей с достаточным содержанием хрома и никеля.
Электрохимическая защита
Процесс коррозии, которая возникает при контакте двух разных металлов, находящихся в электролите, можно остановить использованием системы катодной защиты. Для реализации метода активные центры на поверхности металла необходимо преобразовать в пассивные путем предоставления электронов из другого источника (обычно используют аноды, прикрепленные к поверхности). Металлы, используемые для анодов - алюминий, магний или цинк.
Катодная защита очень эффективна в бытовой технике, однако аноды необходимо часто проверять, что увеличивает расходы на техническое обслуживание.
Коррозионная стойкость металла зависит от его природы, характера среды и температуры.
- Благородные металлы не подвергаются коррозии из-за химической инертности.
- Металлы Al, Ti, Zn, Cr, Ni имеют плотные газонепроницаемые оксидные плёнки, которые препятствуют коррозии.
- Металлы с рыхлой оксидной плёнкой – Fe, Cu и другие – коррозионно неустойчивы. Особенно сильно ржавеет железо.
Различают химическую и электрохимическую коррозию.
| Химическая коррозия сопровождается химическими реакциями. Как правило, химическая коррозия металлов происходит при действии на металл сухих газов, её также называют газовой. |
При химической коррозии также возможны процессы:
Fe + 2HCl → FeCl2 + H2
2Fe + 3Cl2 → 2FeCl3
Как правило, такие процессы протекают в аппаратах химических производств.
| Электрохимическая коррозия – это процесс разрушения металла, который сопровождается электрохимическими процессами. Как правило, электрохимическая коррозия протекает в присутствии воды и кислорода, либо в растворах электролитов. |
В таких растворах на поверхности металла возникают процессы переноса электронов от металла к окислителю, которым является либо кислород, либо кислота, содержащаяся в растворе.
При этом электродами являются сам металл (например, железо) и содержащиеся в нем примеси (обычно менее активные металлы, например, олово).
В таком загрязнённом металле идёт перенос электронов от железа к олову, при этом железо (анод) растворяется, т.е. подвергается коррозии:
Fe –2e = Fe 2+
На поверхности олова (катод) идёт процесс восстановления водорода из воды или растворённого кислорода:
2H + + 2e → H2
O2 + 2H2O + 4e → 4OH –
| Например, при контакте железа с оловом в растворе соляной кислоты происходят процессы: |
Анод: Fe –2e → Fe 2+
Катод: 2H + + 2e → H2
Суммарная реакция: Fe + 2H + → H2 + Fe 2+
Если реакция проходит в атмосферных условиях в воде, в ней участвует кислород и происходят процессы:
Анод: Fe –2e → Fe 2+
Катод: O2 + 2H2O + 4e → 4OH –
Суммарная реакция:
Fe 2+ + 2OH – → Fe(OH)2
4Fe(OH)2 + O2+ 2H2O → 4Fe(OH)3
При этом образуется ржавчина.
Защитные покрытия
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
- Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
- Покрытие краской, лаками, смазками.
- Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Создание сплавов, стойких к коррозии
Физические свойства сплавов могут существенно отличаться от свойств чистых металлов. Добавление некоторых металлов может приводить к повышению коррозионной стойкости сплава. Например, нержавеющая сталь, новые сплавы с большой коррозионной устойчивостью.
Изменение состава среды
Коррозия замедляется при добавлении в среду, окружающую металлическую конструкцию, ингибиторов коррозии. Ингибиторы коррозии — это вещества, подавляющие процессы коррозии.
Электрохимические методы защиты
Протекторная защита: при присоединении к металлической конструкции пластинок из более активного металла – протектора. В результате идёт разрушение протектора, а металлическая конструкция при этом не разрушается.

Коррозия - это разрушение металла под действием окружающей среды. Признаком коррозии является потеря металлического блеска и появление ржавчины на поверхности металла. Коррозия приводит к существенному ухудшению механических свойств металла и его деградации. В зависимости от механизма коррозионного разрушения различают химическую и электрохимическую коррозию.
Химическая коррозия вызывается действием на металл сухих газов и неэлектролитов и не сопровождается появлением электрического тока.
Электрохимическая коррозия обусловлена действием на металл электролитов-растворов, содержащих ионы и являющиеся проводниками электрического тока. При электрохимической коррозии возникает электрический ток. К электролитам относятся водные растворы солей, кислот и щелочей. Если два металла, находящихся в электролите, получают различные электродные потенциалы, то металл с отрицательным потенциалом (анод) отдает свои положительные ионы в раствор и постепенно разрушается (растворяется). Избыточные электроны переходят в металл, чем выше электродный потенциал (катод). Сам катод не претерпевает разрушения, а электроны с катода переходят во внешнюю среду. Чем ниже электродный потенциал металла, тем быстрее он отдает свои ионы в раствор и ниже его коррозионная стойкость.
Химические элементы - металлы и водород - можно расставить в ряд по убыванию их электродного потенциала: Аu, Рt, Ag, Сu, Н, Ni, Fe, Zn, Al. Самый высокий потенциал имеет золото, нулевой потенциал - водород, а самый низкий потенциал из перечисленных элементов имеет алюминий.
Устойчивость стали к коррозии можно повысить, легируя хромом, алюминием или кремнием, которые образуют на поверхности плотные оксидные пленки.
Читайте также:

