Кинетика ферментативных реакций биохимия кратко
Обновлено: 05.07.2024
Кинетика ферментативных реакций — раздел энзимологии, изучающий зависимость скорости химических реакций, катализируемых ферментами, от химической природы реагирующих веществ, а также от факторов окружающей среды.
Для измерения каталитической активности ферментов используют такие показатели, как скорость реакции или активность фермента. Скорость ферментативной реакции определяется изменением количества молекул субстрата или продукта за единицу времени. Скорость ферментативной реакции — мера каталитической активности фермента, её обозначают как активность фермента.
Математически скорость ферментативной реакции выражается в изменении концентрации субстрата (уменьшение) или продукта (увеличение) за единицу времени:
На начальном этапе [0 — t0] скорость реакции прямо пропорциональна времени и имеет линейную зависимость. Графически изменение скорости ферментативной реакции определяется тангенсом угла наклона касательной к кривой профиля реакции. Чем больше угол наклона, тем больше изменение скорости реакции (рис. 2-15).

С течением времени изменение скорости ферментативной реакции в экспериментальных условиях уменьшается, об этом свидетельствует уменьшение угла наклона касательной в момент времени 1. Снижение скорости ферментативной реакции может происходить за счёт ряда факторов: уменьшения концентрации субстрата, увеличения концентрации продукта, который может оказывать ингибирующее действие, могут происходить изменения pH раствора, инактивация фермента и т. д.
На этапе [t1- tx] скорость реакции изменяется нелинейно в зависимости от времени. Поэтому для определения скорости ферментативной реакции чаще всего исследуют изменение скорости на начальном этапе [t0 - t1], где наблюдают линейное изменение концентрации продукта (или субстрата).
Скорость ферментативной реакции зависит от ряда факторов, таких как количество и активность ферментов, концентрация субстрата, температура среды, pH раствора, присутствие регуляторных молекул (активаторов и ингибиторов). Рассмотрим влияние этих факторов на скорость ферментативной реакции.
А. Зависимость скорости ферментативной реакции от количества ферментов
При проведении ферментативной реакции в условиях избытка субстрата скорость реакции будет зависеть от концентрации фермента. Графическая зависимость такой реакции имеет вид прямой линии (рис. 2-16). Однако количество фермента часто невозможно определить в абсолютных величинах, поэтому на практике пользуются условными величинами, характеризующими активность фермента: одна международная единица активности (МЕ) соответствует такому количеству фермента, которое катализирует превращение 1 мкмоль субстрата за 1 мин при оптимальных условиях проведения ферментативной реакции. Оптимальные условия индивидуальны для каждого фермента и зависят от температуры среды, pH раствора, при отсутствии активаторов и ингибиторов.

Рис. 2-16. Зависимость скорости ферментативной реакции (V) от концентрации фермента.

Количество единиц активности nМЕ определяют по формуле:

В 1973 г. была принята новая единица активности ферментов: 1 катал (кат), соответствующий такому количеству катализатора, которое превращает 1 моль субстрата за 1 с. Количество каталов определяют по формуле:

Международная единица ферментативной активности МЕ связана с каталом следующими равенствами:
1 кат = 1 моль S/с = 60 моль S/мин = 60 х 10 6 мкмоль/мин = 6 х 10 7 МЕ,
1 МЕ = 1 мкмоль/мин = 1/60 мкмоль/с = 1/60 мккат = 16,67 нкат.
В медицинской и фармацевтической практике для оценки активности ферментов часто используют международные единицы активности — МЕ. Для оценки количества молекул фермента среди других белков данной ткани определяют удельную активность (уд. ак.) фермента, численно равную количеству единиц активности фермента (nМЕ) в образце ткани, делённому на массу (мг) белка в этой ткани:

По удельной активности судят об очистке фермента: чем меньше посторонних белков, тем выше удельная активность.
Б. Зависимость скорости ферментативной реакции от температуры среды
Повышение температуры до определённых пределов оказывает влияние на скорость ферментативной реакции, подобно влиянию температуры на любую химическую реакцию. С повышением температуры ускоряется движение молекул, что приводит к повышению вероятности взаимодействия реагирующих веществ. Кроме того, температура может повышать энергию реагирующих молекул, что также приводит к ускорению реакции. Однако скорость химической реакции, катализируемая ферментами, имеет свой температурный оптимум, превышение которого сопровождается понижением ферментативной активности, возникающим из-за термической денатурации белковой молекулы (рис. 2-17).
Рис. 2-17. Зависимость скорости ферментативной реакции (V) от температуры.

Для большинства ферментов человека оптимальна температура 37— 38 °С. Однако в природе существуют и термостабильные ферменты. Например, Taq — полимераза, выделенная из микроорганизмов, живущих в горячих источниках, не инактивируется при повышении температуры до 95 °С. Этот фермент используют в научно- практической медицине для молекулярной диагностики заболеваний с использованием метода полимеразной цепной реакции (ПЦР).
В. Зависимость скорости ферментативной реакции от рН среды
Активность ферментов зависит от pH раствора, в котором протекает ферментативная реакция. Для каждого фермента существует значение pH, при котором наблюдается его максимальная активность. Отклонение от оптимального значения pH приводит к понижению ферментативной активности.
Влияние pH на активность ферментов связано с ионизацией функциональных групп аминокислотных остатков данного белка, обеспечивающих оптимальную конформацию активного центра фермента. При изменении pH от оптимальных значений происходит изменение ионизации функциональных групп молекулы белка. Например, при закислении среды происходит протонирование свободных аминогрупп (NH3 + ), а при защелачивании происходит отщепление протона от карбоксильных групп (СОО - ). Это приводит к изменению конформации молекулы фермента и конформации активного центра; следовательно, нарушается присоединение субстрата, кофакторов и коферментов к активному центру. Кроме того, pH среды может влиять на степень ионизации или пространственную организацию субстрата, что также влияет на сродство субстрата к активному центру. При значительном отклонении от оптимального значения pH может происходить денатурация белковой молекулы с полной потерей ферментативной активности.
Оптимум значения pH у разных ферментов различный (рис. 2-18). Ферменты, работающие в кислых условиях среды (например, пепсин в желудке или лизосомальные ферменты), эволюционно приобретают конформацию, обеспечивающую работу фермента при кислых значениях pH. Однако большая часть ферментов организма человека имеет оптимум pH, близкий к нейтральному, совпадающий с физиологическим значением pH (табл. 2-1).
Одним из характерных проявлений жизни является удивительная способность живых организмов кинетически регулировать химические реакции, подавляя стремление к достижению термодинамического равновесия. Ферментативная кинетика занимается исследованием закономерностей влияния химической природы реагирующих веществ (ферментов, субстратов) и условий их взаимодействия (концентрация, рН среды, температуры, присутствие активаторов или ингибиторов) на скорость ферментативной реакции. Главной целью изучения кинетики ферментативных реакций является получение информации, которая может способствовать выяснению молекулярного механизма действия фермента.
Общие принципы кинетики химических реакций применимы и к ферментативным реакциям. Известно, что любая химическая реакция характеризуется константой термодинамического равновесия. Она выражает состояние химического равновесия, достигаемого системой, и обозначается Кр. Так, для реакции:
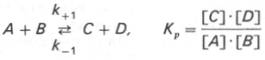
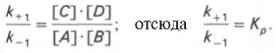
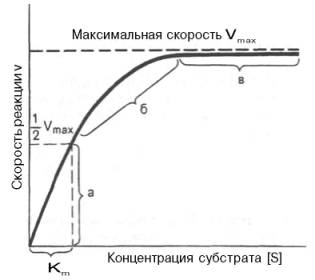
Рис. 4.12. Теоретический график зависимости скорости ферментативной реакции от концентрации субстрата при постоянной концентрации фермента.
а - реакция первого порядка (при [ S ]
Таким образом, константа равновесия равна отношению констант скоростей прямой и обратной реакций. Величину, обратную константе равновесия, принято называть субстратной константой, или, в случае ферментативной реакции, константой диссоциации фермент–субстратного комплекса, и обозначать символом KS. Так, в реакции
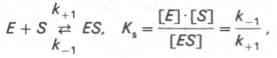
т.е. KSравна отношению произведения концентрации фермента и субстрата к концентрации фермент-субстратного комплекса или отношению констант скоростей обратной и прямой реакций. Следует отметить, что константа KSзависит от химической природы субстрата и фермента и определяет степень их сродства. Чем ниже значение KS, тем выше сродство фермента к субстрату.
При изучении кинетики ферментативных реакций следует учитывать одну важную особенность этих реакций (не свойственную обычным химическим реакциям), связанную с явлением насыщения фермента субстратом. При низкой концентрации субстрата зависимость скорости реакции от концентрации субстрата (рис. 4.12) является почти линейной и подчиняется кинетике первого порядка. Это означает, что скорость реакции S —> Р прямо пропорциональна концентрации субстрата S и в любой момент времени t определяется следующим кинетическим уравнением:
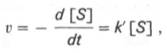
где [S] – молярная концентрация субстрата S; –d[S]/dt – скорость убыли субстрата; k' – константа скорости реакции, которая в данном случае имеет размерность, обратную единице времени (мин –1 или с –1 ).
При высокой концентрации субстрата скорость реакции максимальна, становится постоянной и не зависящей от концентрации субстрата [ S ] . В этом случае реакция подчиняется кинетике нулевого порядка v = k" (при полном насыщении фермента субстратом) и целиком определяется концентрацией фермента. Различают, кроме того, реакции второго порядка, скорость которых пропорциональна произведению концентраций двух реагирующих веществ. В определенных условиях при нарушении пропорциональности говорят иногда о реакциях смешанного порядка (см. рис. 4.12).
Изучая явление насыщения, Л. Михаэлис и М. Ментен разработали общую теорию ферментативной кинетики. Они исходили из предположения, что ферментативный процесс протекает в виде следующей химической реакции:
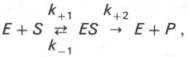
т.е. фермент Е вступает во взаимодействие с субстратом S с образованием промежуточного комплекса ES, который далее распадается на свободный фермент и продукт реакции Р. Математическая обработка на основе закона действующих масс дала возможность вывести уравнение, названное в честь авторов уравнением Михаэлиса–Ментен, выражающее количественное соотношение между концентрацией субстрата и скоростью ферментативной реакции:
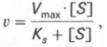
Из уравнения Михаэлиса–Ментен следует, что при высокой концентрации субстрата и низком значении KSскорость реакции является максимальной, т.е. v = Vmax(реакция нулевого порядка, см. рис. 4.12). При низкой концентрации субстрата, напротив, скорость реакции оказывается пропорциональной концентрации субстрата в каждый данный момент (реакция первого порядка).
Следует указать, что уравнение Михаэлиса–Ментен в его классическом виде не учитывает влияние на скорость ферментативного процесса продуктов реакции, например в реакции
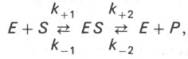
и носит несколько ограниченный характер. Поэтому были предприняты попытки усовершенствовать его. Так, было предложено уравнение Бриггса-Холдейна:
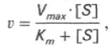
где Кm представляет собой константу Михаэлиса, являющуюся экспериментально определяемой величиной. Она может быть представлена следующим уравнением:
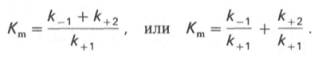
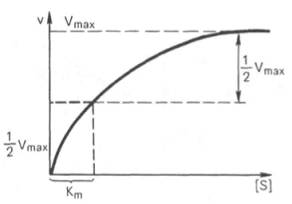
Рис. 4.13. Кривая уравнения Михаэли-са-Ментен: гиперболическая зависимость начальных скоростей катализируемой ферментом реакции от концентрации субстрата.
В числителе представлены константы скоростей распада комплекса ES в двух направлениях (в сторону исходных Е и S и в сторону конечных продуктов реакции Е и Р). Отношение k–1/ k+1представляет собой константу диссоциации ферментсубстратного комплекса KS, тогда:
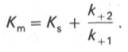
Отсюда вытекает важное следствие: константа Михаэлиса всегда больше константы диссоциации фермент-субстратного комплекса KSна величину
Для определения численного значения Кm обычно находят ту концентрацию субстрата, при которой скорость ферментативной реакции v составляет половину от максимальной Vmax, т.е. если v = 1 /2 Vmaх. Подставляя значение v в уравнение Бриггса–Холдейна, получаем:
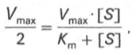
разделив обе части уравнения на Vmах, получим
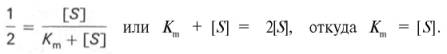
Таким образом, константа Михаэлиса численно равна концентрации субстрата (моль/л), при которой скорость данной ферментативной реакции составляет половину от максимальной.
Определение величины Кm имеет важное значение при выяснении механизма действия эффекторов на активность ферментов и т.д. Константу Михаэлиса можно вычислить по графику (рис. 4.13). Отрезок на абсциссе, соответствующий скорости, равной половине максимальной, будет представлять собой Кm.
Пользоваться графиком, построенным в прямых координатах зависимости начальной скорости реакции v0 от начальной концентрации субстрата [S0], неудобно, поскольку максимальная скорость Vmaxявляется в данном случае асимптотической величиной и определяется недостаточно точно.
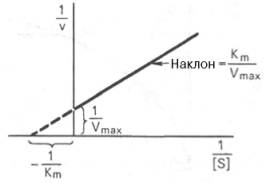
Рис. 4.14. График Лайнуивера-Бэрка.
Для более удобного графического представления экспериментальных данных Г. Лайнуивер и Д. Бэрк преобразовали уравнение Бриггса–Хол-дейна по методу двойных обратных величин исходя из того принципа, что если существует равенство между двумя какими-либо величинами, то и обратные величины также будут равны. В частности, если
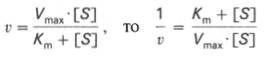
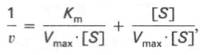
то после преобразования получаем уравнение:
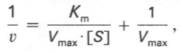
которое получило название уравнения Лайнуивера–Бэрка. Это уравнение прямой линии: у = ах + b. Если теперь в соответствии с этим уравнением построить график в координатах 1/v (y) от l/[S] (x), то получим прямую линию (рис. 4.14), тангенс угла наклона который будет равен величине Km/Vmax; отрезок, отсекаемый прямой от оси ординат, представляет собой l/Vmax(обратная величина максимальной скорости). Если продолжить прямую линию за ось ординат, тогда на абсциссе отсекается отрезок, соответствующий обратной величине константы Михаэлиса – 1/Кm (см. рис. 4.14). Таким образом, величину Кm можно вычислить из данных наклона прямой и длины отрезка, отсекаемого от оси ординат, или из длины отрезка, отсекаемого от оси абсцисс в области отрицательных значений.
Следует подчеркнуть, что значения Vmax, как и величину Кm, более точно, чем по графику, построенному в прямых координатах, можно определить по графику, построенному по методу двойных обратных величин. Поэтому данный метод нашел широкое применение в современной энзимологии. Предложены также аналогичные графические способы определения Кm и Vmaxв координатах зависимости v от v/[S] и [S]/v от [S].
Следует отметить некоторые ограничения применения уравнения Ми-хаэлиса–Ментен, обусловленные множественными формами ферментов и аллостерической природой фермента. В этом случае график зависимости начальной скорости реакции от концентрации субстрата (кинетическая
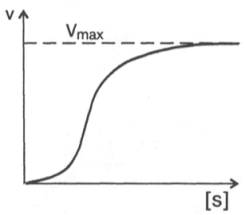
Рис. 4.15. Сигмоидная кинетическая кривая насыщения субстратом.
кривая) имеет не гиперболическую форму, а сигмоидный характер (рис. 4.15) наподобие кривой насыщения гемоглобина кислородом. Это означает, что связывание одной молекулы субстрата в одном каталитическом центре повышает связывание субстрата с другим центром, т.е. имеет место кооперативное взаимодействие, как и в случае присоединения кислорода к 4 субъединицам гемоглобина. Для оценки концентрации субстрата, при которой скорость реакции составляет половину максимальной, в условиях сигмоидного характера кинетической кривой обычно применяют преобразованное уравнение Хилла:
Ферментативная кинетика изучает влияние различных факторов (концентрация S и E, рН, температура, давление, ингибиторы и активаторы) на скорость ферментативных реакций. Главной целью изучения кинетики ферментативных реакций является получение информации, позволяющей глубже понять механизм действия ферментов.
Кинетическая кривая позволяет определить начальную скорость реакции V0.

Кривая субстратного насыщения.

График зависимости V от концентрации субстрата при фиксированной концентрации фермента представляет собой гиперболу. Вначале скорость реакции прямо пропорциональна концентрации субстрата [S] (кинетика первого порядка). Однако при увеличении [S] скорость постепенно достигает максимального значения VMAX. Это означает, что все связывающие участки фермента заняты (насыщены). Скорость реакции на этом участке не зависит от концентрации субстрата (кинетика нулевого порядка). Такую кривую называют кривой субстратного насыщения.
Зависимость скорости реакции от концентрации фермента.

При постоянной концентрации субстрата существует прямо пропорциональная зависимость между скоростью реакции и концентрацией фермента [E] в реакционной смеси. Другими словами, для данной концентрации субстрата скорость реакции возрастает в 2 раза при двукратном увеличении концентрации фермента.
Зависимость скорости реакции от температуры.

Ферменты – вещества белковой природы, проявляют максимальную активность в ограниченном температурном режиме. При температурах не выше 40-50С скорость реакции увеличивается согласно теории химической кинетики. При более высоких температурах тепловая денатурация фермента приводит к полному прекращению ферментативной реакции. Термолабильность ферментов отличает ферменты от неорганических катализаторов.
Зависимость скорости реакции от рН.

Оптимум рН действия большинства ферментов лежит в пределах физиологических значений 6,0-8,0. Пепсин активен при рН 1,5-2,0, что соответствует кислотности желудочного сока. Аргиназа, специфичный фермент печени, активен при 10,0. Влияние рН среды на скорость ферментативной реакции связывают с состоянием и степенью ионизации ионогенных групп в молекуле фермента и субстрата. Этот фактор определяет конформацию белка, состояние активного центра и субстрата, формирование фермент-субстратного комплекса, собственно процесс катализа.
Математическое описание кривой субстратного насыщения, константа Михаэлиса.

Уравнение, описывающее кривую субстратного насыщения, было предложено Михаэлисом и Ментон и носит их имена (уравнение Михаэлиса-Ментен):
V = (VMAX*[S])/(Km+[S]), где Km – константа Михаэлиса. Легко рассчитать, что при V = VMAX/2 Km = [S], т.е. Km – это концентрация субстрата, при которой скорость реакции составляет ½ VMAX.
С целью упрощения определения величины VMAX и Km уравнение Михаэлиса-Ментен можно пересчитать.
1/V = Km/(VMAX*[S]) + 1/VMAX,

1/V = Km/VMAX*1/[S] + 1/VMAX уравнение Лайнуивера-Берка. Уравнение, описывающее график Лайнуивера-Берка – это уравнение прямой линии (y = mx + c), где 1/VMAX – это отрезок, отсекаемый прямой на оси ординат; Km/VMAX - тангенс угла наклона прямой; пересечение прямой с осью абсцисс дает величину 1/Km. График Лайнуивера-Бэрка позволяет определить Km по относительно небольшому числу точек. Этот график также используют при оценке действия ингибиторов, о чем будет сказано ниже.
Значение Km изменяются в широких пределах: от 10 -6 моль/л для очень активных ферментов, до 10 -2 – для малоактивных ферментов.
Оценки Km имеют практическую ценность. При концентрациях субстрата в 100 раз превышающих Km, фермент будет работать практически с максимальной скоростью, поэтому максимальная скорость VMAX будет отражать количество присутствующего активного фермента. Это обстоятельство используют для оценки содержания фермента в препарате. Кроме того, Km является характеристикой фермента, что используется для диагностики энзимопатий.
Ингибирование активности ферментов.
Чрезвычайно характеристикой и важной особенностью ферментов является их инактивация под влиянием определенных ингибиторов.
Ингибиторы – это вещества, вызывающие частичное или полное торможение реакций, катализируемых ферментами.
Ингибирование ферментативной активности может быть необратимым или обратимым, конкурентным или неконкрентным.
Необратимое ингибирование – это стойкая инактивация фермента, возникающая в результате ковалентного связывания молекулы ингибитора в активном центре или в другом особом центре, изменяющим конформацию фермента. Диссоциация столь устойчивых комплексов с регенерацией свободного фермента практически исключена. Для преодоления последствий такого ингибирования организм должен синтезировать новые молекулы фермента.
Обратимое ингибирование – характеризуется равновесным комплексообразованием ингибитора с ферментом за счет нековалентных связей, вследствие чего такие комплексы способны к диссоциации с восстановлением активности фермента.
Классификация ингибиторов на конкурентные и неконкурентные основана на том, ослабляется (конкурентное ингибирование) или не ослабляется (неконкурентное ингибирование) их ингибирующие действие при повышении концентрации субстрата.
Конкурентные ингибиторы – это, как правило, соединения, структура которых сходна со структурой субстрата. Это позволяет им связываться в том же активном центре, что и субстраты, препятствуя взаимодействию фермента с субстратом уже на стадии связывания. После связывания ингибитор может быть превращен в некий продукт или остается в активном центре, пока не произойдет диссоциация.
Обратимое конкурентное ингибирование можно представить в виде схемы:

E↔ E-I → E + P1
+S ( неакт )
Степень ингибирования фермента определяется соотношением концентраций субстрата и фермента.
Классическим примером подобного типа ингибирования является торможение активности сукцинатдегидрогеназы (СДГ) малатом, который вытесняет сукцинат из субстратного участка и препятствует его превращению в фумарат:

Ковалентное связывание ингибитора в активном центре приводит к инактивации фермента (необратимое ингибирование). Примером необратимого конкурентного ингибирования может служить инактивация триозофосфатизомеразы 3-хлорацетолфосфатом. Этот ингибитор является структурным аналогом субстрата – диоксиацетонфосфата и необратимо присоединяется к остатку глутаминовой кислоты в активном центре:

Некоторые ингибиторы действуют менее избирательно, взаимодействуя с определенной функциональной группой в составе активного центра разных ферментов. Так, связывание йодацетата или его амида с SH-группой аминокислоты цистеина, находящийся в активном центре фермента и принемающей участие в катализе, приводит к полной утрате активности фермента:
Поэтому эти ингибиторы инактивируют все ферменты, которые имеют SH-группы, участвующие в катализе.
Необратимое ингибирование гидролаз при действии нервно-паралитических газов (зарин, зоман) обусловлено их ковалентным связыванием с остатком серина в активном центре.
Метод конкурентного ингибирования нашел широкое применение в медицинской практике. Сульфаниламидные препараты – антагонисты п-аминобензойной кислоты, могут служить примером метаболизируемых конкурентных ингибиторов. Они связываются с дигидроптератсинтетазой – бактериальным ферментом, осуществляющим превращение п-аминобензоата в фолиевую кислоту, необходимую для роста бактерий. Бактерия погибает в результате того, что связавшийся сульфаниламид превращается в другое соединение и фолиевая кислота не образуется.
Неконкурентные ингибиторы обычно связываются с молекулой фермента в участке, отличном от места связывания субстрата, и субстрат непосредственно не конкурирует с ингибитором. Поскольку ингибитор и субстрат связываются с разными центрами возможно образование как комплекса E-I, так и комплекса S-E-I. Комплекс S-E-I тоже распадается с образованием продукта, однако с меньшей скоростью, чем E-S, поэтому реакция будет замедляться, но не остановится. Таким образом, могут протекать следующие параллельные реакции:
E↔ E-I ↔ S-E-I → E-I + P
Обратимое неконкурентное ингибирование встречается сравнительно редко.
Неконкурентные ингибиторы называют аллостерическими в отличие от конкурентных (изостерических).
Обратимое ингибирование может быть количественно изучено на основе уравнения Михаэлиса-Ментен.
При конкурентном ингибировании VMAX остается постоянной, а Km возрастает.


При неконкурентном ингибировании снижается VMAX при неизменном Km.


Если продукт реакции ингибирует фермент, катализирующий его образование, такой способ ингибирования называется ретроингибированием или ингибированием по принципу обратной связи. Например, глюкоза тормозит глюкозо-6-фосфатазу, которая катализирует гидролиз глюкозо-6-фосфата.
Биологическое значение такого ингибирования – регуляция определенных метаболических путей (см. следующее занятие).
1. Изучить денатурацию белков под действием растворов минеральных и органических кислот и при нагревании.
2. Обнаружить кофермент НАД в дрожжах.
3. Определить амилазную активность в моче (сыворотке крови).
10. ХАРАКТЕР И ОБЪЕМ ВОЗМОЖНОЙ УЧЕБНО-ИССЛЕДОВАТЕЛЬСКОЙ РАБОТЫ ПО ТЕМЕ
(Указать конкретно характер и форму УИРС: подготовка реферативных выступлений, проведение самостоятельных исследований, имитационная игра, оформление истории болезни с использованием монографической литературы и др. формы)
11. ЛИТЕРАТУРА ДЛЯ ПОДГОТОВКИ К ЗАНЯТИЮ ПРЕПОДАВАТЕЛЯМ:
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
Кинетика ферментативных реакций. Кинетика изучает скорости, механизмы реакций и влияние на них таких факторов, как концентрации ферментов и субстратов, температура, рН среды, присутствие ингибиторов или активаторов.
При постоянной концентрации субстрата скорость реакции прямо пропорциональна концентрации фермента. График зависимости скорости ферментативной реакции от концентрации субстрата имеет вид равнобочной гиперболы.

Зависимость скорости ферментативной реакции от концентрации фермента (а) и субстрата (б)
Зависимость скорости ферментативной реакции от концентрации субстрата описывается уравнением Михаэлиса — Ментен:

где V — стационарная скорость биохимической реакции; Vmax — максимальная скорость; Кm — константа Михаэлиса; [S] — концентрация субстрата.
Если концентрация субстрата низкая, т. е. [S]

Тогда
Таким образом, при низких концентрациях субстрата скорость реакции прямо пропорциональна концентрации субстрата и описывается уравнением первого порядка. Это соответствует начальному прямолинейному участку кривой V = f[S] (рисунок б).
При высоких концентрациях субстрата [S] >> Кm, когда Кm можно пренебречь, уравнение Михаэлиса — Ментен приобретает вид, т.е. V=Vmax.

Таким образом, при высоких концентрациях субстрата скорость реакции становится максимальной и описывается уравнением нулевого порядка. Это соответствует участку кривой V =f [S], параллельному оси абсцисс.
При концентрациях субстрата, численно сравнимых с константой Михаэлиса, скорость реакции возрастает постепенно. Это вполне согласуется с представлениями о механизме ферментативной реакции:

где S — субстрат; Е — фермент; ES — фермент-субстратный комплекс; Р — продукт; k1 — константа скорости образования фермент-субстратного комплекса; k2 — константа скорости распада фермент-субстратного комплекса с образованием исходных реагентов; k3 — константа скорости распада фермент-субстратного комплекса с образованием продукта.
Скорость превращения субстрата с образованием продукта (Р) пропорциональна концентрации фермент-субстратного комплекса [ES]. При малых концентрациях субстрата в растворе имеется некоторое число свободных молекул фермента (Е), не связанных в комплекс (ES). Поэтому при увеличении концентрации субстрата концентрация комплексов растет, следовательно, растет и скорость образования продукта. При больших концентрациях субстрата все молекулы фермента связаны в комплекс ES (явление насыщения фермента), поэтому дальнейшее повышение концентрации субстрата практически не увеличивает концентрацию комплексов и скорость образования продукта остается постоянной.
Таким образом, становится ясен физический смысл максимальной скорости ферментативной реакции. Vmах — это скорость, с которой реагирует фермент, полностью существующий в виде фермент-субстратного комплекса.
Константа Михаэлиса численно соответствует такой концентрации субстрата, при которой стационарная скорость равна половине максимальной. Данная константа характеризует константу диссоциации фермент-субстратного комплекса:

Физический смысл константы Михаэлиса в том, что она характеризует сродство фермента к субстрату. Кm имеет малые значения, когда k1 > (k2 + k3), т.е. процесс образования комплекса ES преобладает над процессами диссоциации ES. Следовательно, чем меньше значения Кm, тем сродство фермента к субстрату больше. И, наоборот, если Кm имеет большое значение, то (k2 + k3) > k1 и процессы диссоциации ES преобладают. В этом случае сродство фермента к субстрату небольшое.
Ингибиторы и активаторы ферментов. Ингибиторами ферментов называются вещества, снижающие активность ферментов. Любые денатурирующие агенты (например, соли тяжелых металлов, кислоты) являются неспецифическими ингибиторами ферментов.
Обратимые ингибиторы — это соединения, которые нековалентно взаимодействуют с ферментом. Необратимые ингибиторы — это соединения, специфически связывающие функциональные группы активного центра и образующие ковалентные связи с ферментом.
Обратимое ингибирование разделяют на конкурентное и неконкурентное. Конкурентное ингибирование предполагает структурное сходство ингибитора и субстрата. Ингибитор занимает место в активном центре фермента, и значительное количество молекул фермента оказывается блокировано. Конкурентное ингибирование можно снять, если повысить концентрацию субстрата. В этом случае субстрат вытесняет конкурентный ингибитор из активного центра.
Обратимое ингибирование может быть неконкурентным в отношении субстрата. В этом случае ингибитор не конкурирует за место присоединения к ферменту. Субстрат и ингибитор связываются с разными центрами, поэтому появляется возможность образования комплекса IE, а также и тройного комплекса IES, который может распадаться с освобождением продукта, но с меньшей скоростью, чем комплекс ES.
По характеру своего действия ингибиторы подразделяются на:
Специфические ингибиторы оказывают свое действие на фермент, присоединяясь ковалентной связью в активном центре фермента и выключая его из сферы действия.
Неспецифическое ингибирование предполагает воздействие на фермент денатурирующих агентов (солей тяжелых металлов, мочевины и др.). В этом случае в результате разрушения четвертичной и третичной структуры белка происходит потеря биологической активности фермента.
Активаторы ферментов — это вещества, увеличивающие скорость ферментативной реакции. Чаще всего в качестве активаторов выступают ионы металлов (Fe2+, Fe3+, Cu2+, Co2+, Mn2+, Mg2+ и т.д.). Различают металлы, находящиеся в составе металлоферментов, являющиеся кофакторами, и выступающие в качестве активаторов ферментов. Кофакторы могут прочно связываться с белковой частью фермента, что же касается активаторов, то они легко отделяются от апофермента. Такие металлы являются обязательными участниками каталитического акта, определяющими активность фермента. Активаторы усиливают каталитическое действие, но их отсутствие не препятствует протеканию ферментативной реакции. Как правило, металл-кофактор взаимодействует с отрицательно заряженными группировками субстрата. Металл с переменной валентностью принимает участие в обмене электронов между субстратом и ферментом. Кроме того, они принимают участие в образовании стабильной переходной конформации фермента, что способствует более быстрому образованию ES комплекса.
Регуляция активности ферментов. Одним из основных механизмов регуляции метаболизма служит регуляция активности ферментов. Одним из примеров является аллостерическая регуляция, регуляция посредством активаторов и ингибиторов. Часто бывает так, что конечный продукт метаболического пути является ингибитором регуляторного фермента. Такой тип ингибирования называется ретроингибированием, или ингибированием по принципу отрицательной обратной связи.
Многие ферменты вырабатываются в виде неактивных предшественников-проферментов, а затем в нужный момент активируются за счет частичного протеолиза. Частичный протеолиз — отщепление части молекулы, которое приводит к изменению третичной структуры белка и формированию активного центра фермента.
Некоторые ферменты-олигомеры могут изменять свою активность за счет ассоциации - диссоциации субъединиц, входящих в их состав.
Многие ферменты могут находиться в двух формах: в виде простого белка и в виде фосфопротеида. Переход из одной формы в другую сопровождается изменением каталитической активности.
Скорость ферментативной реакции зависит от количества фермента, которое в клетке определяется соотношением скоростей его синтеза и распада. Этот способ регуляции скорости ферментативной реакции является более медленным процессом, чем регуляция активности фермента.
Читайте также:

