Интересные факты о броме кратко
Обновлено: 02.07.2024
В начале XIX в. 24-летний француз Антуан Балар открыл новый химический элемент, названный муридом. Он известил об этом Академию наук Парижа, но ему не поверили. На проверку была отправлена делегация, состоящая из 3-х человек.
Эксперты подтвердили появление нового вещества, однако настояли на другом названии. Так открытый элемент стал бромом.
Неметалл с дурным запахом
Некоторые считают, что этот элемент можно использовать в качестве успокоительного средства. Но в чистом виде бром для этой цели не годится. Используют бромид калия. Он на самом деле способен усмирить самых гневливых людей.
Широко применяется в медицине, деревообработке, текстильной промышленности и фотографии:
- при лечении некоторых сердечно-сосудистых заболеваний, язвенной болезни, эпилепсии и др.;
- пропитанная им древесина становится устойчивой к воздействию грибков и плесени;
- для создания красителя, носящего название бром индиго. С помощью него можно получить различные цвета, например, красный и синий;
- когда-то для производства фотографий использовалась фотобумага, основу которой составлял бромид серебра.
Биологическая роль
Этот важный биогенный элемент выполняет ряд функций в человеческом организме:
- участвует в кроветворении;
- балансирует процессы возбуждения и торможения в коре головного мозга;
- как оппонент йода регулирует его поступление в щитовидную железу и предохраняет организм от избытка секреции тироксина;
- участвует в производстве определенных ферментов, например, липазы, которая способствует расщеплению жиров, и амилазы, с чьей помощью перевариваются крахмалы.
В организме среднестатистического человека содержится около 200-300 мг этого вещества. Нехватка брома фиксируется крайне редко. Ее симптомы: бессонница, задержка роста, уменьшение уровня гемоглобина, сбои в работе репродуктивных органов.
Важно знать, что в природе этот элемент является очень ядовитым. Но в человеческий организм он поступает в виде безопасных соединений.
И это далеко не все, что можно рассказать об этом химическом элементе. В статье мы собрали для вас самые интересные факты о броме, какие должны понравиться как детям, так и взрослой аудитории.
Он представляет собой темную красновато-коричневую жидкость при комнатной температуре. Его свойства, в целом, аналогичны другим галогенам, таким как хлор, йод и фтор. Он является очень реактивным окислителем.
Бром – это очень плохой проводник электричества. Вызвано это тем, что он существует как ковалентное соединение двух атомов брома без свободных электронов.
Он очень реактивен. Учитывая его высокую реакционную способность, в чистом виде он очень токсичный и может вызвать химические ожоги кожи. Однако бромид-ион, присутствующий в воде, не токсичен и является микроэлементом, какой ежедневно попадает в наш организм вместе с водой и пищей.
При температуре ниже -7.2 градусов по Цельсию он становится твердым. То есть, он приобретает твердую форму, например, если вы поместите его в морозилку. В жидком состоянии он находится до температуры 58.8 градусов по Цельсию.
По своей плотности он приблизительно в 3 раза превышает плотность воды. Его плотность приблизительно такая же, как плотность твердого алюминия.
Бром и хлор – это единственные галогены, какие имеют более одного природного изотопа. Два встречающихся в природе изотопа брома существуют примерно в равных пропорциях. На долю Br-79 приходится около 51% всего брома, в то время как на долю Br-81 вся остальная часть – 49%. Именно поэтому его атомная масса находится приблизительно посередине, между 79 и 81. Эти изотопы стабильны. Все остальные изотопы брома, какие производят в лабораториях, являются радиоактивными. Они варьируются от Br-66 до Br-97 с периодом полураспада от наносекунд до нескольких часов.
Учитывая его высокую реакционную способность, практически все элементы периодической таблицы образуют с ним соединения. Есть несколько исключений для элементов, не являющихся реактивными, то есть, инертных (благородные газы). Одним из простейших его соединений является Бромоводород (HBr). Бромоводород существует в виде газа, а при растворении в воде становится сильной кислотой.
Образование связей между бромом и углеродом приводит к образованию широкого семейства соединений, известных как броморганические соединения. Это наиболее распространенные органические соединения, содержащие галогены в природе (например, фторорганические и хлорорганические соединения). К примеру, мировые океаны ежегодно выбрасывают миллион тонн бромоформа (CHBr 3) и 60 тысяч тонн бромметана (CH 3 Br).
Тирский пурпур – это краситель, какой использовали древние цивилизации. Он считался элитным красителем в древние времена. Обычно этот краситель получали из мидий и моллюсков. В 1909 году было обнаружено, что тирский пурпур содержит в себе бром.
Из всех химических элементов на нашей планете, он является 44-м по распространенности. Его меньше чем других галогенов, таких как фтор и хлор. Он существует в виде ионных солей в земной коре в количестве около 2.5 частей на 1 000 000. Так как он существует в виде солей, растворимых в воде, он имеет тенденцию встречаться в высоких концентрациях в соленых озерах и минеральных водах. По этой причине его легче всего извлечь именно из этих источников. Что касается основных производителей этого химического элемента, то ими являются США (1 место), Израиль (2 место) и Китай (3 место).
Как уже было отмечено ранее, соединения брома используются в качестве пестицидов в сельском хозяйстве. Они также используются для придания материалам органического происхождения огнеустойчивых свойств. Ранее соединения брома использовались в огнетушителя. Он также содержится в растворах для проявления фотопленки.
Этот химический элемент был открыт двумя разными химиками независимо друг от друга. Первым был немецкий химик Карл Якоб Левих. Он выделил его из минеральной воды, добываемой в местом источнике. Вторым был французский химик Антуан Жером Балар. Он знал, что в водорослях присутствуют и другие галогены, такие как йод. Зола – это соли, оставшиеся после сжигания органических веществ. Поэтому Балар использовал золу морских водорослей для создания солевого раствора, какой после перегонял, в результате чего получил новый галоген бром.
Раньше этот химический элемент использовался в медицине. Его соединения обладают седативным действием и использовались для лечения эпилепсии. Однако с развитием медицины и изучением влияния брома на организм человека стало понятно, что эти соединения очень токсичны. Поэтому в конечном итоге лекарства с его соединениями были заменены на более безопасные аналоги.
Открытие брома произошло в первой трети XIX столетия, независимо друг от друга немецкий химик Карл Якоб Лёвих в 1825 году, а француз Антуан Жером Балар – в 1826 представили миру новый химический элемент. Интересный факт – изначально Балар назвал свой элемент муридом (от латинского muria – рассол), потому что открытие своё сделал, изучая средиземноморские соляные промыслы.

Общая характеристика Брома
Нахождение брома в природе
Бром – широко распространённый химический элемент, во внешней среде встречается практически везде. Особенно много брома находится в солёной воде – морей и озёр, там он имеется в виде бромида калия, бромида натрия и бромида магния. Наибольшее количество брома образуется при испарении морской воды, есть он и в некоторых горных породах, а также в растениях.
В организме человека находятся до 300 мг брома, в основном в щитовидной железе, так же бром содержит кровь, почки и гипофиз, мышцы и костная ткань.
Физические и химические свойства брома
Бром обычно представляет собой едкую тяжёлую жидкость, имеет красно-бурый цвет и резкий, очень неприятный (зловонный) запах. Является единственным из неметаллов, при комнатной температуре находящийся в жидком состоянии.
Бром (а также – пары брома)– токсичное и ядовитое вещество, при работе с ним необходимо применять средства химической защиты, потому что при попадании на кожу и слизистые человека бром образует ожоги.
Состав природного брома – два стабильных изотопа ( 79 Br и 81 Br), молекула брома состоит из двух атомов и имеет химическую формулу Br2.
Суточная потребность организма в броме
Продукты питания богатые бромом
Наряду с имеющимся в организме, бром человек получает с пищевыми продуктами. Основными поставщиками брома являются орехи (миндаль, фундук, арахис), бобовые (фасоль, горох и чечевица), пшеница и макаронные изделия из твёрдых сортов пшеницы, ячневая крупа, молочные продукты, водоросли и практически все виды морской рыбы.

Опасность и вред брома
Элементарный бром – сильнодействующий яд, принимать внутрь его категорически запрещено. Пары брома могут вызвать отёк лёгких, особенно у тех, кто склонен к аллергическим реакциям или имеет заболевания лёгких и дыхательных путей (очень опасны пары брома для астматиков).
Не рекомендуется применять препараты брома людям, в силу специфики работы нуждающимся в стабильной концентрации внимания (водителям, альпинистам, монтажникам-высотникам).
Признаки избытка брома
Переизбыток данного вещества обычно бывает при передозировке препаратов брома, для людей категорически нежелательна, потому что может представлять реальную опасность для здоровья. Основные признаки избытка брома в организме – воспаления и высыпания на коже, сбои в работе пищеварительной системы, общая вялость и подавленность, постоянные бронхиты и риниты, не связанные с простудами и вирусами.
Признаки нехватки брома
Нехватка в организме брома проявляется бессонницей, замедлением роста у детей и подростков, понижением уровня гемоглобина в крови, но, не всегда эти симптому связывают именно с недостаточным количеством брома, поэтому для подтверждения подозрений, нужно посетить доктора и сдать необходимые анализы. Часто из-за нехватки брома повышается риск самопроизвольного прерывания беременности (выкидыш на разных сроках, вплоть до третьего триместра).
Полезные свойства брома и его влияние на организм
Бром (в виде бромидов) применяется при различных заболеваниях, основное его действие – седативное, поэтому препараты брома часто назначаются при нервных расстройствах и нарушениях сна. Соли брома являются эффективным средством для лечения заболеваний, вызывающих судороги (особенно эпилепсии), а также нарушений деятельности сердечно-сосудистой системы и некоторых желудочно-кишечных недугов (язвы желудка и двенадцатиперстной кишки).
Усвояемость брома
Усвояемость брома замедляют хлор, алюминий, йод и фтор, поэтому принимать препараты, содержащие соли брома нужно только после консультации с врачом.
Бром и его влияние на мужскую потенцию
Вопреки ничем не подтверждённым слухам (больше похожим на анекдоты), бром не оказывает угнетающего воздействия на половое влечение и потенцию мужчин. Якобы бром в виде белого порошка добавляют в еду молодым бойцам в армии, а также пациентам мужского пола в псих-диспансерах и заключённым в тюрьмах и колониях. Этому нет ни одного научного подтверждения, а слухи можно объяснить способностью брома (его препаратов) оказывать успокаивающее воздействие.
По некоторым источникам, бром способствует активизации половой функции у мужчин и увеличению как объёма эякулянта, так и количества сперматозоидов, в нём содержащихся.

Применение брома в жизни
Бром применяется не только в медицине (бромид калия и бромид натрия), но и в других областях, например в фотографии, нефтедобыче, в производстве моторного топлива. Бром используется при изготовлении боевых отравляющих веществ, что ещё раз подчёркивает необходимость осторожного обращения с данным элементом.
Б Бром является химическим элементом таблицы Менделеева с атомным номером 35 и условным обозначением Br. Бром при комнатной температуре предствляет собой дымящуюся красно-коричневую жидкость, которая легко испаряется.
Как был открыт Бром

Открытие такого химического элемента как бром было совершено почти одновременно и независимо друг от друга двумя учеными.
Первым является немецкий химик Карл Якоб Левиг. Ему удалось выделить новый элемент из источника минеральных вод в немецком городке Бад-Кройцнах в 1825 году. Для справки этот город является Родиной Левига. Используя раствор минеральной соли насыщенной хлором, Карл Левиг эстрагировал бром диэтиловым эфиром. После испарения эфира на дне оставалась коричневая жидкость. С этой жидкостью в качестве доказательства своего эксперимента, он просился на работу в лабораторию Леопольда Гмелина в Гейдельберге. В результате, публикация этого опыта была отложена и французский химик Антуан Балар опубликовал свою статью раньше.
Статья французского химика была опубликована только в 1826 году. Балар нашел новый химический элемент в золе морских водорослей из солончаков в Монпелье. Морские водоросли в то время использовались для получения йода и содержали в своем составе бром. Он выделил новый элемент из раствора золы водорслей, насыщенных хлором. Свойства этого элемента были похожи на свойства йода и хлора. Балар, проводя свои опыты пытался доказать, что найденое вещество является монохлоридом йода. Когда у него не получилось это доказать он решил зарегистрировать его как новый элемент и назвал его мюрид.
Где и как добывают Бром
На сегодняшний день, мировое производство брома оценивается в 600 000 тонн в год. Лидерами по производству этого элемента являются США, Китай, Израиль и Иордания. В промышленных масштабах исходным материалом для добычи брома является либо раствор солей, либо вода из подземных источников большой глубины. Само получение элементарного брома в промышленных масштабах осуществляется путем окисления растворов бромида хлором. Химическая реакция этого процесса выглядит следующим образом.
При окислении бромида калия при повышенных температурах образуется чистый бром и хлорид калия. Еще одним возможным способом получения брома является его добыча как побочного продукта при переработке калия для изготовления удобрений. С 1970-х годов этот метод перестал быть коммерчески выгодным и от него отказались.
В лабораториях бром получают с помощью химической реакции бромида натрия с серной кислотой и диоксидом марганца. На выходе реакции из бромида натрия получается сульфат марганца, оксид брома, сульфат натрия и вода. После этого из раствора методом перегонки выделяют бром.
Распространенность Брома

Применение Брома

Соединения брома находят широкое применение в разных сферах промышленности. Некоторые соединения изготавливаются из самого брома, другие же изготавливаются из бромистого водорода. Бромистый водород в свою очередь представляет собой двухатомное соединение водорода и брома.
Большую часть коммерческого использования брома приходится на бромированные антипирены. Последние в свою очередь используются в противопожарных средствах защиты. Примером этого могут послужить некоторые огнетушители, а так же противопожарные средства обработки древесины. Так же бромированные антипирены используются в качстве примеси при изготовлении полимеров, различного рода пластмасс, полиэтилена и полипропилена. Еще одним известным применением бромированных антипиренов является изготовление термияески устойчивых эпоксидных смол для печатных плат в электротехнике.
Еще одним значимым применением является использование бромида серебра в качестве светочувствительного компонента фотографических эмульсий. Другим важным применением являлся этиленбромид, который использовался в качестве пиисадки к бензину. Эта присадка помогала избавить бензиновые двигатели от эффекта детонации. В 80-х годах от этой присадки отказались из-за токсичности и разрушения озонового слоя.
До 2005 года бромметан, который явлляется токсичным везеством, широко использовался в качестве пестицидов для фумигации почвы. Он был запрещен по той же причине, что и присадка для бензиновых двигателей. Еще одним значимым применением являлась фармакология, где бромид калия довольно часто использовался в качестве седативного вещества. Другие сферы применения брома составляют буровые растворы высокой плотности, красители и фармацевтические препараты.
Интересные факты

Интересных фактов связанных с бромом достаточно много. Стоит начать с того, что в 2014 году было проведено исследование, которое показало, что бром является необходимым кофактором в биосинтезе коллагена IV, что делает этот элемент необходимым для архитектуры базальной мембраны и развития тканей у животных. Другим интересным предположением является то, что ионы брома могут способствовать различного рода мутациям в ДНК живых организмов. Дибром и ртуть являются единственными веществами, которые при комнатной температуре находятся в жидком состоянии. Еще одним интересным моментом является то, что бром в простом состоянии способен вызывать химические ожоги. Вдыхание его паров способно вызывать одышку, пневмонию и отек легких.
В 1826 году химик из Франции Антуан Жером Балар открыл новый химический элемент бром (Br). Это случилось при изучении рассолов соляных промыслов Средиземноморья. Жидкость обладала крайне неприятным запахом, за что и получила своё название, происходящее от греческого слова bromos — зловоние. Открытие сделало преподавателя колледжа всемирно известным, а вещество было внесено в периодическую таблицу Менделеева.
- Определение и физическая характеристика
- Химическое строение и свойства
- Нахождение в природе
- Промышленное получение
- Применение вещества
- Бром в организме
- Опасность и вред
- Признаки избытка и нехватки

Определение и физическая характеристика
Бром, обозначаемый символом Вг, является галогеном и входит в VII группу периодической таблицы химических элементов. Вещество имеет атомный номер 35, а его атомная масса составляет 79,904 дальтонов. Молярная масса составляет 79,904 г/моль. Относительная молекулярная масса молекулы равна 159,808, а её молярная масса — 160 г/моль. Бром, встречающийся в природе, состоит из двух нуклидов с массовыми числами 79 и 81.
Существует множество искусственных радиоактивных изотопов. Среди них самым интересным считается 80Вr, поскольку на его примере советский физик И. В. Курчатов открыл изомерию атомных ядер.

Вещество представляет собой жидкость красно-бурого оттенка, отличающуюся сильным неприятным запахом. Температура застывания брома составляет -7,2°С. Замёрзший элемент имеет форму красно-коричневых игольчатых кристаллов, блестящих как металл. Кипит элемент при температуре 58,78 °С, превращаясь в пар жёлто-бурого цвета. Плотность вещества в жидком виде — 3,1 г/см3.
Бром плохо растворяется в воде. Так, если её температура не превышает 5,84 °С, то вещество образует тёмно-красные кристаллы. Лучше всего для его растворения подходят органические составы. Извлекать элемент из различных водных соединений позволяет именно это физическое свойство.
Бром в любом физическом виде состоит из двухатомных молекул. Распад на атомы становится хорошо заметен при температуре 800 °C. Но также его можно наблюдать при действии света.
Химическое строение и свойства
Внешние электроны атома имеют конфигурацию 4s24p5. Необходимо отметить, что такое химическое свойство брома, как степень окисления, разнится в зависимости от соединения, к примеру, у гипобромитов этот показатель равен +1, а у броматов он составляет +5.
В соединениях валентность брома переменна. Атом вещества имеет заряд только тогда, когда является ионом, заряд ядра атома составляет 35. Представить электронную формулу брома можно следующим образом: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5. Структурная же формула имеет вид: Br-Br.
Неметалл является химически активным, а потому по способности к реакции располагается между хлором и йодом. Сильное разогревание, иногда сопровождающееся горением, возникает, когда вещество взаимодействует со следующими реагентами:
Так же протекает реакция вещества с некоторыми металлами, к примеру, калием и алюминием. Но большинство металлических элементов плохо реагирует с безводным бромом, потому что на их поверхности образуется защитная плёнка бромида, который не растворяется в этом реагенте.
Самыми устойчивыми к такой реакции, даже при высокой температуре и наличии воды, считаются следующие металлы:

У золота с бромом взаимодействие проходит довольно активно. Кислород, азот и углерод не создают с элементом прямых соединений даже при повышенной температуре. Чтобы эти вещества соединились, химики применяют различные косвенные методы. К примеру, очень непрочный оксид Вr3О8 получают посредством воздействия озона на бром при 80 °C. Реагировать непосредственно с элементом способны галогены, в результате их взаимодействия образуются BrF3, BrCl и другие соединения.
Бром относится к сильным окислителям. Элемент способен вытеснить из химических соединений йод. Само же вещество подвергается вытеснению хлором и фтором.
Выделить чистый неметалл из бромидов на основе воды можно посредством использования сильных окислителей, поместив все реагенты в кислую среду. Растворяясь в воде, вещество вступает с нею в слабую реакцию, результатом которой становится образование бромистоводородной и бромноватистой кислот. Водный раствор элемента называется бромной водой.
Неметалл растворяется в щелочах:
- При низких температурах соединение брома и гидроксидов даёт бромиды и гипобромиты.
- При температуре около 100 °C получаются бромиды и броматы.
Взаимодействие брома и органических соединений чаще всего проходит с характерным присоединением углерода по двойной связи и замещением водорода. Обычно это происходит при воздействии различных катализаторов или света. Ещё одной распространённой химической реакций является бромирование, суть которого заключается во введении атома реагента в соединение посредством химической реакции вещества с ненасыщенной молекулой или замещения водорода.
Нахождение в природе

Основная часть природного брома рассеяна в земной коре. Больше всего вещества содержится в породах, сформированных магмой. Этот элемент можно обнаружить рядом с хлором. Так, соли элемента встречаются в солевых хлорных отложениях, в морской воде, насыщенном растворе соляных озёр и рассолах, находящихся под землёй, которые зачастую связаны с месторождениями соли и нефти. Так как вещество хорошо растворяется в воде, его соли скапливаются в рассолах, оставшихся на месте озёр и заливов.
Неметалл перемещается в форме хорошо растворимых соединений, а потому его довольно сложно встретить в твёрдой минеральной форме. Минералами становятся бромирит AgBr, эмболит Ag (Cl, Вг) и йодэмболит Ag (Cl, Вr, I), которые образуются в зонах окисления сульфидных месторождений серебра, сформировавшихся в областях пустынь и полупустынь.
Промышленное получение
В промышленности для получения брома используют морскую воду, озёрные и подземные рассолы, а также калийные щёлоки. Для выделения вещества применяют хлор. Процедура состоит из следующих этапов:

- В гранитные, керамические или другие устойчивые к бромовому воздействию колонны сверху подают подогретое сырьё.
- Снизу в них направляют хлор и водяной пар или воздух.
- После выхода из устройства бромовые пары оседают в виде жидкости в специальных холодильных установках.
- Полученное вещество отделяют от воды.
- Посредством дистилляции его очищают от хлора.
- Из смеси реактива и воздуха бром выделяют с помощью химических поглотителей. В таких установках может использоваться газообразный сернистый ангидрид. Он реагирует с реактивом при наличии водяного пара, образуя бромистоводородную и серную кислоты.
- Для получения чистого вещества полупродукты подвергают воздействию хлора или кислоты.
- При необходимости проводится их переработка на бромистые соединения без выделения искомого элемента.
Метод с применением воздуха позволяет получать бром из рассолов даже с небольшим количеством вещества. Применять к таким смесям паровой способ экономически невыгодно, поскольку на выделение малого количества реагента тратится значительное количество пара.
Применение вещества
Прежде всего, вещество является основой для создания бромистых солей и различных производных на основе органики. Но и сам реактив, и его соединения довольно широко используются во многих областях жизнедеятельности человека:

- Органические бромиды — синтезирование красителей и лекарств.
- Бромиды щелочных металлов — успокоительные препараты, используемые для лечения неврозов, повышенной раздражительности, гипертонии, эпилепсии.
- Бромид серебра — фотография.
- Бром — изготовление бромистого этила и дибромэтана, участвующих в производстве этиловой жидкости, которую добавляют к бензинам, чтобы снизить их способность к детонации.
- Бромистый метил — инсектициды.
- Органические соединения вещества — производство эффективных огнетушителей.
- Бромная вода — химические анализы, позволяющие определять многие вещества.
Бром в организме
Вещество содержится в тканях всех животных и растений. Его обнаружили практически во всех жидкостях тела. Если человек здоров, то в его организме уровень брома составляет от 0,11 до 2,00 мг/%. Для поддержания этого показателя в сутки необходимо получать не больше 0,8−1 г реактива.
Радиоактивный бром позволил выявить, что вещество поглощается щитовидной железой, почками и мозгом. Бромиды, которые были введены в животные организмы, увеличили концентрацию процессов торможения, проходящих в головном мозге. Они способствовали приведению в норму нервной системы, которая пострадала от чрезмерного напряжения, возникшего в результате подобного процесса.

Но следует учитывать, что химический элемент задерживается в щитовидной железе, вступая в конкуренцию с йодом. Это влияет на работу органа, что отражается на обмене веществ.
Бром плохо усваивается, если в реакции будут участвовать хлор, алюминий, йод и фтор. Чтобы избежать такой ситуации, перед началом лечения препаратами, содержащими бромные соли, необходимо проконсультироваться с врачом.
Опасность и вред
Элементарный бром представляет собой сильнодействующий яд, отнесённый ко второму классу опасности. Его ни в коем случае нельзя принимать внутрь.
Очень опасны пары вещества:
- При концентрации 1 мг/м3 и более газ вызывает кашель, насморк, кровотечение из носа, головокружение и головную боль.
- При концентрациях, превышающих указанный порог, у человека может начаться отёк лёгких, удушье, бронхит, в некоторых случаях возможен смертельный исход.
- Максимальное допустимое значение — 2 мг/м3.
Во избежание отравления все работы с реагентом необходимо осуществлять в специальных шкафах, оборудованных хорошей вытяжной системой. Если же защититься от паров не удалось, то следует подышать сильно разбавленным водным раствором аммиака, возможно применение раствора на этиловом спирте. Для устранения боли в горле, возникшей из-за воздействия отравляющего газа, нужно выпить хорошо нагретое молоко.

В жидком виде попавшее на кожу вещество вызывает ожоги, которые плохо заживают. В случае поражения кожи реагент необходимо тщательно смыть большим количеством воды или сдуть мощной воздушной струёй. Место ожога следует смазать ланолином.
Представителям профессий, требующих постоянной концентрации внимания, к примеру, водителям и альпинистам, применять лекарства на основе брома не рекомендуется. Это обусловлено свойством вещества снимать возбуждённое состояние нервной системы, расслаблять её.
Признаки избытка и нехватки
Чаще всего переизбыток вещества в организме возникает при неправильном употреблении бромосодержащих препаратов. Это состояние может привести к серьёзным проблемам со здоровьем. Признаки избытка микроэлемента:
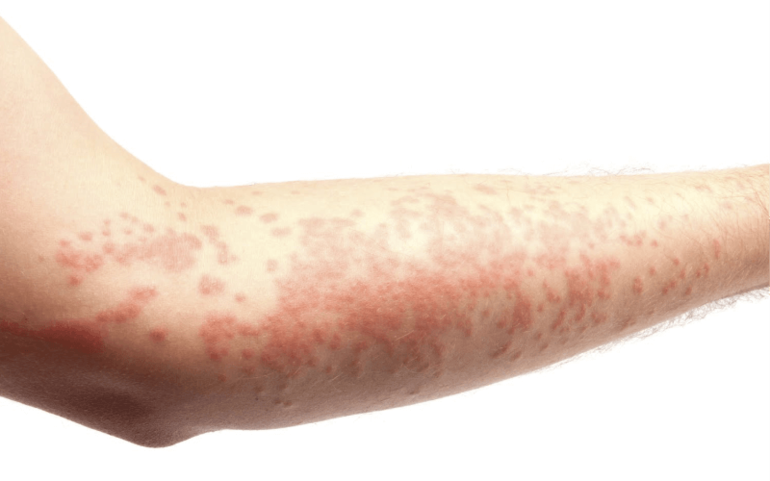
- Кожные воспаления и высыпания.
- Нарушения в работе пищеварительной системы.
- Ощущение усталости, вялости и подавленности.
- Частые бронхиты и риниты при отсутствии простудных и вирусных заболеваний.
Нехватка брома не менее серьёзная проблема. Из-за отсутствия в организме необходимого количества вещества у беременных женщин повышается вероятность выкидыша на разных сроках.
Проявляться недостаток микроэлемента может в виде таких симптомов:
- бессонница;
- замедление роста у детей;
- понижение уровня гемоглобина.
Эти проблемы редко ассоциируются именно с нехваткой брома, но всё же лучше обратиться к врачу и сдать необходимые анализы. Такая мера позволит установить причину недомогания и исключить возможность развития более серьёзных заболеваний.
Бром является важным химическим элементом. Он необходим для нормальной жизнедеятельности растений и животных. Недостаток этого неметалла, как и его избыток, может привести к развитию заболеваний. Кроме того, вещество активно применяется в различных сферах деятельности человека. На его основе создаются лекарственные препараты, химические реагенты и инсектициды.
Читайте также:

