Гидрирование это в химии кратко
Обновлено: 14.05.2024
Гидрированием (гидрогенизацией)называется процесс непосредственного присоединения водорода к различным веществам. Реакция гидрирования в общем виде может быть представлена уравнением:
Реакции гидрирования протекают с уменьшением объема, поэтому их проводят при повышенном давлении (от 0,5 до 40 МПа). Для увеличения выхода конечного продукта процесс проводят в избытке водорода.
Все процессы гидрирования являются каталитическими. В качестве катализаторов используют металлы (Fe, Ca, Ni), а также оксиды и сульфиды металлов. Активность катализаторов повышается при нагреве, поэтому, несмотря на экзотермичность процессов, реакции ведут при повышенных температурах (от 100 до 400 0 С) в зависимости от активности катализатора и реакционной способности реагентов.
Процессы гидрирования широко используются в промышленности для получения растворителей, синтетических смол, поверхностно-активных веществ, моторных топлив, технических смазок и т.п.
При этом в качестве исходного сырья применяются ароматические углеводороды, альдегиды, кетоны, нитросоединения, синтетические жирные кислоты и др.
1) Из бензола гидрированием получают циклогексан:
Из циклогексана впоследствии получают циклогексанон С6Н10О, являющийся широко применяемым растворителем.
2) Из ацетилена гидрированием получают этилен:
3) Гидрогенизацией окиси углерода получают спирты:
СО + Н2 = НСОН (метанол)
4) Гидрогенизацией угля получают бензин, дизельное топливо, фенолы, смазочные масла.
Для каждого процесса гидрирования устанавливают оптимальное время контакта реагирующих веществ с катализатором, обеспечивающее высокий выход целевого продукта. Для разных процессов время контакта изменяется от долей минуты до нескольких часов.
Для проведения процессов гидрирования используются в основном реакторы трубчатого и колонного типа с неподвижным слоем катализатора. Катализатор размещается в специальной катализаторной коробке.
В зависимости от температуры и давления процессы гидрирования могут проводиться в жидкой или парогазовой фазах. Жидкофазное гидрированиеприменяется для веществ с высокой температурой кипения (жиры, карбоновые кислоты). Газофазное гидрирование применяется для веществ с низкой температурой кипения. Гидрирование в парогазовой фазе проводят путем пропускания смеси водорода с парами исходного вещества через неподвижный катализатор.
В соответствие со схемой исходное сырье изначально подогревается и испаряется в испарителе 2. Полученные пары смешиваются с водородом в аппарате 3 и направляются в реактор гидрирования (трубчатого или колонного типа). Образующиеся продукты гидрирования и избыток водорода подают в конденсатор 5 для разделения. Продукты реакции конденсируются и переходят в жидкую фазу, а водород отделяется и подается в линию циркуляции для повторного смешивания с сырьем. В случае избытка водорода его частично подают в факельную систему для сжигания. В аппарате 6 из жидкой фазы отделяют побочные вещества и получают необходимые продукты гидрирования. Как видно из схемы и описания, процесс гидрирования является непрерывным.
Пожарная опасность процессов гидрирования характеризуется следующими факторами:
1. Наличием большого количества горючих веществ. Во всех процессах гидрирования обращается водород. При проведении процессов гидрирования обращается большое количество легковоспламеняющихся и горючих жидкостей, которые используются в качестве сырья и получаются в качестве продуктов гидрирования. Для подогрева исходного сырья используют высокотемпературные органические теплоносители, являющиеся также горючими веществами.
2. Возможностью образования горючей среды внутри реакторов, в испарителях, смесителях и других аппаратах в периоды пуска и остановки. При нормальном (установившемся) режиме горючая среда внутри аппаратов не образуется, поскольку их объем полностью заполнен горючими веществами и доступ окислителя исключен.
3. Возможностью выхода водорода, горючих жидкостей и их паров в объем помещения при появлении неплотностей и повреждений технологического оборудования. При этом если вещества нагреты до высоких температур, то при смешивании с воздухом, возможно, их самовоспламенение.

Наиболее часто повреждения технологического оборудования установок гидрирования происходят из-за образования повышенных давлений, температурных напряжений и протекания процессов коррозии.
Характерными причинами повышения давления являются:
а) Нарушение температурного режима. Для поддержания температурного режима в нормальных пределах необходимо:
─ предусматривать системы автоматического контроля и регулирования температуры в испарителях и реакторах;
─ устраивать системы автоматического регулирования состава парогазовой смеси;
─ устанавливать приборы контроля за температурой и расходом теплоносителей и хладоагентов;
─ обеспечивать систематическую очистку теплообменных поверхностей от отложений, ухудшающих теплоотвод;
─ применять системы световой и звуковой сигнализации о повышении до опасных значений температуры исходных продуктов и реакционной смеси.
б) Увеличение сопротивления насадки катализатора.
в) Попадание жидкого неиспарившегося продукта в реакторы газофазного гидрирования.
Для защиты от повышения давления реакторы необходимо оборудовать предохранительными избыточными клапанами.
Температурные напряжения в металле могут возникать в реакторах трубчатого типа при значительном перепаде температур между трубками и кожухом, а также между реакционной средой и хладоагентом. Для предупреждения повреждений необходимо такие реакторы оборудовать температурными компенсаторами.
Специфичной причиной повреждения реакторов гидрирования является водородная коррозия, а также сероводородная коррозия(за счет наличия примесей сероводорода и других сернистых соединений). Коррозию стенок аппаратов могут также вызывать гидрируемые вещества, например, карбоновые кислоты. Для предотвращения повреждений, вызванных коррозией, необходимо использовать для изготовления реакторов коррозионностойкие материалы (высоколегированные стали, свинец) или изолировать металл от агрессивной среды защитными покрытиями (эмалью, лаками, графитовыми плитками, метлахской плиткой).
Для контроля за состоянием воздушной среды в помещениях реакторного цеха необходимо устанавливать газоанализаторы, сблокированные с приводом аварийной вентиляции, аварийным сбросом газа в факельную систему, перекрытием аварийных задвижек и пуском негорючего газа в реакторы.
4. Возможностью возникновения потенциально-пожароопасных тепловых источников. Специфическими для процессов гидрирования источниками зажигания являются:
─ теплота химической реакции;
─ искровые разряды статического электричества. Заряды статического электричества накапливаются при движении продуктов в трубах, аппаратах и при выходе парогазовой смеси под большим давлением наружу через малые отверстия.
─ теплота самовозгорания сульфидов железа. Сульфиды железа, образующиеся на стенках реакторов, самовозгораются при доступе воздуха (например, при замене катализатора). Для предупреждения этого замену катализатора следует производить под защитой азота.
─ тепловые проявления (искры, дуги, перегрев и т.п.), возникающие при аварийных режимах работы силового, осветительного электрооборудования, сетей автоматического контроля, а также при несоответствии эксплуатируемого электрооборудования требованиям Правил устройства электроустановок.
─ искры и открытое пламя при проведении огневых работ.
─ искры механического происхождения при ремонте или производстве очистных работ.
5. Возможностью быстрого распространения пожара. Применительно к процессам гидрирования можно отметить, что распространение пожара может произойти при обратном проскоке пламени из факельной системы внутрь основных аппаратов. Для того, чтобы этого избежать, необходимо коммуникации факельной системы оборудовать огнепреградителями.
Аварии в реакторах гидрирования и соединенных с ними трубопроводах обычно сопровождаются выходом в помещение большого количества водорода и быстрым нарастанием его концентрации до взрывоопасных пределов. Поэтому цеха гидрирования относят к категориям А по взрывопожарной и пожарной опасности и оборудуют автоматическими установками пожаротушения.
Гидрированием (гидрогенизацией)называется процесс непосредственного присоединения водорода к различным веществам. Реакция гидрирования в общем виде может быть представлена уравнением:
Реакции гидрирования протекают с уменьшением объема, поэтому их проводят при повышенном давлении (от 0,5 до 40 МПа). Для увеличения выхода конечного продукта процесс проводят в избытке водорода.
Все процессы гидрирования являются каталитическими. В качестве катализаторов используют металлы (Fe, Ca, Ni), а также оксиды и сульфиды металлов. Активность катализаторов повышается при нагреве, поэтому, несмотря на экзотермичность процессов, реакции ведут при повышенных температурах (от 100 до 400 0 С) в зависимости от активности катализатора и реакционной способности реагентов.
Процессы гидрирования широко используются в промышленности для получения растворителей, синтетических смол, поверхностно-активных веществ, моторных топлив, технических смазок и т.п.
При этом в качестве исходного сырья применяются ароматические углеводороды, альдегиды, кетоны, нитросоединения, синтетические жирные кислоты и др.
1) Из бензола гидрированием получают циклогексан:
Из циклогексана впоследствии получают циклогексанон С6Н10О, являющийся широко применяемым растворителем.
2) Из ацетилена гидрированием получают этилен:
3) Гидрогенизацией окиси углерода получают спирты:
СО + Н2 = НСОН (метанол)
4) Гидрогенизацией угля получают бензин, дизельное топливо, фенолы, смазочные масла.
Для каждого процесса гидрирования устанавливают оптимальное время контакта реагирующих веществ с катализатором, обеспечивающее высокий выход целевого продукта. Для разных процессов время контакта изменяется от долей минуты до нескольких часов.
Для проведения процессов гидрирования используются в основном реакторы трубчатого и колонного типа с неподвижным слоем катализатора. Катализатор размещается в специальной катализаторной коробке.
В зависимости от температуры и давления процессы гидрирования могут проводиться в жидкой или парогазовой фазах. Жидкофазное гидрированиеприменяется для веществ с высокой температурой кипения (жиры, карбоновые кислоты). Газофазное гидрирование применяется для веществ с низкой температурой кипения. Гидрирование в парогазовой фазе проводят путем пропускания смеси водорода с парами исходного вещества через неподвижный катализатор.
В соответствие со схемой исходное сырье изначально подогревается и испаряется в испарителе 2. Полученные пары смешиваются с водородом в аппарате 3 и направляются в реактор гидрирования (трубчатого или колонного типа). Образующиеся продукты гидрирования и избыток водорода подают в конденсатор 5 для разделения. Продукты реакции конденсируются и переходят в жидкую фазу, а водород отделяется и подается в линию циркуляции для повторного смешивания с сырьем. В случае избытка водорода его частично подают в факельную систему для сжигания. В аппарате 6 из жидкой фазы отделяют побочные вещества и получают необходимые продукты гидрирования. Как видно из схемы и описания, процесс гидрирования является непрерывным.
Пожарная опасность процессов гидрирования характеризуется следующими факторами:
1. Наличием большого количества горючих веществ. Во всех процессах гидрирования обращается водород. При проведении процессов гидрирования обращается большое количество легковоспламеняющихся и горючих жидкостей, которые используются в качестве сырья и получаются в качестве продуктов гидрирования. Для подогрева исходного сырья используют высокотемпературные органические теплоносители, являющиеся также горючими веществами.
2. Возможностью образования горючей среды внутри реакторов, в испарителях, смесителях и других аппаратах в периоды пуска и остановки. При нормальном (установившемся) режиме горючая среда внутри аппаратов не образуется, поскольку их объем полностью заполнен горючими веществами и доступ окислителя исключен.
3. Возможностью выхода водорода, горючих жидкостей и их паров в объем помещения при появлении неплотностей и повреждений технологического оборудования. При этом если вещества нагреты до высоких температур, то при смешивании с воздухом, возможно, их самовоспламенение.
Наиболее часто повреждения технологического оборудования установок гидрирования происходят из-за образования повышенных давлений, температурных напряжений и протекания процессов коррозии.
Характерными причинами повышения давления являются:
а) Нарушение температурного режима. Для поддержания температурного режима в нормальных пределах необходимо:
─ предусматривать системы автоматического контроля и регулирования температуры в испарителях и реакторах;
─ устраивать системы автоматического регулирования состава парогазовой смеси;
─ устанавливать приборы контроля за температурой и расходом теплоносителей и хладоагентов;
─ обеспечивать систематическую очистку теплообменных поверхностей от отложений, ухудшающих теплоотвод;
─ применять системы световой и звуковой сигнализации о повышении до опасных значений температуры исходных продуктов и реакционной смеси.
б) Увеличение сопротивления насадки катализатора.
в) Попадание жидкого неиспарившегося продукта в реакторы газофазного гидрирования.
Для защиты от повышения давления реакторы необходимо оборудовать предохранительными избыточными клапанами.
Температурные напряжения в металле могут возникать в реакторах трубчатого типа при значительном перепаде температур между трубками и кожухом, а также между реакционной средой и хладоагентом. Для предупреждения повреждений необходимо такие реакторы оборудовать температурными компенсаторами.
Специфичной причиной повреждения реакторов гидрирования является водородная коррозия, а также сероводородная коррозия(за счет наличия примесей сероводорода и других сернистых соединений). Коррозию стенок аппаратов могут также вызывать гидрируемые вещества, например, карбоновые кислоты. Для предотвращения повреждений, вызванных коррозией, необходимо использовать для изготовления реакторов коррозионностойкие материалы (высоколегированные стали, свинец) или изолировать металл от агрессивной среды защитными покрытиями (эмалью, лаками, графитовыми плитками, метлахской плиткой).
Для контроля за состоянием воздушной среды в помещениях реакторного цеха необходимо устанавливать газоанализаторы, сблокированные с приводом аварийной вентиляции, аварийным сбросом газа в факельную систему, перекрытием аварийных задвижек и пуском негорючего газа в реакторы.
4. Возможностью возникновения потенциально-пожароопасных тепловых источников. Специфическими для процессов гидрирования источниками зажигания являются:
─ теплота химической реакции;
─ искровые разряды статического электричества. Заряды статического электричества накапливаются при движении продуктов в трубах, аппаратах и при выходе парогазовой смеси под большим давлением наружу через малые отверстия.
─ теплота самовозгорания сульфидов железа. Сульфиды железа, образующиеся на стенках реакторов, самовозгораются при доступе воздуха (например, при замене катализатора). Для предупреждения этого замену катализатора следует производить под защитой азота.
─ тепловые проявления (искры, дуги, перегрев и т.п.), возникающие при аварийных режимах работы силового, осветительного электрооборудования, сетей автоматического контроля, а также при несоответствии эксплуатируемого электрооборудования требованиям Правил устройства электроустановок.
─ искры и открытое пламя при проведении огневых работ.
─ искры механического происхождения при ремонте или производстве очистных работ.
5. Возможностью быстрого распространения пожара. Применительно к процессам гидрирования можно отметить, что распространение пожара может произойти при обратном проскоке пламени из факельной системы внутрь основных аппаратов. Для того, чтобы этого избежать, необходимо коммуникации факельной системы оборудовать огнепреградителями.
Аварии в реакторах гидрирования и соединенных с ними трубопроводах обычно сопровождаются выходом в помещение большого количества водорода и быстрым нарастанием его концентрации до взрывоопасных пределов. Поэтому цеха гидрирования относят к категориям А по взрывопожарной и пожарной опасности и оборудуют автоматическими установками пожаротушения.
ГИДРИ́РОВАНИЕ (гидрогенизация), реакции присоединения водорода по кратным связям молекул органич. соединений, напр.: CH3 C H═CH2 + H2 → CH3 CH 2–CH3 . Наиболее распространено гетерогенное Г. при темп-ре 20–200 °C, давлении H2 1–70 МПа, использовании в качестве катализаторов металлов (Fe, Ni, Со, Pt, Pd, Os), оксидов (NiO, CoO, Cr2O3, MoO2) или сульфидов (WS2, MoS2) металлов и др. Достаточно легко происходит Г. алкинов, алкенов, нитросоединений, труднее – ароматич. углеводородов, альдегидов, кетонов, карбоновых кислот и их производных. В пром-сти осуществляют Г. растит. масел (см. Гидрогенизация жиров ), нефтяных фракций (см. Гидрогенизация нефтепродуктов ). Г. (напр., фенола, бензола, динитрила адипиновой кислоты) применяют для получения промежуточных продуктов.
ГИДРИРОВАНИЕ
ГИДРИРОВАНИЕ (гидрогенизация), присоединение Н2 к орг. соединениям (обратная р-ция наз. дегидрированием). Гидрирование и дегидрирование связаны подвижным равновесием, положение к-рого определяется темп-рой и давлением Н2. Гидрирование обычно происходит при сравнительно низких т-рах (20-200 °С), дегидрирование-при более высоких. Повышение давления благоприятствует гидрированию.
Обычно гидрирование осуществляют в условиях гетерог. или гомог. катализа. В пром-сти Наиб. распространено гетерогенное гидрирование молекулярным водородом. При этом Н2, активированный катализатором, ступенчато присоединяется к субстрату; стадией, лимитирующей скорость гидрирования, обычно является перенос водорода на субстрат. Катализаторы-хим. элементы с недостроенными d-оболочками, чаще всего металлы VIII гр. периодической системы, оксиды и сульфиды металлов, а также многокомпонентные катализаторы.
При гетерог. гидрировании увеличение числа и объема заместителей при кратной связи приводит к затруднению координации соед. с пов-стью катализатора и доступа к нему Н2. Скорость гидрирования часто определяется природой гидрируемой связи. Достаточно легко гидрируются ацетилены, олефины, нитросоединения, труднее-ароматич. углеводороды, альдегиды, кетоны, карбоновые к-ты и их производные (см. табл.). Недостаток процесса-невысокая селективность вследствие протекания побочных р-ций крекинга, гидрогенолиза и т.п.
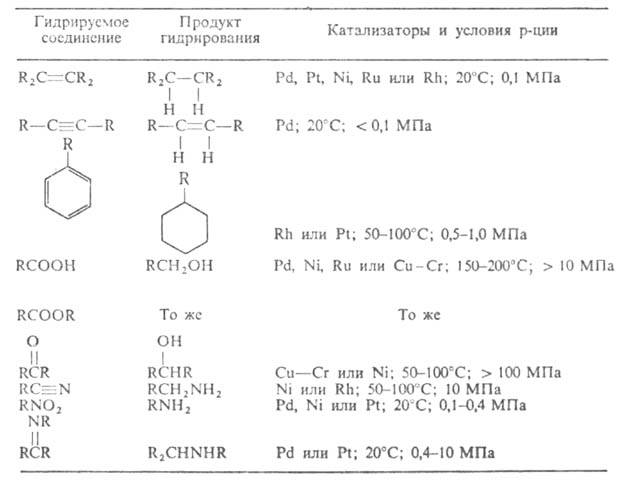
УСЛОВИЯ КАТАЛИТИЧЕСКОГО ГИДРИРОВАНИЯ РАЗЛИЧНЫХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Каталитич. гетерог. гидрирование-один из важнейших процессов хим. пром-сти. См., напр., Гидроочистка, Гидрокрекинг, Гидрогенизация жиров и др.
При гомогенном гидрировании активация водорода и субстрата происходит путем их включения в координац. сферу каталитич. комплекса. При этом идет гетеролитич. или гомолитич. диссоциация водорода, что и создает условия для гидрирования. Связь субстрата с атомом металла катализатора должна быть достаточно лабильной. Алкены, образующие слишком прочные связи, не гидрируются в этих условиях. В кач-ве катализаторов используют соед. переходных металлов: соли, карбонилы, фосфиновые комплексы, двухкомпонентные системы, получаемые взаимод. солей с восстановителями или комплексообразователями (напр., катализаторы Циглера-Натты). Вследствие большей активности катализаторов и соотв. более мягких условий гомог. Гидрирование обычно более избирательно, чем гетерогенное. Важная область применения таких процессов-синтез оптически активных в-в, напр. гидрирование фенилакриловой к-ты, катализируемое комплексами RhCl3 с фосфинами и проводимое в смеси бензол-этанол.
В орг. синтезе широко используется некаталитич. гомог. гидрирование. Доноры водорода в этом случае - металлы в спиртах, к-тах, аммиаке и аминах; комплексные гидриды металлов (напр., Na[BH4], Li[AlH4]), бораны. При некаталитич. гидрировании первоначально идет атака нуклеоф. агента (электрона или гидрид-иона) по месту наименьшей электронной плотности в молекуле ненасыщ. соед. с послед. присоединением протона. При этом поляризованные двойные связи гидрируются легче неполяризованных.
Электроф. ионное гидрирование основано на способности гидрируемого соед. присоединять протон с образованием активного промежут. иона карбения, к-рый в свою очередь отрывает гидрид-ион от подходящего донора. Обычно донорами протонов служат сильные к-ты, напр. трифторуксусная, донорами гидрид-ионов - триалкилсиланы, жирно-ароматич. или неполностью гидрированные ароматич. углеводороды. Ионное гидрирование используют для восстановления нек-рых гетероциклич. соед.-производных тиофена, фурана, индола, для получения соед., меченных дейтерием,
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH - | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | - | - | Н | Н | Н | |
| F - | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | - | Н | Р | Р |
| Cl - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | - | - | - | Н | - | - | Н | - | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | - | Н | ? | Н | Н | ? | М | М | - | Н | ? | ? |
| HSO3 - | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | - | Н | Р | Р |
| HSO4 - | Р | Р | Р | Р | Р | Р | Р | Р | - | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р |
| NO2 - | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | - | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO - | Р | Р | Р | Р | Р | Р | Р | Р | Р | - | Р | Р | - | Р | Р | Р | Р | Р | Р | Р | - | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые (
Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую:
Скопируйте эту ссылку, чтобы разместить результат запроса " " на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки - помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация - такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Читайте также:
|


