Физические свойства солей кратко
Обновлено: 07.07.2024
Химические свойства подразделяются в зависимости от группы соли : кислые, основные и средние.
Кислые обладают термической неустойчивостью, также при нагревании разлагаются на средние соли. Для них характерна нейтрализация со щелочами.
Основные имеют такую же неустойчивость , что и кислые и также разлагаются. Нейтрализация с кислотами.
Средние соли термически неустойчивы и разлагаются. Они в ступают в реакцию обмена с кислотами, основаниями и др. солями.
К физическим можно отнести высокую температуру плавления и разную степень растворимости в воде.
При нормальных условиях соли — твёрдые кристаллические вещества. У солей типичных металлов — ионная кристаллическая решётка, поэтому они имеют сравнительно высокую температуру плавления и нелетучи.
Окраска солей чрезвычайно разнообразна. Отдельные кристаллы некоторых солей бесцветны, однако в массе множество таких мелких кристалликов приобретает белый цвет. Прозрачны и бесцветны отдельные кристаллы галогенидов щелочных металлов, например, хлорида натрия.
Что касается растворимости солей в воде, здесь описание ситуации несколько затруднено тем обстоятельством, что не имеется чётко установленной границы между малорастворимыми и практически нерастворимыми веществами. Поэтому данные в различных таблицах растворимости могут несколько (не очень существенно) отличаться.
Приведём обобщённые сведения о растворимости солей, которыми можно пользоваться, чтобы делать выводы о возможности протекания тех или иных химических реакций.
ОПРЕДЕЛЕНИЕ, КЛАССИФИКАЦИЯ
И ФИЗИЧЕСКИЕ СВОЙСТВА СОЛЕЙ
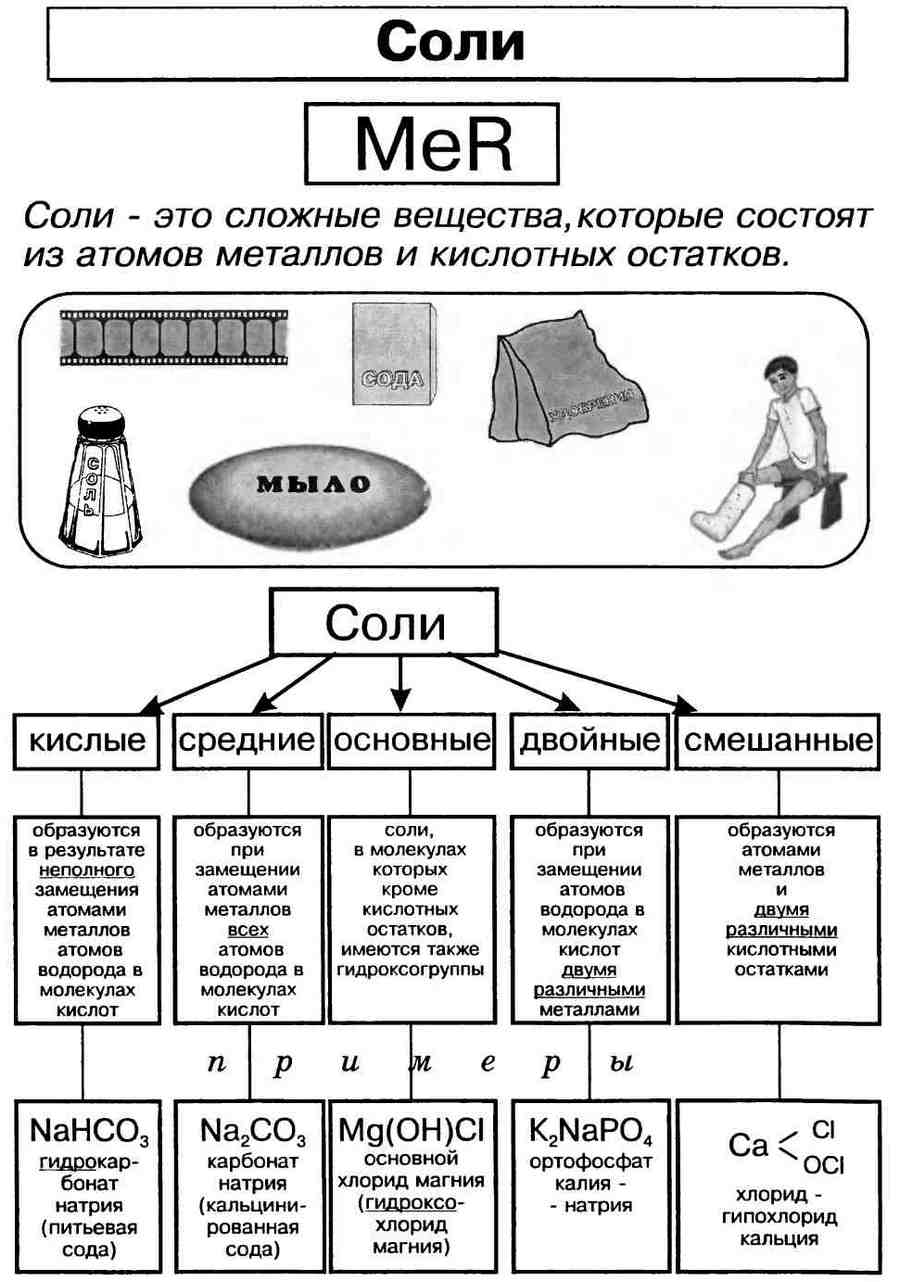
Соли – это электролиты, диссоциирующие в водном растворе на катионы металлов и анионы кислотного остатка. Соли могут быть средними (нормальными), основными, кислыми, двойными и смешанными.

При обычных условиях все соли – твёрдые вещества. Многие соли не имеют цвета, но некоторые ионы придают солям характерную окраску:
Растворимость солей различна. Практически все нитраты, соли натрия, калия, рубидия, цезия и аммония NH4 + растворимы. Среди сульфидов и фосфатов растворимы только фосфаты и сульфиды щелочных металлов.
ХИМИЧЕСКИЕ СВОЙСТВА СРЕДНИХ СОЛЕЙ
- Соли взаимодействуют с металлами. Более активные металлы (более активные восстановители) вытесняют менее активные из растворов их солей:

В этом примере ионы меди Cu 2+ являются окислителем, а цинк – восстановителем.
Активность металла определяется его положением в электрохимическом ряду напряжений металлов:
Li, Cs, К, Ва, Са, Na, Mg, Al, Zn, Cr, Fe, Co, Ni, Sn, Pb, (H2), Cu, Ag, Pt, Au.
Щелочные (Li, Na, K, Rb, Cs) и щёлочноземельные металлы (Ca, Sr, Ва) реагируют с растворами солей иначе. Сначала щелочной или щёлочноземельный металл реагирует с водой раствора соли:
2Na + 2H2O = 2NaOH + H2↑
Образовавшаяся щёлочь реагирует с раствором соли:
Так как в ходе первой реакции выделяется достаточное количество тепла, гидроксид меди (II) разлагается (свойство нерастворимых гидроксидов):
Cu(OH)2 = CuO + H2O
Поэтому вместо меди в такой реакции образуется смесь её оксида и гидроксида.

- Некоторые соли разлагаются при нагревании. Как правило, при нагревании разлагаются соли летучих кислот. Например, карбонаты (кроме карбонатов щелочных металлов) разлагаются с образованием углекислого газа и оксида металла:


ПОЛУЧЕНИЕ СРЕДНИХ СОЛЕЙ
- Реакция взаимодействия оснований с кислотами:
Mg(OH)2 + H2SO4 = MgSO4 + 2H2O
MgO + H2SO4 = MgSO4 + H2O
- Реакция основного и кислотного оксида друг с другом:
MgO + SO3 = MgSO4
- Реакция металла с неметаллом (получение солей бескислородных кислот):

а) по реакции замещения:
б) по реакции обмена (см. взаимодействие солей друг с другом):
MgI2 + HgSO4 = MgSO4 + HgI2↓
ПОЛУЧЕНИЕ КИСЛЫХ СОЛЕЙ
- Неполная нейтрализация двухосновных, трёхосновных, многоосновных кислот основаниями:
2NaOH + H3РO4 = Na2HPO4 + 2H2O
(в результате неполной нейтрализации образовался гидрофосфат натрия);
NaOH + H3РO4 = NaH2PO4 + H2O
(в результате неполной нейтрализации образуется дигидрофосфат натрия).
- Неполная нейтрализация кислотных оксидов, соответствующих двухосновным, трёхосновным, многоосновным кислотам, основаниями (так можно получить только соли кислородсодержащих кислот):
4NaOH + Р2O5 = 2Na2HPO4 + H2O
(в результате неполной нейтрализации образовался дигидрофосфат натрия);
2NaOH + Р2O5 + H2O = 2NaH2PO4
(в результате неполной нейтрализации образовался гидрофосфат натрия).
- Взаимодействие средних солей с соответствующими кислотами:
Na2SO4 + H2SO4 = 2NaHSO4
NaCl (тв.) + H2SO4 (конц.) = NaHSO4 + HCl↑
- Взаимодействие средних солей с оксидами, соответствующими многоосновным кислотам, в водных растворах:
СаСO3 + СO2 + H2O = Са(НСО3)2
(в данном примере взвесь СаСO3 постепенно исчезает, так как образуется хорошо растворимый гидрокарбонат кальция).
Кислые соли, как правило, растворимы лучше соответствующих им средних. Так, например, гидрокарбонат кальция Са(НСО3)2 растворим в воде, в то время как карбонат кальция практически нерастворим.
- Кислые соли нестабильных кислот разлагаются при нагревании с образованием средних солей:

- Кислую соль можно перевести в среднюю, обработав её эквивалентным количеством щёлочи:

- Кислые соли вступают в такие же реакции, как и средние, например в обменные реакции солей друг с другом:

Образец выполнения задания ОГЭ
Задание. И сульфат меди (II), и нитрат серебра взаимодействуют
- 1) с хлоридом калия
- 2) с соляной кислотой
- 3) с оксидом магния
- 4) с железом
Решение. Хлорид калия, сульфат меди (II), нитрат серебра – соли. Растворимые соли взаимодействуют друг с другом, если в результате реакции один из продуктов реакции выпадает в осадок (т. е. образуется малорастворимое в воде вещество). В случае взаимодействия нитрата серебра с хлоридом калия действительно образуется осадок (белый творожистый осадок хлорида серебра):
Но сульфат меди (II) с хлоридом калия не взаимодействует, в данном случае связывания ионов в растворе не происходит. Таким образом, вариант 1 не подходит.
Соляная кислота – сильный электролит. Сильные кислоты взаимодействуют с солями слабых кислот, вытесняя их из солей. Но сульфат меди (II) – соль сильной серной кислоты, а нитрат серебра – соль сильной азотной кислоты. Серная кислота может вытеснить азотную и соляную кислоты из кристаллических солей (не в растворах), так как HNO3 и НCl – летучие кислоты, а серная – нелетучая. Соляная кислота вытеснить серную или азотную не может. Поэтому вариант 2 не подходит.
С оксидами соли взаимодействуют в редких случаях. Например, карбонаты при сплавлении взаимодействуют с оксидом кремния (IV). Средние соли при взаимодействии в растворе с кислотными оксидами соответствующих кислот превращаются в кислые соли (если такие для данных кислот существуют). В данном примере оксид магния не взаимодействует ни с сульфатом меди (II), ни с нитратом серебра. Ответ 3 не подходит.
Обе соли взаимодействуют с железом. Железо находится в электрохимическом ряду напряжений металлов до меди и до серебра:
Правильный ответ – 4 (с железом).

Сложные неорганические соединения, образованные металлами и кислотными остатками, называются солями. Химические свойства солей позволяют получать различные соединения.
Общая формула солей –
где М – металл, Ac – кислотный остаток, n и m – количество атомов металла и кислотного остатка соответственно.
По составу и образованию соли делятся на шесть видов:
- средние(нормальные) – образуются путём полного замещения водорода в кислоте атомами металла или гидроксильной группы в основании кислотными остатками (Na3PO4 образован из H3PO4, CuSO4 – из Cu(OH)2, AlCl3 – из HCl);
- кислые– образуются при неполном замещении водорода в кислотах атомами металла (NaHSO4 образован при присоединении Na к H2SO4, Na2HPO4 – из H3PO4);
- основные– образуются при неполном замещении гидроксильных групп кислотными остатками (CaOHCl образован из Ca(OH)2, FeOHCl2 – из Fe(OH)3);
- двойные– состоят из двух металлов и одного кислотного остатка (КNaSO4);
- смешанные– состоят из одного металла и нескольких кислотных остатков (CaClBr);
- комплексные– состоят из комплексного аниона или катиона ([Cu(NH3)4]SO4).
Наиболее активными являются кислые соли, включающие водород. Химические свойства кислых солей сходны со свойствами кислот. Они взаимодействуют с металлами, их оксидами и гидроксидами, другими солями, щелочами.
Физические свойства
Соли – это кристаллические вещества разных цветов.
Основные физические свойства солей:
- ионная кристаллическая решётка;
- высокие температуры плавления;
- в твёрдом состоянии плохо проводят электричество;
- по растворимости выделяют растворимые, малорастворимые и нерастворимые соли.
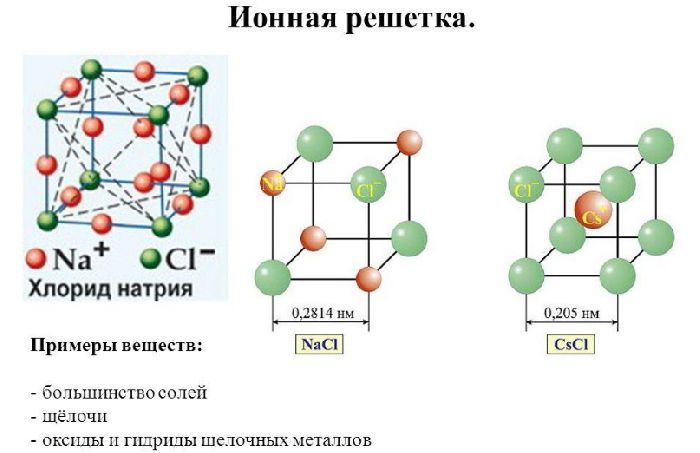
Рис. 2. Ионная кристаллическая решётка.
Некоторые соли имеют ковалентное или промежуточное, образованное ионными и ковалентными связями, строение.
Получение
Соли образуются из кислот и оснований. Реакции кислоты с различными веществами:
-
с активными металлами –
Основания могут взаимодействовать:
Существую также другие способы получения:
-
взаимодействие двух солей –
Химические свойства
Растворимые соли являются электролитами и подвержены реакции диссоциации. При взаимодействии с водой они распадаются, т.е. диссоциируют на положительно и отрицательно заряженные ионы – катионы и анионы соответственно. Катионами являются ионы металлов, анионами – кислотные остатки. Примеры ионных уравнений:
- NaCl → Na + + Cl − ;
- Al2(SO4)3 → 2Al3 + + 3SO4 2− ;
- CaClBr → Ca2 + + Cl – + Br – .
Помимо катионов металлов в солях могут присутствовать катионы аммония (NH4 + ) и фосфония (PH4 + ).
Другие реакции описаны в таблице химических свойств солей.
Реакция
Особенности
Уравнение
Более активный металл вытесняет менее активный
Свойственно солям, образованным более слабыми кислотами. Образуются новые соли
Взаимодействуют соли, образованные нерастворимыми основаниями
Взаимодействуют растворимые соли. Образуется осадок

Рис. 3. Выделение осадка при взаимодействии с основаниями.
Некоторые соли в зависимости от вида разлагаются при нагревании на оксид металла и простые вещества. Например, СаСO3 → СаO + СО2, 2AgCl → Ag + Cl2.
Что мы узнали?
Из урока 8 класса химии узнали об особенностях и видах солей. Сложные неорганические соединения состоят из металлов и кислотных остатков. Могут включать водород (кислые соли), два металла или два кислотных остатка. Это твёрдые кристаллические вещества, которые образуются в результате реакций кислот или щелочей с металлами. Реагируют с основаниями, кислотами, металлами, другими солями.
Читайте также:

