Электрическое производство алюминия кратко
Обновлено: 05.07.2024
На фоне новостей о госперевороте в Гвинее, втором мировом поставщике сырья для алюминия, стоит освежить информацию о том, как производится данный металл и какие страны играют ключевую роль на этом рынке.
Производственная цепочка алюминия выглядит следующим образом:
Добыча бокситов
В мире существует несколько видов алюминиевых руд, но основным сырьем для производства являются именно бокситы. Эта порода добывается преимущественно открытым способом с применением мощной карьерной техники. Около 90% мировых запасов бокситов приходится на страны тропического пояса, причем 70% — на 5 стран: Гвинею, Австралию, Вьетнам, Бразилию и Ямайку.
Крупнейшими производителями бокситов являются Австралия, Гвинея и Китай: там сосредоточено 67% всей мировой добычи.
Производство глинозема (Alumina)
Добытые бокситы дробят, обрабатывают щелочным раствором и выделяют из них глинозем — оксид алюминия Al2O3. В бокситах, как правило, содержится от 40% до 60% глинозема. Полученный глинозем выступает ключевым сырьем в процессе электролиза алюминия. Из одной тонны глинозема в среднем получают 0,5 тонны чистого алюминия.
Электролиз и выплавка первичного алюминия
Под воздействием электрического тока связь между атомами алюминия и кислорода в глиноземе распадается. Алюминий осаждается на дне специальной электролизной ванны, а кислород соединяется с углеродом, входящим в состав анодных блоков, и образует углекислый газ. При производстве одной тонны алюминия выделяется 280 тыс. кубометров газа.
Одной из революционных технологий в производстве алюминия является использование в электролизе инертного анода. При этом выделяемый из глинозема кислород не соединяется с углеродом и выбросов CO2 практически не образуется. В 2021 г. РУСАЛ начал тестовые поставки алюминия, произведенного с использованием такой технологии.
Крупнейшие компании–производители алюминия в мире
Изготовление конечных изделий
После электролиза остатки примесей из алюминия удаляют методом переплавки. Из готового первичного алюминия отливают слитки, которые впоследствии будут использоваться для изготовления конечных изделий.
Прямоугольные слитки называют слябами. Они применяются для проката в тонкие листы и производства алюминиевой фольги, банок для напитков, автомобильных кузовов и пр.
Цилиндрические слитки алюминия используют для экструзии — выдавливания через отверстие необходимой формы. Так производится большинство алюминиевых изделий.
При производстве изделий в алюминий могут внедряться различные добавки для производства сплавов, обладающих необходимыми качествами. В промышленности используется свыше 100 различных марок алюминиевых сплавов.
Переработка
Алюминий, в отличие от стали и некоторых других металлов, не подвержен коррозии и не теряет своих свойств в процессе использования. Изделия из него могут подвергаться переплавке и вторичной переработке в новые продукты — рециклингу.
В развитых странах доля переработки в производстве конечных изделий довольно высока и, по всем прогнозам, будет расти и дальше. По оценке информационного издания Алюминиевый вестник, в странах Евросоюза доля вторичного сырья в автопроме и строительстве достигает 90–95%, в алюминиевой банке — 74%, а в целом в упаковке — 60%.
В России собирается и перерабатывается более 600 тыс. алюминиевого лома. В литой продукции доля вторсырья составляет 59%, в экструзии — 39%, в прокате — 15%.
БКС Мир инвестиций
ОФЗ с доходностью 20% на несколько лет
С 5 по 8 марта торги на всех рынках Московской биржи не проводятся
Западные площадки — минус $100 млрд и проблемы ликвидности
Что делать с акциями ЛУКОЙЛа, когда откроются торги на Мосбирже
Никель на максимумах, палладий и медь догоняют. Что это значит для Норникеля
Опыт Ирана. Валюта и фондовый рынок под санкциями
В чем пересидеть кризис: наличные деньги или акции
Что делать, когда откроются торги на Мосбирже
Алюминий получают путем электролиза глинозема, растворенного в расплавленном электролите, основным компонентом которого является криолит.
Алюминий получают путем электролиза глинозема, растворенного в расплавленном электролите, основным компонентом которого является криолит. В чистом криолите Na3AlF6(3NaF • AlF3) отношение NaF : AlF3 равно 3, для экономии электроэнергии необходимо при электролизе иметь это отношение в пределах 2,6—2,8, поэтому к криолиту добавляют фтористый алюминий AlF3. Кроме того, для снижения температуры плавления в электролит добавляют немного CaF2, MgF2 и иногда NaCl. Содержание основных компонентов в промышленном электролите находится в следующих пределах, %: Na3AlF6 75—90; AlF3 5—12; MgF2 2—5; CaF2 2—4; Al2O3 2—10. При повышении содержания Al2O3 более 10 % резко повышается тугоплавкость электролита, при содержании менее 1,3 % нарушается нормальный режим электролиза.
Электролизная ванна или электролизер, где проводят электролиз, имеет в плане прямоугольную форму. Схема поперечного разреза ванны показана на рис. 247. Кожух 1 из стальных листов охватывает стены ванны, а у больших ванн выполнен с днищем. Внутри имеется слой шамота 2 и далее стены выложены угольными плитами 4, а под образован подовыми угольными блоками 3. Ванна глубиной 0,5—0,6 м заполнена электролитом и находящимся под ним слоем жидкого алюминия.

Угольный анод 6 (иногда их несколько) подвешен на стальных стержнях 8 так, что его нижний конец погружен в электролит, через стержни 8 к аноду подается ток от шин 7.
Мощность электролизера (ванны), определяемая силой подводимого к ней тока, изменяется от 30 кА у ванн малой мощности до 250 кА у ванн большой мощности. Поскольку допустимая удельная плотность проходящего через анод тока составляет 0,65—1,0 А/см 2 , при росте мощности ванн увеличивают площадь анода; размеры поперечного сечения анода мощных ванн достигают 2,8×9 м, размеры ванны (внутри) — 3,8×10 м.
Существующие ванны различаются мощностью и устройством анода: ванны с одним самообжигающимся анодом и верхним токоподводом, с таким же анодом и боковым токоподводом и ванны с анодом из обожженных блоков. Ванна с самообжигающимся анодом и верхним подводом тока показана на рис. 248, а. Анод прямоугольного сечения является непрерывнонаращиваемым. Его кожух сделан из стального листа, в кожух сверху загружают брикеты из углеродистой электродной массы (нефтяной кокс с каменноугольным пеком). Вверху масса плавится, а в нижней части кожуха, где высокие температуры, она спекается, коксуется и превращается в твердый блок. В него запекаются погруженные в электродную массу на разную глубину стальные штыри 7, расположенные в два—четыре ряда вдоль ванны. Эти стержни служат для подвода тока к аноду и для его удержания над ванной, кожух анода крепится над ванной отдельно. В процессе сгорания анода наиболее глубоко расположенные штыри поочередно выдергивают из затвердевшей массы и закрепляют на более высоком уровне, через некоторое время они спекаются с твердеющей массой.

По мере сгорания нижней части анода его с помощью специального механизма опускают, при этом анод скользит внутри кожуха вниз. К нижней части кожуха анода крепится газосборный колокол, предназначенный для улавливания выделяющихся вокруг анода газов.
Электролизные ванны с предварительно обожженными анодами (рис. 248, б) имеют анодный узел, составленный из нескольких (до 20 и более) угольных или графитированных блоков, расположенных в два ряда. В каждом блоке закреплены четыре стальных ниппеля 9, соединенных со штангой 77; это устройство служит для подвода тока и для подвески блока. Сгоревшие блоки заменяют новыми. Над ванной установлен газоулавливающий короб.
Использование обожженных анодов позволило увеличить единичную мощность ванн и сильно сократить выделение вредных канцерогенных веществ, которые образуются при коксовании пека самообжигающихся электродов.
Электролизные ванны размещают в цехе в ряд — по несколько десятков ванн в ряду.
Электролиз ведут при напряжении 4—4,3 В и, как отмечалось, при удельной плотности тока, проходящего через анод, равной 0,65—1,0 А/см 2 . Толщина слоя электролита в ванне составляет 150—250 мм. Температуру ванны поддерживают в пределах 950—970 °С за счет тепла, выделяющегося при прохождении постоянного гока через электролит. Такие температуры имеют место под анодом, а на границе с воздухом образуется корка затвердевшего электролита рис. 247, 9, а у стен ванны — затвердевший слой электролита 10 (гарнисаж).
Необходимая температура ванны, т.е. выделение в слое электролита необходимого количества тепла, обеспечивается при определенном электросопротивлении слоя электролита. Такого электросопротивления достигают, поддерживая в заданных пределах состав электролита и толщину его токопроводящего слоя, т.е. расстояния между анодом и слоем жидкого алюминия в пределах 40—60 мм (увеличение, например, этого расстояния, т.е. электросопротивления слоя электролита, вызывает увеличение выделения тепла при прохождении тока и, соответственно, перегрев электролита).
При приложении напряжения к катоду и аноду составляющие жидкого электролита подвергаются электролитической диссоциации, и расплав состоит из многочисленных катионов и анионов. Состав электролита подобран так, что в соответствии со значениями потенциалов разряда на электродах могут разряжаться только катионы Al 3+ и анионы О 2- , образующиеся при диссоциации Al2O3 в электролите. Соответственно электрохимический процесс на электродах описывается следующими уравнениями:
на катоде 2Al 3+ + 6е → 2Al;
на аноде 3О 2- — 6е → 3O.
Разряжающийся на катоде алюминий накапливается на подине ванны под слоем электролита. Выделяющийся на аноде кислород взаимодействует с углеродом анода с образованием газов СО и СO2, т.е. при этом окисляется низ анода, в связи с чем анод периодически опускают. Газы СО и СO2 выходят из-под анодов вдоль их боковых поверхностей, они содержат выделяющиеся из электролита токсичные фтористые соединения и глиноземную пыль (из самообжигающихся анодов в них также попадают вредные смолистые возгоны); эти газы улавливают и очищают от пыли и фтористых соединений.
По ходу процесса в ванны периодически загружают глинозем; контролируют состав электролита, вводя корректирующие добавки; с помощью регуляторов поддерживают оптимальное расстояние между анодами и жидким алюминием (в пределах 40—50 мм). Глинозем загружают в ванны сверху, пробивая для этого корку спекшегося электролита (рис. 247, 9) с помощью передвигающихся вдоль ванн машин.
Жидкий алюминий извлекают из ванн один раз в сутки или через 2—3 сут с помощью вакуум-ковшей. Вакуум-ковш представляет собой (рис. 249) вмещающую 1,5—5 т алюминия футерованную шамотом емкость, в которой создается разряжение ~ 70 кПа. Соединенную с патрубком 6 ковша заборную трубку погружают сверху в слой жидкого алюминия в ванне и за счет разрежения алюминий засасывается в ковш.

Выделяющиеся анодные газы вначале направляют в горелки, где сжигают СО и возгоны смолы, а затем в газоочистку, где улавливают пыль и фтористые соединения.
Производительность современных электролизных ванн составляет 500—1200 кг алюминия в сутки. Для получения 1 т алюминия расходуется ~ 1,95 т глинозема, ~ 25 кг криолита, 25 кг фтористого алюминия, 0,5—0,6 т анодной массы, 14—16 МВт • ч электроэнергии.
Обычные для других металлов способы получения из окислов: восстановлением в присутствии углерода или электролизом из водных растворов для алюминия неприемлемы.
При восстановлении в присутствии углерода алюминий образует карбид Al4C3. Легкие металлы, в том числе и алюминий, будучи наиболее электроотрицательными в ряду напряжений, не могут быть выделены электролизом из водных растворов их солей, так как на катоде выделяется водород и образуется гидрат окиси алюминия.
Отличительной особенностью металлургии алюминия, как и других легких металлов, является электролиз его в расплавленных средах, а именно электролиз глинозема в расплавленною криолите, который не содержит свободных ионов водорода.
Электролиз осуществляется в ванне, представленной схематично на рис. 160.

Ванна имеет прямоугольную форму и устанавливается на массивном фундаменте. Кожух ванны 1 металлический, подина и стены 2 — угольные, составленные из отдельных плит, связанных скоксованной углеродистой набойкой. Глубина рабочего пространства ванны около 0,5 м. К подине подведен отрицательный полюс 3 источника постоянного тока, сверху в ванну погружены угольные электроды 4, служащие анодами (положительным полюсом), к которым ток подводится по стержням 5 и шинам 6. Глубина погружения электродов невелика, только часть их находится в расплавленном электролите 7; ток протекает через слой расплавленного электролита и металла к отрицательному полюсу.
Прохождение по цепи тока сопровождается не только разложением глинозема, но и выделением значительного количества тепла, которое необходимо для поддержания электролита в расплавленном состоянии. Восстанавливаемый алюминий образует на подине слой жидкого металла 8, электролит образует на стенках ванны гарниссаж 9, а на поверхности корку 10. Выделяющийся на анодах кислород окисляет их до CO и CO2; сгорающие аноды постепенно опускают. По мере расходования глинозема в процессе электролиза новые его порции загружают в электролит и периодически извлекают из ванны алюминий.
Криолит весьма дорог, имеет довольно высокую температуру плавления и летучесть, однако отсутствие в его составе металлов, способных осаждаться на катоде раньше алюминия и способность хорошо растворять Al2O3 представляет столь существенные преимущества, что делают его в настоящее время единственным практически применяемым электролитом.
Изменение соотношения NaF и AlF3 существенно влияет на температуру плавления смеси, понижая ее при отклонении и в одну и в другую сторону. Объясняется это тем, что химическое соединение — криолит 3 NaF*AlF3 имеет наиболее высокую температуру плавления (1000°). Добавка к криолиту NaF или AlF3 ведет к получению смесей, плавящихся при температуре ниже 1000°.
Обычно работают при криолитовом отношении около 2,3—2,7, т. е. с увеличенным против состава криолита содержанием AlF3.
При этом несколько увеличивается летучесть расплава и уменьшается растворимость Al2O3, но уменьшается возможность выделения на катоде натрия. Последний выделяется в большей степени при обогащении расплава фтористым натрием, отчего снижается выход по току.
На понижение температуры расплава благоприятно сказывается также присутствие в электролите глинозема. Однако при содержании в расплавах более 15% (вес.) Al2O3 температура плавления смеси повышается. Практически концентрация глинозема в электролите не превышает 7—10%.
Важнейшее значение в процессе электролиза имеет соотношение удельных весов алюминия и криолита. При комнатной температуре удельный вес алюминия равен 2,7, а криолита 2,95. При 1000° удельный вес алюминия 2,3, а криолита, содержащего 10% AhO3, всего 2,03. Однако эта малая разница в удельных весах алюминия и электролита достаточна для удержания металла на подине под слоем электролита.
Криолит в расплавленном состоянии диссоциирует на ионы по схеме:
а глинозем по схеме: Al2O3 —> 2 Al3+ + 3 О2-.
При этом ионы Al3+ и Na+ переносят ток к катоду, но разряжаются более электроположительные ионы алюминия. К аноду же движутся ионы AlF36- и О2-, где происходит разряд ионов кислорода, т. е. на катоде
Элементарный кислород сжигает уголь анода до CO и CO2.
В процессе электролитического получения алюминия, как и при электролизе других металлов в расплавленных средах, наблюдается явление анодного эффекта, имеющее большое практическое значение и представляющее значительный интерес с теоретической точки зрения.
Глинозем вводится в ванну периодически. К тому моменту, когда загруженная порция глинозема израсходуется и концентрация его снизится от 10 до 1%—2%, напряжение на ванне, обычно не превышающее 4—4,3 в, резко возрастает до 30—40 в. При этом на поверхности анода, погруженной в электролит, возникают электрические дуги, приводящие к разогреву электролита и к усиленному его испарению. Добавка новых порций глинозема и повышение концентрации его в электролите прекращает описанное явление.
При возникновении анодных эффектов повышается расход электроэнергии и более быстро разрушаются аноды, а также повышается улетучивание электролита и ухудшается работа ртутных выпрямителей.
С другой стороны, анодный эффект облегчает контроль за питанием ванны глиноземом, а также за общим ее состоянием, так как резкий скачок напряжения при анодном эффекте свидетельствует о нормальной работе ванны, в то время как запаздывание его или пульсация напряжения свидетельствуют о нарушении нормального хода электролиза.
Поэтому анодные эффекты сводят к минимуму, допуская их для контроля примерно один раз в сутки и реже.
Анодный эффект возникает в результате образования на поверхности анода пленки газов. При достаточной концентрации в расплаве окислов поверхность анодов хорошо смачивается расплавом, и газы легко удаляются с нее. При отсутствии или малой концентрации окислов расплав хуже смачивает поверхность анодов, выделяющиеся пузырьки газа прилипают к ней и образуют пленку, обладающую высоким электрическим сопротивлением. Поэтому резко возрастает напряжение.
Электролиз является сложным процессом, сопровождающимся рядом побочных явлений, например, растворением алюминия в электролите, приводящим к потерям металла. Растворимость алюминия в электролите не превышает 0,1%, но, распространяясь по всему объему ванны и окисляясь до Аl2O3 ка ее поверхности воздухом и выделяющимся на аноде кислородом, алюминий в значительных количествах переходит в электролит. Понижение температуры электролиза способствует ослаблению этого процесса.
Кроме этого, при электролизе электролит впитывается в угольные катодные блоки подины, а также частично испаряется, что ведет к некоторому изменению состава электролита и определяет необходимость его корректирования до определенного состава.
Практический расход электроэнергии, как правило, равен 17 000 квт-ч/т, и нормально работающая ванна выдает около 60 г Al на 1-квт-ч.
Затраты на электроэнергию составляют значительную долю в себестоимости алюминия, поэтому величина выхода по току и энергии определяет в значительной мере экономику процесса.
Выход по току зависит главным образом от плотности тока, температуры и состава электролита, а также от расстояния между электродами.
С ростом температуры от 940 до 990° в силу повышения потерь алюминия за счет растворения выход по току падает. Снижение температуры ниже известного предела и связанное с этим повышение вязкости электролита приводит также к понижению выхода по току.
Изменение состава электролита в сторону повышения в нем концентрации фтористого натрия приводит к понижению выхода по току за счет частичного разряда ионов натрия на катоде. Выделяющийся натрий, мало растворимый в алюминии, всплывает на поверхность ванны и окисляется. Значительное увеличение концентрации фтористого алюминия в электролите приводит к повышению растворимости Al в электролите и также способствует понижению выхода по току.
При сближении электродов снижается выход по току, так как появляется больше возможностей попадания растворенного алюминия в анодное пространство и его окисления. Увеличение междуполюсного расстояния вызывает повышение напряжения и увеличенный расход энергии.
Повышение плотности тока сказывается положительно на выходе по току, так как количество выделяемого на катоде в единицу времени металла увеличивается с повышением плотности тока, в то время как величина обратного растворения алюминия и его окисления при этом практически не изменяются.
Повышение плотности тока сопровождается ростом напряжения, поэтому выбор оптимальной плотности определяется конкретно для каждого отдельного случая. Обычно она выдерживается в пределах 0,8—1,0 а/см2 в сечении анода,
Междуполюсное расстояние на современных ваннах равно 4—5 см.
Наиболее широкое распространение в настоящее время получили электролитные ванны с самообжигающимися анодами.
Ванна, приведенная на рис. 161, установлена на фундаменте. Стальной прямоугольный ее кожух закреплен на фундаменте анкерными болтами. На несколько рядов шамотного кирпича и подушку из углеродистой массы в кожухе уложена подина из угольных блоков, связанных угольной набойкой.
В подовые блоки введены стальные стержни, залитые чугуном, служащие для отвода тока.
Боковая футеровка ванны выложена из угольных плит, изолированных от кожуха.

Над ванной расположен прямоугольный алюминиевый каркас, состоящий из отдельных царг и служащий кожухом самообжигающегося анода. Внутрь каркаса загружают анодную массу. В верхних частях анода масса находится в размягченном состоянии. По мере опускания анода масса перемещается в более горячие зоны, где происходит удаление летучих и коксование. В нижней части анода углеродистая масса полностью спекается за счет тепла, выделяемого из ванны. Каркас выполнен из алюминиевых листов толщиной 1—2 мм и для жесткости укреплен рамой и ребрами жесткости.
В тело анода забивают стальные штыри, служащие для подвода тока и подвески тела анода к анодной раме. Штыри гибкими шинами соединены с основной токоподводящей шиной.
По мере сгорания анода он опускается, каркас его при этом наращивается новыми царгами.
Современные ванны сооружаются на силу тока до 140 000 а.
Продолжительность работы ванн между сроками капитального ремонта достигает 3—4 лет. Обслуживание ванны слагается из следующих операций:
1. Питание глиноземом и обработка ванны.
2. Регулирование температуры ванны и междуполюсного расстояния.
3. Обслуживание анодов.
4. Извлечение алюминия из ванны.
Питание ванны глиноземом осуществляется по мере его расходования. Глинозем насыпается на поверхность ванны, покрытую коркой замерзшего электролита. При возникновении анодного эффекта или при приближении его корку вблизи анода пробивают вручную или пневматическим отбойным молотком и погружают глинозем в расплав. Для ускорения растворения глинозема расплав перемешивают.
Затем с поверхности электролита снимают угольную пену, состоящую из механически запутавшихся частиц углерода, попавших в расплав вследствие механического разрушения анодов. В периоды, когда в ванну вводится глинозем и перемешивается электролит, частицы угля всплывают на поверхность расплава, откуда во время обработки ванны его удаляют шумовками (дырчатыми ложками). При накоплении в ванне большого количества углерода возрастает электрическое сопротивление электролита, что сопровождается сильным его перегревом.
Систематическим наблюдением контролируют криолитовое отношение в ванне, которое стремятся поддерживать ниже 3 (в среднем 2,5). При отклонении от этого числа в ванну вместе с глиноземом вводят AlF3 или NaF.
Уровень электролита в ванне поддерживается около 30 см. Контролируют его, погружая в ванну ломок и замеряя образовавшуюся на нем корку.
Междуполюсным расстоянием называется расстояние от нижней поверхности анода до уровня металла. Это расстояние изменяется путем вертикального перемещения анода. С уменьшением этого расстояния температура ванны понижается, с увеличением повышается. Обычно оно равно 4,5—5 см.
Обслуживание анодов, помимо их перемещения по мере сгорания, заключается в своевременном наращивании кожуха, загрузке анодной массы, забивке штырей в анод, зачистке контактов, выдергивании штырей, перетяжке анодной рамы.
В нижней закоксованной части анод представляет монолитный углеродный блок. Эта часть ограничена сверху областью температуры около 400°; далее в области температур 400—360° находится зона коксования. Над ней в области температур 360—140° находится зона выделения летучих, а далее следует область размягчения массы. Общая высота анода около 1—1,1 м. По мере его сгорания к верхней части кожуха приклепывают примерно раз в месяц очередную царгу и постепенно заполняют ее анодной массой через каждые 7—10 дней. Подводящие ток штыри служат одновременно и для подвески анода. По мере опускания анода нижний ряд штырей приближается к поверхности электролита. Когда это расстояние сократится до 10 см, гибкие токопроводы с нижнего ряда переключают на следующий и временно подвешивают анод за второй ряд штырей. При этом первый ряд освобождается от нагрузки и штыри специальным механизмом выдергиваются из анода.
Постепенно накапливающийся на подине металл удаляют через 3—4 суток сифоном или вакуум-ковшом.
Сифон представляет собой чугунный фасонный тройник, боковой отвод которого погружается в ванну расплавленного металла, а нижний — в ковш. Верхний патрубок подсоединяется к насосу для создания разрежения. Как и во всяком другом случае сифонного слива, ковш необходимо располагать ниже уровня ванны (рис. 162), что является недостатком такого способа удаления алюминия, так как требует устройства приямков, траншей и пр.
Применение вакуум-ковшей исключает необходимость таких устройств, но связано с более глубоким вакуумом, с более сложной и дорогой аппаратурой.

Устройство вакуум-ковша показано на рис. 163. Приемная трубка ковша погружается в расплавленный Al, а патрубок присоединяется к вакуум-линии. Наполненный металлом ковш отсоединяют от линии и краном переносят на площадку для розлива.
Полученный после электролиза металл загрязнен различными механическими примесями, для очистки от которых алюминий перед розливом хлорируют (в числе примесей имеется электролит, глинозем и пр.). Для этого ковш с металлом ставят под колпак и по графитовой трубке вводят в ковш газообразный хлор, подаваемый из баллонов. Хлорирование длится 10—15 мин., образующиеся газы удаляются из-под колпака вентилятором.
При хлорировании образуется летучий АlСl3, который пузырьками выносит неметаллические включения.
Металл из разных ванн разливают в чушки на разливочной машине.
Часть алюминия тут же в цехе используется для изготовления различных сплавов, а другая часть более чистого металла разливается в слитки.
В табл. 43 приведен действующий ГОСТ на первичный алюминий.
В процессе электролиза образуются анодные газы и угольная пена.
Пена содержит до 75% электролита, который регенерируется просеиванием застывшей и измельченной массы, а также флотацией, при которой уголь переходит в пенный продукт, направляемый в канализацию.

Анодные газы содержат до 40 мг/м3 фтора, до 90 мг/м3 пыли криолита и глинозема и до 100 мг/м3 смолы. Газы вредны для людей и растительности, поэтому их очищают, промывая слабыми содовыми растворами в скруббере. Извлекаемые при этом фтористые соли возвращаются в производство.
Современные электролизные цехи — это весьма большие сооружения, в которых установлено до 150 и более ванн.
Ванны располагают в корпусах в два ряда и обслуживают мостовым краном. Цех обеспечивают интенсивной приточной и вытяжной вентиляцией, а также рядом вспомогательных помещений для рафинирования, розлива металла и других операций.
Процесс электролитического получения алюминия, по сравнению с другими металлургическими процессами, хорошо механизирован, и стоимость рабочей силы составляет незначительную долю в общей себестоимости металла. Основными статьями расхода при производстве алюминия являются стоимость глинозема и электроэнергии.

Впервые металлический алюминий был получен химическим путем немецким химиком Ф.Велером в 1821 г. (восстановлением из хлорида алюминия металлическим калием при нагревании). В 1854 г. французский ученый Сент-Клер Девиль предложил электрохимический способ получения алюминия, восстанавливая натрием двойной хлорид алюминия-натрия.
Металлический алюминий получают в три стадии:
- Получение глинозема (Al2O3) из алюминиевых руд;
- Получение алюминия из глинозема;
- Рафинирование алюминия.
Получение глинозема
Около 95 % всего глинозема получают из бокситовых руд.
Бокситовая руда
Боксит (фр. bauxite) (по названию местности Baux на юге Франции) – алюминиевая руда, состоящая из гидроксидов алюминия, оксидов железа и кремния, сырьё для получения глинозёма и глинозёмосодержащих огнеупоров. Содержание глинозёма в промышленных бокситах колеблется от 40 % до 60 % и выше. Используется также в качестве флюса в чёрной металлургии.

Рисунок 1 – Бокситовая руда
Обычно бокситы представляют собой землистую глиноподобную массу, которая может иметь полосчатую, пизолитовую (гороховидную) либо однородную текстуру. В обычных условиях выветривания полевые шпаты (минералы, составляющие большую часть земной коры и являющиеся алюмосиликатами) разлагаются с образованием глин, но в условиях жаркого климата и высокой влажности конечным продуктом их разложения могут оказаться бокситы, т. к. подобная обстановка благоприятствует выносу щелочей и кремнезёма, особенно из сиенитов или габбро. Бокситы перерабатывают в алюминий поэтапно: сначала получают оксид алюминия (глинозём), а затем металлический алюминий (электролитическим способом в присутствии криолита).
Основные примеси в бокситах это Fe2O3, SiO2, TiO2. К малым примесям бокситов относят: Na2O, K2O, CaO, MgO, редкоземельные элементы, Cr, P, V, F, органика.
Обычно бокситы классифицируют:
- по цвету;
- по основному минералу (чаще они бывают смешанными);
- по возрасту.
Основными критериями качества алюминиевой руды являются :
- Кремниевый модуль (Мsi = Al2O3/SiO2 (% масс.)). Чем больше кремниевый модуль тем лучше качество (Мsi = 7);
- Содержание железа в пересчете на Fe2O3. Если содержание Fe2O3около 18 % масс., то боксит считается высокожелезистым. Чем больше содержание железа труднее добыть бокситы;
- Содержание серы. Наличие большого количества серы усложняет переработку боксита;
- Содержание карбонатов в пересчете на CO3 (2-) . Наличие большого количества карбонатов усложняет переработку боксита.
- в производстве глинозема;
- в производстве абразивных материалов;
- в производстве огнеупорных материалов;
- в качестве флюса для выплавки мартеновской стали;
- для сушки газов и чистки нефти от серы;
- в качестве красителя.
На сегодняшний день главными поставщиками боксита являются:
- Австралия – там находятся также огромные залежи Fe, Au, U, Ni, Co, Cuи др. Выгоднее покупать сырье у Австралии, чем перерабатывать свое.
- Гвинея – У России есть несколько купленных мест.
- Центральная Америка: Гайана, Ямайка, Суриман.
- Бразилия.
В Европе все месторождения истощены. Осуществляются поставки бокситов из Греции, но данное сырье является сырьем низкого качества.
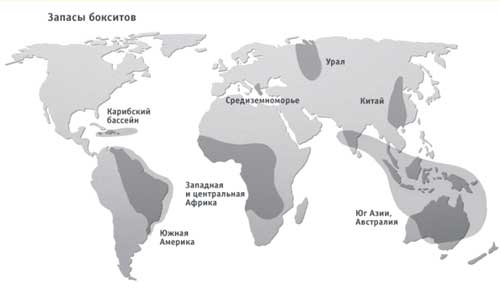
Рисунок 2 – Запасы бокситов в мире
Ниже представлен основных месторождений алюминиевых руд в России.
- Первое месторождение было открыто в 1914 г. под Сант-Петербургов, рядом с городом Тихвин. На данном месторождении было построено 6 заводов. Самый большой - это Волховский алюминиевый завод. На сегодняшний день Тихвинское месторождение истощено и работает в основном на привозном сырье.
- В 1931 г. было открыто уникальное Северо-Уральское месторождение высококачественных бокситов (СУБР). Оно послужило базой для строительства в 1939 г. Уральского алюминиевого завода (УАЗ). А на основе Южно-уральского бокситового рудника (ЮУБР) был построен Богословский алюминиевый завод (БАЗ).
- Североонежское месторождение находится по дороге на Кольский полуостров. В Плане есть, но дата строительства неизвестна.
- Висловское месторождение – чистоглинистое месторождение каолитного типа. Для глинозема не используется.
- Тиманское месторождение (Республика Коми, Варкута). Канадцы заинтересованы в данном месторождении, поэтому планируют строительство заводов ("Коми Суал" - холдинг).
Получение глинозема из бокситовых руд
Поскольку алюминий амфотерен, глинозем получают тремя способами:
- щелочным,
- кислотным;
- электролитическим.
Наибольшее распространение имеет щелочной способ (метод К. И. Байера, разработанный в России в конце позапрошлого столетия и применяемый для переработки высокосортных бокситов с небольшим количеством (до 5 – 6 %) кремнезема). С тех пор техническое выполнение его было существенно улучшено. Схема производства глинозема по способу Байера представлена на рисунке 3.
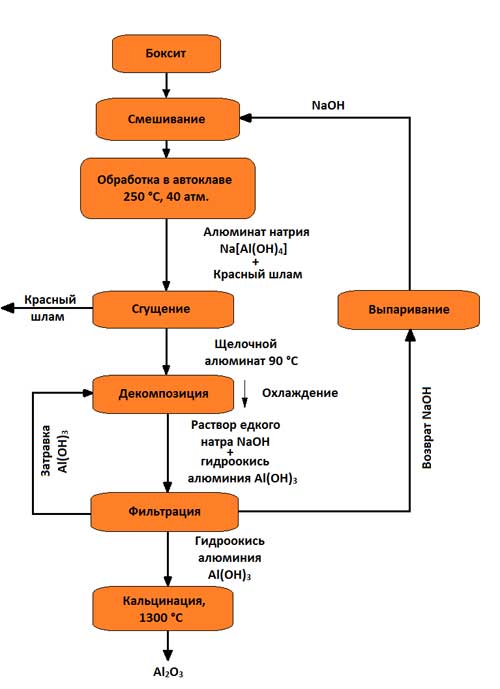
Рисунок 3 – Схема получения глинозема по способу Байера
Сущность способа состоит в том, что алюминиевые растворы быстро разлагаются при введении в них гидроокиси алюминия, а оставшийся от разложения раствор после его выпаривания в условиях интенсивного перемешивания при 169 – 170 °С может вновь растворять глинозем, содержащийся в бокситах. Этот способ состоит из следующих основных операций:
1. Подготовки боксита, заключающийся в его дроблении и измельчении в мельницах; в мельницы подают боксит, едкую щелочь и небольшое количество извести, которое улучшает выделение Al2O3; полученную пульпу подают на выщелачивание;
2. Выщелачивания боксита (в последнее время применяемые до сих пор блоки автоклав круглой формы частично заменены трубчатыми автоклавами, в которых при температурах 230 – 250 °С (500 – 520 К) происходит выщелачивание), заключающегося в химическом его разложении от взаимодействия с водным раствором щелочи; гидраты окиси алюминия при взаимодействии со щелочью переходят в раствор в виде алюмината натрия:
содержащийся в боксите кремнезем взаимодействует со щелочью и переходит в раствор в виде силиката натрия:
в растворе алюминат натрия и силикат натрия образуют нерастворимый натриевый алюмосиликат; в нерастворимый остаток переходят окислы титана и железа, предающие остатку красный цвет; этот остаток называют красным шламом. По окончании растворения полученный алюминат натрия разбавляют водным раствором щелочи при одновременном понижении температуры на 100 °С;
3. Отделения алюминатного раствора от красного шлама обычно осуществляемого путем промывки в специальных сгустителях; в результате этого красный шлам оседает, а алюминатный раствор сливают и затем фильтруют (осветляют). В ограниченных количествах шлам находит применение, например, как добавка к цементу. В зависимости от сорта бокситов на 1 т полученной окиси алюминия приходится 0,6 – 1,0 т красного шлама (сухого остатка);
4. Разложения алюминатного раствора. Его фильтруют и перекачивают в большие емкости с мешалками (декомпозеры). Из пересыщенного раствора при охлаждении на 60 °С (330 К) и постоянном перемешивании извлекается гидроокись алюминия Al(OH)3. Так как этот процесс протекает медленно и неравномерно, а формирование и рост кристаллов гидроокиси алюминия имеют большое значение при ее дальнейшей обработке, в декомпозеры добавляют большое количество твердой гидроокиси – затравки:
5. Выделения гидроокиси алюминия и ее классификации; это происходит в гидроциклонах и вакуум-фильтрах, где от алюминатного раствора выделяют осадок, содержащий 50 – 60 % частиц Al(OH)3. Значительную часть гидроокиси возвращают в процесс декомпозиции как затравочный материал, которая и остается в обороте в неизменных количествах. Остаток после промывки водой идет на кальцинацию; фильтрат также возвращается в оборот (после концентрации в выпарных аппаратах – для выщелачивания новых бокситов);
6. Обезвоживания гидроокиси алюминия (кальцинации); это завершающая операция производства глинозема; ее осуществляют в трубчатых вращающихся печах, а в последнее время также в печах с турбулентным движением материала при температуре 1150 – 1300 °С; сырая гидроокись алюминия, проходя через вращающуюся печь, высушивается и обезвоживается; при нагреве происходят последовательно следующие структурные превращения:
200 °C – 950 °С – 1200 °С.
В окончательно прокаленном глиноземе содержится 30 – 50 % α-Al2O3 (корунд), остальное γ-Al2O2.
Этим способом извлекается 85 – 87 % от всего получаемого глинозема. Полученная окись алюминия представляет собой прочное химическое соединение с температурой плавления 2050 ° С [7].
Получение алюминия электролизом
Электролитическое восстановление окиси алюминия, растворенной в расплаве на основе криолита, осуществляется при 950-970 °С в электролизере. Электролизер состоит из футерованной углеродистыми блоками ванны, к подине которой подводится электрический ток. Выделившийся на подине, служащей катодом, жидкий алюминий тяжелее расплава соли электролита, поэтому собирается на угольном основании, откуда его периодически откачивают (рисунок 4). Сверху в электролит погружены угольные аноды, которые сгорают в атмосфере выделяющегося из окиси алюминия кислорода, выделяя окись углерода (CO) или двуокись углерода (CO2). На практике находят применение два типа анодов:

Рисунок 4 – Схема электролизера
Сила тока на электролизерах составляет 150 000 А. Они включаются в сеть последовательно, т. е. получается система (серия) – длинный ряд электролизеров.
Рабочее напряжение на ванне, составляющее 4 – 5 В, значительно выше напряжения, при котором происходит разложение окиси алюминия, поскольку в процессе работы неизбежны потери напряжения в различных частях системы. Баланс сырья и энергии при получении 1 т алюминия представлен на рисунке 5.
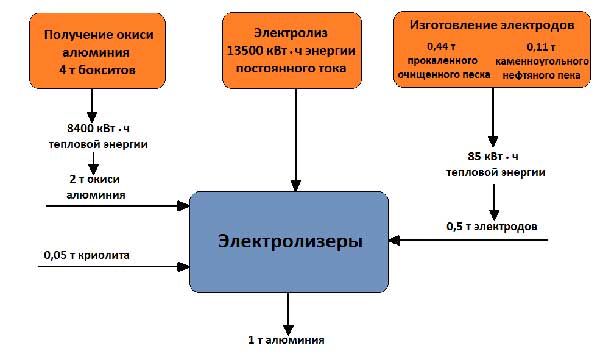
Рисунок 5 – Баланс сырья и энергии при получении 1 т алюминия
Вреакционном сосуде окись алюминия превращается сначала в хлорид алюминия. Затем в плотно изолированной ванне происходит электролиз AlCl3, растворенного в расплаве солей KCl, NaCl. Выделяющийся при этом хлор отсасывается и подается для вторичного использования; алюминий осаждается на катоде.
Преимуществами данного метода перед существующим электролизом жидкого криолитоглиноземного расплава (Al2O3, растворенная в криолите Na3AlF6) считают: экономию до 30 % энергии; возможность применения окиси алюминия, которая не годится для традиционного электролиза (например, Al2O3 с высоким содержанием кремния); замену дорогостоящего криолита более дешевыми солями; исчезновение опасности выделения фтора [7].
Получение рафинированного алюминия
Для алюминия рафинирующий электролиз с разложением водных солевых растворов невозможен. Поскольку для некоторых целей степень очистки промышленного алюминия (Al 99,5 – Al 99,8), полученного электролизом криолитоглиноземного расплава, недостаточна, то из промышленного алюминия или отходов металла путем рафинирования получают еще более чистый алюминий (Al 99,99 R). Наиболее известен метод рафинирования — трехслойный электролиз.
Рафинирование методом трехслойного электролиза
Одетая стальным листом, работающая на постоянном токе (рисунок 6) ванна для рафинирования состоит из угольной подины с токоподводами и теплоизолирующей магнезитовой футеровки. В противоположность электролизу криолитоглиноземного расплава анодом здесь служит, как правило, расплавленный рафинируемый металл (нижний анодный слой). Электролит составляется из чистых фторидов или смеси хлорида бария и фторидов алюминия и натрия (средний слой). Алюминий, растворяющийся из анодного слоя в электролите, выделяется над электролитом (верхний катодный слой). Чистый металл служит катодом. Подвод тока к катодному слою осуществляется графитовым электродом.

Рисунок 6 - Схема электролизера с передним горном для рафинирования алюминия (по Фульда - Гинзбергу)
1 – алюминиевый расплав; 2 – электролит; 3 – рафинированный алюминий высокой частоты; 4 – катод из графита; 5 – магнезитовая стена; 6 – передний горн; 7 – изолирующий слой; 8 – боковая изоляция; 9 – угольная подина; 10 – анодный токопровод; 11 – изоляция подины; 12 – железный короб; 13 – крышка
Ванна работает при 750 – 800 °С, расход электроэнергии составляет 20 кВт ч на 1 кг чистого алюминия, т. е. несколько выше, чем при обычном электролизе алюминия.
Металл анода содержит 25 – 35 % Cu; 7 – 12 % Zn; 6 – 9 % Si; до 5 % Fe и незначительное количество марганца, никеля, свинца и олова, остальное (40 – 55 %) – алюминий. Все тяжелые металлы и кремний при рафинировании остаются в анодном слое. Наличие магния в электролите приводит к нежелательным изменениям состава электролита или к сильному его ошлакованию. Для очистки от магния шлаки, содержащие магний, обрабатывают флюсами или газообразным хлором.
В результате рафинирования получают чистый алюминий (99,99 %) и продукты сегрегации (зайгер-продукт), которые содержат тяжелые металлы и кремний и выделяются в виде щелочного раствора и кристаллического остатка. Щелочной раствор является отходом, а твердый остаток применяется для раскисления.
Рафинированный алюминий имеет обычно следующий состав, %: Fe 0,0005 – 0,002; Si 0,002 – 0,005; Cu 0,0005 – 0,002; Zn 0,0005 – 0,002; Mg следы; Al остальное.
Рафинированный алюминий перерабатывают в полуфабрикат в указанном составе или легируют магнием (таблица 1).
Таблица 1 – Химический состав алюминия повышенной чистоты и первичного алюминия по DIN 1712, лист 1
Читайте также:

