Биосинтез пиримидиновых нуклеотидов кратко
Обновлено: 04.07.2024
А. Образование пиримидиновых нуклеотидов de novo
В отличие от синтеза пуринов, где формирование гетероциклического основания осуществляется на остатке рибозо-5-фосфата, пиримидиновое кольцо синтезируется из простых предшественников: глутамина, СО2 и аспарагиновой кислоты и затем связывается с рибозо-5-фосфатом, полученным от ФРДФ.
Процесс протекает в цитозоле клеток. Синтез ключевого пиримидинового нуклеотида — УМФ идёт с участием 3 ферментов, 2 из которых полифункциональны.
У млекопитающих ключевой, регуляторной реакцией в синтезе пиримидиновых нуклеотидов является синтез карбамоилфосфата из глутамина, СО2 и АТФ, в реакции катализируемой карбамоилфосфатсинтетазой II (КФС II), которая протекает в цитозоле клеток (рис. 10-12). В реакции NH2-rpynna карбамоилфосфата образуется за счёт амидной группы глутамина, что отличает эту реакцию от реакции синтеза карбамоилфосфата в митохондриях в процессе синтеза мочевины из СО2, NH3и АТФ с участием КФС I.
Рис. 10-12. Синтез карбамоилфосфата.

Рис. 10-13. Биосинтез УМФ de novo.

Отщепляясь от КАД-фермента, дигидрооротат подвергается дегидрированию NAD-зaвиcимой дигидрооротатдегидрогеназой и превращается в свободное пиримидиновое основание — оротовую кислоту, или оротат.
В цитозоле оротат становится субстратом бифункционального фермента — УМФ-синтазы, которая обнаруживает оротатфосфорибозилтрансферазную и ОМФ-декарбоксилазную активности. Первоначально фосфорибозильный остаток от ФРДФ переносится на оротат и образуется нуклеотид — оротидин-5'-монофосфат (ОМФ), декарбоксилирование которого даёт уридин-5-мо- нофосфат (УМФ).
Таким образом, шесть последовательных реакций синтеза пиримидиновых нуклеотидов осуществляются тремя ферментами, которые кодируются в геноме человека тремя различными структурными генами.
Биосинтез УДФ, УТФ и цитидиловых нуклеотидов
УМФ под действием специфических нуклеозидмонофосфат (НМФ) и нуклеозиддифосфат (НДФ) киназ превращается в УДФ и УТФ в результате переноса у-фосфатного остатка АТФ на соответствующий субстрат.
НМФ-киназа катализирует следующую реакцию:
УМФ + АТФ —> УДФ + АДФ,
УДФ + АТФ —> УТФ + АДФ.
ЦТФ синтетаза катализирует амидирование УТФ (рис. 10-14), осуществляя АТФ-зависимое замещение кетогруппы урацила на амидную группу глутамина с образованием цитидин-5'-трифосфата (ЦТФ).
Рис. 10-14. Синтез ЦТФ из УТФ.

Б. ‹Запасные› пути синтеза пиримидиновых нуклеотидов
Использование пиримидиновых оснований и нуклеозцдов в реакциях реутилизации препятствует катаболизму этих соединений до конечных продуктов с расщеплением пиримидинового кольца. В ресинтезе пиримидинов участвуют некоторые ферменты катаболизма нуклеотидов. Так, уридинфосфорилаза в обратимой реакции может рибозилировать урацил с образованием уридина.
Урацил + Рибозо-1-фосфат —> Уридин + Н3РО4.
Превращение нуклеозидов в нуклеотиды катализирует уридин-цитидинкиназа.
Часть ЦМФ может превращаться в УМФ под действием цитидиндезаминазы и пополнять запасы уридиловых нуклеотидов.
В. Регуляция синтеза пиримидиновых нуклеотидов
Регуляторным ферментом в синтезе пиримидиновых нуклеотидов является полифункциональный КАД-фермент. УМФ и пуриновые нуклеотиды аллостерически ингибируют, а ФРДФ активирует его карбамоилсинтетазную активность, тогда как активность аспартаттранскарбамоилазного домена ингибирует ЦТФ, но активирует АТФ (рис. 10-15).
Рис. 10-15. Регуляция синтеза пиримидиновых нуклеотидов. КАД-фермент катализирует реакции 1,2, 3; дигидрооротатдегидрогеназа — реакцию 4; УМФ синтетаза — реакции 5 и 6; НМФ киназа — реакцию 7; НДФ киназа — реакцию 8; ЦТФ синтетаза — реацию 9.

Этот способ регуляции позволяет предотвратить избыточный синтез не только УМФ, но и всех других пиримидиновых нуклеотидов и обеспечить сбалансированное образование всех четырёх основных пуриновых и пиримидиновых нуклеотидов, необходимых для синтеза РНК.
Биологическая библиотека - материалы для студентов, учителей, учеников и их родителей.
Наш сайт не претендует на авторство размещенных материалов. Мы только конвертируем в удобный формат материалы, которые находятся в открытом доступе и присланные нашими посетителями.
Если вы являетесь обладателем авторского права на любой размещенный у нас материал и намерены удалить его или получить ссылки на место коммерческого размещения материалов, обратитесь для согласования к администратору сайта.
Разрешается копировать материалы с обязательной гипертекстовой ссылкой на сайт, будьте благодарными мы затратили много усилий чтобы привести информацию в удобный вид.
Синтез пиримидиновых оснований происходит во всех клетках организма. В реакциях синтеза участвует аспарагиновая кислота, глутамин, СО2, затрачивается 2 молекулы АТФ. В отличие от разветвленного синтеза пуринов этот синтез происходит линейно, т.е. пиримидиновые нуклеотиды образуются последовательно, друг за другом.
Условно можно выделить 3 общих этапа синтеза и реакции синтеза УТФ и ЦТФ:
1. Образование карбамоилфосфата
Образование карбамоилфосфата в отличие от синтеза мочевины происходит в цитозоле большинства клеток организма.
2. Образование пиримидинового кольца
Формирование пиримидинового кольца происходит после присоединения аспартата и реакций дегидратации и окисления. Первым пиримидиновым основанием является оротовая кислота .
3. Синтез оротидинмонофосфата и уридинмонофосфорной кислоты
В реакции с фосфорибозилдифосфатом (ФРДФ) к оротовой кислоте присоединяется рибозо-5-фосфат и образуется оротидилмонофосфат, при декарбоксилировании превращающийся в уридинмонофосфат (УМФ).
Источником фосфорибозилдифосфата является первая из двух реакций синтеза фосфорибозиламина при образовании пуринов.
Синтез уридинмонофосфата
4. Синтез уридинтрифосфата
Синтез УТФ осуществляется из УМФ в 2 стадии посредством переноса макроэргических фосфатных групп от АТФ.
Синтез УТФ
5. Синтез цитидинтрифосфата
Образование цитидинтрифосфата (ЦТФ) происходит из УТФ с затратой энергии АТФ при участии глутамина, являющегося донором NH2-группы.
Механизм синтеза пиримидиновых нуклеотидов почти полностью расшифрован благодаря исследованиям П. Рейхарда. Показано, что в клетках животных и в микроорганизмах конечными продуктами синтеза также не являются свободные пиримидиновые основания и остаток рибозы присоединяется к уже сформировавшемуся пиримидиновому кольцу. Синтез начинается с элементарных уровней (СО2, NH3, аспартат), и специфическую ключевую роль выполняет оротовая кислота.
Последовательность химических реакций синтеза пиримидиновых нуклеотидов, в частности УМФ, можно представить в следующем виде:
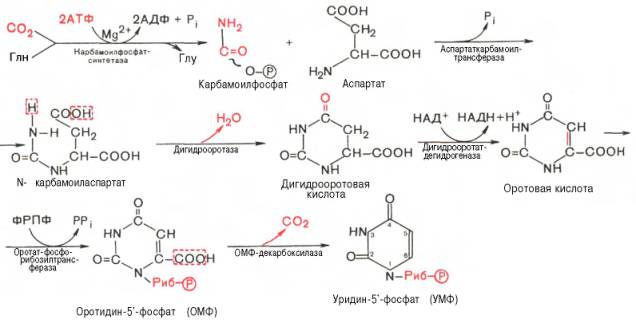
Как видно, I стадия синтеза УМФ включает катализируемое цито-плазматической карбамоилфосфатсинтетазой образование карбамоилфос-фата из глутамина (см. главу 12).
На II стадии карбамоилфосфат реагирует с аспартатом, в результате чего образуется N-карбамоиласпарагиновая кислота. Последняя подвергается циклизации (под действием дигидрооротазы) с отщеплением молекулы воды, при этом образуется дигидрооротовая кислота, которая, подвергаясь дегидрированию, превращается в оротовую кислоту. В этой реакции участвует специфический НАД-содержащий фермент дигидро-оротатдегидрогеназа. Оротовая кислота обратимо реагирует с ФРПФ, являющимся донатором рибозо-фосфата, с образованием оротидин-5'-фос-фата (ОМФ). Декарбоксилирование последнего приводит к образованию первого пиримидинового нуклеотида – уридин-5-фосфата (УМФ).
Превращение УМФ в УДФ и УТФ осуществляется, как и пуриновых нуклеотидов, путем фосфотрансферазных реакций:
Биосинтез цитидиловых нуклеотидов. Предшественником цитидиловых нуклеотидов является УТФ, который превращается в ЦТФ:
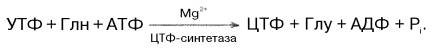
У прокариот в этой реакции используется преимущественно свободный аммиак, в то время как в клетках животных ЦТФ-синтетаза катализирует включение амидной группы глутамина в 4-е положение пиримидинового кольца УТФ. Следует отметить, что образующийся ЦТФ служит отрицательным эффектором регуляторного аллостерического фермента ас-партаткарбамоилтрансферазы, ингибируя по типу обратной связи начальную стадию биосинтеза пиридиновых нуклеотидов. АТФ предотвращает это ингибирование.
Биосинтез тимидиловых нуклеотидов. Тимидиловые нуклеотиды входят в состав ДНК, содержащей дезоксирибозу. Поэтому сначала рассмотрим механизмы синтеза дезоксирибонуклеотидов. При помощи метода меченых атомов было показано, что этот синтез начинается не со свободной дезоксирибозы, а путем прямого восстановления рибонуклеотидов у 2'-го атома углерода. При инкубации меченых предшественников (рибонуклео-тидов) в бесклеточной системе бактерий метку обнаружили в составе дезоксирибонуклеотидов. По данным П. Рейхарда, у Е. coli все 4 рибо-нуклеозиддифосфата восстанавливаются в соответствующие дезоксиана-логи: dАДФ, dГДФ, dЦДФ, dУДФ – при участии сложной ферментной системы, состоящей по меньшей мере из четырех разных ферментов.
Химический смысл превращения рибонуклеотидов в дезоксирибо-нуклеотиды сводится к элементарному акту – восстановлению рибозы в 2-дезоксирибозу, требующему наличия двух атомов водорода. Непосредственным источником последних оказался восстановленный термостабильный белок тиоредоксин, содержащий две свободные SH-группы на 108 аминокислотных остатков. Тиоредоксин легко окисляется, превращаясь в дисульфидную S-S-форму. Для его восстановления в системе имеется специфический ФАД-содержащий фермент тиоредоксинредуктаза (мол. масса 68000), требующая наличия восстановленного НАДФН. Обозначив условно рибонуклеозиддифосфат РДФ, образование дезоксирибонуклеотидов можно представить следующим образом:
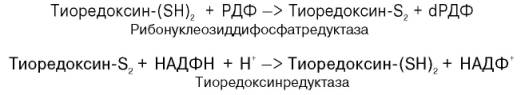
Обе стадии могут быть представлены в виде схемы:
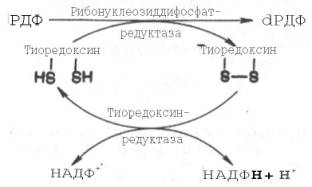
Для синтеза тимидиловых нуклеотидов, помимо дезоксирибозы, требуется также метилированное производное урацила – тимин. Оказалось, что в клетках имеется особый фермент тимидилатсинтаза, катализирующая метилирование не свободного урацила, а dУМФ; реакция протекает по уравнению:
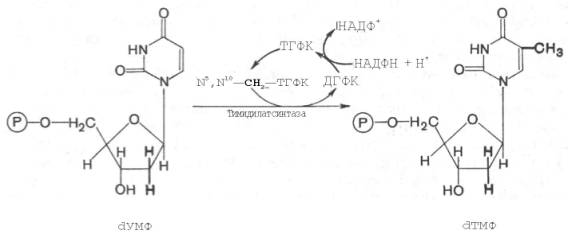
Донором метильной группы в тимидилатсинтазной реакции является N 5 ,N 10 -метилен-ТГФК, которая одновременно отдает и водородный протон, поэтому одним из конечных продуктов реакции является не тетра-гидро-, а дигидрофолиевая кислота (ДГФК). Последняя вновь восстанавливается до ТГФК под действием НАДФН-зависимой дигидрофолат-редуктазы. Из образовавшегося ТМФ путем фосфотрансферазных реакций образуются dТДФ и dTТФ.
Регенерация N 5 ,N 10 –СН2–ТГФК, собственно ее биосинтез, представляет определенный интерес. Оказалось, что этот синтез требует участия аминокислоты серина (донатор метильной группы) и пиридоксальфосфат-содержащего фермента сериноксиметилтрансферазы в соответствии с уравнением:
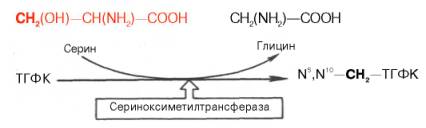
Синтез всех остальных дезоксирибонуклеозид-5'-трифосфатов, непосредственно участвующих в синтезе ДНК, также осуществляется путем фосфорилирования дезоксирибонуклеозид-5'-дифосфатов в присутствии АТФ:
АТФ + dАДФ –> АДФ + dATФ; АТФ + dЦДФ –> АДФ + dЦТФ;
АТФ + dГДФ –> АДФ + dГТФ; АТФ + dТДФ –> АДФ + dТТФ.
Далее на двух схемах суммированы данные о взаимопревращениях пуриновых и пиримидиновых нуклеотидов, а также о связи их с синтезом нуклеиновых кислот. Как видно из схем, в образовании пуриновых и пиримидиновых нуклеотидов специфическое участие принимает ФРПФ, являющийся донором фосфорибозильного остатка в биосинтезе как оро-тидин-5'-фосфата, так и ИМФ; последние считаются ключевыми субстратами в синтезе нуклеиновых кислот в клетках.
5.4.1. Структура пиримидинового ядра проще, чем структура пуринового, и путь биосинтеза его короче.
Главное отличие от биосинтеза пуринов заключается в том, что сборка пиримидинового ядра не требует участия фосфорибозилпирофосфата (ФРПФ). Пиримидиновая структура сначала образуется, а потом взаимодействует с ФРПФ с образованием нуклеотидов.
Предшественниками атомов углерода и азота пиримидинового кольца являются СО2 и аминокислоты глутамин и аспартат (рисунок 5.6).

Рисунок 5.6. Происхождение атомов пиримидинового ядра.
5.4.2. При взаимодействии СО2 и глутамина образуется карбамоилфосфат. Реакция протекает в цитозоле с затратой АТФ.

Следует напомнить, что карбамоилфосфат также образуется в процессе синтеза мочевины, но эта реакция происходит только в митохондриях печени и катализируется другим ферментом.
Карбамоилфосфатсинтетаза, участвующая в биосинтезе пиримидинов, - аллостерический фермент, он ингибируется УТФ, пуриновыми нуклеотидами, активируется ФРПФ.
5.4.3. Следующая реакция биосинтеза пиримидинов – образование карбамоиласпартата. Реакцию катализирует аспартат-транскарбамоилаза (АТК-аза).

АТК-аза – аллостерический фермент, его ингибитором является цитидинтрифосфат (ЦТФ) – конечный продукт биосинтеза пиримидиновых нуклеотидов.
Дальнейший путь образования пиримидиновых нуклеотидов представлен на рисунке 5.7.

Рисунок 5.7. Схема синтеза пиримидиновых нуклеотидов.
5.5. Особенности биосинтеза дезоксирибонуклеотидов
5.5.1. Дезоксирибонуклеотиды входят в состав ДНК. Содержание дезоксирибонуклеотидов в клетке обычно низкое и повышается только перед репликацией ДНК.
Дезоксирибонуклеотиды образуются в результате восстановления рибонуклеотидов. Эта реакция катализируется рибонуклеотидредуктазой (рисунок 5.8).

Рисунок 5.8. Схема образования дезоксирибонуклеотидов.
В процессе восстановления рибонуклеозиддифосфатов окисляется донор электронов – тиоредоксин. Окисленный тиоредоксин восстанавливается тиоредоксинредуктазой за счёт восстановленного НАДФ.
5.5.2. Тимидинмонофосфат образуется из дезоксиуридинмонофосфата при участии фермента тимидилатсинтазы. Источником метильной группы в реакции служит 5,10-метилен-тетрагидрофолиевая кислота (5,10-метилен-ТГФК), которая окисляется до дигидрофолиевой. Тетрагидрофолиевая кислота регенерируется дигидрофолатредуктазой в реакции, которая требует участия НАДФН. Образование 5,10-метилен-ТГФК происходит в реакции ТГФК с серином или глицином (см. тему 3).

Рисунок 5.9. Схема образования тимидилового нуклеотида.
5.6. Нарушения обмена нуклеотидов.
5.6.1. При нарушениях пуринового обмена часто наблюдается гиперурикемия – повышение содержания мочевой кислоты в крови. Гиперурикемия может быть первичной или вторичной.
Первичная гиперурикемия является ведущим симптомом подагры – полиэтиологического заболевания, как правило, наследственной природы. Гиперурикемия при подагре обусловлена главным образом, избыточным образованием образованием мочевой кислоты, а также снижением её экскреции с мочой. Значительная и длительная гиперурикемия сопровождается отложением солей мочевой кислоты в хрящевой ткани, сухожилиях и слизистых сумках суставов. Накопление кристаллов уратов в тканях может вызывать резкую воспалительную реакцию (подагрический артрит), что приводит впоследствии к деформации сустава. Избыток мочевой кислоты способствует также образованию уратных камней в нижних отделах мочевыводящих путей.
Повышение уровня мочевой кислоты в крови отмечается также при наследственных дефектах некоторых ферментов:
Синдром Леша-Нихана (полное отсутствие ГГФРТ) наследуется как сцепленный с Х-хромосомой рецессивный признак. Болезнь характеризуется параличом, сопровождающимся судорогами, стремлением к членовредительству и тяжёлой гиперурикемией. Вследствие ферментативного дефекта нарушается переход гуанина и гипоксантина в ГМФ и ИМФ соответственно и указанные пуриновые основания превращаются в мочевую кислоту. Кроме того, повышенная концентрация ФРПФ способствует усилению синтеза пуринов de novo. Биохимическая основа неврологических отклонений при синдроме Леша-Нихана неизвестна.
Гликогеноз I типа или болезнь Гирке (дефицит глюкозо-6-фосфатазы) сопровождается повышением активности пентозофосфатного пути и приводит к повышению внутриклеточного уровня рибозо-5-фосфата, из которого синтезируется ФРПФ. Повышенный уровень ФРПФ приводит к увеличению синтеза пуринов de novo. Для данного заболевания характерен также лактатный ацидоз, приводящий к повышению порога секреции уратов почками; это способствует накоплению уратов в организме.
Вторичная гиперурикемия сопутствует заболеваниям, сопровождающимся усиленным распадом клеток (лейкозы, серповидно-клеточная анемия, сахарный диабет, псориаз).
5.6.2. Реже встречается гипоурикемия – снижение содержания мочевой кислоты в крови. Она может быть связана с понижением реабсорбции уратов из клубочкового фильтрата в почках. В этом случае наблюдается увеличение экскреции мочевой кислоты с мочой.
Гипоурикемия развивается и при недостаточности ксантиноксидазы, возникающей при генетическом дефекте фермента или при тяжёлом поражении печени. Это состояние сопровождается повышенной экскрецией гипоксантина и ксантина (ксантинурией), а также образованием в почках ксантиновых камней.
5.6.3. Описаны два иммунодефицитных заболевания, связанные с недостаточностью ферментов метаболизма пуринов. Недостаточность аденозиндезаминазы сопровождается снижением количества и нарушением функции как тимусных лимфоцитов (Т-клеток), так и лимфоцитов костного мозга (В-клеток). При недостаточности пуриннуклеозид-фосфорилазы функции В-клеток остаются нормальными, но значительно нарушаются функции Т-клеток. Метаболические нарушения при данных заболеваниях связаны с накоплением дезоксирибонуклеозидтрифосфатов (дГТФ и дАТФ), которые аллостерически ингибируют рибонуклеотидредуктазу. Это, в свою очередь, приводит к снижению содержания в Т-лимфоцитах предшественников синтеза ДНК, главным образом дЦТФ. Таким образом, Т-клетки размножаться не могут.
Структура пиримидинового кольца проще, и путь биосинтеза пиримидинов короче, чем у пуринов. Амидный азот глутамина и диоксид углерода обеспечивает атомы 2 и 3 кольца пиримидина после преобразования их в карбамоилфосфат. Другие четыре атома кольца происходят из аспартата. Так же как и в случае с пуриновыми нуклеотидами, углеводная часть поставляется ФРПФ.
Карбамоилфосфат.Образование пиримидиновых нуклеотидов начинается с синтеза карбамоил фосфата, который протекает в цитозоле тканей, способных к образованию пиримидинов (наиболее высокая активность синтеза в селезенке, тимусе, ЖКТ и яичках).
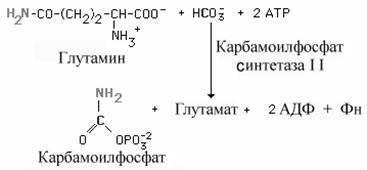 |
Карбамоил фосфат, как упоминалось в главе об обмене аминокислот, используется также в синтезе мочевины.
Его образование в клетках катализируется двумя разными карбамоилфосфат синтетазами - I и II.Основные различия между ними приведены в таблице 9-3.
| Сравнительная характеристика карбомоилфосфат синтетаз I и II | ||
| Карбамоил фосфат синтетаза I | Карбамоил фосфат синтетаза II | |
| Распределение в тканях | Преимущественно печень | Во всех тканях |
| Клеточная локализация | Митохондрия | Цитозоль |
| Метаболический путь | Синтез мочевины | Биосинтез пиримидинов |
| Источник азота | Ионы аммония | Аминогруппа глутамина |
Карбамоилфосфат синтетаза II (КФС II) предпочитает амид глутамина свободному аммиаку и не требует N-ацетилглутамата в качестве косубстрата. У человекаn КФСII, аспартат-транскарбамоилазная, и дигидрооротазная активности - это части одного мультифункционального белка.
Образование оротовой кислоты. Ключевая реакция.Первая уникальная для биосинтеза пиримидинов реакция – это реакция конденсации карбамоилфосфата и аспартата с образованием карбамоиласпартата, катализируемая аспартаттранскарбамоилазой (реакция
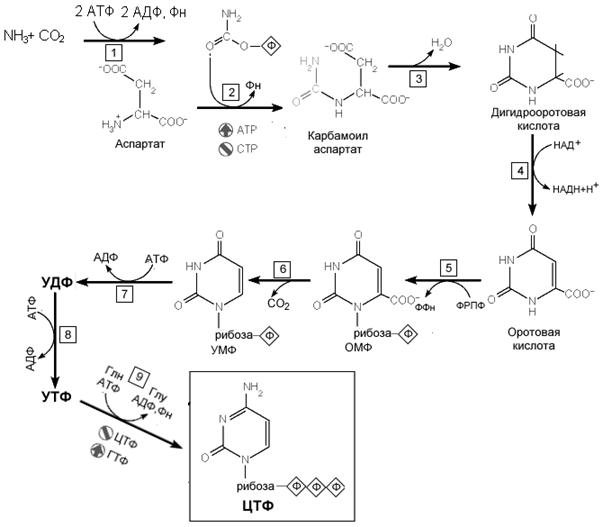
2). Затем дигидрооротаза катализирует отщепление Н2О с образованием кольцевой структуры (реакция -3). Дегидрогеназа дигидрооротата, используя НАД + в качестве кофермента, формирует оротовую кислоту - основного предшественника пиримидиновых
. Реакции синтеза пиримидиновых нуклеотидов
оснований (реакция 4).
Образование нуклеотидов. Образование мононуклеотида происходит в реакции 5 путем присоединения к оротовой кислоте остатка рибоза-5-фосфата. Донором моносахарида служит ФРПФ. Первый пиримидиновый мононуклеотид - оротидинмонофосфат (ОМР). Эта реакция катализируется оротат-фосфорибозилтрансферазой — ферментом, аналогичным гипоксантин-гуанин— фосфорибозилрансферазе и аденин-фосфорибозил трансферазе, которые участвуют в фосфорибозилировании пуриновых колец при их реутилизации.
Первый главный пиримидиновый рибонуклеотид - уридиловая кислота (уридинмонофосфат, УМФ) образуется путем декарбоксилирования оротидилата (реакция б). Дигидрооротатдегидрогеназа — митохондриальный фермент. Все остальные ферменты, участвующие в синтезе пиримидинов de novo, локализуются в цитозоле. УМФ подвергается двукратному янием аминоимидазолилрибозилфосфатсинтетазы
участвующие в синтезе пиримидинов de novo, локализуются в цитозоле. УМФ подвергается двукратному фосфорилированию и образующийся УТФ аминируется с участием глутамина и АТФ и образованием ЦТФ (реакция 9).
Регуляция синтеза пиримидиновых нуклеотидовКлючевым ферментом синтеза пиримидиновых нуклеотидов у человека является цитоплазматическая КФС II. УТФ тормозит активность этого фермента, конкурируя с ATФ. ФРПФ является активатором этого фермента. Имеются и другие участки регуляции (например, OMФ декарбоксилаза ингибируется УМФ и ЦМФ). Однако при нормальных условиях эти участки имеют ограниченное значение. У бактерий ключевым регуляторным ферментом является аспартат транскарбомоилаза. У них имеется только одна карбомоилфосфат синтетаза, так как они не имеют митохондрий. Карбомоилфосфат, таким образом, находится на развилке метаболических путей, которая ведет или к образованию пиримидиновых нуклеотидов или к синтезу аргинина.
Суммарная сравнительная характеристика путей синтеза пуриновых и пиримидиновых нуклеотидов приводится в следующей таблице.
| Таблица 9-5. Сравнительная характеристика путей синтеза пуриновых и пиримидиновых нуклеотидов | ||
| Путь синтеза пуринов | Путь синтеза пиримидинов | |
| Последовательность синтеза | 1.Образование N-гликозидной связи 2.Сборка кольцевой структуры | 1.Сборка кольцевой структуры 2.Образование N-гликозидной связи |
| Ключевая реакция | Образование фосфорибозилами на(фосфорибозиамидотрансфераза) | Образование карбамоилфос фата (Аспартат транскарба моилаза) |
| Локализация в клетке | Цитозоль | Митохондрии и цитозоль |
| Ферментгная орнганизация | Отдельные ферменты и полифункциональные (3) | Отдельные ферменты и полифункциональные (2) |
| Регуляция | Торможение ИМФ,АМФ и ГМФ вна нескольких уровнях | Торможение УТФ карбамоилфосфатсинтетазы II |
Структура пиримидинового кольца проще, и путь биосинтеза пиримидинов короче, чем у пуринов. Амидный азот глутамина и диоксид углерода обеспечивает атомы 2 и 3 кольца пиримидина после преобразования их в карбамоилфосфат. Другие четыре атома кольца происходят из аспартата. Так же как и в случае с пуриновыми нуклеотидами, углеводная часть поставляется ФРПФ.

Карбамоилфосфат.Образование пиримидиновых нуклеотидов начинается с синтеза карбамоил фосфата, который протекает в цитозоле тканей, способных к образованию пиримидинов (наиболее высокая активность синтеза в селезенке, тимусе, ЖКТ и яичках).
 |
Карбамоил фосфат, как упоминалось в главе об обмене аминокислот, используется также в синтезе мочевины.
Его образование в клетках катализируется двумя разными карбамоилфосфат синтетазами - I и II.Основные различия между ними приведены в таблице 9-3.
| Сравнительная характеристика карбомоилфосфат синтетаз I и II | ||
| Карбамоил фосфат синтетаза I | Карбамоил фосфат синтетаза II | |
| Распределение в тканях | Преимущественно печень | Во всех тканях |
| Клеточная локализация | Митохондрия | Цитозоль |
| Метаболический путь | Синтез мочевины | Биосинтез пиримидинов |
| Источник азота | Ионы аммония | Аминогруппа глутамина |
Карбамоилфосфат синтетаза II (КФС II) предпочитает амид глутамина свободному аммиаку и не требует N-ацетилглутамата в качестве косубстрата. У человекаn КФСII, аспартат-транскарбамоилазная, и дигидрооротазная активности - это части одного мультифункционального белка.
Образование оротовой кислоты. Ключевая реакция.Первая уникальная для биосинтеза пиримидинов реакция – это реакция конденсации карбамоилфосфата и аспартата с образованием карбамоиласпартата, катализируемая аспартаттранскарбамоилазой (реакция

2). Затем дигидрооротаза катализирует отщепление Н2О с образованием кольцевой структуры (реакция -3). Дегидрогеназа дигидрооротата, используя НАД + в качестве кофермента, формирует оротовую кислоту - основного предшественника пиримидиновых
. Реакции синтеза пиримидиновых нуклеотидов
оснований (реакция 4).
Образование нуклеотидов. Образование мононуклеотида происходит в реакции 5 путем присоединения к оротовой кислоте остатка рибоза-5-фосфата. Донором моносахарида служит ФРПФ. Первый пиримидиновый мононуклеотид - оротидинмонофосфат (ОМР). Эта реакция катализируется оротат-фосфорибозилтрансферазой — ферментом, аналогичным гипоксантин-гуанин— фосфорибозилрансферазе и аденин-фосфорибозил трансферазе, которые участвуют в фосфорибозилировании пуриновых колец при их реутилизации.
Первый главный пиримидиновый рибонуклеотид - уридиловая кислота (уридинмонофосфат, УМФ) образуется путем декарбоксилирования оротидилата (реакция б). Дигидрооротатдегидрогеназа — митохондриальный фермент. Все остальные ферменты, участвующие в синтезе пиримидинов de novo, локализуются в цитозоле. УМФ подвергается двукратному янием аминоимидазолилрибозилфосфатсинтетазы
участвующие в синтезе пиримидинов de novo, локализуются в цитозоле. УМФ подвергается двукратному фосфорилированию и образующийся УТФ аминируется с участием глутамина и АТФ и образованием ЦТФ (реакция 9).
Регуляция синтеза пиримидиновых нуклеотидовКлючевым ферментом синтеза пиримидиновых нуклеотидов у человека является цитоплазматическая КФС II. УТФ тормозит активность этого фермента, конкурируя с ATФ. ФРПФ является активатором этого фермента. Имеются и другие участки регуляции (например, OMФ декарбоксилаза ингибируется УМФ и ЦМФ). Однако при нормальных условиях эти участки имеют ограниченное значение. У бактерий ключевым регуляторным ферментом является аспартат транскарбомоилаза. У них имеется только одна карбомоилфосфат синтетаза, так как они не имеют митохондрий. Карбомоилфосфат, таким образом, находится на развилке метаболических путей, которая ведет или к образованию пиримидиновых нуклеотидов или к синтезу аргинина.
Суммарная сравнительная характеристика путей синтеза пуриновых и пиримидиновых нуклеотидов приводится в следующей таблице.
Читайте также:

