Свойства растворов электролитов конспект
Обновлено: 07.07.2024
· Обеспечить развития умений и навыков учащихся составлять ионные уравнения химических реакций, выражения констант диссоциации слабых электролитов, решать задачи по определению водородного показателя водных растворов;
· Содействовать развитию чувства ответственности учащихся через использование заданий из различных вариантов КИМов.
1. Организация начала учебного занятия.
1.1.Приветствие, организация внимания учащихся.
1.2.Психологическая подготовка учащихся к плодотворной работе на уроке.
- Еще раз напомним себе, что растворы электролитов широко применяются , во-первых, в различных сферах деятельности человека. Во-вторых, они имеют большое значение для живых организмов, т. к. питательные вещества усваиваются именно в виде растворов. В-третьих, сложные физико-химические процессы в организмах также протекают в растворах. В-четвертых, растворами являются физиологические жидкости – плазма крови, лимфа, желудочный сок и т. д.
Но прежде, чем идти дальше, сначала вспомним некоторые аспекты из уже изученного материала:
- работа у доски (карточки):
1. Напишите выражения констант равновесия для обратимых процессов и определите условия (t, C (О2), P), при которых химическое равновесие смещается в сторону продуктов реакции:

2. Выберите из перечня веществ: H2SO4, KCl, Al(OH)3, H2S, Na2SO4, LiOH, H2CO3, C2H5OH, Zn(OH)2, HNO3, CH4, CH3COOH, СаО формулы слабых электролитов и напишите для них (составляя уравнения диссоциации выбранных веществ по первой ступени) выражения констант диссоциации (Кд1).

С помощью этого видеоурока учащиеся вспомнят основные свойства кислот, оснований, солей в свете теории электролитической диссоциации.
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Свойства растворов электролитов"
Исследуем электропроводность уксусной кислоты.
Уксусная кислота – слабый электролит, поэтому электропроводность невысокая. При разбавлении раствора водой электропроводность увеличивается.
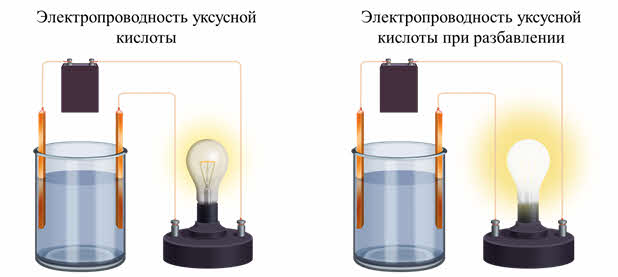
Как же изменяется электропроводность раствора при увеличении концентрации? Например, при растворении хлорида натрия в воде ионы двигаются хаотично, при увеличении концентрации раствора ионов становится больше. Движение ионов становится затруднённым, поэтому электропроводность уменьшается.

Свойства электролитов – это свойства образующих их ионов.
А если вещества имеют одни и те же ионы? Сходны ли они по свойствам?
Раствор каждого вещества обладает определёнными свойствами. Обычно, в растворах электролитов преобладают ионы, на которые диссоциируют электролиты, поэтому свойства растворов – это свойства данных ионов.
В растворах кислот всегда присутствуют гидратированные ионы водорода.

Общие свойства щелочей определяют гидроксид-ионы.

При смешивании щёлочи и кислоты получим соль. Свойства растворов солей обусловлены катионами металлов и анионами кислотных остатков.

Кислоты – это электролиты, при диссоциации которых в качестве катионов образуются только катионы водороды.
Составим уравнение электролитической диссоциации азотной, серной и сернистой кислоты. Азотная и серная кислоты являются сильными электролитами, поэтому они диссоциируют полностью с образованием катионов водорода и анионов кислотных остатков.

Сернистая кислота – двухосновная кислота и является слабым электролитом, поэтому диссоциирует ступенчато.

Число ступеней диссоциации зависит от основности кислоты. У сернистой кислоты будет две ступени диссоциации. Первая ступень диссоциации – отщепление одного иона водорода. На второй ступени диссоциации идёт отщепление иона водорода от сложного гидрокарбоната иона.

Обнаружить ионы водорода в растворах кислот можно с помощью индикаторов. Лакмус в растворах кислот меняет фиолетовый цвет на красный, метилоранж оранжевый цвет – на красный.

Кислоты вступают в химические реакции с металлами, стоящими в ряду активности до водорода. Например, в реакции цинка с соляной кислотой образуется соль – хлорид цинка и водород.

Кислоты реагируют с основными оксидами с образованием солей и воды. Так, в реакции серной кислоты с оксидом меди два образуется соль – сульфат меди два и вода.
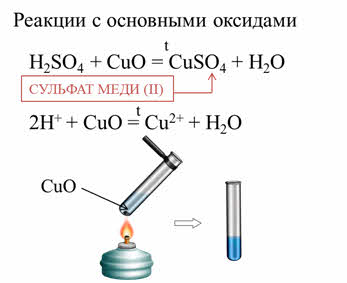
Кислоты реагируют с основаниями. В реакции соляной кислоты со щёлочью – гидроксидом калия образуется соль – хлорид калия и вода.
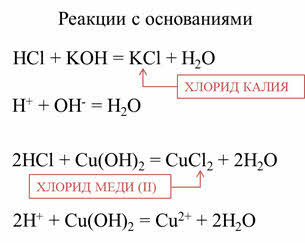
В реакции соляной кислоты с гидроксидом меди два образуется соль – хлорид меди два и вода.
Кислоты также реагируют с солями, образованными более слабыми кислотами. Например, в реакции соляной кислоты с карбонатом натрия образуется соль – хлорид натрия, углекислый газ и вода.

Таким образом, свойства кислот обусловлены наличием в их растворах катионов водорода.
Основания – это электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы.
Составим уравнение электролитической диссоциации гидроксида калия и гидроксида кальция. Эти вещества являются сильными электролитами и дисоциируют полностью по одной ступени. При диссоциации этих оснований образуются катионы металлов и гидроксид-ионы.

Слабые многокислотные основания диссоциируют ступенчато и число ступеней диссоциации определяется кислотностью слабого основания.

Так, у слабого двухкислотного основания гидроксида железа два две ступени диссоциации. На первой ступени отщепляется один гидроксид-ион, а на второй ступени отщепляется гидроксид-ион от сложного катиона.

Присутствие растворимых оснований – щелочей в растворах обнаруживается при помощи индикаторов.
Фенолфталеин в растворах щелочей малиновый, лакмус – синий, а метиловый оранжевый – жёлтый.

Щёлочи – активные вещества. Они реагируют с кислотными оксидами. Так, в реакции гидроксида натрия с оксидом углерода четыре образуется соль – карбонат натрия и вода, в реакциях щелочей с кислотами образуется также соль и вода. Например, в реакции гидроксида натрия с соляной кислотой образуется соль – хлорид натрия и вода.
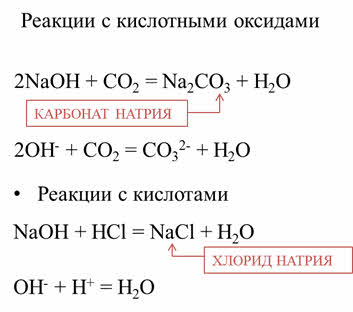
Щёлочи также реагируют с солями. Например, в реакции гидроксида калия с хлоридом меди два образуется нерастворимое основание – гидроксид меди два и соль – хлорид калия.

Таким образом, свойства щелочей обусловлены наличием в их растворах гидроксид-ионов.
Амфотэрные гидроксиды – это слабые электролиты, которые при диссоциации образуют одновременно катионы водорода и гидроксид-ионы, то есть они диссоциируют по типу кислоты и по типу основания.
К амфотэрным гидроксидам относятся гидроксид бериллия, гидроксид цинка, гидроксид олова два, гидроксид алюминия, гидроксид хрома три и другие.
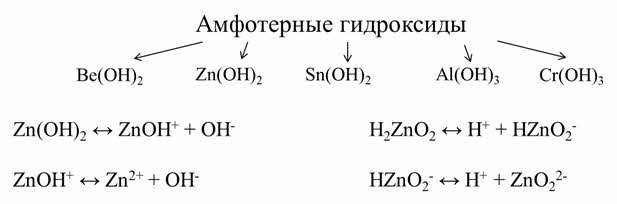
В амфотэрных гидроксидах имеются связи между атомами металла и кислорода и между атомами кислорода и водорода. Эти связи сравнимы по своей прочности. Поэтому может происходить как разрыв связей между металлом и кислородом с образованием гидроксид-ионов (это диссоциация по типу основания), так и разрыв связей между кислородом и водородом с образованием катионов водорода (это диссоциация по типу кислоты).
Соли – это электролиты, при диссоциации которых образуются катионы металлов и анионы кислотных остатков.
Средние соли – сильные электролиты, образующие при диссоциации катионы металла и анионы кислотного остатка. Например, при диссоциации карбоната калия образуются катионы калия и карбонат-ионы, при диссоциации сульфата алюминия образуются катионы алюминия и сульфат-ионы.

Кислые соли – сильные электролиты, диссоциирующие на катион металла и сложный анион, в состав которого входят атомы водорода и кислотный остаток.

Так, при диссоциации гидрокарбоната натрия на первой ступени образуется катион натрия и гидрокарбонат-ион, на второй ступени гидрокарбонат-ион частично диссоциирует на катион водорода и карбонат-ион.
Основные соли – это электролиты, которые при диссоциации образуют анионы кислотного остатка и сложного катиона, состоящего из атомов металла и гидроксогруппы.
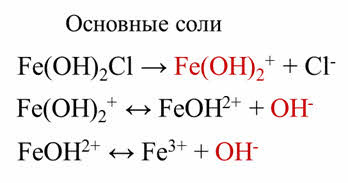
Например, при диссоциации дигидроксохлорида железа три на первой ступени диссоциации образуется сложный катион и хлорид-ион. Затем сложный катион частично диссоциирует с образование гидроксид-иона.
Свойства солей обусловлены способностью катионов металлов и анионов кислотных остатков связываться с ионами, противоположными по заряду, с образованием осадков, то есть нерастворимых солей и оснований или более слабых кислот.
Соли реагируют с металлами более активными, чем металлы, образующие соли. Так, в реакции сульфата меди два с железом образуется соль – сульфат железа два и медь.

Соли также реагируют с кислотами, которые являются более сильными, чем те, которые входят в состав соли. Например, в реакции карбоната калия с азотной кислотой образуется соль – нитрат калия, углекислый газ и вода.

Соли реагируют с другими солями. При этом в реакцию должны вступать две растворимые соли. Так, в реакции хлорида бария с сульфатом натрия образуется соль – сульфат бария в виде осадка и соль – хлорид натрия.

Соли реагируют и со щелочами. Например, в реакции хлорида железа три и гидроксида натрия образуется осадок – гидроксид железа три и соль – хлорид натрия.

Таким образом, свойства солей обусловлены наличием в их растворах катионов металлов и анионов кислотных остатков, их образующих.
Следовательно, свойства растворов электролитов обусловлены ионами, образующимися при их диссоциации. Свойства кислот обусловлены ионами водорода, образующимися при диссоциации кислот, свойства оснований обусловлены гидроксид-ионами, а свойства солей обусловлены катионами металла и анионами кислотного остатка, которые образуются при диссоциации солей.

Урок обобщения знаний по теме "Свойства растворов электролитов" с мультимедийным сопровождением. Урок ориентирован на обобщение, систематизацию и углубление знаний учащихся об электролитической диссоциации, электролитах, о свойствах водных растворов.Тип урока-комбинированный. Вид урока- проблемно-исследовательский. В ходе урока прослеживается закрепление умений и навыков химического эксперимента, умение работать с таблицами, справочными материалами, дополнительной литературой.
"Свойства растворов электролитов"
Урок обобщения знаний с мультимедийным сопровождением.(слайд 1)
- обобщить, систематизировать и углубить знания учащихся об электролитической диссоциации, электролитах, об их свойствах водных растворов;
- закрепить умение учащихся определять принадлежность веществ к сильным или слабым электролитам, записывать уравнения реакций между электролитами;
- развивать мышление учащихся, научить их делать логические выводы из наблюдений;
- закрепить умения и навыки химического эксперимента, умение работать с таблицами, справочными материалами, дополнительной литературой, опорными конспектами;
- подготовка учащихся к единому государственному экзамену.
Тип урока: комбинированный.
Вид урока: проблемно-исследовательский.
Оборудование: учебник О.С.Габриеляна "Химия. 11 класс. Профильный уровень", таблица растворимости, индикаторная шкала, штатив с пробирками, растворы индикаторов, сульфата меди (2), хлорида бария, гидроксида натрия, нитрата серебра, серной кислоты, карбонат кальция, сульфат магния, соляная кислота, сульфат железа(2), йодид калия, хлорид железа(3), ортофосфат натрия.
1. Вводная часть
Учитель: Сегодня у нас немного необычный урок, у нас присутствуют гости, которые видели вас в 5 и 6 классах умными, любознательными, интересующимися и хотят видеть такими и сейчас.
Тема нашего урока "Свойства растворов электролитов". Сегодня вы покажете, что знаете и чему научились при изучении данной темы. На прошлых уроках мы познакомились с одной из величайших теорий, на которую опирается химическая наука - электролитическая диссоциация. ТЭД широко и плодотворно применяется для объяснения многообразных физических и химических явлений в растворах, установления между ними тесной связи. Она, по словам Аррениуса, "оказалась применимой и полезной во всех областях современной науки".
Целями нашего урока являются: (зачитать цели) (слайд 2)
Учитель: Так как вам осталось всего полгода до окончания школы и поступления в ВУЗы, то я вас разделила на 3 группы, согласно трем ступеням высшего образования: магистры, специалисты, бакалавры.
Я вам раздаю инструктивные карты, в которых даны вопросы и задания на которые будет отвечать ваша группа, а лидер распределит, кто именно.
Итак, мы начинаем:
1.Фронтальный опрос:
1.Кто является основоположником теории электролитической диссоциации?
(слайд 3) Информация о С. Аррениусе
2.Какие ученые внесли свой вклад в развитие теории электролитической диссоциации?
3.Какой процесс называется электролитической диссоциацией?
4.Какие вещества называются электролитами?
5.Давайте вспомним основные положения ТЭД.
2.Работа с группами
1.При диссоциации каких веществ образуются только катионы водорода? -магистры
2.При диссоциации каких веществ образуются только анионы гидроксогруппы? - специалисты
3.При диссоциации каких веществ образуются катионы металла и анионы кислотного остатка? - бакалавры
4.Чем определяются химические свойства растворов электролитов? - магистры
5.Какие виды химических связей характерны для молекул электролитов? -специалисты
6.Дать понятие степени электролитической диссоциации. Какое значение может приобретать степень ЭД? -бакалавры
7.Слабым электролитом является:
1)HF 2)HCl 3)HBr 4)HI
8.Вещество, которое не является электролитом:
(слайд 7)
9.Сильным электролитом в водном растворе является
10.Какие электролиты являются сильными? -магистры
11.Какие электролиты являются слабыми? - специалисты
12.Как влияет константа диссоциации на силу электролита? -бакалавры
13.Ионы I - образуются при диссоциации
(слайд 9)
14.В качестве анионов только ионы ОН - образуются при диссоциации
15.Вещество, при диссоциации которого образуются катионы Na + , H + , а также анионы SO4 2- , являются
1)кислотой 2)щелочью 3)средней солью 4)кислой солью
16.Дать характеристику воды, как слабого электролита. -магистры
17.Что такое ионное произведение воды? -специалисты
18.Чем можно охарактеризовать среду водного раствора? -магистры
19.Сколько типов сред растворов различают? -бакалавры
20.Чем характеризуется нейтральная среда растворов? -бакалавры
21.Чем характеризуется кислотная среда растворов? -магистры
22.Чем характеризуется щелочная среда растворов? -специалисты
23.Какой показатель используется для характеристики среды раствора? -специалисты
24.Как на практике определяется среда раствора? - магистры
Эксперимент. Техника безопасности при работе с кислотами и щелочами.
В трёх пробирках даны растворы кислоты, щёлочи и воды. Определить с помощью индикаторов, в какой пробирке находится каждый раствор.
3. Выполнение заданий части Б единого государственного экзамена.
1.Установите соответствие между солью и реакцией среды её в водном растворе

Электролиты – это вещества, растворы и расплавы которых проводят электрический ток.
Электрический ток – это упорядоченное движение заряженных частиц под действием электрического поля. Таким образом, в растворах или расплавах электролитов есть заряженные частицы. В растворах электролитов, как правило, электрическая проводимость обусловлена наличием ионов.
Ионы – это заряженные частицы (атомы или группы атомов). Разделяют положительно заряженные ионы (катионы) и отрицательно заряженные ионы (анионы).
Электролитическая диссоциация — это процесс распада электролита на ионы при его растворении или плавлении.
Разделяют вещества — электролиты и неэлектролиты. К неэлектролитам относятся вещества с прочной ковалентной неполярной связью (простые вещества), все оксиды (которые химически не взаимодействуют с водой), большинство органических веществ (кроме полярных соединений — карбоновых кислот, их солей, фенолов) — альдегиды, кетоны, углеводороды, углеводы.
К электролитам относят некоторые вещества с ковалентной полярной связью и вещества с ионной кристаллической решеткой.
В чем же суть процесса электролитической диссоциации?
Поместим в пробирку несколько кристаллов хлорида натрия и добавим воду. Через некоторое время кристаллы растворятся. Что произошло?
Хлорид натрия – вещество с ионной кристаллической решеткой. Кристалл NaCl состоит из ионов Na + и Cl — . В воде этот кристалл распадается на структурные единицы-ионы. При этом распадаются ионные химические связи и некоторые водородные связи между молекулами воды. Попавшие в воду ионы Na + и Cl — вступают во взаимодействие с молекулами воды. В случае хлорид-ионов можно говорить про электростатическое притяжение дипольных (полярных) молекул воды к аниону хлора, а в случае катионов натрия оно приближается по своей природе к донорно-акцепторному (когда электронная пара атома кислорода помещается на вакантные орбитали иона натрия). Окруженные молекулами воды ионы покрываются гидратной оболочкой. Диссоциация хлорида натрия описывается уравнением:
NaCl = Na + + Cl –

При растворении в воде соединений с ковалентной полярной связью, молекулы воды, окружив полярную молекулу, сначала растягивают связь в ней, увеличивая её полярность, затем разрывают её на ионы, которые гидратируются и равномерно распределяются в растворе. Например, соляная ксилота диссоциирует на ионы так: HCl = H + + Cl — .

При расплавлении, когда происходит нагревание кристалла, ионы начинают совершать интенсивные колебания в узлах кристаллической решётки, в результате чего она разрушается, образуется расплав, который состоит из ионов.
Процесс электролитической диссоциации характеризуется величиной степени диссоциации молекул вещества:
Степень диссоциации — это отношение числа продиссоциировавших (распавшихся) молекул к общему числу молекул электролита. Т.е., какая доля молекул исходного вещества распадается в растворе или расплаве на ионы.
Nпродисс — это число продиссоциировавших молекул,
Nисх — это исходное число молекул.
По степени диссоциации электролиты делят на делят на сильные и слабые.
Сильные электролиты (α≈1):
1. Все растворимые соли (в том числе соли органических кислот — ацетат калия CH3COOK, формиат натрия HCOONa и др.)
2. Сильные кислоты: HCl, HI, HBr, HNO3, H2SO4 (по первой ступени), HClO4 и др.;
3. Щелочи: NaOH, KOH, LiOH, RbOH, CsOH; Ca(OH)2, Sr(OH)2, Ba(OH)2.
Сильные электролиты распадаются на ионы практически полностью в водных растворах, но только в ненасыщенных. В насыщенных растворах даже сильные электролиты могут распадаться только частично. Т.е. степень диссоциации сильных электролитов α приблизительно равна 1 только для ненасыщенных растворов веществ. В насыщенных или концентрированны растворах степень диссоциации сильных электролитов может быть меньше или равна 1: α≤1.
Слабые электролиты (α
1. Слабые кислоты, в т.ч. органические;
2. Нерастворимые основания и гидроксид аммония NH4OH;
3. Нерастворимые и некоторые малорастворимые соли (в зависимости от растворимости).
Неэлектролиты:
1. Оксиды, не взаимодействующие с водой (взаимодействующие с водой оксиды при растворении в воде вступают в химическую реакцию с образованием гидроксидов);
2. Простые вещества;
3. Большинство органических веществ со слабополярными или неполярными связями (альдегиды, кетоны, углеводороды и т.д.).

Как диссоциируют вещества? По степени диссоциации различают сильные и слабые электролиты.
Сильные электролиты диссоциируют полностью (в насыщенных растворах), в одну ступень, все молекулы распадаются на ионы, практически необратимо. Обратите внимание — при диссоциации в растворе образуются только устойчивые ионы. Самые распространенные ионы можно найти в таблице растворимости — это ваша официальная шпаргалка на любом экзамене. Степень диссоциации сильных электролитов примерно равна 1. Например, при диссоциации фосфата натрия образуются ионы Na + и PO4 3– :
Диссоциация слабых электролитов : многоосновных кислот и многокислотных оснований происходит ступенчато и обратимо. Т.е. при диссоциации слабых электролитов распадается на ионы только очень небольшая часть исходных частиц. Например, угольная кислота:
HCO3 – ↔ H + + CO3 2–
Гидроксид магния диссоциирует также в 2 ступени:
Mg(OH)2 ⇄ Mg(OH) + OH –
Mg(OH) + ⇄ Mg 2+ + OH –
Кислые соли диссоциируют также ступенчато, сначала разрываются ионные связи, затем — ковалентные полярные. Например, гидрокабонат калия и гидроксохлорид магния:
KHCO3 ⇄ K + + HCO3 – (α=1)
HCO3 – ⇄ H + + CO3 2– (α + + Cl – (α=1)
MgOH + ⇄ Mg 2+ + OH – (α 1. При растворении в воде электролиты диссоциируют (распадаются) на ионы.
2. Причина диссоциации электролиты в воде – это его гидратация, т.е. взаимодействие с молекулами воды и разрыв химической связи в нем.
3. Под действием внешнего электрического поля положительно заряженные ионы двигаюися к положительно заряженному электроду — катоду, их называют катионами. Отрицательно заряженные электроны двигаются к отрицательному электроду – аноду. Их называют анионами.
4. Электролитическая диссоциация происходит обратимо для слабых электролитов, и практически необратимо для сильных электролитов.
5. Электролиты могут в разной степени диссоциировать на ионы — в зависимости от внешних условий, концентрации и природы электролита.
6. Химические свойства ионов отличаются от свойств простых веществ. Химические свойства растворов электролитов определяются свойствами тех ионов, которые из него образуются при диссоциации.
Примеры .
1. При неполной диссоциации 1 моль соли общее количество положительных и отрицательных ионов в растворе составило 3,4 моль. Формула соли – а) K2S б) Ba(ClO3)2 в) NH4NO3 г) Fe(NO3)3
Решение: для начала определим силу электролитов. Это легко можно сделать по таблице растворимости. Все соли, приведенные в ответах — растворимые, т.е. сильные электролиты. Далее, запишем уравнения электролитической диссоциации и по уравнению определим максимально число ионов в каждом растворе:
а) K2S ⇄ 2K + + S 2– , при полном распаде 1 моль соли образуется 3 моль ионов, больше 3 моль ионов не получится никак;
б) Ba(ClO3)2 ⇄ Ba 2+ + 2ClO3 – , опять при распаде 1 моль соли образуется 3 моль ионов, больше 3 моль ионов не образуется никак;
в) NH4NO3 ⇄ NH4 + + NO3 – , при распаде 1 моль нитрата аммония образуется 2 моль ионов максимально, больше 2 моль ионов не образуется никак;
г) Fe(NO3)3 ⇄ Fe 3+ + 3NO3 – , при полном распаде 1 моль нитрата железа (III) образуется 4 моль ионов. Следовательно, при неполном распаде 1 моль нитрата железа возможно образование меньшего числа ионов (неполный распад возможен в насыщенном растворе соли). Следовательно, вариант 4 нам подходит.
Читайте также:

