Мыла и синтетические моющие средства конспект
Обновлено: 06.07.2024
CH 2 -OH | CH-OH | CH 2 -OH CH 2 -O-CO-C 15 H 31 | CH-O-CO-C 15 H 31 | CH 2 -O-CO-C 15 H 31 C 17 H 35 СООNa CH 3 CH 2 COOCH 3 Найдите среди предложенных формул формулу мыла.
Вспомните, о каких недостатках мыла мы говорили с вами ранее? Какие виды пятен бывают на одежде? Когда человек начал использовать для своих нужд мыло?
Цели урока: Дать понятие о СМС и ПАВ, Рассмотреть их получение и механизм действия при стирке, Проанализировать влияние ПАВ и фосфатов на окружающую среду и здоровье человека. Синтетические моющие средства.
Первое СМС появилось только в 1916 году. Изобретение немецкого химика Фрица Понтера предназначалось только для промышленного использования. Бытовые СМС выпускаются с 1935 года, когда они стали менее вредными для кожи рук. 1. Понятие о СМС и моющем процессе. С тех пор разработан целый ряд СМС узкого назначения, а их производство – это важнейшая отрасль химической промышленности.
Не последнее место в списке бытовой химии занимают стиральные порошки. Стирка – самый трудоемкий процесс в нашем быту. А помощниками в стирке являются поверхностно-активные вещества (ПАВ).
Поверхностно-активные вещества - это органические соединения, содержащие в молекулах одновременно две противоположные по свойствам группы: полярную (гидрофильную) и неполярную (гидрофобную).
отрыв грязевых частиц от очищаемой поверхности, перевод нерастворимых в воде грязевых частиц в раствор, удержание этих плавающих частиц в моющем растворе, т.е. предотвращение ресорбции. Моющий процесс сводится к обеспечению 3 этапов:
1) получение сложного моноэфира серной кислоты и высшего спирта (например, цетилового) C 16 H 33 OH + H 2 SO 4 → цетиловый конц. спирт серная к-та → C 16 H 33 O-SO 2 -OH + H 2 O цетилсерная к-та 2. Основные этапы производства ПАВ.
2) нейтрализация полученного соединения щелочью C 16 H 33 O-SO 2 -OH + NaOH → → C 16 H 33 O-SO 2 -ONa + H 2 O натриевая соль цетилсерной к-ты
В целом производство ПАВ сводится к следующим этапам технологического процесса:
Лабораторный опыт. Цель опыта : изучить взаимодействие жесткой воды с растворами мыла и стирального порошка. Перед вами 2 пробирки: в одной – мыльный раствор, в другой – раствор стирального порошка, а в колбочке – жесткая вода. Прилейте небольшое количество жесткой воды к растворам мыла и СМС, закройте пробкой и встряхните. Что вы наблюдаете? Как это можно объяснить?
1) обладают в 10 раз большей моющей способностью, чем мыла, т.к. кислотный остаток серной кислоты лучше сорбируется частицами загрязнения, 2) не боятся жесткой и даже морской воды, т.к. кальциевые соли алкилсерной кислоты растворимы в воде. Характеристика ПАВ, используемых в СМС:
4. Компоненты стиральных порошков и их функции. Фосфаты - уменьшают жесткость воды и увеличивают эффективность стирки. Полимеры – предотвращают ресорбцию. Силикаты – дополнительно защищают от коррозии. Перборат натрия – отбеливает. Оптический отбеливатель - маскирует пятна. Энзимы - способствуют расщеплению белковых и жировых пятен на одежде.
5. Воздействие СМС на окружающую среду и организм человека. - ПАВ отрицательно влияют на качество подземных питьевых вод и само очищающую способность водоемов, на использующих эту воду флору и фауну, - водные растворы ПАВ дают стойкую пену, препятствуя аэрации и ухудшая тем самым биохимическую очистительную способность водоемов, - водные растворы ПАВ усиливают коррозию металлов, - проникая в организм, ПАВ способны вызвать грубые нарушения иммунитета, развитие аллергии, поражение мозга, печени, почек, легких, они способствуют возникновению злокачественных опухолей. ! ПАВ являются одними из наиболее распространенных загрязнителей объектов окружающей среды, прежде всего, водных ресурсов:
Например, в Германии, Италии, Австрии, Норвегии, Швейцарии и Нидерландах применение фосфатных порошков запрещено законом. Во Франции, Великобритании, Испании содержание фосфатов в СМС строго регламентировано (не более 12%). ! Попадая после стирки вместе со сточными водами в водоемы, фосфаты принимаются действовать как удобрения. Водоросли начинают расти с неимоверной силой. Это приводит не только к засорению водоемов, но и к дефициту воды и кислорода, а, следовательно, и к гибели гидробионтов. В стиральных порошках, кроме ПАВ, используются фосфаты. На Западе уже более 10 лет назад отказались от применения порошков, содержащих фосфатные добавки.
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
МЫЛА И СИНТЕТИЧЕСКИЕ МОЮЩИЕ СРЕДСТВА
Урок химии в 10 классе (повышенный уровень обучения)
по технологии проблемного обучения
Цели урока:
§ Создать условия для формирования у учащихся понятий о составе и строении мыла и синтетических моющих средств, сходстве и различии их моющих свойств, способах получения;
§ развивать исследовательские умения (наблюдать, сравнивать, анализировать, объяснять наблюдаемые явления, формулировать выводы), совершенствовать навыки проведения химического эксперимента;
§ способствовать воспитанию у учащихся экологической культуры, ответственного отношения к своему здоровью.
Форма урока: урок - исследование.
Оборудование и реактивы: персональный компьютер, мультимедийный проектор, экран, С D - R диск с записью аудио-видео файла (реклама
Опережающее домашнее задание:
группе исследователей: с помощью рекомендованной учителем литературы изучить механизмы моющего действие мыла и синтетических моющих средств;
группе аналитиков: проанализировать состав синтетических моющих средств, подготовить информацию о назначении входящих в них компонентов;
группе экологов: изучить вопрос об экологических проблемах, связанных с использованием синтетических моющих средств;
I . ВСТУПЛЕНИЕ (организация класса, актуализация знаний, создание соответствующего эмоционального настроения, определение целей урока).
Вступительное слово учителя.
План изучения темы:
1. Поверхностно-активные вещества (ПАВ), механизм моющего действия
мыла и синтетических моющих средств, их состав и строение.
2. Сравнительная характеристика свойств мыла и синтетических моющих
средств, их применение.
3. Качественное определение мыла.
4. Получение мыла и синтетических моющих средств.
5. Экологические проблемы, связанные с применением синтетических
II . ОСНОВНАЯ ЧАСТЬ (изучение нового материала).
1. Поверхностно-активные вещества (ПАВ), механизм моющего действия
мыла и синтетических моющих средств, их состав и строение.
Учитель сообщает учащимся, что основу всех моющих средств составляют поверхностно–активные вещества (ПАВ). Группе исследователей было поручено изучить литературу о ПАВ и выяснить, чем объясняется моющее действие мыла и синтетических моющих средств.
Выступление исследователей.
В настоящее время известно много различных ПАВ, входящих в состав синтетических моющих средств. По характеру гидрофильных и гидрофобных групп их можно разделить на три класса (слайд 4):
•Анионоактивные вещества при растворении диссоциируют на катионы и анионы, при этом носителем поверхностно-активных свойств является анион. Например: алкилсульфаты – соли сложных эфиров высших спиртов и серной кислоты СН3-(СН2)15-СН2-О- SO 2 - ONa ; алкилсульфонаты –соли сульфокислот СН3-(СН2)15-СН2- SO 2 - ONa и др.
• Катионоактивные вещества при растворении в воде также диссоциируют на ионы, но носителем поверхностно-активных свойств является катион. В основном это соли четырёхзамещённого аммония
При этом один из радикалов содержит 12-18 атомов углерода, а остальные – короткие радикалы (метил, этил).
• Неионогенные вещества, которые в водных растворах практически не диссоциируют на ионы. Например, R -(СН2-СН2 O ) n -СН2-СН2- OH – алкилполиэтиленгликоль.
Мыло, как моющее средство, известно человеку уже очень давно. Однако оно не было доступным всем людям. Моя бабушка была из бедной семьи, к тому же её родители рано умерли, и она осталась сиротой. Бабушка рассказывала, как стирали в бедных семьях. Для стирки использовали древесную золу. Вы все себе представляете золу?
С трудом верится, что с её помощью можно отстирать грязь, правда?
А давайте попробуем объяснить моющее действие золы. (Учащимся предлагается вспомнить, что является основным минеральным компонентом древесной золы. Это поташ - К2СО3. Учащиеся вспоминают, что карбонат калия подвергается гидролизу по аниону, создавая щелочную среду. В щелочной среде происходит гидролиз жиров и других органических веществ, создающих загрязнения. Продуктами их щелочного гидролиза являются соли жирных карбоновых кислот, т. е. образуется не что иное, как мыло).
Поверхностно-активные вещества - лишь компонент мыла и синтетических моющих средств, обуславливающий их моющее действие. А почему мыла и СМС бывают разного цвета, имеют разные запахи, разное назначение и так далее? Какие ещё вещества входят в состав моющих средств. Давайте послушаем ребят из группы аналитиков (слайд 5).
Выступление аналитиков.
Щелочные добавки (кальцинированная сода и силикаты) улучшают моющую способность СМС, так как частично расщепляют жиры.
Умягчители воды (триполифосфат натрия и др.) вводятся для устранения жёсткости воды.
Химические отбеливатели (перборат натрия, перкарбонат натрия и другие пероксидные соединения) отбеливают за счёт образования активного кислорода.
Оптические отбеливатели – флуоресцирующие вещества, которые оседают на ткани при стирке, при этом бельё приобретает яркость и белизну.
Энзимы (ферменты) вводятся для стирки белья с загрязнениями белкового характера (кровь, яичный белок, молоко и др.). Стабилизаторы пены используются при производстве СМС для ручной стирки.
Пеногасители , наоборот, добавляют в СМС для машинной стирки, так
как сильное пенообразование чревато поломкой машины.
Комплексоны используются с целью связывания катионов железа, магния, кальция, благодаря чему изделия сохраняют яркость красок.
Антиресорбенты вводятся для предотвращения повторного оседания загрязнений на белье.
Отдушки призваны придать моющему средству и белью приятный запах, это синтетические ароматизаторы.
2. Сравнительная характеристика свойств мыла и синтетических моющих средств, их применение.
На этом этапе урока учащиеся экспериментально исследуют свойства мыла и синтетических моющих средств. Результаты исследований заносятся в учебно-исследовательскую карту (приложение 1).
Лабораторный опыт 1.
Определение реакции среды ( рН) водных растворов мыла и синтетических моющих средств
Испытайте растворы мыла и синтетических моющих средств индикаторами фенолфталеином и лакмусом. Определите численное значение рН с помощью универсальной индикаторной бумаги. Данные эксперимента занесите в таблицу:

Конспект урока по химии разработан для 10 классов. Архив содержит презентацию, раздаточный материал.
— изучить состав, получение, свойства мыла и синтетических моющих средств, познакомить учащихся с историей мыла как необходимого компонента быта; прогнозировать моющие свойства СМС.
Развивающие:
— развитие ассоциативного и логического мышления, понятийного аппарата, экспериментальных умений и навыков, мотивирующего начала в процессе познания; выявление причинно-следственных связей; формирование практико-ориентированного направления познавательной деятельности.
Воспитательные:
— воспитание научно-материалистического мировоззрения; культуры пользования химическими препаратами в быту; экологическое воспитание.
Оборудование: мультимедийный проектор, экран, презентация, набор упаковок мыла разных сортов, упаковки синтетических моющих средств (СМС), емкости для замачивания, лоскутки ткани, раздаточный материал; тестовые задания.
Реактивы: раствор СМС, жесткая вода.
Тип урока: комбинированный урок
Формы работы учащихся: индивидуальная, фронтальная работа.
Организационный этап.
Актуализация знаний
Изучение нового материала
Закрепление знаний
Домашнее задание
1. Организационный этап.
- проверка готовности группы к уроку;
Здравствуйте ребята! Сегодня у нас с вами необычный урок – мы проведем соревнование, но не между вами. И чтоб познакомиться с участниками соревнований, предлагаю посмотреть небольшой видеоролик.
2. Мотивация.
Вот на этом и последующих уроках мы с вами и попытаемся дать ответы на эти вопросы.
Сейчас, чтоб не терять времени, я замочу образцы ткани, на которых предварительно были поставлены пятна от кетчупа, кофе и маркера. Мне нужно 4 помощника, которые помогут потереть пятна. Растворы с СМС приготовлены в соответствии с рекомендациями производителей. Обратите внимание, что образцы тканей кладутся в раствор, куда предварительно был насыпан и растворен порошок, а не порошок сыпется на ткань, как часто показывают в рекламных роликах. Почему именно такой порядок? На этот вопрос, надеюсь, вы сможете дать ответ в конце нашего урока.
3. Актуализация знаний. Фронтальный опрос. А пока идет стирка…(слайд 2)
1)Дайте определение бытовым химикатам? (Бытовые химикаты — это отдельные химические вещества, а чаще смеси веществ, которые используются в быту с определённым назначением.)
2)Как классифицируют бытовые химикаты по назначению(моющие, чистящие, универсальные, для ухода за мебелью, для уход за автомобилями, средства гигиены и косметики и т.д.)
3) Какие бывают бытовые химикаты по агрегатному состоянию?(жидкие и твердые)
4)Назовите основные правила обращения с бытовыми химикатами?
5) С чем связана жесткость воды?(с наличием ионов кальция и магния).Какая вода у нас в водопроводах?(жесткая). О жесткости мы вспомнили неслучайно, это нам пригодится для понимания действия мыла и синтетических моющих средств.
4. Изучение нового материала.
Перед изучением нового материала давайте еще раз обратим внимание на тему урока. …А теперь подумаем, на какие вопросы мы должны ответить в ходе изучения нового материала. (Что такое мыло? Как его получают, каков его химический состав, каким мылом пользоваться для умывания, каким для стирки? Какие бывают виды мыла? И зачем же мы покупаем стиральные порошки под названием СМС? Какова от них польза, а может быть от них больше вреда? Есть ли отличия между порошками? И т.д. )
Итак, давайте составим план, по которому будем работать.
Мыло – определение, состав.
СМС – определение, состав.
Механизм действия СМС.
Влияние СМС на окружающую среду и организм человека.
1) Мыло(слайд 3) Обратимся к этикетке от мыла и изучим состав. На первом месте стоят – натриевые соли масел и жиров. Обычные мыла состоят главным образом из смеси солей пальмитиновой, стеариновой и олеиновой кислот. Натриевые соли образуют твердые мыла, калиевые соли — жидкие мыла.
Мыло – натриевые или калиевые соли высших карбоновых кислот,
полученные в результате гидролиза жиров в щелочной среде.
Общая формула твердого мыла: R-COONa; жидкого мыла: R-COOK. Получают мыло (слайд4) в результате щелочного гидролиза жира: Основываясь на этой реакции, французский химик М.Э.Шеврёль поставил производство мыла на научную основу.

Основной состав любого твердого мыла одинаков. Это натриевые соли высших карбоновых кислот, обычно получаемых из жиров природного происхождения. Отличия заключаются в добавках, которые вносят в мыло в зависимости от его назначения. Основное назначение мыла – гигиеническое. Отрицательным свойством мыла является образование свободной щелочи при его растворении в воде. Щелочь эта может вызывать раздражение, шелушение, сухость кожи.
Обычно мыло утрачивает свою моющую способность в жёсткой воде, поскольку растворимые натриевые или калиевые соли высших карбоновых кислот выступают в обменную реакцию с растворимыми гидрокарбонатами щелочноземельных металлов, главным образом кальция:
2C 17 H 35 COONa + Ca(HCO 3 ) 2 (C 17 H 35 COO) 2 Ca + 2NaHCO 3 .
Решить эту проблему химикам удалось, синтезировав новые моющие вещества – СМС.(слайд 5). Еще в XIX веке русский химик Г.С. Петров действием серной кислоты на продукты переработки нефти получил синтетические моющие средства, которые прекрасно мылятся в жесткой воде.
2)СМС. Если мы рассмотрим и сравним этикетки различных стиральных порошков (слайд 6), то в общем сможем записать, что (слайд7)
СМС = ПАВ + добавки.
Поверхностно-активные вещества (ПАВ) являются основой всех СМС и отвечают собственно за отделение загрязнения от ткани.
Антиресорбенты (силикаты, КМЦ, триполифосфат натрия), чтобы частички грязи не оседали на ткань повторно.
Химические и оптические отбеливатели отвечают за белизну ткани.
Энзимы отвечают за удаление специфических загрязнений.
Смягчители воды (фосфаты, фосфонаты, цеолиты)
Если все это семейство веществ работает слаженно и на совесть, чистота ткани гарантирована.
3). Механизм действия стирального порошка.
Моющее средство должно успешно выполнять две функции: удаление частиц грязи с очищаемой поверхности и перенос их в раствор.
Первая будет взаимодействовать с поверхностью загрязненной ткани, а вторая – с водой; частицы грязи перейдут в водный раствор вместе с моющими веществами. Такие вещества и получили названия поверхностно-активных веществ (ПАВ) (слайд 9)

(слайд 10)Полярный конец обуславливает ее растворимость в воде, неполярный (углеводородный) затрудняет, тормозит это растворение и стремится вытеснить молекулу мыла из внутренних слоев воды на ее поверхность, то есть на границу ее раздела с воздухом, ибо воздух, являясь гидрофобным веществом, имеет средство к гидрофобной части молекулы мыла.
Обладая такими свойствами, молекулы ПАВ, растворяясь в воде, будут стремиться вытеснить молекулы воды из пограничного слоя и занять их место.

Расположение молекул ПАВ на поверхности воды
Таким образом, на поверхности водного раствора происходит так называемый процесс адсорбции - скопление полярных молекул ПАВ, где они, концентрируясь, образуют сплошное покрытие – адсорбционный слой, который как бы обволакивает поверхность воды. По существу на этой поверхности образуется слой нового вещества, имеющий меньшее поверхностное натяжение, чем вода. Следовательно, и поверхностное натяжение этого водного раствора соответственно понижается.
Растворение молекулы аниона ПАВ в грязном жире углеводородного конца
Таким образом, моющие способности стирального порошка определяются поверхностно-активными веществами.
Моющий процесс можно изобразить следующим образом:

а — грязевая частица на поверхности материала; б — адсорбция моющего вещества на частице грязи; в — отрыв частицы грязи от отмываемой поверхности; г — частица грязи в моющем растворе; д — пузырьки воздуха с адсорбированными молекулами моющего вещества (пена); Е — слипшиеся пузырьки пены и частицы грязи; ж — адсорбционный слой моющего раствора на границе раздела воздух — вода
Итак, ответьте теперь на вопрос, который мы ставили в начале урока? Почему сначала СМС растворяют, а потом замачивают и стирают ткань?
А сейчас пришло время подвести итог соревнований порошков. Сравним их эффективность воздействия на пятна от маркера, кофе томатной пасты и определим наиболее эффективное СМС.
Синтетические моющие средства (СМС¸ детергенты) – это жидкие, пастообразные и порошкообразные вещества, которые содержат поверхностно-активные вещества, а также другие органические и неорганические вещества, повышающие эффективность поверхностно-активных веществ.
Их производство основано на дешевой сырьевой базе – продуктах переработки нефти.
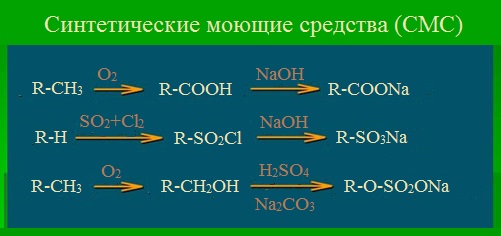
Синтетические моющие средства – натриевые соли синтетических кислот (сульфокислот — RSO3H), сложных эфиров высших спиртов и серной кислоты — алкилсульфаты — ROSO2OН).
Синтетические моющие средства в основном состоят из алкилсульфатных солей натрия RO-SO2-ONa.
Как синтетическое мыло, так и мыло, получаемое из жиров, плохо моет в жесткой воде. Взаимодействуя с ионами кальция и магния, которые содержатся в жесткой воде, мыла образуют нерастворимые кальциевые и магниевые соли:
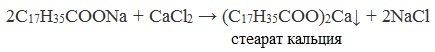
В результате этого мыло образует вместо пены пленку на поверхности воды и расходуется бесполезно.
Малорастворимые соли кальция и магния оседают на ткани, забивают поры, делают ткань грубой, менее эластичной, с плохой воздухо- и влагопроницаемостью. Такие ткани приобретают сероватый оттенок, а окраска становится блеклой. А осевшие на ткани известковые мыла приводят к снижению ее прочности.
Этого недостатка лишены синтетические моющие средства. Они характеризуются более высокой моющей способностью, доступностью сырья для их производства.
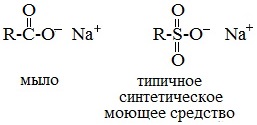
Алкилсульфаты — соли сложных эфиров высших спиртов и серной кислоты. В общем виде образование таких солей можно изобразить уравнениями:
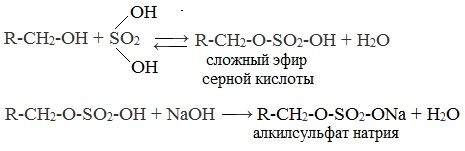
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках
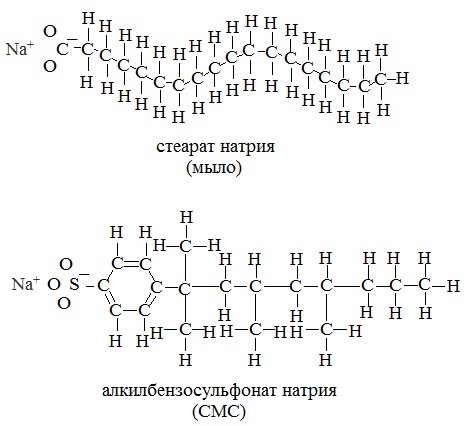
Распространенными синтетическими моющими средствами являются алкилбензолсульфонаты. Алкилбензолсульфонат натрия – основной компонент многих детергентов (стиральных порошков):
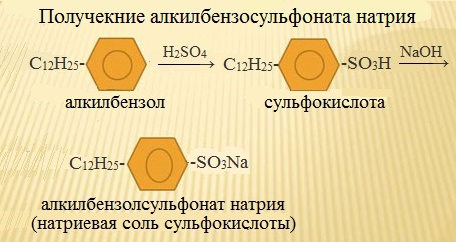
В отличие от нерастворимых стеаратов кальция и магния, которые образуются при стирке в жесткой воде и осаждаются на ткани, кальциевые и магниевые соли синтетических моющих средств растворимы в воде. Поэтому СМС моют как в мягкой, так и в жесткой воде, обладают высокой смачивающей способностью.
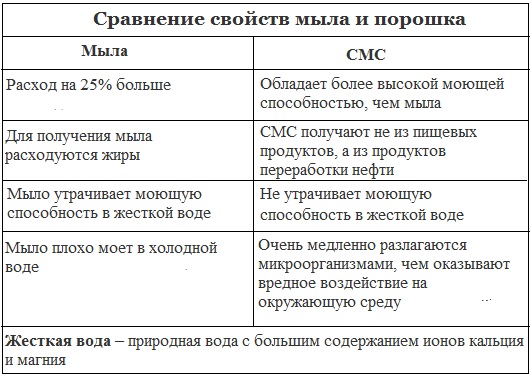
Расход СМС по сравнению с мылом гораздо меньше (около 25% мыла идет на связывание ионов кальция и магния).
Синтетические моющие средства высвобождают сотни тысяч тонн пищевого сырья – растительных масел и жиров.
Повсеместное использование СМС создает свои проблемы. СМС в отличие от мыла трудно поддаются биологическому разложению и, попадая со сточными водами в реки и озера, загрязняют окружающую среду и оказывают вредное воздействие на живые организмы.
Мыла, полученные из жиров, содержат неразветвленные углеводородные цепи, которые разрушаются бактериями. В то же время в состав некоторых СМС входят алкилсульфаты или алкил(арил)сульфонаты с углеводородными цепями, имеющими разветвленное или ароматическое строение. Такие соединения бактерии разрушить не могут.
Типичный стиральный порошок содержит приблизительно 70% синтетического моющего средства и около 30% неорганических фосфатов.
Фосфаты удаляют растворимые соли кальция. Но, эти фосфаты попадают в сточные воды. Загрязнение фосфатами рек, озер приводит к размножению зеленых и сине-зеленых водорослей (цветение воды), особенно в замкнутых водоемах. Зеленые растения поглощают кислород, содержащийся в воде, в результате чего происходит постепенная гибель водных растений и животных и их разложение.
Недостатки мыла и их устранение
1. Плохая моющая способность в жесткой воде, содержащей растворимые соли кальция и магния.
Взаимодействуя с ионами кальция и магния, которые содержатся в жесткой воде, мыла образуют нерастворимые кальциевые и магниевые соли. Для этого требуется большой расход мыла.
Способы устранения
В состав мыла вводят вещества-комплексообразователи, способствующие смягчению воды (натриевые соли этилендиамин-тетрауксусной кислоты – ЭДТА, ЭДТА-Na2, химическая формула — C10H14N2Na2O8
2. Мыло сушит кожу, способствует расщеплению кожного сала и его удалению, понижает защитную реакцию кожи (способствует проникновению болезнетворных бактерий).
В водных растворах мыло частично гидролизуется (взаимодействует с водой).
При этом образуется определенное количество щелочи, которая способствует расщеплению кожного сала и его удалению.
Калиевые соли высших карбоновых кислот (жидкое мыло) лучше растворяются в воде и поэтому обладают более сильным моющим действием.
Но в тоже время мыло оказывает вредное воздействие на кожу рук и тела.
Это связано с тем, что верхний тончайший слой кожи имеет слабокислую реакцию (рН =5,5) и за счет этого препятствует проникновению болезнетворных бактерий в более глубокие слои кожи.
Умывание мылом приводит к нарушению рН, (реакция становится слабощелочная), раскрываются поры кожи, что приводит к понижению естественной защитной реакции.
При слишком частом использовании мыла кожа сохнет, иногда воспаляется.
Способы устранения
Для уменьшения данного негативного воздействия в современные сорта мыла добавляют:
- слабые кислоты (лимонная кислота, борная кислота, бензойная кислота и др.), которые нормализуют рН
- глицерин, вазелиновое масло, пальмовое масло, кокосовое масло, диэтаноламиды кокосового и пальмового масел и т.д. для смягчения кожи и предотвращения попадания бактерий в поры кожи.
Эксперимент
Можно сравнить мыла и СМС (стиральный порошок) проверив с помощью индикаторов, какая среда характерна для наших моющих средств.
При добавлении лакмуса в раствор мыла и в раствор СМС он приобретает синий цвет, а фенолфталеин – малиновый, то есть реакция среды щелочная. Кстати, если моющее средство предназначено для стирки хлопчатобумажных тканей, то реакция среды должна быть щелочной, а если для шелковых и шерстяных тканей – нейтральной.
А что происходит с мылом и СМС в жесткой воде?
Добавим в одну пробирку раствор мыла, а в другую раствор СМС, взболтаем их. Что вы наблюдаете? В эти же пробирки добавим хлорид кальция и взболтаем содержимое пробирок. Что вы наблюдаете теперь? Раствор СМС пенится, а в растворе мыла образуются нерастворимые соли:
Читайте также:

