Конспект 8 класс по химии 28 параграф
Обновлено: 07.07.2024
Химия – это наука о веществах, их свойствах, превращениях веществ и явлениях, сопровождающих эти превращения.
Химия 8 класс
Первоначальные химические понятия. Кислород. Горение. Водород. Вода. Растворы. Количественные отношения в химии. Важнейшие классы неорганических соединений. Периодический закон и строение атома. Строение вещества. Химическая связь.
Химия 9 класс
Электролитическая диссоциация. Кислород и сера. Азот и фосфор. Углерод и кремний. Общие свойства металлов. Металлы IA—IIIA-групп периодической таблицы химических элементов. Железо. Металлургия. Краткий обзор важнейших органических веществ (Углеводороды, производные углеводородов).
Справочники для ОГЭ
Специальные конспекты по химии, в которых в сжатой форме повторяются основные школьные темы, для экспресс-подготовки к Основному Государственному Экзамену по химии.
Химия 10 класс
Химия 11 класс
Справочники для ЕГЭ
Специальные конспекты по химии, в которых в сжатой форме повторяются основные школьные темы, для экспресс-подготовки к Единому Государственному Экзамену по химии.
Решения задач по химии
Источники идей и источники цитат для конспектов по Химии:
(с) Цитаты из вышеуказанных учебных пособий использованы на сайте в незначительных объемах, исключительно в учебных и информационных целях (пп. 1 п. 1 ст. 1274 ГК РФ).
Конспекты по химии 8 класс собраны по порядку на этой странице. Они помогут вам наглядно показать учебный материал на своих уроках, а ученик с их помощью сможет самостоятельно изучить любую тему урока по видео или конспекту. Это готовые материалы для учителя химии, которые можно удобно использовать на каждом своем уроке.

21. Кислоты
Химия 8 класс

22. Соли
Химия 8 класс

23. Кристаллические решетки
Химия 8 класс

24. Чистые вещества и смеси
Химия 8 класс
25. Физические явления
Химия 8 класс
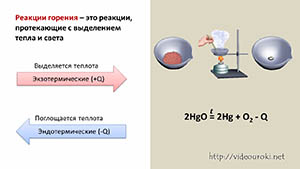
26. Химические явления. Закон сохранения массы веществ
Химия 8 класс

27. Химические уравнения
Химия 8 класс
28. Реакции разложения
Химия 8 класс
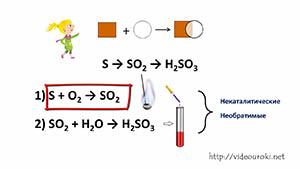
29. Реакции соединения
Химия 8 класс
30. Реакции замещения
Химия 8 класс

Получайте новое первыми










Лицензия на право ведения образовательной деятельности №5251 от 25.08.2017 г.
Закон сохранения массы веществ, открытый М. В. Ломоносовым в 1748 г., гласит:
| масса веществ, вступивших в химическую реакцию, равна массе веществ, получившихся в результате её. |
Материальными носителями массы веществ являются атомы химических элементов, из которых состоят как вступившие в реакцию вещества (реагенты), так и образовавшиеся в результате её новые вещества (продукты реакции). Поскольку при химических реакциях атомы не образуются и не разрушаются, а происходит лишь их перегруппировка, то становится очевидным справедливость открытого М. В. Ломоносовым и подтверждённого позднее А. Лавуазье закона.
В справедливости закона сохранения массы веществ можно легко убедиться на простом опыте. Поместим в колбу немного красного фосфора, закроем её пробкой и взвесим на весах (рис. 96). Затем колбу осторожно нагреем. О том, что произошла химическая реакция, можно определить по появлению в колбе густого белого дыма, состоящего из оксида фосфора (V), который образовался при взаимодействии фосфора с кислородом. При повторном взвешивании колбы с продуктами этой реакции мы убедимся, что масса веществ в колбе не изменилась, хотя и произошло превращение фосфора в его оксид.

Рис. 96.
Экспериментальная проверка закона сохранения массы веществ:
а — взвешивание колбы с фосфором до реакции; б — горение фосфора в закрытой колбе; в — взвешивание колбы с продуктом реакции
Этот же вывод будет нами сделан и при проведении ещё одного простого, но очень наглядного опыта. В специальный сосуд нальём отдельно соляную кислоту и раствор щёлочи, например гидроксида натрия (рис. 97). К раствору щёлочи добавим несколько капель индикатора — фенолфталеина, отчего раствор окрасится в малиновый цвет. Закроем прибор пробкой, уравновесим гирями на весах, отметим массу, а затем сольём растворы. Малиновая окраска исчезнет, потому что кислота и щёлочь прореагировали друг с другом. Масса же сосуда с полученными продуктами реакции не изменилась.

Рис. 97.
Опыт, подтверждающий закон сохранения массы вещества
На основании этого закона пишут химические предложения, т. е. составляют уравнения химических реакций с помощью химических слов — формул.
| Химическим уравнением называют условную запись химической реакции с помощью химических формул и математических знаков. |
Запишем, например, уравнение реакции водорода с кислородом. Сначала составим схему реакции — укажем формулы веществ, вступающих в реакцию (водород Н2 и кислород O2) и образующихся в результате её (вода Н2O), и соединим их стрелкой:

Рис. 98.
Составление уравнения реакции взаимодействия водорода и кислорода
Так как число атомов кислорода в левой части вдвое больше, чем в правой, запишем перед формулой воды коэффициент 2:
Но теперь в правой части уравнения стало четыре атома водорода, а в левой их осталось два. Чтобы уравнять число атомов водорода, запишем перед его формулой в левой части коэффициент 2. Так как мы уравняли число атомов каждого элемента в левой и правой частях уравнения, заменим стрелку на знак равенства:
Теперь, наверное, вам понятно, почему такую запись называют уравнением (рис. 99).

Рис. 99.
Закон сохранения массы веществ на примере реакции, уравнение которой 2Н2 + O2 = 2Н2O
Для составления уравнений химических реакций, кроме знания формул реагентов и продуктов реакции, необходимо верно подобрать коэффициенты.
Это можно сделать, используя несложные правила,
1. Перед формулой простого вещества можно записывать дробный коэффициент, который показывает количество вещества реагирующих и образующихся веществ.
Так, для рассмотренного выше примера:
число атомов кислорода в правой и левой частях уравнения можно сделать равными с помощью коэффициента 1/2, поставив его перед формулой кислорода:
Но так как коэффициент показывает не только количество вещества, но и число молекул (атомов), а половину молекулы взять невозможно, лучше переписать приведённое уравнение, удвоив все коэффициенты в нём:
Приведём ещё пример составления уравнения реакции горения этана С2Н6, содержащегося в природном газе. Известно, что в результате этого процесса образуются углекислый газ и вода. Схема этой реакции:
Уравняем число атомов углерода и водорода:
Теперь в правой части уравнения реакции 7 атомов кислорода, а в левой — только 2. Уравняем число атомов кислорода, записав перед формулой 02 коэффициент 3,5 (7:2 = 3,5):
И наконец, перепишем полученное уравнение реакции, удвоив коэффициенты перед формулами всех участников реакции:
2. Если в схеме реакции есть формула соли, то вначале уравнивают число ионов, образующих соль.
Например, взаимодействие серной кислоты и гидроксида алюминия описывают схемой:

Образующаяся в результате реакции соль — сульфат алюминия Al2(SO4)3 — состоит из ионов алюминия Аl3+ и сульфат-ионов . Уравняем их число, записав перед формулами H2SO4 и Аl(OН)3 соответственно коэффициенты 3 и 2:
Чтобы уравнять число атомов водорода и кислорода, воспользуемся третьим правилом.
3. Если участвующие в реакции вещества содержат водород и кислород, то атомы водорода уравнивают в предпоследнюю очередь, а атомы кислорода — в последнюю.
Следовательно, уравняем число атомов водорода. В левой части схемы реакции 12 атомов водорода, а в правой — только 2, поэтому перед формулой воды запишем коэффициент 6:
Индикатором верности расстановки коэффициентов является равенство числа атомов кислорода в левой и правой частях уравнения реакции — по 24 атома кислорода. Поэтому заменим стрелку на знак равенства:
4. Если в схеме реакции имеется несколько формул солей, то необходимо начинать уравнивание с ионов, входящих в состав соли, содержащей большее их число.
Например, взаимодействие растворов фосфата натрия и нитрата кальция описывают схемой:

Наибольшее число ионов содержит один из продуктов реакции — фосфат кальция Са3(РO4)2, поэтому уравнивают ионы, которыми образована эта соль, — Са 2+ и :
и, наконец, ионы Na + и N0 - 3:
- Химические уравнения.
- Правила подбора коэффициентов в уравнениях реакций.

1. Дайте общую характеристику элемента водорода. Приведите примеры соединений, содержащих водород, и напишите их формулы.
*Цитирирование задания со ссылкой на учебник производится исключительно в учебных целях для лучшего понимания разбора решения задания.
Популярные решебники 8 класс Все решебники

Главная задача сайта: помогать школьникам и родителям в решении домашнего задания. Кроме того, весь материал совершенствуется, добавляются новые сборники решений.
Читайте также:

