Гомологи и изомеры алканов 10 класс конспект урока
Обновлено: 07.07.2024
Конспект урока по теме "Гомологический ряд и номенклатура алканов".
| Вложение | Размер |
|---|---|
| gomologicheskiy_ryad_nomenklatura_alkanov..doc | 39 КБ |
Предварительный просмотр:
Тема: Гомологический ряд и номенклатура алканов.
Цель: Ознакомить учащихся с составом и номенклатурой углеводородов ряда
Тип урока: Урок изучения нового материала.
Содержание и ход урока.
I. Организационный момент.
II. Формирование новых знаний, умений и навыков.
Предельными называются углеводороды, в молекулах которых все атомы углерода соединены между собой одинарной связью и полностью насыщены атомами водорода.
Общее название предельных углеводородов по международной номенклатуре – алканы. Общая формула алканов: C n H 2n + 2 .
Простейшим представителем предельных углеводородов является метан – СН 4 . К предельным углеводородам относятся также ряд углеводородов, смотрим таблицу №2. Рассматривая состав углеводородов, мы видим, что каждый последующий член этого ряда отличается от предыдущего на СН 2 группу.
Вещества, сходные по строению и химическим свойствам, но отличающиеся друг от друга по составу молекул на одну или несколько СН 2 групп, называют гомологами.
Гомологи, расположенные в порядке возрастания их относительной молекулярной массы, образуют гомологический ряд. СН 2 группу называют гомологической разностью. Смотрим таблицу №2.
Первые четыре представителя предельных углеводородов имеют исторически сложившиеся названия. Названия следующих предельных углеводородов образуют из греческих и латинских числительных с добавлением суффикса – ан .
При отрыве одного атома водорода от молекулы алкана получается углеводородный радикал, его название образуют от названия соответствующего углеводорода путем замены суффикса – ан на – ил :
СН 4 --- СН 3 С 2 Н 6 ---- С 2 Н 5 С 3 Н 8 ----- С 3 Н 7
метан метил этан этил пропан пропил
Для того чтобы назвать углеводород с разветвленной цепью атомов углерода, надо выделить главную и боковые цепи. Главная содержит большее число последовательно соединенных атомов углерода, она самая длинная. С ней могут быть связаны несколько боковых цепей – радикалов.
Алгоритм составления названия алкана с разветвленной цепью.
- Выбрать самую длинную цепь и пронумеровать атомы углерода в ней. Нумерацию начинают с того конца цепи, к которому ближе стоит радикал. Если радикалов несколько, то нумеруют так, чтобы атомы углерода, с которыми связаны радикалы, получили минимальные номера, т.е. сумма цифр в названии должна иметь наименьшее значение.
- Назвать радикалы в порядке увеличения количества углерода.
- Перед названием каждого радикала указать номера атомов углерода, с которыми связаны радикалы.
- Если один и тот же атом углерода связан с двумя одинаковыми радикалами, то цифру, указывающую на номер этого атома, нужно повторить дважды.
- Число одинаковых радикалов указать числовыми приставками ( ди- - два, три- - три, тетра- - четыре). Все цифры в названиях отделяют от слов дефисами, а друг от друга – запятыми.
- Назвать углеводород по числу атомов углерода в пронумерованной цепи.
Назовите по систематической номенклатуре следующие углеводороды:
Выбираем самую длинную цепь и пронумеруем атомы углерода в ней. В данном случае нумерацию начинаем слева, потому что к этому концу ближе расположен радикал.
СН 3 – СН – СН – СН 2 – СН 3
В молекуле имеются два радикала, у второго и третьего углеродного атома. Определяем название алкана по количеству атомов углерода в главной цепи. Следовательно, алкан имеет название: 2-метил, 3этил пентан.
2- метил, 4- этил гексан.
С 2 Н 5 СН 3 СН 2
3-метил, 2,5 диметил нонан.
Если известно название алкана, то по названию можно написать структурную формулу алкана.
Например: Напишите структурные формулы следующих веществ:
3 – метил, 3- этилпентан, 2,3,4 – триметил – 2 –изопропилгексан.
СН 3 –СН 2 – С – СН 2 – СН 3
СН 3 – С – СН- СН- СН 2 – С Н 3
III. Применение знаний, умений и навыков.
- Назовите по международной номенклатуре следующие соединения:
а) СН 3 СН 2 – СН 3
СН 3 - С - СН - СН – СН 3
б) СН 3 СН 2 – СН 3 СН 2 – СН 2 – СН 3
СН 3 – С - С - СН 2 - С – СН 2 – СН 3
СН 3 СН 2 – СН 3 СН
СН 3 – СН 2 - С – СН 2 – С – СН 3
Н 3 С – СН 2 СН 2 – СН 3
- Напишите структурные формулы следующих веществ:
а) 2,2,3 – триметил- 4,6- диэтил- 5 – пропилоктан;
б) 4-метил – 3- этилгептан;
в) 2,3,6 – триметилгептан.
IV. Д/З s 4, упр.1,4,5,6.
По теме: методические разработки, презентации и конспекты

"Алкины. Строение. Гомологический ряд. Изомерия, номенклатура. Физические свойства"
Урок "Алкины. Строение. Гомологический ряд. Изомерия, номенклатура. Физические свойства" составлен на основе системно-деятельностного подхода.
10 кл.Гомологический ряд алкинов,изомерия и номенклатура. Получение.
Основные понятия (впервые вводимые): тройная химическая связь, SP – гибридизация.Демонстрация: получение ацетилена карбидным способом.Оборудование: таблица строения ацетилена, кодоскоп.Цель урок.

презентация Строение и номенклатура алканов
презентация предназначена для изучения гомологического ряда,строения и номенклатуры алканов.

конспект урока "Номенклатура алканов"
Конспект урока в 10 классе по базовому уровню.

знакомство обучающихся с алканами, их строением, изомерией, физическими свойствами.

открытый урок по теме: "Алкены. Строение. Гомологический ряд этилена. Номенклатура. Изомерия алкенов"
Урок разработан в виде урока-игры.


организация деятельности учащихся, направленной на прочное усвоение знаний по строению, номенклатуре, изомерии алканов.
дать понятие класса алканов, их общую формулу, гомологический ряд, рассмотреть строение метана и sp 3 -гибридизацию;
способствовать усвоению гомологии, изомерии и номенклатуры, характерной для класса алканов;
проверить уровень усвоения учебного материала по теме урока.
воспитывать мировоззрение и единую химическую картину мира;
воспитывать дисциплинированность, ответственное отношение к учебному труду;
показать тесную связь химии с жизнью;
формировать умение работать самостоятельно.
развивать творческую активность и самостоятельность учеников, показав пути самостоятельного освоения материала;
развивать умения выделять главное, существенное;
развивать химически грамотную речь, образное и логическое мышление;
развивать объективную самооценку.
I. Организационный момент. (2 мин)
1.Организация внимания и порядка в классе, взаимное приветствие, проверка присутствующих, проверка готовности класса к уроку.
2. Подведение учащихся к теме урока.
- что изучает Органическая химия - изучает углеводороды и их производные.
- Какие соединения мы называем углеводородами - орг. соединения, состоящие из двух элементов - углерода и водорода
- напишите общую формулу предельных углеводородов
- почему они называются предельными
- написать формулы метана - молекулярную, структурную, электронную
СМОТРИМ ФРАГМЕНТ СТРОЕНИЕ АЛКАНОВ
Посмотрите первые 5 пунктов плана и сформулируйте цель урока.
3. Объяснение темы.
АЛКАНЫ – это насыщенные углеводороды, в молекулах которых атомы углерода соединены между собой только одинарной связью.
Моделирование молекул предельных углеводородов.
Оборудование: пластилин 2-х цветов, палочки.
В ходе работы заполняем таблицу. Лабораторную работу проводим парами.
Соберите шаростержневую модель молекулы метана. На шарике, имитирующем атом углерода, наметьте четыре равноудалённые друг от друга точки и вставьте стержни, к которым присоединены водородные шарики. Получили модель молекулы метана. Сделайте пять одинаковых моделей. (слайд №10)
Отнимите от каждой из двух молекул по 1 атому водорода и соедините остатки (радикалы) вместе. Получили модель молекулы этана. Сделайте 2-ю такую же модель. (слайд №11)
Если отнять от этана молекулу водорода, то получим радикал – этил. К этилу присоединим радикал метил и получим пропан.
При соединении между собой двух этилов образуется молекула бутана. (слайд №12)
Отнимем от молекулы бутана один водород, и на его место присоединим радикал метил. Получили ещё один гомолог – пентан. (слайд №13,14)
Метан, этан, пропан, бутан, пентан и т. д. – гомологи.
Гомологи – вещества, сходные по строению и свойствам, но отличающиеся друг от друга по составу на одну или несколько групп – СН2 – .
Возьмём модель молекулы пентана.
Н – С – С – С – С – С – Н пентан С5Н12
Отнимем группу СН3 – и присоединим её на место Н у второго атома С. Получим
Отнимем ещё одну группу СН3 – и присоединим её опять у второго атома С
на место второго атома Н. Получим:
Изомеры – это вещества, имеющие одинаковый качественный и количественный состав, но разные строение и свойства.
Назовём эти вещества:
составления названий органических веществ.
Выбрать в молекуле самую длинную цепочку углеродных атомов.
Пронумеровать цепочку с того конца, к которому ближе разветвление молекулы.
Основа названия – название углеводорода с тем же числом углеродных атомов, что и в самой длинной цепи.
Перечислить перед основой названия все заместители основной цепи с указанием номеров углеродных атомов, при которых они стоят. Если одинаковых заместителей несколько, перед их названиями ставят приставки ди-, три-, тетра- и т. д.
Отделить запятыми все цифры друг от друга, буквы от цифр – дефисом. Если при одном углеродном атоме имеется не один, а два заместителя, его цифру повторить в названии дважды.
Углеводороды нормального строения обозначают буквой н, например:
Н – С – С – С – С – С – Н С5Н12 н-пентан
Н – С – С – С – С – Н С5Н12 2-метилбутан
Н – С – С – С – Н С5Н12 2,2 –диметилпропан
Заключение Итак, мы изучили пространственное строение предельных углеводородов, узнали, что такое гомологи, изомеры, научились их называть.
Проверим наши знания. (слайд №17,18)
Дан ряд формул веществ. Выберите из них гомологи и изомеры.
Например, гомологи 1,3,4. изомеры 1 и 5, 3 и 7.
Ответы: Гомологи 1и 4, 3 и 6
Изомеры 1,3 и 5; 2, 4 и 6
Названия алканов и алкильных заместителей
атом углерода находится в 1-ом валентном состоянии sp 3 ;
четыре σ-связи углерода направлены в пространстве под углом 109°28';
молекула метана СН4 – имеет форму правильного тетраэдра;
длина углеродной связи — 0,154 нм.
ЗАКРЕПЛЕНИЕ Написание структурных формул.
Сначала записывают открытую цепь, затем нумеруют атомы углерода и расставляют заместители. В заключение дописывают атомы водорода, чтобы каждый атом углерода оказался четырехвалентным. Рассмотрим на примере 2,5,6-триметилоктан.
4. Закрепление темы
1. Напишите структурные формулы следующих веществ:
а) 2,3 – диметилбутана,
б) 2,4 – диметил - 3 – этилпентана
2. Если вы усвоили номенклатуру алканов, то сможете самостоятельно назвать каждый из них. Перепишите в тетрадь структурные формулы алканов, приведенные в задании и назовите эти вещества.
5. Подведение итогов урока
Вернутся к плану урока, посмотреть 1-5 пунктов, ответить на вопросы
- достигли ли мы поставленной цели?
- что нового на уроке узнали?
- что было интересным?
6. Домашнее задание
Параграф 8 тестовые задания стр 34
Гомологи и изомеры алканов
1. Алканы – это алифатические (ациклические), насыщенные углеводороды, в которых все валентности атомов углерода, не затраченные на образование простых С – С связей, насыщены атомами водорода.
2. Общая формула алканов – СnH2n+2
В таблице представлены некоторые представители ряда алканов и их радикалы.
Тренажёр "Гомологический ряд алканов"
Из таблицы видно, что эти углеводороды отличаются друг от друга количеством групп - СН2 -.Такой ряд сходных по строению, обладающих близкими химическими свойствами и отличающихся друг от друга числом данных групп называется гомологическим рядом. А вещества, составляющие его называются гомологами.
Гомологи – вещества сходные по строению и свойствам, но отличающиеся по составу на одну или несколько гомологических разностей (- СН2 -)

пространственное строение – тетраэдрическое
Углеродная цепь - зигзаг (если n ≥ 3)
σ – связи (свободное вращение вокруг связей)
длина (-С-С-) 0,154 нм
энергия связи (-С-С-) 348 кДж/моль
Все атомы углерода в молекулах алканов находятся в состоянии sр3-гибридизации

угол между связями С-C составляет 109°28', поэтому молекулы нормальных алканов с большим числом атомов углерода имеют зигзагообразное строение (зигзаг). Длина связи С-С в предельных углеводородах равна 0,154 нм (1нм=1*10-9м).
Образование молекулы метана

а) электронная и структурная формулы;
б) пространственное строение

Строение молекулы этана С2Н6

Строение молекулы пропана С3Н8 – цепь зигзагообразная

Тренажёр "Состав и строение алканов"
4. Изомерия – характерна СТРУКТУРНАЯ изомерия цепи с С4

Один из этих изомеров (н-бутан) содержит неразветвленную углеродную цепь, а другой — изобутан — разветвленную (изостроение).
Атомы углерода в разветвленной цепи различаются типом соединения с другими углеродными атомами. Так, атом углерода, связанный только с одном другим углеродным атомом, называется первичным, с двумя другими атомами углерода – вторичным, с тремя – третичным, с четырьмя – четвертичным.

С увеличением числа атомов углерода в составе молекул увеличиваются возможности для разветвления цепи, т.е. количество изомеров растет с ростом числа углеродных атомов.
Трудно себе представить наш быт без голубых язычков огня кухонной плиты или газовой зажигалки. В этих устройствах сгорают углеводороды одного и того же класса — алканы. Различие лишь в том, что бытовой газ представляет собой главным образом метан СН4, а в резервуаре зажигалки находятся под давлением сжиженные газы пропан С3Н8 и бутан С4Н10.
Углеводороды, молекулы которых не содержат кратных связей, называют предельными или насыщенными.
Своё название предельные углеводороды получили потому, что все валентности углеродных атомов в их молекулах насыщены атомами водорода до предела.
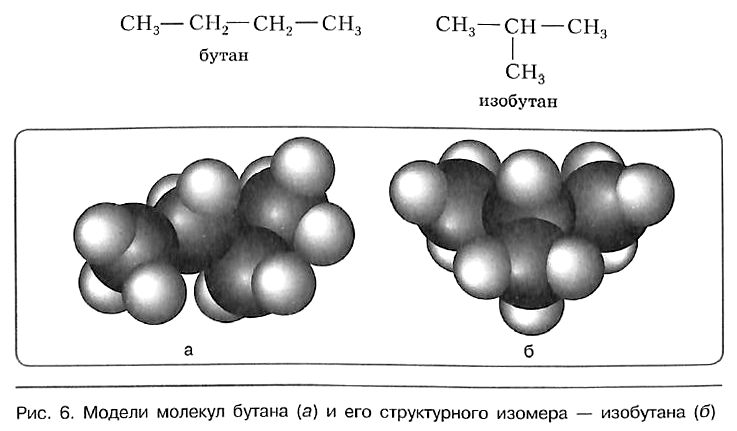
Сокращённая структурная формула пропана СН3—СН2—СН3. Для бутана возможно написание двух структурных формул: в одной углеродная цепь имеет линейное, а в другой — разветвлённое строение:
Свойства бутана и изобутана различны: бутан имеет более низкие температуры кипения и плавления. По отношению друг к другу бутан и изобутан являются изомерами, различающимися строением углеродной цепи. Изомерия углеродной цепи — вариант структурной изомерии.

В молекулах алканов углеродные цепи открытые, т. е. незамкнутые. Но предельными могут быть и углеводороды, имеющие замкнутую углеродную цепь. Этот класс соединений называют циклоалканами. Некоторые циклоалканы, например циклогексан С6Н12, входят в состав нефти.
Простейший представитель алканов — метан СН4. Именно это соединение является родоначальником гомологического ряда алканов.
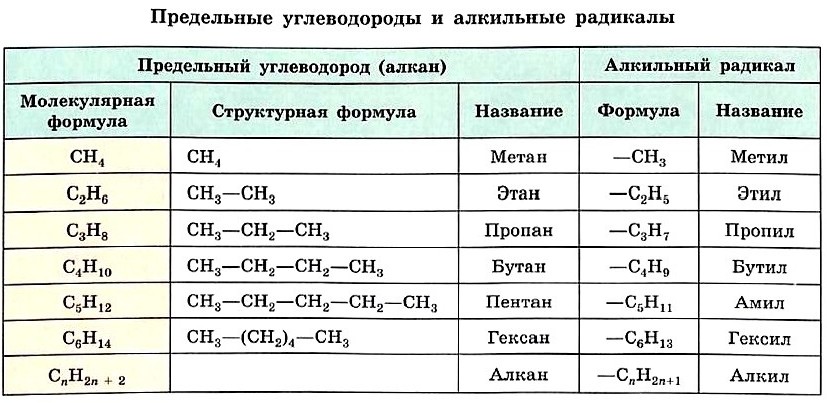
Формулу каждого последующего члена гомологического ряда легко получить из формулы предыдущего, заменив один атом водорода в молекуле на группу СН3. Так, второй гомолог ряда алканов — этан — имеет формулу СН3—СН3. Формулы и названия первых шести представителей алканов с неразветвлённой цепью атомов углерода приведены в таблице.
Если от молекулы алкана мысленно отщепить один атом водорода, мы получим частицу со свободной валентностью у атома углерода — радикал.
Название радикала, соответствующего предельному углеводороду, т. е. алкильного радикала, строится так: суффикс -ан заменяют на -ил, а состав будет подчиняться общей формуле С n Н2 n +1. Формулы и названия алкильных радикалов, приведённые в таблице, нужно запомнить, чтобы уметь называть органические вещества с разветвлённой углеродной цепью.

Номенклатура алканов
Для построения названий органических веществ, в частности предельных углеводородов, используют свод правил — номенклатуру. В соответствии с так называемой международной, или систематической, номенклатурой при составлении названий алканов руководствуются следующими правилами:
- 1) выбирают в молекуле самую длинную цепь атомов углерода;
- 2) нумеруют атомы углерода в цепи с того конца, к которому ближе разветвление;
- 3) записывают основу названия вещества — название углеводорода с тем же числом углеродных атомов, что и в пронумерованной цепи;
- 4) перед основой названия перечисляют все заместители основной цепи с указанием номеров атомов углерода, при которых они стоят. Если одинаковых заместителей несколько, перед их названиями ставят приставки ди-, три-, тетра-,
- 5) все цифры друг от друга отделяют запятыми, буквы от цифр — дефисом. Если при одном углеродном атоме имеется не один, а два заместителя, его цифра повторяется в названии дважды;
- 6) перед названием предельного углеводорода нормального (неразветвлённого) строения ставят букву н-.

Проиллюстрируем эти правила примерами названий алканов.
Физические и химические свойства алканов
Метан и его газообразные гомологи (до бутана включительно) содержатся в природном и попутном нефтяном газах. Жидкие алканы — основная часть нефти. Твёрдые предельные углеводороды (парафин) растворены в нефти, которая и служит источником их получения.
При обычных условиях алканы не реагируют с концентрированными кислотами и щелочами, не окисляются сильными окислителями, такими как перманганат калия.

Однако при нагревании химическое поведение алканов резко меняется. Все алканы горят бледно-голубым пламенем с образованием углекислого газа и воды:
Горение алканов сопровождается выделением большого количества теплоты, что определяет их использование в качестве топлива.
Следует помнить, что углеводороды относятся к пожаро- и взрывоопасным веществам. Утечка бытового газа грозит страшными последствиями. Для того чтобы вовремя обнаружить наличие в воздухе бытового газа, к нему добавляют вещества с резким неприятным запахом — одоранты. Если вы почувствовали на кухне, в подъезде или на улице запах газа, следует немедленно обратиться в экстренную службу по телефону 104, проветрить помещение и ни в коем случае не пользоваться открытым огнём или электроприборами. В случае пожара службу спасения вызывают по телефону 101 или 112 (с сотового телефона бесплатно).
Предельные углеводороды используют не только как топливо, но и в качестве сырья для химической промышленности, поскольку их свойства отнюдь не ограничиваются реакцией горения.

В предельных углеводородах атомы водорода могут замещаться другими атомами или группами, в частности атомами галогенов (хлора и брома). Эти реакции замещения протекают ступенчато при освещении смеси газов:

Галогенпроизводные алканов — прекрасные растворители, хладагенты (рабочие жидкости, которыми заправляют бытовые холодильники и промышленные холодильные установки), реагенты для органического синтеза.

Если предельные углеводороды нагревать без доступа воздуха при более высокой температуре, то они не выдерживают такого воздействия и разлагаются. Например, из метана при нагревании свыше 1000 °С образуется два ценных продукта — сажа (углерод) и водород:
Сажу, полученную таким образом, используют для изготовления автомобильных шин и резины, она входит в состав красок и туши.

Алканы с неразветвлённой цепью углеродных атомов при нагревании превращаются в более устойчивые соединения с разветвлённой цепью. Например, из н-бутана можно получить изобутан:
Поскольку состав исходного вещества и продукта реакции одинаков, эти соединения являются изомерами. Именно поэтому такой процесс получил название реакция изомеризации.
При нагревании в присутствии катализатора алканы способны вступать в реакцию отщепления. Что же могут отщеплять молекулы предельных углеводородов? Если предположить, что углеродная цепь остаётся без изменения, то отщепляться могут только молекулы водорода.
Этилен С2Н4 — представитель непредельных углеводородов, о которых пойдёт речь в следующем параграфе.


Урок усвоения нового материала раскрывает понятия гомологии, изомерии и номенклатуры алканов с применением ИКТ и игровых моментов.
Описание разработки
Цель:
организация деятельности учащихся, направленной на прочное усвоение знаний по строению, номенклатуре, изомерии алканов.
Задачи урока:
- дать понятие класса алканов, их общую формулу, гомологический ряд, рассмотреть строение метана и sp 3 -гибридизацию;
- способствовать усвоению гомологии, изомерии и номенклатуры, характерной для класса алканов;
- проверить уровень усвоения учебного материала по теме урока.
- воспитывать мировоззрение и единую химическую картину мира;
- воспитывать дисциплинированность, ответственное отношение к учебному труду;
- показать тесную связь химии с жизнью;
- формировать умение работать самостоятельно.
- развивать творческую активность и самостоятельность учеников, показав пути самостоятельного освоения материала;
- развивать умения выделять главное, существенное;
- развивать химически грамотную речь, образное и логическое мышление;
- развивать объективную самооценку.
Ход урока
I. Организационный момент. (2 мин)
1. Организация внимания и порядка в классе, взаимное приветствие, проверка присутствующих, проверка готовности класса к уроку.
2. Подведение учащихся к теме урока.
Органическая химия изучает углеводороды и их производные.
Какие соединения мы называем углеводородами
Посмотрите первые 5 пунктов плана и сформулируйте цель урока.
- Определение. Формула.
- Строение.
- Гомологический ряд.
- Изомерия.
- Номенклатура.
- Способы получения.
- Физические свойства.
- Химические свойства.
- Применение.
3. Объяснение темы.
АЛКАНЫ – это насыщенные углеводороды, в молекулах которых атомы углерода соединены между собой только одинарной связью.
Названия алканов и алкильных заместителей
- атом углерода находится в 1-ом валентном состоянии sp 3 ;
- четыре σ-связи углерода направлены в пространстве под углом 109°28';
- молекула метана СН4 – имеет форму правильного тетраэдра;
- длина углеродной связи — 0,154 нм.
Написание структурных формул.
Сначала записывают открытую цепь, затем нумеруют атомы углерода и расставляют заместители. В заключение дописывают атомы водорода, чтобы каждый атом углерода оказался четырехвалентным. Рассмотрим на примере 2,5,6-триметилоктан.
4. Закрепление темы
1. Напишите структурные формулы следующих веществ:
а) 2,3 – диметилбутана,
б) 2,4 – диметил - 3 – этилпентана
2. Если вы усвоили номенклатуру алканов, то сможете самостоятельно назвать каждый из них. Перепишите в тетрадь структурные формулы алканов, приведенные в задании и назовите эти вещества.
Читайте также:

