Алкадиены диеновые углеводороды конспект
Обновлено: 06.07.2024
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
ТЕМА УРОКА : ДИЕНЫ И КАУЧУК
Алкадиены - непредельные (ненасыщенные) углеводороды, имеющие в молекуле две двойных связи С=С. Каждая такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкадиены также называют диеновыми углеводородами. Первый член гомологического ряда - пропадиен - CH 2 =C=CH 2 . Общая формула их гомологического ряда - C n H 2n-2 .
Номенклатура и изомерия алкадиенов
Названия алкенов формируются путем добавления суффикса "диен" к названию алкана с соответствующим числом: пропадиен, бутадиен, пентадиен и т.д.
При составления названия алкадиена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойные связи. Нумерация атомов углерода в ней начинается с того края, к которому ближе двойная связь. В конце названия указывают атомы углерода, у которых начинается двойная связь.

Атомы углерода, прилежащие к двойной связи находятся в sp 2 гибридизации.
Для алкадиенов характерна изомерия углеродного скелета, положения двойных связей, межклассовая изомерия с алкинами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.

Классификация по положению двойных связей
В зависимости от того, как чередуются двойные связи в молекуле алкадиена, они подразделяются на следующие типы:
Кумулированные двойные связи
В случае, если две двойные связи прилежат к одному и тому же атому углерода.
Пример - пропадиен-1,2 (аллен) - CH 2 =C=CH 2
В молекуле аллена все атомы углерода находятся в состоянии sp 2 гибридизации.
Сопряженные двойные связи
В случае, если две двойные связи разделены одной одинарной связью. В результате такого взаиморасположения в молекулах возникает сопряжение: формируется единое π-электронное облако.
Помните, что сигма-связи (σ-связи) перекрываются вдоль линии плоскости, а пи-связи (π-связи) над и под линией плоскости (линией, соединяющей центры атомов).

Пример - бутадиен-1,3 - CH 2 =CH-CH=CH 2
Изолированные двойные связи
В случае, если две двойные связи разделены двумя и более одинарными связями.
Пример - пентадиен-1,4 - CH 2 =CH-CH 2 -CH=CH 2
Получение алкадиенов
Алкадиены получают несколькими способами:
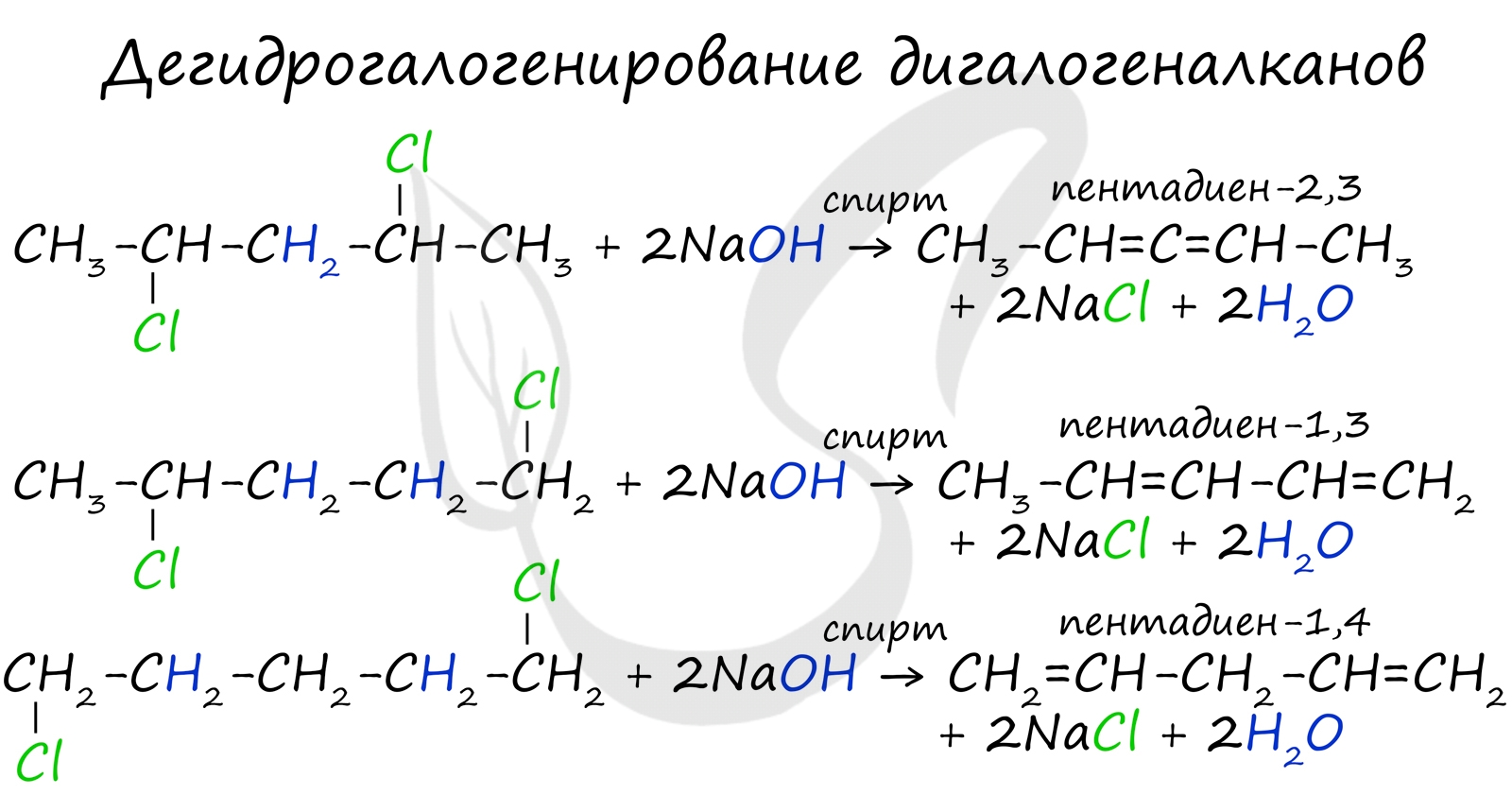
Дегидрогалогенирование дигалогеналканов
В результате реакции молекулы алкана, содержащей два атома галогена, со спиртовым (!) раствором щелочи получается алкадиен. В зависимости от положения галогенов возможны разные варианты.
Отщепление идет по правилу Зайцева: атом водорода отщепляется от соседнего, наименее гидрированного атома углерода.

Синтез С.В. Лебедева
Сергей Васильевич Лебедев в 1927 году разработал первый промышленный способ получения синтетического каучука из этилового спирта.
Каучук занимает важное место в промышленности благодаря своим свойствам: водонепроницаемости, эластичности и способности к электроизоляции. Путем вулканизации из каучука получают резину, используемую повсеместно.

Дегидрирование алканов
В результате отщепления водорода от молекулы алкана образуются двойные связи. Дегидрирование происходит при повышенной температуре и в присутствии катализатора.
![]()

Химические свойства алкадиенов
Алкадиены - ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны. Наличие сопряженных двойных связей увеличивает реакционную способность молекулы и обуславливает необычный механизм некоторых реакций.
Гидрирование
Водород присоединяется к атомам углерода, образующим двойную связь. Пи-связь (π-связь) рвется, остается единичная сигма-связь (σ-связь).
![]()

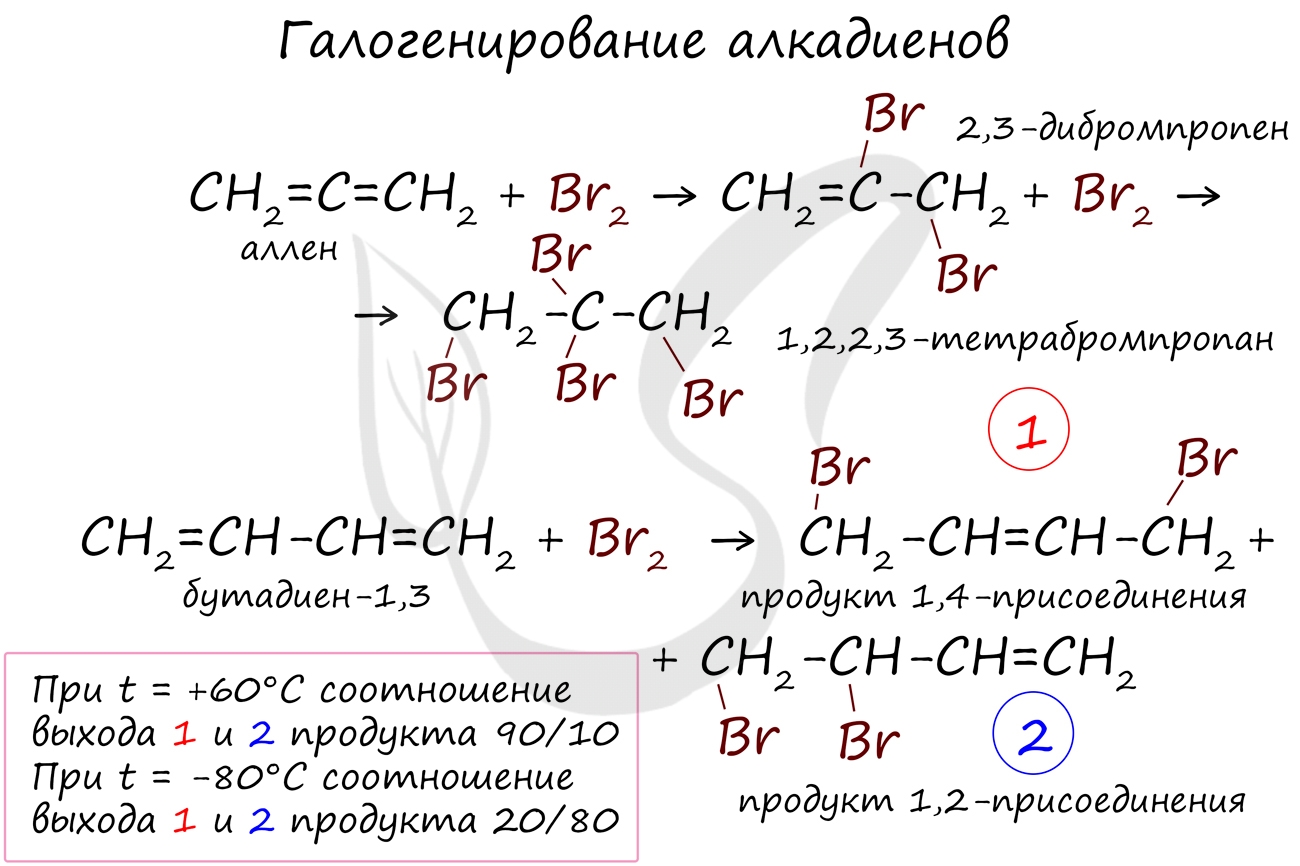
2. Галогенирование
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение брома по кратным связям к органическому веществу.
В случае, если двойные связи находятся в сопряжении, выход продуктов во многом зависит от температуры. Например, в ходе галогенирования бутадиена-1,3 при -80°C преимущественно получается продукт 1,2-присоединения, а при +60°C - продукт 1,4-присоединения.
![]()

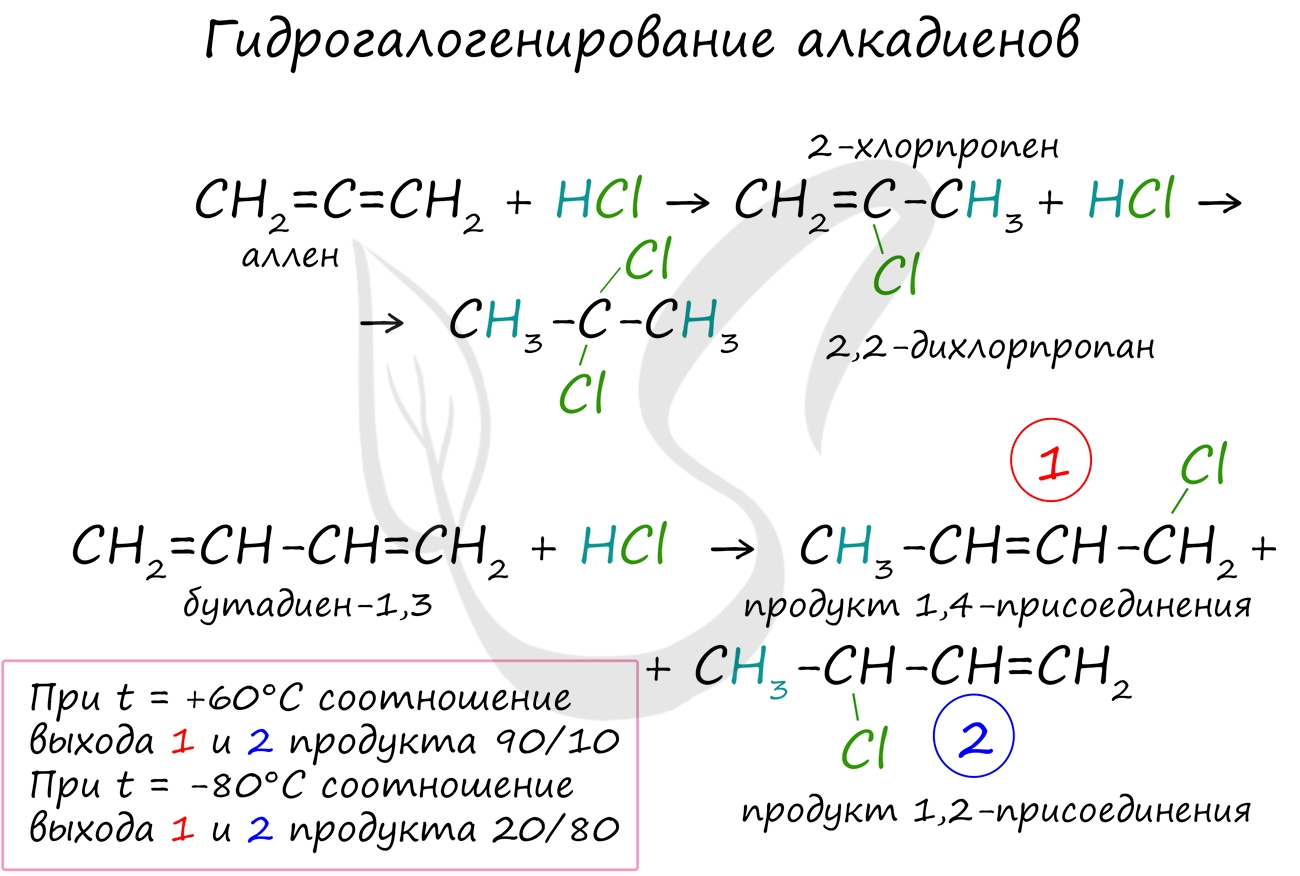
3. Гидрогалогенирование
Алкадиены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена - к наименее гидрированному атому углерода.
![]()

4. Окисление
При горении алкадиены, как и все органические соединения, сгорают с образованием углекислого газа и воды - полное окисление.
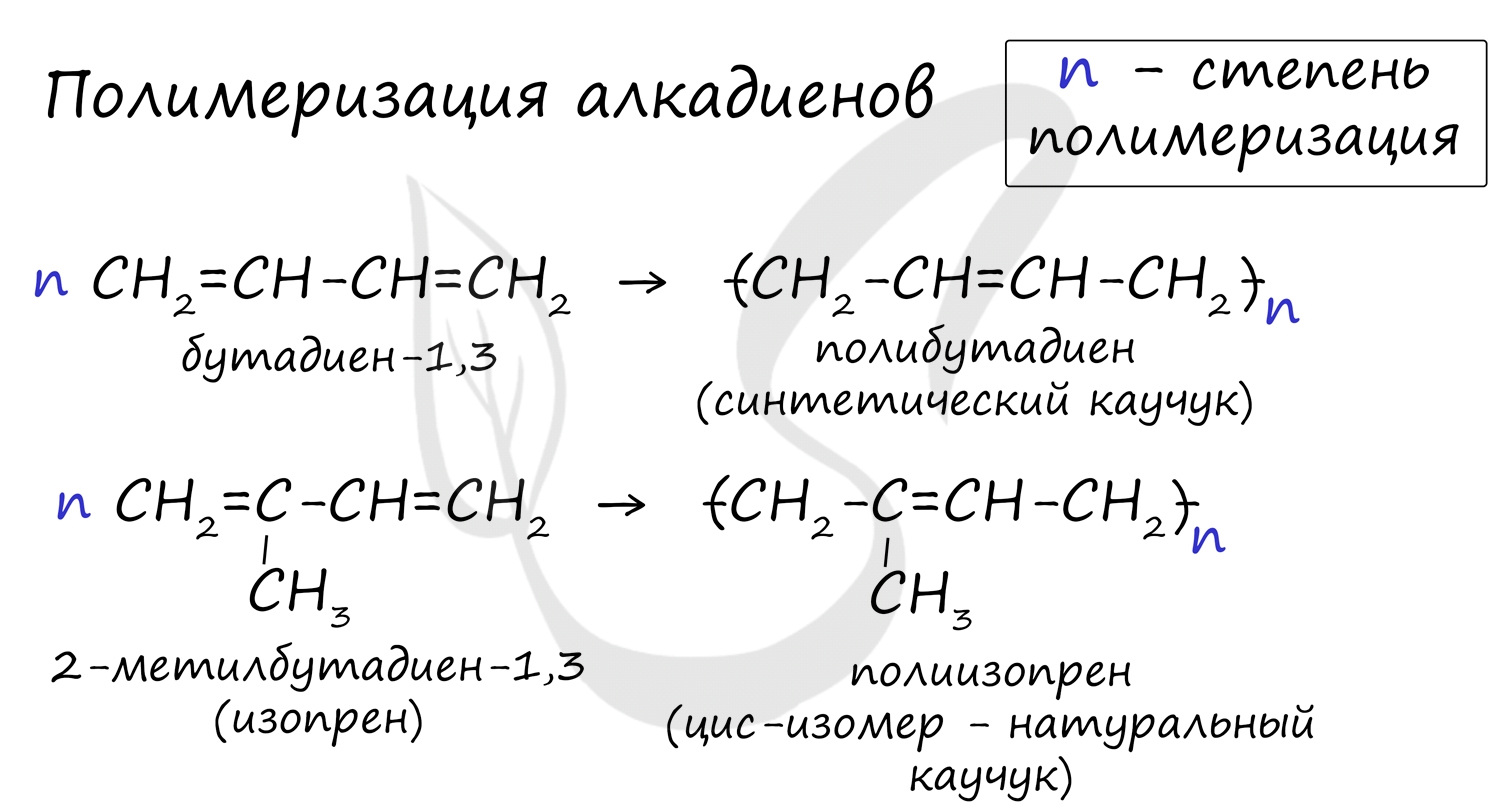
5. Полимеризация
Полимеризация - цепная реакция синтеза полимеров, при котором молекула полимера образуется путем последовательного соединения молекул мономеров.
Индекс "n", степень полимеризации, обозначает число мономерных звеньев, которые входят в состав полимера.

Диеновые углеводороды в основном применяются для синтеза каучуков:

9. Натуральный и синтетический каучуки
Натуральный каучук получают из млечного сока (латекса) каучуконосного дерева гевеи, растущего в тропических лесах Бразилии.
При нагревании без доступа воздуха каучук распадается с образованием диенового углеводорода – 2-метилбутадиена-1,3 или изопрена. Каучук – это стереорегулярный полимер, в котором молекулы изопрена соединены друг с другом по схеме 1,4- присоединения с цис- конфигурацией полимерной
Стереорегулярное строение каучука
Молекулярная масса натурального каучука колеблется в пределах от 7 ·10 4 до 2,5 ·10 6 .
транс - Полимер изопрена также встречается в природе в виде гуттаперчи.
Натуральный каучук обладает уникальным комплексом свойств: высокой текучестью, устойчивостью к износу, клейкостью, водо- и газонепроницаемостью. Для придания каучукунеобходимых физико-механических свойств: прочности, эластичности, стойкости к действию растворителей и агрессивных химических сред – каучук подвергают вулканизации нагреванием до 130-140°С с серой. В упрощенном виде процесс вулканизации каучука можно представить следующим образом:
Атомы серы присоединяются по месту разрыва некоторых двойных связей и линейные молекулы каучука "сшиваются" в более крупные трехмерные молекулы – получается резина, которая по прочности значительно превосходит невулканизированный каучук. Наполненные активной сажей каучуки в виде резин используют для изготовления автомобильных шин и других резиновых изделий.
Строение резины.
В 1932 году С.В.Лебедев разработал способ синтеза синтетического каучука на основе бутадиена, получаемого из спирта. И лишь в пятидесятые годы отечественные ученые осуществили каталитическую стереополимеризацию диеновых углеводородов и получили стереорегулярный каучук, близкий по свойствам к натуральному каучуку. В настоящее время в промышленности выпускают каучук, в котором содержание звеньев изопрена, соединенных в положении 1,4, достигает 99%, тогда как в натуральном каучуке они составляют 98%. Кроме того, в промышленности получают синтетические каучуки на основе других мономеров – например, изобутилена, хлоропрена, и натуральный каучук утратил свое монопольное положение.
Для вулканизации каучука берётся немного серы 2 – 3 % от общей массы. Если добавить к каучуку более 30 % серы, то она присоединится по линии разрыва почти всех π – связей и образуется жёсткий материал – эбонит.
ЗАДАНИЕ: Составьте опорный конспект
Тема. Диены. Каучук.
2. Общая формула –
Схематическое изображение строения молекул бутадиена -1,3 (а) и вид модели сверху (б). Перекрывание электронных облаков между С 1 –С 2 и С 3 –С 4 больше, чем между С 2 –С 3 .
Запомнить!
· Связи ______ (вращение относительно двойной С-С связи ___________)
· Длина связи (-С = С – С = С – С – С -)
4. Классификация алкадиенов:
1) углеводороды с __________________ двойными связями,
пропадиен или аллен CH 2 =C=CH 2
2) углеводороды с __________________ двойными связями,
3) углеводороды с ___________________двойными связями,
бутадиен-1,3 или дивинил CH 2 =CH–CH=CH 2
5. Изомерия сопряженных диенов
1. Изомерия _______________________________________________;
2. Изомерия _________________________________________________:
3. _________________________ изомерия с алкинами и циклоалкенами.
Например, формуле С 4 Н 6 соответствуют следующие соединения:
6. Получение диеновых углеводородов CnH 2 n- 2
Запишите уравнения реакций промышленных способов получения алкадиеновых углеводородов:

Алкадиены (диены). Каучуки
Ключевые слова конспекта: Алкадиены (диены, диеновые углеводороды). Сопряжённые диены. Реакция Лебедева. Каучуки: натуральный, синтетические (бутадиеновый, изопреновый). Вулканизация каучука. Резина. Эбонит.
Понятие о сопряжённых алкадиенах
В соответствии с третьим положением теории химического строения даже незначительные изменения в структуре вещества могут существенно изменить его химические свойства, а следовательно, сделать незаменимым для производства жизненно необходимых материалов. Не будь углеводородов этого класса, нам пришлось бы обходиться без резины и каучука, а точнее без всего бесчисленного ассортимента изделий, изготовленных из этих материалов.
Большое значение в производстве каучуков имеют диеновые углеводороды особого строения: в их молекулах две двойные связи разделены одной одинарной. Такие диены называют сопряжёнными диенами.
Простейший сопряжённый диен — бутадиен-1,3 имеет формулу СН2=СН—СН=СН2. Как видите, в международных названиях алкадиенов указывают номера обоих атомов углерода, от которых начинаются двойные связи в молекуле.

Ещё один важнейший диеновый углеводород — 2-метилбутадиен-1,3 (его чаще называют изопрен) имеет формулу
Способы получения алкадиенов

Для получения диеновых углеводородов в промышленности используют реакцию дегидрирования, т. е. отщепления водорода. В качестве исходного вещества берут предельный углеводород с тем же строением углеродной цепи, что и у получаемого продукта. Понятно, что для образования двух двойных связей С=С алкан должен отдать четыре атома, т. е. две молекулы водорода. Например, для синтеза изопрена в качестве исходного вещества необходимо взять 2-метилбутан:

или
Рассмотренная реакция наглядно показывает, что в составе алкадиенов на четыре атома водорода меньше, чем в молекулах соответствующих предельных углеводородов, и на два атома водорода меньше, чем в молекулах соответствующих алкенов.

Алкадиены. Химические свойства
Будучи непредельными углеводородами, алкадиены, подобно алкенам, склонны к реакциям присоединения. Они так же, как алкены, обесцвечивают бромную воду и раствор перманганата калия.

Особенность реакций присоединения диеновых углеводородов состоит в том, что две сопряжённые связи проявляют себя как единое целое. Присоединение галогена происходит не по одной двойной связи, а за счёт крайних атомов углерода сопряжённой системы двойных связей:

или

Продукт реакции 1,4-дибромбутен-2 также содержит двойную связь и, следовательно, тоже способен присоединять молекулу брома:

Аналогичным образом диеновые углеводороды присоединяют водород (реакция гидрирования):
Каучук и продукты его вулканизации
Сопряжённые диеновые углеводороды способны к реакциям полимеризации, в результате которых получают синтетические каучуки.
Каучуки можно рассматривать как продукты полимеризации сопряжённых диенов или их производных. Каучуки относят к эластомерам. Такое название эти полимеры получили потому, что обладают эластичностью (от греч. elastikos — растяжимый), т. е. способностью обратимо изменять форму под действием внешних сил. Другие ценные свойства каучуков — водо- и газонепроницаемость — также широко используют в промышленном производстве.
Природными источниками каучука служат растения, богатые млечным соком: гевея, фикусы, молочаи, одуванчики. В промышленных масштабах натуральный (природный) каучук получают из сока тропического дерева гевеи. Такой каучук можно рассматривать как продукт полимеризации изопрена, или 2-метилбутадиена-1,3.
Каучуконосы нашей страны (одуванчики кок-сагыз и тау-сагыз) содержат очень мало млечного сока, а потому не могут использоваться в качестве источника натурального каучука. Проблему получения синтетического каучука решил коллектив учёных под руководством академика С. В. Лебедева в 1931 г. Этот каучук назвали бутадиеновым каучуком, поскольку в качестве мономера для его получения был выбран бутадиен-1,3. В процессе полимеризации двойные связи алкадиена разрываются, за счёт освободившихся валентностей крайних углеродных атомов растёт полимерная цепь. Одновременно с этим между центральными атомами углерода образуется двойная связь:

Коллективом под руководством С. В. Лебедева был разработан также уникальный способ получения исходного диенового углеводорода — бутадиена-1,3 — на основе этилового спирта:

или
Эту реакцию называют реакцией Лебедева.
Синтетический бутадиеновый каучук обладает такими ценными качествами, как газо- и водонепроницаемость, однако уступает натуральному в эластичности.

В 60-х гг. прошлого столетия был получен эластичный синтетический каучук на основе изопрена — синтетический изопреновый каучук:
По эластичности и износоустойчивости изопреновый каучук сходен с природным и так же, как бутадиеновый, используется для производства шин.
Общая формула СnH2n-2 отражает состав не только алкадиенов, но и ацетиленовых углеводородов. Речь о них пойдёт в следующем конспекте.

Алкадиены – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствуют две двойные связи между атомами углерода С=С.
Общая формула алкадиенов CnH2n-2 (как у алкинов, а также циклоалкенов), где n ≥ 3.
Наличие двух двойных связей между атомами углерода очень сильно влияет на свойства углеводородов. В этой статье мы подробно остановимся на свойствах, способах получения и особенностях строения алкадиенов.
Свойства алкадиенов определяются их строением и взаимных расположением двойных связей в молекуле.
Изолированные двойные связи разделены в углеродной цепи двумя или более σ-связями С–С. Например, в пентадиене-1,4:
Изолированные алкадиены проявляют свойства алкенов.
Кумулированные двойные связи расположены в углеродной цепи у одного атома углерода.
Например , пропадиен:
Кумулированные алкадиены неустойчивы.
Сопряженные двойные связи разделены одной σ-связью С-С.
Например , бутадиен-1,3:
Сопряженные алкадиены обладают характерными свойствами, которые отличаются от свойств алкенов.
Строение сопряженных алкадиенов
Молекула бутадиена-1,3 содержит четыре атома углерода в sp 2 —гибридизованном состоянии.
π-Электроны двойных связей образуют единое π-электронное облако (сопряженную систему) и делокализованы (равномерно распределены) между всеми атомами углерода.

Это соответствует плоскому строению молекулы бутадиена-1,3.
| Образуется единая сопряженная π-система, которая может вступать во взаимодействие целиком, используя все четыре р-орбитали π-связей. |

Аналогичное устроены и другие сопряженные алкадиены.
Например , 2-метилбутадиен-1,3:

Сопряжение в молекуле алкадиенов можно также схематично изобразить так:
Для алкадиенов характерна структурная и пространственная изомерия.
Структурная изомерия
Для алкенов характерна структурная изомерия – изомерия углеродного скелета, изомерия положения кратных связей и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры положения двойных связей отличаются положением двойных связей.
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Алкадиены являются межклассовыми изомерами с алкинами и циклоалкенами с общей формулой — CnH2n-2.
Изомеры углеродного скелета отличаются строением углеродного скелета.
| Пентадиен-1,3 | 2-Метилбутадиен-1,3 |
 |  |
Пространственная изомерия
Для некоторых алкадиенов характерна пространственная изомерия: цис-транс-изомерия и оптическая.
Алкадиены, которые обладают достаточно большим углеродным скелетом, могут существовать в виде оптических изомеров. В молекуле алкадиена должен присутствовать асимметрический атом углерода (атом углерода, связанный с четырьмя различными заместителями).
Цис-транс-изомерия обусловлена отсутствием вращения по двойной связи у некоторых алкадиенов.
Алкадиены, имеющие у каждого из двух атомов углерода при двойной связи различные заместители, могут существовать в виде двух изомеров, отличающихся расположением заместителей относительно плоскости π-связи.
Алкадиены, в которых одинаковые заместители располагаются по одну сторону от плоскости двойной связи, это цис-изомеры. Алкадиены, в которых одинаковые заместители располагаются по разные стороны от плоскости двойной связи, это транс-изомеры.
Цис-транс-изомерия не характерна для тех алкадиенов, у которых хотя бы один из атомов углерода при двойной связи имеет два одинаковых соседних атома.

В названиях алкадиенов для обозначения двух двойных связей используется суффикс -ДИЕН.
| Например, алкадиен имеет название бутадиен-1,3. |

При этом правила составления названий (номенклатура) для алкадиенов в целом такие же, как и для алканов.
Для простейших алкадиенов применяются также исторически сложившиеся (тривиальные) названия:
Сопряженные алкадиены – непредельные нециклические углеводороды, в молекулах которых две двойные связи образуют сопряженную систему.
Химические свойства алкадиенов похожи на свойства алкенов. Алкадиены также легко вступают в реакции присоединения и окисления.
| Химические свойства сопряженных алкадиенов отличаются от алкенов некоторыми особенностями, которые обусловлены делокализацией электронной плотности π-связей. |
1. Реакции присоединения
Для алкадиенов характерны реакции присоединения по одной из двойных связей С=С, либо по обоим связям. Реакции с водой, галогенами и галогеноводородами протекают по механизму электрофильного присоединения. При присоединении одной молекулы реагента к алкадиену рвется только одна двойная связь. При присоединении двух молекул реагента к алкадиену разрываются обе двойные связи.
| Помимо присоединения по одной из двух двойных связей (1,2-присоединение), для сопряженных диенов характерно так называемое 1,4-присоединение, когда в реакции участвует вся делокализованная система из двух двойных связей, реагент присоединяется к 1 и 4 атому углерода сопряженной системы, а двойная связь образуется между 2 и 3 атомами углерода. |
1.1. Гидрирование алкадиенов
Гидрирование алкадиенов протекает в присутствии металлических катализаторов, при нагревании и под давлением.
При присоединении одной молекулы водорода к дивинилу образуется смесь продуктов (бутен-1 и бутен-2):

Соотношение продуктов 1,2- и 1,4- присоединения зависит от условий реакции.
| При комнатной и повышенной температуре основным продуктом реакции является 1,4-продукт (бутен-2). |
При полном гидрировании дивинила образуется бутан:

1.2. Галогенирование алкадиенов
Присоединение галогенов к алкадиенам происходит даже при комнатной температуре в растворе (растворители — вода, CCl4).
| При взаимодействии с алкадиенами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на двойную связь. |
| Например, при взаимодействии бутадиена-1,3 с бромной водой преимущественно протекает 1,4 присоединение и образуется 1,4-дибромбутен-2: |

Побочным продуктом бромирования дивинила является 3,4-дибромбутен-1:

При полном бромировании дивинила образуется 1,2,3,4-тетрабромбутан:

1.3. Гидрогалогенирование алкадиенов
Алкадиены взаимодействуют с галогеноводородами. При присоединении хлороводорода к бутадиену-1,3 преимущественно образуется 1-хлорбутен-2:
3-Хлорбутен-1 образуется в небольшом количестве.
При присоединении полярных молекул к алкадиенам образуется смесь изомеров. При этом выполняется правило Марковникова.
| Правило Марковникова: при присоединении полярных молекул типа НХ к алкадиенам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода при двойной связи. |
1.4. Полимеризация
Полимеризация — это процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
nM → Mn (M – это молекула мономера)
| Полимеризация алкадиенов протекает преимущественно по 1,4-механизму, при этом образуется полимер с кратными связями, называемый каучуком. |
Продукт полимеризации дивинила (бутадиена) называется искусственным каучуком:

При полимеризации изопрена образуется природный (натуральный) каучук:

2. Окисление алкадиенов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на мягкое и жесткое.
2.1. Мягкое окисление алкадиенов
Мягкое окисление алкадиенов протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкадиена разрываются только π-связи и окисляются атомы углерода при двойных связях. При этом образуются четырехатомные спирты.

| Обесцвечивание алкадиенами водного раствора перманганата калия, как и в случае алкенов – качественная реакция на двойную связь. |
2.2. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) происходит полный разрыв двойных связей С=С и связей С-Н у атомов углерода при двойных связях. При этом у окисляемых атомов углерода образуются связи с атомами кислорода.
Так, если у атома углерода окисляется одна связь, то образуется группа С-О-Н (спирт). При окислении двух связей образуется двойная связь с атомом углерода: С=О, при окислении трех связей — карбоксильная группа СООН, четырех — углекислый газ СО2.
Можно составить таблицу соответствия окисляемого фрагмента молекулы и продукта:
При окислении бутадиена-1,3 перманганатом калия в среде серной кислоты возможно образование щавелевой кислоты и углекислого газа:

2.3. Горение алкадиенов
Алкадиены, как и прочие углеводороды, горят в присутствии кислорода с образованием углекислого газа и воды.
В общем виде уравнение сгорания алкадиенов выглядит так:
| Например, уравнение сгорания бутадиена: |
1. Дегидрирование алканов
Отщепление водорода от бутана — это промышленный способ получения дивинила. Реакция протекает при нагревании в присутствии оксида хрома (III):

Изопрен получают каталитическим дегидрированием изопентана (2-метилбутана):

2. Синтез Лебедева
Н агревание этанола в присутствии катализатора (смесь оксидов Al2O3, MgO, ZnO) – это промышленный способ получения дивинила из этанола (синтез Лебедева).
При этом образуются бутадиен-1,3, вода и водород:

3. Дегидратация двухатомных спиртов
Под действием серной кислоты вода отщепляется от бутандиола-1,3. При этом образуется дивинил и вода:
4. Дегидрогалогенирование дигалогеналканов
Под действием спиртовых растворов щелочей протекает отщепление атомов галогена и водорода и образуются вода, соль и алкадиен.
При этом атомы галогенов в дигалогеналкане должны располагаться не у одного и не у соседних атомов углерода.
1,3-Дихлорбутан реагирует со спиртовым раствором гидроксида калия с образованием бутадиена-1,3:
Диеновыми называются углеводороды, которые содержат в своем составе две двойные связи. Общая формула алкадиенов СnH2n – 2. Атомы углерода по двойной связи находятся в состоянии sp 2 -гибридизации.
Диеновые углеводороды в зависимости от расположения двойных связей делятся на:
- углеводороды с кумулированными двойными связями:
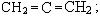
- углеводороды с сопряженными двойными связями:
- углеводороды с изолированными двойными связями:

Особый интерес среди диеновых углеводородов представляют углеводороды с сопряженными двойными связями. Наибольшее практическое значение имеют дивинил, или 1, 3 - бутадиен (легко сжижающийся газ, т. кип = – 4,5 °C), и изопрен, или 2 - метил - 1, 3 - бутадиен (жидкость с т. кип = 34 °С). По химическим свойствам диеновые углеводороды подобны алкенам. Они легко вступают в реакции присоединения и окисления. Однако сопряженные диены отличаются некоторыми особенностями, которые обусловлены делокализацией (рассредоточением) p-электронов. Молекула 1, 3 - бутадиена СН2 = СН - СН = СН2 содержит четыре атома углерода, которые находятся в состоянии sp 2 - гибридизации, и имеет плоское строение.
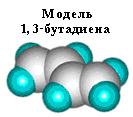
p-электроны двойных связей образуют единое p-электронное облако (сопряженную систему) и делокализованы между всеми атомами углерода.
Порядок связей между атомами углерода имеет промежуточное значение между одинарной и двойной, т.е. нет чисто одинарной и чисто двойных связей.
Получение диеновых углеводородов. Общие способы получения диенов аналогичны способам получения алкенов.
1. Дегидрирование алканов.
Этим путем получают в промышленности дивинил из бутана:
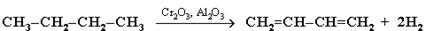
Каталитическим дегидрированием изопентана (2-метилбутана) получают изопрен:
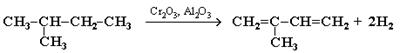
2. Синтез дивинила по Лебедеву:
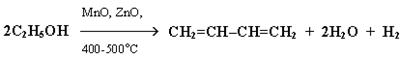
3. Дегидратация гликолей (двухатомных спиртов, или алкандиолов):
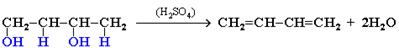
4. Действие спиртового раствора щелочи на дигалогеналканы:
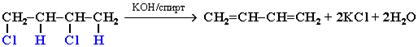
5. Получение из отходов бродильных производств:
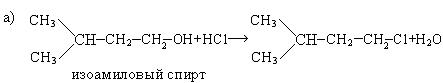
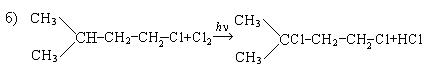
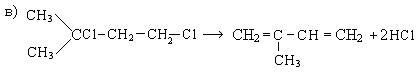
Химические свойства. Типичными реакциями диеновых углеводородов, так же как и алкенов, являются реакции электрофильного присоединения и полимеризации.
Реакции электрофильного присоединения (АdЕ). Электронные особенности сопряженных диенов приводят к тому, что реакции АdE протекают в 1, 2- и 1, 4 - положениях:
1. Галогенирование:
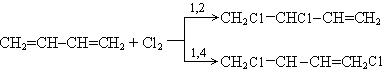
Механизм реакции:
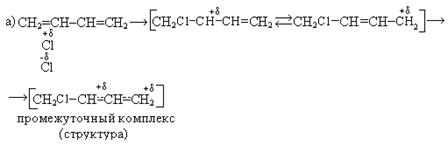
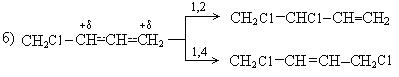
В зависимости от изменения условий реакции мы можем регулировать выходы продуктов 1, 2- и 1, 4 - присоединения.
Бромирование диеновых углеводородов проходит аналогично:
1, 2 - присоединение:
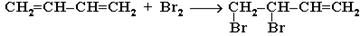
1, 4 - присоединение:
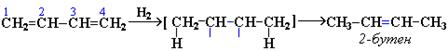
При избытке брома присоединяется еще одна его молекула по месту оставшейся двойной связи с образованием 1, 2, 3, 4 - тетрабромбутана.
2. Гидрогалогенирование. Реакция также протекает в 1, 2- и 1, 4 - положениях:
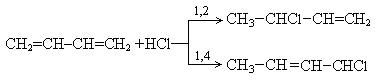
3. Гидрирование. При гидрировании 1, 3 - бутадиена преимущественно получается 2 - бутен, т.е. происходит 1, 4 - присоединение. При этом двойные связи разрываются, к крайним атомам углерода С1 и С4 присоединяются атомы водорода, а свободные валентности образуют двойную связь между атомами С2 и С3:
В присутствии катализатора Ni получается продукт полного гидрирования:
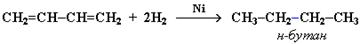
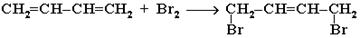
Присоединение галогенов, галогенводородов, воды и других полярных реагентов происходит, как уже сказано, по механизму электрофильного присоединения. К реакциям присоединения можно также отнести реакции димеризации, характерные для диенов. Подобные конденсации получили название диеновых синтезов.
4. Диеновый синтез (реакция Дильса-Альдера). В органическом синтезе широко применяется реакция присоединения к сопряженным диенам соединений, содержащих кратные связи (так называемых диенофилов). Реакция идет как 1, 4 - присоединение и приводит к образованию циклических продуктов:
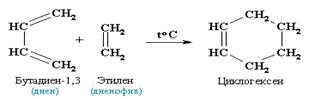
Реакции полимеризации. Диеновые углеводороды с сопряженными связями способны полимеризоваться с образованием каучуков. Важнейшими мономерами для получения каучуков являются дивинил, изопрен и 2, 3 - диметилбутадиен.

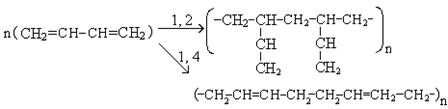
До 1950 года полимеризацию диенов проводили в условиях радикального механизма. При этом получались атактические структуры, далекие от свойств натурального каучука.
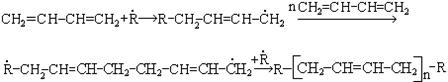
Использование катализаторов Цинглера-Натта позволило получать каучук с упорядоченной структурой:
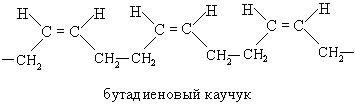
Основу полимерной структуры натурального каучука составляет цис-полиизопрен. Аналог натурального каучука был получен синтетически с использованием катализаторов Цинглера-Натта:
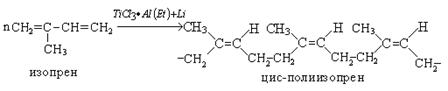
Транс-полиизопрен называется гуттаперчей:
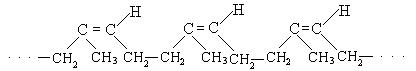
Для практического использования каучуки превращают в резину. Резина – это вулканизованный каучук, где в качестве наполнителя используется сажа. Суть процесса вулканизации заключается в том, что нагревание смеси каучука и серы приводит к образованию трехмерной сетчатой структуры из линейных макромолекул каучука, придавая ему повышенную прочность. Атомы серы присоединяются по двойным связям макромолекул и образуют между ними сшивающие дисульфидные мостики:
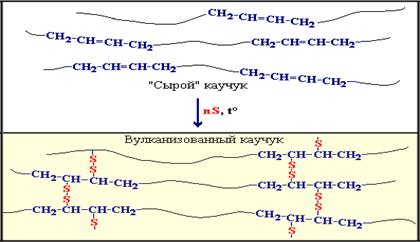
Сетчатый полимер более прочен и проявляет повышенную упругость – высокоэластичность (способность к высоким обратимым деформациям). В зависимости от количества сшивающего агента (серы) можно получать сетки с различной частотой сшивки. Предельно сшитый натуральный каучук – эбонит – не обладает эластичностью и представляет собой твердый материал. Вулканизация устраняет липкость полимеров, повышает эластичность. Резина используется для изготовления шин.
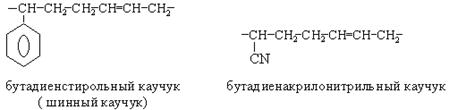
Большое значение имеет сополимеризация диеновых углеводородов с другими мономерами – стиролом, акрилонитрилом:
Диеновыми называются углеводороды, которые содержат в своем составе две двойные связи. Общая формула алкадиенов СnH2n – 2. Атомы углерода по двойной связи находятся в состоянии sp 2 -гибридизации.
Диеновые углеводороды в зависимости от расположения двойных связей делятся на:
- углеводороды с кумулированными двойными связями:
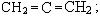
- углеводороды с сопряженными двойными связями:
- углеводороды с изолированными двойными связями:

Особый интерес среди диеновых углеводородов представляют углеводороды с сопряженными двойными связями. Наибольшее практическое значение имеют дивинил, или 1, 3 - бутадиен (легко сжижающийся газ, т. кип = – 4,5 °C), и изопрен, или 2 - метил - 1, 3 - бутадиен (жидкость с т. кип = 34 °С). По химическим свойствам диеновые углеводороды подобны алкенам. Они легко вступают в реакции присоединения и окисления. Однако сопряженные диены отличаются некоторыми особенностями, которые обусловлены делокализацией (рассредоточением) p-электронов. Молекула 1, 3 - бутадиена СН2 = СН - СН = СН2 содержит четыре атома углерода, которые находятся в состоянии sp 2 - гибридизации, и имеет плоское строение.

p-электроны двойных связей образуют единое p-электронное облако (сопряженную систему) и делокализованы между всеми атомами углерода.
Порядок связей между атомами углерода имеет промежуточное значение между одинарной и двойной, т.е. нет чисто одинарной и чисто двойных связей.
Получение диеновых углеводородов. Общие способы получения диенов аналогичны способам получения алкенов.
1. Дегидрирование алканов.
Этим путем получают в промышленности дивинил из бутана:
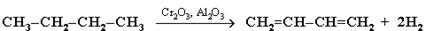
Каталитическим дегидрированием изопентана (2-метилбутана) получают изопрен:
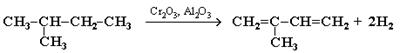
2. Синтез дивинила по Лебедеву:
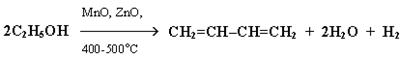
3. Дегидратация гликолей (двухатомных спиртов, или алкандиолов):

4. Действие спиртового раствора щелочи на дигалогеналканы:
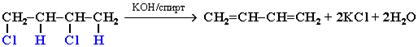
5. Получение из отходов бродильных производств:
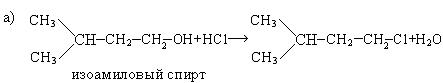
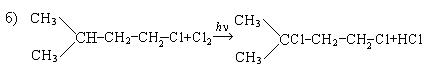

Химические свойства. Типичными реакциями диеновых углеводородов, так же как и алкенов, являются реакции электрофильного присоединения и полимеризации.
Реакции электрофильного присоединения (АdЕ). Электронные особенности сопряженных диенов приводят к тому, что реакции АdE протекают в 1, 2- и 1, 4 - положениях:
1. Галогенирование:

Механизм реакции:
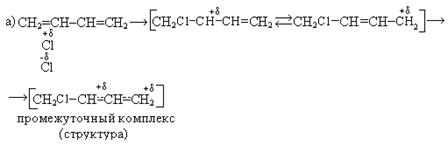

В зависимости от изменения условий реакции мы можем регулировать выходы продуктов 1, 2- и 1, 4 - присоединения.
Бромирование диеновых углеводородов проходит аналогично:
1, 2 - присоединение:
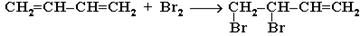
1, 4 - присоединение:
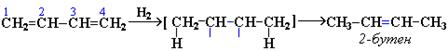
При избытке брома присоединяется еще одна его молекула по месту оставшейся двойной связи с образованием 1, 2, 3, 4 - тетрабромбутана.
2. Гидрогалогенирование. Реакция также протекает в 1, 2- и 1, 4 - положениях:

3. Гидрирование. При гидрировании 1, 3 - бутадиена преимущественно получается 2 - бутен, т.е. происходит 1, 4 - присоединение. При этом двойные связи разрываются, к крайним атомам углерода С1 и С4 присоединяются атомы водорода, а свободные валентности образуют двойную связь между атомами С2 и С3:
В присутствии катализатора Ni получается продукт полного гидрирования:
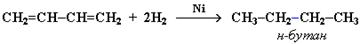
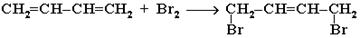
Присоединение галогенов, галогенводородов, воды и других полярных реагентов происходит, как уже сказано, по механизму электрофильного присоединения. К реакциям присоединения можно также отнести реакции димеризации, характерные для диенов. Подобные конденсации получили название диеновых синтезов.
4. Диеновый синтез (реакция Дильса-Альдера). В органическом синтезе широко применяется реакция присоединения к сопряженным диенам соединений, содержащих кратные связи (так называемых диенофилов). Реакция идет как 1, 4 - присоединение и приводит к образованию циклических продуктов:

Реакции полимеризации. Диеновые углеводороды с сопряженными связями способны полимеризоваться с образованием каучуков. Важнейшими мономерами для получения каучуков являются дивинил, изопрен и 2, 3 - диметилбутадиен.

До 1950 года полимеризацию диенов проводили в условиях радикального механизма. При этом получались атактические структуры, далекие от свойств натурального каучука.
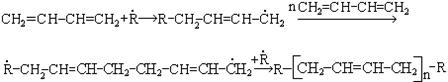
Использование катализаторов Цинглера-Натта позволило получать каучук с упорядоченной структурой:

Основу полимерной структуры натурального каучука составляет цис-полиизопрен. Аналог натурального каучука был получен синтетически с использованием катализаторов Цинглера-Натта:

Транс-полиизопрен называется гуттаперчей:

Для практического использования каучуки превращают в резину. Резина – это вулканизованный каучук, где в качестве наполнителя используется сажа. Суть процесса вулканизации заключается в том, что нагревание смеси каучука и серы приводит к образованию трехмерной сетчатой структуры из линейных макромолекул каучука, придавая ему повышенную прочность. Атомы серы присоединяются по двойным связям макромолекул и образуют между ними сшивающие дисульфидные мостики:

Сетчатый полимер более прочен и проявляет повышенную упругость – высокоэластичность (способность к высоким обратимым деформациям). В зависимости от количества сшивающего агента (серы) можно получать сетки с различной частотой сшивки. Предельно сшитый натуральный каучук – эбонит – не обладает эластичностью и представляет собой твердый материал. Вулканизация устраняет липкость полимеров, повышает эластичность. Резина используется для изготовления шин.
Большое значение имеет сополимеризация диеновых углеводородов с другими мономерами – стиролом, акрилонитрилом:
Алкадиены - непредельные (ненасыщенные) углеводороды, имеющие в молекуле две двойных связи С=С. Каждая такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкадиены также называют диеновыми углеводородами. Первый член гомологического ряда - пропадиен - CH2=C=CH2. Общая формула их гомологического ряда - CnH2n-2.
Номенклатура и изомерия алкадиенов
Названия алкенов формируются путем добавления суффикса "диен" к названию алкана с соответствующим числом: пропадиен, бутадиен, пентадиен и т.д.
При составления названия алкадиена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойные связи. Нумерация атомов углерода в ней начинается с того края, к которому ближе двойная связь. В конце названия указывают атомы углерода, у которых начинается двойная связь.
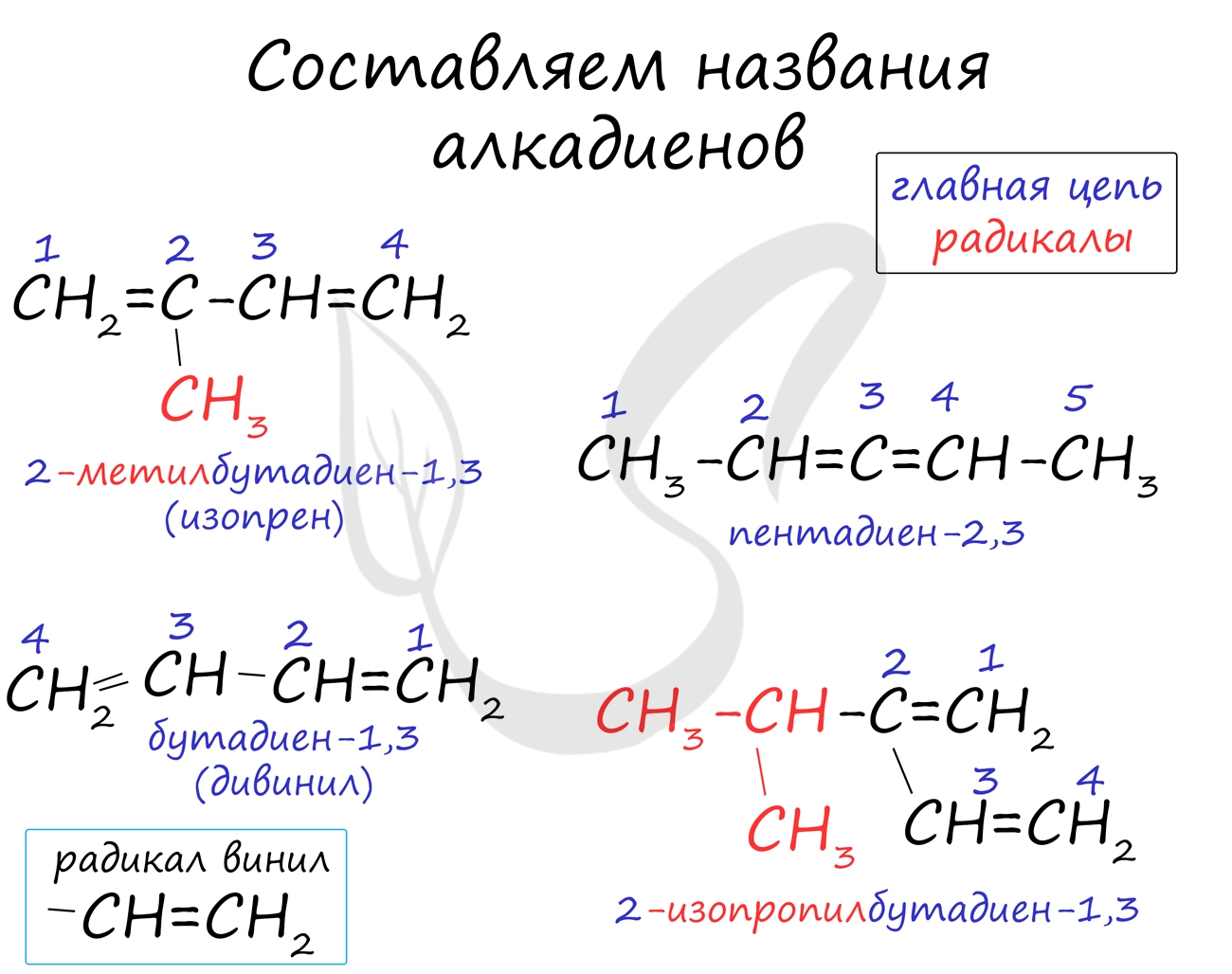
Атомы углерода, прилежащие к двойной связи находятся в sp 2 гибридизации.
Для алкадиенов характерна изомерия углеродного скелета, положения двойных связей, межклассовая изомерия с алкинами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
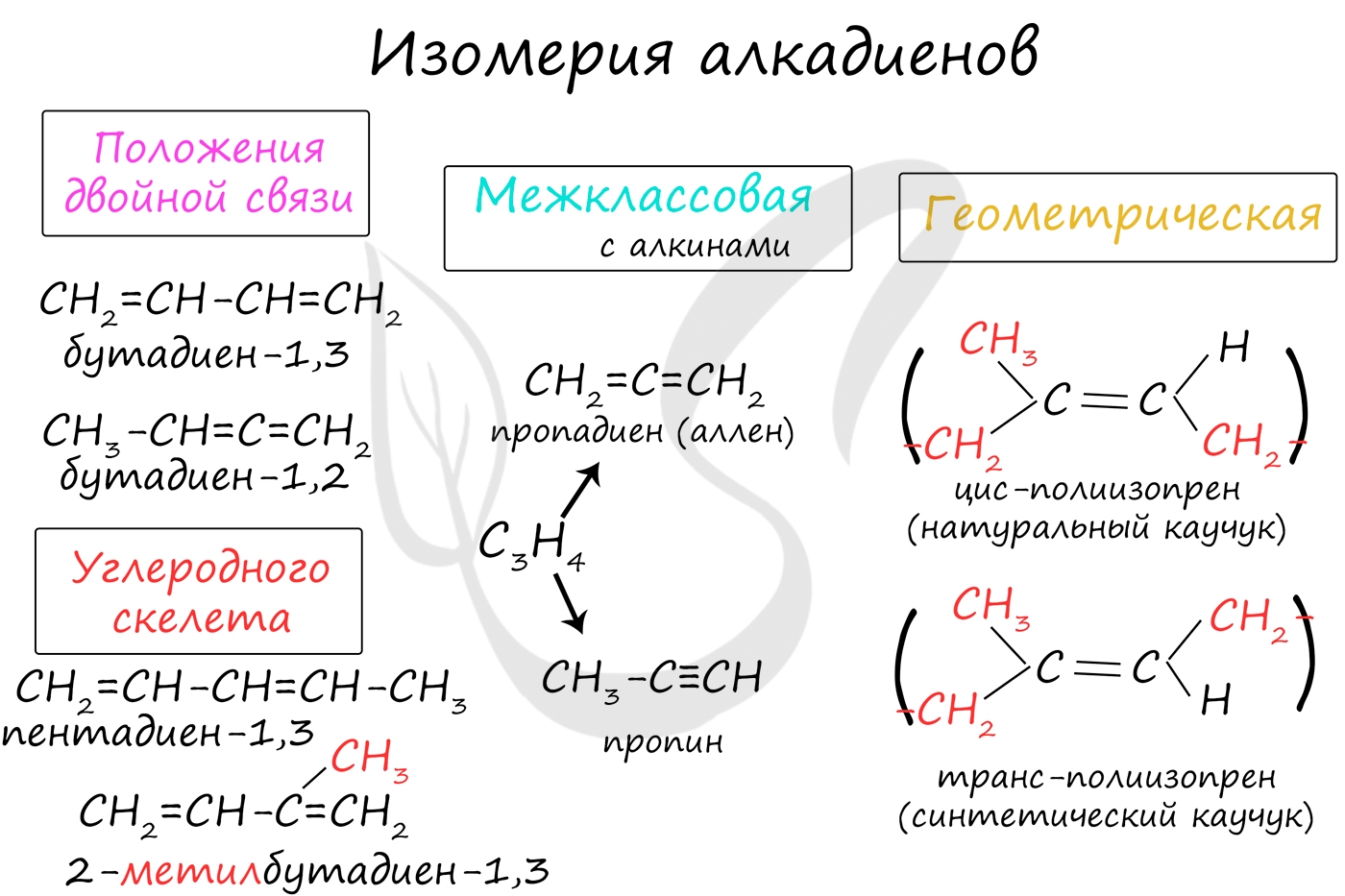
Также к синтетическим каучукам относится бутадиен-1,3 (дивинил).
Классификация по положению двойных связей
-
Кумулированные двойные связи
В случае, если две двойные связи прилежат к одному и тому же атому углерода.
Пример - пропадиен-1,2 (аллен) - CH2=C=CH2
В молекуле аллена крайние атомы углерода находятся в состоянии sp 2 -гибридизации, а центральный атом - sp-гибридизации.
В случае, если две двойные связи разделены одной одинарной связью. В результате такого взаиморасположения в молекулах возникает сопряжение: формируется единое π-электронное облако.
Помните, что сигма-связи (σ-связи) перекрываются вдоль линии плоскости, а пи-связи (π-связи) над и под линией плоскости (линией, соединяющей центры атомов).
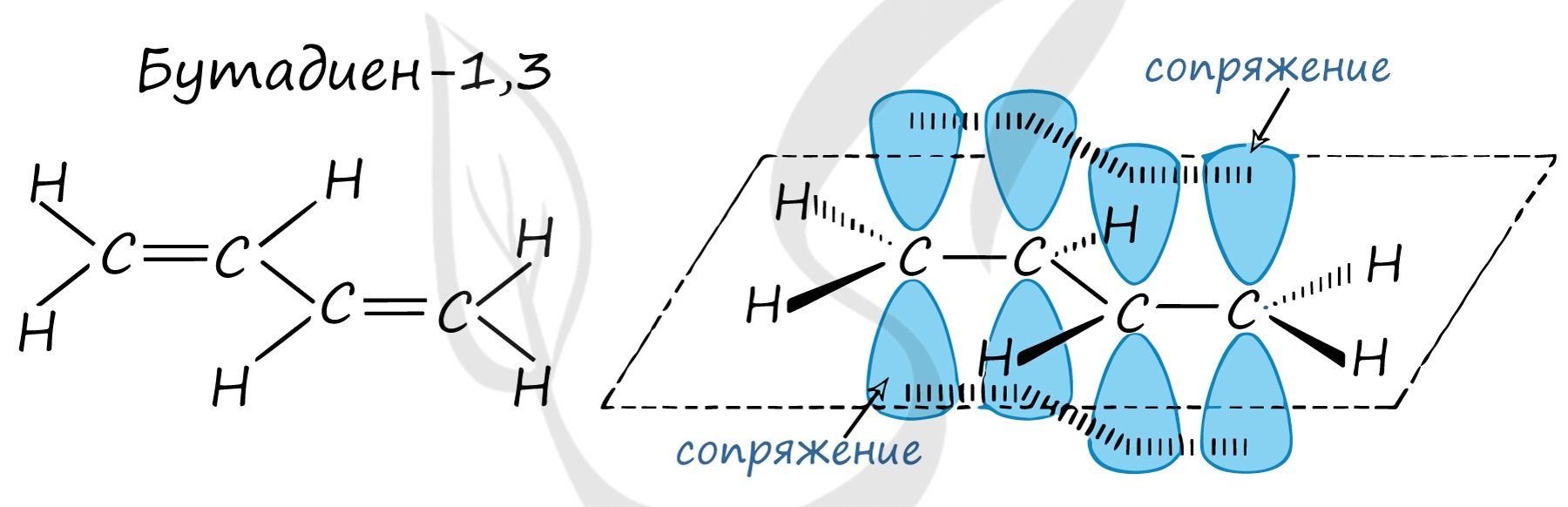
В случае, если две двойные связи разделены двумя и более одинарными связями.
Получение алкадиенов
В результате реакции молекулы алкана, содержащей два атома галогена, со спиртовым (!) раствором щелочи получается алкадиен. В зависимости от положения галогенов возможны разные варианты.
Отщепление идет по правилу Зайцева: атом водорода отщепляется от соседнего, наименее гидрированного атома углерода.
Сергей Васильевич Лебедев в 1927 году разработал первый промышленный способ получения синтетического каучука из этилового спирта.
Каучук занимает важное место в промышленности благодаря своим свойствам: водонепроницаемости, эластичности и способности к электроизоляции. Путем вулканизации из каучука получают резину, используемую повсеместно.

В результате отщепления водорода от молекулы алкана образуются двойные связи. Дегидрирование происходит при повышенной температуре и в присутствии катализатора.
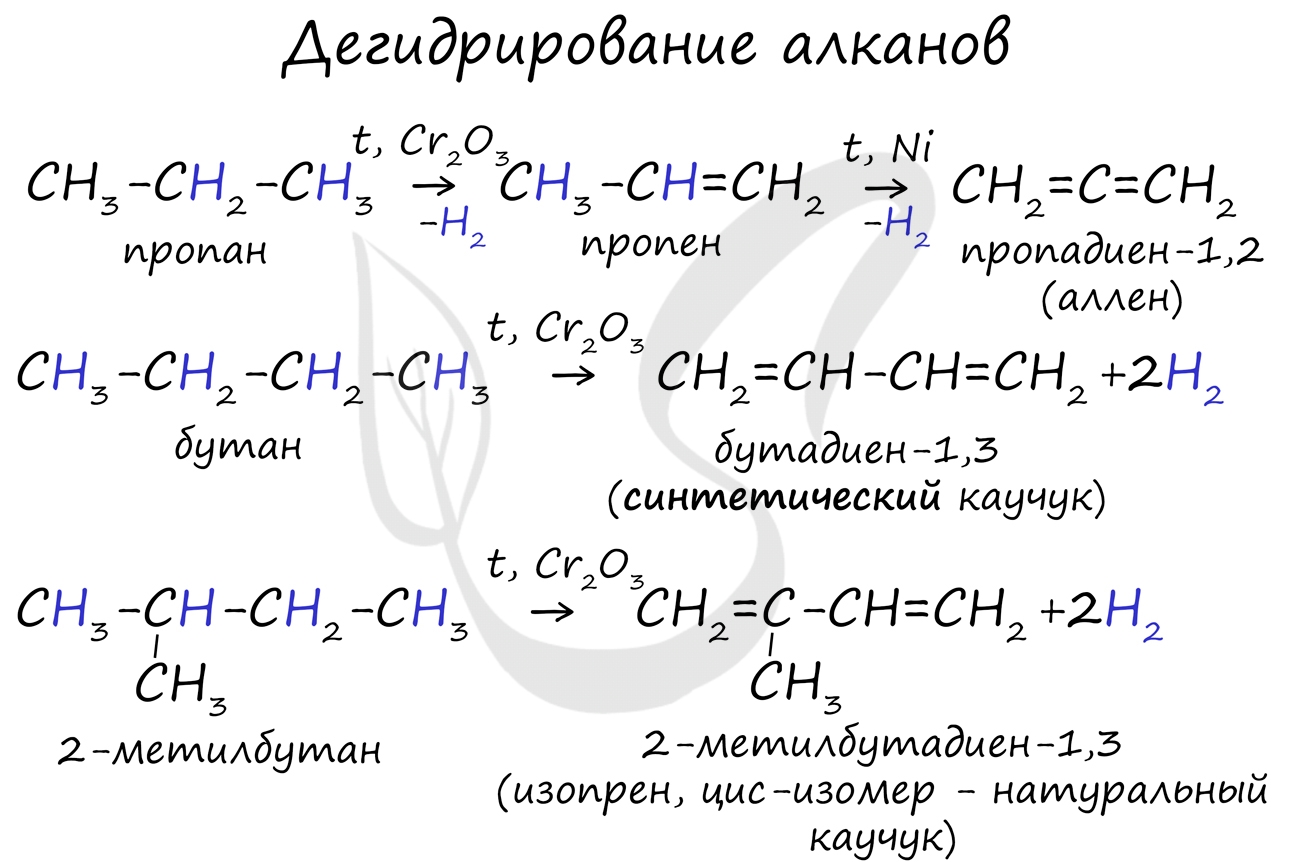
Химические свойства алкадиенов
Алкадиены - ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны. Наличие сопряженных двойных связей увеличивает реакционную способность молекулы и обуславливает необычный механизм некоторых реакций.
Водород присоединяется к атомам углерода, образующим двойную связь. Пи-связь (π-связь) рвется, остается единичная сигма-связь (σ-связь).
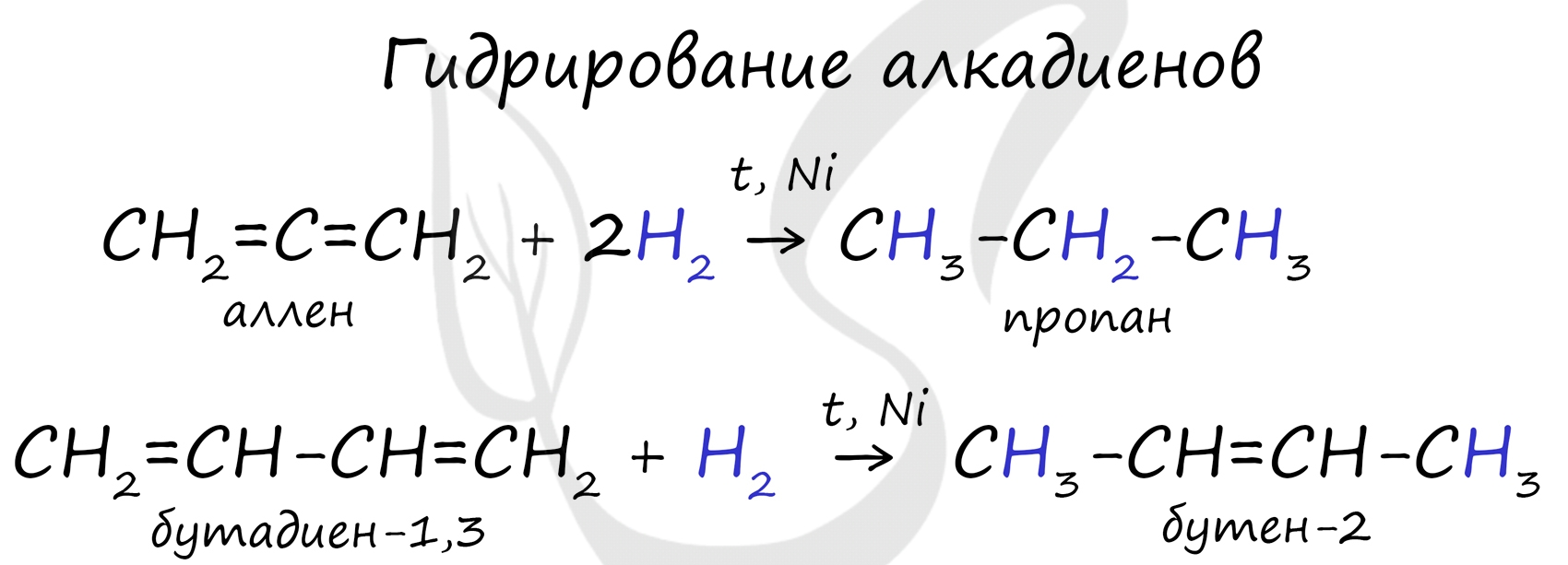
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение брома по кратным связям к органическому веществу.
В случае, если двойные связи находятся в сопряжении, выход продуктов во многом зависит от температуры. Например, в ходе галогенирования бутадиена-1,3 при -80°C преимущественно получается продукт 1,2-присоединения, а при +60°C - продукт 1,4-присоединения.
Алкадиены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена - к наименее гидрированному атому углерода.
При горении алкадиены, как и все органические соединения, сгорают с образованием углекислого газа и воды - полное окисление.
Полимеризация - цепная реакция синтеза полимеров, при котором молекула полимера образуется путем последовательного соединения молекул мономеров.
Индекс "n", степень полимеризации, обозначает число мономерных звеньев, которые входят в состав полимера.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Читайте также:


