Личностные качества бутлерова кратко
Обновлено: 05.07.2024
Гипермаркет знаний>>Химия>>Химия 11 класс>> Химия: Теория строения химических соединений А. М. Бутлерова
Предпосылки создания теории
Накопление фактологического материала
Ко времени создания А. М. Бутлеровым теории химического строения органических веществ (1861 г.) были известны многие десятки и сотни тысяч органических соединений.
В конце XVIII в. французский химик А. Лавуазье показал, что вещества, получаемые из организмов растений и животных (отсюда их название — органические вещества), содержат, в отличие от минеральных, лишь немногие элементы: углерод, водород, кислород, азот, а иногда фосфор и серу. Так как углерод обязательно присутствует во всех органических соединениях, то органическую химию по предложению А. Кекуле с середины XIX в. стали называть химией соединений углерода.
Позднее немецкий химик К. Шорлеммер дал более точное определение этой науки: органическая химия — это химия углеводородов и их производных (то есть соединений, которые могут быть получены на основе углеводородов).
Работы предшественников А. М. Бутлерова
Такие формулы несколько похожи на современные. Но сторонники теории типов не считали их отражающими реальное строение веществ и писали множество различных формул одного соединения в зависимости от химических реакций, которые пытались записать с помощью этих формул. Строение молекул они считали принципиально непознаваемым, что наносило вред развитию науки.
• в 1828 г. Ф. Велер из неорганического вещества (цианата аммония) синтезировал мочевину;
• в 1842 г. русский химик Н. Н. Зинин получил анилин;
• в 1845 г. немецкий химик А. Кольбе синтезировал уксусную кислоту;
• в 1854 г. французский химик М. Бертло синтезировал жиры, и, наконец,
• в 1861 г. сам А. М. Бутлеров синтезировал сахароподобное вещество.
5. В середине XVIII в. химия становится более строгой наукой. В результате работ Э. Франкланда и А. Кекуле утвердилось понятие о валентности атомов химических элементов. Кекуле развил представление о четырехвалентности углерода. Благодаря трудам Канниццаро четче стали понятия об атомных и молекулярных массах, уточнены их значения и способы определения.
В 1860 г. более 140 ведущих химиков из разных стран Европы собрались на международный конгресс в г. Карлсруэ. Конгресс стал очень важным событием в истории химии: были обобщены успехи науки и подготовлены условия для нового этапа в развитии органической химии — появления теории химического строения органических веществ А. М. Бутлерова (1861 г.), а также для фундаментального открытия Д. И. Менделеева — Периодического закона и системы химических элементов (1869 г.).
Личностные качества А. М. Бутлерова
А. М. Бутлерова отличали энциклопедичность химических знаний, умение анализировать и обобщать факты, прогнозировать. Он предсказал существование изомера бутана, а затем получил его, равно как изомер бутилена — изобутилен.
Бутлеров Александр Михайлович (1828—1886)
А. М. Бутлеров создал первую в России школу химиков-органиков, из которой вышли блестящие ученые: В. В. Марковников, Д. П. Коновалов, А. Е. Фаворский и др.
Основные положения теории строения химических соединений
Теория химического строения органических соединений, выдвинутая А. М. Бутлеровым во второй половине прошлого века (1861 г.), была подтверждена работами многих ученых, в том числе учениками Бутлерова и им самим. Оказалось возможным на ее основе объяснить многие явления, до той поры не имевшие толкования: изомерию, гомологию, проявление атомами углерода четырехвалентности в органических веществах. Теория выполнила и свою прогностическую функцию: на ее основе ученые предсказывали существование неизвестных еще соединений, описывали свойства и открывали их.
Так, в 1862—1864 гг. А. М. Бутлеров рассмотрел изомерию пропиловых, бутиловых и амиловых спиртов, определил число возможных изомеров и вывел формулы этих веществ. Существование их позднее было экспериментально доказано, причем некоторые из изомеров синтезировал сам Бутлеров.
В течение XX в. положения теории химического строения химических соединений были развиты на основе новых воззрений, распространившихся в науке: теории строения атома, теории химической связи, представлений о механизмах химических реакций. В настоящее время эта теория имеет универсальный характер, то есть справедлива не только для органических веществ, но и для неорганических.
Первое положение. Атомы в молекулах соединяются в определенном порядке в соответствии с их валентностью. Углерод во всех органических и в большинстве неорганических соединений четырехвалентен.
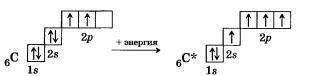
Очевидно, что последнюю часть первого положения теории легко объяснить тем, что в соединениях атомы углерода находятся в возбужденном состоянии:
а) атомы четырехвалентного углерода могут соединяться друг с другом, образуя различные цепи:
- открытые разветвленные
- открытые неразветвленные
- замкнутые
б) порядок соединения атомов углерода в молекулах может быть различным и зависит от вида ковалентной химической связи между атомами углерода — одинарной или кратной (двойной и тройной).
Второе положение. Свойства веществ зависят не только от их качественного и количественного состава, но и от строения их молекул.
Это положение объясняет явление изомерии. Вещества, имеющие одинаковый состав, но разное химическое или пространственное строение, а следовательно, и разные свойства, называют изомерами. Основные виды изомерии:
Структурная изомерия, при которой вещества различаются порядком связи атомов в молекулах:
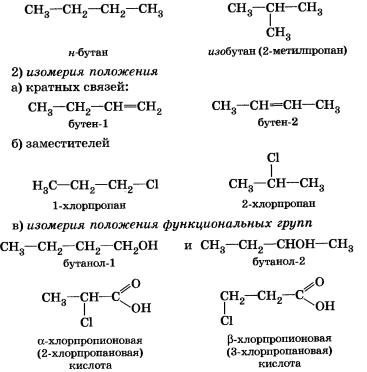
1) изомерия углеродного скелета
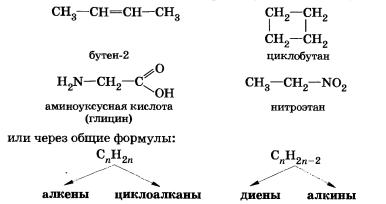
3) изомерия гомологических рядов (межклассовая)
Пространственная изомерия, при которой молекулы веществ отличаются не порядком связи атомов, а положением их в пространстве: цис-транс-изомерия (геометрическая).
Эта изомерия характерна для веществ, молекулы которых имеют плоское строение: алкенов, циклоалканов и др.
К пространственной изомерии относится и оптическая (зеркальная) изомерия.
Четыре одинарные связи вокруг атома углерода, как вы уже знаете, расположены тетраэдрически. Если атом углерода связан с четырьмя различными атомами или группами, то возможно разное расположение этих групп в пространстве, то есть две пространственные изомерные формы.
Две зеркальные формы аминокислоты аланина (2-аминопропановой кислоты) изображены на рисунке 17.
Представьте себе, что молекулу аланина поместили перед зеркалом. Группа —NH2 находится ближе к зеркалу, поэтому в отражении она будет впереди, а группа —СООН — на заднем плане и т. д. (см. изображение справа). Алании существует в двух пространственных формах, которые при наложении не совмещаются одна с другой.
Универсальность второго положения теории строения химических соединений подтверждает существование неорганических изомеров.

Так, первый из синтезов органических веществ — синтез мочевины, проведенный Велером (1828 г.), показал, что изомерны неорганическое вещество — цианат аммония и органическое — мочевина:
Если заменить атом кислорода в мочевине на атом серы, то получится тиомочевина, которая изомерна роданиду аммония, хорошо известному вам реактиву на ионы Fе 3+ . Очевидно, что тиомочевина не дает этой качественной реакции.
Третье положение. Свойства веществ зависят от взаимного влияния атомов в молекулах.
![]()
Например, в уксусной кислоте в реакцию со щелочью вступает только один из четырех атомов водорода. На основании этого можно предположить, что только один атом водорода связан с кислородом:
С другой стороны, из структурной формулы уксусной кислоты можно сделать вывод о наличии в ней одного подвижного атома водорода, то есть о ее одноосновности.
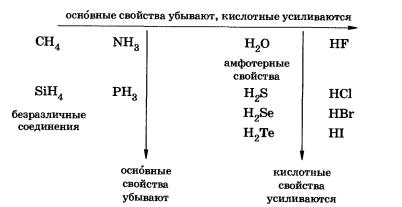
Чтобы убедиться в универсальности положения теории строения о зависимости свойств веществ от взаимного влияния атомов в молекулах, которое существует не только у органических, но и у неорганических соединений, сравним свойства атомов водорода в водородных соединениях неметаллов. Они имеют молекулярное строение и в обычных условиях представляют собой газы или летучие жидкости. В зависимости от положения неметалла в Периодической системе Д. И. Менделеева можно выявить закономерность в изменении свойств таких соединений:
Метан не взаимодействует с водой. Отсутствие основных свойств у метана объясняется насыщенностью валентных возможностей атома углерода.
Аммиак проявляет основные свойства. Его молекула способна присоединять к себе ион водорода за счет его притяжения к неподеленной электронной паре атома азота (донорно-акцепторный механизм образования связи).
У фосфина РН3 основные свойства слабо выражены, что связано с радиусом атома фосфора. Он значительно больше радиуса атома азота, поэтому атом фосфора слабее притягивает к себе атом водорода.
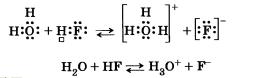
В периодах слева направо увеличиваются заряды ядер атомов, уменьшаются радиусы атомов, увеличивается сила отталкивания атома водорода с частичным положительным зарядом §+, а потому кислотные свойства водородных соединений неметаллов усиливаются.
В главных подгруппах сверху вниз увеличиваются радиусы атомов элементов, атомы неметаллов с 5- слабее притягивают атомы водорода с 5+, уменьшается прочность водородных соединений, они легко диссоциируют, а потому их кислотные свойства усиливаются.
Различная способность водородных соединений неметаллов к отщеплению или присоединению катионов водорода в растворах объясняется неодинаковым влиянием, которое оказывает атом неметалла на атомы водорода.
Различным влиянием атомов в молекулах гидроксидов, образованных элементами одного периода, объясняется также изменение их кислотно-основных свойств.
Гидроксид натрия NаОН. Так как у атома водорода радиус очень мал, его сильнее Притягивает к себе атом кислорода и связь между атомами водорода и кислорода будет более прочной, чем между атомами натрия и кислорода. Гидроксид алюминия Аl(0Н)3 проявляет амфотерные свойства.
В хлорной кислоте НСlO4 атом хлора с относительно большим положительным зарядом прочнее связан с атомом кислорода и сильнее отталкивает от себя атом водорода с 6+. Диссоциация происходит по кислотному типу.
Основные направления развития теории строения химических соединений и ее значение
Во времена А. М. Бутлерова в органической химии широко использовали эмпирические (молекулярные) и структурные формулы. Последние отражают порядок соединения атомов в молекуле согласно их валентности, которая обозначается черточками.
Для простоты записи часто используют сокращенные структурные формулы, в которых черточками обозначают только связи между атомами углерода или углерода и кислорода.
Сокращенные структурные формулы
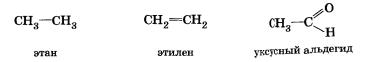
Затем, по мере развития знаний о природе химической связи и о влиянии электронного строения молекул органических веществ на их свойства, стали пользоваться электронными формулами, в которых ковалентную связь условно обозначают двумя точками. В таких формулах часто показывают направление смещения электронных пар в молекуле.
Именно электронным строением веществ объясняют мезомерный и индукционный эффекты.
Индукционный эффект — смещение электронных пар гамма-связей от одного атома к другому вследствие их разной электроотрицательности. Обозначается (—>).
Индукционный эффект атома (или группы атомов) отрицательный (-/), если этот атом имеет большую электроотрицательность (галогены, кислород, азот), притягивает к себе электроны гамма-связи и приобретает при этом частичный отрицательный заряд. Атом (или группа атомов) имеет положительный индукционный эффект (+/), если он отталкивает электроны гамма-связей. Этим свойством обладают некоторые предельные радикалы С2H5 ). Вспомните правило Марковникова о том, как присоединяется к алкенам (пропену) водород и галоген галогеноводорода и вы поймете, что это правило носит частный характер. Сравните эти два примера уравнений реакций:

[[Теория_строения_химических_соединений_А._М._Бутлерова|]]
В молекулах отдельных веществ проявляются и индукционный, и мезомерный эффекты одновременно. В этом случае они или усиливают друг друга (в альдегидах, карбоновых кислотах), или взаимно ослабляются (в хлорвиниле).
Результатом взаимного влияния атомов в молекулах является перераспределение электронной плотности.
Идею о пространственном направлении химических связей впервые высказали французский химик Ж. А. Ле Бель и голландский химик Я. X. Вант-Гофф в 1874 г. Предположения ученых полностью подтвердила квантовая химия. На свойства веществ значительное влияние оказывает пространственное строение их молекул. Например, мы уже приводили формулы цис- и транс-изомеров бутена-2, которые отличаются по своим свойствам (см. рис. 16).
Средняя энергия связи, которую необходимо разорвать при переходе одной формы в другую, равна примерно 270 кДж/моль; такого большого количества энергии при комнатной температуре нет. Для взаимного перехода форм бутена-2 из одной в другую необходимо одну ковалентную связь разорвать и взамен образовать другую. Иными словами, этот процесс — пример химической реакции, а обе рассмотренные формы бутена-2 представляют собой различные химические соединения.
Вы, очевидно, помните, что важнейшей проблемой при синтезе каучука было получение каучука стереорегулярного строения. Необходимо было создать такой полимер, в котором структурные звенья располагались бы в строгом порядке (натуральный каучук, например, состоит только из цис-звеньев), ведь от этого зависит такое важнейшее свойство каучука, как его эластичность.
Современная органическая химия различает два основных типа изомерии: структурную (изомерию цепи, изомерию положения кратных связей, изомерию гомологических рядов, изомерию положения функциональных групп) и стереоизоме-рию (геометрическую, или цис-транс-изомерию, оптическую, или зеркальную, изомерию).
Итак, вы смогли убедиться в том, что второе положение теории химического строения, четко сформулированное А. М. Бутлеровым, было неполным. С современных позиций это положение требует дополнения:
свойства веществ зависят не только от их качественного и количественного состава, но и от их:
Создание теории строения веществ сыграло важнейшую роль в развитии органической химии. Из науки преимущественно описательной она превращается в науку созидательную, синтезирующую, появилась возможность судить о взаимном влиянии атомов в молекулах различных веществ (см. табл. 10). Теория строения создала предпосылки для объяснения и прогнозирования различных видов изомерии органических молекул, а также направлений и механизмов протекания химических реакций.
На основе этой теории химики-органики создают вещества, которые не только заменяют природные, но по своим свойствам значительно их превосходят. Так, синтетические красители гораздо лучше и дешевле многих природных, например известных в древности ализарина и индиго. В больших количествах производят синтетические каучуки с самыми разнообразными свойствами. Широкое применение находят пластмассы и волокна, изделия из которых используют в технике, быту, медицине, сельском хозяйстве.
Значение теории химического строения А. М. Бутлерова для органической химии можно сравнить со значением Периодического закона и Периодической системы химических элементов Д. И. Менделеева для неорганической химии. Недаром в обеих теориях так много общего в путях их становления, направлениях развития и общенаучном значении. Впрочем, в истории любой другой ведущей научной теории (теории Ч. Дарвина, генетике, квантовой теории и т. д.) можно найти такие общие этапы.
1. Установите параллели между двумя ведущими теориями химии — Периодическим законом и Периодической системой химических элементов Д. И. Менделеева и теорией химического строения органических соединений А. М. Бутлерова по следующим признакам: общее в предпосылках, общее в направлениях их развития, общее в прогностической роли.
2. Какую роль сыграла теория строения химических соединений в становлении Периодического закона?
3. Какие примеры из неорганической химии подтверждают универсальность каждого из положений теории строения химических соединений?
4. Фосфористая кислота Н3РО3 относится к двухосновным кислотам. Предложите ее структурную формулу и рассмотрите взаимное влияние атомов в молекуле этой кислоты.
5. Напишите изомеры, имеющие состав С3Н8O. Назовите их по систематической номенклатуре. Определите виды изомерии.
6. Известны следующие формулы кристаллогидратов хлорида хрома(III): [Сг(Н20)6]Сl3; [Сг(Н20)5Сl]Сl2 • Н20; [Сг(Н20)4 * С12]Сl • 2Н2О. Как вы назовете описанное явление?
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
Свидетельство и скидка на обучение каждому участнику
Зарегистрироваться 15–17 марта 2022 г.

Описание презентации по отдельным слайдам:

Теория строения
химических соединений
А. М. Бутлерова


Теория строения органических соединений
Теория химического строения органических соединений, выдвинутая А. М. Бутлеровым во второй половине прошлого века (1861 г.), была подтверждена работами многих ученых, в том числе учениками Бутлерова и им самим.
Оказалось возможным на ее основе объяснить многие явления, до той поры не имевшие толкования: изомерию, гомологию, проявление атомами углерода четырехвалентности в органических веществах.
Теория выполнила и свою прогностическую функцию: на ее основе ученые предсказывали существование неизвестных еще соединений, описывали свойства и открывали их.

Основные положения теории строения химических соединенй
1. Атомы в молекулах соединяются в определенном порядке в соответствии с их валентностью. (Углерод четырехвалентен).
а) атомы четырехвалентного углерода могут соединяться друг с другом, образуя различные цепи:
открытые неразветвленные
замкнутые
б) порядок соединения атомов углерода в молекулах может быть различным и зависит от вида ковалентной химической связи между атомами углерода — одинарной или кратной (двойной и тройной):

Второе положение
Свойства веществ зависят не только от их качественного и количественного состава, но и от строения их молекул.
Это положение объясняет явление изомерии.
Вещества, имеющие одинаковый состав, но разное химическое или пространственное строение, а следовательно, и разные свойства, называют изомерами.

Виды изомерии:
Структурная ( изомерия углеродного скелета; изомерия положения; изомерия гомологических рядов)
Пространственная ( цис -, трансизомерия)

Структурная изомерия
Структурная изомерия, при которой вещества различаются порядком связи атомов в молекулах:
1) изомерия углеродного скелета
2) изомерия положения
бутен-1
б) заместителей
1-хлорпропан
2-хлорпропан
в) изомерия положения функциональных групп
3) изомерия гомологических рядов (межклассовая)

Пространственная изомерия
Пространственная изомерия, при которой молекулы веществ отличаются не порядком связи атомов, а положением их в пространстве: цис-, трансизомерия (геометрическая).

Третье положение
Третье положение. Свойства веществ зависят от взаимного влияния атомов в молекулах.
Например, в уксусной кислоте в реакцию со щелочью вступает только один из четырех атомов водорода. На основании этого можно предположить, что только один атом водорода связан с кислородом:
С другой стороны, из структурной формулы уксусной кислоты можно сделать вывод о наличии в ней одного подвижного атома водорода, то есть о ее одноосновности.

Создание теории строения веществ сыграло важнейшую роль в развитии органической химии.:
1. Из науки преимущественно описательной она превращается в науку созидательную, синтезирующую, появилась возможность судить о взаимном влиянии атомов в молекулах различных веществ.
2. Теория строения создала предпосылки для объяснения и прогнозирования различных видов изомерии органических молекул, а также направлений и механизмов протекания химических реакций.
3. На основе этой теории химики-органики создают вещества, которые не только заменяют природные, но по своим свойствам значительно их превосходят. Так, синтетические красители гораздо лучше и дешевле многих природных, например известных в древности ализарина и индиго. В больших количествах производят синтетические каучуки с самыми разнообразными свойствами. Широкое применение находят пластмассы и волокна, изделия из которых используют в технике, быту, медицине, сельском хозяйстве.
Значение теории химического строения А. М. Бутлерова для органической химии можно сравнить со значением Периодического закона и Периодической системы химических элементов Д. И. Менделеева для неорганической химии.
А.М. Бутлеров – один из величайших русских ученых, он русский и по ученому образованию, и по оригинальности трудов.
“… я люблю свою страну, как мать, а свою науку – как дух, который благословляет, освещает и объединяет все народы для блага и мирного развития духовных и материальных богатств”.
При изучении этого раздела мы с учащимися выбрали форму защиты учебных проектов.
Защита учебного проекта включает в себя написание реферата и его презентацию другим участникам.
- Выбор темы учебного проекта.
- Написание реферата.
- Защита проекта.
- Дмитрий Иванович Менделеев – гениальный русский химик.
- Александр Михайлович Бутлеров – величайший русский ученый.
- Гроссе Э. Химия для любознательных. 1987 г.
- Тищенко В.Е., Младенцев М.Н. Дмитрий Иванович Менделеев, его жизнь и деятельность (Университетский период) 1861-1890 М. 1993 г.
- Дмитриев И.С. “Особая миссия Менделеева – Аргументы и факты, Санкт-Петербургский университет” 1996 г.
- Стариков В.И. “Д.И. Менделеев” 1984 г. Свердловск.
- Макареня А.А. “Менделеев в Петербурге” Лениздат. 1982 г.
- Годы жизни. Место рождения. Семья. Увлечение.
- Личностные качества.
- Совместная деятельность
- Предпосылки.
- История открытия.
- Научные теории
- Триумф.
- Основные направления развития двух теорий.
- Философские законы развития.
- Значение
П этап – этап самостоятельной работы учащихся с учебником и дополнительной литературой.
Ш этап – обмен информацией, запись учащимися основного содержания в тетрадь.
Годы жизни. Место рождения Семья. Увлечения.
Менделеев Дмитрий Иванович 1834-1907 гг
Выступления учащихся в тезисах:
Бутлеров А.М. – родился 15 сентября 1828 г. в городе Чистоноле Казанской губернии. Отец Бутлерова, Михаил Васильевич, участник Отечественной войны 1812 года, после отставки в чине подполковника жил в родовом селе Бутлеровка; мать Софья Александровна, скончалась в 19 лет, через несколько дней после рождения сына. Воспитанный отцом, человеком образованным, Саша во всем хотел походить на него.
Учился Бутлеров в частном пансионе, потом в первой Казанской гимназии. В 10 лет хорошо владел французским и немецким языками, занимался химическими опытами (один из них закончился взрывом, и преподаватели пансиона отправили провинившегося в карцер, повесив ему на грудь дощечку с надписью “великий химик”, собирал коллекции растений и насекомых.
В 1846 г. Александр заболел тифом и чудом выжил, а вот заразившийся от него отец скончался. Бутлерову было 18 лет, учился он на естественном отделении Казанского университета.
Менделеев Д.И. – родился в Сибири, в городе Тобольске. 8 февраля 1834 года семнадцатым и последним ребенком в семье Ивана Павловича Минделеева, директора Тобольской гимназии. В том же году отец Д.И. Минделеева ослеп. Когда Дмитрию было 13 лет – умер отец и все заботы о семье перешли к матери, Марии Дмитриевне, женщине выдающегося ума и энергии. Она успевала одновременно вести небольшой стеклянный завод и заботиться о детях, которым дала прекрасное по тому времени образование. Она умерла в 1850 г. Менделеев сохранил до конца своих дней благодарную о ней память.
Учился Д.И. Менделеев в Главном педагогическом институте в Петербурге у выдающихся учителей, умевших вызвать глубокий интерес к науке. Это были лучшие научные силы, того времени, академики и профессора Петербургского университета, такие, как математик М.В. Остроградский, физик Э.Х. Ленц, химик А.А. Воскресенский.
В 23 года от роду Д.И. Менделеев защитил диссертацию на степень магистра и стал доцентом Петербургского университета, где читал сначала неорганическую, а затем органическую химию.
В 1865 году он защитил диссертацию “О соединении спирта с водой” на степень доктора химии и через два года становится во главе кафедры неорганической (общей) химии.
По свидетельству современников, Бутлеров был одним из лучших лекторов своего времени: он безраздельно владел аудиторией благодаря ясности и строгости изложения, которые сочетались у него с образностью языка.
Умение отдыхать – и в студенческие и в зрелые годы помогало Александру Михайловичу самозабвенно работать.
Общительный и дружелюбный, готовый к шутке и спору, скромный и трудолюбивый – таким запомнили Бутлерова многочисленные друзья, коллеги и ученики.
Д.И.Менделеева
Д.И. Менделеев обладал удивительно ясным химическим мышлением, он всегда ясно представлял конечные цели своей творческой работы: предвидение и пользу.
Это был могучий человек, потому что сделанное им под силу только гиганту, благодаря крепости духа, уверенности в том, что дело его необходимо.
Д.И. Менделеев – настоящий патриот. Это человек, любящий свою родину, страну, где родился. Он своей работой, всей своей жизнью способствовал благу и процветанию своей родины. Дмитрий Иванович – классический пример патриота России.
- Энциклопедичность химических знаний;
- Умение анализировать и обобщать факты;
- Научное прогнозирование;
- Русский менталитет и русский патриотизм.
Весной 1868 г. по инициативе знаменитого химика Менделеева Александра Михайловича Бутлерова пригласили в Петербургский университет, где он начал читать лекции и получил возможность организовать частную химическую лабораторию. Бутлеров разработал новую методику обучения студентов, предложив ныне повсеместно принятый лабораторный практикум.
Сохранились сведения о совместной преподавательской работе Бутлерова и Менделеева на кафедре химии Петербургского университета:
- неоднократно Д.И. Менделеев и А.М. Бутлеров принимали вместе экзамены по химии.
- совместно участвовали в работе совета по защите диссертаций.
- в их отношениях была и взаимная поддержка и практика заблуждений.
В 1861 г. Бутлеров излагает свою теорию строения органических соединений, и, любопытное совпадение
- в том же году Менделеев публикует две работы, целиком посвященные органической химии. Выходит его учебник “Органическая химия”, через два года появляется второе издание. За свой труд Д.И. Менделеев удостаивается Демидовской премии – высшей научной награды России того времени.
Предпосылки периодического закона:
Ко времени открытия Периодического закона было известно 63 элемента и описаны свойства их многочисленных соединений.
Работы ученых – предшественников Д.И. Менделеева: классификация Берцелиуса, триады Деберейнера, спираль Шанкуртуа, октавы Ньюлендса, таблица Мейера.
Съезд химиков в Карлсруэ, когда окончательно утвердилось атомно-молекулярное учение.
Предпосылки теории химического строения:
Известны сотни тысяч органических соединений, состоящих из углерода, водорода, кислорода, реже – азота, фосфора и серы.
Работы предшественников А.М. Бутлерова: введение термина радикал и теории радикалов; теория типов; введение термина “изометрия”; Франкланд и Кекуле утвердили понятие о валентности элементов; Кекуле развил представление о четырех-валентности углерода; Канницаро уточнил атомные и молекулярные массы.
Оба признавали заслуги Берцелиуса как разработчика первооснов классификации.
История открытия Периодического закона и теории строения.
Д.И. Менделеев и А.М. Бутлеров обобщили накопленный фактологический материал и дополнив его, положили в основу своих трудов.
Обе работы похожи тем, что авторство их неоднократно приписывалось западным химикам.
Однако Д.И. Менделеев расположил элементы в ряд по возрастанию атомного веса.
Главная особенность таблицы Д.И. Менделеева в том, что в вертикальных рядах размещены химически сходные элементы: литий и натрий, бериллий и магний, фтор и хлор, кислород и сера. При таком расположении ясно проявилась периодичность свойств у химических элементов. Так было сделано величайшее открытие эпохи.
Научные теории:
Периодический закон и периодическая система химических элементов Д.И. Менделеева.
Теория строения органических соединений А.М. Бутлерова.
Обе ведущие теории современной химии были созданы великими русскими учеными и составляют вклад отечественной химии в мировую химическую науку. Обе теории прошли испытание временем и блестяще его выдержали, развиваясь и обогащаясь современными открытиями в химии.
Д.И. Менделеев предсказывает, описывает и указывает пути открытия еще неизвестных науке галлия, скандия и германия, назвав их экабор, экаалюминий, экасилиций.
Менее чем через шесть лет предсказания Д.И. Менделеева подтвердились. Жизнь продолжала проверять менделеевский закон на прочность.
Наконец пришло время триумфа. В 1875 г. был открыт галлий, 1879 г. – скандий, 1886 г. – германий. Существование в природе более 10 элементов предсказал Д.И. Менделеев.
Триумфом теории химического строения органических соединений Бутлерова явилось правильное объяснение на основе этой теории явлений изометрии.
В 1864-1866 годах выходит из печати тремя выпусками книга Бутлерова “Введение к полному изучению органической химии”. Этот вдохновенный труд был откровением Бутлерова – химика экспериментатора и философа, перестроившего весь накопленный наукой материал по принципу химического строения.
Книга Бутлерова вызвала настоящую революцию в химической науке. Она стала путеводной звездой в громадном большинстве исследований в области органической химии. Вышли издания почти на всех европейских языках.
Основные направления развития двух теорий:
Развитие обоих теорий происходит по философским законам (по спирали): формулировки положений корректируются в связи с новейшими научными открытиями, однако суть их остается прежней.
Философские законы развития:
Свойства химических элементов зависят от:
- их относительных масс,
- зарядов их атомных ядер;
- периодичности в изменении внешних электронных слоев атомов;
Свойства органических веществ зависят от:
- их химического строения,
- их пространственного строения,
- их электронного строения.


Периодический закон оказался могучим научным орудием исследования, т.к. все дальнейшие поиски элементов осуществлялись с помощь этого закона.
Периодический закон является всеобщим законом природы, т.к. все физические и химические свойства вещества определяются строением атомов.
Созданная Д.И. Менделеевым на основе периодического закона периодическая система химических элементов играет роль путеводной звезды в развитии химии, физики и всего естествознания.
Последующее развитие атомной физики, открытие строения атомов позволили раскрыть причины периодичности в свойствах химических элементов, открытой Д.И. Менделеевым.
Создание теории химического строения органических веществ сыграло важнейшую роль в развитии органической химии. Из науки описательной она превращается в науку созидательную, синтезирующую, появилась возможность судить о взаимном влиянии атомов в молекулах различных веществ.
Теория химического строения создала предпосылки для объяснения и прогнозирования различных видов изомерии органических молекул, а также направлений и механизмов протекания химических реакций.
На основе этой теории химики создают вещества, которые заменяют природные, а иногда и превосходят по свойствам (каучуки, пластмассы, красители).
В обеих теориях так много общего в путях их становления, направлениях развития, общее в прогностической роли, общенаучном значении.
Завещание Д.И. Менделеева.
“Периодическому закону будущее не грозит разрушением, а лишь развитие и надстройки обещаются”.
“… когда мы будем знать ближе натуру химической энергии, самый род атомного движения – когда законы механики получат и здесь приложение, тогда учение о химическом строении падет, … чтобы войти в низменном виде в круг новых, более широких воззрений.”
“Менделеев и Бутлеров! Это два титана, которые держат на своих плечах восточный портал всемирного интернационального здания химии” - так высоко оценил заслуги ученых академик А.Е. Арбузов на Менделеевском съезде проходившем в Казани в 1928 году.
Итак рассмотрены все вопросы плана. В тетрадях у учащихся записана важнейшая информация по данной теме.
Много дополнительной информации они услышали.
Проведение научно-практической конференции, посвященной изучению жизни и деятельности, выдающихся русских ученых Дмитрия Ивановича Менделеева и Александра Михайловича Бутлерова воспитывает у учащихся чувство гордости за свою страну и развивает интерес к изучаемому предмету.
А.М. Бутлеров – один из величайших русских ученых, он русский и по ученому образованию, и по оригинальности трудов.
“… я люблю свою страну, как мать, а свою науку – как дух, который благословляет, освещает и объединяет все народы для блага и мирного развития духовных и материальных богатств”.
При изучении этого раздела мы с учащимися выбрали форму защиты учебных проектов.
Защита учебного проекта включает в себя написание реферата и его презентацию другим участникам.
Подготовка конференции включала несколько этапов:
- Выбор темы учебного проекта.
- Написание реферата.
- Защита проекта.
- Дмитрий Иванович Менделеев – гениальный русский химик.
- Александр Михайлович Бутлеров – величайший русский ученый.
- Гроссе Э. Химия для любознательных. 1987 г.
- Тищенко В.Е., Младенцев М.Н. Дмитрий Иванович Менделеев, его жизнь и деятельность (Университетский период) 1861-1890 М. 1993 г.
- Дмитриев И.С. “Особая миссия Менделеева – Аргументы и факты, Санкт-Петербургский университет” 1996 г.
- Стариков В.И. “Д.И. Менделеев” 1984 г. Свердловск.
- Макареня А.А. “Менделеев в Петербурге” Лениздат. 1982 г.
На первом этапе подготовки учащимся дается примерный перечень тем для работы:
- Годы жизни. Место рождения. Семья. Увлечение.
- Личностные качества.
- Совместная деятельность
- Предпосылки.
- История открытия.
- Научные теории
- Триумф.
- Основные направления развития двух теорий.
- Философские законы развития.
- Значение
П этап – этап самостоятельной работы учащихся с учебником и дополнительной литературой.
Ш этап – обмен информацией, запись учащимися основного содержания в тетрадь.
Годы жизни. Место рождения Семья. Увлечения.
Менделеев Дмитрий Иванович 1834-1907 гг
Выступления учащихся в тезисах:
Бутлеров А.М. – родился 15 сентября 1828 г. в городе Чистоноле Казанской губернии. Отец Бутлерова, Михаил Васильевич, участник Отечественной войны 1812 года, после отставки в чине подполковника жил в родовом селе Бутлеровка; мать Софья Александровна, скончалась в 19 лет, через несколько дней после рождения сына. Воспитанный отцом, человеком образованным, Саша во всем хотел походить на него.
Учился Бутлеров в частном пансионе, потом в первой Казанской гимназии. В 10 лет хорошо владел французским и немецким языками, занимался химическими опытами (один из них закончился взрывом, и преподаватели пансиона отправили провинившегося в карцер, повесив ему на грудь дощечку с надписью “великий химик”, собирал коллекции растений и насекомых.
В 1846 г. Александр заболел тифом и чудом выжил, а вот заразившийся от него отец скончался. Бутлерову было 18 лет, учился он на естественном отделении Казанского университета.
Менделеев Д.И . – родился в Сибири, в городе Тобольске. 8 февраля 1834 года семнадцатым и последним ребенком в семье Ивана Павловича Минделеева, директора Тобольской гимназии. В том же году отец Д.И. Минделеева ослеп. Когда Дмитрию было 13 лет – умер отец и все заботы о семье перешли к матери, Марии Дмитриевне, женщине выдающегося ума и энергии. Она успевала одновременно вести небольшой стеклянный завод и заботиться о детях, которым дала прекрасное по тому времени образование. Она умерла в 1850 г. Менделеев сохранил до конца своих дней благодарную о ней память.
Учился Д.И. Менделеев в Главном педагогическом институте в Петербурге у выдающихся учителей, умевших вызвать глубокий интерес к науке. Это были лучшие научные силы, того времени, академики и профессора Петербургского университета, такие, как математик М.В. Остроградский, физик Э.Х. Ленц, химик А.А. Воскресенский.
В 23 года от роду Д.И. Менделеев защитил диссертацию на степень магистра и стал доцентом Петербургского университета, где читал сначала неорганическую, а затем органическую химию.
В 1865 году он защитил диссертацию “О соединении спирта с водой” на степень доктора химии и через два года становится во главе кафедры неорганической (общей) химии.
Личностные качества.
А.М. Бутлерова
По свидетельству современников, Бутлеров был одним из лучших лекторов своего времени: он безраздельно владел аудиторией благодаря ясности и строгости изложения, которые сочетались у него с образностью языка.
Умение отдыхать – и в студенческие и в зрелые годы помогало Александру Михайловичу самозабвенно работать.
Общительный и дружелюбный, готовый к шутке и спору, скромный и трудолюбивый – таким запомнили Бутлерова многочисленные друзья, коллеги и ученики.
Д.И.Менделеева
Д.И. Менделеев обладал удивительно ясным химическим мышлением, он всегда ясно представлял конечные цели своей творческой работы: предвидение и пользу.
Это был могучий человек, потому что сделанное им под силу только гиганту, благодаря крепости духа, уверенности в том, что дело его необходимо.
Д.И. Менделеев – настоящий патриот. Это человек, любящий свою родину, страну, где родился. Он своей работой, всей своей жизнью способствовал благу и процветанию своей родины. Дмитрий Иванович – классический пример патриота России.
Обоих ученых отличали от других химиков:
- Энциклопедичность химических знаний;
- Умение анализировать и обобщать факты;
- Научное прогнозирование;
- Русский менталитет и русский патриотизм.
Совместная деятельность.
Весной 1868 г. по инициативе знаменитого химика Менделеева Александра Михайловича Бутлерова пригласили в Петербургский университет, где он начал читать лекции и получил возможность организовать частную химическую лабораторию. Бутлеров разработал новую методику обучения студентов, предложив ныне повсеместно принятый лабораторный практикум.
Сохранились сведения о совместной преподавательской работе Бутлерова и Менделеева на кафедре химии Петербургского университета:
- неоднократно Д.И. Менделеев и А.М. Бутлеров принимали вместе экзамены по химии.
- совместно участвовали в работе совета по защите диссертаций.
- в их отношениях была и взаимная поддержка и практика заблуждений.
В 1861 г. Бутлеров излагает свою теорию строения органических соединений, и, любопытное совпадение
- в том же году Менделеев публикует две работы, целиком посвященные органической химии. Выходит его учебник “Органическая химия”, через два года появляется второе издание. За свой труд Д.И. Менделеев удостаивается Демидовской премии – высшей научной награды России того времени.
Предпосылки периодического закона:
Ко времени открытия Периодического закона было известно 63 элемента и описаны свойства их многочисленных соединений.
Работы ученых – предшественников Д.И. Менделеева: классификация Берцелиуса, триады Деберейнера, спираль Шанкуртуа, октавы Ньюлендса, таблица Мейера.
Съезд химиков в Карлсруэ, когда окончательно утвердилось атомно-молекулярное учение.
Предпосылки теории химического строения:
Известны сотни тысяч органических соединений, состоящих из углерода, водорода, кислорода, реже – азота, фосфора и серы.
Работы предшественников А.М. Бутлерова: введение термина радикал и теории радикалов; теория типов; введение термина “изометрия”; Франкланд и Кекуле утвердили понятие о валентности элементов; Кекуле развил представление о четырех-валентности углерода; Канницаро уточнил атомные и молекулярные массы.
Оба признавали заслуги Берцелиуса как разработчика первооснов классификации.
История открытия Периодического закона и теории строения.
Д.И. Менделеев и А.М. Бутлеров обобщили накопленный фактологический материал и дополнив его, положили в основу своих трудов.
Обе работы похожи тем, что авторство их неоднократно приписывалось западным химикам.
Однако Д.И. Менделеев расположил элементы в ряд по возрастанию атомного веса.
Главная особенность таблицы Д.И. Менделеева в том, что в вертикальных рядах размещены химически сходные элементы: литий и натрий, бериллий и магний, фтор и хлор, кислород и сера. При таком расположении ясно проявилась периодичность свойств у химических элементов. Так было сделано величайшее открытие эпохи.
Научные теории:
Периодический закон и периодическая система химических элементов Д.И. Менделеева.
Теория строения органических соединений А.М. Бутлерова.
Обе ведущие теории современной химии были созданы великими русскими учеными и составляют вклад отечественной химии в мировую химическую науку. Обе теории прошли испытание временем и блестяще его выдержали, развиваясь и обогащаясь современными открытиями в химии.
Д.И. Менделеев предсказывает, описывает и указывает пути открытия еще неизвестных науке галлия, скандия и германия, назвав их экабор, экаалюминий, экасилиций.
Менее чем через шесть лет предсказания Д.И. Менделеева подтвердились. Жизнь продолжала проверять менделеевский закон на прочность.
Триумф.
Наконец пришло время триумфа. В 1875 г. был открыт галлий, 1879 г. – скандий, 1886 г. – германий. Существование в природе более 10 элементов предсказал Д.И. Менделеев.
Триумфом теории химического строения органических соединений Бутлерова явилось правильное объяснение на основе этой теории явлений изометрии.
В 1864-1866 годах выходит из печати тремя выпусками книга Бутлерова “Введение к полному изучению органической химии”. Этот вдохновенный труд был откровением Бутлерова – химика экспериментатора и философа, перестроившего весь накопленный наукой материал по принципу химического строения.
Книга Бутлерова вызвала настоящую революцию в химической науке. Она стала путеводной звездой в громадном большинстве исследований в области органической химии. Вышли издания почти на всех европейских языках.
Основные направления развития двух теорий :
Развитие обоих теорий происходит по философским законам (по спирали): формулировки положений корректируются в связи с новейшими научными открытиями, однако суть их остается прежней.
Философские законы развития:
Свойства химических элементов зависят от:
- их относительных масс,
- зарядов их атомных ядер;
- периодичности в изменении внешних электронных слоев атомов;
Свойства органических веществ зависят от:
- их химического строения,
- их пространственного строения,
- их электронного строения.


Значение:
Периодический закон оказался могучим научным орудием исследования, т.к. все дальнейшие поиски элементов осуществлялись с помощь этого закона.
Периодический закон является всеобщим законом природы, т.к. все физические и химические свойства вещества определяются строением атомов.
Созданная Д.И. Менделеевым на основе периодического закона периодическая система химических элементов играет роль путеводной звезды в развитии химии, физики и всего естествознания.
Последующее развитие атомной физики, открытие строения атомов позволили раскрыть причины периодичности в свойствах химических элементов, открытой Д.И. Менделеевым.
Создание теории химического строения органических веществ сыграло важнейшую роль в развитии органической химии. Из науки описательной она превращается в науку созидательную, синтезирующую, появилась возможность судить о взаимном влиянии атомов в молекулах различных веществ.
Теория химического строения создала предпосылки для объяснения и прогнозирования различных видов изомерии органических молекул, а также направлений и механизмов протекания химических реакций.
На основе этой теории химики создают вещества, которые заменяют природные, а иногда и превосходят по свойствам (каучуки, пластмассы, красители).
В обеих теориях так много общего в путях их становления, направлениях развития, общее в прогностической роли, общенаучном значении.
Завещание Д.И. Менделеева.
“Периодическому закону будущее не грозит разрушением, а лишь развитие и надстройки обещаются”.
Завещание А.М.Бутлерова.
“… когда мы будем знать ближе натуру химической энергии, самый род атомного движения – когда законы механики получат и здесь приложение, тогда учение о химическом строении падет, … чтобы войти в низменном виде в круг новых, более широких воззрений.”
“Менделеев и Бутлеров! Это два титана, которые держат на своих плечах восточный портал всемирного интернационального здания химии” - так высоко оценил заслуги ученых академик А.Е. Арбузов на Менделеевском съезде проходившем в Казани в 1928 году.
Итак рассмотрены все вопросы плана. В тетрадях у учащихся записана важнейшая информация по данной теме.
Много дополнительной информации они услышали.
Проведение научно-практической конференции, посвященной изучению жизни и деятельности, выдающихся русских ученых Дмитрия Ивановича Менделеева и Александра Михайловича Бутлерова воспитывает у учащихся чувство гордости за свою страну и развивает интерес к изучаемому предмету
Читайте также:

