Оксихлорид алюминия получение доклад
Обновлено: 05.07.2024
Настоящая статья посвящена исследованию возможности применения коагулянтов на основе оксихлорида алюминия в технологии едконатрового умягчения воды. В статье рассмотрены основные методы умягчения природных вод. Показано, что существующие на действующих очистных сооружениях технологии не снижают концентрацию солей жесткости, что приводит к необходимости применения различных методов умягчения воды, внедрение которых в технологические цепочки не всегда возможно. Применение различных методов умягчения воды ограничено высокими капитальными затратами, связанными с необходимостью устройства дополнительных реагентных хозяйств и закупкой дорогостоящего оборудования, а также образованием в ряде случаев высококонцентрированных солевых стоков. Применение широко известного метода едконатрового умягчения ограничивается необходимостью обработки воды коагулянтами на основе солей железа, которые на сегодняшний день менее распространены по сравнению с алюминиевыми коагулянтами. Дальнейшее развитее едконатрового умягчения связано с возможностью применения в качестве реагентов интенсифицирующих процессы осаждения коагулянтов на основе оксихлорида алюминия. Введение оксихлорида алюминия в реагентноумягченную воду с последующим ее подкислением позволяет добиться необходимых показателей качества по таким критериям, как рН, концентрация солей жесткости и остаточного алюминия.

1. ГОСТ 2761-84. Источники централизованного хозяйственно-питьевого водоснабжения. Гигиенические, технические требования и правила выбора. – М.: Изд-во стандартов, 1999. – 11 с.
3. Технологические и проектные решения реконструкции сооружений очистки воды нижнего течения р. Дон. / С.И. Игнатенко, А.Ю. Черкесов, Л.Н. Фесенко и др. // Техновод. – 2016. – С. 75–85.
4. Беликов С.Е. Водоподготовка. Справочник для профессионалов. Под ред. д.т.н., действительного члена Академии промышленной экологии С. Е. Беликова. – М.: Аква-Терм, 2007. – 240 с.
9. Драгинский В.Л. Коагуляция в технологии очистки природных вод / В.Л. Драгинский, Л.П. Алексеева, С.В. Гетманцев. – М., 2005. – 576 с.
10. Линевич С.Н., Гетманцев С.В. Коагуляционный метод водообработки: теоретические основы и практическое использование. – М.: Наука, 2007. – С. 230.
Многолетние наблюдения за качественным составом нижнего течения р. Дон (водозаборы г. Новочеркасск, г. Шахты и х. Хапры) за период с 2011 по 2017 гг. показали, что максимальное значение по общей жесткости составило 11,8 град. (в среднем не более 7,5–8,5 град.), что превыщает предельно допустимое значение более чем на 60 %. В периоды, когда были зафиксированы превышения ПДК по общей жесткости, общая минерализация также превышала нормативно установленные границы. Максимально зафиксированное солесодержание составило 1268 мг/л, при средних значениях 750–800 мг/л. Необходимо отметить, качество воды в нижнем течении реки Дон по данным показателям ухудшается в зимне-весенний период года, когда на очистные сооружения нет дополнительной нагрузки в виде фитопланктона, взвешенных веществ, запахов и привкусов.
Применяемые на водопроводных очистных станциях (ВОС) технологии водоподготовки разработаны и в ведены в практику в 1950–1970-е гг. Методы обработки воды заложенные в них, предусматривают возможности умягчения воды. В связи с этим в процессе работы таких сооружений эксплуатирующие организации сталкиваются с предписаниями Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека о доведении показателей качества очищенной воды до требований СанПиН 2.1.4.1074-01 [2]. При проектировании новых водоочистных сооружений и разработке решений по реконструкции существующих государственная экспертиза также вполне обоснованно требует предусматривать мероприятия направленные на снижение содержания солей кальция и магния в воде.
Снижение общей жесткости (и реже – общей минерализации) является наиболее сложной и, прежде всего, экономически затратной задачей воды, что может быть достигнуто методами ионного обмена, мембранным разделением (нанофильтрация или обратный осмос), или методом осаждения.
В результате применения метода ионного обмена (Na-катионирование) образуется до 30 % вторичных загрязнений, в виде отработанных регенерационных растворов, отмывочных и взрыхляющих вод. Вторичные загрязнения представляют собой хорошо растворимые хлоридно-кальциево-магниевые рассолы с концентрацией солей до 80–100 г/л, для переработки и захоронения которых на сегодняшний день не существует экономически обоснованных технологий. Необходимо отметить, что при применении данного метода значительная часть себестоимости воды приходится именно на обработку (утилизацию) отходов водоочистки на выпарных и кристаллизационных установках, что по затратам значительно превосходит само ионообменное умягчение.
Преимущества метода осаждения (реагентного умягчения) в сравнении с рассмотренными методами заключаются в следующем:
– процесс реагентного умягчения возможно проводить в существующих сооружениях – осветлителях со слоем взвешенного осадка или отстойниках различного типа, эффективность и надежность работы которых может быть значительно повышена путем установки в них тонкослойных модулей;
– при реагентном умягчении воды в осветлителе происходит также ее обезжелезивание, осветление и обесцвечивание;
– удаление из воды ионов кальция, магния и карбоната осуществляется переводом этих ионов в нерастворимую фазу (карбонат кальция и гидроксид магния), наиболее удобную для последующей переработки и утилизации;
– метод относительно прост, не требует сложного и дорогостоящего оборудования, значительно менее энергоемкий, позволяет достичь нормативных показателей по общей жесткости и солесодержанию.
Доведение качества воды до нормативов СанПиН 2.1.4.1074-01 методами осаждения возможно с применением извести, извести и соды, едкого натра (с известью или содой, либо без них) [3–5]. При известковом методе умягчения воды удаляется только карбонатная жесткость. Однако из-за неполноты выпадения солей и без дополнительного подогрева воды остаточная жесткость будет превышать теоретическое значение на 0,5–1,0 мг-экв/л и, возможно, не снизится до нормативных значений. Известково-содовый метод пригоден для умягчения воды любого ионного состава, но дозы реагентов при этом резко возрастают (на величину некарбонатной жесткости).
Умягчение едким натром, как альтернатива известковому методу, возможно, если качество исходной воды отвечает условию 2НСО3 - + СО2 > Са 2+ . Доза едкого натра при этом, мг-экв./дм3, будет равной
где Дк – доза коагулянта, мг-экв/л; ИNaOH – избыток едкого натра, ≈ 0,5 мг-экв/л. Едко-натровая обработка, в отличие от известкования, не пылит, не требует громоздкой аппаратуры для гашения извести и подготовки ее к дозированию.
Едкий натр (NaOH) представляет собой щелочной реагент, при добавлении в воду которого происходит смещение pH среды в сильнощелочную сторону. В щелочной среде (при рН ≥ 9,8–10,0) начинается интенсивное образование малорастворимых соединений карбоната кальция и гидроксида магния, которые в дальнейшем могут быть эффективно удалены из воды при помощи существующих технологических вооружений [4, 5]:
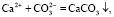
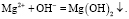
Интенсификация процессов осаждения нерастворимых соединений, как правило, проводится с применением коагулянтов. Для обработки сильно щелочных вод рекомендуется применение коагулянтов на основе солей железа, поскольку образующийся при гидролизе солей алюминия AlOH3, в сильно щелочной среде образует растворимые алюминат ионы [6]. Так согласно [7, 8] эффективность работы сульфата алюминия Al2(SO4)3 в сильнощелочной среде резко падает, и применение его становится неэффективным.
В практике водоподготовки на сегодняшний день распространено применение в качестве коагулянта оксихлорида алюминия (ОХА), однако результатов исследований об эффективности применения ОХА при обработке вод с рН ≥ 8,5 в литературных источниках не встречается. Достоинством данного коагулянта в первую очередь является его действие в большом диапазоне pH среды, что может благоприятно сказаться на процессах водоподготовки с применением едко-натрового метода умягчения. Однако как было указано выше, применение данного коагулянта может привести к возрастанию содержания остаточного алюминия в воде с превышением его предельно допустимой концентрации 0,5 мг/дм3.
При добавлении в воду оксихлорида алюминия происходит его гидролиз с образованием гидроксида алюминия – малорастворимого соединения, выпадающего в осадок при pH = 5–11единиц, и свободных ионов Н+ и Cl-.
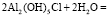
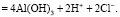
Однако при использовании едконатрового метода умягчения pH обрабатываемой воды превышает 8,5 и гидроксид алюминия начинает переходить в форму алюминат-иона [Al(OH)4]-, растворимого в воде. Тем самым, с увеличением pH среды, увеличивается и концентрация остаточного алюминия в воде.
На рис. 1 представлено распределение гидроксокомплексов алюминия по формам в зависимости от pH среды [9].
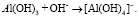
Согласно действующим требованиям потребителю допускается подавать воду величиной водородного показателя в пределах 6–9 единиц рН [2], вследствие чего воду, прошедшую в реагенте умягчение, необходимо подкислять с доведением показателя pH до величины равновесного насыщения, с целью предотвращения коррозии и выпадения карбонатов на поверхности трубопроводов [10]. Для снижения pH среды было принято решение обрабатываемую воду подкислять раствором HCl, поскольку применение данного реагента в меньшей степени оказывает влияние на солесодержание воды в сравнении с серной кислотой. При введении в воду соляной кислоты совместно с реакциями нейтрализации карбонат- и гидроксид-ионов будет протекать реакция образования гидроксида алюминия:
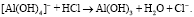
На первом этапе проводили опыты по применению едконатрового метода умягчения с пробной коагуляцией в мерном цилиндре, объемом 1 дм3. Качество сырой воды, поступающей на ВОС г. Новочеркасск из реки Дон, по состоянию на март 2017 г. характеризовалось следующими показателями: жесткость общая – 7,8 °Ж, кальций (Са2+) – 4,0 мг-экв./дм3, магний (Mg2+) – 3,3 мг-экв./дм3, гидрокарбонат-ион (HCO3-) – 4,0 мг-экв./дм3, температура – 8,7 °С, рН = 8,08.
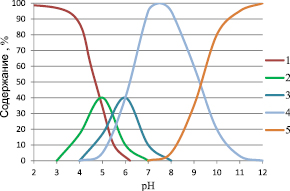
Рис. 1. Влияние pH раствора на распределение гидроксокомплексов алюминия: 1 – [Al(H2O)6]3+, 2 – [Al(OH)(H2O)5]2+, 3 – [Al(OH)2(H2O)4]+, 4 – Al(OH)3, 5 – [Al(OH)4]
Оксихлорид алюминия (Al2(OH)nCl6-n) синонимы: полиоксихлорид алюминия, гидроксохлорид алюминия, полиалюминия хлорид, гидрохлорид полиалюминия.
Оксихлорид алюминия – коагулянт современного поколения. Благодаря инновационным технологиям, оксихлорид алюминия обладает свойствами, которые позволяют обеспечить высокое качество очистки воды от загрязнений еще при первоначальной стадии очищения.
Повседневно применяют и достаточно успешно – для очищения воды питьевого значения. Также стоит отметить, что этот реагент эффективно используется в очистке воды ГРЭС, ТЭЦ, сельскохозяйственных, индустриальных предприятий, заводов и т.д.
Содержание и физико-химические свойства
Оксихлорид алюминия: свойства и качественные отличия от реагентов других производителей:
- интенсифицирует процесс подготовки воды, повышая ее качество;
- эффективность обработки достигается, как при высоких, так и при минусовых температурах самой воды до - 4 C;
- независимость от температур очищаемой воды, поскольку реагент обладает высокой степенью коагуляции;
- для очистки сильно зацветших и мутных вод низкой температуры самый оптимальный вариант;
- в уже очищенной воде остаток алюминия в разы ниже запросов СанПиН 2.1.4.1074-01;
- располагает полимерными качествами, что существенно отличает полиалюминия хлорид от подобной продукции. Иногда необходимо отказаться от флокулянтов, что собственно позволяет сделать полимерный состав;
- фактически не модифицирует щелочность воды, обладает огромным диапазоном оптимальных рН;
- растворяется быстро (без остатка), подогрева воды перед эксплуатацией на этапе приготовления раствора не требуется;
- значительно снижает либо исключает вообще – образование каких-либо (в т. ч. гипсовых) отложений в трубопроводах и технологическом оборудовании;
- срок сохранения твердого реагента 36 месяцев, в растворе – до 6 м.
- всесезонный завоз реагентов в любые труднодоступные регионы России.
Цена на оксихлорид алюминия выше, чем на аналогичные реагенты - менее эффективные коагулянты. Но за счет экономичности, соответственно и экономного применения коагулянта в целом, не актуальности дополнительных реагентов в водоподготовке, износ оборудования – минимальный. Важнейший фактор: цена соответствующая качеству Оксихлорид алюминия вывели его в лидирующие позиции среди подобной продукции.
Поставки
Заказать или купить коагулянт Оксихлорид алюминия возможно в специальных полипропиленовых мешках вес 25кг, либо упаковках биг-бэг. Наша компания предлагает самые выгодные цены на данный реагент, кроме того мы сами осуществляем фасовку и максимально быструю транспортировку в не зависимости от погодных условий. При этом у нас разработана программа специальных скидок и выгодных предложений для постоянных и оптовых клиентов. Наша компания одна из немногих, кто предоставляет гарантию качества сертифицированной продукции.
Помимо реагентов, обусловливающих только понижение рН растворов силикатов - кислот и их ангидридов, для активации используют соли, которые способны образовывать при реакции малорастворимые соединения. К ним относятся кислые алюминий-и железосодержащие коагулянты, алюминат натрия, оксихлорид алюминия и др. Реакции активации разными реагентами приведены в работах [ 19 ( стр. [46]
К мероприятиям по интенсификации процесса водоподготовки для конкретного периода относятся следующие: интенсификация процесса коагуляции за счет подбора типа и дозы коагулянта, флокулянта, применение замутнителей. Исходя из полученных результатов, для первого подпериода паводка рекомендуется применение оксихлорида алюминия вместо сульфата алюминия совместно с анионным флокулянтом. Для первого, второго, третьего периодов рекомендуется понижение отношения окисляемости к мутности за счет искусственного повышения мутности, то есть применение замутнителей: глины, клиноптилолита; применение катионного флокулянта. Для первого периода интенсификация возможна за счет увеличения дозы сульфата алюминия. В четвертом периоде рекомендуется применение оксихлорида алюминия совместно с анионным флокулянтом. Для первого, второго, третьего и четвертого периодов возможна интенсификация за счет применения активированного угля. [47]
Это соединение способно вступать в обменные реакции с солями с образованием основных солей алюминия аналогичного состава ( 1 А1203 на 1 экв. Так, при прибавлении к ультрафильтрату золя Na2S04 выпадает в виде белого осадка оксисульфат алюминия состава 2A1203 - H2S04, который при медленном осаждении может быть выделен в кристаллическом виде. Сам оксихлорид алюминия хорошо растворим в воде, сравнительно мало адсорбируется окисью алюминия и в обычных А1203 - золях большая часть его находится в истинно-растворенном состоянии в интермицелляр-ной жидкости золя. [48]
Сульфат алюминия ( глинозем) А12 ( 5О4) з - 18 Н2О ( плотность 1 62 т / м3, насыпная масса J. В результате применения сульфата алюминия степень минерализации воды увеличивается. Алюминат натрия NaAlO2, оксихлорид алюминия А12 ( ОН) 5С1, полихлорид алюминия [ Al2 ( OH) nCle - n ] m ( SO4) r ( где l w Sm lO), алюмокалиевые [ A1K ( SO4) 2 - 18Н2О ] и алюмоаммонийные [ A1 ( NH4) ( SO4) 2 - 12H2O ] квасцы имеют меньшую стоимость и дефицитность, чем сульфат алюминия. [49]
Учитывая сильные хлорирующие свойства ЧХУ при относительно низких температурах, нами проведены исследования процесса хлорирования металлического алюминия газообразным хлором с добавками ЧХУ. Результаты исследований открывают новые перспективы использования ЧХУ в производстве хлорида и оксихлорида алюминия из металлического алюминия и глинозема. [50]
Учитывая сильные хлорирующие свойства ЧХУ при относительно низких температурах нами проведены исследования процесса хлорирования металлического алюминия газообразным хлором с добавками ЧХУ. Результаты исследований открывают новые перспективы использования ЧХУ в производстве хлорида и оксихлорида алюминия из металлического алюминия и глинозема. [51]
Техническая окись алюминия, называемая глиноземом, получается из бокситов или нефелина. Способ ее получения основан на выделении щелочного алюмината, самопроизвольно разлагающегося в водных растворах с выделением гидроокиси алюминия и последующим превращением гидрата в безводный глинозем при температуре 1150 - 1200 С. Более чистый продукт, содержащий 99.999 % А1203, получается из водных растворов оксихлорида алюминия . [52]
На некоторых отечественных заводах технический Т1С14 очищают следующим образом. Четыреххлористый титан заливают в реактор и включают мешалку. Через загрузочное устройство добавляют увлажненную поваренную соль ( или влажный активированный уголь), количество влаги в которой достаточно для превращения А1С13 в нерастворимый оксихлорид алюминия . Далее суспензию перекачивают на предварительное отстаивание или фильтрование. [53]
Диспергированные, коллоидные и взвешенные частички примесей природных вод в большинстве случаев имеют одинаковые заряды, что обусловливает возникновение межмолекулярных сил отталкивания и агрегативную устойчивость. Поскольку в технологии очистки воды предусматривается частичное или полное удаление примесей, агрегативную устойчивость частичек стремятся нарушить, а заряд их устранить или снизить до очень малых значений. Этого достигают добавлением к воде сульфатов алюминия, железа ( II) и железа ( III), хлорида алюминия, хлорида железа ( III), алюмината натрия, оксихлорида алюминия и других веществ, которые, являясь коагулянтами, либо нарушают агрегативную устойчивость системы, либо образуют вследствие гидролиза коллоиды, сорбирующие примеси из воды. [54]
В крупнотонна жном производстве наиболее рациональным является одновременное сливание растворов при интенсивном их перемешивании. Как показал опыт [233], такой способ осаждения гидрогелей позволяет стабильно получать весьма однородные по составу гидрогели. Водный раствор алюмината натрия в отсутствие избытка щелочи малостабилен. Водные растворы оксихлорида алюминия весьма стабильны. Следует, однако, отметить, что оксихлорид алюминия, несмотря на некоторые положительные качества, вероятно, нельзя рекомендовать в качестве исходного материала в производственной технологии получения цеолита. [56]
Тонкодисперсные взвеси удаляют из воды с помощью коагулирования, т.е. обработки воды химическими реагентами, которые вызывают укрупнение взвешенных частиц и ускоряют их осаждение. Природные воды нередко содержат во взвешенном состоянии почвенные органические вещества, кремниевую кислоту, различные глинистые минералы, которые при гидролизе образуют отрицательно заряженные коллоидные частицы. Добавление коагулянтов вызывает их осаждение. Обычно в качестве коагулянтов используют сульфат алюминия A12 ( SO4) - 18H2O, оксихлорид алюминия А12 ( ОН) 5С1 Н2О и хлорид железа ( III) или их смесь. [57]
К мероприятиям по интенсификации процесса водоподготовки для конкретного периода относятся следующие: интенсификация процесса коагуляции за счет подбора типа и дозы коагулянта, флокулянта, применение замутнителей. Исходя из полученных результатов, для первого подпериода паводка рекомендуется применение оксихлорида алюминия вместо сульфата алюминия совместно с анионным флокулянтом. Для первого, второго, третьего периодов рекомендуется понижение отношения окисляемости к мутности за счет искусственного повышения мутности, то есть применение замутнителей: глины, клиноптилолита; применение катионного флокулянта. Для первого периода интенсификация возможна за счет увеличения дозы сульфата алюминия. В четвертом периоде рекомендуется применение оксихлорида алюминия совместно с анионным флокулянтом. Для первого, второго, третьего и четвертого периодов возможна интенсификация за счет применения активированного угля. [58]
В крупнотонна жном производстве наиболее рациональным является одновременное сливание растворов при интенсивном их перемешивании. Как показал опыт [233], такой способ осаждения гидрогелей позволяет стабильно получать весьма однородные по составу гидрогели. Водный раствор алюмината натрия в отсутствие избытка щелочи малостабилен. Водные растворы оксихлорида алюминия весьма стабильны. Следует, однако, отметить, что оксихлорид алюминия , несмотря на некоторые положительные качества, вероятно, нельзя рекомендовать в качестве исходного материала в производственной технологии получения цеолита. [59]
Заявка
КИЕВСКИЙ ОРДЕНА ЛЕНИНА ПОЛИТЕХНИЧЕСКИЙИНСТИТУТ ИМ. 50-ЛЕТИЯ ВЕЛИКОЙ ОКТЯБРЬСКОЙСОЦИАЛИСТИЧЕСКОЙ РЕВОЛЮЦИИ
ШУТЬКО АЛЕКСАНДР ПЕТРОВИЧ, ОЛЕЙНИКОВ СЕРГЕЙ ЛЕОНИДОВИЧ, САМАНДАСЮК ПЕТР АЛЕКСЕЕВИЧ
МПК / Метки
Код ссылки
Способ очистки растворимых солей вольфрамовой кислоты и раствора хлористого кальция для изготовления люминофоров

Номер патента: 104440
. основного материала.Предлтагаемый способ позволяет значительно упростить очистку растворимых солей вольфрамовой кислоты и раствор хлористого кальЦИЯ ДЛЯ ИЗГОТОВЛСНИЯ ТПОМИНС(рЭрСВЭто достигается тем, что растворимые соли вольфрамовой кислоты(рильтруют через колонку, содержащую смесь окиси алюминия н сульфида цинка в весовом соотношении 20:1Очистка раствора хлористого кальция осуществляется хроматографированием на окиси алюминия.Очищенные растворы солей воль фрамовой кислоты и хлористого кальция содержат примесь железа в количестве не более 4 10 "596 и меднне более 1 -10 5%.Способ очистки растворимых солей вольфрамовой кислоты и раствора хлористого кальция для изготовления люминофоров, отл ич а ющи й ся тем, что, с целью почученття.
Способ изготовления полуфабрикатов из алюминиевых сплавов системы алюминий-цинк-магний-медь

Номер патента: 662022
. в течениевсего процесса экструдирования. После экструдирования заготовка нагревается до 482-521 оС в течение2-40 час, предпочтительно 6-8 час,Эта температура превышает темпера туру солидуса вы:окопрочных сплавовтипа 7000. Интенсивность нагревапоэтому не должна превышать 83 С вочас,чтобы избежать опасность оплавленияя.66022 под закалку до 48 2-521 С в течениеовремени, достаточного для перевода сплава в твердый раствор (обычно 4-8 час), Закалку проводят в воду с температурой 38 С. Старение может проводиться, например, по режиму 102-127 С в течение 70-75 час (Т 6) или двухступенчатому старению по режиму 102-120 ОС 6 час + 171-182 С 7. 5-9, 5 час (Т 73) . Режим Т 6 обеспечивает максимальную прочность, режим Т 7 3 - высокую стойкость к ко.
Способ получения пиперидинпроизводных эфиров 4, 5-диалкил-3 оксипиррол-2-карбоновых кислот или их физиологически совместимых солей с кислотами
Номер патента: 957768
. промывают собранные экстракты 2 н. раствором едкого цатра и водой и высушивают сульфатом натрия. После отгонки эфира и избыточного эпибромгидрина остаток экстрагируют гептаном. Получают 122 г целевого продукта с Т 70-71 С.7 95774Найдено, %: С 63,1; Н 7,21 М 5,5,с, н 9 О.Вычислено,Ъ: С 63,4 у Н 7,2; М 5,3.П р и м е р 7. 1-(2-Карбометокси 4,5-диметилпиррол-З-окси)-2,3-эпоксипропан,5.Аналогично примеру 5 получают из17 г 2-карбометокси-З-гидро,5-диметилпиррола, 20 г эпибромгидрина и29 г сухого карбоната калия в 100 млацетона 18,5 г целевого продукта с 10Т 85-87 С.Найдено,Ъ: С 58,5; Н 6,7; М 6,5.С, Н,МОВычислено,Ъ: С 58,7; Н 6,7; М 6,2.П р и м е р 8. 1-(2-Карбоэтокси4-бутил-метилпиррол-З-окси)-2,3 эпоксипропан.Аналогично примеру 5 из 35.
Способ получения производных пенициллановой кислоты или их аддитивных солей с кислотами

Номер патента: 1122230
. антибактериаль-. При использовании антибактериального соединения по изобретению наМлекопитающих, особенно на людях,такое соединение может применятьсясамо по себе или оно может смешиваться с другими антибиотическимн веществами и/или фармацевтически применимыми носителями или разбавителями. Указанный носитель или разбавитель выбирают на основе предполагаемого вида применения. Так, например, когда выбирают предпочтительный оральный вид применения, антибактериальное предлагаемое соединение может использоваться в форме таблеток, капсул, лепешек, порошков, сиропов, эликсиров, водных растворов и суспензий в соответствии со стандартной Фармацевтической практикой. Соотношение активного ингредиента н носителя обычно зависит от химической природы.
Способ получения производных 1-(циклогексил)-4-арил-4 пиперидинкарбоновой кислоты или их фармацевтически приемлемых солей с кислотами
Номер патента: 1132788
. получая 27 ч. (72,6 Х) 4-(4-Фтор-метилфенил)-1-(4-метилденилсульфонил)-4-пиперидинкарбонитрила.П р и м е р 8. Смесь 35,8 ч.4-(2-фторфенил)-1-(4-метилфенилсуль- З 5 Фонил)-4-пиперидинкарбонитрила и 50 ч. 753-ного раствора серной кислоты перемешивают в течение 4 ч. прио150 С. По каплям добавляют 192 ч. этанола. После завершения реакции перемешивание продолжают в течение 5 ч при температуре кипения с обратным холодильником. Реакционную смесь охлаждают и выливают на измельченный лед. Реакционную массу подщелачивают гидроокисью аммония и продукт экстрагируют дихлорметаном. Экстракт сушат, фильтруют и упаривают, получая 17,2 ч. (68,4) этилового эфира 4-(2-фторфенил)-4-пиперидинкарбоновой кислоты в виде остатка. Используя ту же методику.
Обычно оксихлорид алюминия получается обработкой металлического алюминия соляной кислотой, или его растворением в растворе хлорида алюминия при 90°С.
Полиоксихлорид алюминия представляет собой высокоэффективный неорганический коагулянт, образующий устойчивые соединения со многими неорганическими и органическими веществами. Реагент находит применение в пищевой, косметической и кожевенной промышленности, в коммунальном хозяйстве, используется для очистки и кондиционирования питьевой воды, в процессах водоподготовки для ТЭЦ, ГРЭС, котельных, для очистки воды в бассейнах. Применяется преимущественно в холодное время года.
Гидроксохлорид алюминия призван заменить устаревший сульфат алюминия, т.к. сульфат алюминия не во всех случаях обеспечивает требуемое качество очистки. Особенно затруднительно его использование при низких температурах, так как при данных температурах образуются такие высокодисперсные осадки продуктов гидролиза коагулянта, что их трудно отделить от очищаемой воды методами отстаивания и фильтрации. Применение оксихлорида алюминия, повышает скорость коагуляции коллоидных частиц органических и неорганических загрязнений, не подщелачивая воду и обеспечивает более высокое качество очистки воды без каких-либо отложений и с минимальным содержанием остаточного алюминия в воде. Здесь следует отметить, что полиоксихлорид алюминия позволяет получить питьевую воду с содержанием остаточного алюминия в пределах 0,05-0,10 мг/л, что более, чем в два раза меньше, чем норма Всемирной Организации Здравоохранения (0,20 мг/л).
Преимущества:
- доза коагулянта снижается в четыре-пять раз (20-25%) от количества сернокислого алюминия);
- практически не изменяется рН очищаемой воды, что позволяет отказаться от использования щелочных агентов для нейтрализации;
- более широкий рабочий диапазон рН;
- продукт обладает большей способностью к полимеризации, что ускоряет хлопьеобразование и осаждение коагулированной взвеси;
- обеспечивается максимально высокая эффективность очистки воды от взвешенных веществ и металлов;
- применение при более низких температурах воды, чем сернокислый алюминий (ниже 4-8°С);
- приводит к снижению коррозионной активности воды (отсутствие избыточных сульфатов);
- при использовании дает низкое остаточное содержание алюминия;
- не слеживается при хранении, имеет длительный срок использования;
- улучшаются санитарно-гигиенические условия труда, снижается трудоемкость и эксплуатационные затраты.
Представленные преимущества способствуют:
- уменьшению скорости коррозии металлов в системах водоснабжения и теплоснабжения, за счет исключения образования агрессивной углекислоты;
- возможности отказа от использования щелочных агентов;
- сокращению в 10 раз количества введенных в воду анионов в сравнении с традиционными коагулянтами;
- обеспечению максимально высокой эффективности очистки воды от взвешенных веществ и металлов;
- возможности использования при более низких температурах воды, чем сернокислый алюминий;
- снижению коррозионной активности воды (отсутствие избыточных сульфатов);
- улучшению санитарно-гигиенические условия труда, снижению трудоемкости и эксплуатационных затрат;
- снижению содержания хлорорганических соединений;
- обеспечению содержания остаточного алюминия менее 0,2 мг/л;
- минимизации расхода реагента в пределах 0,3 – 3,0 мг алюминия на литр воды.
Наша компания предлагает для Вас оксихлорид алюминия в виде раствора либо в виде твердого вещества
Раствор оксихлорида алюминия
Внешний вид водного раствора оксихлорида алюминия — прозрачная бесцветная жидкость (допускаются серый или белый оттенок), срок хранения которой составляет 6 месяцев.
Читайте также:

