Нарушение работы вилочковой железы доклад
Обновлено: 02.07.2024
История относительно интенсивного изучения вилочковой железы ( glandula thymus, thymus ) насчитывает около 400 лет. Начало его относится к 1614 г., когда профессор Базельского университета Феликс Платтер описал происшедшую у него
История относительно интенсивного изучения вилочковой железы (glandula thymus, thymus) насчитывает около 400 лет. Начало его относится к 1614 г., когда профессор Базельского университета Феликс Платтер описал происшедшую у него на глазах внезапную смерть 5-месячного ребенка, при вскрытии трупа которого не было найдено никаких причин, способных объяснить смерть, кроме очень большого тимуса. Смерть этого ребенка тогда впервые связали с огромным тимусом, назвав данное состояние тимическим удушьем — asthma thymicum.
В середине XIX в. профессор Венского университета Карл Рокитанский высказал предположение об инкреторной функции вилочковой железы. Данная концепция была положена в основу представлений о тимико-лимфатическом статусе [1, 2] как врожденной особенности конституции, предрасполагающей к внезапной смерти от незначительных причин. В симптомокомплекс тимико-лимфатического статуса включались первичная гиперфункция вилочковой железы, гипоплазия надпочечников, сердца и аорты [1–5]. С этого времени причиной тимической смерти стали считать острую надпочечниковую недостаточность [3, 4]. Однако отсутствие характерных для тимико-лимфатического состояния признаков во многих случаях при такой смерти, в том числе и симптомов надпочечниковой недостаточности, позволило поставить под сомнение и данную концепцию.
В начале 1960-х гг. было доказано, что тимус является центральным органом иммунной системы. С этого времени вилочковая железа рассматривается в качестве железы внутренней секреции, действие гормонов которой направлено на дифференцировку тимических лимфоцитов. Открытие основной функции вилочковой железы — продукции Т-лимфоцитов и регуляции иммунитета, а также принадлежность ее к системе эндокринных желез позволяют рассматривать данный орган как коммутатор иммунной и эндокринной систем. В серии работ отечественных исследователей последних 20 лет доказывается, что дети с большой вилочковой железой относятся к числу иммунодефицитных лиц.
Однако проведенные исследования показали, что тимомегалия является лишь одним из симптомов того состояния, которое существует у детей, имеющих увеличенную вилочковую железу [7]. В связи с отсутствием другого термина, отражающего сущность состояния, которое имеет место у детей с увеличенной вилочковой железой (соответствующей тимомегалии в понимании патологоанатомов), предлагаем называть его синдромом Платтера.
Диагностика тимомегалии в клинической практике
Ориентировочная диагностика тимомегалии может быть проведена с помощью объективного исследования: осмотра, пальпации, перкуссии. Однако оценка результатов во многом субъективна и зависит от опыта исследователя [7].
Из инструментальных методов, позволяющих объективно выявить тимомегалию, используются рентгенодиагностика и ультразвуковое исследование (УЗИ).
Рентгенодиагностика. Методологической основой рентгенодиагностики увеличенного тимуса является следующее положение: в норме у детей любого возраста на стандартных рентгенограммах грудной клетки в прямой проекции тень тимуса не должна выходить за пределы тени сосудистого пучка и сердца.
В целях диагностики тимомегалии на рентгенограммах грудной клетки в прямой проекции мы применяли кардио-тимико-торакальный индекс (КТТИ) по J. Gewolb [8] и вазокардиальный индекс (ВКИ) [7]. Оба индекса определяются на стандартных рентгенограммах грудной клетки в прямой проекции. КТТИ представляет собой частное от деления ширины сосудистого пучка на уровне бифуркации трахеи (точка carina) на ширину грудной клетки на уровне купола диафрагмы. ВКИ представляет собой частное от деления ширины сосудистого пучка на уровне бифуркации трахеи (точка carina) на максимальную ширину тени сердца. Максимальная ширина тени сердца определяется как сумма двух перпендикулярных отрезков, опущенных на вертикальную линию (проведенную через середину позвоночного столба) из максимально удаленных от нее точек сердца слева и справа (рис. 1).
УЗИ. УЗИ тимуса в нашей стране впервые было проведено у новорожденных детей С. М. Воеводиным [9]. Путем клинико-морфологических сопоставлений нами были разработаны коэффициенты пересчета линейных параметров тимуса в более привычные для клиницистов формы (объема и массы органа). Округленные величины указанных коэффициентов, по нашим данным, равны 0,7 (для массы) и 0,5 (для объема). Таким образом, величины массы и объема тимуса при ультразвуковом сканировании вычисляются следующим образом:
М = 0,7 в a в b в c;
V = 0,5 в a в b в c,
где a, b, c — линейные параметры тимуса (ширина, длина, передне-задний размер, выраженные в см); 0,7 и 0,5 коэффициенты пересчета линейных параметров на массу и объем органа соответственно [10]. Для практических целей массу и объем вилочковой железы достаточно определять так, как это указано выше: без вычисления объема и массы отдельных долей.
Методом центильного распределения нами были определены нормальные значения массы и объема тимуса для детей в возрасте 1–24 мес (табл. 2). При превышении массы и объема тимуса выше верхних предельных значений нормы состояние ребенка следует расценивать как тимомегалию.
На основании анализа более 5000 рентгенограмм, выполненных у детей грудного возраста при подозрении на пневмонию, диагноз которой рентгенологически не был подтвержден, тимомегалия нами была выявлена у 35% пациентов 1 — 3 мес, у 15% детей в возрасте 3–6 мес, у 8% — в возрасте 7–15 мес, у 2% — в возрасте 16 — 36 мес, а в популяции детей старше 3 лет частота выявления тимомегалии не превышала 0,5% [8].
Наблюдение за одними и теми же детьми на протяжении длительного отрезка времени позволило нам сделать вывод, что тимомегалия в детском возрасте может быть как транзиторной, так и стойкой.
Анализ родословных позволил выявить у родственников первой и второй линии родства детей с синдромом Платтера высокую частоту встречаемости злокачественных новообразований, аутоиммунных заболеваний и заболеваний системы эндокринных органов. Так, злокачественные новообразования встречаются в каждой третьей семье, где есть дети с синдромом Платтера, с такой же частотой в этих семьях регистрируются эндокринные заболевания (преимущественно сахарный диабет и заболевания щитовидной железы). В семьях детей с синдромом Платтера статистически чаще, чем в семьях детей из выборки общей популяции, распространены аутоиммунные заболевания (диффузные болезни соединительной ткани) и туберкулез. Помимо этого, многие родители детей с указанным синдромом в дошкольном и младшем школьном возрасте относились к группе часто болеющих, т. е. к группе детей имевших повышенную склонность к острым респираторным вирусным инфекциям (ОРВИ).
Характер перечисленных заболеваний (склонность к вирусным, аутоиммунным, онкологическим заболеваниям, туберкулезу) может указывать на существование у близких родственников детей с синдромом Платтера недостаточной активности клеточного звена иммунной системы, поскольку, согласно современным воззрениям, все перечисленные заболевания находятся под контролем Т-клеточного иммунитета, формируемого вилочковой железой. При этом не совсем ясно, чем объясняется высокая отягощенность родственников детей с синдромом Платтера болезнями системы эндокринных органов. Однако не следует забывать о том, что эндокринные заболевания (в том числе сахарный диабет, диффузный токсический зоб, гипотиреоз) могут иметь аутоиммунный генез.
В таком случае у близких родственников детей с синдромом Платтера отчетливо просматривается тенденция к заболеваниям, связанным с иммунными механизмами клеточного типа, контролирующимися вилочковой железой. Это позволяет предполагать возможность передачи детям, у которых развился синдром Платтера, какого-то дефекта Т-звена иммунной системы.
Антенатальный период у большинства детей с синдромом Платтера осложняется хронической гипоксией, обусловленной острыми инфекционными заболеваниями или обострением хронических экстрагенитальных заболеваний матерей, наличием у них сосудистой дистонии, анемии, гестозов.
Осложненное течение интранатального периода отмечается не менее чем у 2/3 детей с синдромом Платтера. Наиболее частыми осложнениями этого периода явились стремительные или затяжные роды, приведшие к наложению щипцов или экстренному кесареву сечению.
Группа детей с указанным синдромом по фенотипу гетерогенна. 90% детей имеют мягкие округлые формы тела, некоторую пастозность тканей, относительно крупные черты уплощенного лица, прямой тип лба, широкоовальные глаза, относительно короткий нос с низким переносьем, средней величины или толстые губы, слабый изгиб профиля, короткую шею. Дети этой группы имеют как бы увеличенные поперечные размеры тела: широкое лицо, широкая грудная клетка, широкие плечи, широкие ладони и стопы, относительно короткие и широкие пальцы. Около 3/4 детей-европеоидов этой подгруппы имеют нежную, но несколько утолщенную, слабопигментированную белую кожу, для которой характерно быстрое развитие ожога после инсоляции, светлую окраску волос и глаз, слабое развитие мускулатуры, сниженную физическую активность. Дети данной подгруппы отличаются хорошим (и даже избыточным) аппетитом и высокими темпами роста.
В дошкольном и младшем школьном возрасте у них отмечаются хорошее развитие подкожного жирового слоя, слабое развитие мускулатуры, снижение общего тонуса и тургора тканей, а также физической активности, замедленная реакция на внешние раздражители, замедленное образование новых условных рефлексов, ослабление процессов внутреннего торможения с преобладанием реакций внешнего торможения.
Клиническая характеристика детей с синдромом Платтера включает характеристику системы лимфоидных органов, которая, согласно мнению большинства исследователей, отличается генерализованной гиперплазией системы лимфоидных органов: лимфатических узлов, лимфатических фолликулов корня языка, задней поверхности глотки, поверхности надгортанника, гипертрофией небных и глоточной миндалин. Наши наблюдения, однако, показали, что состояние периферических лимфоидных органов зависит от воздействия антигенного стимула — при отсутствии такого воздействия генерализованная гиперплазия периферического лимфоидного аппарата не развивается [7].
К числу особенностей физического развития детей грудного и раннего возраста относятся: высокие темпы увеличения длины тела, слабое развитие скелетной мускулатуры, несвоевременность и неправильный порядок прорезывания молочных зубов, относительно позднее начало самостоятельной ходьбы.
В эмоциональной сфере в первые 2–3 мес жизни обращает внимание менее выраженный комплекс оживления (за счет снижения двигательной активности).
Начало становления речи у детей с синдромом Платтера не отличалось от такового у детей соответствующего возраста в популяции в целом: гуление, слоги и первые слова у них появлялись своевременно.
К возрасту 10–11 мес они начинали произносить первые одно- и двусложные слова, к 1 году количество активно произносимых слов достигало 10–12. В дальнейшем 8% детей данной группы до 2-летнего возраста продолжали пользоваться только этими 10–12 словами. В возрасте 4,5–6 лет 25% детей этой группы страдали дислалией, требующей проведения корригирующих логопедических занятий в условиях детской поликлиники или в условиях специализированного детского сада. У отдельных пациентов нарушение, связанное с произношением звуков, сохранялось и в подростковом возрасте.
Состояние здоровья детей с синдромом Платтера. Здесь рассматриваются только те заболевания и патологические состояния, которые достоверно чаще встречались у детей с указанным синдромом, по сравнению с детьми из общей популяции. При анализе структуры выявленных заболеваний наибольшую по численности группу составили аномалии развития (выявлены у 80% наблюдавшихся пациентов) — пороки развития, множественные стигмы дизэмбриогенеза, биохимические дефекты. Пороки развития чаще проявлялись гипоплазией органов и тканей: широкие отверстия паховых каналов и пупочного кольца, септальные дефекты в сердце, гипоплазия аорты, сердца, легких, почек, щитовидной железы и др.
Вторая группа заболеваний была представлена патологическими состояниями нервной системы. Наряду с заболеваниями нервной системы, обусловленными биохимическими дефектами (синдром Менкеса; ганглиозидоз Gm1; фенилкетонурия; галактоземия), обращали на себя внимание такие синдромы, как гипертензионно-гидроцефальный (у 49%), фебрильных судорог (у 20%), мышечной гипотонии (у 18%) и вегетативно-висцеральной дисфункции (у 12,5%). Включение в комплекс обследования электрофизиологических методов, компьютерной и ядерно-магнитно-резонансной томографии привело к существенному увеличению частоты выявления гипертензионно-гидроцефального синдрома (выявлен у 90%). Указанный синдром у 2/3 детей сочетался с синдромами фебрильных судорог и вегетативно-висцеральных дисфункций, однако последние два синдрома у части детей встречались и изолированно.
Изолированный синдром вегетативно-висцеральных дисфункций характеризовался крайне выраженным полиморфизмом проявлений: нарушение терморегуляции, дыхания, сердечной деятельности, функции желудочно-кишечного тракта, пароксизмальное повышение артериального давления и другие расстройства. Мы склонны считать, что синдром вегето-висцеральных дисфункций у детей с синдромом Платтера встречается значительно чаще, чем у указанных 12,5% пациентов. На существование гиподиагностики синдрома вегето-висцеральных дисфункций могут указывать выявленные нами фенотипические особенности детей, в том числе очень хороший (скорее избыточный) аппетит, склонность к задержке жидкости, как бы немотивированный субфебрилитет. Наши наблюдения показали, что у большинства детей с якобы немотивированным субфебрилитетом последний хорошо контролировался мочегонными средствами, что явно указывает на связь этого симптома с ликворной гипертензией, в том числе с повышением давления в области третьего желудочка мозга — месте локализации центра терморегуляции.
У детей с синдромом Платтера обращал на себя внимание и синдром мышечной гипотонии, который у ряда пациентов был настолько сильно выражен, что специалисты высказывали предположение о наличии у них болезни Верднига–Гоффманна или миелодисплазии.
Таким образом, частое выявление у детей с синдромом Платтера внутренней гидроцефалии, изолированного синдрома вегето-висцеральных дисфункций, наличие вегетативных нарушений указывает на возможность нарушения функции диэнцефальной области. Изменения со стороны скелетной мускулатуры трактовать сложнее. Однако если учесть, что средний мозг, примыкающий к области сильвиева водопровода, контролирует регуляцию мышечного тонуса и сигналы к мышцам поступают через ретикулярную формацию по двум ретикулоспинальным путям [11], то это нарушение может быть рассмотрено с позиции существования у данного контингента детей внутренней гидроцефалии и расстройства ликвородинамики, поскольку гипоталамус, таламус и ретикулярная формация являются звеньями единой суперфункциональной системы, корригирующей гомеостатические программы наиболее сложных вегетативных, эндокринных, трофических и психических функций [12].
Все исследователи, занимавшиеся изучением особенностей лиц со стойкой тимомегалией (а основную группу в них, вне всякого сомнения, составляют дети с синдромом Платтера), обращали внимание на их пониженную физическую активность.
При специальном опросе 72 пациентов в возрасте 10–24 лет с синдромом Платтера у 46% из них было отмечено негативное отношение к физическим нагрузкам, особенно к бегу на длинные дистанции и езде на велосипеде. Подростки и лица молодого возраста, способные передать ощущения, появлявшиеся при физической нагрузке, отмечали на ее фоне чувство слабости, ощущение нехватки воздуха.
Когда у 30 подростков с синдромом Платтера, не имевших органических заболеваний сердца, было проведено эхокардиографическое исследование сердца на аппарате 128 х Р — ACUSON (США) с определением массы миокарда левого желудочка сердца, у 27 из них индексированная (относительно массы тела) масса миокарда левого желудочка сердца оказалась достоверно меньше (р
Л. Г. Кузьменко, доктор медицинских наук, профессор
РУДН, Москва
Анатомическое строение вилочковой железы, признаки её заболевания. Опухоли вилочковой железы. Признаки проявления тимомегалии, тимиколимфатический статус. Возрастная инволюция тимуса. Характеристика последствий нарушений функций вилочковой железы.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 16.11.2015 |
| Размер файла | 17,5 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Министерство сельского хозяйства РФ
Кафедра патологической физиологии
Вилочковая железа (тимус) является центральным органом иммунной системы позвоночных. Находится в грудной полости в районе переднего средостения, немного далее перикарда.
Состоит из двух долей, которые могут быть сращены или же просто плотно прилегают друг к другу. Нижняя часть каждой доли широкая, а верхняя узкая; таким образом, верхний полюс может напоминать двузубую вилочку (отсюда и название).
Орган покрыт капсулой из плотной соединительной ткани, от которой в глубину отходят перемычки, делящие его на дольки.
Вырабатывает Т-лимфоциты и гормоны: тимозин, тималин, тимопоэтин, инсулиноподобный фактор роста-1 (ИФР-1), тимусный гуморальный фактор-все они являются белками (полипептидами).
В тимусе Т-лимфоциты заселяют корковую зону, где активно размножаются и созревают, обучаются распознавать свои клетки, приобретают различные рецепторы и маркеры на мембранах . 95% Т-лимфоцитов погибает в здесь, так как неспособны распознавать свои и чужие клетки. Из тимуса выходят достаточно зрелые, дифференцированные Тh, TS и Tr лимфоциты, но в неактивном состоянии.
Вилочковая железа (тимус, зобная железа) является одним из самых главных и необходимых органов для деятельности, а также формирования иммунной системы.
Нарушения функций вилочковой железы
Дистопия - нарушение, при котором зобная железа располагается не в предназначенном месте. Когда происходит нарушение функции или железа отсутствует, могут возникнуть нарушения в клеточном иммунитете, благодаря чему, возможность сопротивления организма животного различным инфекционным заболеваниям снизится. Помимо этого могут возникнуть и аутоиммунные заболевания, когда с распознанием клеток собственного организма иммунная система не справляется, начинает их атаковать и разрушать ткани организма.
К числу аутоиммунных заболеваний относят миастению (заболевание мышечной и нервной системы, которое проявляется быстрой утомляемостью и слабостью мышц), артрит ревматоидный и разнообразные болезни щитовидной железы.
Вследствие нарушений функционирующего клеточного иммунитета Т - лимфоцитов чаще возникают и различные злокачественные опухоли.
Инволюцию вилочковой железы у взрослых животных (сокращение в размерах) могут вызвать радиация, плохое питание, разнообразные инфекции.
Признаки и причины заболеваний вилочковой железы
Функциональные нарушения тимуса могут быть не только с рождения, они могут появиться и благодаря поражению тканей вилочковой железы (у взрослых животных) под действием различных факторов.
В значительной степени встречается увеличенная вилочковая железа --тимомегалия. К этому могут привести как инфекции, так и различные факторы извне, оказывающие негативное влияние на организм. Данная разновидность заболевания переходит и генетически. В значительных количествах случаев патология вилочковой железы в раннем возрасте у детенышей развивается благодаря неправильным процессам в период беременности матери, в случаях поздней беременности, нефропатии, или же при инфекционной зараженности матери.
Определяется вилочковая железа у детенышей по следующим симптомам: увеличиваются все лимфатические узлы, а также тканевая часть задней поверхности глотки, рентгеновский снимок показывает увеличенный тимус. Помимо этого возможны и другие аномалии в развитии (грыжа, вывих бедренной кости, и т.п.). вилочковая опухоль тимомегалия инволюция
К одним из главных симптомов относятся нарушение сердечного ритма, появление мраморного рисунка на коже, гипотония, гипергидроз. Сюда же следует отнести и гипоплазию половых органов у самок и крипторхизм у самцов.
К признакам появления тимомегалии следует отнести быструю потерю и увеличение веса детеныша, немалый вес его на момент рождения. Также данное заболевание сопровождается бледностью кожных покровов. Очень часто симптомами заболевания вилочковой железы является повышенная температура.
Патофизиология тимуса
Тимиколимфатический статус(Status thymico-lymphaticus)-
состояние, связанное с увеличением тимуса по сравнению с нормой и ослабление его инволюции. Наблюдается гиперплазия лимфоидной ткани, лимфоцитоз,гипоплазия надпочечников,органов иммунной защиты. Главной особенностью тимико-лимфатического статуса является чрезвычайная чувствительность к воздействию препаратов, не вызывающих у здоровых животных какой-либо реакции, например эфирный наркоз, который таким больным абсолютно противопоказан
Миастения (myasthenia gravis pseudoparalytica) - заболевание, характеризующееся нарастающей мышечной слабостью и патологической утомляемостью мускулатуры. Оно начинается с нарушений деятельности глотательных, жевательных, и глазодвигательных мышц (особенно типично поражение мышцы, поднимающей верхнее веко, затем в процесс включаются и другие мускулы. В тяжелых случаях поражается дыхательные мышцы (в том числе и диафрагма), что может привести к развитию сначала хронической дыхательной недостаточности, а затем и асфиксии, и угрожать жизни. Болезнь имеет прогрессирующее течение, но для нее характерны достаточно длительные ремиссии.
Согласно современным данным патогенез этого заболевания связан с аутоиммунным поражением постсинаптических рецепторов ацетилхолина. Исследования, проведенные с применением радиоизотопной методики, показали, что в мышце при миастении количество ацетилхолиновых рецепторов уменьшается на 75-90%. Данные факты были подтверждены и электронномикроскопически. Сказанное свидетельствует о постсинаптической блокаде возбуждения. Уменьшение количества рецепторов связано с их повреждением специфическими аутоантителами. Данная концепция подтверждается наличием в крови у 80-90% больных миастенией аутоантител к ацетилхолиновым рецепторам, а также эффективностью ее иммунносупрессивной терапии. В тимусе у таких пациентов обнаруживаются Т- и В-лимфоциты, повреждающие ацетилхолиновые рецепторы, а также - определенные морфологические изменения. Только у 10-20% пациентов тимус соответствует нормальному . В остальных случаях отмечается увеличение количества В-лимфоцитов и ретикулярных клеток в периваскулярных пространствах и периферических отделах железы, а также отсутствие лимфатических фолликулов. В значительном проценте случаев тимус гиперплазирован.
Существует представление, что возникновение миастении связано с повышением активности в организме холинэстеразы, вследствие чего резко снижается количество ацетилхолина - важнейшего медиатора проведения возбуждения. При блокаде холинэстеразы у больных животных восстанавливается двигательная функция мышц, а при прекращении этой блокады проявления миастении вновь начинают нарастать. При миастении нарушаются также тканевое дыхание, креатин-креатининовый и электролитный обмен (накопление кальция).
Опухоли вилочковой железы
· Тимома -- из эпителиальных клеток вилочковой железы
· Т-клеточная лимфома -- из лимфоцитов и их предшественников
Пре-Т-лимфобластные опухоли в ряде случаев имеют первичную локализацию в тимусе и выявляются как массивный инфильтрат в средостении с последующей быстрой трансформацией в лейкоз.
Функции тимуса снижаются:
· При стрессе и лечебном применении глюкокортикоидов и половых гормонов
· При действии излучений
· При хронических воспалительных процессах
· При заболеваниях, сопровождающихся гормональными нарушениями
Последствия гипофункции тимуса:
· Снижение резистентности к патогенам
· Повышение частоты развития аутоиммунных заболеваний
Последствия нарушений функций тимуса:
· Уменьшение числа лимфоцитов
· Утрата лимфатическими узлами фолликулярного строения (отсутствуют зародышевые центры, их место занимают ретикулоэндотелиальные элементы, которые гиперплазируются)
· Атрофируются пейеровы бляшки
· Подавляется иммунологическая реактивность организма
· Развивается гиперчувствительность замедленного типа
· Снижается образование антител
Таким образом, любые нарушения функций вилочковой железы приводят к снижению иммунной системы организма, что отрицательно сказывается на всех его структурах.
Список используемой литературы
1. Балаболкин М.И. Эндокринология. Изд-во: Универсум паблишинг,Москва,1998.
2. Глушен С.В.. Цитология и гистология. Курс лекций. -- Минск, 2003.
3. Ройт А., Бростофф Дж., Мейл Д. Иммунология. М.2000.
4. Ярилин А.А. Тимус. Возможности и значимость оценки его функции. Лекции.
Подобные документы
Анатомическое строение и функции вилочковой железы - важного органа иммунной системы. Анализ влияния гормонов на функции тимуса. Гистологическое строение, нарушения в работе и заболевания вилочковой железы. История научного изучения вилочковой железы.
реферат [1,1 M], добавлен 05.07.2016
Расположение и функции вилочковой железы, относящейся к центральным органам иммунной системы. Возрастная инволюция вилочковой железы, которая характеризуется постепенным замещением ее ткани жировой клетчаткой. Фазы акцендентальной трансформации тимуса.
презентация [1,0 M], добавлен 21.11.2013
Возрастная инволюция тимуса. Функции вилочковой железы. Врожденная и приобретенная тимомегалия. Фазы акцендентальной трансформации тимуса. Аплазия, гипо- и дисплазия вилочковой железы. Наследственная недостаточность периферической лимфоидной ткани.
презентация [1,0 M], добавлен 12.10.2016
Основные функции вилочковой железы: лимфопоэтическая, иммунорегуляторная и эндокринная. Рассмотрение возрастной инволюции вилочковой железы как причины падения активности клеточного иммунитета. Классификация фаз акцендентальной трансформации тимуса.
презентация [1020,3 K], добавлен 23.02.2014
Доброкачественные и злокачественные опухоли щитовидной железы. Морфологические варианты аденомы щитовидной железы, их характеристика, клинические симптомы, особенности диагностики и лечения. Классификация злокачественных новообразований щитовидной железы.
презентация [3,1 M], добавлен 02.04.2017
Статистика заболеваемости раком молочной железы, основные причины его развития. Типы рака молочной железы по анатомической форме роста. Клинические признаки фиброзно-кистозной мастопатии. Симптомы фиброаденомы, ее виды. Самообследование молочной железы.
презентация [365,3 K], добавлен 14.07.2015
Тимома как опухоль, происходящая из эпителиальных клеток мозгового или коркового слоя вилочковой железы, либо ее остатков. Диагностика тимом, методы лечения, описание операционного вмешательства по поводу тимомы. Эмбриональные опухоли средостения.
II кафедра клинической хирургии (заведующий - профессор Тимофей Павлович Макаренко) Центрального института усовершенствования врачей на базе Центральной клинической больницы № 1МПС.
Публикация посвящается памяти Василия Дмитриевича Стоногина (1933-2005)
Заболевания вилочковой железы изучаются врачами различных специальностей: невропатологами, эндокринологами, иммунологами, гемато¬логами, хирургами, патогистологами и др. Проблема миастении является относительно изученной; в последние годы установлено участие вилочковой железы в таком жизненно важном процессе, как выработка (регулировка) иммунитета.
Опухоли и кисты вилочковой железы, миастения и некоторые аутоиммунные заболевания требуют хирургического лечения. Значительный вклад в этот сложный раздел внесли отечественные и зарубежные хирурги (А. Н. Бакулев и Р. С. Колесникова; В. Р. Брайцев; Б. К. Осипов; Б. В. Петровский; М. И. Кузин и соавт.; С. А. Гаджиев и В. Васильев; Viets, и др.).
С 1966 по 1973 год мы наблюдали 105 больных с различными заболеваниями переднего средостения, из них 66 с различными заболеваниями вилочковой железы. Эти больные были разделены на следующие клинические группы: 1-я - 30 больных с гиперплазией вилочковой железы и явлениями миастении; 2-я - 23 больных с опухолями вилочковой железы (тимомами), из них с доброкачественными 15, в том числе с явлениями миастении 9; со злокачественными 8, в том числе с явлениями миастении 5; 3-я - 4 больных с кистами вилочковой железы, все без миастении; 4-я - 3 больных с тератоидными образованиями; 13-я - 2 больных - лимфогранулематоз с изолированным поражением вилочковой железы; 6-я - 4 больных с апластической анемией на фоне аутоиммунной агрессии вилочковой железы.
Из 66 больных 65 были оперированы: 62 произведена радикальная и 3 эксплоративная операция.
С явлениями миастении под нашим наблюдением было 44 больных, из которых 43 (13 мужчин и 30 женщин) оперированы; возраст оперированных был от 14 до 55 лет, причем возраст большинства (25 больных) - от 15 до 30 лет. Среди больных с опухолями вилочковой железы преобладали 30-40-летние (13 больных).
Миастения - сложное нейроэндокринное заболевание, основным проявлением которого является слабость и особенно быстрая, патологическая мышечная утомляемость после физической нагрузки. Наряду с этим, согласно исследованиям ряда авторов (М. И. Кузин и соавт., и др.), при ми¬астении нарушается функция многих органов и систем (сердечно-сосудистой, дыхательной, пищеварительной, обмена веществ и т. д.).
Клиника миастении хорошо известна, однако правильный диагноз больному с миастенией нередко ставят после продолжительного наблюдения. У 32 из 44 наших больных правильный диагноз был поставлен только через 6-8 месяцев после появления первых признаков заболевания. Это объяс¬няется малой выраженностью клинической картины миастении в начальной стадии и плохой осведомленностью практических врачей, к которым впервые обращаются за помощью больные миастенией (невропатологи, окулисты, отоларингологи, терапевты).
При выраженной генерализованной форме миастении диагноз не труден. В начальной стадии и в случаях, когда миастения носит локализован¬ный характер (бульбарная, глазная, скелетно-мышечная, глоточно-лицевая), у наших больных предполагались самые разнообразные диагнозы, вплоть до подозрения на симуляцию. Считаем необходимым подчеркнуть особую важность прозериновой пробы, имеющей дифференциально-диагностическое значение. У больных миастенией внутримышечная инъекция 1-2 мл 0,05% раствора прозерина устраняет мышечную слабость и быструю утомляемость, в то время как при миопатиях и мышечной слабости, вызванных другими причинами, инъекция прозерина не дает эффекта. Имеют значение динамометрия, эргометрия и электромиография.
Общепризнано, что лечение миастении должно проводиться комплексно с участием 3-4 специалистов: невропатолога, терапевта-эндокринолога, анестезиолога-реаниматолога и хирурга. На основании большого клинического материала (сотни оперированных и наблюдаемых в отдаленном периоде) авторы подчеркивают преимущество оперативного лечения миастении перед консервативным (М. И. Кузин; А. С. Гаджиев и соавт., и др.). Результаты оперативного лечения лучше, если операцию производят впервые 2-2,5 года от начала заболевания. В более поздние сроки операция оказывается менее эффективной. Отсюда вытекает особая важность ранней диагностики миастении.
Из 43 оперированных нами больных в первый год заболевания миастенией поступили лишь 12, в сроки от 1 года до 3 лет - 23 и после 3 лет - 8 больных. Следовательно, больные поступали в клинику для оперативного лечения поздно.
Специальным методом исследования вилочковой железы является рентгеноконтрастный - пневмомедиастинография, которая позволяет судить о степени увеличения вилочковой железы, её структуре - отдель¬ный узел с четко ограниченными контурами или опухоль с инфильтрирую¬щим ростом и т. д.
Наличие у больного выраженной клинической картины прогрессирующей миастении является показанием к операции, так как все консервативные методы лечения, включая и рентгенотерапию, дают лишь временное улучшение.
У больных миастенией необходима специальная предоперационная подготовка, цель которой - снижение проявлений миастении путем индивидуального подбора дозы лекарственных препаратов. Дозировки препаратов подбирают строго индивидуально, с таким расчетом, чтобы в течение суток не наблюдалось периодов миастенического истощения, не наступало миастенического криза. Предоперационная подготовка, являясь симптоматической терапией, оказывает некоторое лечебное действие, что имеет положительное значение для предстоящей операции. Однако не у всех больных предоперационная подготовка, несмотря на ее комплексность и интенсивность, оказывается эффективной.
Вопрос о необходимости предоперационной рентгенотерапии нельзя считать окончательно решенным. Только 5 из наших больных перед операцией получали рентгеновское облучение, причем каких-либо улучшений в течении послеоперационного периода мы у них не отметили. У больных, оперированных по поводу злокачественной тимомы с явлениями миастении, предоперационное облучение играет важную роль в ближайшем исходе операции и в какой-то степени влияет на сроки наступления рецидива заболевания (М. И. Кузин и соавт.).
Большинство операций по поводу миастении нами выполнено из переднего доступа путем полной срединной продольной стернотомии. Наиболее ответственным моментом операции является отделение железы от левой плечеголовной вены. Ранение этого сосуда опасно из-за массивного кровотечения и возможной воздушной эмболии. В одном случае произошло ранение этой вены, закончившееся благополучно (был наложен боковой сосудистый шов). При операции следует избегать наложения зажимов на железистую ткань, раздавливания её.
У 3 наших больных было сочетание миастении и загрудинного зоба. Произведены тимэктомия и субтотальная струмэктомия.
У 26 больных во время операции была повреждена медиастинальная плевра, в том числе у 8 больных с обеих сторон. Осложнений, связанных с операционным пневмотораксом, не было. Если во время операции плевра не повреждена, переднее средостение дренируется одной резиновой трубкой, конец которой выводят в нижний угол раны или через отдельный прокол ниже мечевидного отростка и соединяют с отсосом. Вслед за тимэктомией трахеостома (превентивно) была наложена 5 больным.
Если сама операция тимэктомии по сравнению с другими торакальными операциями не представляет особой сложности, то течение послеоперационного периода у ряда больных сопровождается осложнениями, на 1-м месте среди которых стоит миастенический криз. Поэтому операции по поводу миастении возможны только в тех учреждениях, где можно обеспечить круглосуточное наблюдение анестезиолога-реаниматолога, а также многодневную аппаратную вентиляцию лёгких.
Вопрос о назначении антихолинэстеразных препаратов в послеоперационном периоде окончательно не решен. С целью уменьшения гиперсекреции бронхов лучше назначать прозерин с небольшими дозами атропина.
Тяжелый миастенический криз с расстройством дыхания, сердечной деятельности, глотания и т. д. наблюдали в первые дни после операции у 26 больных. Вывести из криза консервативными мероприятиями удалось 7 больных; 19 больным была наложена трахеостома с переводом их на аппаратное дыхание, длительность которого составляла от 3 до 40 суток. Через трахеостому систематически круглосуточно аспирируют слизь из трахеобронхиального дерева. Питание больных, находящихся на аппаратном дыхании, осуществляется через зонд. Помимо медикаментозного лече¬ния, применения кислорода, использования дыхательной гимнастики, в последние годы всем больным миастенией в послеоперационном периоде проводится лечебный массаж всего тела, повторяемый несколько раз в день.
Трахеостомическую трубку удаляют после того, как у больного стойко восстанавливается самостоятельное дыхание.
Из 43 оперированных по поводу миастении в первые дни после операции умерли 3 больных. Это относится к периоду, когда в клинике только осваивались эти операции. Все больные оперированы в тяжелом состоянии. Отдаленные результаты прослежены у 26 больных: выздоровление наступило у 17 и улучшение (больные принимают антихолинэстеразные препараты) - у 8 больных; состояние осталось без изменений у 3 больных. Двое оперированных умерли от рецидива злокачественной тимомы (один - с явлениями миастении через 3 года, другой - с инфарктом миокарда).
Доброкачественные опухоли вилочковой железы (тимомы) представля¬ют собой узлы округленной формы с плотной капсулой. При гистологическом исследовании в этих опухолях наряду с соединительнотканными клетками обнаруживаются фибробласты и концентрически расположенные вытянутые эпителиальные клетки, напоминающие тельца Гассаля. Эти опухоли по строению напоминают склерозирующую ангиому, еще их называют ретикулярной перителиомой (Pope и Osgood). Особое место занимают липотимомы. Одни авторы относят их к доброкачественным опухолям, другие - к злокачественным (Andrus и Foot). Опухоли эти нередко достигают боль¬ших размеров и состоят из жировой дольчатой ткани, содержащей скопления тимоцитов и гассалевых телец. Если в опухоли преобладает жировая ткань, её рекомендуют называть липотимомой, если преобладают элементы вилочковой железы - тимолипомой.
Среди наших больных мы наблюдали 3 (2 мужчин и 1 женщину, все старше 40 лет) с липотимомой. У них опухоль была небольших размеров, с ровными четкими границами; опухоль была расценена нами как доброкачественная. Заболевание сопровождалось умеренно выраженными явлениями миастении. Один из этих больных поступил с жалобами на слабость и быструю утомляемость; при дальнейшем обследовании у него была выявлена тяжелая гипопластическая анемия. Больной оперирован; в ближайшем послеоперационном периоде отмечены благоприятные результаты.
Из 15 наших больных с доброкачественными тимомами у 9 (4 мужчин и 5 женщин) были явления миастении, у остальных опухоль ничем себя не проявляла и была выявлена случайно.
Злокачественные тимомы - плотные, различных размеров бугристые опухоли, нередко прорастающие капсулу. У больных с этими новообразованиями из-за быстрого роста опухоли, прорастания соседних органов или сдавления их рано развивается синдром медиастинальной компрессии. Больные жалуются на боли за грудиной, чувство давления в грудной клетке и др. Нередко злокачественные тимомы протекают с явлениями миастении, отмеченной нами у 5 из 8 больных. Злокачественная тимома может протекать и совершенно бессимптомно. Приводим пример.
Больной М., 19 лет, поступил 17.III.1966 года. Жалоб нет. После окончания средней школы при прохождении медицинского обследования для поступления в учебное заведение у него рентгенологически было выявлено опухолевое образование в переднем средостении. Признаков миастении нет. Пневмомедиастинография: в переднем средостении со всех сторон окутанное газом образование продолговатой формы размером 15*5 см, с участками просветления в центре; заключение: опухоль вилочковой железы, возможно, с участками распада. Произведена тимэктомия. Гистологически: злокачественная тимома ретинулоклеточного типа. Проведена послеоперационная рентгенотерапия. Осмотрен через 4 года после операции:, жалоб нет, состояние хорошее, признаков рецидива нет.
Дифференциальный диагноз доброкачественных и злокачественных тимом нередко бывает трудным. Злокачественная тимома по рентгенологическим признакам напоминает лимфогранулематоз и лимфосаркому. В отличие от этих образований тимома располагается непосредственно за грудиной, обычно бывает овально-сплющенной или конусовидной формы. Всякая тимома, протекает она с явлениями миастении или без них, подлежит удалению, В литературе имеются указания, что каждую тимому следует рассматривать как потенциально злокачественную опухоль (Б. В. Петровский; Seybold и соавт., и др.).
Кисты вилочковой железы встречаются довольно редко. Обычно это тонкостенные образования различных размеров, расположенные в толще железы, выполненные желтоватой или коричневатой жидкостью. Из-за эла¬стичности этих образований признаков сдавления окружающих органов не наблюдается. Клиническая картина кист, если они протекают без миастении, бедна. Как правило их обнаруживают случайно, при профилактическом осмотре. Все наши 4 больных (3 женщины и 1 мужчина) были старше 40 лет (41 год - 48 лет). Ни у одного больного не было признаков миастении, хотя описаны сочетания кисты вилочковой железы и миастении. Все были оперированы (тимэктомия) с благоприятным результатом.
У 3 оперированных нами больных опухоль переднего средостения по гистологическому строению была тератомой. Учитывая тесную связь образования с остатками вилочковой железы и наличие в самом образовании ткани вилочковой железы, мы расценили опухоль как тератому вилочковой железы. У 2 больных на основании признаков (появление в мокроте сальных масс, волос у одной больной, а также обнаружение органоидных включений на рентгенограмме у другой) диагноз был поставлен до операции, у третьей больной - лишь во время операции. Из 3 оперированных больных у 2 при¬шлось удалить не только тератоидное образование, но и долю лёгкого из-за вовлечения последнего в процесс (прорыв нагноившейся тератомы в верхнедолевой бронх). Высокая степень злокачественного превращения тератоидных образований, возможность нагноения и другие осложнения убеждают в необходимости раннего и радикального хирургического удаления этих новообразований.
Вопрос о возможности изолированного поражения вилочковой железы лимфогранулематозом представляется спорным. Мы наблюдали 2 больных, у которых до операции был установлен диагноз “опухоль вилочковой железы”. После операции, при гистологическом исследовании препаратов, диагноз был изменен: изолированное поражение лимфогранулематозом вилочковой железы. Принимая во внимание указания о возможности изолированного поражения вилочковой железы на ранних стадиях заболевания (С. А. Гаджиев и В. В. Васильев), оба эти наблюдения мы отнесли к патологии вилочковой железы. После операции за больными ведётся наблюдение в течение 5 лет. Признаков рецидива и генерализации процесса нет.
Заболевание, заключающееся в сочетании патологии вилочковой желе¬зы и гипопластической анемии, которая возникает вследствие избирательного поражения костного мозга без изменения продукции лейкоцитов и тромбоцитов, впервые описано Кацнельсоном в 1922 году. Позже было предположено, что вилочковая железа влияет на гемопоэтическую функцию костного мозга, регуляцию состава белковых фракций, состояние лимфоидной системы и т. д. (Soutter и соавт.). С тех пор опубликованы данные некоторых авторов об отдельных операциях на вилочковой железе при различных болезнях крови (А. Н. Бакулев, 1958; Chaemers и Boheimer, и др.). К настоящему времени нами произведены 4 операции тимэктомии у больных гипопластической анемией. О результатах этих операций говорить пока рано, так как после них прошел небольшой срок. Ближайшие результаты удовлетворительные у 3 больных.
- В вилочковой железе возникает ряд патологических процессов, которые требуют оперативного лечения.
- Оперативное лечение по поводу миастении оправдано как при наличии рентгенологически и клинически определяемой опухоли, так и лишь при гиперплазии вилочковой железы.
- Операцию рекомендуется производить в ближайшее время после установления диагноза. Лучевое лечение целесообразно проводить после удаления злокачественной опухоли или если произвести радикальную операцию невозможно.
1) Бакулев А. Н., Колесникова Р. С. Хирургическое лечение опухолей и кист средостения. М., 1967.
2) Брайцев В. Р. Врожденные дизонтогенетические образования средостения и легких. М., 1960.
3) Гаджиев С. А., Догель Л. В., Ваневский В. Л. Диагностика и хирургическое лечение миастении. Л., 1971.
4) Гаджиев С. А., Васильев В. Мед газета, 1973, №15.
5) Кузин М. И. Клин мед, 1969, № 11, с. 6.
6) Кузин М. И., Успенский Л. В., Волков Б. П. Вести, хир., 1972, №7, с.48.
7) Осипов Б. К. Хирургические заболевания легких и средостения. М., 1961.
8) Петровский Б. В. Хирургия средостения. М., 1960.
9) Andгus W., Fооt N., J. thorac. Surg., 1937, v. 6. p. 648.
10) Chaemers G., Boheimer K., Brit. med. J., 1954, v.2, p.1514.
11) Pope R., О s g о о d R., Am. J. Path., 1953, v. 20, p. 85.
12) S е у b о 1 d W., D о n a 1 d М. С., J. thorac. Surg. Clagett C. et al., 1950, v. 20, p.195.
13) Soutter G., Sommers Sh. R e 1 m о n Ch. et al. Ann. Surg., 1957, v. 146, p. 426.
14) Viets H., Brit. med. J., 1950, v. 1, p.139.
Данные об авторах:
| 1) Виктор Львович Маневич – профессор, доктор медицинских наук, 2-я кафедра клинической хирургии ЦОЛИУв. |  |
| 2) Василий Дмитриевич Стоногин – доцент 2-й кафедры хирургии ЦОЛИУв, заведующий учебной частью кафедры, кандидат медицинских наук. E-mail: svas70@mail.ru |  |
Восстановление текста, компьютерная графика - Сергей Васильевич Стоногин.
Любое копирование материала запрещено без письменного разрешения авторов и редактора.
С самого рождения он готовит наш организм к встрече с бактериями, вирусами и другими чужеродными микроорганизмами. Но эта крошечная железа выполняет не только защитную функцию, в ней вырабатываются тимические гормоны. Они способствуют восстановлению клеток, тем самым замедляя старение нашего организма.
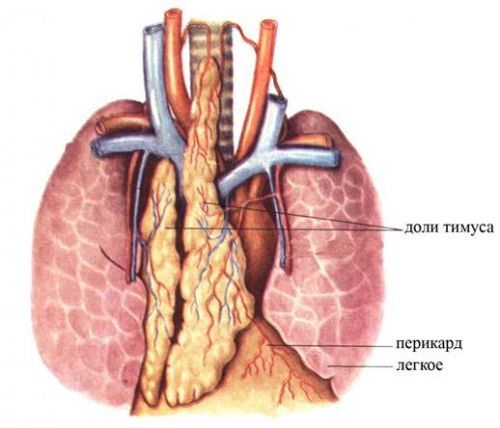
Внешний вид и строение
Тимус человека находится в верхнем отделе грудной клетки, имеет розовато-серый цвет и состоит из двух долей — правой и левой. Он окружен капсулой из соединительной ткани, от которой через каждую долю проходят волокна, разделяя железу на несколько небольших частей.
Доли вилочковой железы неодинакового размера. В некоторых случаях они соединены, а иногда разделены, но тесно прилегают друг к другу. Верхняя их часть более узкая, проходит рядом с трахеей и напоминает вилочку из двух зубьев. Нижняя — шире, располагается за грудиной на уровне третьего-четвертого межреберья и прикрывает крупные сосуды сердца, а также часть перикарда.
Тимус новорожденного младенца весит 10–12 грамм. Он постоянно растет и к моменту половой зрелости достигает своей максимальной массы — 30–40 грамм, после чего постепенно уменьшается в размерах и утрачивает свои основные функции. Этот процесс называется акцидентальной инволюцией тимуса.
К 25 годам вес зобной железы уменьшается до 20–25 грамм, к 55 — до 15 грамм, к 65 составляет примерно 6 грамм. После инволюции большую часть работы за выработку лимфоцитов у взрослых людей берут на себя селезенка и лимфатические железы.
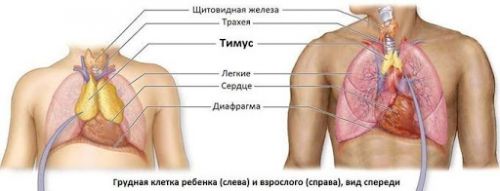
Функции и гормоны вилочковой железы
Т-клетки делятся на три типа:
- клетки-киллеры, уничтожают инфицированные клетки;
- клетки-хелперы, отвечают за создание антител В-клетками и за работу других типов Т-клеток в борьбе с инородными агрессорами;
- клетки-регуляторы (супрессоры), подавляют В-клетки и другие Т-клетки, выступая блюстителями порядка.
Выработка тимусовых пептидов и новых Т-клеток снижается постепенно. К старости вилочковая железа замещается жировой и соединительной тканью. Это одна из причин, по которой у пожилых людей организм становится уязвимее для разных недугов. А стрессы, некачественное питание, вредные привычки многократно увеличивают естественную потерю функций тимуса.
Кроме обучения лимфоцитов, зобная железа вырабатывает гормоны, необходимые для полноценной работы организма:
- ИФР-1;
- тимозин;
- тималин;
- тимопоэтин.
Особенности гормонов тимуса
ИФР-1 или инсулиноподобный фактор роста 1 — полипептидный гормон, схожий по функциям на инсулин. Он участвует в синтезе белка и влияет на рост мышечной и костной ткани, а также:
- защищает сердечно-сосудистую систему от раннего старения;
- ускоряет обмен веществ;
- увеличивает действие инсулина.
Нарушение баланса ИФР приводят к серьёзным последствиям для организма:
- В детском возрасте недостаток соматомедина (другое название ИФР) вызывает задержку развития и роста.
- Дефицит у взрослых может спровоцировать хрупкость костей, ослабить мышцы, изменить структуру жиров, нарушая метаболизм.
- Переизбыток гормона повышает риск развития диабета, гипертонии, заболеваний сердца и сосудов.
Тимозин — полипептид, который регулирует развитие скелета, участвует в углеводном и кальциевом обмене, стимулирует выработку гонадотропных гормонов в гипофизе. А также:
- укрепляет иммунную систему при активных инфекционных и воспалительных проблемах;
- обеспечивает противоопухолевый иммунитет;
- предотвращает септические осложнения;
- ускоряет рост волос и заживление ран.
До полового созревания тимозин отвечает за активное продуцирование лимфоцитов, участвуя в формировании иммунитета.
Тимулин — гормон, активно взаимодействующий с цинком и регулируемый гипофизом. Основные функции:
- контроль за соотношением Т- и В-лимфоцитов;
- усиление фагоцитоза (захвата и уничтожения клетками-киллерами болезнетворных микробов);
- стимуляция процессов восстановления поврежденных тканей и кроветворения;
- улучшение клеточного метаболизма.
Тимулин важен для профилактики аутоиммунных, иммунодефицитных, эндокринных заболеваний в любом возрасте. Также он борется с нарушениями обмена цинка в организме.
Тимпоэтин — полипептид, состоящий из 49 аминокислот. Его задачи:
- формировать и контролировать деятельность Т-клеток (подавлять или стимулировать, в зависимости от ситуации);
- блокировать передачу нервных импульсов.
Низкая концентрация тимпоэтина угрожает здоровью, потому что это снижает активность Т-клеток, ответственных за иммунитет.
Диагностика
Чтобы проверить работу иммунной системы, назначают лабораторные исследования. Анализ крови поможет определить общее количество лимфоцитов и иммуноглобулинов, активность Т-клеток. Для оценки структурных изменений в зобной железе прибегают к методу биопсии.
Проводят и инструментальную диагностику:
- рентгенографию;
- УЗИ;
- КТ и МРТ.
Важно! Делать выводы о вовлечении тимуса в патологический процесс можно только после комплексного обследования других органов нейроэндокринной и иммунной систем.
Заболевания тимуса и их симптомы
Так как тимус регулирует работу иммунной системы, нарушение его деятельности нередко приводит к серьезным заболеваниям.
Патологий, влияющих на железу, достаточно много: начиная от генетических факторов, которые проявляются после рождения, и заканчивая онкологическими заболеваниями в пожилом возрасте.
Аплазия и гипоплазия (синдром Ди Джорджи)
Болезнь характеризуется недоразвитием или полным отсутствием тимуса по причине генетической мутации. Иммунные клетки не созревают, поэтому организм беззащитен перед инфекциями. Чаще всего встречается гипоплазия, когда орган развит слабо, но все-таки он есть.
Справка! Швейцарский синдром — тяжелая форма иммунного дефицита у младенцев первого года жизни, которая проявляется легочными инфекциями, кандидозом в ротовой полости, расстройством кишечного всасывания, гипотрофией. Свое название термин получил после возникновения серьезного иммунного дефицита у детей, проживающих в Швейцарии.
- укороченная впадина между носом и верхней губой;
- увеличенное расстояние между глазницами;
- низкое расположение ушных раковин;
- маленький размер верхней или нижней челюсти.
Кроме истинной гипоплазии, существует и приобретенная. Она может развиться после тяжелой формы воспаления легких, лучевой терапии, длительных гнойных процессов.
Гиперплазия
В отличие от атрофии гиперплазия — это увеличение тимуса из-за разрастания его тканей. Возникает по причине эндокринных нарушений, онкологических заболеваний, приема стероидов, ответной реакции организма на ожоги 3–4 степени и серьезные травмы, после химиотерапии.
- цианоз кожи;
- увеличение миндалин и лимфоузлов;
- частый сухой кашель;
- повышенное потоотделение;
- низкое артериальное давление;
- склонность к простудным заболеваниям.
Основной метод лечения гиперплазии — операция.
Тимома
Это новообразование в вилочковой железе. Чаще всего недуг поражает людей старше 40 лет. Коварство болезни в том, что на ранних стадиях она никак себя не проявляет. Доброкачественная тимома растет медленно, не выходит за пределы органа и не дает о себе знать годами.
Первые сигналы человек ощущает тогда, когда опухоль давит на органы средостения. При выходе опухоли за пределы тимуса возникает синдром нижней полой вены.
- боль в груди, отдающая в плечо, шейный отдел, между лопатками;
- тяжесть в голове;
- отечность и синюшный оттенок кожи лица;
- опущение верхнего века;
- кашель;
- одышка;
- шум в ушах.
Лечение зависит от степени распространения образования. Чаще всего это тимэктомия — удаление опухоли хирургическим путем.
Миастения
Это нейроэндокринное заболевание, ослабляющее поперечно-полосатые мышцы. При этой болезни человек испытывает слабость в разных мышцах.
- двоение в глазах;
- птоз;
- нарушение жевания и глотания;
- слабость в конечностях;
- проблемы с дыханием.
Различают генерализованную, бульбарную, глазную, туловищную формы миастении, поэтому клинические проявления отличаются и зависят от пораженного органа. Лечат болезнь консервативным методом, в тяжелых случаях прибегают к удалению вилочковой железы.
Кроме указанных патологий, следует отметить и заболевания, вызванные дефектами Т-лимфоцитов. Много жалоб, связанных с органом, исходит по причине приобретенного иммунодефицита. Он вызывает аутоиммунные (рассеянный склероз, ревматоидный артрит), аллергические, инфекционные, онкологические болезни. Вот почему многие задаются вопросом, как улучшить работу тимуса, и ищут способы замедления его атрофии.
Болезнями вилочковой железы занимаются врачи разных направлений: эндокринологи, иммунологи, невропатологи, гематологи, хирурги.
Читайте также:

