Почему выделение или поглощение теплоты относится к общим признакам химических реакций кратко
Обновлено: 05.07.2024
I. Признаки и условия протекания химических реакций
Вы уже знаете многие вещества, наблюдали их превращения и сопровождающие эти превращенияпризнаки.
Самым главным признаком химической реакции является образование новых веществ. Но об этом сожно судить и по некоторым внешним признакам протекания реакций.
Внешние признаки протекания химических реакций:
- выпадение осадка
- изменение цвета
- выделение газа
- появление запаха
- поглощение и выделение энергии (тепла, электричества, света)
Очевидно, что для возникновения и течения химических реакций необходимы некоторые условия:
- соприкосновение исходных веществ (реагентов)
- нагревание до определенной температуры
- применение веществ, ускоряющих химическую реакцию (катализаторов)
II. Тепловой эффект химической реакции
Д.И. Менделеев указывал: важнейшим признаком всех химических реакций является изменение энергии в процессе их протекания.
В каждом веществе запасено определенное количество энергии. С этим свойством веществ мы сталкиваемся уже за завтраком, обедом или ужином, так как продукты питания позволяют нашему организму использовать энергию самых разнообразных химических соединений, содержащихся в пище. В организме эта энергия преобразуется в движение, работу, идет на поддержание постоянной (и довольно высокой!) температуры тела.
Выделение или поглощение теплоты в процессе химических реакций обусловлено тем, что энергия затрачивается на процесс разрушения одних веществ (разрушение связей между атомами и молекулами) и выделяется при образовании других веществ (образование связей между атомами и молекулами).
Энергетические изменения проявляются либо в выделении, либо в поглощении теплоты.
Реакции протекающие с поглощением энергии называются эндотермическими (от латинского "эндо" - внутрь).
Чаще всего энергия выделяется или поглощается в виде теплоты (реже - в виде световой или механической энергии). Эту теплоту можно измерить. Результат измерения выражают в килоджоулях (кДж) для одного МОЛЯ реагента или (реже) для моля продукта реакции. Количество теплоты, выделяющееся или поглощающееся при химической реакции, называется тепловым эффектом реакции (Q).
Экзотермическая реакция:
Исходные вещества → продукты реакций + Q кДж
Эндотермическая реакция:
Исходные вещества → продукты реакций - Q кДж
Тепловые эффекты химических реакций нужны для многих технических расчетов. Представьте себя на минуту конструктором мощной ракеты, способной выводить на орбиту космические корабли и другие полезные грузы.
Допустим, вам известна работа (в кДж), которую придется затратить для доставки ракеты с грузом с поверхности Земли до орбиты, известна также работа по преодолению сопротивления воздуха и другие затраты энергии во время полета. Как рассчитать необходимый запас водорода и кислорода, которые (в сжиженном состоянии) используются в этой ракете в качестве топлива и окислителя?
Без помощи теплового эффекта реакции образования воды из водорода и кислорода сделать это затруднительно. Ведь тепловой эффект - это и есть та самая энергия, которая должна вывести ракету на орбиту. В камерах сгорания ракеты эта теплота превращается в кинетическую энергию молекул раскаленного газа (пара), который вырывается из сопел и создает реактивную тягу.
В химической промышленности тепловые эффекты нужны для расчета количества теплоты для нагревания реакторов, в которых идут эндотермические реакции. В энергетике с помощью теплот сгорания топлива рассчитывают выработку тепловой энергии.
Врачи-диетологи используют тепловые эффекты окисления пищевых продуктов в организме для составления правильных рационов питания не только для больных, но и для здоровых людей - спортсменов, работников различных профессий. По традиции для расчетов здесь используют не джоули, а другие энергетические единицы - калории (1 кал = 4,1868 Дж). Энергетическое содержание пищи относят к какой-нибудь массе пищевых продуктов: к 1 г, к 100 г или даже к стандартной упаковке продукта. Например, на этикетке баночки со сгущенным молоком можно прочитать такую надпись: "калорийность 320 ккал/100 г".
Область химии, занимающаяся изучением тепловых эффектов, химических реакций, называется термохимией.
Уравнения химических реакций, в которых указан тепловой эффект, называют термохимическими.
FOR-DLE.ru - Всё для твоего DLE ;)
Привет, я Стас ! Я занимаюсь так называемой "вёрсткой" шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и "статейки" для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 2 Объясните причину сохранения массы веществ при химических реакциях.
В результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка. Так как число атомов до реакции и после неё остаётся неизменным, то их общая масса тоже не изменяется.
Задание 3 Почему выделение или поглощение теплоты относится к общим признакам химических реакций?
Выделение или поглощение теплоты обусловлено тем, что энергия затрачивается на процесс разрушения одних веществ (разрушение связей между атомами и молекулами) и выделяется при образовании других веществ (образование связей между атомами и молекулами), а химическая реакция - это явление, при котором разрушаются соединения и структуры реагентов и образуются новые соединения продуктов реакции.
Задание 4 При горении дров, на первый взгляд, закон сохранения массы не действует. Опровергните это утверждение.
При горении дров образуются газообразные продукты реакции, которые улетучиваются в атмосферу. Закон сохранения массы веществ в этом случае не нарушается, т. к. газообразные продукты реакции тоже имеют массу.
Задание 5 Какие виды превращения энергии в химических реакциях вам известны?
Тепловая, световая, механическая и электрическая.
Приведите примеры, когда энергетические изменения являются для практики более важными, чем превращения, происходящие с веществами в ходе реакции.
Горение бензина в двигателе внутреннего сгорания. Горение угля в печи. Сгорание природного газа на ТЭЦ. Горение свечи для освещения помещения. Детонация взрывчатых веществ для производства различных взрывных работ. Электролиз воды для получения водорода

С помощью этого видеоурока учащиеся рассмотрят основные признаки химических реакций: образование осадка, выделение газа, изменение цвета, выделение или поглощение теплоты.

В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Признаки химических реакций"
Химические реакции – это превращения одних веществ в другие, которые сопровождаются явлениями, называемыми признаками химических реакций.
Основными признаки химических реакций являются:
· выделение или поглощение теплоты;
· выпадение и растворение осадка.
Рассмотрим каждый из этих признаков.

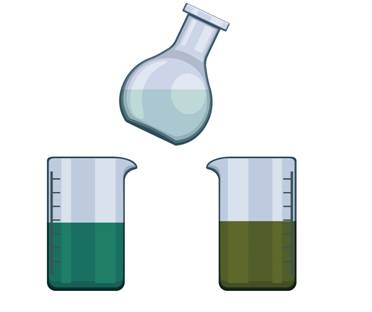
Рассмотрим ещё один опыт, в ходе которого происходит изменение цвета раствора. В одном стакане у нас находится фиолетово-розовый раствор, который представляет собой раствор перманганата калия в щелочной среде, а во втором стакане – оранжевый раствор, который представляет собой подкисленный раствор дихромата калия. Добавляем в каждый стакан бесцветный раствор сульфита натрия. В первом стакане раствор становится зелёного цвета, во втором – также приобретает зелёную окраску.
В стакан с водой добавим несколько кристалликов перманганата калия, а затем сюда же поместим таблетку аскорбиновой кислоты. Перемешаем всё. Раствор становится бесцветным. Во всех этих опытах мы наблюдали изменение цвета.

В газовых зажигалках можно увидеть бесцветную жидкость, которая является смесью двух газов: пропана и бутана. Здесь они в жидком состоянии, потому что находятся под высоким давлением. Если нажать на кнопку зажигалки, послышится характерное шипение – это газы вырываются наружу. Происходит реакция горения пропана и бутана.

Таким образом, переход пропана и бутана в жидкое состояние – это физическое явление, а горение этих газов – химическое. В данном эксперименте мы наблюдали выделение света и тепла – это также признаки химических реакций.
Рассмотрим ещё один признак химической реакции – образование и растворение осадка. В два химических стакана, содержащих бесцветный раствор гидроксида натрия и желтоватый раствор жёлтой кровяной соли, добавим раствор хлорида железа. В первом стакане образуется осадок бурого цвета, а во втором – осадок синего цвета.

Если в первый стакан с бурым осадком добавить соляную кислоту, то осадок начинает растворяться.
Благодаря образованию нерастворимого вещества карбоната кальция в результате химических превращений в пещерах растут сталактиты и сталагмиты. Такие процессы длятся тысячелетиями.

Рассмотрим ещё один признак химической реакции – образование газа. В пробирку с кусочками мрамора добавим соляной кислоты. Происходит бурное выделение пузырьков газа.

Поглощение и выделение тепла выражаются при помощи термохимических уравнений. Тепловой эффект реакции называется энтальпией.
Например, реакция горения углерода, а проще говоря, угля, идет с выделением тепла и является экзотермической:
С + О2 = СО2 + 4О2 кДж.
Значит, при сгорании 1 моля углерода выделяется 402 кДж тепла. Благодаря этой реакции можно всегда рассчитать, сколько тепла выделится при сгорании разного количества углерода.
Реакция окисления азота идет с поглощением тепла и является эндотермической:
N2 + О2 = 2NО -180,8 кДж.

Электростанции, работающие на угле, выделяют в атмосферу продукт его сгорания — углекислый газ, или оксид углерода
Почему выделение или поглощение теплоты относится к общим признакам химической реакции.

Так как при образовании новых веществ или при их разложении поглощается или выделяется тепло.

Верно ли что : 1)Процесс кристаллизации расплава хлорида лития сопровождается в выделении тепла , что является признаком протекания химической реакции?
Верно ли что : 1)Процесс кристаллизации расплава хлорида лития сопровождается в выделении тепла , что является признаком протекания химической реакции.
2)Выделение газа может быть как физическим явлением , так и признаком протекания химического процесса .

Рассчитайте, выделением или поглощением теплоты сопровождается термическое разложение хлорида аммония?
Рассчитайте, выделением или поглощением теплоты сопровождается термическое разложение хлорида аммония?
Пожалуйста, как можно подробнее.

Какие классификации химических реакций вам известны?
Какие классификации химических реакций вам известны?
Какие признаки лежат в их основе?
Привидите примеры реакций выделенных типов и их уравнения.

Реакции, протекающие с поглощением теплоты, называются : а)Термическими б)Эндотермическими в)Экзотермическими?
Реакции, протекающие с поглощением теплоты, называются : а)Термическими б)Эндотермическими в)Экзотермическими.

Процесс горения - это Физическое явление Химическая реакция, идущая с поглащение теплоты Химическая реакция идущая с выделением теплоты Химическая реакция окисления веществ, идущая с выделением теплот?
Процесс горения - это Физическое явление Химическая реакция, идущая с поглащение теплоты Химическая реакция идущая с выделением теплоты Химическая реакция окисления веществ, идущая с выделением теплоты и света.

Признаки химических реакций?
Признаки химических реакций.

Может ли растворение кристалических веществ происходить без выделения или поглощения теплоты?
Может ли растворение кристалических веществ происходить без выделения или поглощения теплоты?

Выделение газа признак химической реакции между : 1) NaOH и HCL 2) CuO и HCL 3) Zn и H2S4O 4) CaO и СO2 почему?
Выделение газа признак химической реакции между : 1) NaOH и HCL 2) CuO и HCL 3) Zn и H2S4O 4) CaO и СO2 почему?

По каким признакам можно однозначно сказать, что мы наблюдаем не физический процесс, а химическую реакцию : А) выделение газа ; Б) выделение энергии ; В) выпадение осадка ; Г) нельзя однозначно сказат?
По каким признакам можно однозначно сказать, что мы наблюдаем не физический процесс, а химическую реакцию : А) выделение газа ; Б) выделение энергии ; В) выпадение осадка ; Г) нельзя однозначно сказать.

Признаком химической реакции не является : а) выделение света б) выпадение осадка в) нагревание г) изменение цвета?
Признаком химической реакции не является : а) выделение света б) выпадение осадка в) нагревание г) изменение цвета.
Читайте также:

