Что такое давление газа чем оно обусловлено в физике кратко
Обновлено: 04.07.2024
Давление в физике представляет собой один из трех ключевых термодинамических макроскопических характеристик для измерения любой газовой системы.
Газ — это одно из четырех, включая плазму, агрегатных состояний материи, характеризующееся очень слабыми связями между составляющими его частицами, а также их большой подвижностью.
В газообразной среде частицы в определенной концентрации расположены не упорядоченно и перемещаются в хаотичном порядке в разных направлениях с одинаковой вероятностью. Подобное строение не позволяет газам сохранять стабильность объема и формы даже при малом внешнем силовом воздействии. Для любого газа, включая одноатомный, значение средней кинетической энергии его частиц в виде атомов и молекул будет превышать энергию межмолекулярного взаимодействия между ними.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Кроме того, расстояние, на которое удалены частицы, значительно превышает их собственные размеры. В том случае, когда молекулярными взаимодействиями и габаритами частиц допускается пренебрегать, газ считают идеальным. Для такой формы материи характерен только один тип внутреннего взаимодействия в виде упругих столкновений. Так как размер частиц пренебрежимо мал по сравнению с расстоянием, на которое они удалены, вероятность столкновений частиц между собой будет низкой.
По этой причине в идеальной газовой среде можно наблюдать лишь столкновения частиц со стенками сосуда. Какой-либо реальный газ с хорошей точностью можно отнести к идеальному, когда их температура выше, чем комнатная, а давление несущественно больше, чем атмосферное.
Причина возникновения давления в газах
Давление газа нельзя объяснить теми же причинами, что и давление твердого тела на опору. Расстояние, на которое удалены молекулы газообразной среды, существенно больше. В результате хаотичного движения они сталкиваются между собой и со стенками сосуда, который они занимают. Давление газа на стенки сосуда и вызвано ударами его молекул.
Данный параметр увеличивается по мере того, как нарастает сила ударов молекул о стенки. Газ характеризуется одинаковым давлением во всех направлениях, которое является следствием хаотичного движения огромного числа молекул.
Важно отметить, что газ оказывает давление на дно и стенки сосуда, объем которого он занимает, во всех направления равномерно. В связи с этим, воздушный шарик сохраняет форму, несмотря на то, что его оболочка достаточно эластична.
Свойства давления газа:
- Если объем уменьшается, то давление газа возрастает, а во время увеличения объема, давление будет снижаться при постоянных величинах массы и температуры вещества.
- Газ, находящийся в закрытом сосуде, характеризуется давлением, которое возрастает по мере увеличения температуры вещества при условии постоянства его массы и объема.
- В том случае, когда масса газа увеличивается, его давление также будет возрастать и наоборот.
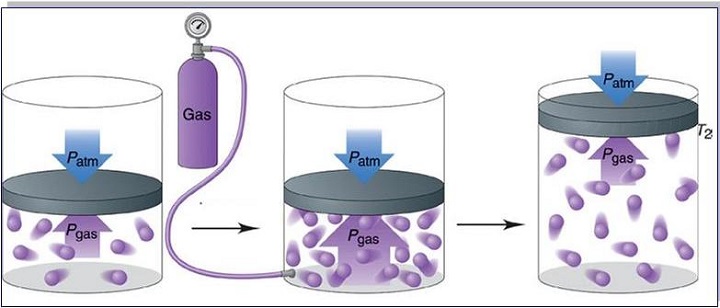
Запись формул для определения давления газа начинают с выяснения причин, по которым оно возникает в рассматриваемой системе. Исходя из физического смысла, давление представляет собой величину, равную отношению силы, перпендикулярно воздействующей на некоторое основание, к площади этого основания:
Как было отмечено ранее, для идеальной газовой системы характерен лишь один тип взаимодействия — это абсолютно упругие столкновения. В процессе частицы передают количество движения Δp стенкам сосуда в течение времени соударения Δt. В данном случае применим второй закон Ньютона:
Таким образом, конкретно сила F является причиной формирования давления на стенки сосуда. Данная величина F, производимая одной частицей, незначительна. Однако, когда количество частиц огромно, они в совокупности создают ощутимый эффект, проявляемый в виде наличия давления в сосуде.
Формула давления идеального газа из молекулярно-кинетической теории
Объяснение концепции идеального газа построено на основных положениях молекулярно-кинетической теории, которая вытекает из принципов статистической механики. Наука получила активное развитие во второй половине XIX, благодаря таким ученым, как Джеймс Максвелл и Людвиг Больцман. Основы дисциплины были заложены еще Бернулли в первой половине XVIII века.
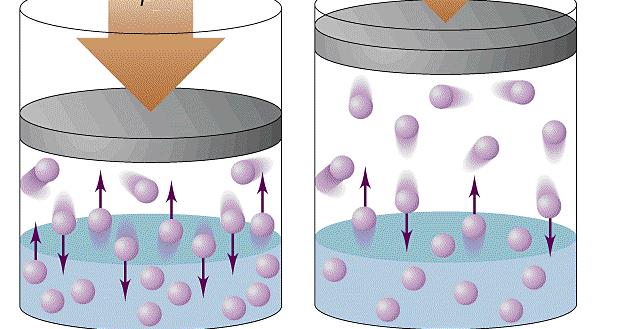
Исходя из статистики Максвелла-Больцмана, все частицы в системе обладают разными скоростями движения. При этом можно наблюдать небольшой процент частиц со скоростями, приближенными к нулю, и малую долю частиц, обладающих огромной скоростью. Средняя квадратичная скорость в этом случае будет соответствовать некоторой величине, не изменяющейся с течением времени.
Средняя квадратичная скорость частиц однозначно характеризует температуру газа. Используя приближения молекулярно-кинетической теории в виде невзаимодействующих безразмерных и хаотично движущихся частиц, получают формулу для расчета давления газа в сосуде:
где N является количеством частиц в системе; V обозначает объем; v представляет собой среднюю квадратичную скорость; m является массой одной частицы.
При наличии указанных в формуле параметров, выраженных в единицах СИ, можно вычислить давление газа в сосуде.
Второй способ записи основного уравнения МКТ
В середине 30-х годов XIX столетия французскому инженеру Эмилю Клапейрону удалось обобщить накопленный до этого времени экспериментальный опыт изучения поведения газов во время разнообразных изопроцессов и получить формулу, которую в будущем назвали универсальным уравнением состояния идеального газа:
n является количеством вещества в молях; T представляет собой температуру по абсолютной шкале и обозначается в кельвинах.
Величина R является универсальной газовой постоянной. Этот термин был введен в уравнение русским химиком Д.И. Менделеевым. Исходя из этого, запись уравнения называют законом Клапейрона-Менделеева.
С помощью данного выражения можно определить формулу для расчета давления газа:
Полученное уравнение объясняет линейный рост давления при увеличении температуры в условиях стабильности объема. Если объем уменьшается с сохранением температуры, то давление увеличивается по гиперболе. Данные закономерности явления отражены в законах Гей-Люссака и Бойля-Мариотта.
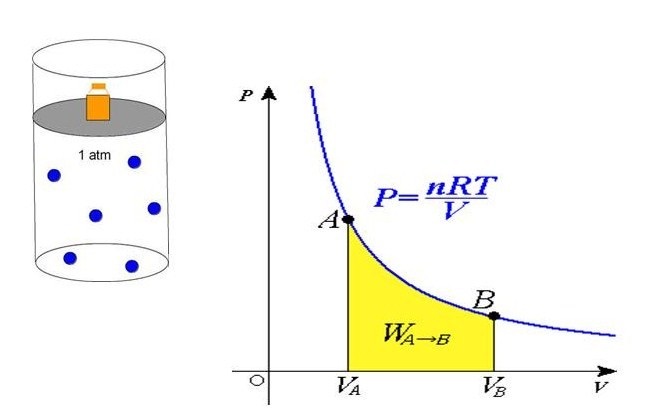
Сравнивая представленное выражение с записью формулы, которая вытекает из положений молекулярно-кинетической теории, можно установить связь кинетической энергии одной частицы, либо системы в общем, и абсолютной температуры.
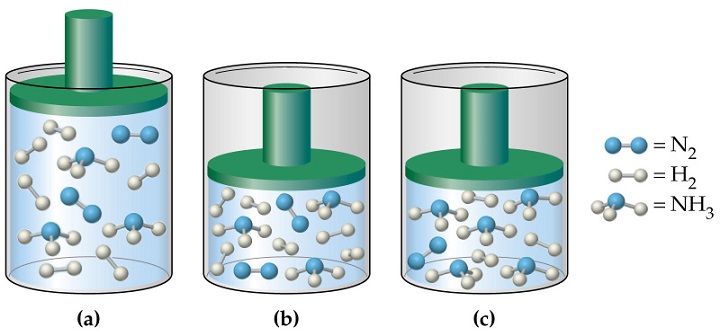
Важно отметить, что при расчетах с использованием формулы для Р, вытекающей из уравнения Клапейрона, связь с химическим составом газа отсутствует. Если давление определяют с помощью выражения, согласно понятию молекулярно-кинетической теории, то данную связь следует учитывать в виде параметра m. В том случае, когда определяют давление смеси идеальных газов, применяют один из следующих методов:
- Расчет средней массы частиц m, либо среднего значения молярной массы М с учетом атомных процентов каждого газа в смеси.
- Применение закона Дальтона, согласно которому давление в системе равно сумме парциальных давлений всех ее компонентов.
Пример
Предположим, что молекулы кислорода движутся со средней скоростью в 500 м/с. Требуется рассчитать, каково давление в сосуде, объем которого равен 10 литров, содержащий 2 моль молекул.
Для того чтобы найти ответ, следует применить формулу для Р из молекулярно-кинетической теории:
Из-за неизвестных параметров m и N требуется выполнить некоторые преобразования формулы:
Таким образом, удельный объем сосуда в кубических метрах равен 0,01. Молярная масса молекулы кислорода М составляет 0,032 кг/моль. Данные параметры можно подставить в уравнение вместе со скоростью и количеством вещества. Тогда Р = 533333 Па, что представляет собой давление в 5,3 атмосферы.
ДАВЛЕНИЕ ГАЗА — сила, с которой давит газ, стремясь к расширению под действием теплового движения его молекул; оно выражается обычно в кгс/см 2 , или в атм (1 атм соответствует давлению 1,03 кгс/см 2 ).
Геологический словарь: в 2-х томах. — М.: Недра . Под редакцией К. Н. Паффенгольца и др. . 1978 .
Смотреть что такое "ДАВЛЕНИЕ ГАЗА" в других словарях:
давление газа — 3.6 давление газа: Избыточное давление движущегося газа относительно атмосферного давления. Источник: ГОСТ Р 52057 2003: Краны для газовых аппаратов. Общие технические требования и методы испытаний … Словарь-справочник терминов нормативно-технической документации
давление газа — dujų slėgis statusas T sritis Standartizacija ir metrologija apibrėžtis Dujų molekulių, atsitrenkiančių į indo sienas, slėgis. atitikmenys: angl. gas pressure vok. Gasdruck, m rus. давление газа, n pranc. pression de gaz, f … Penkiakalbis aiškinamasis metrologijos terminų žodynas
давление газа — dujų slėgis statusas T sritis fizika atitikmenys: angl. gas pressure; gaseous pressure vok. Gasdruck, m rus. давление газа, n pranc. pression de gaz, f … Fizikos terminų žodynas
давление газа — статическое давление движущегося газа относительно атмосферного давления. Единица физической величины килопаскаль (кПа). (Смотри: ГОСТ Р 51733 2001. Котлы газовые центрального отопления, оснащенные атмосферными горелками, номинальной тепловой… … Строительный словарь
Давление газа рабочее — давление газа рабочее: максимально возможное давление газа, установленное проектом, при котором обеспечивается режим эксплуатации газопровода. Источник: Методические рекомендации по определению и обоснованию технологических потерь природного… … Официальная терминология
давление газа р, кПа — 3.1.4 давление газа р, кПа: Статическое давление движущегося газа относительно атмосферного давления. Источник: ГОСТ Р 54439 2011: Котлы газовые для центрального отопл … Словарь-справочник терминов нормативно-технической документации
давление газа, р, мбар — 3.1.10 давление газа, р, мбар: Статическое давление движущегося газа относительно атмосферного давления. Источник … Словарь-справочник терминов нормативно-технической документации
общее давление газа-наполнителя газового ионизационного детектора — общее давление газа наполнителя Сумма парциальных давлений газов внутри газового ионизационного детектора. [ГОСТ 19189 73] Тематики детекторы ионизирующих излучений Синонимы общее давление газа наполнителя EN filling gas total pressure of gas… … Справочник технического переводчика

Из курса физики 7 класса известно, что газ — это состояние вещества, при котором молекулы имеют достаточную скорость и энергию, чтобы преодолевать силы взаимного притяжения и удаляться друг от друга, заполняя весь предоставленный объём. Важнейшей характеристикой газа является давление. Рассмотрим эту тему подробнее, приведём формулу давления газа.
Давление в газах
Как известно из механики, давление — это мера распределения силы по некоторой площади. Она равна отношению величины силы, действующей на тело, к площади, на которой распределено действие.
Молекулы газа, заполняя предоставленный объём сосуда, непрерывно сталкиваются друг с другом и со стенками. Силы соударений отдельных молекул сливаются в одну общую силу. При этом из-за хаотичности движения молекул в любой точке газа есть молекулы, движущиеся во всех направлениях. А значит, эта сила есть в любой точке газа, и действует она также во всех направлениях. Причём, чем большую область мы будем рассматривать, тем больше в ней будет молекул, и тем большая сила будет действовать на границы этой области.
Получается, что в любой точке газа соударения молекул создают некоторую силу, пропорциональную площади, причём отношение этих двух величин постоянно. Это и есть давление газа.
Связь температуры и давления
Итак, давление газа создаётся хаотически движущимися молекулами в результате постоянных соударений. Следовательно, чем больше средняя скорость движения молекул, тем больше будет давление газа. А мера средней скорости молекул — это температура. Значит, если газ содержится в некотором постоянном объёме, то его давление будет пропорционально температуре. Данный закон был установлен в конце XVIII в. Ж. Шарлем и получил его имя.
Закон Шарля гласит, что отношение давления газа к его абсолютной температуре при неизменном объёме остаётся постоянным:
- $p$ — давление газа;
- $T$ — абсолютная температура газа.
Закон Шарля — это один из газовых законов молекулярно-кинетической теории (МКТ), связывающих макроскопические газовые параметры: давление, температуру и объём. Закон Шарля описывает ситуацию, когда объём газа постоянен.

Рис. 2. Газовые законы.
Основное уравнение МКТ
Поскольку давление газа обуславливается хаотическим движением молекул, то его величина может быть определена, исходя из концентрации молекул, массы и средней скорости молекулы:
- $p$ — давление газа;
- $n$ — число молекул в единице объёма (концентрация);
- $m_0$ — масса молекулы;
- $ v_^2$ — среднеквадратичная скорость молекулы.
Данное соотношение называется основным уравнением МКТ. Оно связывает средние параметры одной молекулы с давлением газа. Температура в эту формулу не входит, однако она неявно присутствует в ней в виде среднеквадратичной скорости, которая пропорциональна температуре.

Рис. 3. Молекулярно-кинетическая теория.
Что мы узнали?
Давление газа обуславливается постоянными ударами молекул газа о стенки сосуда и между собой. Давление при постоянном объёме растёт при росте температуры. Величина давления может быть определена с помощью основного уравнения МКТ.
Никому не нравится быть под давлением. И не важно, под каким. Об этом спела еще группа Queen вместе с Дэвидом Боуи в своем знаменитом сингле "Under pressure". Что такое давление? Как понять давление? В чем оно измеряется, какими приборами и методами, куда направлено и на что давит. Ответы на эти и другие вопросы – в нашей статье про давление в физике и не только.
Давление в физике
Если преподаватель давит на вас, задавая каверзные задачки, мы сделаем так, чтобы вы смогли верно на них ответить. Ведь понимание самой сути вещей – ключ к успеху! Итак, что такое давление в физике?
Давление – скалярная физическая величина, равная силе, действующей на единицу площади поверхности.
В международной системе СИ измеряется в Паскалях и обозначается буквой p. Единица измерения давления – 1 Паскаль. Русское обозначение – Па, международное – Pa.
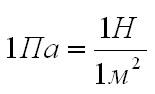
Согласно определению, чтобы найти давление, нужно силу разделить на площадь.
Любая жидкость или газ, помещенный в сосуд, оказывает на стенки сосуда давление. Например, борщ в кастрюле действует на ее дно и стены с некоторым давлением. Формула определения давления жидкости:
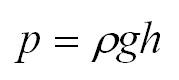
Одно из важнейших свойств жидкостей - изотропность. Это значит, что по закону Паскаля во всех направлениях жидкости производимое ею давление передается одинаково. Кстати, подробнее о жидкостях, их свойствах и движении читайте в нашем материале про уравнение Бернулли.
Наиболее распространенный в быту прибор для определения давления – барометр. Но в чем измеряют давление? Кроме паскаля существуют и другие внесистемные единицы измерения:
- атмосфера;
- миллиметр ртутного столба;
- миллиметр водяного столба;
- метр водяного столба;
- килограмм-сила.
В зависимости от контекста применяются разные внесистемные единицы.
Например, когда вы слушаете или читаете прогноз погоды, там и речи не идет о паскалях. Говорят о миллиметрах ртутного столба. Один миллиметр ртутного столба – это 133 Паскаля. Если вы ездите за рулем, то наверное знаете, что нормальное давление в колесах легкового автомобиля - около двух атмосфер.

Давление в шинах - это давление газа. Оно обусловлено столкновениями молекул воздуха с поверхностью шины
Атмосферное давление
Атмосфера – это газ, точнее, смесь газов, которая удерживается у Земли благодаря гравитации. Атмосфера переходит в межпланетное пространство постепенно, а ее высота – примерно 100 километров.
Нормальное атмосферное давление принято считать равным 101325 Па. Это давление на уровне мирового океана при температуре 0 градусов Цельсия. Такое же давление при этой же температуре оказывает на свое основание столб ртути высотой 766 миллиметров.
Чем больше высота над уровнем моря, тем ниже атмосферное давление. Например, на вершине горы Джомолунгма оно составляет всего одну четвертую от нормального атмосферного давления.

Эверест. На его вершине давление в 4 раза меньше, чем у подножия
Артериальное давление
Еще один пример, где мы сталкиваемся с давлением в повседневной жизни – это измерение кровяного давления.
Артериальное давление – это кровяное давление, т.е. давление, которое кровь оказывает на стенки сосудов, в данном случае – артерий.
Если вы измерили артериальное давление и оно у вас 120 на 80, то все хорошо. Если 90 на 50 или 240 на 180, то вам уже точно будет неинтересно разбираться, в чем это давление измеряется и что это вообще значит.
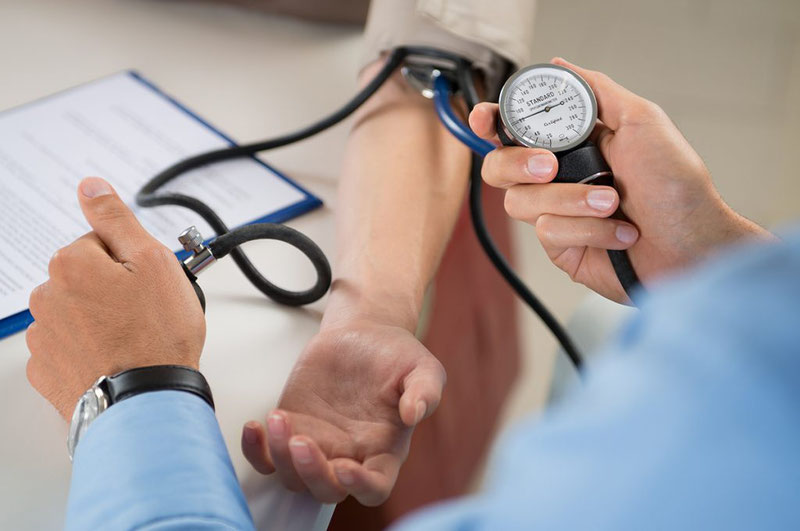
Артериальное давление - давление крови на стенки артерий
Тем не менее, возникает вопрос: 120 на 80 чего именно? Паскалей, миллиметров ртутного столба, атмосфер или еще каких-то единиц измерения?
Артериальное давление измеряется в миллиметрах ртутного столба. Оно определяет превышение давления жидкости в кровеносной системе над атмосферным давлением.
Кровь оказывает давление на сосуды и тем самым компенсирует действие атмосферного давления. Будь иначе, нас бы просто раздавило огромной массой воздуха над нами.
Но почему в измерении артериального давления две цифры?
Кстати! Для наших читателей сейчас действует скидка 10% на любой вид работы
Дело в том, что кровь движется в сосудах не равномерно, а толчками. Первая цифра (120) называется систолическим давлением. Это давление на стенки сосудов в момент сокращения сердечной мышцы, его величина – наибольшая. Вторая цифра (80) определяет наименьшее значение и называется диастолическим давлением.
При измерении фиксируются значения систолического и диастолического давлений. Например, для здорового человека типичное значение артериального давления составляет 120 на 80 миллиметров ртутного столба. Это означает, что систолическое давление равно 120 мм. рт. ст., а диастолическое – 80 мм рт. ст. Разница между систолическим и диастолическим давлениями называется пульсовым давлением.
Физический вакуум
Вакуум – это отсутствие давления. Точнее, практически полное его отсутствие. Абсолютный вакуум является приближением, как идеальный газ в термодинамике и материальная точка в механике.
В зависимости от концентрации вещества различают низкий, средний и высокий вакуум. Наилучшее приближение к физическому вакууму – космическое пространство, в котором концентрация молекул и давление минимальны.

В космосе наблюдается почти полное отсутствие давления
Давление – основной термодинамический параметр состояния системы. Определить давление воздуха или другого газа можно не только по приборам, но и пользуясь уравнениями, формулами и законами термодинамики. А если у вас нет времени разбираться, студенческий сервис поможет решить любую задачу на определение давления.
Читайте также:
- Как ж б ламарк объяснял многообразие видов в природе кратко
- Какие материалы используются для обойных работ кратко
- Для чего нужны развивающие игры в детском саду
- Каким впервые предстает перед гриневым и читателем комендант крепости капитан миронов кратко
- Чем отличается бизнесмен от предпринимателя кратко

