Что называют уравнением химической реакции что показывает химическое уравнение кратко
Обновлено: 08.07.2024
ХИМИЧЕСКОЕ УРАВНЕНИЕ, краткий способ описания химической реакции. Символы, обозначающие вступающие в реакцию вещества, находятся в левой части уравнения, а обозначения продуктов реакции – в правой:
где в скобках указано агрегатное состояние, Q – тепловой эффект реакции. Это уравнение описывает химическую реакцию между натрием и хлором с образованием хлорида натрия (поваренная соль). Натрий – металл, бурно реагирующий с водой, хлор – ядовитый газ, но, соединяясь друг с другом, эти элементы образуют вполне безвредное вещество, необходимое для жизни. Это пример реакций присоединения. Известны также химические реакции замещения, обмена, разложения и пр.; реакции могут быть обратимые, ионные, окислительно-восстановительные, ядерные и др. в зависимости от принципа классификации реакций: по формальному признаку, по механизму реакций, по термодинамическим или кинетическим параметрам и т.д. См. также ПРЕВРАЩЕНИЯ ВЕЩЕСТВ.
Реакции присоединения
Число атомов данного элемента в левой части уравнения равно числу этих атомов в правой части, другими словами, вещество в ходе химической реакции не возникает из ничего и не уничтожается. Химическая реакция, в которой выделяется тепло, например реакция (1), называется экзотермической, а реакция, которая протекает только при подводе тепла извне, например реакция (2), – эндотермической. Почти все химические реакции сопровождаются выделением или поглощением тепла, но в уравнениях это часто не указывают, если только не рассматриваются термодинамические аспекты процесса.
Реакции замещения
В реакции (4) металлический цинк замещает водород в соляной кислоте. В реакции (5) медь замещает серебро в нитрате серебра. В реакции (6) хлор замещает бром в бромиде кальция.
Реакции обмена (двойного замещения) XY + UV → XV + UY
Реакция (7) – типичный пример кислотно-основной реакции (реакции нейтрализации), продуктами которой являются соль и вода. В реакции (8) в результате взаимодействия иона бария Ba 2+ , принадлежащего нитрату бария Ba(NO3)2, c сульфат-ионом серной кислоты образуется осадок сульфата бария BaSO4. В реакциях (7) и (8) реагирующие вещества обмениваются катионами.
Реакции разложения (расщепления)
В реакции (9) синие кристаллы гидратированного сульфата меди разлагаются при нагревании, при этом гидратная вода превращается в пар. Реакция (10) протекает при относительно невысокой температуре в присутствии катализатора – диоксида марганца. Катализатор ускоряет химическую реакцию, оставаясь при этом неизменным (см. также КАТАЛИЗ). Реакция (11) применяется в промышленности: известняк (карбонат кальция CaCO3) при интенсивном нагревании разлагается, образуя негашеную известь (оксид кальция CaO) – важную составную часть цемента.
Обратимые реакции
Стрелки в прямом и обратном направлениях указывают, что продукты реакции взаимодействуют с образованием исходных реагентов, другими словами, реакция идет в обоих направлениях. Систему, в которой протекает обратимая реакция, можно уподобить двум водоемам, соединенным узкой протокой, в которых обитают два или несколько видов рыб. Рыбы беспрепятственно переплывают из одного водоема в другой, так что в конце концов каждый водоем оказывается заселенным смешанной популяцией постоянного состава. Это и есть состояние равновесия.
Количества исходных веществ и продуктов реакции сильно зависят от давления, температуры и концентрации реагирующих веществ.
Ионные реакции.
Химические уравнения можно записывать с указанием заряда исходных веществ и продуктов реакции (+, –, 0 означают положительный, отрицательный и нулевой электрические заряды соответственно; их помещают вверху справа от символа химического элемента). Члены уравнения в правой и левой его частях, отвечающие группам атомов одинакового состава, несущих одинаковый заряд, можно сокращать, как это принято в алгебраических уравнениях:
Ион серебра Ag + несет один положительный заряд; следовательно, на каждый атом меди, образующий двухзарядный положительный ион, должно приходиться два иона серебра, поскольку суммы зарядов в левой и правой частях уравнений должны быть одинаковы. После сокращения одинаковых членов в обеих частях уравнения получаем уравнение (16), которое выражает химические превращения, произошедшие в реакции. Приведенные выше уравнения – это три разных способа представления одной и той же химической реакции: ее молекулярная форма, полная и сокращенная ионные формы.
Ядерные реакции.
Ядерные реакции можно отнести к химическим лишь весьма условно, поскольку в них элемент превращается в изотоп того же элемента или другой элемент. Иногда какая-то часть вещества в ядерной реакции исчезает, и этот процесс сопровождается высвобождением огромного количества энергии; такие процессы происходят при взрыве атомной бомбы или в ядерном реакторе. Обычно в уравнениях ядерных реакций фигурируют нейтроны ( ), протоны ( ), электроны ( ), a -частицы ( ), g -лучи ( ) и позитроны ( ). Верхний левый индекс обозначает массу частицы, а нижний левый – ее заряд. Приведем уравнения типичных ядерных реакций:
Суммы верхних индексов в левой и правой частях уравнения должны быть одинаковыми; то же самое относится к нижним индексам. Может показаться, что масса вещества в ходе ядерных реакций (17)–(19) не изменяется. В действительности же вследствие взаимодействия элементарных частиц в ядре и изменения их массы покоя у продуктов масса может оказаться чуть меньше, чем у исходных веществ. Именно с исчезновением этого незначительного количества вещества, которое превращается в энергию согласно уравнению Эйнштейна Е = mc 2 , и связана разрушительная сила ядерного взрыва. Протекающая при этом реакция описывается уравнением (19). В уравнении (17) (криптон) испускает нейтрон с образованием изотопа с тем же атомным номером (36), но массой, меньшей на единицу.
Окислительно-восстановительные реакции.
В ходе окислительно-восстановительной реакции меняется заряд элементов (их степень окисления), что и учитывается при написании уравнения. Потеря электрона называется окислением, а приобретение – восстановлением. Число отданных и приобретенных в ходе реакции электронов должно быть одинаковым, и исходя из этого устанавливаются соотношения между всеми участниками реакции. Рассмотрим реакцию
Приведем более сложный пример – окислительно-восстановительную реакцию между медью и концентрированной азотной кислотой:
В ходе этой реакции Сu 0 теряет 2 электрона, превращаясь в ион Сu 2+ , а N 5+ принимает 1 электрон, превращаясь в N 4+ . Чтобы уравнять число отданных электронов с числом приобретенных, вводим коэффициент 2 перед NO2 в правой части, а чтобы число атомов азота при этом осталось прежним, умножаем HNO3 в левой части на 2. Cu(NO3)2 в правой части содержит два иона , степень окисления N в которых равна +5. Чтобы сохранить число ионов в левой части с той же степенью окисления, добавляем в левой части 2 молекулы HNO3. Далее, чтобы уравнять 4H + , содержащихся в молекулах HNO3, записываем в правой части 2H2O. В левой части имеем 3 Ч 4 = 12 ионов кислорода, содержащихся в кислоте. Эти 12 ионов кислорода присутствуют и в правой части: 2 в воде, 4 в NO2 и 6 в нитрате меди Cu(NO3)2. Аналогичным образом можно записывать любые, более сложные уравнения.
Применение.
Химические уравнения используются химиками-технологами при расчете характеристик производственных процессов. Так, с их помощью определяется количество реагентов (сырья), необходимое для получения данного количества продукта. См. также ХИМИЯ.
Когда химические вещества вступают во взаимодействие, химические связи между их атомами разрушаются и образуются новые, уже в других сочетаниях. В результате одни вещества превращаются в другие.
Рассмотрим реакцию горения метана, происходящую в конфорке газовой плиты:
.jpg)
Молекула метана (CH₄) и две молекулы кислорода (2O₂) вступают в реакцию, образуя молекулу углекислого газа (CO₂) и две молекулы воды (2H₂O). Связи между атомами углерода (С) и водорода (H) в метане, а также между атомами кислорода (O) разрываются, и образуются новые связи между атомами углерода и кислорода в молекуле углекислого газа (CO₂) и между атомами водорода и кислорода в молекуле воды (H₂O).
Картинка даёт наглядное представление о том, что произошло в ходе реакции. Но зарисовывать сложные химические процессы такими схемами неудобно. Вместо этого учёные используют уравнения химических реакций.
Химическое уравнение — это условная запись химической реакции с помощью формул и символов.
Их записывают в виде схемы, в которой отражён процесс превращения. В левой части располагаются формулы реагентов — веществ, вступающих в реакцию. Завершается уравнение продуктами реакции — веществом или веществами, которые получились в результате.
Новые вещества образуются потому, что изменяются связи между атомами, но сами атомы не возникают из ниоткуда и не исчезают в никуда. На рисунке видно, что атом углерода из состава метана перешёл в состав углекислого газа, атом водорода — в состав воды, а атомы кислорода распределились между молекулами углекислого газа и воды. Число атомов не изменилось.
Согласно закону сохранения массы, общая масса реагентов всегда равна общей массе продуктов реакции. Именно поэтому запись химической реакции называют уравнением.
Виды химических реакций
Вещества вступают в реакции по-разному, можно выделить четыре наиболее частых варианта:
.jpg)
- Соединение. Два или несколько реагентов образуют один продукт. В реакцию могут вступать как простые вещества, так и сложные. Например, простые вещества водород и кислород взаимодействуют и образуют сложное — воду:
.jpg)
Сложное вещество негашёная известь соединяется с водой, и образуется новое сложное вещество — гашёная известь:
.jpg)
- Разложение. Обратный процесс: одно вещество распадается на несколько более простых. Например, если нагреть известняк, получаются негашёная известь и углекислый газ:

Стрелка вверх означает, что образовался газ. Он улетучивается и больше не участвует в реакции.
- Замещение. В реакции участвуют два вещества — простое и сложное. Если атомы химического элемента в простом веществе более активны, они замещают атомы одного из менее активных химических элементов в составе сложного вещества.
В примере атомы цинка замещают атомы водорода в составе хлороводорода, и образуется хлорид цинка:

- Обмен. Два сложных вещества обмениваются составными частями, в результате получаются два новых сложных вещества. В такой реакции обязательно образуется вода, газ или осадок.
.jpg)
Стрелка вниз означает, что вещество выпало в осадок, поскольку оно нерастворимо.
Коэффициенты в уравнениях химических реакций
Чтобы составить уравнение химической реакции, важно правильно подобрать коэффициенты перед формулами веществ.
Коэффициент в химических уравнениях означает число молекул (формульных единиц) вещества, необходимое для реакции. Он обозначается числом перед формулой (например, 2NaCl в последнем примере).
Коэффициент не следует путать с индексом (числом под символом химического элемента, например, О₂). Индекс обозначает количество атомов этого элемента в молекуле (формульной единице).
.jpg)
Чтобы узнать общее число атомов элемента в формуле, нужно умножить его индекс на коэффициент вещества. В примере на картинке (2H₂O) — четыре атома водорода и два кислорода.
Подобрать коэффициент — значит определить, сколько молекул данного вещества должно участвовать в реакции, чтобы она произошла. Далее мы расскажем, как это сделать.
Алгоритм составления уравнений химических реакций
Для начала составим схему химической реакции. Например, образование оксида магния (MgO) в процессе горения магния (Mg) в кислороде (O₂). Обозначим реагенты и продукт реакции:
.jpg)
Чтобы схема стала уравнением, нужно расставить коэффициенты. В левой части схемы два атома кислорода, а в правой — один. Уравняем их, увеличив число молекул продукта:
.jpg)
Теперь число атомов кислорода до и после реакции одинаковое, а число атомов магния — нет. Чтобы уравнять их, добавим ещё одну молекулу магния. Когда количество атомов каждого из химических элементов в составе веществ уравнено, вместо стрелки можно ставить равно:
.jpg)
Уравнение химической реакции составлено.
Рассмотрим реакцию разложения. Нитрат калия (KNO₃) разлагается на нитрит калия (KNO₂) и кислород (О₂):
.jpg)
В обеих частях схемы по одному атому калия и азота, а атомов кислорода до реакции 3, а после — 4. Необходимо их уравнять.
Для начала удвоим коэффициент перед реагентом:
.jpg)
Теперь в левой части схемы шесть атомов кислорода, два атома калия и два атома азота. В левой по-прежнему по одному атому калия и азота и четыре атома кислорода. Чтобы уравнять их, в правой части схемы нужно удвоить коэффициент перед нитритом калия.
.jpg)
Снова посчитаем число атомов каждого химического элемента в составе веществ до и после реакции: два атома калия, два атома азота и шесть атомов кислорода. Равенство достигнуто.
Химические уравнения не только позволяют предсказать, что произойдёт при взаимодействии тех или иных веществ, но и помогают рассчитать их количественное соотношение, необходимое для реакции.
Записали!
Скоро с вами свяжется консультант, расскажет об обучении в нашей онлайн-школе.
Проверьте вашу электронную почту — там письмо о том, что стоит сделать перед консультацией.
Записали!
Скоро с вами свяжется консультант, расскажет об обучении в нашей онлайн-школе.
Проверьте вашу электронную почту — там письмо о том, что стоит сделать перед консультацией.
Записали!
Скоро с вами свяжется консультант, расскажет об обучении в нашей онлайн-школе.
Проверьте вашу электронную почту — там письмо о том, что стоит сделать перед консультацией.

У нас вы сможете учиться в удобном темпе, делать упор на любимые предметы и общаться со сверстниками по всему миру.
Условную запись химической реакции посредством химических знаков и формул называют химическим уравнением.
В левой части уравнения пишут формулы веществ, вступающих в реакцию. В правой – продукты этой реакции. В левой и правой частях уравнения должно быть одинаковое число атомов.
Для того чтобы началась реакция, во многих случаях требуется нагревание. Тогда в уравнениях реакций над знаком равенства ставят знак t.
Если в результате реакции выделяется газ, рядом с его формулой ставят стрелку, направленную вверх (↑).
Если вещество выпадает в осадок, то рядом с формулой этого вещества ставят стрелку, направленную вниз (↓).
Различные процессы, происходящие с веществами, сопровождаются разрывом и образованием различных связей. Чтобы представить происходящее в понятном виде используют специальные уравнения. С их помощью можно предсказать, что произойдёт при взаимодействии элементов даже без опытов. Это фактически отражение реакций в доступном виде. Существуют определённые правила, позволяющие решать химические уравнения, которые необходимо знать при изучении химии.
- Основные термины и понятия
- Виды химических реакций
- Окислительно-восстановительный процесс
- Классический алгоритм
- Решение методом полуреакций
- Использование онлайн-расчёта

Основные термины и понятия

Составление уравнений химических реакций невозможно без знания определённых обозначений, показывающих, как проходит реакция. Объединение атомов, имеющих одинаковый ядерный заряд, называют химическим элементом. Ядро атома состоит из протонов и нейтронов. Первые совпадают с числом атомного номера элемента, а значение вторых может варьироваться. Простейшими веществами называют элементы, состоящие из однотипных атомов.
Любой химический элемент описывается с помощью символов, условно обозначающих структуру веществ. Формулы являются неотъемлемой частью языка науки. Именно на их основе составляют уравнения и схемы. По своей сути они отражают количественный и качественный состав элементов. Например, запись HNO3 сообщает, что в соединении содержится одна молекула азотной кислоты, а оно само состоит из водорода, азота и кислорода. При этом в состав одного моля азотной кислоты входит по одному атому водорода и азота и 3 кислорода.
Символика элементов, условное обозначение, представляет собой химический язык. В значке содержится информация о названии, массовом числе и порядковом номере. Международное обозначение принято, согласно периодической таблице Менделеева, разработанной в начале 1870 года.
Взаимодействующие между собой вещества называются реагентами, а образующиеся в процессе реакции — продуктами. Составление и решение химических уравнений фактически сводится к определению результатов реакций, поэтому просто знать формулы веществ мало, нужно ещё уметь подбирать коэффициенты. Располагаются они перед формулой и указывают на количество молекул или атомов, принимающих участие в процессе. С правой стороны от химического вещества ставится индекс, указывающий место элемента в системе.
Записывают уравнения в виде цепочки, в которой указываются все стадии превращения вещества начиная с левой части. Вначале пишут формулы элементов в исходном состоянии, а затем последовательно их преобразование.
Виды химических реакций
Химические явления характеризуются тем, что из двух и более элементов образуются новые вещества. Уравнения описывают эти процессы. Впервые с объяснениями протекания реакций знакомят в восьмом классе средней образовательной школы на уроках неорганической химии. Ученикам демонстрируют опыты, в которых явно наблюдаются различия в протекании реакций.
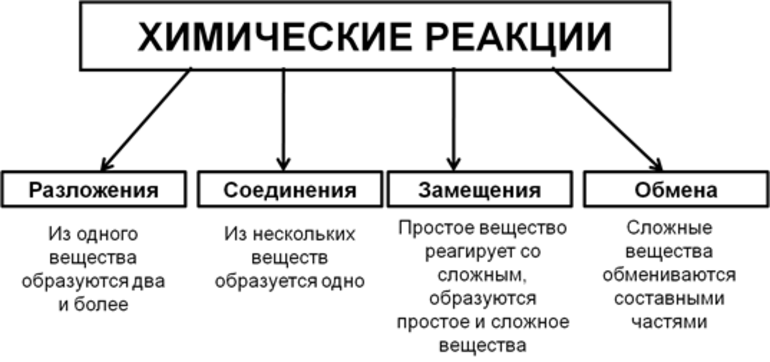
Всего существует 4 типа химического взаимодействия веществ:
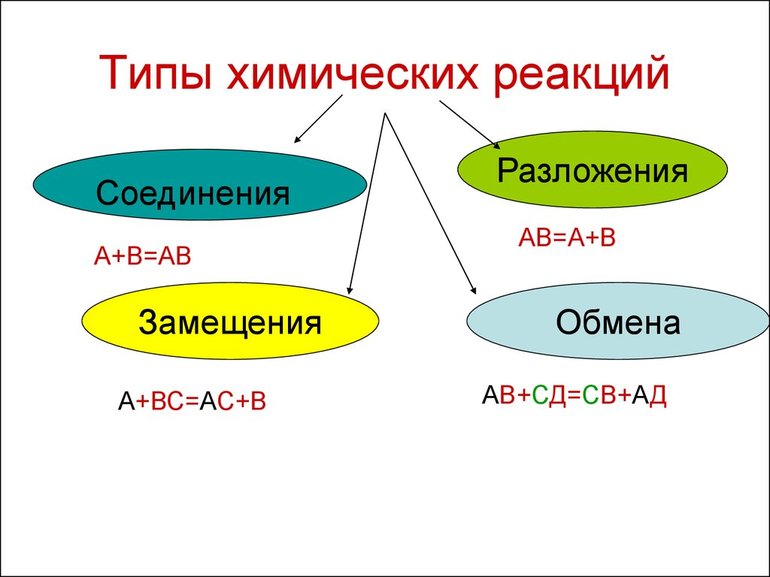
- Соединение. В реакцию могут вступать 2 простых вещества: металл и неметалл или неметалл и неметалл. Например, алюминий с серой образуют сульфид алюминия. Кислород, взаимодействуя с водородом, превращается в воду. Объединятся могут 2 оксида с растворимым основанием, как оксид кальция с водой: CaO + H2O = Ca (OH)2 или основной оксид с кислотным: CaO + SO3 = CaSO4.
- Разложение. Это процесс обратный реакции соединения: было одно вещество, а стало несколько. Например, при пропускании электрического тока через воду получается водород и кислород, а при нагревании известняка 2 оксида: CaCO3 = CaO + CO2.
- Замещение. В реакцию вступают 2 элемента. Один из них простой, а второй сложный. В итоге образуются 2 новых соединения, при котором атом простого вещества заменяет сложный, как бы вытесняя его. Условие протекания процесса: простое вещество должно быть более активным, чем сложное. Например, Zn + 2HCl = ZnCl2 + H2. Величину активности можно узнать из таблицы ряда электрохимических напряжений.
- Обмен. В этом случае между собой реагируют 2 сложных элемента, обменивающиеся своими составными частями. Условием осуществления такого типа реакции является обязательное образование воды, газа или осадка. Например, CuO + 2HCl = CuCl2 + H2O. Чтобы узнать, смогут ли вещества прореагировать, используют таблицу растворимости.
Основными признаками химических реакций является изменение цвета, выделение газа или образование осадка. Различают их по числу веществ, вступивших в реакцию и образовавшихся продуктов. Правильное определение типа реакции особо важно при составлении химических уравнений, а также определения свойств и возможностей веществ.
Окислительно-восстановительный процесс

Составление большинства реакций сводится к подбору коэффициентов. Но при этом могут возникнуть трудности с установлением равновесия, согласно закону сохранения массы веществ. Чаще всего такая ситуация возникает при решении заданий, связанных с расстановкой количества атомов в уравнениях окислительно-восстановительных процессов.
Под ними принято понимать превращения, протекающие с изменением степени окисления элементов. При окислении происходит процесс передачи атомом электронов, сопровождающийся приобретением им положительного заряда или ионом, после чего он становится нейтральным. При этом также происходит процесс восстановления, связанный с присоединением элементарных частиц атомом.
Для составления уравнений необходимо определить восстановитель, окислитель и число участвующих в реакции электронов. Коэффициенты же подбирают с помощью метода электронно-ионного баланса (полуреакций). Его суть состоит в установлении равенства путём уравнивания количества электронов, отдаваемых одним элементом и принимаемым другим.
Классический алгоритм
В основе решения задач этим методом — закон сохранения массы. Согласно ему, совокупная масса элементов до реакции и после остаётся неизменной. Другими словами, происходит перегруппировка частиц. Если рассматривать решение химического уравнения поэтапно, оно будет состоять из трёх шагов:
- Написания формул элементов, вступающих в реакцию с левой стороны.
- Указания справа формулы образующихся веществ.
- Уравнивания числа атомов с добавлением коэффициентов.
Перед тем как переходить к сложным соединениям, лучше всего потренироваться на простых. Например, нужно составить уравнение, описывающее взаимодействие двух сложных веществ: гидроксида натрия и серной кислоты. При таком соединении образуется сульфат натрия и вода.
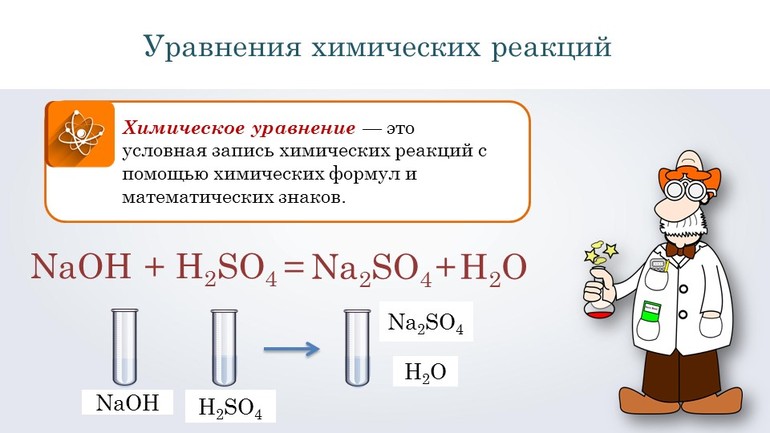
Согласно алгоритму, в левой части уравнения необходимо записать реагенты, а в правой продукты реакции: NaOH + H2SO 4 → Na 2SO4 + H2O. Теперь следует уравнять коэффициенты. Начинают с первого элемента. В примере это натрий. В правой части содержится 2 его атома, а в левой один, поэтому необходимо возле реагента поставить цифру 2. Затем нужно уровнять водород. В результате получится выражение: 2 NaOH + H2SO 4 → Na2 SO4 +2H2O.
Ещё одним наглядным примером является процесс реакции тринитротолуола с кислородом. При их взаимодействии образуется: C7H5N3O6 + O2 → CO2 + H2O + N2. Исходя из того, что слева находится нечётное число атомов H и N, а справа чётное, нужно их уравнять: 2C7H5N3O6 + O2 → CO2 + H2O + N2.
Теперь становится понятным, что 14 и 10 атомов углерода и водорода должны образовать 14 долей диоксида и 5 молекул воды. При этом 6 атомов азота превратятся в 3. Итоговое уравнение будет выглядеть как 2C7H5N3O6 + 10,5O2 → 14CO2 + 5H2O + 3N2.
Перед тем как начинать тренировку по составлению уравнений, следует научиться расставлять валентность. Это параметр, равный числу соединившихся атомов каждого элемента. Фактически это способность к соединению. Например, в формуле NH3 валентность атома азота равна 3, а водорода 1.
Решение методом полуреакций
Алгоритм для решения примеров химических уравнений проще рассмотреть на конкретном задании. Пускай необходимо описать процесс окисления пирита азотной кислоты с малой концентрацией: FeS2 + HNO3. Решать этот пример необходимо в следующей последовательности:
- Определить продукты реакции. Так как кислота является сильным окислителем, сера получит максимальную степень оксидации S6+, а железо Fe3+. HNO3 может восстановиться до одного из двух состояний NO2 или NO.
- Исходя из состава ионов и правила, что вещества, переходящие в газовую форму или плохо растворимые, записываются в молекулярном виде, верным будет записать: FeS2 — Fe3+ + 2SO2−4. Гидролизом можно пренебречь.
- В записи уравнивают кислород. Для этого в левую часть добавляют 8 молекул воды, а в правую 16 ионов водорода: FeS2 + 8H20 — Fe3+ + 2SO2−4 + 16H+. Так как заряда в левой части нет, а в правой он равный +15, то серное железо должно будет отдать 15 электронов. Значит, уравнение примет вид: FeS2 + 8H20 — 15e → Fe3+ + 2SO2−4 + 16H+.
- Теперь переходят к реакции восстановления нитрата иона: NO-3 →NO. Для её составления нужно отнять у оксида азота 2 атома кислорода. Делают это путём прибавления к левой части 4 ионов водорода, а правой — 2 молекул воды. В итоге получится: NO-3 + 4H+ → NO + 2H2O.
- Полученную формулу уравнивают добавлением к левой части 3 электронов: NO-3 + 4H+ 3e → NO + 2H2O.
- Объединяют найденные выражения и записывают результат: FeS2 + 8H20 + 5NO-3 + 20H+ → Fe3+ + 2SO2−4 + 16H+ + 5NO + 10H2O.
Уравнение можно сократить на 16H + и 8H2O. В итоге получится сокращённое выражение окислительно-восстановительной реакции: FeS2 + 5NO - 3 + 4 H + = Fe3 + + 2SO 2- 4 + 5NO + 2H2O.
Такой алгоритм считается классическим, но для упрощения понимания лучше использовать способ электронного баланса. Процесс восстановления переписывают как N5+ + 3e → N2+. Степень же окисления составить сложнее. Сере нужно приписать степень 2+ и учесть, что на 1 атом железа приходится 2 атома серы: FeS2 → Fe3++ 2S6+. Запись общего баланса будет выглядеть: FeS2 + 5N5+ = Fe3+ + 2S6+ + 5N2+.
Пять молекул потратятся на окисление серного железа, а ещё 3 на образование Fe (NO3)3. После уравнения двух сторон запись реакции примет вид, аналогичный полученному с использованием предыдущего метода.
Использование онлайн-расчёта

Простые уравнения решать самостоятельно довольно просто. Но состоящие из сложных веществ могут вызвать трудности даже у опытных химиков. Чтобы получить точную формулу и не подбирать вручную коэффициенты, можно воспользоваться онлайн-калькуляторами. При этом их использовать сможет даже пользователь, не особо разбирающийся в науке.
Чтобы расстановка коэффициентов в химических уравнениях онлайн происходила автоматически, нужно лишь подключение к интернету и исходные данные. Система самостоятельно вычислит продукты реакции и уравняет обе стороны формулы. Интересной особенностью таких сайтов является не только быстрый и правильный расчёт, но и описание правил с алгоритмами, по которому выполняются действия.
Читайте также:
- Школа 148 челябинск педагогический состав
- Почему в конце 17 века османская империя начала постепенно ослабевать кратко
- Как называют в настоящее время болезнь путешественников и что является ее основной причиной кратко
- Роскомнадзор что проверяет в школе
- При каких условиях работа силы положительная отрицательная равна нулю кратко

