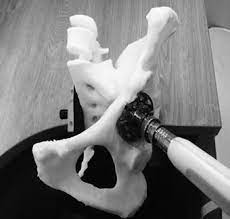
Сообщение моделирование в травматологии и ортопедии
Обновлено: 05.07.2024
Процесс совершенствования методов лечения переломов и других дефектов костей представляет собой важную практическую задачу. Многие методы лечения подразумевают использование различных механических конструкций, в том числе аппаратов внешней фиксации. Применение аппарата внешней фиксации для каждого пациента должно быть спланировано и рассчитано с обеспечением максимальной эффективности лечения, удобства его использования для врача и пациента, а также с учетом экономии времени на его сборку, установку и проведение манипуляций.
Современное производство уже немыслимо без систем автоматизированного проектирования (САПР), представляющих собой автоматизированные системы, реализующие информационную технологию выполнения функций проектирования [1]. Совершенствование методов лечения переломов в значительной мере связано с развитием и применением методов конечноэлементного моделирования для задач травматологии и ортопедии.
Системы автоматизации способны решать проектноконструкторские и расчетные задачи любого уровня. Для моделирования и исследования процессов объемного напряженнодеформированного состояния трехмерных стержневых устройств существует достаточно много специализированных и общеинженерных пакетов конечноэлементного анализа (программных комплексов ANSYS, NASTRAN, COSMOS и др.), которые могут использоваться в комбинации с другими видами физического анализа [2].
Быстрое развитие компьютерной графики обеспечило высококачественную 3Dвизуализацию анатомических структур пациента. Мультиспиральная компьютерная томография (МСКТ) для диагностики заболеваний и повреждений опорнодвигательной системы дает полное представление о количественных изменениях опорных тканей, их анатомотопографических взаимоотношениях, позволяет получать 3D и виртуальные реконструкции [3]. Задачу автоматизированного сопровождения работы хирурга во многих случаях можно рассматривать как техническую задачу и использовать для ее решения эффективные и проверенные методы и технологии компьютерной графики и CAD/CAE/CAMсистем. В настоящее время такой подход реализуется с помощью специальных технологий подготовки хирургического вмешательства. Они называются Computer Aided или Assisted Surgery — CAS технологиями. Разработка этих технологий в странах Запада была начата в середине 1990х годов, и в настоящее время эти методы очень широко используются в западной медицине [4].
Цель внедрения САПР — максимально использовать возможности программного обеспечения при решении прикладных задач. В основе стимула внедрения САПР в травматологию и ортопедию лежит стремление к достижению совершенно определенных целей:
- сокращение сроков подбора оптимальной конструкции аппарата внешней фиксации для решения конкретной задачи лечения;
- повышение качества собираемых компоновок, обеспечивающих максимальную стабильность фиксации и возможности пространственного позиционирования отломков кости;
- унификация компоновок и устройств, возможность создания библиотеки компоновок аппарата, применяемого для конкретной задачи, с отслеживанием эффективности ее использования;
- увеличение эффективности лечения вследствие более продуманной подборки конструкции;
- снижение сроков нахождения больного на лечении, времени подготовки операции, уменьшение количества неудовлетворительных результатов и получение финансовой отдачи от вложенных в САПР средств.
Благодаря внедрению САПР в области травматологии и ортопедии могут быть решены следующие задачи:
- быстрая подборка оптимальной компоновки аппарата внешней фиксации;
- прогнозирование функциональных возможностей аппарата. Оценка последовательности и количества манипуляций с заведомым исключением излишних;
- разработка модифицированных конструкций на базе существующей;
- возможность оценки эффективности лечения выбранной конструкцией;
- унификация и стандартизация компоновок для конкретного вида дефекта;
- накопление базы данных элементов, вариантов компоновок по видам лечения, создание справочноинформационных ресурсов и библиотек с описанием типовых решений, процедур, материалов;
- мобильное планирование изменения компоновки аппарата без привлечения пациента. Упрощение процесса согласования компоновок и своевременного обнаружения ошибок.
Применение CAD/CAM/CAE программного обеспечения для анализа состояния опорнодвигательного аппарата пациентов позволяет после анализа и обмера поврежденной кости или сустава для пациентов спроектировать, собрать или изготовить индивидуальный аппарат, имплантат или протез, точно соответствующий анатомии больного.
Использование САПР дает возможность внедрить прототипирование. Технологии 3Dпечати обеспечивают осуществление наглядного представления предмета, а также быстрое изготовление требуемых наглядных пособий по различным предметным областям. Пример модели, напечатанной на 3Dпринтере, представлен на рис. 1.
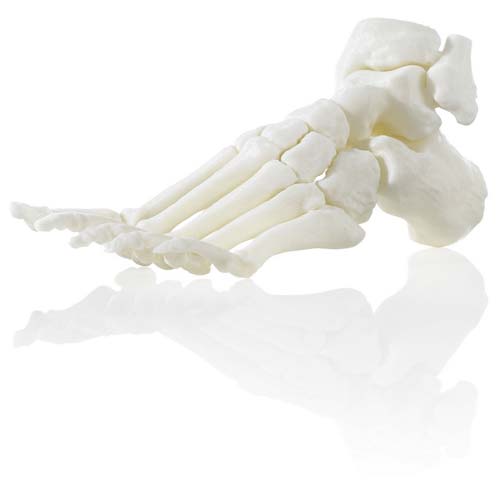
Рис. 1. Модель скелета стопы человека, напечатанная на 3D-принтере
Технологии 3Dпечати в медицине позволяют осуществить моделирование внутренних органов при подготовке к операциям, предварительную проработку имплантируемых частей. Точные размеры и форма дефекта той или иной кости определяются посредством компьютерной томографии. Физические 3Dмодели являются незаменимыми помощниками для улучшения условий обслуживания пациентов и работы врачей [5].
Внедрение 3Dмоделирования и организация коллективной работы в автоматизированной системе — неотъемлемая часть эффективной и разумной организации деятельности крупных клиниконаучных медицинских учреждений в современных условиях.
Рассмотрим несколько примеров использования САПР в травматологии и ортопедии.
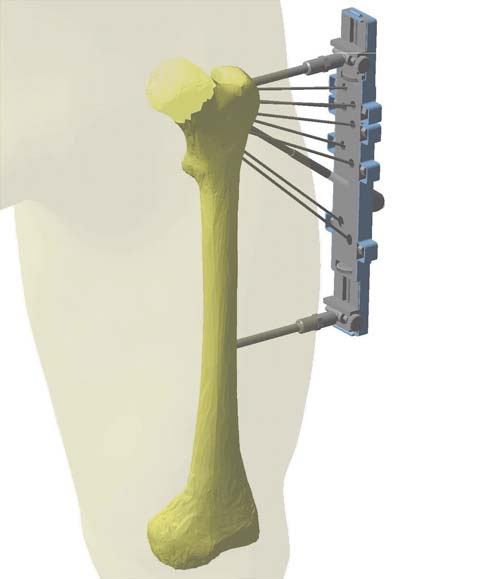
Рис. 2. Моделирование на стадии предоперационного планирования, устройство для лечения переломов проксимального отдела бедренной кости
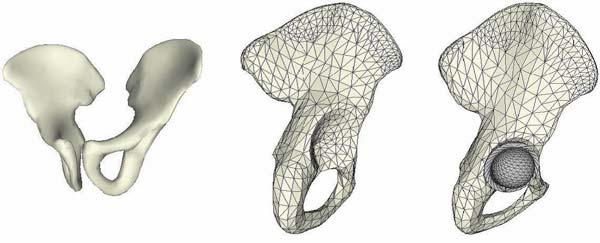
Рис. 3. Трехмерная модель тазовой кости, построенная по данным компьютерной томографии
В РНИИТО им. Р.Р. Вредена построена конечноэлементная модель тазовой кости со встроенной чашкой и головкой и без них (рис. 3). В данной работе с помощью конечноэлементного моделирования проводится анализ прочности крепления эндопротеза при учете дисплазии [6].
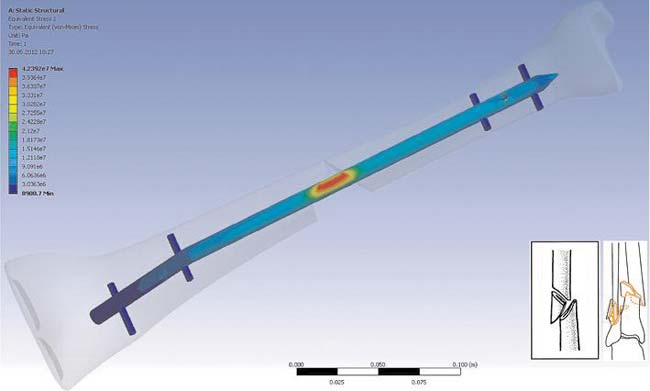
Рис. 5. Напряженное состояние металлоконструкции для перелома типа В2 в условиях утраты репозиционного эффекта (слева дана цветовая шкала величин эквивалентных напряжений по vonMises, Па)
Основная сложность фиксирующих конструкций, проектируемых для травматологии, — разнообразное сочетание геометрических размеров и форм стержней, большой диапазон вектора действующих на конструкцию сил, наличие регулировочных узлов и др. Пространственные конструкции отличает высокая степень сложности. Эти причины являются стимулом для перехода на 3Dпроектирование и анализ.
Теоретические исследования методом конечных элементов позволяют более объективно оценить поведение поврежденной кости и интерполировать полученные данные в клиническую практику при расчете допустимых нагрузок в процессе реабилитации [10].
Алгоритм использования конечноэлементного анализа при планировании операции:
- Изучение данных обследования (полученные из КТсканирования, МикроКТ, МРТ и ультразвука).
- Обработка изображений.
- 3Dреконструкция, создание модели кости (прототип), расположение отломков.
- Моделирование конструкции аппарата (протеза), виртуальное наложение аппарата.
- Построение конечноэлементной сетки.
- Определение сил, контактов, свойств материалов.
- Расчет и при необходимости корректировка конструкции аппарата.
Математика, механика, биология — во взаимодействии этих трех наук многие ученые видят важнейшее средство решения актуальных медицинских задач современности. Внедрение САПР в клиническую практику является неотъемлемой частью прогресса в области медицины травматологии и ортопедии.
Переломы бедренных костей являются одними из самых распространенных среди переломов длинных трубчатых костей. При лечении переломов бедренных костей могут быть применены различные виды остеосинтеза: интрамедуллярный, накостный, чрескостный. В настоящее время широко распространены методики погружного (накостного) остеосинтеза. После проведения остеосинтеза сохраняется значительный процент осложнений, что обуславливает актуальность совершенствования лечения данных видов травм. В статье приводятся результаты использования компьютерного моделирования накостного остеосинтеза для выбора оптимальной металлоконструкции для остеосинтеза переломов у 30 пациентов травматологического стационара. По результатам исследования сделан вывод о снижении количества осложнений, связанных с нестабильностью металлоконструкции после операции, по сравнению с группой сравнения в 3 раза и увеличение хороших результатов лечения на 20 %. Дается оценка целесообразности использования компьютерного моделирования на этапе предоперационного планирования.

3. Марков Д.А., Ямщиков О.Н., Норкин И.А., Афанасьев Д.В. Моделирование остеосинтеза диафизарных переломов бедренной кости. // Вопросы травматологии и ортопедии. – 2012. – № 3. – С. 12–16.
4. Ямщиков О.Н., Киреев С.Н., Марков Д.А., Емельянов С.А. Макет программно-информационного комплекса для травматологии и ортопедии. // Вестник Тамбовского университета. Серия: Естественные и технические науки. – 2011. – № 16(1). – С. 336–338.
5. Ямщиков О.Н., Марков Д.А., Абдулнасыров Р.К., Афанасьев Д.В., Ненашев А.А. Компьютерное моделирование в предоперационном планировании при лечении переломов бедренной кости. // Вестник Тамбовского университета. Серия: Естественные и технические науки. – 2010. – № 15(5). – С. 1508–1510.
Переломы диафизарной части бедренной кости встречаются часто, до 10,4–23,9 % переломов длинных трубчатых костей [2]. Актуальность данного вида травм обусловлена их высокой травматичностью, кровопотерей, высоким риском осложнений как в первые часы после травмы, так и в отдаленном периоде. При лечении переломов бедренных костей могут быть применены различные виды остеосинтеза: интрамедуллярный, накостный, чрескостный. Различные методики погружного остеосинтеза наиболее часто рекомендуются Ассоциацией остеосинтеза [1, 5]. Положительной стороной накостного остеосинтеза является возможность точной репозиции и прочной фиксации отломков костей в сочетании с хорошим анатомическим результатом лечения. Преимуществом интрамедуллярного остеосинтеза является возможность проведения закрытой репозиции и ранняя активизация пациентов. Однако, при неправильном использовании накостных пластин возрастает риск их деформации и перелома, что приводит к необходимости удаления поврежденной металлоконструкции и проведения повторного остеосинтеза. В связи с открытым доступом также сохраняется риск инфекционных осложнений [1, 5]. Применение метода чрескостного остеосинтеза наиболее оправдано при фиксации отломков в остром периоде, когда применение других методов нежелательно, при лечении посттравматических дефектов костей, ложных суставов, несостоятельном остеосинтезе, а также различных врожденных патологиях опорно-двигательной системы [1, 2, 5].
Не прекращаются поиски новых оптимальных методов лечения и усовершенствования имеющихся методик для лечения переломов данной локализации. Вопрос выбора наиболее оптимальной конструкции для лечения переломов диафиза бедренных костей ложится на оперирующего хирурга, который подбирает металлоконструкцию на основании собственного опыта и предпочтений в соответствии с рекомендациями и стандартами лечения данной патологии и оснащенностью лечебного учреждения. В связи с этим могут возникать затруднения во время проведения операции. Неправильный подбор металлоконструкции и недостаточная прочность фиксации отломков кости может приводить к таким осложнениям, как перелом пластин и винтов, вторичное смещение отломков и т.д. Поэтому правильный выбор металлоконструкции при предоперационном планировании остается актуальной задачей [4, 5].
Для выбора металлоконструкции для остеосинтеза с учетом индивидуальных особенностей пациента и перелома разработан программно-информационный комплекс для прогнозирования хирургического лечения травм и их последствий [4]. Созданный программно-информационный комплекс позволяет виртуально произвести остеосинтез данного перелома с применением рекомендуемых металлоконструкций с учетом анатомических особенностей области перелома. По данным компьютерного моделирования операции оценивается качество остеосинтеза, наличие подвижности отломков, распределение нагрузки. Благодаря наличию виртуальной базы данных моделей бедренных костей и остеофиксаторов возможно учитывать индивидуальный характер перелома, а также анатомические особенности пациента [3, 4].
Цель исследования: анализ результатов автоматизированного выбора металлоконструкции на основе компьютерного моделирования для остеосинтеза переломов бедренных костей.
Материалы и методы исследования
Группа сравнения включала 30 пациентов, которым произведен накостный остеосинтез переломов бедренных костей с применением пластин без предоперационного компьютерного моделирования.
Группа пациентов, которым произведены операции после проведения компьютерного моделирования также составила 30 человек.
Пациенты поступали в стационар после острой травмы в сроки от 3 часов до 2 суток с момента перелома. У всех больных диагностированы переломы диафиза бедренной кости. Средний возраст пациентов – 51,6 лет. Обследование и лечение пациентов в до- и послеоперационном периоде проводилось согласно стандартам для данной нозологии.
В целях предоперационного планирования производилась рентгенография поврежденного сегмента в стандартных и, при необходимости, дополнительных проекциях. Во время предоперационного планирования учитывалось наличие или отсутствие остеопороза, пол, возраст, индекс массы тела, сопутствующие заболевания, физическая активность пациента до травмы. Операции выполнялись в операционной на ортопедическом операционном столе под контролем электронного оптического преобразователя. Пациенты активизировались на 2 сутки после операции. С 2–5-го дня обучали ходьбе при помощи костылей, разрешалась ходьба с помощью костылей без нагрузки на оперированную нижнюю конечность. Частичная опора, равная 50 % массы тела пациента, разрешалась спустя 1 месяц после операции в период формирования незрелой костной мозоли. В этот же период производилась контрольная рентгенография. Полная опора через 3 месяца при наличии рентгенологических признаков текущей консолидации. Отдаленные результаты у пациентов наблюдали в сроки от 6 до 24 месяцев. Оценка проводилась по данным контрольных рентгенограмм, выполняемых в 3–6–12–24 месяца после операции, наличию консолидации перелома, болевого синдрома и его интенсивности, возможности самостоятельного передвижения.
Рис. 1. Пример моделирования перелома бедренной кости в соответствии с данными рентгенографии
В обеих группах пациентов в качестве остеофиксаторов были рассмотрены накостные пластины. Выбор металлоконструкции выполнялся согласно общепринятым классификациям и рекомендациям. В первой группе пациентов предоперационного компьютерного моделирования не проводилось.
Для подбора металлоконструкции во второй группе проводили компьютерное моделирование остеосинтеза бедренной кости с использованием программно-информационного комплекса. Для проведения моделирования в каждом случае из антропометрической базы данных программно-информационного комплекса выбиралась модель бедренной кости, наиболее подходящая для данного пациента. Остеофиксаторы выбирали из базы данных металлоконструкций программно-информационного комплекса. Для данной группы пациентов в качестве остеофиксаторов рассматривали накостную пластину, фиксированную винтами.
Рис. 2. Пример модели бедренной кости, соответствующей клиническому случаю с металлоконструкцией
Во время компьютерного моделирования при расчетах напряжений и полей смещений использовали нагрузку силой, соответствующей опоре на конечность в вертикальном положении до 50 % веса тела (нагрузка на конечность в момент активизации больной через 2 месяца после операции) и нагрузке при сгибании в положении сидя без опоры на конечность (вес конечности ниже уровня перелома).
Проанализировав величины напряжений в межотломковом пространстве, делали вывод о состоятельности виртуальной фиксации отломков. В случае если по данным моделирования накостный остеосинтез был несостоятелен, проводилось повторное компьютерное моделирование с другими металлоконструкциями. По данным повторного моделирования выбиралась оптимальная металлоконструкция.
Результаты исследования и их обсуждение
В исследуемой группе в результате компьютерного моделирования в 22 случаях из 30 получены данные, подтверждающие состоятельность остеосинтеза в предложенных условиях с применением пластин. В 8 случаях прочность остеосинтеза оказалась недостаточной, сохранялось значительное смещение отломков в зоне перелома при нагрузках. По данным компьютерного моделирования в группе исследования накостный остеосинтез произведён 22 пациентам, 8 произведён блокируемый интрамедуллярный остеосинтез.
В группе сравнения получены следующие результаты: хорошие – 21 (70 %); удовлетворительные – 9 (30 %).
Осложнения: перелом пластины – 1, миграция пластины с переломом винтов – 2, вторичное смещение отломков – 2, замедленная консолидация перелома – 3.
Рис. 3. Пример визуализации результатов расчета модели соответствующих параметру эквивалентное напряжение Мизеса
У 20 прооперированных пациентов сроки активизации соответствовали планируемым.
В группе исследования получены следующие результаты: хорошие – 27 (90 %); удовлетворительные – 3 (10 %).
Осложнения: перелом пластины – 0, миграция пластины с переломом винтов – 1, миграция винтов – 1, замедленная консолидация перелома – 1.
У 26 прооперированных пациентов сроки активизации соответствовали планируемым.
Таким образом, при применении метода компьютерного моделирования в группе исследования из 30 пациентов получены хорошие результаты лечения в 90 % случаев. Вместе с тем, в группе, где компьютерное моделирование не проводилось хорошие результаты лечения получены в 70 %. Осложнения после остеосинтеза во второй группе пациентов также наблюдались реже в 3 раза.
Выводы
Проведение предоперационного компьютерного моделирования позволило оптимизировать процесс установки металлоконструкции во время операции, улучшить качество лечения и добиться сокращения затрат на лечение благодаря снижению доли осложнений и связанных с ними повторных госпитализаций, операций, превышения сроков реабилитации и восстановления трудоспособности.
Таким образом, для улучшения качества лечения переломов диафиза бедренной кости методом накостного остеосинтеза можно рекомендовать проведение предоперационного компьютерного моделирования.
Для чего применяют предоперационное 3D-моделирование в ортопедии?
Как проводят 3D-моделирование при переломах и эндопротезировании суставов?
10-15 лет назад печать протезов на 3D принтере казалась чем-то фантастическим. Сейчас эту технологию активно применяют в ведущих клиниках мира. Изготовление металлоконструкций для остеосинтеза (лечение переломов), замещения участков кости и суставов позволяет тысячам пациентов сохранить подвижность и качество жизни.
Еще больше повысить эффективность операции и снизить риски можно благодаря предоперационному 3D-моделированию. КТ и МРТ-снимки пациента обрабатывают с помощью специальной программы – она создает объемную модель, работая с которой хирург планирует операцию. После этого при необходимости фрагменты распечатывают на 3D-принтере для более детального изучения модели. Это позволяет повысить точность и эффективность операции, сокращая время ее проведения и реабилитационный период.
Что такое предоперационное 3D-моделирование?
Предоперационное 3D-моделирование – это относительная новая технология, сфера применения которой быстро расширяется. Вначале ее активно использовали в челюстно-лицевой хирургии, где важна максимальная точность манипуляций и прогнозируемый результат. Последние годы ее интегрировали в стоматологию, пластическую хирургию, ортопедию и другие оперативные направления.
Суть 3D-моделирования заключается в том, что врач получает объемную модель, с которой может работать как в виртуальном пространстве, так и в реальности - распечатав на 3D-принтере.
В компьютерной программе специалист может:
рассмотреть фрагменты кости с разных сторон;
при переломе сопоставить обломки кости или сустава;
примерить протез и подобрать наилучший;
спроектировать индивидуальный трансплантат или конструкцию для остеосинтеза;
спланировать операцию, выбрать наименее травматичный доступ, учитывая расположение сосудов, мышц и связок.
Так хирург получает возможность подобрать наилучшее решение проблемы и прогнозировать результат с максимальной точностью. В ходе операции ему не нужно тратить время на подбор деталей. Также пациент получает индивидуально подобранный трансплантат или протез, что снижает риск осложнений.
Преимущества предоперационного 3D-моделирования

Предварительное 3D-моделирование имеет много преимущества. Во время исследований было установлено, что благодаря такой подготовке:
сокращается длина разреза минимум на 1-1,5 см;
сокращается время операции на 20-30%;
увеличивается точность установки протезов и металлоконструкций на 15%;
восстановление подвижности конечностей происходит быстрее на 40-50%.
При каких операциях используют 3D-моделирование?
В ортопедии и травматологии предоперационное 3D-моделирование применяют при:
травмах и болезнях суставов;
ревизионном протезировании (замене искусственного сустава);
Специалисты "Оксфорд Медикал" рассказывают, что такая подготовка имеет особое значение при сложных переломах, когда повреждены несколько костей, они имеют неровные края, присутствуют множественные осколки и т.д. В первую очередь это касается травм ключицы, таза, бедра, плеча, запястья или суставов – при внутрисуставных переломах 3D-планирование сильно упрощает качественное проведение операции.
Также программа позволяет примерить металлоконструкцию для правильного сращения кости и суставный протез при эндопротезировании. С ее помощью проектируют индивидуальные модели протезов.
При опухолях хирург может в виртуальном пространстве удалить ее, оценить состояние кости и мягких тканей после и при необходимости подобрать трансплантат.
Для чего применяют предоперационное 3D-моделирование в ортопедии?
3D-моделирование перед операцией позволяет:
точно определить положение фрагментов кости, пострадавшей в результате перелома, размеры и форму обломков;
в виртуальном пространстве восстановить ее целостность, подобрать или разработать необходимые детали для фиксации;
определить необходимость использования трансплантата вместо части кости, чтобы восстановить ее форму;
подобрать наиболее подходящий протез для замены сустава и ревизионного эндопротезирования;
при опухолях смоделировать удаление и разработать методику восстановления костной и мягких тканей;
визуализировать расположение сосудов, чтобы минимизировать риск повреждения во время операции;
в программе спланировать все этапы операции, снизить риск осложнений и время ее проведения.
Как проводят 3D-моделирование при переломах и эндопротезировании суставов?![3D-моделирование операции в ортопедии в Оксфорд Медикал]()
Для проведения предоперационного 3Д-моделирования используют снимки компьютерной и магнитно-резонансной томографии (МРТ). Во время исследования происходит сканирование пораженной области при помощи рентгеновского (КТ) или электромагнитного (МРТ) излучения. Компьютерная программа обрабатывает снимки и формирует объемную модель, которую можно поворачивать во всех направлениях и соединять с другими деталями, например, суставным протезом.
В некоторых случаях модели костей и суставов распечатывают на 3D-принтере. В результате получается изделие, идентичное по форме и размеру кости пациента. Так врач и пациент могут визуализировать и обсудить предстоящую операцию.
Обычно, такая подготовка занимает всего несколько дней.
3D-моделирование требует наличия специального компьютерного обеспечения и умения хирурга работать с ним, а потому, пока, доступно далеко не во всех клиниках.

В данной статье придется больше внимания уделять технологическим, чем медицинским аспектам. Но так уж действует цепная реакция научно-технического прогресса: прорыв в одной области знания зачастую приводит к настоящим революциям во многих других, подчас очень далеких отраслях.
В самом деле, что общего между передним краем компьютерной графики, – трехмерным моделированием и 3D-печатью, – и столь специфическим разделом стоматологической науки, как зубопротезирование? Между тем, связь есть. Более того: сегодня этот вектор является одним из наиболее перспективных, – наряду с прямой заменой разрушенных и удаленных зубов новыми, выращенными из имплантированных зубных зачатков. Но речь ниже пойдет именно о протезировании, т.е. о замещении утраченных органов искусственными.
2. История методов
Мы говорим о двух методах, медицинском и техническом, хотя их истории совершенно несопоставимы по продолжительности и темпам. Согласно археологическим находкам, попытки заполнять промежутки в зубных дугах предпринимались еще две с половиной тысячи лет назад, а скорее всего, и ранее. С этой целью в различных регионах земного шара использовались панцири мидий, кости животных, зубы других людей, и пр. Одним из пионеров современной ортопедической стоматологии как отрасли медицины стал французский придворный врач Пьер Фошар, разработавший ряд приспособлений и методологических приемов, не утративших актуальность по сей день. Однако в повседневную медицинскую практику зубопротезирование, долгое время остававшееся очень проблематичной и дорогой техникой, стало входить лишь в ХIХ-ХХ вв. На сегодняшний день широко распространены различные конструкции съемных и стационарных (мостообразных, штифтовых и др.) протезов, а также титановых имплантатов, которые обнаружили достаточную биоинертность и приемлемо низкий процент отторжений.
В медицине математическое 3D-моделирование нашло воплощение, прежде всего, в различных томографических технологиях диагностики (КТ, МСКТ, МРТ, 3D-УЗ-сканеры), однако оказалось востребованным также в пластической хирургии, травматологии, ортопедии, – в частности, в ортопедической стоматологии.
3. Преимущества
4. Недостатки
Метод виртуального 3D-моделирования в ортопедической стоматологии развивается быстро, и возможности его далеко еще не исчерпаны. Однако два главных недостатка пока не преодолены: очень высокая стоимость оборудования (на уровне полумиллиона долларов) и монополия производителей на данные сканирования (прочитать их и построить модель возможно, как правило, только в авторизованных производителем лабораториях). Впрочем, ситуация все же меняется к лучшему: некоторые поставщики стоматологических 3D-сканеров и принтеров сегодня отказываются от абсолютного права собственности на получаемые цифровые промеры, а по мере отработки и оптимизации производственных технологий стоимость создания ортопедических 3D-моделей из пластика будет снижаться.
Заболевания ![частые заболевания]()
Жалобы и симптомы ![Жалобы и симптомы]()
- Патологии костей
- Травмы и паталогии суставов
- Проблемы со связками и сухожилиями
- Травмы мягких тканей
Если вы обнаружили у себя подобные симптомы, возможно, это сигнал заболевания, поэтому рекомендуем проконсультироваться с нашим специалистом.
Диагностика ![Диагностика]()
Наши цены ![Типичные жалобы]()
- Консультация врача травматолога-ортопеда от 3000 рублей
Мы стараемся оперативно обновлять данные по ценам, но, во избежание недоразумений, просьба уточнять цены в клинике.
Данный прайс-лист не является офертой. Медицинские услуги предоставляются на основании договора.
Читайте также: