Полиморфизм химия сообщение 11 класс
Обновлено: 02.07.2024
В металловедении под полиморфизмом понимают любые изменения в кристаллографической форме решётки материала. Поэтому аллотропическое или полиморфное превращение играет важную роль в свойствах и использовании металлов, склонных к подобным изменениям.
Суть явления
Полиморфные превращения происходят в ответ на изменения внешних факторов – температуры, давления, либо того и другого вместе.
Так, например, происходит с углеродом, который встречается в двух различных полиморфных формах- графита с гексагональной структурой и алмаза - с изометрической. Вещество FeS2 чаще всего встречается в виде пирита с изометрической структурой, но оно также может иметь ромбическое внутреннее расположение, и тогда его называют марказитом. Существуют и другие примеры.
Свойства вещества определяются не только его химическим составом, но и геометрией составляющих атомов и ионов, а также природой связывающих их электрических сил.
Большинство минералов представляют собой соединения, состоящие из двух или более элементов; их формулы получены на основе количественного химического анализа и указывают относительные пропорции составляющих элементов. Поэтому наблюдаются значительные вариации в ионах, которые занимают определенные атомные позиции в их структуре. Например, содержание железа в родохрозите (MnCO3) может варьироваться в широких пределах, поскольку двухвалентное железо (Fe 2+ ) замещает катионы марганца (Mn 2+ ) в структуре родохрозита.
Поэтому формула данного минерала может быть дана в более общих терминах, а именно (Mn, Fe) CO3. Она показывает, что, хотя количество марганца и железа меняется, но отношение катиона к отрицательно заряженной анионной группе остается фиксированным: один атом Mn 2+ или Fe 2+ к одной группе CO3. Такое изменение является результатом замены одного иона или ионной группы другим в конкретной структуре. Это явление называется ионным замещением или твердым раствором. Возможны три типа твердого раствора:
- замещающий;
- промежуточный;
- упущенный.
Замещающий твердый раствор является наиболее распространенной разновидностью: пример с родохрозитом это подтверждает. Однако на степень замещения могут влиять и другие факторы, наиболее важным из которых является размер иона. Ионы двух разных элементов могут свободно заменять друг друга, только если их ионные радиусы различаются примерно на 15 процентов или меньше.
На аллотропические превращения влияет также температура, соответствующая началу роста кристаллов. Чем выше температура, чем более обширен термический беспорядок в кристаллической структуре и тем менее требовательны требования к пространству. В результате ионное замещение, которое не могло произойти в кристаллах, выращенных при низких температурах, может присутствовать в кристаллах, выращенных при более высоких температурах. Так, высокотемпературная форма KAlSi3O8 (санидин) может содержать больше натрия вместо калия, чем низкотемпературные аналоги данного минерала.
Дополнительным фактором, влияющим на ионное замещение, является поддержание баланса между положительными и отрицательными зарядами в структуре. Замена одновалентного иона (например, Na + ) двухвалентным ионом (например, Ca 2+ ) требует дополнительных замен, чтобы структура оставалась электрически нейтральной.
Условия для полиморфного превращения
Стабильность химических связей атомов и ионов металлов определяют электрические силы. Физические и химические свойства минералов по большей части объясняются типами этих связывающих сил, среди которых:
- твёрдость:
- температура начала плавления;
- электропроводность;
- теплопроводность;
- коэффициент теплового расширения.
Твёрдость и температура плавления кристалла увеличиваются (а коэффициент теплового расширения уменьшается) пропорционально прочности такой связи. Чем сильнее электрические связи, тем большее количество тепла потребуется для их разделения.
Электрические силы, называемые химическими связями, можно разделить на пять типов:
- ионные;
- ковалентные;
- металлические;
- ван-дер-ваальсовы;
- водородные.
Такая классификация в значительной степени обусловлена целесообразностью, поскольку химические связи в данном металле могут фактически обладать характеристиками более чем одного типа связи.
Ионные связи проявляются в тенденции атомов металлов приобретать или терять электроны, пока их внешние орбитали не станут стабильными; Обычно это достигается за счет заполнения этих орбиталей максимально допустимым числом валентных электронов.
Кристаллы с ионной связью обычно обладают умеренной твёрдостью и удельным весом, довольно высокими температурами плавления и плохой теплопроводностью и электропроводностью.
Ковалентные связи образуются только между резко полярными веществами, которых среди металлов практически не встречается. В отличие от солей, металлы обладают высокой пластичностью, прочностью, пластичностью и проводимостью. Многие из них характеризуются более низкой твёрдостью и более высокими температурами плавления и кипения, чем, например, материалы с ковалентной связью. Все эти свойства являются результатом металлического механизма связи, который можно представить как набор положительно заряженных ионов, погруженных в облако валентных электронов. Притяжение между катионами и электронами удерживает кристалл вместе.
Электроны не связаны с каким-либо конкретным катионом и, таким образом, могут свободно перемещаться по структуре. У некоторых металлов (натрий, цезий, рубидий и калий) лучистая энергия света может вызвать полное удаление электронов с их поверхностей Этот результат известен как фотоэлектрический эффект. Подвижность электронов отвечает за способность металлов проводить тепло и электричество.
Самородные металлы - единственные минералы, демонстрирующие чистую металлическую связь.
Связи Ван-дер-Ваальса и водородные связи характерны для газов, органических жидкостей и некоторых твёрдых тел, поэтому здесь не рассматриваются.
Механизм превращения
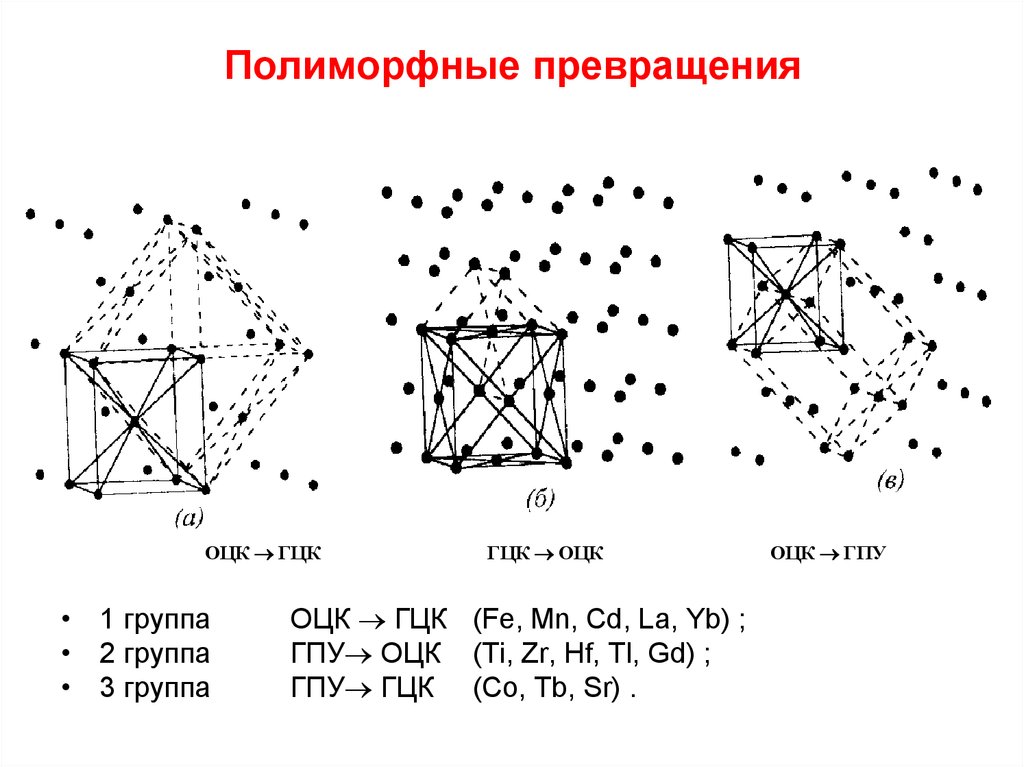
Наибольшей интенсивностью полиморфных превращений обладают самородные металлы, которые объединяются в три группы:
- Группа золота, состоящая из золота, серебра, меди и свинца;
- Платиновая группа, состоящая из платины, палладия, иридия и осмия;
- Группа железа, содержащая железо и никель.
Гораздо слабее полиморфизм выявляется у ртути, тантала, олова и цинка.
Золото, серебро и медь являются членами одной группы (столбца) периодической таблицы элементов и, следовательно, имеют схожие химические свойства. В некомбинированном состоянии их атомы соединены довольно слабой металлической связью. поэтому атомы расположены в простом кубическом расположении с плотной упаковкой. И золото, и серебро имеют атомный радиус 1,44 × 10 –7 мм, что позволяет твёрдому раствору полностью образовываться между ними. Радиус меди значительно меньше (1,28 Å), и поэтому медь только в ограниченной степени заменяет золото и серебро. Из-за схожей кристаллической структуры металлы группы золота обладают схожими физическими свойствами, поэтому хорошо кристаллизуются в изометрической системе и имеют высокую плотность упаковки.
Аналогичен механизм аллотропного превращения у металлов платиновой группы..
Металлы группы железа изометричны и имеют простую кубическую упакованную структуру, чем объясняется лёгкость происходящих полиморфных превращений.
Почему полиморфное превращение также называют перекристаллизацией?
Полиморфизм - это способность вещества кристаллизоваться в различные кристаллические формы, которые называются кристаллическими модификациями. Полиморфы имеют одинаковое жидкое или газообразное состояние, но в твёрдом состоянии ведут себя по-разному.
Для всех металлов, испытывающих аллотропические превращения, кристаллические структуры подвижны и могут видоизменяться в нескольких разных пропорциях.
Некоторые полиморфные формы могут быть стабильными только в том случае, когда при кристаллизации присутствует небольшое количество растворителя.
Таким образом, перекристаллизация – процесс перестройки одной кристаллической решётки в другую – обязательно сопровождается и определёнными полиморфными превращениями.
(от греч. polymorphos-многообразный), способность твердых в-в и жидких кристаллов существовать в двух или неск. формах с разл. кристаллич. структурой и св-вами при одном и том же хим. составе. Такие формы наз. полиморфными модификациями. Взаимные превращения полиморфных модификаций наз. полиморфными переходами. П. простых в-в принято называть аллотропией, но понятие П. не относят к некристаллич. аллотропным формам (таким, как газообразные О 2 и О 3 ). П. широко распространен в самых разнообразных классах в-в. Типичный пример полиморфных форм - модификации углерода: алмаз и лонсдейлит, в к-рых атомы объединены ковалентными связями в пространств. каркас; графит, в структуре к-рого имеются слои наиб. прочно связанных атомов; карбин, построенный из бесконечных линейных цепочек. Эти модификации резко различаются по св-вам. В случае молекулярных кристаллов (в частности, орг. в-в) П. проявляется в разл. упаковке молекул, имеющих одинаковую структурную ф-лу; здесь переход от одной модификации к другой осуществляется без разрыва ковалентных связей, но конформация молекул может существенно меняться (конформационный П.).
Известны также полиморфные модификации, отличающиеся степенью упорядоченности. Напр., в кристаллич. структуре высокотемпературной формы бензотиофена (существующей выше -11 °С) молекулы статистически ориентированы четырьмя разл. способами, в то время как в структуре низкотемпературной формы все молекулы ориентированы одним определенным образом. Особый вид П. связан со своб. вращением молекул или атомных группировок. Так, в кристаллах NH 4 NO 3 при 84°С происходит полиморфный переход, обусловленный возникновением вращения ионов вокруг оси третьего порядка; в интервале от 125°С до т-ры плавления ионы и вращаются вокруг центров масс, эффективно приобретая сферич. форму.
Частный случай П.- политипизм (политипия). Политип-ные модификации представляют собой разл. варианты наложения одинаковых двухмерных структурных фрагментов; при этом два параметра решетки неизменны, а третий меняется, оставаясь кратным постоянной величине. Напр., для SiC известно более 40 политипных модификаций (политипов). Политипия наблюдается также у ZnS, CdI 2 , глинистых минералов и др.
С точки зрения термодинамики, полиморфные модификации обычно являются фазами, причем различают два типа П. Если каждая из двух модификаций устойчива в определенном интервале т-р и давлений, эти фазы наз. энантио-тропными. В принципе одна энантиотропная фаза должна переходить в другую при вполне определенных условиях, и переход должен осуществляться в любом направлении. Однако энантиотропные превращения м. б. настолько кинетически заторможены, что метастабильная модификация существует неограниченно долго. Напр., алмаз и мн. др. минералы метастабильны при атм. давлении и комнатной т-ре. Вместе с тем, нек-рые полиморфные переходы протекают настолько быстро, что можно визуально наблюдать растрескивание кристалла или движение границы раздела фаз.
Если одна из двух модификаций термодинамически неустойчива при всех т-рах ниже точки плавления, эти две модификации наз. монотропными (напр., модификации пропилбензола). В этом случае осуществим только односторонний переход метастабильной модификации в стабильную. Метастабильную фазу можно получить только из переохлажденной жидкости (или пара). При энантиотропии каждой из двух модификаций соответствует определенная область на диаграмме состояния; при монотропии такая область имеется лишь для устойчивой модификации. Интерпретация таких диаграмм состояния осуществляется с помощью кривых зависимости своб. энергии Fот т-ры при постоянном давлении. Поскольку при любой т-ре устойчива фаза с миним. своб. энергией, в случаях, показанных на рис. а и б, модификации I и II соотв. энантиотропны и монотропны (точки пересечения кривых отвечают равновесию модификаций между собой и с жидкой фазой).

Зависимость свободной энергии от т-ры для жидкости и полиморфных модификаций: а - модификации I и II энантиотропны, б-модификаиии I и II монотропны; ж-жидкость.
Полиморфные переходы, согласно принятой в термодинамике классификации, подразделяются на переходы I и II рода. Последние (в отличие от переходов первого рода) не сопровождаются скачкообразным изменением энтропии; теплоемкость в точке такого перехода проходит через высокий и острый максимум. Изменение кристаллич. структуры при переходе второго рода невелико, а в нек-рых случаях практически отсутствует (напр., при переходе a-Fe в b-Fe, происходящем при 769°С, теряются ферромагн. св-ва). Переходами второго рода часто являются переходы типа порядок - беспорядок, переходы с появлением внутр. вращения (напр., в случае NH 4 NO 3 ).
П. открыл М. Клапрот в 1798, он обнаружил, что минералы кальцит и арагонит имеют одинаковый хим. состав-СаСО 3 . Затем это явление было изучено Э. Митчерлихом (1822) на кристаллах арсенатов, фосфатов и серы.
Лит.: Физика и химия твердого состояния органических соединений, пер. с англ., М., 1967; Проблемы физики и химии твердого состояния органических соединений, пер. с англ., М., 1968; Верма А., Рам Кришна П., Полиморфизм и политипизм в кристаллах, пер. с англ., М., 1969; Бок и и Г. Б., Кристаллохимия, 3 изд., М., 1971; Изюмов Ю. А., Сыромятников В. Н., Фазовые переходы и симметрия кристаллов, М., 1984. П. М. Зоркий.
Химическая энциклопедия. — М.: Советская энциклопедия . Под ред. И. Л. Кнунянца . 1988 .

Факты современной науки еще далеко не опровергают мнений и наблюдений философов; напротив, превращение металлов (полиморфизм) возможно; это совершившийся, доказанный факт и в этом не может сомневаться ни один непредубежденный ум.
Установим сначала плодотворный принцип, принятый в настоящее время всеми химиками: свойства тел зависят от их молекулярного состава.
В природе мы встречаем большое число полиформных тел, которые получают весьма различные свойства, смотря по системе, в которой они кристаллизуются, хотя, вместе с тем, состав их не претерпевает никакого изменения. Так, ромбоэдрическая углекислая известь, или известковый шпат, и призматическая углекислая известь, или аррагонит, совершенно одинакового состава, а, между тем, свойства их весьма различны. Наука достигла возможности воспроизводить эти две соли, по желанию, в обеих формах. Одна из этих солей обладает способностью двойного преломления, другая не имеет этого свойства; одна гораздо плотнее другой; одна, наконец, кристаллизуется при обыкновенной температуре, а другая – только при температуре 100 градусов.
Всем известно, что сера обладает различными свойствами, смотря по температуре, которой подвергают ее, и по кристаллической форме, придаваемой ей. Множество металлических окислов, каковы, например, некоторые окислы железа и хрома, замещая в солях другие основания, придают им и другие свойства и притом в весьма типичных формах. Окислы цинка, ртути, многие соединения этих металлов изменяют свои свойства под влиянием изменения молекулярного состава, произведенного теплотой или электрическими силами. Губчатая платина, глина, накаленная добела, производят, вследствие простого погружения их в смесь кислорода и водорода, соединение этих двух газов, т.е. образуют воду.
Не встречаемся ли мы ежедневно с подобными же явлениями и в органическом мире? Не преобразуется ли крахмал в сахар от одного соприкосновения с серной кислотой, так что эта последняя нисколько не изменяется в своем составе? Не присутствию ли азотистого вещества обязано своим происхождением явление брожения, явление, которое производит в органических веществах столь любопытные преобразования? Наконец, синерод, этот сложный радикал, не есть ли продукт действия щелочного основания на азотистое вещество? Я бы мог привести в подтверждение вышеупомянутого принципа тысячи других примеров, если бы только не боялся упрека в хвастовстве знаниями. Поэтому я просто повторю еще раз, что нет ничего вернее той мысли, что конституция тела, изменяясь, приобретает новые свойства, продолжая сохранять свою непосредственную природе, или, если хотите, свой состав.
Следовательно, достаточно открыть такое тело, которое своей каталитической силой могло бы подействовать на преобразуемое тело, а тогда для преобразования сего последнего останется только привести его в некоторые условия соприкосновения с первым.
Многие кристаллические вещества имеют одинаковые структуры. В то же время одно и то же вещество может образовывать разные кристаллические структуры. Это находит отражение в явлениях изоморфизма и полиморфизма.
Изоморфизм заключается в способности атомов, ионов или молекул замещать друг друга в кристаллических структурах. Этот термин (от греческих "изос" - равный и "морфе" - форма) был предложен Э. Мичерлихом в 1819 г. Закон изоморфизма бы сформулирован Э. Мичерлихом в 1821 г. таким образом: "Одинаковые количества атомов, соединенные одинаковым способом, дают одинаковые кристаллические формы; при этом кристаллическая форма не зависит от химической природы атомов, а определяется только их числом и относительным положением".
Изоморфизм широко распространен в природе. Большинство минералов представляет собой изоморфные смеси сложного переменного состава. Например, в минерале сфалерите ZnS до 20% атомов цинка могут быть замещены атомами железа (при этом ZnS и FeS имеют разные кристаллические структуры). С изоморфизмом связано геохимическое поведение редких и рассеянных элементов, их распространение в горных породах и рудах, где они содержатся в виде изоморфных примесей.
Изоморфное замещение определяет многие полезные свойства искусственных материалов современной техники - полупроводников, ферромагнетиков, лазерных материалов.
Многие вещества могут образовывать кристаллические формы, имеющие различные структуру и свойства, но одинаковый состав (полиморфные модификации). Полиморфизм - способность твердых веществ и жидких кристаллов существовать в двух или нескольких формах с различной кристаллической структурой и свойствами при одном и том же химическом составе. Это слово происходит от греческого "полиморфос" - многообразный. Явление полиморфизма было открыто М.Клапротом, который в 1798 г. обнаружил, что два разных минерала - кальцит и арагонит - имеют одинаковый химический состав СаСО3.
Полиморфизм простых веществ обычно называют аллотропией, в то же время понятие полиморфизма не относится к некристаллическим аллотропным формам (например, газообразным О2 и О3). Типичный пример полиморфных форм - модификации углерода (алмаз, лонсдейлит, графит, карбины и фуллерены), которые резко различаются по свойствам. Наиболее стабильной формой существования углерода является графит, однако и другие его модификации при обычных условиях могут сохраняться сколь угодно долго. При высоких температурах они переходят в графит. В случае алмаза это происходит при нагревании выше 1000 °С в отсутствие кислорода. Обратный переход осуществить гораздо труднее. Необходима не только высокая температура (1200-1600 °С), но и гигантское давление - до 100 тысяч атмосфер. Превращение графита в алмаз проходит легче в присутствии расплавленных металлов (железа, кобальта, хрома и других).
В случае молекулярных кристаллов полиморфизм проявляется в различной упаковке молекул в кристалле или в изменении формы молекул, а в ионных кристаллах - в различном взаимном расположении катионов и анионов. Некоторые простые и сложные вещества имеют более двух полиморфных модификаций. Например, диоксид кремния имеет десять модификаций, фторид кальция - шесть, нитрат аммония - четыре. Полиморфные модификации принято обозначать греческими буквами α, β, γ, δ, ε. начиная с модификаций, устойчивых при низких температурах.
При кристаллизации из пара, раствора или расплава вещества, имеющего несколько полиморфных модификаций, сначала образуется модификация, менее устойчивая в данных условиях, которая затем превращается в более устойчивую. Например, при конденсации пара фосфора образуется белый фосфор, который в обычных условиях медленно, а при нагревании быстрее превращается в красный фосфор. При обезвоживании гидроксида свинца вначале (около 70 °С) образуется менее устойчивый при низких температурах желтый β-PbO, около 100 °С он превращается в красный α-PbO, а при 540 °С - снова в β-PbO.
Переход одной полиморфной модификации в другую называется полиморфными превращениями. Эти переходы происходят при изменении температуры или давления и сопровождаются скачкообразным изменением свойств.

Процесс перехода одной модификации в другую может быть обратимым или необратимым. Так, при нагревании белого мягкого графитоподобного вещества состава BN (нитрид бора) при 1500-1800 °С и давлении в несколько десятков атмосфер образуется его высокотемпературная модификация - боразон, по твердости близкий к алмазу. При понижении температуры и давления до значений, отвечающих обычным условиям, боразон сохраняет свою структуру. Примером обратимого перехода может служить взаимные превращения двух модификаций серы (ромбической и моноклинной) при 95 °С.
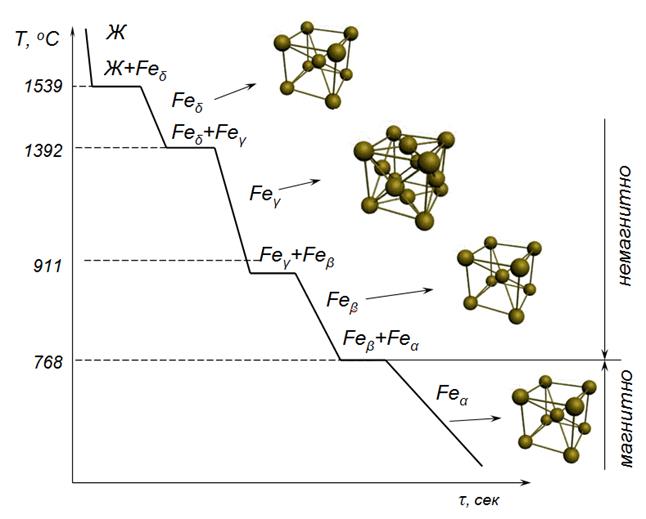
Полиморфные превращения могут проходить и без существенного изменения структуры. Иногда изменение кристаллической структуры вообще отсутствует, например, при переходе α-Fe в β-Fe при 769 °С структура железа не меняется, однако исчезают его ферромагнитные свойства.
Вопрос 8. Уравнение Бернулли. Измерение расхода и скорости.
Многие кристаллические вещества имеют одинаковые структуры. В то же время одно и то же вещество может образовывать разные кристаллические структуры. Это находит отражение в явлениях изоморфизма и полиморфизма.
Изоморфизм заключается в способности атомов, ионов или молекул замещать друг друга в кристаллических структурах. Этот термин (от греческих "изос" - равный и "морфе" - форма) был предложен Э. Мичерлихом в 1819 г. Закон изоморфизма бы сформулирован Э. Мичерлихом в 1821 г. таким образом: "Одинаковые количества атомов, соединенные одинаковым способом, дают одинаковые кристаллические формы; при этом кристаллическая форма не зависит от химической природы атомов, а определяется только их числом и относительным положением".
Изоморфизм широко распространен в природе. Большинство минералов представляет собой изоморфные смеси сложного переменного состава. Например, в минерале сфалерите ZnS до 20% атомов цинка могут быть замещены атомами железа (при этом ZnS и FeS имеют разные кристаллические структуры). С изоморфизмом связано геохимическое поведение редких и рассеянных элементов, их распространение в горных породах и рудах, где они содержатся в виде изоморфных примесей.
Изоморфное замещение определяет многие полезные свойства искусственных материалов современной техники - полупроводников, ферромагнетиков, лазерных материалов.
Многие вещества могут образовывать кристаллические формы, имеющие различные структуру и свойства, но одинаковый состав (полиморфные модификации). Полиморфизм - способность твердых веществ и жидких кристаллов существовать в двух или нескольких формах с различной кристаллической структурой и свойствами при одном и том же химическом составе. Это слово происходит от греческого "полиморфос" - многообразный. Явление полиморфизма было открыто М.Клапротом, который в 1798 г. обнаружил, что два разных минерала - кальцит и арагонит - имеют одинаковый химический состав СаСО3.
Полиморфизм простых веществ обычно называют аллотропией, в то же время понятие полиморфизма не относится к некристаллическим аллотропным формам (например, газообразным О2 и О3). Типичный пример полиморфных форм - модификации углерода (алмаз, лонсдейлит, графит, карбины и фуллерены), которые резко различаются по свойствам. Наиболее стабильной формой существования углерода является графит, однако и другие его модификации при обычных условиях могут сохраняться сколь угодно долго. При высоких температурах они переходят в графит. В случае алмаза это происходит при нагревании выше 1000 °С в отсутствие кислорода. Обратный переход осуществить гораздо труднее. Необходима не только высокая температура (1200-1600 °С), но и гигантское давление - до 100 тысяч атмосфер. Превращение графита в алмаз проходит легче в присутствии расплавленных металлов (железа, кобальта, хрома и других).
В случае молекулярных кристаллов полиморфизм проявляется в различной упаковке молекул в кристалле или в изменении формы молекул, а в ионных кристаллах - в различном взаимном расположении катионов и анионов. Некоторые простые и сложные вещества имеют более двух полиморфных модификаций. Например, диоксид кремния имеет десять модификаций, фторид кальция - шесть, нитрат аммония - четыре. Полиморфные модификации принято обозначать греческими буквами α, β, γ, δ, ε. начиная с модификаций, устойчивых при низких температурах.
При кристаллизации из пара, раствора или расплава вещества, имеющего несколько полиморфных модификаций, сначала образуется модификация, менее устойчивая в данных условиях, которая затем превращается в более устойчивую. Например, при конденсации пара фосфора образуется белый фосфор, который в обычных условиях медленно, а при нагревании быстрее превращается в красный фосфор. При обезвоживании гидроксида свинца вначале (около 70 °С) образуется менее устойчивый при низких температурах желтый β-PbO, около 100 °С он превращается в красный α-PbO, а при 540 °С - снова в β-PbO.
Переход одной полиморфной модификации в другую называется полиморфными превращениями. Эти переходы происходят при изменении температуры или давления и сопровождаются скачкообразным изменением свойств.
Процесс перехода одной модификации в другую может быть обратимым или необратимым. Так, при нагревании белого мягкого графитоподобного вещества состава BN (нитрид бора) при 1500-1800 °С и давлении в несколько десятков атмосфер образуется его высокотемпературная модификация - боразон, по твердости близкий к алмазу. При понижении температуры и давления до значений, отвечающих обычным условиям, боразон сохраняет свою структуру. Примером обратимого перехода может служить взаимные превращения двух модификаций серы (ромбической и моноклинной) при 95 °С.
Полиморфные превращения могут проходить и без существенного изменения структуры. Иногда изменение кристаллической структуры вообще отсутствует, например, при переходе α-Fe в β-Fe при 769 °С структура железа не меняется, однако исчезают его ферромагнитные свойства.
Вопрос 8. Уравнение Бернулли. Измерение расхода и скорости.
Читайте также:

