Полезные ископаемые титан сообщение 4 класс
Обновлено: 07.07.2024
Титан (лат. Titanium) - химический элемент IV группы периодической системы Менделеева, 4 периода, имеет номер 22. Атом Титана содержит 22 электрона на 7 оболочках вокруг ядра с зарядом +22. Атомная масса приблизительно равна 48.
Титан - легкий серебристо-белый металл, по внешнему виду похож на сталь. Обладает низкой теплопроводностью, которая в 13 раз меньше теплопроводности алюминия и в 4 раза - железа. Титан относится к переходным элементам. Данный металл плавится при довольно высокой температуре (1668°С) и кипит при 3300 °С. Его плотность сравнительно мала (4500 кг/м3). Стоит также отметить, что его механическая прочность примерно вдвое больше, чем чистого железа, и почти в шесть раз выше прочности алюминия.
Титан в виде двуокиси был открыт английским любителем-минералогом У. Грегором в 1791 в магнитных железистых песках местечка Менакан (Англия). Грегор растворил пробу найденного черного песка, смешанного с тонким грязно-белым песком, в соляной кислоте; при этом из песка выделилось 46% железа. Оставшуюся часть пробы Грегор растворил в серной кислоте, причем почти все вещество перешло в раствор, за исключением 3,5% кремнезема. После упаривания сернокислотного раствора остался белый порошок в количестве 46% пробы. Продолжая исследования порошка, Грегор пришел к выводу, что он представляет собой соединение железа с каким-то неизвестным металлом.
В 1795 немецкий химик М. Г. Клапрот установил, что минерал рутил представляет собой природный окисел этого же металла, названного им "титаном". Выделить титан в чистом виде долго не удавалось, лишь в 1910 американский учёный М.А. Хантер получил металлический титан нагреванием его хлорида с натрием в герметичной стальной бомбе; полученный им металл был пластичен только при повышенных температурах и хрупок при комнатной из-за высокого содержания примесей.
Свойства титана во многом зависят от степени его чистоты, поэтому разработка способов массового производства особо чистого титана является одной из важнейших проблем промышленности. Дело в том, что союз титана с кислородом (а именно в виде такого соединения элемент обычно и встречается в природе) является одним из самых прочных в химии. Ни электрический ток, ни высокие температуры не в силах вырвать титан из объятий кислорода.
Применяемый в промышленности технический титан содержит примеси кислорода, азота, железа, кремния и углерода, повышающие его прочность, снижающие пластичность и влияющие на температуру полиморфного превращения, которое происходит в интервале 865-920 °C.
Титан - один из распространённых элементов, среднее содержание его в земной коре составляет 0,57% по массе. Титан постоянно присутствует в тканях растений, накапливается у позвоночных животных, преимущественно в роговых образованиях, селезёнке, надпочечниках, щитовидной железе, плаценте; плохо всасывается из желудочно-кишечного тракта. У человека суточное поступление титана с продуктами питания и водой составляет 0,85 мг, выводится с мочой и калом (0,33 и 0,52 мг соответственно). Этот металл относительно малотоксичен.
Интересно, что тонкая титановая стружка при недостаточной смазке может загораться в процессе механической обработки. А при достаточной концентрации кислорода в окружающей среде и повреждении окисной плёнки путём удара или трения возможно загорание металла при комнатной температуре и в сравнительно крупных кусках.

Титан – лёгкий прочный металл серебристо-белого цвета. Существует в двух кристаллических модификациях: α-Ti с гексагональной плотноупакованной решёткой, β-Ti с кубической объёмно-центрированной упаковкой, температура полиморфного превращения α↔β 883 °C.Титан и титановые сплавы сочетают легкость, прочность, высокую коррозийную стойкость, низкий коэффициент теплового расширения, возможность работы в широком диапазоне температур.
СТРУКТУРА
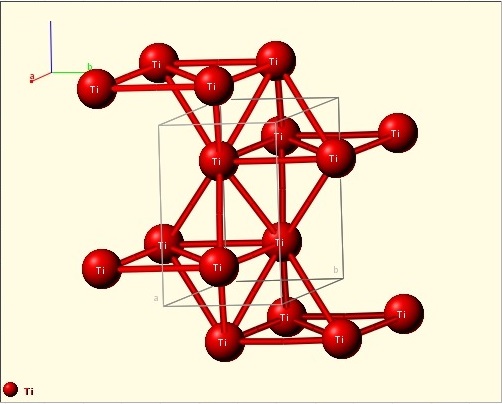
Кристаллическая структура кристалла
Титан имеет две аллотропические модификации. Низкотемпературная модификация, существующая до 882 °C, имеет гексагональную плотноупакованную решетку с периодами а = 0,296 нм и с = 0,472 нм. Высокотемпературная модификация имеет решетку объемноцентрированного куба с периодом а = 0,332 нм.
Полиморфное превращение (882 °C) при медленном охлаждении происходит по нормальному механизму с образованием равноосных зерен, а при быстром охлаждении – по мартенситному механизму с образованием игольчатой структуры.
Титан обладает высокой коррозионной и химической стойкостью благодаря защитной окисной пленке на его поверхности. Он не корродирует в пресной и морской воде, минеральных кислотах, царской водке и др.
СВОЙСТВА

Точка плавления 1671 °C, точка кипения 3260 °C, плотность α-Ti и β-Ti соответственно равна 4,505 (20 °C) и 4,32 (900 °C) г/см³, атомная плотность 5,71×1022 ат/см³. Пластичен, сваривается в инертной атмосфере.
Применяемый в промышленности технический титан содержит примеси кислорода, азота, железа, кремния и углерода, повышающие его прочность, снижающие пластичность и влияющие на температуру полиморфного превращения, которое происходит в интервале 865-920 °С. Для технического Титана марок ВТ1-00 и ВТ1-0 плотность около 4,32 г/см 3 , предел прочности 300-550 Мн/м 2 (30-55кгс/мм 2 ), относительное удлинение не ниже 25%, твердость по Бринеллю 1150-1650 Мн/м 2 (115-165 кгс/мм 2 ). Является парамагнетиком. Конфигурация внешней электронной оболочки атома Ti 3d24s2.
Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок.
При обычной температуре покрывается защитной пассивирующей пленкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной). Титановая пыль имеет свойство взрываться. Температура вспышки 400 °C.
ЗАПАСЫ И ДОБЫЧА

Основные руды: ильменит (FeTiO3), рутил (TiO2), титанит (CaTiSiO5).
На 2002 год, 90 % добываемого титана использовалось на производство диоксида титана TiO2. Мировое производство диоксида титана составляло 4,5 млн т. в год. Подтвержденные запасы диоксида титана (без России) составляют около 800 млн т. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т., а рутиловых — 49.7—52.7 млн т. Таким образом, при нынешних темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет.
Россия обладает вторыми в мире, после Китая, запасами титана. Минерально-сырьевую базу титана России составляют 20 месторождений (из них 11 коренных и 9 россыпных), достаточно равномерно рассредоточенных по территории страны. Самое крупное из разведанных месторождений находится в 25 км от города Ухта (Республика Коми). Запасы месторождения оцениваются в 2 миллиарда тонн.
Концентрат титановых руд подвергают сернокислотной или пирометаллургической переработке. Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана их при 850 °C восстанавливают магнием.
ПРОИСХОЖДЕНИЕ

Титан находится на 10-м месте по распространённости в природе. Содержание в земной коре — 0,57 % по массе, в морской воде — 0,001 мг/л. В ультраосновных породах 300 г/т, в основных — 9 кг/т, в кислых 2,3 кг/т, в глинах и сланцах 4,5 кг/т. В земной коре титан почти всегда четырёхвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках.
Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. До 30 % TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит CaTiSiO5. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые.
Месторождения титана находятся на территории ЮАР, России, Украины, Китая, Японии, Австралии, Индии, Цейлона, Бразилии, Южной Кореи, Казахстана. В странах СНГ ведущее место по разведанным запасам титановых руд занимает РФ (58.5%) и Украина (40.2%).
ПРИМЕНЕНИЕ

Изделия из титана
Титановые сплавы играют большую роль в авиационной технике, где стремятся получить наиболее легкую конструкцию в сочетании с необходимой прочностью. Титан легок по сравнению с другими металлами, но в то же время может работать при высоких температурах. Из титановых сплавов изготовляют обшивку, детали крепления, силовой набор, детали шасси, различные агрегаты. Также данные материалы применяются в конструкциях авиационных реактивных двигателей. Это позволяет уменьшить их массу на 10-25%. Из титановых сплавов производят диски и лопатки компрессора, детали воздухозаборника и направляющего аппарата, крепеж.
Также титан и его сплавы используют в ракетостроении. Ввиду кратковременной работы двигателей и быстрого прохождения плотных слоев атмосферы в ракетостроении в значительной мере снимаются проблемы усталостной прочности, статической выносливости и отчасти ползучести.
Технический титан из-за недостаточно высокой теплопрочности не пригоден для применения в авиации, но благодаря исключительно высокому сопротивлению коррозии в ряде случаев незаменим в химической промышленности и судостроении. Так его применяют при изготовлении компрессоров и насосов для перекачки таких агрессивных сред, как серная и соляная кислота и их соли, трубопроводов, запорной арматуры, автоклав, различного рода емкостей, фильтров и т.п. Только титан обладает коррозионной стойкостью в таких средах, как влажный хлор, водные и кислые растворы хлора, поэтому из данного металла изготовляют оборудование для хлорной промышленности. Из титана делают теплообменники, работающие в коррозионно активных средах, например в азотной кислоте (не дымящей). В судостроении титан используется для изготовления гребных винтов, обшивки морских судов, подводных лодок, торпед и т.д. На титан и его сплавы не налипают ракушки, которые резко повышают сопротивление судна при его движении.
Титановые сплавы перспективны для использования во многих других применениях, но их распространение в технике сдерживается высокой стоимостью и дефицитностью титана.
Титан (Ti) один из металлов периодической системы Дмитрия Ивановича Менделеева. Нашел широкое применение в промышленности, благодаря свои свойствам. В дальнейшем был адаптирован под бытовые потребности, как вещество, обеспечивающее длительный срок службы изделий.
История открытия
Явление нового элемента связано с именами Грегора и Клапрота. Оба выделили его практически одновременно 1791 и 1795 гг. соответственно.

Мартин Генрих Клапрот
В 1805 г. был выделен вновь Вокленом из анатаза. При этом чистый титан был получен в Голландии более чем через век после выделения.
Происхождение названия
Свое наименование получил вследствие сравнения с титанами в древнегреческой мифологии М. Клапротом. При этом исследователь не был знаком в полной мере со свойствами элемента, на тот момент они практически не известны.
При этом представители французской школы пытались найти название, соответствующее характеристикам металла. Однако Мартин остановился на мифологии (как было ранее с ураном).
Нахождение в природе
В природе титан представлен в виде соединений с кислородом. Чистые формы не встречаются.

Под влиянием метеорологических условий по строению приближается к корунду (соединению алюминия с кислородом). Его обнаруживают в морской глине, в алюминиевых рудах с железом и кремнием.
Титан представлен в минералах: титанит, титаномагнетит, рутил. Известны австралийские, бразильские, канадские месторождения последнего. Минерал представлен в виде букрита и анатаза.
Широко встречаемым минералом служит титанат железа (ильменит). Крупные месторождения представлены в России, Северной Америке.
Крупные месторождения
Лидирующее место занимает Китай, далее следует Российская Федерация, Северная Америка (Канада). Самое крупное месторождение, где добывают титан в РФ, расположено на территории республики Коми и называется Ярегское нефтяное месторождение.
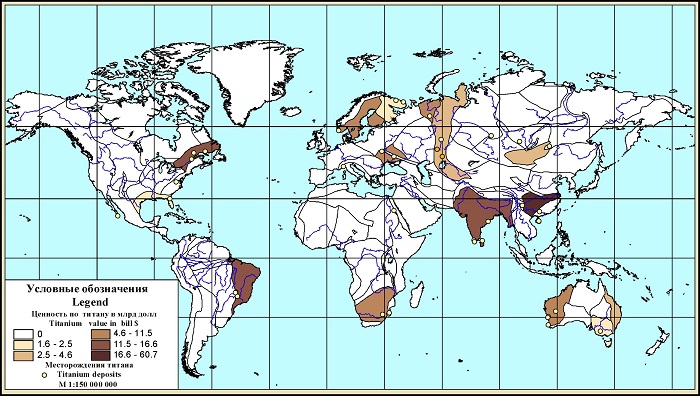
В десятку стран лидеров по добыче титана входят:
Мировые запасы и производство титана
Представленные в Канаде около 1/5 мировой добычи приходится на ильменитовые руды. В Китае 1/10 часть выпуска обеспечивается месторождением Лак-Тико.
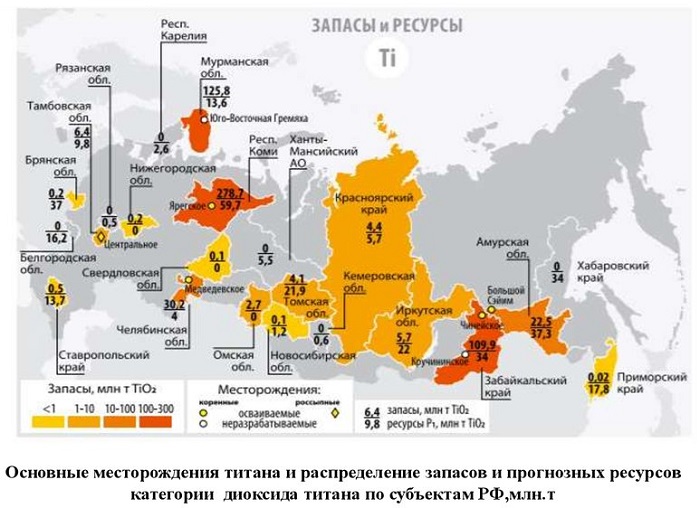
РФ производит меньше 1% титанового концентрата. Однако месторождение в Коми признано вторым по масштабу после Китая. Также лопаритовые руды экспортируются преимущественно Россией (Ловозерск). Последние используют в производстве редкоземельных металлов (в том числе титана).
Получение титана
Источник металла – диоксид титана. Его образование происходит в процессе переработки ильменита. В результате образуется титановый шлак, который подвергается дальнейшей переработке. К концентрату добавляют серную кислоту, на выходе образуется двуокись титана.

Другой способ заключается в соединении с углеродом (кокс), хлором и дальнейшим нагреванием в присутствии магния.
Также применяют восстановление кальцием диоксида титана. Последний процесс заключается в проведении электрического тока, что ведет к разложению оксида кальция (кислород на аноде и собственно кальций).
Кислород выступает в роли окислителя, кальций, будучи металлом, переходит к катоду, попутно восстанавливая титан. Процесс происходит несколько раз. Исходом реакции служит титановая губка, требующая очищения.
Физические свойства
Элемент расположен в четвертой группе в системе Д. И. Менделеева, под номером 22. В соединении атом обладает валентностью (II). Электронная конфигурация представлена формулой: [Ar] 3d24s2.

Вес атома (масса) около 47,9 а.е.м. Переход альфа титана в бета титан происходит при температуре 883 0 С. Теплота плавления 18,8 кДж/моль. Подвергается кипению при 3180 0 С. Обладает теплопроводностью, составляющей 22,09 Вт/(м*К).
Титан обладает высокой ковкостью, пластичностью, низкой твердостью. Однако сплавы, содержащие титан, относятся к высокотвердым, но хрупким соединениям.
Серебристое вещество, по строению относится к металлам, имеет голубоватый оттенок. Обладает низкой плотностью. Высокая температура плавления (1670 0 С).
В соединениях Ti способен проявить степень окисления (+2) (Ti+2H2, Ti+2O, Ti+2(OH)2, Ti+2F2, Ti+2Cl2, Ti+2Br2), (+3) (Ti+32O3, Ti+3(OH)3, Ti+3F3, Ti+3Cl3, Ti+32S3) и (+4) (Ti+4F4, Ti+4H4, Ti+4Cl4, Ti+4Br4).
Химические свойства
Устойчив к коррозии, по свойствам приближается хромоникелевой стали. Последнее обусловлено пленкой, образуемой на его поверхности. Воздух не меняет механических свойств.

При нагревании свыше 600 0 С металл становится хрупким, усиливается поглощение кислорода. При нагревании более 910 0 С взаимодействует с газообразными соединениями углерода, реабсорбирует азот.
При присоединении водорода, титан приобретает "водородную хрупкость". Данный эффект проявляется повышенной ломкостью при перепадах напряжения. Устойчив в кислотах.
Использование титана и его сплавов
Выделяют несколько технических сплавов с разной маркировкой ВТ1-00; ВТ1-0. В состав обоих входят:
Описание титановой руды
Титановая руда представляет собой природное соединение, содержащее выгодное для извлечения и переработки количество титана.
Металл окрашен в серебристо-белый цвет. Окраска элемента в порошке — серовато-черная. Он непрозрачен и не дает свечения под ультрафиолетом.

Структура
Титан относится к элементам гексагональной сингонии. Известны две полиморфные модификации: низкотемпературная с гексагональной плотноупакованной решеткой и высокотемпературная с кубической объемно-центрированной упаковкой атомов. Температура перехода одной модификации в другую — 883 градуса.

Свойства
Элемент под номером 22 в таблице Менделеева обладает высокой прочностью, пластичностью, устойчивостью к коррозии и свойствами парамагнетиков. При температуре в 3260 градусов металл начинает кипеть. В нем могут содержаться примеси кислорода, железа, кремния, азота, углерода, которые увеличивают прочность, при этом понижая пластичность металла.
Титан начинает плавиться при температуре в 1671 градус. Он становится настолько вязким, что налипает на режущее устройство. Поэтому при работе с материалом часто используют специальные смазки.
Титан не подвергается коррозии в воде, а также кислотах и даже царской водке.
Посмотрите видео о наглядных испытаниях свойств титана:
Происхождение
Титановая руда образуется под действием различных природных факторов на разных глубинах. Металл занимает 10 место в списке самых распространенных элементов земной коры. Он заключен в более чем 70 минералов, из которых самыми богатыми по содержанию являются титанит, лопарит, перовскит, ильменит, лейкоксен, рутил.
Метаморфогенные месторождения появляются в результате действия метаморфизма на первично-магматические руды и древние россыпи. Такие залежи представляют собой крупнейшие в мире месторождения титана.
Экзогенные месторождения титана делятся на прибрежно-морские и континентальные. Больший интерес представляют прибрежно-морские россыпи, содержащие ильменит, рутил, циркон. В них размеры зерен минералов достигают более 0,1 мм. Добывают полезное ископаемое в россыпях в основном в Австралии, Индии, Бразилии, на Шри-Ланке.
Титан магматического происхождения распространен в Амурской области — в Баладекском, Джугджурском, Коларском массивах.
В земной коре титан встречается только в соединении с кислородом. Его содержание в морской воде оценивается в 0,001 мг/л, в то время как в глинистых сланцах и его может быть сосредоточено до 4,5 кг/тонн.

Классификация
Титановые руды после переработки подвергаются процессам обогащения. В результате этого получают полезные сплавы с улучшенными характеристиками компонентов. В промышленности выделяется несколько разновидностей сплавов.
Титан легирует с алюминием, марганцем, хромом, ванадием, оловом, молибденом. Поэтому выделяет многокомпонентные и простые сплавы.
По механическим свойствам сплавы разделяют на:
- высокопрочные;
- среднепрочные;
- низкопрочные (с повышенной пластичностью).
В зависимости от способа изготовления говорят о литейных и деформируемых сплавах.
Сами руды в основном делятся по концентрации содержащегося в них титана на:
- богатые;
- бедные;
- забалансовые.
Подробнее о классах сплавов титана:
Месторождения и запасы в России и в мире
География титановых руд обширна, так как они распространены повсеместно. В России насчитывается около 20 месторождений титановых руд. Запасы титановых руд в мире составляют более 1 млрд тонн. В одном только ильмените всей планеты заключено около 650 млн тонн элемента.
Крупнейшие залежи титаномагнетитовых руд расположены в Чинейском месторождении в Забайкалье. На Кольском полуострове, в месторождении Африканда, открытом в 1935 году, насчитывается более 52 миллионов тонн титана.
В таблице приведен список стран-лидеров по содержанию запасов полезного ископаемого:
| Страна | Запасы титана в минералах, % | Основные области добычи |
| Австралия | ильменит — 3%, рутил — 24% | Прибрежно-морские россыпи в разных частях континента |
| Канада | ильменит — 9%, рутил — 6% | Рудный район Садбери |
| ЮАР | ильменит — 10%, рутил — 18% | Бушвельдский комплекс |
| Норвегия | ильменит — 15%, рутил — 1% | Провинция Эйгерсунн, месторождения Тельнес, Кодали |
| Страны СНГ | ильменит — 26%, рутил — 1% | Титановые руды в России: Южный Урал, Тува. |
На карте мира запасы титановых руд заметно преобладают на Австралийском, Североамериканском и Африканском континентах. Обычно полезные ископаемые отмечают специальным условным обозначением. В географии знак титановых руд представлен ромбом с закрашенной левой стороной.
При добыче титана часто получают и другие полезные компоненты — ванадий, цирконий, железо, ниобий, тантал, торий, редкие земли.
Добыча и переработка титановых руд
Титановые руды могут залегать как глубоко под землей, так и на поверхности. По этой причине разработано несколько способов добычи полезного металла.
Способы добычи
В том случае, когда руды представляют собой жилы, расположенные на небольшой глубине, прибегают к карьерному методу добычи. В зависимости от твердости выбирают горнодобывающую и буровзрывную технику. После извлечения руда подвергается дроблению и дальнейшей переработке.
Если полезное ископаемое добывается из коренного месторождения, то строят подземный комплекс сооружений, называемый шахтой. Это наиболее трудоемкий, а также финансово затратный способ.
В большинстве случаев титан находился в минералах россыпей. В песках он не требует измельчения, так как размеры зерен уже достаточно малы. Для добычи используют специальные гидравлические устройства, земснаряды, драги, экскаваторы.
Посмотрите про добычу титана в Украине:
Методы обогащения
После добычи в два этапа осуществляется процесс обогащения. Сначала концентрат отделяют из пустой массы, а затем из него извлекают отдельные минеральные индивиды.
Чаще всего применяются гравитационные методы, которые наиболее эффективны из-за разницы в удельном весе. Титан обычно подвергают мокрому или сухому обогащению в водной или воздушной средах соответственно.
Процесс флотации обозначает способность минеральных агрегатов удерживаться на границе раздела двух фаз. Для образования флотационной среды используют специальные образователи, с учетом индивидуальных свойств руды. Например, рутил флотируется олеиновой кислотой, а перовскит изначально обрабатывается серной кислотой.
Различие в физических свойствах позволяет использовать метод магнитной или электрической сепарации. В процессе обогащения нужные компоненты легко отделяются от пустой породы в специальных сепараторах с электрическим или магнитным полем. Минералы с отличными характеристиками меняют свою траекторию во время движения, отделяясь от остальной массы.
Сплавы
Полученные в процессе обогащения концентраты подвергают плавлению в электродуговых печах. Титан является жаростойким элементом, поэтому температура в печи достигает 1700 градусов.
При необходимости титановые руды рафинируют для удаления ненужных примесей.
Сплав титана и золота Сплав титана и 10% других металлов (в основном алюминий)
Промышленное применение
Титан — стратегически важное сырье, играющее большую роль в производстве. Металл используется в космонавтике, ракетостроении, авиации, машиностроении.
С помощью титана создают специальные арматуры, емкости, трубы и детали, которые применяют в автомобильной технике, строительстве и химической промышленности.
Титан считается необходимым сырьем для создания военной техники. С его помощью делают трубы, глушители, пропеллеры, турбины и другие части танков, судов и самолетов.
На основе титана создаются медицинские протезы, а также спортивные снаряды. Он нашел широкое применение и в искусстве. Титан используется при создании художественных изделий и скульптур.
Стоимость титановой руды
Титановая руда — востребованное на современном рынке сырье. Повышенная прочность металла наряду с его устойчивостью к коррозии позволяет разрабатывать перспективные способы применения элемента.
Делитесь статьей с друзьями в социальных сетях. Оставляйте свои интересные факты и знания о руде на титан в комментариях.
Читайте также:
- Если срок лизинга адреса клиентом dhcpv4 истекает какое сообщение отправляет клиент на сервер dhcp
- Работа человеческого сердца как пример автоколебания физика сообщение кратко
- Шкода кодиак сообщение на панели приборов вода в топливном фильтре
- Вязание в наше время сообщение
- Микробиология на службе человека сообщение

