Оксид азота сообщение по химии
Обновлено: 28.06.2024
Общая характеристика, основные физические и химические свойства оксида азота (I). Порядок и принципы его получения в лабораторных условиях и направления применения в промышленных масштабах. Окислительно-восстановительная двойственность оксида азота (II).
| Рубрика | Химия |
| Вид | доклад |
| Язык | русский |
| Дата добавления | 12.12.2014 |
| Размер файла | 86,5 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Азот образует с кислородом ряд оксидов; все они могут быть получены из азотной кислоты или ее солей.
Оксид N2O, или закись азота, получается при нагревании нитрата аммония:
Оксид азота (I) представляет собою бесцветный газ со слабым запахом и сладковатым вкусом.
Ни с водой, ни с кислотами, ни со щелочью оксид азота (I) не реагирует.
Вдыхание небольших количеств оксида азота (I) приводит к притуплению болевой чувствительности, вследствие чего этот газ иногда применяют в смеси с кислородом для наркоза.
Оксид NO, или окись азота, представляет собой бесцветный трудно сжижаемый газ. По химическим свойствам оксид азота (II) относится к числу безразличных оксидов, так как не образует никакой кислоты.
В лаборатории оксид азота (II) обычно получают взаимодействием 30-35%-ной азотной кислоты с медью:
В промышленности он является промежуточным продуктом при производстве азотной кислоты.
Для оксида азота (II) характерна окислительно-восстановительная двойственность. Под действием сильных окислителей он окисляется, а в присутствии сильных восстановителей - восстанавливается. Например, он легко окисляется кислородом воздуха до диоксида азота:
оксид лабораторный азот химический
Диоксид (или двуокись) азота NO2 - бурый ядовитый газ, обладающий характерным запахом. Он легко сгущается в красноватую жидкость которая при охлаждении постепенно светлеет замерзает, образуя бесцветную кристаллическую массу
Диоксид азота - очень энергичный окислитель. Многие вещества могут гореть в атмосфере, отнимая от него кислород. Пары NO2 ядовиты. Вдыхание их вызывает сильное раздражение дыхательных путей и может привести к серьезному отравлению.
При растворении в воде вступает в реакцию с водой, образуя азотную и азотистую кислоты.
Оксид N2O3, или азотистый ангидрид, представляет собой темно-синюю жидкость,
Оксиду соответствует азотистая кислота HNO2.
Оксид азота (V), или азотный ангидрид, N2O5 белые кристаллы, уже при комнатной температуре постепенно разлагающиеся на N2O и NO.
Он может быть получен действием фосфорного ангидрида на азотную кислоту:
Оксид азота (V) - очень сильный окислитель. Многие органические вещества при соприкосновении с ним воспламеняются. В воде оксид хорошо растворяется с образованием азотной кислоты.
Если нагревать нитрат калия или натрия, то они теряют часть кислорода и переходят в соли азотистой кислоты HNO2. Разложение идет легче в присутствии свинца, связывающего выделяющийся кислород:
Соли азотистой кислоты - нитриты - образуют кристаллы, хорошо растворимые в воде (за исключением нитрита серебра). Нитрит натрия применяется при производстве различных красителей.
При действии на раствор какого-нибудь нитрита разбавленной серной кислотой получается свободная азотистая кислота:
Она принадлежит к числу слабых кислот и известна только в сильно разбавленных водных растворах. При концентрировании раствора или при его нагревании азотистая кислота распадается:
Азотная кислота не отличается прочностью. Уже под влиянием света она постепенно разлагается:
Азотная кислота принадлежит к числу наиболее сильных кислот.
Характерным свойством азотной кислоты является ее ярко выраженная окислительная способность. Азотная кислота - один из энергичнейших окислителей. Многие неметаллы легко окисляются, превращаясь в соответствующие кислоты. Так, сера при кипячении с азотной кислотой постепенно окисляется в серную кислоту, фосфор - в фосфорную. Тлеющий уголек, погруженный в концентрированную HNO3, ярко разгорается.
Азотная кислота действует почти на все металлы (за исключением золота, платины, тантала, родия, иридия), превращая их в нитраты, а некоторые металлы - в оксиды.
Сильно разбавленная азотная кислота взаимодействует с активными металлами - цинком, магнием, алюминием - с образованием иона аммония, дающего с кислотой нитрат аммония. Обычно одновременно образуются несколько продуктов.
При действии азотной кислоты на металлы водород, как правило, не выделяется.
Азотная кислота - одно из важнейших соединений азота: в больших количествах она расходуется в производстве азотных удобрений, взрывчатых веществ и органических красителей, служит окислителем во многих химических процессах, используется в производстве серной кислоты по нитрозному способу, применяется для изготовления целлюлозных лаков, кинопленки.
Соли азотной кислоты называются нитратами. Все они хорошо растворяются в воде, а при нагревании разлагаются с выделением кислорода. При этом нитраты наиболее активных металлов переходят в нитриты:
Нитраты большинства остальных металлов при нагревании распадаются на оксид металла, кислород и диоксид азота. Например:
Наконец, нитраты наименее активных металлов (например, серебра, золота) разлагаются при нагревании до свободного металла:
Легко отщепляя кислород, нитраты при высокой температуре являются энергичными окислителями. Их водные растворы, напротив, почти не проявляют окислительных свойств.
Наиболее важное значение имеют нитраты натрия, калия, аммония и кальция, которые на практике называются селитрами.
Подобные документы
Бесцветный негорючий газ с приятным сладковатым запахом и привкусом. Смеси оксида азота с эфиром, циклопропаном, хлорэтилом. Химические свойства и получение оксида азота. Симптомы отравления веселящим газом и оказание первой медицинской помощи.
презентация [1,5 M], добавлен 10.09.2013
Характеристика азота – элемента 15-й группы второго периода периодической системы химических элементов Д. Менделеева. Особенности получения и применения азота. Физические и химические свойства элемента. Применение азота, его значение в жизни человека.
презентация [544,3 K], добавлен 26.12.2011
Открытие, физические и химические свойства азота. Круговорот азота в природе. Промышленный и лабораторный способы получения чистого азота. Химические реакции азота в нормальных условиях. Образование природных залежей полезных ископаемых, содержащих азот.
презентация [226,7 K], добавлен 08.12.2013
История открытия азота, его формула и свойства, нахождение в природе и химические реакции, которые происходят непосредственно в природе при участии азота. Методы связывания, получение и свойства нескольких важнейших соединений, области применения азота.
курсовая работа [896,1 K], добавлен 22.05.2010
Биологические и не биологические процессы фиксации азота. Открытие бактерий рода азотобактер. Соединения азота, формы их распространения и области применения. Физические и химические свойства азота, его распространение в природе и способы получения.
реферат [64,7 K], добавлен 22.04.2010
Как распространены оксидные соединения в природе. Какие оксиды образуют природные минералы. Химические свойства диоксида углерода, углекислого газа, карбона (II) оксида, красного, магнитного и бурого железняков, оксида хрома (III), оксида кальция.
презентация [1,7 M], добавлен 19.02.2017
Нахождение азота в природе, его физические и химические свойства. Выделение азота из жидкого воздуха. Свойство жидкого азота при испарении резко понижать температуру. Получение аммиака и азотной кислоты. Образование и скопление селитры в природе.

Оксид азота – химическое соединение группы окисей азота, в котором азот присутствует во II степени окисления. Он имеет один непарный радикальный электрон, следовательно, является нестабильным, имеет высокую реакционную способность и обладает свойствами свободного радикала.
Оксид азота или окись азота, а также известный как монооксид азота представляет собой молекулу с химической формулой NO. Это свободные радикалы, которые является важным промежуточным продуктом химических реакций.
В организмах млекопитающих и человека оксид азота является важной составляющей клеточных сигнальных молекул, участвующих во многих физиологических и патологических процессах. Это мощный вазодилататор с коротким, в несколько секунд, периодом полураспада в крови.
В конце 80-х годов было доказано, что особые ферментные системы организмов способны синтезировать газ оксида азота. Это происходит в результате окисления гуанидиновой группы аминокислоты L-аргинина с одновременным синтезом цитруллина.
Получение оксида азота
В лабораторных условиях получение оксида азота возможно путем проведения реакции разбавленной азотной кислоты с медью или восстановлением азотистой кислоты в виде нитрита натрия или нитрита калия.
Основным природным источником оксида азота являются электрические разряды молний в грозу. Оксид азота является побочным продуктом, возникающим при сгорании веществ в автомобильных двигателях и топлива на электростанциях.
Также получение оксида азота возможно из свободных элементов, для этого необходимо при температуре 1200-1300°C провести соединение азота с кислородом.
Применение оксида азота
Оксид азота используется в медицине для расширения кровеносных сосудов при ишемической болезни сердца путем уменьшения нагрузки на сердце.
Оксид азота используется при неотложной помощи для содействия капиллярному расширению легких для лечения первичной легочной гипертензии у новорожденных, связанной с врожденными дефектами. Терапия оксидом азота значительно повышает качество жизни и, в некоторых случаях, спасает жизнь детей с риском развития заболевания сосудов легких.
Оксид азота также вводится в виде спасительной терапии у больных с острой правожелудочковой недостаточностью, которая является вторичной по отношению к легочной эмболии.
В пищевой промышленности оксид азота известен под названием пищевая добавка Е942 и используется в качестве пропеллента и упаковочного газа.
Свойства оксида азота
Оксид азота – это бесцветный газ с температурой плавления -163,6°С и температурой кипения -151,7°С. Молекулярная формула оксида азота – NO, молярная масса – 30.01 грамм/моль, плотность – 1,3402 г дм, растворимость в воде – 74 см3/дм3, показатель преломления – 1.0002697.
Польза оксида азота

Оксид азота широко применяется в традиционной медицине при различных заболеваниях и оказывает положительное влияние на:
- Систему кровообращения – регуляторные свойства оксида азота оказывают влияние на циркуляцию крови по всему телу, увеличивают диаметр кровеносных сосудов и предотвращают образование тромбов. Он помогает эндотелиальным клеткам контролировать кровеносные сосуды. Оксид азота также повышает уровень кислорода внутри тела, понижает уровень артериального давления и помогает в оптимальном режиме функционировать сердцу;
- Иммунную систему – иммунные клетки в организме человека синтезируют оксид азота, чтобы уничтожать бактерии и вирусы, способные вызывать инфекции. Известно также свойство оксида азота предотвращать появление доброкачественных и злокачественных опухолей в клетках организма;
- Уровень выносливости - оксид азота повышает уровень выносливости мышечных клеток, что позволяет выдерживать более тяжелые нагрузки и с легкостью вести более активную деятельность;
- Повышение реакции нервных клеток – оксид азота действует как внутриклеточный посредник между различными клетками в организме, в том числе, нервными клетками. При достаточном содержании оксида азота в организме связь между нервными клетками становится быстрее, что приводит к быстроте реакции на внешние раздражители, увеличению фокуса и бдительности;
- Повышение сексуальной энергии – применение оксида азота стимулирует, бодрит и усиливает сексуальные механизмы реагирования в организме. Сенсорные и психические стимуляции, вызываемые нервными клетками под действием оксида азота, приводят к расслаблению мышц и притоку крови к пенису, благодаря чему происходит эрекция. Таким же образом процесс протекает и в женском организме, под действием оксида азота приток крови увеличивается в тканях влагалища;
- Облегчение боли – оксид азота обеспечивает долгосрочное облегчение от боли, связанной с артритом и воспалением суставов. Он способен активировать противовоспалительные механизмы в клетках организма, и способствует уменьшению воспаления;
- Увеличение мышечной массы – добавки содержащие оксид азота расширяют кровеносные каналы, улучшают кровообращение и увеличивают мышечную массу. При увеличении потока крови увеличивается количество питательных веществ в мышцах, что приводит к увеличению их размера;
- Внутриклеточные связи – оксид азота улучшает процесс связи между различными клетками в организме, в том числе, между нервными клетками и клетками мозга. Применение добавок содержащих оксид азота приводит к улучшению памяти, повышению уровня концентрации и способности к обучению.
Вред оксида азота
Применение оксида азота у большинства людей не вызывает побочных эффектов, однако, в случаях передозировки он приводит к диарее, слабости, тошноте, головной боли, учащению пульса и сердцебиения, задержкам воды, усталости, раздражениям на коже и сухости во рту.
Также побочными эффектами применения оксида азота являются проблемы с дыханием, сильная аллергия или сыпь, крапивница, зуд, одышка, опасные для жизни осложнения астмы, внезапный озноб, потливость, тремор, рвота и обмороки. В некоторых случаях применение оксида азота приводит к вспышкам герпеса, расширению сосудов и кровотечениям.
Нашли ошибку в тексте? Выделите ее и нажмите Ctrl + Enter.
Наши почки способны очистить за одну минуту три литра крови.
Американские ученые провели опыты на мышах и пришли к выводу, что арбузный сок предотвращает развитие атеросклероза сосудов. Одна группа мышей пила обычную воду, а вторая – арбузный сок. В результате сосуды второй группы были свободны от холестериновых бляшек.
74-летний житель Австралии Джеймс Харрисон становился донором крови около 1000 раз. У него редкая группа крови, антитела которой помогают выжить новорожденным с тяжелой формой анемии. Таким образом, австралиец спас около двух миллионов детей.
Печень – это самый тяжелый орган в нашем теле. Ее средний вес составляет 1,5 кг.
Кроме людей, от простатита страдает всего одно живое существо на планете Земля – собаки. Вот уж действительно наши самые верные друзья.
В Великобритании есть закон, согласно которому хирург может отказаться делать пациенту операцию, если он курит или имеет избыточный вес. Человек должен отказаться от вредных привычек, и тогда, возможно, ему не потребуется оперативное вмешательство.
Когда влюбленные целуются, каждый из них теряет 6,4 ккалорий в минуту, но при этом они обмениваются почти 300 видами различных бактерий.
Люди, которые привыкли регулярно завтракать, гораздо реже страдают ожирением.
Каждый человек имеет не только уникальные отпечатки пальцев, но и языка.
Согласно мнению многих ученых, витаминные комплексы практически бесполезны для человека.
Даже если сердце человека не бьется, то он все равно может жить в течение долгого промежутка времени, что и продемонстрировал нам норвежский рыбак Ян Ревсдал. Его "мотор" остановился на 4 часа после того как рыбак заблудился и заснул в снегу.
У 5% пациентов антидепрессант Кломипрамин вызывает оргазм.
Кариес – это самое распространенное инфекционное заболевание в мире, соперничать с которым не может даже грипп.
Согласно исследованиям, женщины, выпивающие несколько стаканов пива или вина в неделю, имеют повышенный риск заболеть раком груди.
Многие наркотики изначально продвигались на рынке, как лекарства. Героин, например, изначально был выведен на рынок как лекарство от детского кашля. А кокаин рекомендовался врачами в качестве анестезии и как средство повышающее выносливость.

Катаракта. Как побороть страхи и наконец подарить себе отличное зрение
Любое оперативное вмешательство пугает, даже самое незначительное. Допустить мысль о том, что какие-то манипуляции будут выполняться с глазами, может и вовсе по.
Все оксиды азота, кроме N2O, ядовитые вещества.
Оксид азота (I) N2O – это бесцветный газ со слабым запахом и сладковатым вкусом, хорошо растворимый в воде, но не взаимодействует с ней. При достаточно высокой температуре разлагается по уравнению:
Наиболее важными являются оксиды азота (II) и (IV).
Оксид азота (II) NO – бесцветный газ, не имеет запаха. В воде малорастворим, относится, как и N2O, к несолеобразующим оксидам. Оксид азота (II) NO образуется из азота и кислорода при сильных электрических разрядах (например, во время грозы в воздухе) или при высокой температуре:
В лаборатории оксид азота (II) получают, например, при взаимодействии меди и разбавленной азотной кислоты:
Оксид азота (II) в промышленности получают каталитическим окислением аммиака и используют для получения азотной кислоты:
Оксид азота (II) на воздухе легко окисляется до оксида азота (IV):

Оксид азота (IV) NO2 – ядовитый газ бурого цвета, имеет характерный запах. Хорошо растворяется в воде. Оксид азота (IV) является смешанным оксидом, которому соответствуют две кислоты: азотистая HNO2 и азотная HNO3. Поэтому взаимодействие с водой происходит по уравнению:
При взаимодействии NO2 с водой в присутствии кислорода (на воздухе) образуется только азотная кислота:
При растворении NO2 в щелочи, например NaOH, образуются две соли (нитрат и нитрит) и вода:
В избытке кислорода образуется только нитрат натрия:
Ниже 22 0 С молекулы оксида азота (IV) NO2 легко соединяются попарно и образуют бесцветную жидкость состава N2O4, которая при охлаждении до – 10,2 0 С превращается в бесцветные кристаллы.
В лаборатории NO2 можно получить при взаимодействии, например, меди с концентрированной азотной кислотой:
В промышленности NO2 получают путем окисления NO кислородом и далее используют для получения азотной кислоты.
Оксид азота (III) N2O3 – это темно-синяя жидкость, является кислотным оксидом. При взаимодействии с водой образуется азотистая кислота:

Оксид азота (V) N2O5 – бесцветные кристаллы, хорошо растворимые в воде с образованием азотной кислоты:
Азотная кислота
Физические свойства
Азотная кислота HNO3 – бесцветная жидкость, имеет резкий запах, легко испаряется, кипит при температуре 83 0 С. При попадании на кожу азотная кислота может вызвать сильные ожоги (на коже образуется характерное желтое пятно, его сразу же следует промыть большим количеством воды, а затем нейтрализовать содой). С водой азотная кислота смешивается в любых соотношениях.
Обычно применяемая в лаборатории концентрированная азотная кислота содержит 63% HNO3. При хранении довольно легко, особенно на свету разлагается по уравнению:
Выделяющийся газ NO2 окрашивает азотную кислоту в бурый цвет.
Химические свойства

Кислотно – основные свойства
Азотная кислота – одна из наиболее сильных кислот. В водных растворах она полностью диссоциирована на ионы:
Как и все кислоты, она реагирует:
в) с солями более слабых кислот:
Окислительно – восстановительные свойства
Азотная кислота является одним из сильнейших окислителей. Ее окислительно-восстановительные свойства обусловлены присутствием в молекуле HNO3 атома азота в высшей степени окисления N +5 в составе кислотного остатка NO3 — . Окислительные свойства кислотного остатка NO3 — значительно сильнее, чем ионов водорода Н + , поэтому азотная кислота взаимодействует практически со всеми металлами, кроме золота и платины, находящимися в конце ряда напряжений. Так как окислителем в HNO3 являются ионы NO3 — , а не ионы Н + , то при взаимодействии HNO3 с металлами практически никогда не выделяется водород. Нитрат-ионы NO3 — при взаимодействии HNO3 с металлами восстанавливаются тем полнее, чем более разбавлена кислота и чем более активен металл. На следующей схеме показано, какие продукты могут образоваться при восстановлении HNO3:

Концентрированная HNO3 при взаимодействии с наиболее активными металлами (до Al в ряду напряжений) восстанавливается до N2O. Например:
Концентрированная HNO3 при взаимодействии с менее активными металлами (Ni, Cu, Ag, Hg) восстанавливается до NO2. Например:
Аналогично концентрированная азотная кислота реагирует с некоторыми неметаллами. Неметалл при этом окисляется до оксокислоты. Например:
Следует отметить, что концентрированная HNO3 пассивирует такие металлы, как Fe, Al, Cr. Сущность пассивирования заключается в образовании на поверхности металла тонкой, но очень плотной оксидной плёнки, предохраняющей металл от дальнейшего взаимодействия с кислотой; например:
Разбавленная HNO3 реагирует с наиболее активными металлами (до Al) с образованием аммиака или нитрата аммония NH4NO3:
При взаимодействии разбавленной азотной кислоты с менее активными металлами образуется оксид азота (II) NO:
Таким же образом разбавленная HNO3 взаимодействует с некоторыми неметаллами:

Получение
В лаборатории азотную кислоту получают при взаимодействии безводных нитратов с концентрированной серной кислотой:
В промышленности получение азотной кислоты идет в три стадии:
- Растворение оксида азота (IV) в воде и избытком кислорода:
Применение
Азотную кислоту применяют для получения азотных удобрений, лекарственных и взрывчатых веществ.
Соли азотной кислоты
Соли азотной кислоты называются нитратами. Нитраты калия, натрия, аммония и кальция называются селитрами. Селитры применяют как минеральные азотные удобрения, так как азот является одним из основных элементов питания растений.
Все соли азотной кислоты хорошо растворимы в воде.
Соли азотной кислоты, как и она сама, являются сильными окислителями.
При нагревании все нитраты разлагаются с выделением кислорода, характер других продуктов разложения зависит от положения металла в ряду напряжений:
Если внимательно взглянуть на азот в периодической системе химических элементов Д. И. Менделеева, то можно заметить, что он имеет переменную валентность. Это значит, что азот образует сразу несколько бинарных соединений с кислородом. Некоторые из них были открыты недавно, а некоторые - изучены вдоль и поперек. Существуют малостабильные и устойчивые оксиды азота. Химические свойства каждого из этих веществ совершенно разные, поэтому при их изучении нужно рассматривать как минимум пять оксидов азота. Вот о них и пойдет речь в сегодняшней статье.
Оксид азота (I)
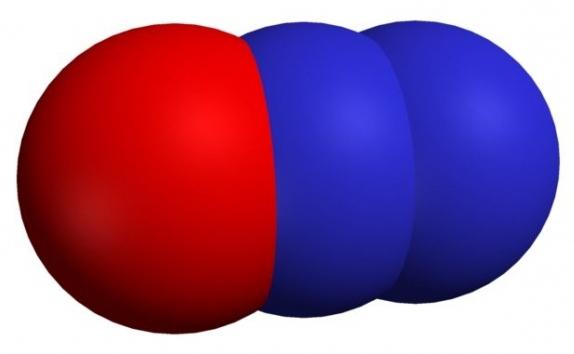
Формула - N2O. Иногда его могут называть оксонитридом азота, оксидом диазота, закисью азота или веселящим газом.
В обычных условиях представлен бесцветным газом, имеющим сладковатый запах. Его могут растворять вода, этанол, эфир и серная кислота. Если газобразный оксид одновалентного азота нагреть до комнатной температуры под давлением 40 атмосфер, то он сгущается до бесцветной жидкости. Это несолеобразующий оксид, разлагающийся во время нагревания и показывающий себя в реакциях как восстановитель.
Этот оксид образуется, когда нагревают сухой нитрат аммония. Другой способ его получения - термическое разложение смеси "сульфаминовая + азотная кислота".
Используется в качестве средства для ингаляционного наркоза, пищевая промышленность знает этот оксид как добавку E942. С его помощью также улучшают технические характеристики двигателей внутреннего сгорания.
Оксид азота (II)
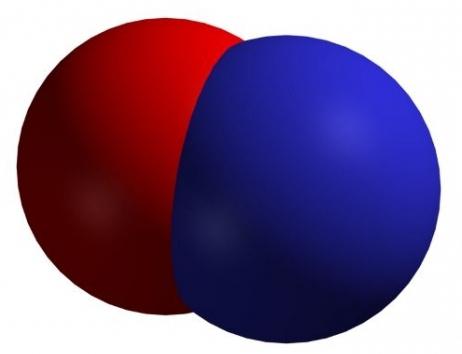
При нормальных условиях имеет вид бесцветного газа, который плохо растворяется в воде. Его трудно сжижить, однако в твердом и жидком состояниях это вещество имеет голубой цвет. Данный оксид может окисляться кислородом воздуха
Его довольно просто получить, для этого нужно нагреть до 1200-1300 о С смесь азота и кислорода. В лабораторных условиях он образуется сразу при нескольким опытах:
- Реакция меди и 30%-ного раствора азотной кислоты.
- Взаимодействие хлорида железа, нитрита натрия и соляной кислоты.
- Реакция азотистой и иодоводородной кислот.
Это одно из веществ, из которых получают азотную кислоту.
Оксид азота (III)

В нормальных условиях является жидкостью, которая имеет синий цвет, а в стандартных - бесцветным газом. Чистый оксид существует только в твердом агрегатном состоянии.
Образуется при взаимодействии 50%-ной азотной кислоты и твердого оксида трехвалентного мышьяка (его также можно заменить крахмалом).
С помощью этого вещества в лабораториях получают азотистую кислоту и ее соли.
Оксид азота (IV)
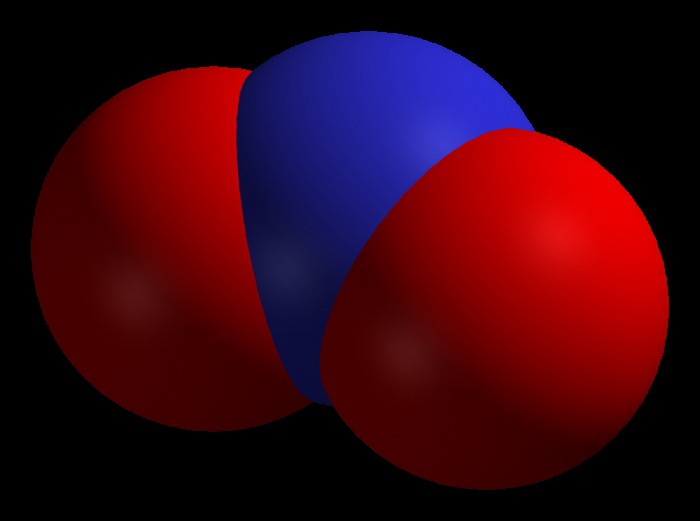
Последнее название соответствует одному из его свойств. Ведь этот оксид имеет вид или красно-бурого газа или желтоватой жидкости. Ему присуща высокая химическая активность.
Данный оксид получают при взаимодействии азотной кислоты и меди, а также во время термического разложения нитрата свинца.
С помощью него производят серную и азотную кислоты, окисляют жидкое ракетное топливо и смесевые взрывчатые вещества.
Оксид азота (V)
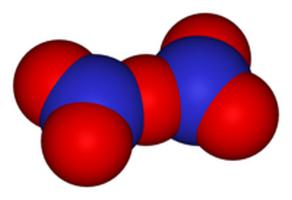
Формула - N2O5. Может встречаться под названиями пентаоксида диазота, нитрата нитроила или азотного ангидрида.
Имеет вид бецветных и очень летучих кристаллов. Они могут плавиться при температуре 32,3 о С.
Этот оксид образуется при нескольких реакциях:
- Дегидрация азотной кислоты оксидом пятивалентного фосфора.
- Пропускание сухого хлора над нитратом серебра.
- Взаимодействие озона с оксидом четырехвалентного азота.
Из-за своей крайней неустойчивости в чистом виде нигде не используется.
Заключение
В химии существует девять оксидов азота, приведенные выше являются только классическими соединениями этого элемента. Остальные четыре - это, как уже было сказано, нестабильные вещества. Однако их все объединяет одно свойство - высокая токсичность. Выбросы оксидов азота в атмосферу приводят к ухудшению состояния здоровья живущих поблизости от промышленных химических предприятий людей. Симптомы отравления каким-либо из этих веществ - токсический отек легких, нарушение работы центральной нервной системы и поражение крови, причина которого - связывание гемоглобина. Поэтому с оксидами азота необходимо осторожно обращаться и в большинстве случаев использовать средства защиты.
В науке известно несколько видов оксида азота. Некоторые из них используются в медицинской практике и промышленных целях. Часть соединений крайне неустойчивы и не имеют практического значения. Химические вещества этой группы оказывают воздействие на организм человека и принимают участие в обмене веществ.
Виды и свойства
Азот — вещество, которое образует несколько групп оксидов. Все они обладают разной молярной массой и физическими характеристиками. В группу солеобразующих входят:
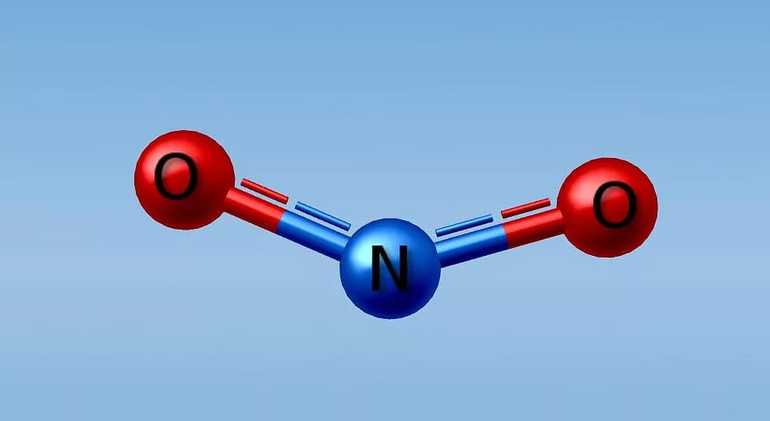
- Триоксид диазота (III). Химическая формула N2O3, кратность связи равна 3. Вещество имеет вид жидкости тёмно-синего цвета, плотность которой меньше плотности воды. Кристаллизуется при температуре -100 градусов. Этот кислотный оксид реагирует со щелочами, образуя соли. С водой образует азотистую кислоту: N2O3+H2O = 2HNO2.
- Двуокись азота (IV) — NO2. Атомы в молекуле расположены под углом к друг другу. Вещество является ядовитым газом бурого цвета, имеет характерный запах. Легко растворимо в воде. Оксид образует 2 кислоты — азотную и азотистую. Азотная кислота образуется в присутствии воздуха и воды. Со щелочами образует 2 соли — нитрат и нитрит. При температуре меньше 22 градусов молекулы димеризуются и образуется N2O4. Образуется жидкость, которая при дальнейшем охлаждении превращается в кристаллы.
- Пентаоксид (V) — N2O5. Другое название — азотный ангидрид. Представляет собой кристаллы, имеющие белую окраску. При нормальной температуре и давлении легко разлагается. При низких температурах сохраняет высокую степень устойчивости. Обладает свойствами окислителя и восстановителя.
Несолеобразующие соединения
Второй класс соединений — несолеобразующие. В неё входят оксид одновалентного и двухвалентного азота. Вещество с формулой N2O имеет линейное строение молекулы. Представляет собой газ, не имеющий цвета. В нормальных условиях вещество инертно. Обладает сладковатым вкусом и слабым запахом. Легко растворяется в воде, однако не вступает с ней в химические реакции. С водородом реагирует со взрывом. Не вступает в химические реакции с кислотами и основаниями.
При небольшом нагревании быстро разлагается, проявляет свойства окислителя. Окисляет металлы, водород, сернистый газ и прочее. Растворяясь в воде, образует азотную кислоту. В результате таких реакций образуется свободная форма азота.
Вступая в контакт с окислителями, N2O выступает в роли восстановителя. К примеру, раствор перманганата в серной кислоте окисляет закись азота до образования монооксида. В водном растворе окисляет диоксид серы до серной кислоты.
Монооксид (II) — NO. При низких температурах молекулы димеризуются и образуют новое вещество. Окись азота представляет собой газ без цвета и запаха, малорастворимый в воде. В присутствии кислорода загорается, образуется диоксид — вещество коричневого цвета. Под действием хлора или озона легко окисляется. Жидкая и твёрдая форма имеет голубую окраску. Вступает во взаимодействие с основаниями и основными оксидами.
Получение в природе и промышленности
В природе азот встречается преимущественно в чистом виде. Во время грозы азот и кислород вступают во взаимодействие при высокой температуре. Образуется монооксид: N2+O2 = 2NO.
В промышленных условиях получают следующие соединения:

- При разложении нитрата аммония образуется оксид азота, формула которого выглядит как N2O. Уравнение химической реакции записывается следующим образом: NH4NO3 → N2O+2H2O.
- На производстве получение оксида азота (I) происходит путём окисления аммиака. Химический процесс нуждается в присутствии катализатора, в роли которого выступает платина.
- В лабораторных условиях монооксид получают путём взаимодействия меди и разбавленной азотной кислоты. Другой способ получения — окисление хлорида железа или йодоводорода в результате взаимодействия с азотной кислотой.
- Двуокись получается в результате взаимодействия монооксида с атомами кислорода.
- Лабораторным путём NO2 (IV) получается при взаимодействии концентрированной азотной кислоты с медью. Второй вариант — разложение нитрата меди или свинца.
- Азотистый ангидрид можно получить из оксидов при низкой температуре.
Живые организмы также вырабатывают соединения азота. Растения способны вырабатывать монооксид азота несколькими способами:
- С помощью фермента синтазы и аминокислоты аргинина. Хотя некоторые учёные считают, что в растительных клетках нет прямых аналогов этого фермента.
- С помощью фермента нитрат-редуктазы, который находится в клеточных оболочках. Вещество способно восстанавливать нитраты и нитриты, которые растение получает из почвы.
- Посредством транспортировки электронов в митохондриях.
- Путём окисления аммиака или восстановления нитратов и нитритов без участия катализаторов.
Практическое применение
Химические свойства оксида азота нашли практическое применение. Их используют в медицинской практике, военной, пищевой и химической промышленности. Наиболее часто соединения используются в следующих целях:
- Влияние оксида азота на организм человека используется в медицинской практике. В хирургии применяется для дачи ингаляционного наркоза в смеси с кислородом (2 части кислорода на 8 частей закиси азота).
- Поскольку NO2 обладает свойствами сильного окислителя, он используется в производстве ракетного топлива. Когда вещество взаимодействует с гидразином, образуется колоссальное количество энергии. Кроме того, оно используется для изготовления взрывчатых смесей.
- Соединение NO2 применяется в химии для производства серной и азотной кислоты.
- С помощью NO улучшают технические качества двигателей внутреннего сгорания у автомобилей.
- В пищевой промышленности вещество применяется в качестве добавки для улучшения вкуса готовых продуктов. На упаковках ему соответствует символ Е942.
- Монооксид и оксид трёхвалентного азота используется в химической промышленности в качестве сырья для производства азотной кислоты и её солей.
Влияние на живые организмы
Монооксид азота — высокотоксичное соединение. Поступая в организм в больших концентрациях, способен изменить структуру гемоглобина, что взывает кислородное голодание. Оксид азота (IV) — крайне ядовитое вещество, представляющее опасность для здоровья и жизни.
Монооксид азота — вторичный посредник, который участвует в механизмах внутриклеточной и межклеточной передачи импульсов. Это вещество вырабатывают практически все живые организмы, от одноклеточных до млекопитающих.
Изначально окись азота была известна как эндотелиальный сосудорасширяющий фактор. Она образовалась в организме из аминокислоты аргинина. В химическом процессе участвуют молекулы кислорода, НАДФ и синтаза оксида азота. Другой способ образования вещества — восстановление неорганических солей азотной кислоты.
Эндотелиальные клетки сосудов передают сигнал гладкомышечным элементам, в результате сосуды расширяются и усиливается местный кровоток. Молекула оксида азота обладает способностью легко проникать через мембраны клеток. Благодаря этому она служит для обмена сигналами. Это благотворно влияет на состояние сердечно-сосудистой системы. Снижается риск ишемии миокарда и развития гипертонической болезни.
Уровень эндогенной окиси азота могут повышать растительные продукты — руккола, шпинат, свёкла, петрушка и прочие. Получение вещества из растительных продуктов требует присутствия сапрофитных микроорганизмов. В норме они живут в ротовой полости человека.
Читайте также:

