Сочинение про химический элемент калий
Обновлено: 04.07.2024
Содержание калия в магматических горных породах. Главные калийсодержащие минералы. Основные типы месторождений, схемы обогащения и применение. Изучение обменных реакций расплавленных едкого калия и металлического натрия. Процесс производства гранулята.
| Рубрика | Химия |
| Вид | доклад |
| Язык | русский |
| Дата добавления | 19.12.2013 |
| Размер файла | 21,1 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
КАЛИЙ, К (от араб, аль-кали -- поташ * а. Potassium, potash; н. Kalium; ф. potassium; и. potasio), -- химический элемент I группы периодической системы Менделеева, атомный номер 19, атомная масса 39,102. Природный калий состоит из двух стабильных изотопов 39 К (93,08%), 41 К (6,91%) и одного радиоактивного 40 К (0,01%) с периодом полураспада 1,39*10 9 лет. Открыт английским химиком Г. Дэви в 1807.
Калий -- один из наиболее распространённых петрогенных элементов земной коры -- 2,5% (по массе). В магматических горных породах содержание калия закономерно увеличивается с ростом их кислотности. Кларк калия в ультраосновных горных породах 0,03%, в основных 0,83%, средних 2,3%, в кислых 3,34%. Максимальные концентрации калия (до 7%) -- в щелочных породах агпаитового ряда. Главные калийсодержащие минералы в этих породах: щелочные полевые шпаты, слюды, нефелин, лейцит. При выветривании магматических горных пород основная часть калия накапливается глинами, в которых содержание калия 2,28% (по массе), а часть калия, перешедшая в раствор, с течением времени захватывается микроорганизмами, донными осадками (например, в глауконитах содержание К2О достигает 7,5%). Поэтому океанические воды содержат только 0,039% калия. При испарении морской воды в органических замкнутых объёмах осаждаются калийсодержащие минералы сильвинит, карналлит, каинит, полигалит. В результате интенсивного испарения морской воды в прошлые геологические эпохи, особенно в пермский период, были образованы крупные месторождения калийных солей. Основные типы месторождений, схемы обогащения и применение см. в ст. Калийные соли.
Радиоактивный изотоп 40 К -- важный источник глубинного тепла на ранней стадии эволюции Земли. Превращение 40 К 40 Ar используется для определения абсолютного возраста пород, содержащих калиевые минералы. Металлический калий получают путём обменных реакций между металлическим натрием и гидрооксидом или хлоридом калия, а также электролизом расплавов KOH. Металлический калий используется для получения надпероксида KO2, который служит источником кислорода в регенерационных устройствах в замкнутых объёмах (например, на подводных лодках), для восстановления титана из расплавов его солей (TiCl4). Сплавы калия с натрием (40-90% калия), жидкие при комнатной температуре, используются в качестве теплоносителей в ядерных реакторах. Человечество знакомо с калием больше полутора веков. В лекции, прочитанной в Лондоне 20 ноября 1807 г., Хэмфри Дэви сообщил, что при электролизе едкого кали он получил "маленькие шарики с сильным металлическим блеском. Некоторые из них сейчас же после своего образования сгорали со взрывом". Это и был калий. Калий - замечательный металл. Замечателен он не только потому, что режется ножом, плавает в воде, вспыхивает на ней со взрывом и горит, окрашивая пламя в фиолетовый цвет. И не только потому, что этот элемент - один из самых активных химически. Все это можно считать естественным, потому что соответствует положению щелочного металла калия в таблице Менделеева. Калий замечателен своей незаменимостью для всего живого и примечателен как всесторонне "нечетный" металл. Обратите внимание: его атомный номер 19, атомная масса 39, во внешнем электронном слое - один электрон, валентность 1+. Как считают химики, именно этим объясняется исключительная подвижность калия в природе. Он входит в состав нескольких сотен минералов. Он находится в почве, в растениях, в организмах людей и животных. Он - как классический Фигаро: здесь - там - повсюду.
Зачем нужен металлический калий? Металлический калий используют как катализатор в производстве некоторых видов синтетического каучука, а также в лабораторной практике. В последнее время основным применением этого металла стало производство перекиси калия К2О2, используемой для регенерации кислорода. Сплав калия с натрием служит теплоносителем в атомных реакторах, а в производстве титана - восстановителем.
Из соли и щелочи
Получают калий чаще всего в обменной реакции расплавленных едкого калия и металлического натрия: KOH+NaNaOH+К. Процесс идет в ректификационной колонне из никеля при температуре 380. 440 o C. Подобным образом получают элемент N 19 и из хлористого калия, только в этом случае температура процесса выше - 760. 800 o C. При такой температуре и натрий, и калий превращаются в пар, а хлористый калий (с добавками) плавится. Пары натрия пропускают через расплавленную соль и конденсируют полученные пары калия. Этим же способом получают и сплавы натрия с калием. Состав сплава в большой мере зависит от условий процесса.
Селитра или селитры?
Правильнее - селитры. Это общее название азотнокислых солей щелочных и щелочноземельных металлов. Если же говорят просто "селитра" (не "натриевая" или "кальциевая" или "аммиачная", а просто - "селитра"), то имеют в виду нитрат калия. Этим веществом человечество пользуется уже больше тысячи лет - для получения черного пороха. Кроме того, селитра - первое двойное удобрение: из трех важнейших для растений элементов в ней есть два - азот и калий. Вот как описал селитру Д.И. Менделеев в "Основах химии": "Селитра представляет бесцветную соль, имеющую особый прохладительный вкус. Она легко кристаллизуется длинными, по бокам бороздчатыми, ромбическими, шестигранными призмами, оканчивающимися такими же пирамидами. Ее кристаллы (уд. вес 1,93) не содержат воды. При слабом накаливании (339њ) селитра плавится в совершенно бесцветную жидкость. При обыкновенной температуре в твердом виде КNO3 малодеятельная и неизменна, но при возвышенной температуре она действует как весьма сильное окисляющее средство, потому что может отдать смешанным с нею веществам значительное количество кислорода. Брошенная на раскаленный уголь селитра производит быстрое его горение, а механическая смесь ее с измельченным углем загорается от прикосновения с накаленным телом и продолжает сама собою гореть. При этом выделяется азот, а кислород селитры идет на окисление угля, вследствие чего и получаются углекалиевая соль (Имеется в виду поташ.) и углекислый газ. В химической практике и технике селитра употребляется во многих случаях как окислительное средство, действующее при высокой температуре. На этом же основано применение ее для обыкновенного пороха, который есть механическая смесь мелко измельченных: серы, селитры и угля".
Процесс производства гранулята идентичен процессу, который используется при производстве розового хлористого калия вплоть до окончания последнего этапа просушки. После этого этапа высушенный порошок прессуется в плитки под давлением 200-220 атмосфер, затем плитки.
Калий был открыт осенью 1807 года английским химиком Дэви при электролизе твёрдого едкого кали. Увлажнив едкий кали, ученый выделил металл, которому дал название потассий, намекая на производство поташа (необходимого ингредиента для изготовления моющих средств) из золы. Своё привычное название металл получил через два года, в 1809г, инициатором переименования вещества стал Л.В. Гильберт, предложивший название калий (от арабского аль-кали – поташ).

Общая характеристика калия
Калий (лат. Kalium) является мягким щелочным металлом, элементом главной подгруппы I группы, IV периода периодической системы химических элементов Д.И. Менделеева, имеет атомный номер 19 и обозначение – К.
Нахождение в природе
Калий в свободном состоянии в природе не встречается, он входит в состав всех клеток. Достаточно распространённый металл, занимает 7-е место по содержанию в земной коре (calorizator). Основными поставщиками калия являются Канада, Белоруссия и Россия, имеющие крупные месторождения данного вещества.
Физические и химические свойства
Калий – легкоплавкий металл серебристо-белого цвета. Имеет свойство окрашивать открытый огонь в яркий фиолетово-розовый цвет.
Калий имеет высокую химическую активность, это сильный восстановитель. При реакции с водой происходит взрыв, при длительном нахождении на воздухе полностью разрушается. Поэтому калий требует определённых условий для хранения – его заливают слоем керосина, силикона или бензина, для исключения вредных для металла контактов с водой и атмосферой.
Продукты питания богатые калием
Основными пищевыми источниками калия являются сушёные абрикосы, дыня, бобы, киви, картофель, авокадо, бананы, брокколи, печень, молоко, ореховое масло, цитрусовые, виноград, все зелёные овощи с листьями, листья мяты, семечки подсолнуха. Калия достаточно много в рыбе и молочных продуктах. Вообще, калий входит в состав почти всех растений. Яблочный уксус и мёд – чемпионы по содержанию калия.

Суточная потребность в калии
Суточная потребность организма человека в калии зависит от возраста, физического состояния и даже места проживания. Взрослым здоровым людям нужно 2,5г калия, беременным женщинам – 3,5г, спортсменам – до 5-ти грамм калия ежедневно. Количество необходимого калия для подростков рассчитывается по весу – 20 мг калия на 1 кг массы тела.
Полезные свойства калия и его влияние на организм
Калий вместе с натрием регулирует водный баланс в организме и нормализует ритм сердца, поддерживает концентрацию и физиологические функций магния.
Калий участвует в процессе проведения нервных импульсов и передачи их на иннервируемые органы. Способствует лучшей деятельности головного мозга, улучшая снабжение его кислородом. Оказывает положительное влияние при многих аллергических состояниях. Калий необходим для осуществления сокращений скелетных мышц. Калий регулирует содержание в организме солей, щелочей и кислот, чем способствует уменьшению отёков.
Калий содержится во всех внутриклеточных жидкостях, он необходим для нормальной жизнедеятельности мягких тканей (мышц, сосудов и капилляров, желез внутренней секреции и т.д.)
Усвояемость калия
Калий всасывается в организм из кишечника, куда поступает с пищей, выводится с мочой обычно в таком же количестве. Излишний калий выводится из организма тем же путём, не задерживается и не накапливается. Препятствиями для нормального всасывания калия могут послужить чрезмерное употребление кофе, сахара, алкоголя.
Взаимодействие с другими
Калий работает в тесном контакте с натрием и магнием, при росте концентрации калия из организма стремительно выводится натрий, а уменьшение количества магния может нарушить усвоение калия.

Признаки нехватки калия
Нехватка калия в организме характеризуется мышечной слабостью, быстрой утомляемостью, снижением иммунитета, сбоями в работе миокарда, нарушениями показателей артериального давления, учащённым и затруднённым дыханием. Кожные покровы могут шелушиться, повреждения плохо заживают, волосы становятся очень сухими и ломкими. Происходят сбои в работе желудочно-кишечного тракта – тошнота, рвота, расстройства желудка вплоть до гастрита и язвы.
Признаки избытка калия
Переизбыток калия наступает при передозировке препаратов, содержащих калий и характеризуется нервно-мышечными расстройствами, повышенной потливостью, возбудимостью, раздражительностью и плаксивостью. Человек постоянно испытывает чувство жажды, которое приводит к частым мочеиспусканиям. Желудочно-кишечный тракт реагирует кишечными коликами, чередованием запоров и поносов.
Применение калия в жизни
Калий в виде основных соединений находит широкое применение в медицине, сельском хозяйстве и промышленности. Калийные удобрения необходимы для нормального роста и вызревания растений, а всем известная марганцовка, это не что иное, как перманганат калия, испытанный временем антисептик.
Калий - элемент первой группы (по старой классификации - главной подгруппы первой группы), четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий - это мягкий щелочной металл серебристо-белого цвета.
3. Калий очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь.
4. Во многих свойствах калий очень близок натрию, но с точки зрения биологической функции и использования клетками живых организмов они антагонистичны.
5. Плотность калия меньше плотности воды и равна 0,8629 г/см3.
6. Как и все щелочные металлы, калий легко плавится (температура плавления 63,51°C) и начинает испаряться уже при сравнительно невысоком нагревании (температура кипения калия 761°C).
7. При нагревании на воздухе калий сгорает фиолетово-красным пламенем. С водой и разбавленными кислотами калий взаимодействует с взрывом (воспламеняется образующийся водород (H)): 2K + 2H2O = 2KOH + H2
8. В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах.
9. Кларк калия в земной коре составляет 2,4 % (5-й по распространённости металл, 7-й по содержанию в коре элемент). Концентрация в морской воде - 380 мг/л
11. Жидкий при комнатной температуре сплав калия и натрия используется в качестве теплоносителя в замкнутых системах, например, в атомных силовых установках на быстрых нейтронах. Кроме того, широко применяются его жидкие сплавы с рубидием и цезием. Сплав состава: натрий 12 %, калий 47 %, цезий 41 % - обладает рекордно низкой температурой плавления −78 °C. Соли калия широко используются в гальванотехнике, так как, несмотря на относительно высокую стоимость, они часто более растворимы, чем соответствующие соли натрия, и потому обеспечивают интенсивную работу электролитов при повышенной плотности тока.
12. Соединения калия - это важнейший биогенный элемент и потому применяются в качестве удобрений. Калий является одним из трех базовых элементов, которые необходимы для роста растений наряду с азотом и фосфором. В отличие от азота и фосфора, калий является основным клеточным катионом. При его недостатке у растения прежде всего нарушается структура мембран хлоропластов - клеточных органелл, в которых проходит фотосинтез. Внешне это проявляется в пожелтении и последующем отмирании листьев. При внесении калийных удобрений у растений увеличивается вегетативная масса, урожайность и устойчивость к вредителям.
13. Рекомендуемая суточная доля калия составляет для детей от 600 до 1700 миллиграммов, для взрослых - от 1800 до 5000 миллиграммов. Потребность в калии зависит от массы тела, физической активности, физиологического состояния, и климата места проживания
14. Металлический калий может вызвать очень сильные ожоги кожи, при попадании мельчайших частичек калия в глаза возникают тяжелые поражения с потерей зрения, поэтому работать с металлическим калием можно только в защитных перчатках и очках. Загоревшийся калий заливают минеральным маслом или засыпают смесью талька и NaCl. Хранят калий в герметично закрытых железных контейнерах под слоем обезвоженного керосина или минерального масла.
15. Многим известно такое вещество, как цианистый калий; но не многие знают, где его используют. А используют его для гальванического серебрения а также золочения неблагородных металлов, извлечения дорогостоящих металлов, а именно серебра и золота, из руд.
Ещё по теме:
На данный момент я уже лично посетил более 400 предприятий, а вот и ссылки на все мои промрепортажи:
Человеческий мозг непрерывно обучается. Нет разницы, чем мы занимаемся и какие конкретно действия повторяем день изо дня. Для прочного закрепления привычки требуется постоянное повторение и мозг обязательно обучится новому, даже претерпит изменения в своём физическом теле. Когда-то учёные начали узнавать наш мир. Они составляли причинно-следственные связи и удивлялись, открывая новые законы природы. Так, одной из задач для учёных стала тайна элемента калий — химический элемент, который важен для живых существ.
- История открытия
- Калий в природе
- Способы получения
- Физические свойства
- Химические характеристики
- Сфера применения

История открытия
Атомный номер калия 19, что указывает на его расположение в химической таблице Менделеева.
Примерная молярная масса 39,1 г/моль.
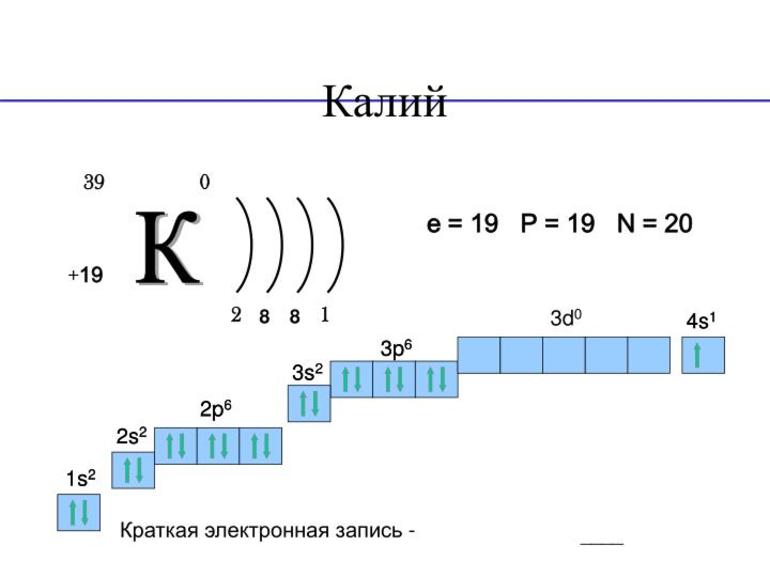
Электронная конфигурация калия 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1

Единственная возможная степень окисления +1 (плюс один).
На внешнем энергетическом уровне имеется всего 1 электрон. Это значит, что максимальная валентность элемента 1.
Кристаллическая решётка простого вещества кубическая объёмно-центрированная.
В 1807 году английский химик Х. Дэви опытным путём получил потассий (латинское название — потассиум). Именно так изначально был назван калий. Проводя электролиз каустической воды и расплавов поташа, учёный заметил образование мягкого легкоплавкого металла. Такое достижение подтолкнуло его к новым открытиям и он стал изучать химические и физические свойства нового вещества.
Калий в природе

После многолетних поисков выяснилось, что в природе калий не находится в чистом виде. Он один из десяти элементов, которые составляют большую часть окружающего мира.
- Сильвинита KCl·NaCl.
- Карналлита KCl·MgCl 2 ·6H 2 O.
- Каинита KCl·MgSO 4 ·6H 2 O.
- Зола растений как поташ K 2 CO 3.
Способы получения
Современные условия позволяют учёным получать калий несколькими способами.
Уравнение взаимодействия с жидким натрием расплавленного основания при 380−450°C или хлорида при 760- 890 °C: Na + KOH = NaOH + K
Электролиз расплава хлорида в смеси с карбонатом калия при температуре около 700 °C:
Физические свойства
Легкоплавкий металл серебристого цвета. При надрезе быстро образует оксидную плёнку после нескольких секунд контакта с кислородом, что объясняет требования особых условий содержания в помещениях. Хранится только в посуде с керосином, силиконами или бензином. Обладает хорошей растворимостью при соединении со ртутью. Образует амальгамы.
На соединение с водой реагирует взрывом. При поднесении горелки окрашивает пламя в розово-фиолетовый цвет.
Химические характеристики
Калий имеет много общего с натрием. Это обусловлено их расположением в периодической таблице химических элементов Д. И. Менделеева. Оба элемента — щелочные металлы, которые ярко выражают свои свойства. Однако у потассия металлические свойства проявляются сильнее, чем у натрия и кальция, но слабее, чем у рубидия.
Калию свойственно проявлять такие характеристики, которые делают его незаменимым для химической промышленности:
- Химически активен.
- Легко отдаёт электроны.
- Сильный восстановитель.
Оксиды или пероксиды
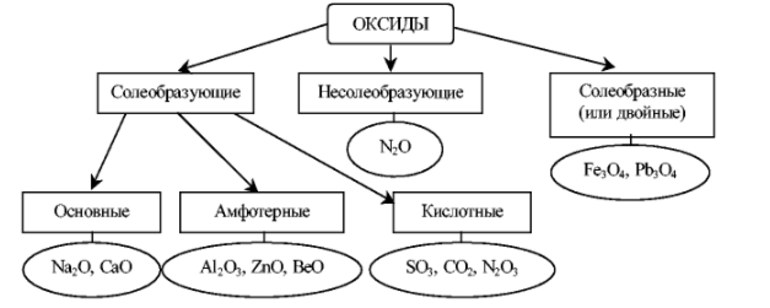
При взаимодействии с кислородом образует не оксид, а пероксид или супероксид, что заметно невооружённым глазом (очень быстро образует оксидную плёнку на поверхности).
Может образовать оксид только лишь при медленном нагревании до температуры меньше 180 °C при низком содержании кислорода в окружающей среде.
Оксиды ярко проявляют основные свойства. Как и сам металл, бурно реагируют с водой, кислотными оксидами и самими кислотами. Практического применения в промышленности они не нашли, используются для обучения в университетах.
Пероксиды — белые порошки с жёлтым тоном. Хорошо растворяются в воде, образуя щёлочи и пероксид водорода.
Сильные окислители, поэтому обрели популярность в текстильной промышленности как отбеливающее средство.
Гидроксиды калия
Гидроксиды калия и натрия имеют особые названия: едкий кали и едкий натри. Белые, твёрдые, непрозрачные вещества. Очень гигроскопичны, это значит, что быстро впитывают влагу и требуют особого внимания при работе с ними. Лаборанту необходимо надевать перчатки и защитные очки, иначе получит сильный ожог и раздражение слизистых оболочек. Кристаллы плавятся при температуре 360 °C. Гидроксиды относят к щелочам, они быстро растворяются в воде, выделяя большое количество тепла.
Сфера применения

Соединения калия используют в качестве удобрений, что свидетельствует о его ценных биологических характеристиках. Один из важнейших компонентов биосистемы вместе с азотом и фосфором. Помимо этого, необходим обмен элемента в натриево-калиевом насосе клетки любого живого организма.
Большую популярность приобрел в гальванотехнике. Соли металла быстро растворяются, по сравнению с солями натрия. Это свойство позволяет устанавливать высокие цены компаниям, которые занимаются обработкой калия.
Жидкий сплав калия и натрия используется в качестве теплоносителей в атомных установках. Необходимое условие: комнатная температура.
Особые соединения калия

Бромид используется в фармацевтике для изготовления успокоительных лекарств.
Карбонат, хлорид и нитрат пользуются популярностью у садоводов, так как представляют собой удобрения, обогащённые большим количеством полезных микроэлементов.
Перманганат применяется в химических лабораториях для получения кислорода, а также ранее широко применялся в быту благодаря своим антисептическим свойствам.
Пероксид и супероксид обеспечивают регенерацию воздуха на подводных лодках и противогазах, благодаря своей способности поглощать углекислый газ и выделять кислород.

Из описания характеристик калия с другими элементами становится понятно, что это крайне важная составляющая организма, которая должны взаимодействовать с другими металлами и неметаллами, чтобы обеспечить гармоничный рост и развитие организма. Норма потребления этого элемента для человека — 2040 мг в сутки.
Роль этого металла и реакций организма, в которых он принимает участие, имеют большое значение для строения клеток, из которых состоит любой живой организм. Благодаря образованию различных химических связей, калий помог человечеству добиться новых вершин в кораблестроении, садоводстве, фармацевтической промышленности.
Повсеместное нахождение в природе позволяет добывать металл и его соединения беспрерывно, а благодаря успехам учёных в области химии возможно регулировать плотность содержания калия в препаратах. При соблюдении правильных пропорций и составлении схем алгоритмов можно предугадать пользу или вред.
Калий может быть полезным, но также он способен обрекать людей на тяжкие мучения, такие как: ожоги рук, раздражение слизистых оболочек. Об этом следует помнить всем, кто стремится узнать больше о свойствах этого металла. Прежде чем начинать работу с опасными веществами, лучше узнать всё о многолетнем опыте предшественников, чтобы избежать печальных и необратимых последствий.
Читайте также:

