Злокачественные опухоли кроветворной ткани реферат
Обновлено: 06.07.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Лейкоз: причины появления, симптомы, диагностика и способы лечения.
Определение
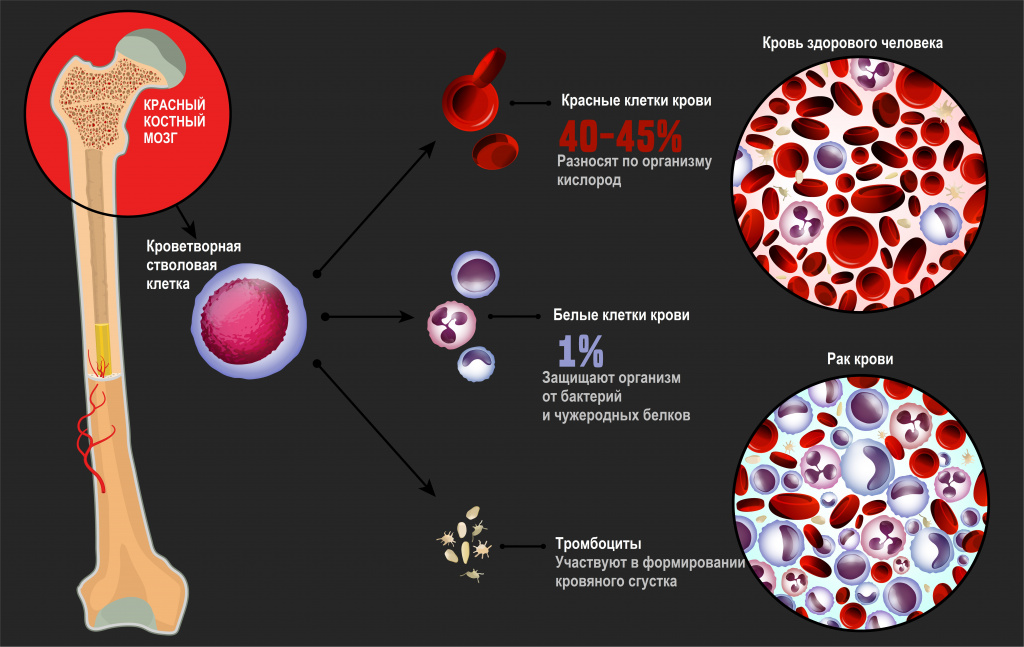
Лейкозы – большая группа заболеваний кроветворной системы. Кроветворение (гемопоэз) – это многоэтапный процесс образования форменных элементов крови в специализированных органах кроветворения. К форменным элементам крови относятся лейкоциты (белые кровяные тельца), которые участвуют во врожденном и приобретенном иммунитете, эритроциты (красные кровяные тельца), которые осуществляют транспорт кислорода и углекислого газа, и тромбоциты, обеспечивающие свертываемость крови.
Главный орган, где располагаются полипотентные стволовые клетки, - костный мозг, который как раз и поражается при лейкозах.
В результате повреждения (мутации) в генетическом материале полипотентной стволовой клетки-предшественницы нарушается процесс созревания клеток. При остром лейкозе возникает большое количество незрелых (бластных) клеток, из которых образуется опухоль, разрастается в костном мозге, замещает нормальные ростки кроветворения и имеет тенденцию к метастазированию – распространению с током крови или лимфы в здоровые органы. При хронических лейкозах заболевание течет годами, происходит частичная задержка созревания клеток и опухоль образуется из созревающих и зрелых клеток.
Причины возникновения лейкозов
К факторам риска развития лейкоза относятся:
- ионизирующая радиация: лучевая терапия по поводу других опухолей, облучение на рабочем месте, ультрафиолетовое излучение;
- воздействие на организм химических канцерогенных веществ;
- некоторые вирусы: HTLV (Т-лимфотропный вирус человека);
- бытовые факторы: добавки в пищевые продукты, курение, плохая экологическая обстановка;
- наследственная предрасположенность к раковым заболеваниям.
Лейкозы подразделяют на острые и хронические, а по типу поражения ростка кроветворения - на лимфоидные и миелоидные. Острый лейкоз никогда не переходит в хронический, а хронический не может стать острым (но его развитие может перейти в стадию бластного криза).
В зависимости от преобладания тех или иных опухолевых клеток выделяют бластные, цитарные и недифференцированные лейкозы.
Острый лимфобластный лейкоз (ОЛЛ) диагностируется у лиц любого возраста, начиная с младенческого и заканчивая пожилым, однако пик заболеваемости приходятся на детский возраст (60% пациентов с ОЛЛ моложе 20 лет). Острый лимфобластный лейкоз – самая распространенная опухоль кроветворной ткани у детей, которая составляет 30% всех злокачественных опухолей детского возраста. Заболеваемость ОЛЛ у пациентов пожилого возраста неуклонно возрастает: так, ежегодная частота ОЛЛ увеличивается с 0,39 случая на 100 тыс. населения в возрасте 35–39 лет, до 2,1 случая на 100 тыс. населения в возрасте ≥85 лет. Кроме того, приблизительно 30% ОЛЛ диагностируются в возрасте ≥60 лет.
Острым миелоидным лейкозом (ОМЛ) страдает в среднем 3-5 человек на 100 тыс. населения в год. Заболеваемость резко возрастает в возрасте старше 60 лет и составляет 12–13 случаев на 100 тыс. населения у лиц в возрасте старше 80 лет.
Хронический лимфобластный лейкоз (ХЛЛ) – самый частый вид лейкозов у взрослых, в то время как у детей этот вид опухоли не регистрируется. В европейских странах его частота составляет 4 случая на 100 тыс. населения в год и непосредственно связана с возрастом. У лиц старше 80 лет она составляет более 30 случаев на 100 тыс. в год.
Хронический миелолейкоз (ХМЛ) – редкое заболевание: 0,7 на 100 тыс. взрослого населения, пик заболеваемости приходится на 50-59 лет, однако до 33% больных ОМЛ - люди моложе 40 лет.
Симптомы лейкозов
Острый лейкоз в большинстве случаев дебютирует резко - внезапно повышается температура, появляются озноб, боль в горле, в суставах, отмечается резко выраженная слабость. Реже острый лейкоз может проявиться кровотечением. Иногда острый лейкоз начинается с постепенного ухудшения состояния больного, появления невыраженной боли в суставах и костях, кровоточивости. В единичных случаях возможно бессимптомное начало заболевания. У многих больных увеличиваются лимфоузлы и селезенка.
При хроническом лейкозе на начальной стадии, которая длится от года до трех лет, пациенты могут ни на что не жаловаться. Иногда беспокоят слабость, потливость, частые простудные заболевания, могут отмечаться тупые, ноющие боли в костях.
При подавлении эритроидного ростка, дающего красные кровяные тельца, возникает анемия и гемическая гипоксия (снижение количества кислорода в крови). При этом пациенты отмечают слабость, утомляемость, бледность кожных покровов.
При поражении мегакариоцитарного ростка падает количество тромбоцитов, поэтому возникает кровоточивость десен, слизистой оболочки носа, пищеварительного тракта, образуются синяки, кровоизлияния в различные органы. При прогрессировании лейкоза могут развиваться массивные кровотечения в результате ДВС синдрома (синдрома диссеминированного внутрисосудистого свертывания).
В результате недостатка лейкоцитов и снижения иммунитета развиваются инфекционные осложнения различной степени тяжести, что чаще всего проявляется лихорадкой.
Могут возникать язвенно-некротическая ангина, перитонзиллярные абсцессы, некротический гингивит, стоматит, пиодермия, параректальные абсцессы, пневмония, пиелонефрит. Существует значимый риск тяжелого течения инфекционных осложнений вплоть до развития сепсиса.
С током крови и лимфы опухолевые клетки попадают в здоровые органы, нарушают их структуру и функцию - наиболее подвержены метастатическим процессам печень, селезенка, лимфатические узлы, но метастазы могут поражать и кожу, и мозговые оболочки, и почки, и легкие.
Основные причины летальности у пациентов с лейкозом связаны с тем, что осложнения могут спровоцировать развитие сепсиса, полиорганную недостаточность, кровоизлияния в различные органы. Острый лейкоз без лечения приводит к смертельному исходу в течение нескольких недель или месяцев.
Диагностика лейкозов
Диагностика лейкозов основывается на оценке морфологических особенностей клеток костного мозга и периферической крови. Поэтому всем пациентам с подозрением на лейкоз назначают общий анализ крови с подсчетом лейкоцитарной формулы и определением числа тромбоцитов.
Клинический анализ крови – одно из основных лабораторных исследований для количественной и качественной оценки всех классов форменных элементов крови. Включает цитологическое исследование мазка крови с подсчетом процентного содержания разновидностей лейкоцитов (определение общего количества лейкоцитов и процентного соотношения основных субпопуляций лейкоцитов: нейтрофилов, лимфоцитов, моноцитов, эозинофилов и базофилов) и определение скорости оседания эритроцитов.
Для определения объема опухолевого поражения, вероятности развития синдрома лизиса опухоли рекомендовано выполнение общетерапевтического биохимического анализа крови: АСТ, АЛТ, общий билирубин, глюкоза, мочевина, креатинин, общий белок, ЛДГ, магний, натрий, калий, кальций.
Определение уровня АЛТ в сыворотке крови применяют преимущественно в диагностике и контроле течения болезней печени, а также в комплексных биохимических исследованиях.
Определение уровня АСТ в сыворотке крови используют преимущественно в диагностике и контроле течения болезней печени, а также в комплексных биохимических исследованиях.
Определение уровня билирубина в сыворотке крови используют для выявления поражений печени различного происхождения, закупорки желчных путей, гемолитической анемии, желтухи новорожденных.
Глюкоза – основной источник энергии для метаболических процессов в организме человека, является обязательным компонентом большинства внутриклеточных структур, участвует в синтезе нуклеиновых кислот (рибоза, дезоксирибоза), образует соединения с белками (гликопротеиды, протеогликаны) и липидами (гликолипиды).
Мочевина – конечный продукт расщепления белковых молекул, выводимый из организма почками. Определение уровня мочевины в сыворотке крови используют для оценки выделительной функции почек и контроля эффективности лечения пациентов с почечными заболеваниями.
Креатинин – продукт метаболизма мышечных клеток, удаляется из крови почками. Тест используют в качестве маркера функции почек для диагностики и мониторинга острых и хронических болезней почек, а также в скрининговых обследованиях.
Общий белок выступает показателем белкового обмена, отражающим содержание всех фракций белков в сыворотке крови. Тест используется в комплексных биохимических обследованиях пациентов при различных заболеваниях.
Лактатдегидрогеназа – гликолитический фермент, участвующий в конечных этапах превращений глюкозы. Тест используют в диагностике различных заболеваний (сердца, печени, мышц, почек, легких, системы крови).
Магний – один из основных катионов организма. Исследование магния в сыворотке крови в комплексе с другими электролитами используют для выявления нарушений электролитного баланса.
Определение уровня калия, натрия и хлора в сыворотке крови используется для скрининга электролитов и исследования кислотно-щелочного дисбаланса.
Общий кальций – основной компонент костной ткани и важнейший биогенный элемент, обладающий важными структурными, метаболическими и регуляторными функциями в организме.
Для определения вероятности развития тяжелых коагуляционных нарушений (как геморрагических, так и тромботических) рекомендовано исследование свертывающей системы крови.
Базовый набор тестов, применяемый для скрининговой оценки состояния свертывающей системы крови.
С целью исключения поражения почек выполняют общий анализ мочи.
Общий анализ мочи – комплексная оценка ряда физических и химических параметров мочи, а также элементов мочевого осадка, нацеленное на выявление патологии почек и мочевыводящих путей.
Диагностику хронического лейкоза проводят с помощью иммунофенотипического исследования лимфоцитов крови (ИФТ) методом проточной цитометрии.
Рекомендовано проведение стернальной пункции (пункции грудины) для получения цитологического препарата костного мозга и цитологическое и цитохимическое исследование мазка с целью уточнения диагноза и определения прогноза.
В ряде случаев показана биопсия опухолевого образования или лимфатического узла (или другого метастатического очага) и патологоанатомическое исследование полученного биопсийного материала.
Кроме того, врач может рекомендовать проведение иммунофенотипирования гемопоэтических клеток-предшественниц в костном мозге, цитогенетическое исследование аспирата костного мозга, молекулярно-генетические исследования мутаций в генах и др.
Из инструментальных методов диагностики проводятся:
-
эхокардиография для оценки функционального состояния сердечной мышцы;
Исследование, позволяющее оценить функциональные и органические изменения сердца, его сократимость, а также состояние клапанного аппарата.
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
Исследование, позволяющее получить данные о состоянии органов грудной клетки и средостения.
Сканирование внутренних органов брюшной полости для оценки его функционального состояния и наличия патологии.
Лечение лейкозов
Лечение лейкозов проводится в стационаре. Медикаментозное воздействие на опухоль специальными препаратами, губительно действующими на быстро делящиеся клетки, называется химиотерапией. При лечении острых лейкозов химиотерапию проводят в несколько этапов: индукция ремиссии, консолидация (закрепление) ремиссии, поддерживающая терапия и профилактика нейролейкемии (метастазирования опухолевых лейкозных клеток в головной и спинной мозг).
Период индукции ремиссии - это начальный этап, цель которого максимально уменьшить опухолевую массу и достичь ремиссии. Обычно для этого требуется 1-2 курса химиотерапии. Далее идет консолидация достигнутого эффекта - наиболее агрессивный и высокодозный этап лечения, задачей которого является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток. Этот этап также занимает 1-2 курса. За ним следует противорецидивное или поддерживающее лечение. При некоторых вариантах острых лейкозов требуется профилактика или, при необходимости, лечение нейролейкемии.
Для разных видов лейкозов у разных возрастных групп профессиональными сообществами разработаны схемы химиотерапии.
При лечении ХМЛ основными препаратами выбора являются ингибиторы тирозинкиназы, применяемые в непрерывном режиме – ежедневно, длительно, постоянно. Перерывы в приеме могут способствовать снижению эффективности терапии и прогрессированию заболевания. В случае неэффективности терапии может быть проведена трансплантацию гемопоэтических стволовых клеток или костного мозга.
В терапии ХЛЛ цели и схемы терапии химиотерапии определены возрастом пациента, числом и тяжестью сопутствующих заболеваний. Разработаны протоколы лечения для разных пациентов, в том числе схемы моно- и полихимиотерапии. Для профилактики инфекционных осложнений применяют внутривенное введение иммуноглобулина, рекомендована вакцинация от гриппа и пневмококковой инфекции.
Помимо химиотерапии пациенту может потребоваться трансфузионная терапия: переливание эритроцитарной массы, тромбоцитарной массы, изотонических растворов.
При присоединении инфекций показана антибиотикотерапия. На фоне лечения могут возникать тромботические осложнения, что требует антикоагулянтной терапии. Пациентам высокого риска в связи с вероятностью рецидива лейкоза применяют трансплантацию гемопоэтических стволовых клеток.
Профилактика лейкозов
Так как причины возникновения лейкозов не установлены, методов специфической профилактики до сих пор не существует.
Однако доказано, что между курением и риском развития острого лейкоза существует дозовая зависимость, которая особенно очевидна для лиц старше 60 лет.
Ряд исследователей предполагают, что около 20% случаев ОМЛ являются следствием курения.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Опухоли кроветворной и лимфоидной тканей составляют приблизительно 8% от всех злокачественных новообразований, и все вместе входят в число 6 самых частых видов злокачественных заболеваний.
Предлагаем Вашему вниманию краткий, но очень подробный обзор онкологических заболеваний кроветворной системы.
Филиалы и отделения, где лечат злокачественные заболевания крови
Отдел лекарственного лечения опухолей
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
тел: 8 (494) 150 11 22
Отдел лекарственного лечения злокачественных новообразований
Заведующая отделом, д.м.н. ФАЛАЛЕЕВА Наталья Александровна
тел: 8 (484) 399 – 31-30
Злокачественные заболевания крови (современное обозначение: опухоли кроветворной и лимфоидной тканей ,онкогематологические заболевания , устаревшее название – гемобластозы , в бытовом понимании -рак крови ) – эти понятия объединяют различные по своим клиническим и биологическим свойствам, прогнозу и подходам к лечению заболевания, общим для которых является происхождение из той или иной клетки крови, находящейся на том или ином этапе развития. Иными словами, в организме здорового человека клетки-родоначальницы кроветворения непрерывно образуются новые клетки крови, такой процесс образования, развития и созревания клеток крови — лейкоцитов, эритроцитов, тромбоцитов носит название гемопоэз.

Существующие классификационные системы опухолей лимфоидной и кроветворной тканей основываются на детальной иммуноморфологической характеристике опухоли, подкрепленной в ряде случаев дополнительной информацией о генетической и молекулярной ее структуре.
Иммунофенотипирование при лейкозе или лимфоме

– необходимый диагностический этап при остром лейкозе или лимфоме. Это комплексная характеристика типа клеток. С использованием иммунологических методов возможно выявление особых структур, антигенов, на поверхности клетки (как правило, белковых молекул, так называемых CD (claster differentiation), кластер дифференцировки). Комплекс данных антигенов составляет иммунологический фенотип (иммунофенотип) на основании которого каждая клетка может быть отнесена к определенному классу: негемопоэтическая, гемопоэтическая, миелоидная, лимфоидная, T-клетка, В-клетка, клетка-предшественник. В соответствии с иммунофенотипом определяется иммунологический вариант заболевания, что является принципиальным для выбора правильной терапии на этапе диагноза.
Цитогенетический метод исследования крови
в настоящее время входит в перечень необходимых диагностических мероприятий при большинстве онкогематологических заболеваний. Данный метод позволяет:
• Провести точную диагностику большинства опухолевых заболеваний системы крови.
• Определить прогноз заболевания.
• Использовать таргетную (точечную, прицельную терапию) при обнаружении определенных цитогенетических перестроек.
В основе развития онкогематологических заболеваний лежат перестройки (поломки) генетического материала в клетках кроветворной и лимфоидной тканей. Эти события приводят к трансформации нормальных кроветворных клеток в опухолевые. Они не затрагивают другие клетки организма (в т.ч. половые клетки). По этой причине онкогематологические заболевания, за редким исключением, не передаются по наследству. Хромосомные перестройки можно обнаружить при помощи стандартного цитогенетического исследования или более чувствительного метода – интерфазного анализа с использованием зондов (маркеров) к конкретным участкам хромосом (метод FISH). В ряде случаев цитогенетические изменения могут происходить на субмикроскопическом уровне (т.к называемые точечные мутации). Такие изменения возможно детектировать только с помощью ультратонких высокочувствительных методов молекулярного исследования (метод ПЦР- полимеразная цепная реакция).
Чем продиктована необходимость проведения молекулярно-цитогенетических исследований у онкогематологических больных? В настоящее время хорошо изучен ряд цитогенетических изменений, являющихся уникальными специфическими маркерами для различных вариантов опухолевых заболеваний системы крови. Их обнаружение является достоверным критерием диагноза. Яркими примерами могут служить транслокация t(9:22) или филадельфийская хромосома, присутствующая во всех случаях хронического миелолейкоза; транслокация t(15;17) - при остром промиелоцитарном лейкозе, транслокация t(8;14) – при лимфоме Беркитта. Кроме того, расшифровка цитогенетических событий привела к созданию таргетных препаратов, которые в отличие от химиопрепаратов обладают селективным действием на опухолевые клетки. Так, использование иматиниба при обнаружении филадельфийской хромосомы кардинально изменило прогноз хронического миелолейкоза.
В ходе больших международных исследований было обнаружено различное течение онкогематологических заболеваний в зависимости от обнаружения тех или иных хромосомных перестроек или мутаций генов. Известны изменения, ассоциированные с благоприятным, промежуточным или неблагоприятным агрессивным течением заболевания. Таким образом, молекулярно-цитогенетические характеристики являются предикторами прогноза. На этой основе при различных онкогематологических заболеваниях на ряду с другими признаками разрабатываются программы терапии разной интенсивности (риск-адаптированная терапия).
Среди опухолей кроветворной и лимфоидной тканей различают лимфомы и лейкозы. Исторически сложилось разделение лимфоидных опухолей (лимфом) на лимфому Ходжкина и неходжкинские лимфомы. Неходжкинские лимфомы в зависимости от клеточной линии подразделяются на В-клеточные, Т- и NK-клеточные опухоли. На сегодняшний день на основании морфоиммунологических и генетических характеристик выделяется несколько десятков видов неходжкинских лимфом, для многих из которых созданы обособленные терапевтические программы. Лейкозы представляют собой разнородную группу заболеваний, делятся на острые и хронические в зависимости от субстрата опухоли: при острых лейкозах основная масса клеточного субстрата представлена незрелыми клетками (бластами ), при этом блок дифференцировки происходит очень рано, на этапе клеток-родоначальниц кроветворения, в отличие от хронических лейкозов, где опухолевые клетки представлены зрелыми и созревающими элементами. Также принципиально важным является деление лейкозов на миелоидные и лимфоидные, что возможно только при проведении качественного морфо- цитохимического, иммунофенотипического и молекулярно-генетического исследований клеток крови еще до начала лечения.
Опухоли кроветворной и лимфоидной тканей составляют приблизительно 8% от всех злокачественных новообразований, и все вместе входят в число 6 самых частых видов злокачественных заболеваний. Уровень смертности при этом значительно снизился в последнее два десятилетии, что является следствием появления новых высоко эффективных программ лечения.
Филиалы и отделения Центра, в которых лечат злокачественные заболевания кроветворной системы
Заведующая отделом, д.м.н. ФАЛАЛЕЕВА Наталья Александровна
8 (484) 399 – 31-30, г. Обнинск, Калужской области
Заведующий отделом, д.м.н. ФЕДЕНКО Александр Александрович
Согласно Международной гистологической и цитологической классификации опухолевых заболеваний кроветворной и лимфоидной тканей, в основу которой положен клеточный состав новообразований и характер распространения, опухоли системы крови, или гемобластозы, делят на две группы:
— лейкозы (лейкемии) — системные опухолевые заболевания кроветворной ткани;
— лимфомы — регионарные опухолевые заболевания кроветворной и/или лимфоидной ткани.
Такое деление является в значительной степени условным, поскольку ограниченный опухолевый рост и диффузная опухолевая инфильтрация могут иметь место одновременно или последовательно у одного больного.
Лейкемии и лимфомы, включая лимфому Ходжкина, составляют приблизительно 8% от всех злокачественных новообразований и все вместе входят в число 6 самых частых видов злокачественных опухолей. В США каждый год лейкемиями заболевает около 25000 человек, из них умирает 15000-20000. Уровень смертности в последнем десятилетии резко снизился в результате повышения эффективности терапии. Острые лейкемии составляют около 50-60% от всех лейкемий, причем острая миелобластная лейкемия встречается несколько чаще, чем острая лимфобластная лейкемия. Хронические лейкемии составляют около 40-50% от всех лейкемий, причем хроническая лимфоцитарная лейкемия встречается несколько чаще, чем хроническая миелоцитарная лейкемия (рис. 16.1).
Монобластная лейкемия подразделяется на два типа лейкемий: острую монобластную (тип Шиллинга) и острую миеломонобластную (тип Нигели). Не существует хронических форм лейкемий данного типа.
А. Острая моноцитарная (монобластная) лейкемия характеризуется пролиферацией монобластов. Они могут быть отдифференцированы от других бластов только при использовании цитохимических маркеров (табл. 16.2).
Б. Острая миеломоноцитарная лейкемия характеризуется наличием бластов, которые имеют признаки миелобластов и монобластов как морфологически, так и цитохимически.
Выделение подтипов лейкозов (лейкемий), согласно предложенной классификации, отражающей уровень блока дифференцировки бластов, является очень важным для клиники, поскольку каждый тип имеет свою специфическую схему лечения.
Главная цель обучения — уметь определять клинико-морфологические проявления опухолей кроветворной ткани, объяснить вероятные причины и механизм развития, оценить исход и определить значение осложнений для организма.
Для чего необходимо уметь:
— определить видимые макро- и микроскопически проявления подтипов острых и хронических лейкозов (лейкемий), объяснить механизм развития, исход и оценить их значение;
— определить видимые макро- и микроскопически проявления ходжкинских и неходжкинских лимфом, объяснить механизм развития, исход и оценить их значение;
Лейкемия (лейкоз) — это системное прогрессирующее разрастание незрелой опухолевой ткани в органах кроветворения с гематогенным распространением в другие органы и ткани.
Характерной особенностью лейкозов является быстрая диссеминация (распространение) опухолевых клеток по системе кроветворения. Вследствие этого, уже на ранних этапах заболевание приобретает системный характер. Наряду с костным мозгом наиболее часто наблюдается поражение селезенки, лимфатических узлов, лимфатических образований (Пейеровы бляшки, солитарные лимфоидные фолликулы) по ходу желудочно-кишечного тракта, печени и других органов. Объем лейкозных разрастаний и их распространенность в организме могут быть различными в зависимости от формы лейкоза, стадии болезни, проведенного лечения. Эти лейкозные разрастания называют лейкемический инфильтрат.
Этиология. Причина многих случаев лейкемий остается неизвестной. Но, поскольку опухолевая природа лейкозов не вызывает сомнения, вопросы этиологии лейкозов и опухолей, по-видимому, однотипны. Лейкозы — полиэтиологические заболевания. В возникновении их могут быть повинны различные факторы, способные вызвать мутацию клеток кроветворной ткани. Среди этих факторов следует отметить следующие:
Вирусы. Предполагают, что вирусы, которые вызывают лейкемию у животных, могут вызывать ее и у человека. Впервые было описано в Японии, что ретровирус (человеческий Т-лимфотропный вирус I типа [HTLV-I]) является причиной возникновения одного из типов Т-лимфоцитарной лейкемии у человека. Доказано также, что родственный вирус, HTLV-II, является причиной многих типов хронических Т-клеточных лейкемий.
Ионизирующее излучение стало причиной многочисленных случаев лейкемии у первых радиологов и жителей Хиросимы и Нагасаки после атомной бомбардировки. Доказано повышение заболеваемости лейкемией у детей при внутриутробном облучении, а также развитие ее у больных, которые получали лучевую терапию при лечении анкилозирующего спондилита и болезни Ходжкина.
Химические вещества. Описаны случаи, когда причиной лейкемий были мышьяк, бензол, фенилбутазон и хлорамфеникол. Те же самые цитотоксические лекарства, которые используются для лечения опухолей, могут стать причиной развития лейкемий.
При аплазии костного мозга любой этиологии увеличивается предрасположенность к возникновению лейкемий.
Иммунодефицитные состояния. Возникновение лейкемий при иммунодефицитах связано со снижением иммунного надзора, что приводит к нарушению разрушения потенциально неопластических гемопоэтических клеток.
Генетический фактор. Нарушения структуры хромосом довольно часто обнаруживаются у больных с лейкемиями. Первым подтверждением данного факта стала находка Филадельфийской хромосомы (маленькая 22 хромосома, образующаяся в результате взаимной транслокации генетического материала между 22 и 9 хромосомами) при хронической миелоцитарной лейкемии. Представляет интерес тот факт, что у детей с синдромом Дауна (трисомия по 21 хромосоме) в 20 раз выше риск заболевания лейкемией. Также риск увеличивается при заболеваниях, связанных с нестабильностью хромосом (синдром Блюма, анемия Фанкони).
Лейкозы (лейкемии) классифицируются по нескольким характеристикам:
По клиническому течению:
1. Острые лейкозы (лейкемии) — начинаются остро, быстро прогрессируют, при отсутствии лечения приводят к смерти в течение нескольких месяцев. В крови обычно определяется большое количество бластных клеток.
2. Хронические лейкозы (лейкемии) начинаются постепенно и медленно прогрессируют, даже при отсутствии лечения больные могут прожить несколько лет. В крови выявляются обычно незрелые, но с тенденцией к созреванию клетки.
По гисто- (цито-) генезу, характеру и направлению дифференцировки разрастающихся клеток:
Среди острых лейкозов выделяют:
Среди хронических лейкозов в зависимости от ряда созревающих клеток гемопоэза выделяют лейкозы миелоцитарного, лимфоцитарного и моноцитарного происхождения:
1. Лейкозы миелоцитарного происхождения:
— хронический миелоидный лейкоз;
— истинная полицитемия Вакеза-Ослера и др.
2. Лейкозы лимфоцитарного происхождения:
— хронический лимфоидный лейкоз;
— лимфоматоз кожи (болезнь Сезари);
— парапротеинемические лейкозы (миеломная болезнь, первичная макроглобулинемия Вальденстрема, болезнь тяжелых цепей Франклина).
3. Лейкозы моноцитарного происхождения:
— хронический моноцитарный лейкоз;
По картине периферический крови:
1. Лейкемические, которые характеризуются значительным увеличением количества лейкоцитов, в том числе и лейкозных клеток, в периферической крови (десятки и сотни тысяч, иногда до миллиона в 1 мкл крови). Это наиболее частая форма.
2. Сублейкемические, при которых количество лейкоцитов несколько выше нормы (15-25 тысяч в 1 мкл крови), но в крови определяются опухолевые клетки.
3. Алейкемические, при которых количество лейкоцитов в пределах нормы, в крови не определяются опухолевые клетки. Этот тип наблюдается редко, но он возникает обычно уже на ранних этапах заболевания. С целью диагностики используют трепанобиопсию крыла подвздошной кости или пунктат костного мозга грудины.
4. Лейкопенические, при которых количество лейкоцитов ниже нормы, иногда может достигать одной тысячи, но могут быть качественные изменения, обусловленные появлением лейкозных клеток.
Клиника и морфология лейкозов зависит от степени зрелости и гистогенеза клеток.
Острые лейкемии характеризуется острым началом (высокая лихорадка, явления тяжелой интоксикации) и быстрой прогрессией заболевания. Заболевание встречается во всех возрастных группах, включая детей и лиц пожилого возраста. Наиболее частыми формами острых лейкозов являются острый лимфобластный лейкоз (лейкемия) и острый миелобластный лейкоз (лейкемия). Острая лимфобластная лейкемия в основном встречается в раннем детском возрасте (пик в 3-4 года). Острая миелобластная лейкемия встречается в любом возрасте, но наиболее часто у подростков (пик в 15-20 лет). Острые лейкемии характеризуются пролиферацией бластов без признаков дифференцирования. Для острого недифференцированного лейкоза характерна инфильтрация всех органов кроветворения и паренхиматозных органов недифференцированными однородного вида мелкими, круглыми, гиперхромными клетками гемопоэза I-II классов (то есть полипотентными клетками-предшественниками и частично детерминированными клетками-предшественниками миело - и лимфопоэза). Острый недифференцированный лейкоз протекает как септическое заболевание. И при миелобластной, и при лимфобластной лейкемиях в периферической крови определяется лейкоцитоз (увеличение количества лейкоцитов) с наличием бластов. При остром лейкозе в периферической крови находят так называемый лейкемический провал (hiatus leucemicus) — резкое увеличение бластных клеток и единичные зрелые элементы при отсутствии переходных созревающих форм. Иногда количество лейкоцитов может быть не увеличено, но бласты обязательно присутствуют. Очень редко в крови отсутствуют и бласты (алейкемическая лейкемия). Однако в пунктате костного мозга изменения находят при любых формах лейкемий. Отмечается диффузное поражение ткани костного мозга, опухолевые клетки вытесняют другие гемопоэтические ростки и жировую ткань. Костный мозг губчатых и трубчатых костей при лимфобластной лейкемии на всем протяжении становится сочным, малиново-красным (вид малинового желе). При миелобластной лейкемии он приобретает зеленоватый (гноевидный) оттенок, поэтому его называют пиоидный костный мозг. При острой лимфобластной лейкемии и острой моноцитарной лейкемии часто наблюдается увеличение лимфатических узлов, при острой миелобластной лейкемии оно обычно отсутствует. Увеличение селезенки относительно небольшое (по сравнению с хроническими формами лейкоза), масса ее достигает 500-600 граммов.
В крови пациентов наблюдается снижение количества других форменных элементов из-за вытеснения этих ростков неопластическими клетками. В результате возникает анемия, которая обычно тяжелая и быстро развивающаяся, проявляется бледностью кожных покровов и симптомами гипоксии. Тромбоцитопения (снижение количества тромбоцитов) приводит к возникновению петехиальных кровоизлияний (геморрагический диатез). В основе развития геморрагического диатеза лежит также повышение проницаемости сосудистой стенки, которое обусловлено малокровием и интоксикацией. Нейтропения (снижение количества нейтрофильных лейкоцитов) проявляется в виде частых инфекционных заболеваний и изъязвлений (некроз) на слизистых оболочках. Некрозы чаще всего развиваются в слизистой полости рта, миндалин (некротическая ангина), желудочно-кишечного тракта. Иногда могут возникать инфаркты селезенки. Причиной некрозов могут служить лейкемические инфильтраты, которые суживают просвет сосудов. Резкое снижение иммунитета и общей реактивности организма сопровождается активацией инфекций и развитием альтеративного воспаления.
У больных с промиелобластной лейкемией может развиться синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром), т.к. в гранулах опухолевых клеток содержится обилие тромбопластических веществ, которые в большом количестве попадают в кровоток при гибели клеток.
В печени при всех формах острого лейкоза разрастания бластных клеток могут локализоваться как в области портальных трактов, так и по ходу синусоидных капилляров, что сопровождается деструкцией печеночных балок, дистрофическими изменениями гепатоцитов, вплоть до их очагового некроза.
При поражении кожи очаговые лейкозные пролифераты располагаются в поверхностных и глубоких слоях дермы, преимущественно вокруг сосудов, волосяных фолликулов и потовых желез. Это может сопровождаться некрозом и изъязвлением эпидермиса.
Лечение больных предусматривает применение цитостатических препаратов и антибиотиков.
Согласно Международной гистологической и цитологической классификации опухолевых заболеваний кроветворной и лимфоидной тканей, в основу которой положен клеточный состав новообразований и характер распространения, опухоли системы крови, или гемобластозы, делят на две группы:
лейкозы (лейкемии) – системные опухолевые заболевания кроветворной ткани;
лимфомы – регионарные опухолевые заболевания кроветворной и/или лимфоидной ткани.
Такое деление является в значительной степени условным, поскольку ограниченный опухолевый рост и диффузная опухолевая инфильтрация могут иметь место одновременно или последовательно у одного больного.
Лейкемии и лимфомы, включая лимфому Ходжкина, составляют приблизительно 8% от всех злокачественных новообразований и все вместе входят в число 6 самых частых видов злокачественных опухолей. Острые лейкемии составляют около 50-60% от всех лейкемий, причем острая миелобластная лейкемия встречается несколько чаще, чем острая лимфобластная лейкемия. Хронические лейкемии составляют около 40-50% от всех лейкемий, причем хроническая лимфоцитарная лейкемия встречается несколько чаще, чем хроническая миелоцитарная лейкемия (рис. 1).

Рис. 1. Заболеваемость различными видами лейкемий в зависимости от возраста
ОЛЛ – острая лимфобластная лейкемия;
Рекомендуемые материалы
Презентация № 7 по теме Болезни системы кровообращения как медико-социальная проблема (Общественное здоровье и здравоохранение)
ХЛЛ – хроническая лимфоцитарная лейкемия;
ОМЛ – острая миелобластная лейкемия;
ХМЛ – хроническая миелоцитарная лейкемия.
Монобластная лейкемия подразделяется на два типа лейкемий: острую монобластную (тип Шиллинга) и острую миеломонобластную (тип Нигели). Не существует хронических форм лейкемий данного типа.
Острая моноцитарная (монобластная) лейкемия характеризуется пролиферацией монобластов. Они могут быть отдифференцированы от других бластов только при использовании цитохимических маркеров (табл. 2).
Острая миеломоноцитарная лейкемия характеризуется наличием бластов, которые имеют признаки миелобластов и монобластов как морфологически, так и цитохимически.
Цитохимическая идентификация острых лейкемий
Множеств. ядрышки, палочки Ауэра
1 Все подтипы острой лимфобластной лейкемии можно отдифференцировать от других типов лейкемий по присутствию специфичных лимфоцитарных антигенов (см. табл. 3 и 5).
Выделение подтипов лейкозов (лейкемий), согласно предложенной классификации, отражающей уровень блока дифференцировки бластов, является очень важным для клиники, поскольку каждый тип имеет свою специфическую схему лечения.
Лейкемия (лейкоз) – это системное прогрессирующее разрастание незрелой опухолевой ткани в органах кроветворения с гематогенным распространением в другие органы и ткани.
Характерной особенностью лейкозов является быстрая диссеминация (распространение) опухолевых клеток по системе кроветворения. Вследствие этого, уже на ранних этапах заболевание приобретает системный характер. Наряду с костным мозгом наиболее часто наблюдается поражение селезенки, лимфатических узлов, лимфатических образований (Пейеровы бляшки, солитарные лимфоидные фолликулы) по ходу желудочно-кишечного тракта, печени и других органов. Объем лейкозных разрастаний и их распространенность в организме могут быть различными в зависимости от формы лейкоза, стадии болезни, проведенного лечения. Эти лейкозные разрастания называют лейкемический инфильтрат.
Подклассы острой лимфобластной лейкемии
Антигены Т-клеток (CD2, CD3, CD5, CD7, CD8)
Антиген В-клеток (CD19)
Из нулевых клеток
Самые первые распознаваемые как В-клетки
Этиология. Причина многих случаев лейкемий остается неизвестной. Но, поскольку опухолевая природа лейкозов не вызывает сомнения, вопросы этиологии лейкозов и опухолей, по-видимому, однотипны. Лейкозы – полиэтиологические заболевания. В возникновении их могут быть повинны различные факторы, способные вызвать мутацию клеток кроветворной ткани. Среди этих факторов следует отметить следующие: вирусы, ионизирующее излучение, химические вещества, аплазии костного мозга, иммунодефицитные состояния, генетические факторы.
Классификация
Лейкозы (лейкемии) классифицируются по нескольким характеристикам:
По клиническому течению:
· Острые лейкозы (лейкемии) – начинаются остро, быстро прогрессируют, при отсутствии лечения приводят к смерти в течение нескольких месяцев. В крови обычно определяется большое количество бластных клеток.
· Хронические лейкозы (лейкемии) начинаются постепенно и медленно прогрессируют, даже при отсутствии лечения больные могут прожить несколько лет. В крови выявляются обычно незрелые, но с тенденцией к созреванию клетки.
По гисто- (цито-) генезу, характеру и направлению дифференцировки разрастающихся клеток:
Среди острых лейкозов выделяют:
Среди хронических лейкозов в зависимости от ряда созревающих клеток гемопоэза выделяют лейкозы миелоцитарного, лимфоцитарного и моноцитарного происхождения:
Лейкозы миелоцитарного происхождения:
ü хронический миелоидный лейкоз;
ü истинная полицитемия Вакеза-Ослера и др.
Лейкозы лимфоцитарного происхождения:
ü хронический лимфоидный лейкоз;
ü лимфоматоз кожи (болезнь Сезари);
ü парапротеинемические лейкозы (миеломная болезнь, первичная макроглобулинемия Вальденстрема, болезнь тяжелых цепей Франклина).
Лейкозы моноцитарного происхождения:
ü хронический моноцитарный лейкоз;
По картине периферический крови:
· Лейкемические, которые характеризуются значительным увеличением количества лейкоцитов, в том числе и лейкозных клеток, в периферической крови (десятки и сотни тысяч, иногда до миллиона в 1 мкл крови). Это наиболее частая форма.
· Сублейкемические, при которых количество лейкоцитов несколько выше нормы (15-25 тысяч в 1 мкл крови), но в крови определяются опухолевые клетки.
· Алейкемические, при которых количество лейкоцитов в пределах нормы, в крови не определяются опухолевые клетки. Этот тип наблюдается редко, но он возникает обычно уже на ранних этапах заболевания. С целью диагностики используют трепанобиопсию крыла подвздошной кости или пунктат костного мозга грудины.
· Лейкопенические, при которых количество лейкоцитов ниже нормы, иногда может достигать одной тысячи, но могут быть качественные изменения, обусловленные появлением лейкозных клеток.
Острые лейкемии характеризуются пролиферацией бластов без признаков дифференцирования. Для острого недифференцированного лейкоза характерна инфильтрация всех органов кроветворения и паренхиматозных органов недифференцированными однородного вида мелкими, круглыми, гиперхромными клетками гемопоэза I-II классов (то есть полипотентными клетками-предшественниками и частично детерминированными клетками-предшественниками миело- и лимфопоэза). Острый недифференцированный лейкоз протекает как септическое заболевание. И при миелобластной, и при лимфобластной лейкемиях в периферической крови определяется лейкоцитоз (увеличение количества лейкоцитов) с наличием бластов. При остром лейкозе в периферической крови находят так называемый лейкемический провал (hiatus leucemicus) – резкое увеличение бластных клеток и единичные зрелые элементы при отсутствии переходных созревающих форм. Иногда количество лейкоцитов может быть не увеличено, но бласты обязательно присутствуют. Очень редко в крови отсутствуют и бласты (алейкемическая лейкемия). Однако в пунктате костного мозга изменения находят при любых формах лейкемий. Отмечается диффузное поражение ткани костного мозга, опухолевые клетки вытесняют другие гемопоэтические ростки и жировую ткань. Костный мозг губчатых и трубчатых костей при лимфобластном лейкозе на всем протяжении становится сочным, малиново-красным (вид малинового желе). При миелобластном лейкозе он приобретает зеленоватый (гноевидный) оттенок, поэтому его называют пиоидный костный мозг. При острой лимфобластной лейкемии и острой моноцитарной лейкемии часто наблюдается увеличение лимфатических узлов, при острой миелобластной лейкемии оно обычно отсутствует. Увеличение селезенки относительно небольшое (по сравнению с хроническими формами лейкоза), масса ее достигает 500-600 граммов.
В крови пациентов наблюдается снижение количества других форменных элементов из-за вытеснения этих ростков неопластическими клетками. В результате возникает тяжёлая анемия, тромбоцитопения, нейтропения, проявляющаяся в виде частых инфекционных заболеваний и изъязвлений (некроз) на слизистых оболочках. Некрозы чаще всего развиваются в слизистой полости рта, миндалин (некротическая ангина), желудочно-кишечного тракта. Иногда могут возникать инфаркты селезенки. Причиной некрозов могут служить лейкемические инфильтраты, которые суживают просвет сосудов. Резкое снижение иммунитета и общей реактивности организма сопровождается активацией инфекций и развитием альтеративного воспаления.
У больных с промиелобластной лейкемией может развиться синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром), т.к. в гранулах опухолевых клеток содержится обилие тромбопластических веществ, которые в большом количестве попадают в кровоток при гибели клеток.
В печени при всех формах острого лейкоза разрастания бластных клеток могут локализоваться как в области портальных трактов, так и по ходу синусоидных капилляров, что сопровождается деструкцией печеночных балок, дистрофическими изменениями гепатоцитов, вплоть до их очагового некроза.
При поражении кожи очаговые лейкозные пролифераты располагаются в поверхностных и глубоких слоях дермы, преимущественно вокруг сосудов, волосяных фолликулов и потовых желез. Это может сопровождаться некрозом и изъязвлением эпидермиса.
· кровотечение (геморрагический диатез), кровоизлияние в мозг;
· присоединение инфекций (сепсис) и др.
Отличия хронических лейкозов от острых: у больных развивается общее хроническое малокровие, происходит увеличение внутренних органов в результате дистрофических изменений и инфильтрации их опухолевыми клетками (лейкемические инфильтраты). При всех хронических лейкемиях происходит увеличение селезенки, генерализованное увеличение лимфатических узлов.
Селезенка при хроническом лимфоцитарном лейкозе увеличивается до 1 кг. При хроническом миелоцитарном лейкозе ее вес может достигать 5-6 кг (в норме 120-150 гр.), пульпа вида гнилой сливы.
Лимфатические узлы значительно увеличены, мягкие. При лимфолейкозе они сливаются в огромные плотноватые пакеты, на разрезе сочные, бело-розовые, при миелоцитарном лейкозе – серо-красного цвета. При любом хроническом лейкозе рисунок лимфоузла стерт в результате разрастания незрелой опухолевой ткани. Хроническая лимфоцитарная лейкемия с поражением лимфоузлов идентична мелкоклеточной лимфоцитарной лимфоме (Т- и В-типы – ранее назывались высокодифференцированная лимфоцитарная лимфома). В той или иной мере выражена лейкозная инфильтрация ткани миндалин, групповых и солитарных лимфатических фолликулов кишечника, почек, кожи, иногда головного мозга и его оболочек (нейролейкемия).
Печень увеличена в большей степени при миелоцитарном лейкозе, чем при лимфоцитарном за счет лейкемических инфильтратов. Лейкемические инфильтраты располагаются преимущественно при миелоцитарном лейкозе внутри дольки между печеночными балками, при лимфоцитарном – по ходу триад. Лейкемические инфильтраты при миелоцитарном лейкозе полиморфны (за счет большего количества переходных форм), цитоплазма в клетках четко выражена, ядра светлые, содержат рыхлый диффузно расположенный хроматин. При лимфолейкозе инфильтраты мономорфные, представлены мелкими примерно одинаковыми, круглыми с гиперхромными (компактное расположение хроматина) лимфоцитарными опухолевыми клетками. Миелобласты сложно морфологически отдифференцировать от лимфобластов, за исключением следующих случаев:
· когда они содержат палочки Ауэра – фиолетовые кристаллические цитоплазматические включения;
· когда имеется видимая дифференцировка в промиелоциты, в цитоплазме которых определяются крупные гранулы;
· при использовании цитохимических и иммунологических методов исследования (табл. 2, 3 и 6).
Таким образом, хронические лимфолейкозы характеризуются:
o значительным увеличением размеров как иммунокомпетентных, так и паренхиматозных органов;
o отсутствием геморрагического диатеза;
o отсутствием некрозов, которые могут появиться в период бластного криза.
Хронический эритромиелоз, эритремия, истинная полицитемия (болезнь Вакеза-Ослера), первичная макроглобулинемия Вальденстрема, болезнь тяжелых цепей, хронический моноцитарный лейкоз являются редкими заболеваниями.
Наибольшее значение среди группы хронических парапротеинемических лейкозов имеет миеломная болезнь.
Миеломная болезнь (миелома, болезнь Рустицкого-Калера) характеризуется неопластической пролиферацией плазматических клеток (плазмобластов) с продукцией моноклоновых иммуноглобулинов (парапротеинов) или их фрагментов. В зависимости от класса и типа синтезируемых и секретируемых парапротеинов выделяют следующие иммунохимические варианты: G-, A-, D-, E-миелому, миелому Бенс-Джонса (болезнь легких цепей) и др. Клинические и морфологические проявления вариантов сходны. Обычно миелома протекает по алейкемическому варианту, но возможно и наличие в крови миеломных клеток.
В зависимости от характера миеломных инфильтратов различают следующие формы:
Миелома может протекать в солитарной форме, в виде одиночного узла, но чаще она бывает множественной.
Опухолевые инфильтраты чаще всего появляются в плоских костях (ребра, кости черепа) и позвоночнике, реже – в трубчатых костях (плечевая, бедренная кость). Разрастающаяся опухолевая ткань ведет к деструкции костной ткани и развитию патологических переломов. При диффузном разрастании опухолевой кроветворной ткани наблюдается остеолизис и остеопороз – образование гладкостенных, как бы штампованных дефектов. Помимо костного мозга и костей, миеломноклеточные инфильтраты постоянно отмечаются во внутренних органах.
При миеломной болезни в связи с секрецией опухолевыми клетками парапротеина часто развивается AL-амилоидоз. Наибольшее значение среди парапротеинемических изменений имеет парапротеинемический нефроз, или миеломная нефропатия. В основе парапротеинемического нефроза лежит избыточное накопление в канальцах и в строме мозгового, а затем и коркового вещества парапротеина Бенс-Джонса, ведущее к нефросклерозу. Такие почки получили название “миеломные сморщенные почки”. Развивающаяся уремия является в 30% случаев причиной смерти больных миеломой. Другой частой причиной смерти служит присоединение инфекций.
Поскольку опухолевые лимфоциты, начиная с момента их возникновения, быстро разносятся кровотоком по организму, то все лимфомы относятся к злокачественным новообразованиям. Опухолевая пролиферация лимфоцитов, поражающая какую-то одну область организма без тенденции к диссеминированию (для которой действительно можно применить термин “доброкачественная”) наблюдается очень редко. Однако по клиническому течению многие злокачественные лимфомы протекают “доброкачественно” (то есть с низкой скоростью роста и длительным периодом выживания).
Злокачественные лимфомы наиболее часто поражают лимфатические узлы и менее часто лимфоидную ткань в других органах (миндалины глотки, солитарные фолликулы и пейеровы бляшки тонкой кишки, селезенку).
Злокачественные лимфомы делятся на:
Лимфома Ходжкина выделена отдельно, т.к. источник происхождения ее точно не установлен.
Неходжкинские лимфомы классифицируются:
По характеру роста опухоли:
По цитологической характеристике:
ü лимфоцитарные (наличие их дискутируется);
ü пролимфоцитарные (из малых и больших расщепленных клеток, то есть В-клеточные)
По клоновому принципу:
ü лимфомы из натуральных киллеров (NK).
По степени злокачественности:
o низкой (пролимфоцитарные и пролимфоцитарно-лимфобластные с фолликулярным ростом);
o умеренной (пролимфоцитарные с диффузным ростом);
o высокой (лимфобластные и иммунобластные).
Различия между лимфомами и лейкемиями
Опухолевые лимфоциты циркулируют в крови и зачастую они широко распространяются по лимфоидной ткани организма. Если доминирует поражение костного мозга и увеличение количества лимфоцитов в крови, то этот процесс называют лейкемией. Если преобладает поражение лимфоидной ткани, то этот процесс называется лимфомой. Разделение это условное. Так, у детей иногда используется термин лимфома-лейкемия, т.к. эти две формы могут сосуществовать. При лимфомах тоже может значительно повышаться количество лейкоцитов в крови.
Опухолевую пролиферацию лимфоидных клеток необходимо отличать от нормальной пролиферации, которая возникает во время иммунного ответа (реактивная гиперплазия). Иногда сложно дифференцировать эти два состояния. Наиболее важными критериями являются нарушение структуры лимфоузла и наличие моноклональности опухолевых клеток.
Нарушение структуры лимфатических узлов, особенно если оно сочетается с потерей нормальных взаимоотношений клеток различных типов, является признаком опухолевой природы данных изменений.
Пролиферация при иммунном ответе является поликлональной, т.е. наблюдается размножение многих клонов лимфоцитов. Большинство лимфоцитов при лимфомах происходят из одного клона (т.е. они моноклональны). Моноклональная природа пролиферирующих лимфоцитов является наилучшим подтверждением их опухолевой природы и может быть доказана иммуногистохимически наличием моноклональных легких или тяжелых цепей иммуноглобулинов на клеточной поверхности или в цитоплазме В-клеток. Доказано, что в поликлональной популяции лимфоцитов количество клеток, синтезирующих λ и κ легкие цепи приблизительно равно, а в моноклональной популяции обнаруживаются или λ, или κ легкие цепи.
НОМЕНКЛАТУРА И КЛАССИФИКАЦИЯ НЕХОДЖКИНСКИХ ЛИМФОМ
Лимфомы, как и другие опухоли, классифицируются на основе сходства с нормальными клетками, на которые они больше всего похожи. Раньше при классификации возникали проблемы, так как классификация нормальных клеток лимфоидной ткани постоянно изменялась на протяжении нынешнего столетия. Классификация неходжкинских лимфом также изменялась несколько раз и модифицировалась по мере развития исследований лимфоидной ткани. В последние годы получено экспериментальное подтверждение существования в кроветворной ткани единой полипотентной клетки – стволовой, или родоначальной, способной к дифференцировке по всем росткам миело- и лимфопоэза, и убедительно продемонстрировано, что свойствами стволовой клетки не обладают ретикулярные элементы стромы кроветворных органов. Большинство исследователей считает, что стволовой клеткой является клетка типа малого лимфоцита.
Классификация неходжкинских лимфом (основана на классификации Лукаса и Коллинза)
Читайте также:

