Жировое перерождение печени биохимия реферат
Обновлено: 05.07.2024
“Стеатоз печени” – это описательный термин, означающий накопление капель жира, жировых включений в гепатоцитах. Стеатоз может быть очаговым или диффузным.
Неалкогольный стеатогепатит (НАСГ) – клинический синдром стеатоза и воспаления печени, который устанавливается по результатам биопсии печени, после исключения других причин заболевания печени. НАСГ, как правило, носит характер диффузного процесса.
Гистологические изменения в печени, сходные с картиной алкогольного гепатита, впервые описаны в 1980г. Ludwig и сотр. у пациентов, не употреблявших алкоголь в количествах, вызывающих повреждение печени.
Частота выявления НАСГ среди больных, которым проводилась биопсия печени, составляет примерно 7—9% в западных странах и 1,2% в Японии. Алкогольный гепатит встречается в 10—15 раз чаще.
Обследование больших групп пациентов с криптогенным циррозом печени, включавшее оценку сопутствующих заболеваний и факторов риска, позволило выдвинуть предположение, что во многих случаях (до 60-80%) цирроз печени “неясной этиологии” развивается на фоне нераспознанного НАСГ.
Этиологические факторы и факторы риска. Выделяют случаи первичного и вторичного стеатоза печени и НАСГ (табл. 7.1).
Таблица 7.1. Этиологические факторы неалкогольного стеатогепатита
| Первичный НАСГ | Вторичный НАСГ |
|---|---|
| Ожирение Сахарный диабет (в особенности - синдром резистентности к инсулину) Гиперлипидемия | Лекарственные препараты (амиодарон, глюкокортикоиды, синтетические эстрогены, тамоксифен, пергексилина малеат, метотрексат, тетрациклин, нестероидные противовоспалительные средства (аспирин, вальпроат натрия, ибупрофен, др.), нифедипин (?), дилтиазем (?) и пр.) Синдром мальабсорбции (как следствие наложения илео-еюнального анастомоза, билиарно-панкреатической стомы, гастропластики по поводу ожирения, расширенной резекции тонкой кишки и пр.). Быстрое похудание Длительное (свыше 2 нед.) парентеральное питание (в особенности - не содержащее жиров или не сбалансированное по содержанию углеводов и жиров) Смешанные нарушения (синдром избыточного бактериального обсеменения кишечника (на фоне дивертикулеза тонкой кишки и пр.)) Абеталипротеинемия Липодистрофия конечностей Болезнь Вильяма-Крисчена Болезнь Вильсона-Коновалова |
Первичный НАСГ, как правило, ассоциирован с эндогенными нарушениями липидного и углеводного обмена. Наиболее высок риск развития стеатоза печени у лиц с ожирением, инсулинонезависимым сахарным диабетом, гипертриглицеридемией.
Вторичный НАСГ индуцируется внешними воздействиями и развивается на фоне некоторых метаболических расстройств, приема ряда медикаментов, синдрома мальабсорбции. Отмечены случаи развития НАСГ на фоне недостаточности альфа-1-антитрипсина.
Примерно у 42% пациентов не удается выявить факторов риска развития заболевания. Исследуется роль наследственной предрасположенности. Среди пациентов с НАСГ чаще встречаются гетерозиготы по C282Y.
Патогенез. Патогенез стеатоза печени и НАСГ плохо изучен. Принято считать, что стеатоз печени является ступенью, предшествующей развитию стеатогепатита. Ряд исследователей выражает сомнение, что избыточное накопление липидов как таковое может быть причиной вторичного воспаления, поскольку выраженному стеатозу печени не всегда сопутствуют явления гепатита.
На рис. 7.1 и 7.2 схематично представлена роль печени в липидном обмене.
Рис. 7.1. Участие печени в жировом обмене
Рис. 7.2. Основные этапы метаболизма липидов в гепатоците
Избыточное накопление жира в ткани печени (в гепатоцитах и звездчатых клетках) может быть следствием:
- повышения поступления свободных жирных кислот (СЖК) в печень;
- снижения скорости β-окисления СЖК в митохондриях печени;
- повышения синтеза жирных кислот в митохондриях печени;
- снижения синтеза или секреции липопротеинов очень низкой плотности (ЛПОНП) и экспорта триглицеридов в составе ЛПОНП.
Предполагают, что, независимо от причин развития стеатоза, в основе воспалительно-некротических изменений в печени лежат универсальные механизмы. Будучи высокореактогенными соединениями, СЖК служат субстратом перекисного окисления липидов (ПОЛ). ПОЛ сопровождается повреждением митохондрий, лизосом, клеточных мембран. Продукты ПОЛ стимулируют коллагенообразование, образование телец Мэллори (агрегатов мономеров цитокератина).
Существует противоположная гипотеза, согласно которой воспалительные изменения, индуцируемые неизвестными стимулами, вызывают дисфункцию гепатоцитов с развитием жировой дистрофии.
При НАСГ наблюдается повышенная активность цитохрома P450 2E1 в печени, что сопровождается образованием активных радикалов кислорода и усилением реакций ПОЛ.
Предполагается, что для инициации стеатонекроза необходимо определенное воздействие, приводящее к формированию активных форм кислорода в митохондриях.
Первичный НАСГ. У пациентов с избыточной массой тела имеются более выраженные запасы СЖК в организме, и нередко - повышенное содержание СЖК в плазме крови. Кроме того, для этой категории больных достаточно характерна пониженная чувствительность периферических рецепторов к инсулину. Уровень инсулина крови нередко повышен. Инсулин активизирует синтез СЖК и триглицеридов (ТГ), снижает скорость бета-окисления СЖК в печени и секрецию липидов в кровоток. Таким образом, при синдроме резистентности к инсулину содержание жира в органе может возрастать.
Вторичный НАСГ. Механизм развития стеатогепатита как осложнения длительного тотального парентерального питания остается неизвестным. Возможно, он носит мультифакторный характер (табл. 7.2).
Таблица 7.2. Возможные механизмы развития стеатоза печени и стеатогепатита на фоне длительного тотального парентерального питания
| Чрезмерно высокая скорость инфузии растворов глюкозы (при превышении максимальной скорости утилизации глюкозы (4-5 г/кг) происходит синтез жиров). Избыточное введение липидных эмульсий (фагоцитоз липидных капель в печени). Питание, несбалансированное по аминокислотам, жирам и углеводам (приводит к возрастанию внутрипеченочного синтеза липидов). Дефицит поступления карнитина, холина, эссенциальных жирных кислот, глутамина. Воздействие токсичных метаболитов аминокислот и желчных кислот. Отрицательное влияние дисбаланса желудочно-кишечных гормонов. |
При синдроме мальабсорбции патогенетическое значение имеют дефицит поступления пищевых факторов (метионина, холина, необходимых для синтеза лецитина, обеспечивающего тонкое диспергирование липидов в клетке), а также быстрое похудание (повышенная мобилизация СЖК из жировых депо).
Исследованы некоторые механизмы развития вторичного лекарственного НАСГ.
В качестве примеров можно привести следующие.
В метаболизме аспирина и вальпроата натрия участвует коэнзим А - катализатор бета-окисления СЖК. При применении данных препаратов возможно развитие “перераспределительного дефицита” коэнзима А.
Тетрациклин, помимо подавляющего влияния на бета-окисление СЖК, нарушает секрецию ТГ гепатоцитами.
Амиодарон не только угнетает бета-окисление в митохондриях (приводит к накоплению субстратов ПОЛ), но и нарушает процесс переноса электронов в дыхательной цепи, способствуя формированию активных форм кислорода. Поэтому гепатотоксичное влияние амиодарона обычно не ограничивается стеатозом, и выражается в развитии НАСГ. Предполагается также, что амиодарон (его метаболиты?) и триметоприм/сульфаметоксазол подавляют лизосомальный катаболизм фосфолипидов, что приводит к развитию фосфолипидоза.
Эстрогены вызывают ультраструктурные изменения митохондрий, с подавлением процессов бета-окисления.
Интерферон – альфа блокирует транскрипцию митохондриальной ДНК.
Генетическая предрасположенность к развитию НАСГ также связана с накоплением потенциально токсичных СЖК в цитоплазме в результате дефектов бета-окисления, обусловленного нарушением захвата карнитина гепатоцитом, “челночного механизма” переноса жирных кислот в митохондрии (протекающего с участием ряда ферментов и карнитина),дисфункцией какого-либо звена мультиферментного комплекса бета-окисления. Изменения структуры митохондриальной ДНК сопровождаются угнетением системы окислительного фосфорилирования и восстановления необходимых для бета-окисления NADH и FADH2. В этих случаях развиваются, как правило, полиорганные расстройства.
Врожденные нарушения синтеза мочевины сопровождаются накоплением в печени аммиака, угнетающего бета-окисление жирных кислот.
Существуют патогенетические параллели с морфологическими особенностями стеатоза печени (табл. 7.3).
Клинические проявления. Большинство пациентов, страдающих стеатозом печени и НАСГ (65%-80%), - женщины, и большинство из них имеет избыточную массу тела, на 10-40% превышающую идеальную. Инсулин-независимый сахарный диабет обнаруживается у 25% - 75% пациентов.
Средний возраст больных на момент диагностики НАСГ составляет 50 лет.
При осмотре у 75% больных обнаруживается гепатомегалия. Увеличение селезенки имеет место примерно в 25% случаев. Желтуха, асцит, “печеночные знаки” выявляются редко.
Индекс массы тела выступает как единственный независимый фактор для оценки степени жировой инфильтрации печени.
Содержание в печени гликогена, липидов, белков и минералов. Роль печени в углеводном обмене, обмене липидов, белковом обмене. Метаболизм алкоголя и жирных кислот в печени. Образование и пути использования фосфатидной кислоты. Желчные кислоты и пигменты.
| Рубрика | Биология и естествознание |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 08.06.2015 |
| Размер файла | 571,4 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
1. Химический состав печени: содержание гликогена, липидов, белков, минеральный состав.
2. Роль печени в углеводном обмене: поддержание постоянной концентрации глюкозы, синтез и мобилизация гликогена, глюконеогенез, основные пути превращения глюкозо-6-фосфата, взаимопревращения моносахаридов.
3. Роль печени в обмене липидов: синтез высших жирных кислот, ацилглицеролов, фосфолипидов, холестерола, кетоновых тел, синтез и обмен липопротеинов, понятие о липотропном эффекте и липотропных факторах.
4. Роль печени в белковом обмене: синтез специфических белков плазмы крови, образование мочевины и мочевой кислоты, холина, креатина, взаимопревращения кетокислот и аминокислот.
5. Метаболизм алкоголя в печени, жировое перерождение печени при злоупотреблении алкоголем.
6. Обезвреживающая функция печени: стадии (фазы) обезвреживания токсических веществ в печени.
7. Обмен билирубина в печени. Изменения содержания желчных пигментов в крови, моче и кале при различных видах желтух (надпечёночной, паренхиматозной, обтурационной).
8. Химический состав желчи и её роль; факторы, способствующие образованию желчных камней.
Печень является органом, занимающим уникальное место в обмене веществ. В каждой печёночной клетке содержится несколько тысяч ферментов, катализирующих реакции многочисленных метаболических путей. Поэтому печень выполняет в организме целый ряд метаболических функций. Важнейшими из них являются:
· биосинтез веществ, которые функционируют или используются в других органах. К этим веществам относятся белки плазмы крови, глюкоза, липиды, кетоновые тела и многие другие соединения;
· биосинтез конечного продукта азотистого обмена в организме - мочевины;
· участие в процессах пищеварения - синтез желчных кислот, образование и экскреция желчи;
· биотрансформация (модификация и конъюгация) эндогенных метаболитов, лекарственных препаратов и ядов;
· выделение некоторых продуктов метаболизма (желчные пигменты, избыток холестерола, продукты обезвреживания).
Роль печени в обмене углеводов
Основная роль печени в обмене углеводов заключается в поддержании постоянного уровня глюкозы в крови. Это осуществляется путём регуляции соотношения процессов образования и утилизации глюкозы в печени.
В клетках печени содержится фермент глюкокиназа, катализирующий реакцию фосфорилирования глюкозы с образованием глюкозо-6-фосфата. Глюкозо-6-фосфат является ключевым метаболитом углеводного обмена; основные пути его превращения представлены на рисунке 1.
Пути утилизации глюкозы
После приёма пищи большое количество глюкозы поступает в печень по воротной вене. Эта глюкоза используется прежде всего для синтеза гликогена (схема реакций приводится на рисунке 2). Содержание гликогена в печени здоровых людей обычно составляет от 2 до 8% массы этого органа.
Гликолиз и пентозофосфатный путь окисления глюкозы в печени служат в первую очередь поставщиками метаболитов-предшественников для биосинтеза аминокислот, жирных кислот, глицерола и нуклеотидов. В меньшей степени окислительные пути превращения глюкозы в печени являются источниками энергии для обеспечения биосинтетических процессов.
Рисунок 1 Главные пути превращения глюкозо-6-фосфата в печени. Цифрами обозначены: 1 - фосфорилирование глюкозы; 2 - гидролиз глюкозо-6-фосфата; 3 - синтез гликогена; 4 - мобилизация гликогена; 5 - пентозофосфатный путь; 6 - гликолиз; 7 - глюконеогенез
Рисунок 2 Схема реакций синтеза гликогена в печени
Рисунок 3 Схема реакций мобилизации гликогена в печени
Пути образования глюкозы
В некоторых условиях (при голодании низкоуглеводной диете, длительной физической нагрузке) потребность организма в углеводах превышает то количество, которое всасывается из желудочно-кишечного тракта. В таком случае образование глюкозы осуществляется с помощью глюкозо-6-фосфатазы, катализирующей гидролиз глюкозо-6-фосфата в клетках печени. Непосредственным источником глюкозо-6-фосфата служит гликоген. Схема мобилизации гликогена представлена на рисунке 3.
Мобилизация гликогена обеспечивает потребности организма человека в глюкозе на протяжении первых 12 - 24 часов голодания. В более поздние сроки основным источником глюкозы становится глюконеогенез - биосинтез из неуглеводных источников.
Основными субстратами для глюконеогенеза служат лактат, глицерол и аминокислоты (за исключением лейцина). Эти соединения сначала превращаются в пируват или оксалоацетат - ключевые метаболиты глюконеогенеза.
Глюконеогенез - процесс, обратный гликолизу. При этом барьеры, создаваемые необратимыми реакциями гликолиза, преодолеваются при помощи специальных ферментов, катализирующих обходные реакции (см. рисунок 4).
Из других путей обмена углеводов в печени следует отметить превращение в глюкозу других пищевых моносахаридов - фруктозы и галактозы.
Рисунок 4 Гликолиз и глюконеогенез в печени
Ферменты, катализирующие необратимые реакции гликолиза: 1 - глюкокиназа; 2 - фосфофруктокиназа; 3 - пируваткиназа.
Ферменты, катализирующие обходные реакции глюконеогенеза: 4 -пируваткарбоксилаза; 5 - фосфоенолпируваткарбоксикиназа; 6 -фруктозо-1,6-дифосфатаза; 7 - глюкозо-6-фосфатаза.
Роль печени в обмене липидов
В гепатоцитах содержатся практически все ферменты, участвующие в метаболизме липидов. Поэтому паренхиматозные клетки печени в значительной степени контролируют соотношение между потреблением и синтезом липидов в организме. Катаболизм липидов в клетках печени протекает главным образом в митохондриях и лизосомах, биосинтез - в цитозоле и эндоплазматическом ретикулуме. Ключевым метаболитом липидного обмена в печени является ацетил-КоА, главные пути образования и использования которого показаны на рисунке 5.
Рисунок 5 Образование и использование ацетил-КоА в печени
Метаболизм жирных кислот в печени
Пищевые жиры в виде хиломикронов поступают в печень через систему печёночной артерии. Под действием липопротеинлипазы, находящейся в эндотелии капилляров, они расщепляются до жирных кислот и глицерола. Жирные кислоты, проникающие в гепатоциты, могут подвергаться окислению, модификации (укорочению или удлинению углеродной цепи, образованию двойных связей) и использоваться для синтеза эндогенных триацилглицеролов и фосфолипидов.
Синтез кетоновых тел
При в-окислении жирных кислот в митохондриях печени образуется ацетил-КоА, подвергающийся дальнейшему окислению в цикле Кребса. Если в клетках печени имеется дефицит оксалоацетата (например, при голодании, сахарном диабете), то происходит конденсация ацетильных групп с образованием кетоновых тел (ацетоацетат, в-гидроксибутират, ацетон). Эти вещества могут служить энергетическими субстратами в других тканях организма (скелетные мышцы, миокард, почки, при длительном голодании - головной мозг). Печень не утилизирует кетоновые тела. При избытке кетоновых тел в крови развивается метаболический ацидоз. Схема образования кетоновых тел - на рисунке 6.
Рисунок 6 Синтез кетоновых тел в митохондриях печени
Образование и пути использования фосфатидной кислоты
Общим предшественником триацилглицеролов и фосфолипидов в печени является фосфатидная кислота. Она синтезируется из глицерол-3-фосфата и двух ацил-КоА - активных форм жирных кислот (рисунок 7). Глицерол-3-фосфат может образоваться либо из диоксиацетонфосфата (метаболит гликолиза), либо из свободного глицерола (продукт липолиза).
Рисунок 7 Образование фосфатидной кислоты (схема)
Для синтеза фосфолипидов (фосфатидилхолина) из фосфатидной кислоты необходимо поступление с пищей достаточного количества липотропных факторов (веществ, препятствующих развитию жировой дистрофии печени). К этим факторам относятся холин, метионин, витамин В12, фолиевая кислота и некоторые другие вещества. Фосфолипиды включаются в состав липопротеиновых комплексов и принимают участие в транспорте липидов, синтезированных в гепатоцитах, в другие ткани и органы. Недостаток липотропных факторов (при злоупотреблении жирной пищей, хроническом алкоголизме, сахарном диабете) способствует тому, что фосфатидная кислота используется для синтеза триацилглицеролов (нерастворимых в воде). Нарушение образования липопротеинов приводит к тому, что избыток ТАГ накапливается в клетках печени (жировая дистрофия) и функция этого органа нарушается. Пути использования фосфатидной кислоты в гепатоцитах и роль липотропных факторов показаны на рисунке 8.
Рисунок 8 Использование фосфатидной кислоты для синтеза триацилглицеролов и фосфолипидов. Липотропные факторы обозначены знаком
Печень является основным местом синтеза эндогенного холестерола. Это соединение необходимо для построения клеточных мембран, является предшественником желчных кислот, стероидных гормонов, витамина Д3. Первые две реакции синтеза холестерола напоминают синтез кетоновых тел, но протекают в цитоплазме гепатоцита. Ключевой фермент синтеза холестерола - в-гидрокси-в-метилглутарил-КоА-редуктаза (ГМГ-КоА-редуктаза)ингибируется избытком холестерола и желчными кислотами по принципу отрицательной обратной связи (рисунок 9).
Рисунок 9 Синтез холестерола в печени и его регуляция
Липопротеины - белково-липидные комплексы, в состав которых входят фосфолипиды, триацилглицеролы, холестерол и его эфиры, а также белки (апопротеины). Липопротеины транспортируют нерастворимые в воде липиды к тканям. В гепатоцитах образуются два класса липопротеинов - липопротеины высокой плотности (ЛПВП) и липопротеины очень низкой плотности (ЛПОНП).
Роль печени в обмене белков
Печень является органом, регулирующим поступление азотистых веществ в организм и их выведение. В периферических тканях постоянно протекают реакции биосинтеза с использованием свободных аминокислот, либо выделение их в кровь при распаде тканевых белков. Несмотря на это, уровень белков и свободных аминокислот в плазме крови остаётся постоянным. Это происходит благодаря тому, что в клетках печени имеется уникальный набор ферментов, катализирующих специфические реакции обмена белков.
Пути использования аминокислот в печени
После приёма белковой пищи в клетки печени по воротной вене поступает большое количество аминокислот. Эти соединения могут претерпевать в печени ряд превращений, прежде чем поступить в общий кровоток. К этим реакциям относятся (рисунок 10):
а) использование аминокислот для синтеза белков;
б) трансаминирование - путь синтеза заменимых аминокислот; осуществляет также взаимосвязь обмена аминокислот с глюконеогенезом и общим путём катаболизма;
в) дезаминирование - образование б-кетокислот и аммиака;
г) синтез мочевины - путь обезвреживания аммиака (схему см. в разделе "Обмен белков");
д) синтез небелковых азотсодержащих веществ (холина, креатина, никотинамида, нуклеотидов и т.д.).
Рисунок 10 Обмен аминокислот в печени (схема)
В клетках печени синтезируются многие белки плазмы крови: альбумины (около 12 г в сутки), большинство б- и в-глобулинов, в том числе транспортные белки (ферритин, церулоплазмин, транскортин, ретинолсвязывающий белок и др.). Многие факторы свёртывания крови (фибриноген, протромбин, проконвертин, проакцелерин и др.) также синтезируются в печени.
Обезвреживающая функция печени
В печени обезвреживаются неполярные соединения различного происхождения, в том числе эндогенные вещества, лекарственные препараты и яды. Процесс обезвреживания веществ включает две стадии (фазы):
1) фаза модификации - включает реакции окисления, восстановления, гидролиза; для ряда соединений необязательна;
2) фаза конъюгации - включает реакции взаимодействия веществ с глюкуроновои и серной кислотами, глицином, глутаматом, таурином и другими соединениями.
Более подробно реакции обезвреживания будут рассмотрены в разделе "Биотрансформация ксенобиотиков".
Желчеобразовательная функция печени
Желчь - жидкий секрет желтовато-коричневого цвета, выделяемый печёночными клетками (500-700 мл в сутки). В состав желчи входят: желчные кислоты, холестерол и его эфиры, желчные пигменты, фосфолипиды, белки, минеральные вещества (Nа+, К+, Са2+, Сl-) и вода.
Являются продуктами метаболизма холестерола, образуются в гепатоцитах. Различают первичные (холевая, хенодезоксихолевая) и вторичные (дезоксихолевая, литохолевая) желчные кислоты. В желчи присутствуют главным образом желчные кислоты, конъюгированные с глицином или таурином (например, гликохолевая, кислота, таурохолевая кислота и т.д.).
Желчные кислоты принимают непосредственное участие в переваривании жиров в кишечнике:
· оказывают на пищевые жиры эмульгирующее действие;
· активируют панкреатическую липазу;
· способствуют всасыванию жирных кислот и жирорастворимых витаминов;
· стимулируют перистальтику кишечника.
При нарушении оттока желчи желчные кислоты проникают в кровь и мочу.
С желчью выводится из организма избыток холестерола. Холестерол и его эфиры присутствуют в желчи в виде комплексов с желчными кислотами (холеиновые комплексы). При этом отношение содержания желчных кислот к содержанию холестерола (холатный коэффициент) должно быть не ниже 15. В противном случае нерастворимый в воде холестерол выпадает в осадок и откладывается в виде камней желчного пузыря (желчно-каменная болезнь).
Из пигментов в желчи преобладает конъюгированный билирубин (моно- и диглюкуронид билирубина). Он образуется в клетках печени в результате взаимодействия свободного билирубина с УДФ-глюкуроновой кислотой. При этом снижается токсичность билирубина и увеличивается его растворимость в воде; далее конъюгированный билирубин секретируется в желчь.
При нарушении оттока желчи (механическая желтуха) в крови значительно увеличивается содержание прямого билирубина, в моче обнаруживается билирубин, в кале и моче снижено содержание стеркобилина. Дифференциальную диагностику желтух см. в разделе "Обмен сложных белков".
печень обмен метаболизм пигмент
Из ферментов, обнаруженных в желчи, следует в первую очередь отметить щелочную фосфатазу. Это экскреторный фермент, синтезируемый в печени. При нарушении оттока желчи активность щелочной фосфатазы в крови возрастает.
Подобные документы
Кровоснабжение и функции печени, описание строения печеночной дольки как функциональной единицы. Участие печени в белковом обмене, синтезе белков крови, углеводном обмене, синтезе гликогена, жировом обмене, выработке желчи. Строение желчных протоков.
презентация [1,2 M], добавлен 27.03.2019
Общая характеристика и основные этапы обмена липидов, особенности процесса переваривания. Порядок всасывания продуктов переваривания липидов. Исследование различных органов и систем в данном процессе: стенок и жировой ткани кишечника, легких и печени.
презентация [4,5 M], добавлен 31.01.2014
Специфические свойства, структура и основные функции, продукты распада жиров, белков и углеводов. Переваривание и всасывание жиров в организме. Расщепление сложных углеводов пищи. Параметры регулирования углеводного обмена. Роль печени в обмене веществ.
курсовая работа [261,6 K], добавлен 12.11.2014
Обмен сложных белков. Переваривание, всасывание и промежуточный обмен липидов. Жирорастворимые и водорастворимые витамины. Регуляция обмена углеводов. Теплообмен и регуляция температуры тела. Регуляция липидного обмена. Роль печени в обмене веществ.
презентация [10,2 M], добавлен 05.04.2014
Биохимия алкоголизма; социальные, психологические и физиологические факторы его развития. Генетическая предрасположенность к алкоголизму. Гены, отвечающие за метаболизм алкоголя и контролирующие нейропсихические функции. Метаболизм алкоголя в печени.
Что такое жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
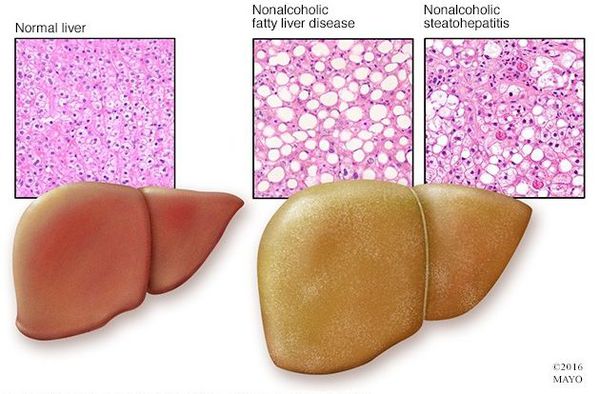
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печении или жировой гепатоз, неалкогольный стеатогепатит) — это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
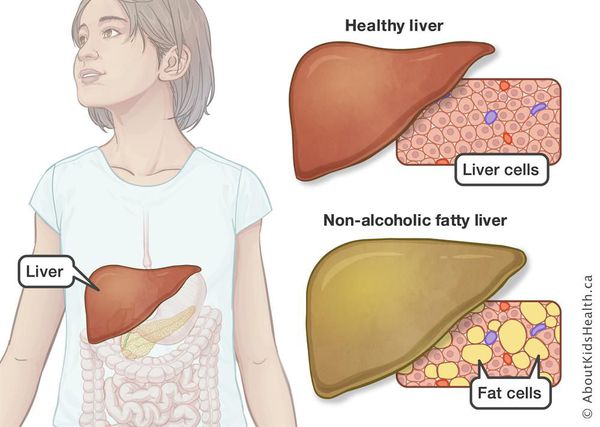
Все эти изменения неуклонно приводят к:
- разрушению клеток печени (неалкогольный стеатогепатит);
- накоплению жировой и формированию фиброзной ткани, что вызывает уже необратимые, структурные (морфологические) изменения паренхимы печени;
- изменению биохимического состава крови;
- развитию метаболического синдрома (гипертоническая болезнь, ожирение, сахарный диабет);
- в конечном итоге, циррозу.
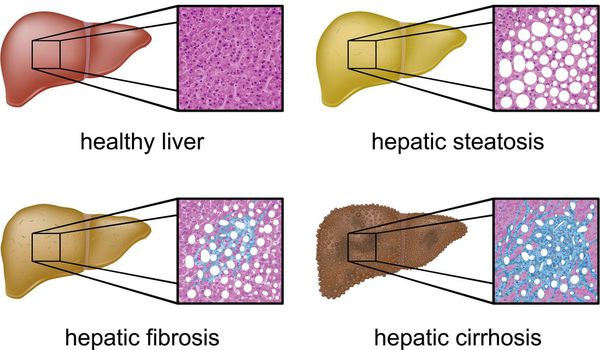
Метаболический синдром — широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией. [2] [3] [4]
В большинстве случаев НАЖБП развивается после 30 лет. [7]
Факторами риска данного заболевания являются:
- малоподвижный образ жизни (гиподинамия);
- неправильное питание, переедание;
- длительный приём лекарственных препаратов;
- избыточная масса тела и висцеральное ожирение;
- вредные привычки.
Основными причинам развития НАЖБП являются: [11]
- гормональные нарушения;
- нарушение жирового обмена (дисбаланс липопротеидов плазмы);
- нарушение углеводного обмена (сахарный диабет);
- артериальная гипертензия;
- ночная гипоксемия (синдром обструктивного апноэ сна).
При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %. [3]
Ожирение определяется по формуле вычисления индекса массы тела (ИМТ): ИМТ = вес (кг) : (рост (м)) 2 . Если человек, например, весит 90 кг, а его рост — 167 см, то его ИМТ = 90 : (1,67х1,67) = 32,3. Этот результат говорит об ожирении I степени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
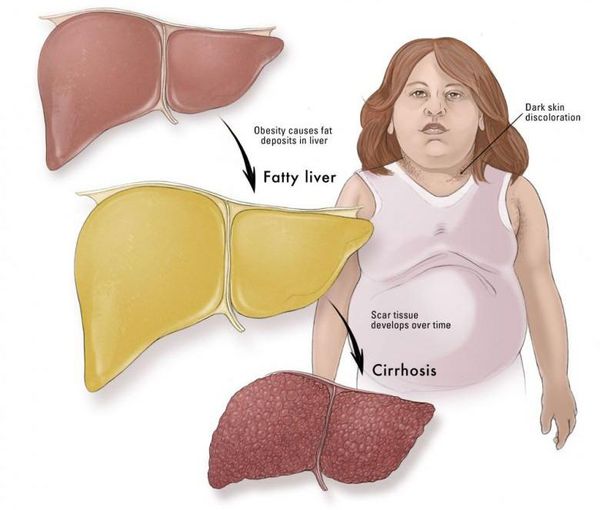
Часто НАЖБП сопутствуют заболевания желчного пузыря: хронический холецистит, желчнокаменная болезнь. Реже, в запущенных случаях, возникают признаки портальной гипертензии: увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости). Как правило, данные симптомы наблюдаются на стадии цирроза печени. [7]
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
- избыточное поступление свободных жирных кислот (FFA) в печень;
- усиленный синтез свободных жирных кислот печени;
- пониженный уровень бета-окисления свободных жирных кислот;
- снижение синтеза или секреции липопротеинов очень высокой плотности. [7]
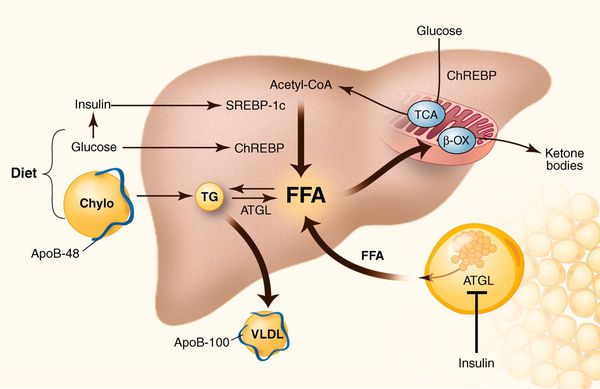
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот, что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид. [2]
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной, раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах, в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов, которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз. [2]
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов. [7] CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Кроме того, патогенетическое значение в формировании НАЖБП имеет эндотоксин-опосредованное повреждение, которое, в свою очередь, усиливает выработку провоспалительных цитокинов (ФНО-α, ИЛ-6 и ИЛ-8), приводящих к нарушению целостности мембран гепатоцитов и даже к их некрозу [9] , а также к развитию воспалительной клеточной инфильтрации как в портальных трактах, так и в дольках печени, что приводит к стеатогепатиту.
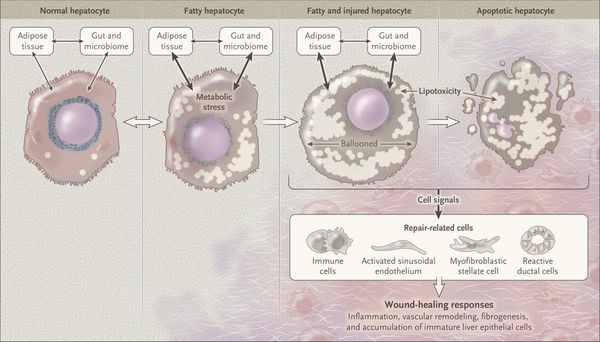
Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt: [9] [10] [11]
- I степень (мягкий НАСГ) — стеатоз крупнокапельный, не более 33-66% поражённых гепацитов;
- II степень (умеренный НАСГ) — крупно- и мелкокапельный, от 33% до 66% поражённых гепацитов;
- III степень (тяжелый НАСГ) — крупно- и мелкокапельный, больше 60% поражённых гепацитов.
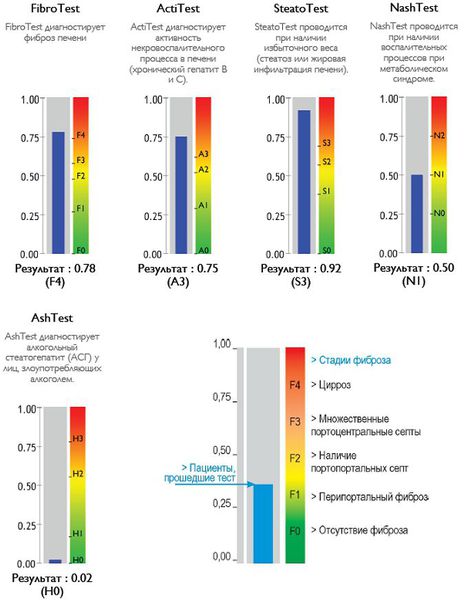
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
- S1 (до 33% жировой инфильтрации);
- S2 ( 33-60% жировой инфильтрации)
- S3 (более 60% жировой инфильтрации)
- F1,F2, F3, цирроз.
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
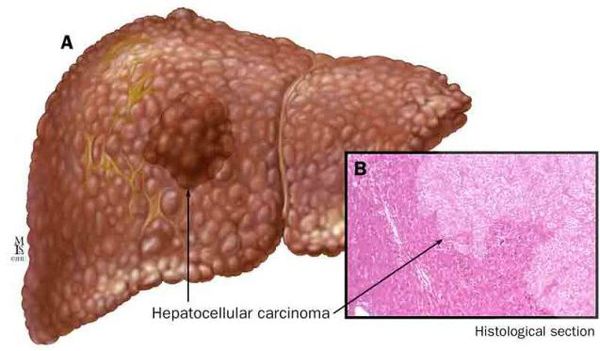
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени — гепатоцеллюлярную карциному. [9] Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов. [7]
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
Кода первые два этапа завершены, исследуется структурное состояние печени при помощи УЗИ [4] , МСКТ, МРТ и эластометрии (FibroScan), при необходимости исследуется морфологическое состояние — биопсия печени. [3]
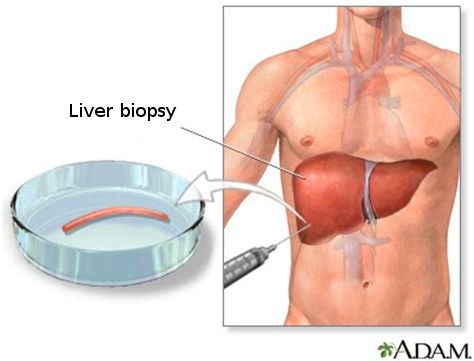
С помощью эластометрии исследуется эластичность мягких тканей. Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
В процессе лечения производится:
- коррекция углеводного, жирового (липидного) обмена веществ;
- нормализация процессов окисления в клетке;
- влияние на основные факторы риска;
- снижение массы тела;
- улучшение структуры печени на обратимых стадиях.
После лечения наступает заметное улучшение дезинтоксикационной (защитной), пищеварительной и метаболической функции печени, пациенты теряют в весе, улучшается общее самочувствие, повышается умственная и физическая работоспособность.
Курсовые программы лечения занимают от трёх до шести месяцев и подбираются в зависимости от степени выраженности метаболических нарушений. К ним относятся:
Программы включают в себя предварительное обследование, постановку диагноза и медикаментозное лечение, которое состоит из двух этапов:
- инфузионная терапия с пролонгацией приёма препаратов внутрь, подбор диеты и физической активности;
- сдача контрольных анализов и оценка результатов.
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Жировой гепатоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Жировой гепатоз (жировая дистрофия печени, стеатоз) — заболевание, при котором в клетках печени накапливается жир. При этом воспалительные явления отсутствуют или выражены слабо. Накопление жира может быть реакцией печени на различные токсические воздействия, например, употребление алкоголя, прием некоторых лекарственных препаратов, нередко этот процесс связан с метаболическим синдромом.
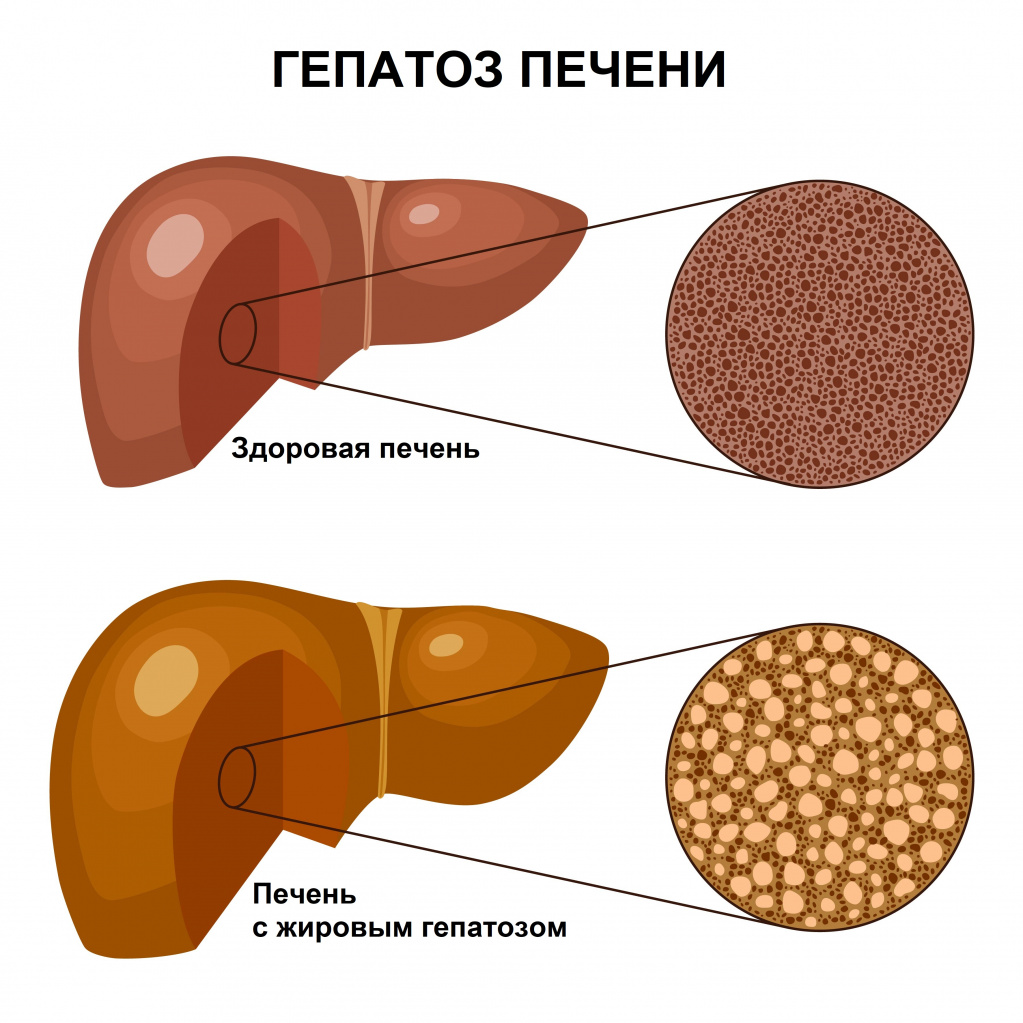
В зависимости от этиологии повреждения выделяют две группы заболеваний: неалкогольную жировую болезнь печени (НАЖБП) и алкогольную болезнь печени (АБП). Каждое из этих заболеваний может ограничиться гепатозом, а может прогрессировать до гепатита (воспалительного заболевания печени) или даже цирроза (замещения ткани печени соединительной тканью). Все это – стадии одного процесса.
Причины появления гепатоза
Главная причина развития и прогрессирования НАЖБП - нездоровый образ жизни: высококалорийное питание, избыточное потребление насыщенных жиров (продуктов животного происхождения – жирных сортов мяса, молочных продуктов высокой жирности), рафинированных углеводов (сахара, хлебобулочных и кондитерских изделий) в сочетании с недостаточной физической активностью.
Метаболический синдром – это комплекс метаболических, гормональных и клинических нарушений, являющихся факторами риска развития сердечно-сосудистых заболеваний, в основе которых лежит инсулинорезистентность и компенсаторная гиперинсулинемия.
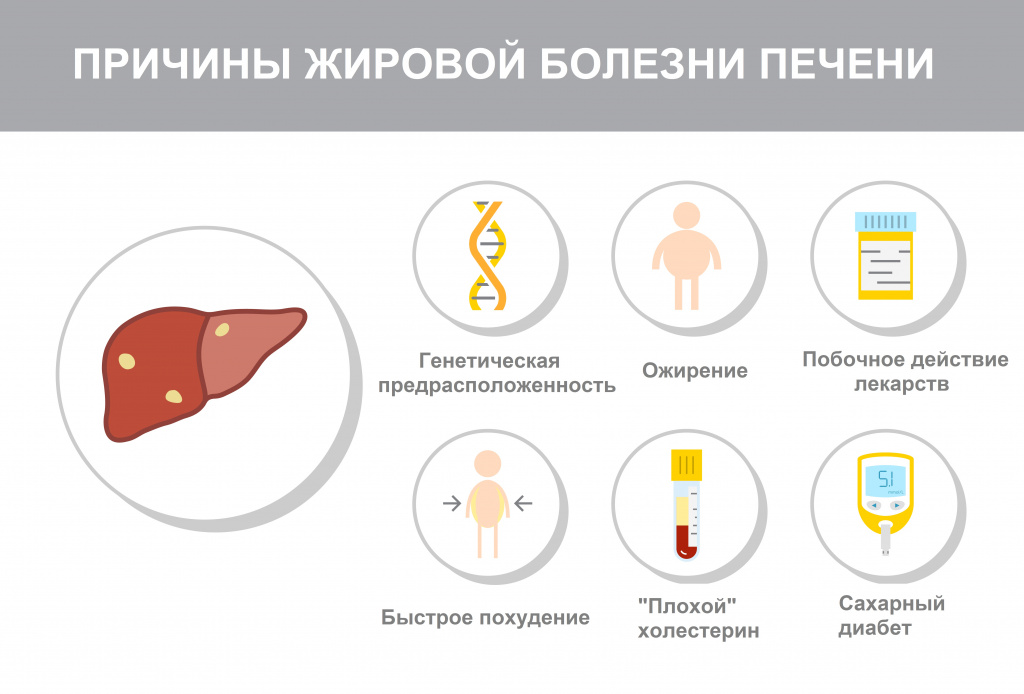
Инсулин – это гормон, вырабатываемый поджелудочной железой и обеспечивающий поступление глюкозы из крови в клетки. При инсулинорезистентности снижается чувствительность клеток к инсулину – возникает голодание клеток на фоне достаточного количества глюкозы в крови. Для поддержания нормального транспорта глюкозы требуется повышенная концентрация инсулина в крови, что и становится спусковым механизмом всех составляющих метаболического синдрома:
Важным критерием, позволяющим отличить АБП от НАЖБП, служит употребление пациентами алкоголя в токсичных для печени дозах, т.е. более 40 г чистого этанола в сутки для мужчин и более 20 г для женщин.
Однако вероятность поражения печени зависит не только от количества потребляемых спиртных напитков, но и от качества алкогольного напитка, типа потребления алкоголя и времени его воздействия, а также от индивидуальной и генетической предрасположенности, особенностей питания, инфицирования вирусами гепатита В и С.
Классификация гепатоза
В зависимости от типа отложения жира:
- очаговый диссеминированный гепатоз (зачастую не имеет клинических проявлений);
- выраженный диссеминированный гепатоз;
- зональный гепатоз (жир накапливается в разных отделах печени);
- диффузный гепатоз (микровезикулярный стеатоз).
Симптомы гепатоза
Большинство пациентов с гепатозом не предъявляют никаких жалоб. Болезнь нередко диагностируют случайно при обследовании по другому поводу. В случае неалкогольной жировой болезни печени у некоторых пациентов в клинической картине присутствуют различные проявления метаболического синдрома: ожирение, повышение артериального давления, признаки нарушения обмена глюкозы, холестерина.
Часть пациентов с гепатозом, независимо от его этиологии, предъявляет жалобы неспецифического характера - на повышенную утомляемость, ноющую боль или дискомфорт в области правого подреберья без четкой связи с приемом пищи.
Диагностика гепатоза
Нередко врач может заподозрить у пациента наличие гепатоза уже в процессе сбора анамнеза. Специалист оценивает режим питания и физическую активность, уточняет вопрос об употреблении алкоголя, приеме лекарственных препаратов.
При разговоре с пациентом и ознакомлении с медицинской документацией врач может обнаружить проявления метаболического синдрома, что будет говорить в пользу НАЖБП.
Важная роль в оценке состояния печени принадлежит лабораторной диагностике. Исследуют такие показатели биохимического анализа крови, как АсАТ, АлАТ, гамма-глутамилтранспептидаза, щелочная фосфатаза, билирубин общий, билирубин прямой. При гепатозе может определяться их незначительное повышение.
Определение уровня АСТ в сыворотке крови используют преимущественно в диагностике и контроле течения болезней печени, а также в комплексных биохимических исследованиях.
Жировая дегенерация печени является одной из форм неалкогольной жировой болезни печени (НАЖБП).
3. Неалкогольный цирроз печени (NASH Cirrhosis). Наличие признаков цирроза с текущими или предыдущими гистологическими признаками стеатоза или стеатогепатита.
4. Криптогенный цирроз (Cryptogenic Cirrhosis) - цирроз без очевидных этиологических причин. Пациенты с криптогенным циррозом обычно имеют высокие факторы риска, ассоциированные с метаболическими расстройствами, такими как ожирение и метаболический синдром. Всё чаще криптогенный цирроз, при детальной проверке, оказывается заболеванием, ассоциированным с алкоголем.
5. Оценка активности НАЖБП (NAS). Совокупность баллов, вычисляемая при комплексной оценке признаков стеатоза, воспаления и балонной дистрофии. Является полезным инструментом для полуколичественного измерения гистологических изменений ткани печени у пациентов с НАЖБП в клинических испытаниях.
К настоящему времени в перечне заболеваний МКБ-10 отсутствует единый код, отражающий полноту диагноза НАЖБП, поэтому целесообразно использовать один из нижеприведенных кодов:
- К 76.0 - Жировая дегенерация печени, не классифицированная в других рубриках
- K75.81 - Неалкогольный стеатогепатит (НАСГ)
- K74.0 - Фиброз печени
- К 74.6 - Другой и неуточненный цирроз печени.\

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Типы жировой дегенерации печени:
1. Макровезикулярный тип. Накопление жира в гепатицитах носит локальный характер и ядро гепатоцита сдвигается в сторону от центра. При жировой инфильтрации печени макровезикулярного (крупнокапельного) типа в качестве аккумулируемых липидов, как правило, выступают триглицериды. При этом морфологическим критерием жирового гепатоза является содержание триглицеридов в печени свыше 10% сухой массы.
2. Микровезикулярный тип. Накопление жира происходит равномерно и ядро остается на месте. При микровезикулярной (мелкокапельной) жировой дегенерации скапливаются другие ( не триглицериды) липиды (например, свободные жирные кислоты).
Выделяют также очаговый и диффузный стеатоз печени. Чаще всего встречается диффузный стеатоз, который носит зональный характер (вторая и третья зона дольки).
Этиология и патогенез
Вторичная жировая болезнь печени может быть результатом следующих факторов.
1. Алиментарные факторы:
- резкое снижение массы тела;
- хроническая белково-энергетическая недостаточность.
2. Парентеральное питание (в т.ч введение глюкозы).
4. Метаболические заболевания:
- дислипидемии;
- сахарный диабет II типа;
- триглицеридемия и др.
Эпидемиология
Признак распространенности: Распространено
Соотношение полов(м/ж): 0.8
Точные данные о распространенности жировой дегенерации печени отсутствуют.
Предположительно распространенность составляет от 1% до 25% от общей популяции в различных странах. В развитых странах средний уровень - 2-9%. Многие находки случайно обнаруживаются во время биопсии печени, выполняемой по другим показаниям.
Наиболее часто заболевание выявляется в возрасте 40-60 лет, хотя ни один возраст (кроме детей на грудном вскармливании) не исключает диагноз.
Соотношение полов неизвестно, но предполагается превалирование женского пола.
Факторы и группы риска
В группу высокого риска входят:
2. Лица сахарным диабетом 2-го типа или нарушением толерантности к глюкозе. У 60% больных эти состояния встречаются в комплексе с жировой дистрофией, у 15% - с неалкогольным стеатогепатитом. Тяжесть поражения печени имеет связь с тяжестью нарушения обмена глюкозы.
3. Лица с диагностированной гиперлипидемией, которая выявляется у 20-80% больных неалкогольным стеатогепатитом. Характерным фактом является более частое сочетание неалкогольного стеатогепатита с гипертриглицеридемией, чем с гиперхолестеринемией.
4. Женщины среднего возраста.
Клиническая картина
Клинические критерии диагностики
ожирение; слабость; гепатомегалия; спленомегалия; дискомфорт в правом верхнем отделе живота; артериальная гипертензия
Cимптомы, течение
У большинства больных неалкогольной жировой болезнью печени жалобы отсутствуют.
Могут проявляться следующие симптомы:
- незначительный дискомфорт в верхнем правом квадранте живота (около 50%);
- боль в верхнем правом квадранте живота (30%);
- слабость (60-70%);
- умеренная гепатоспленомегалия Гепатоспленомегалия - одновременное значительное увеличение печени и селезенки
(50-70%).
Диагностика
Общие положения. На практике подозрение на неалкогольный стеатогепатит возникает при наличии у пациента ожирения, гипертриглицеридемии и повышения уровня трансаминаз. Диагноз уточняется лабораторно и с помощью биопсии. Методы визуализации для подтверждения на ранних стадиях пригодны мало.
Анамнез: исключение злоупотребления алкоголем, лекарственных поражений, семейного анамнеза заболеваний печени.
При диагностике неалкогольной жировой болезни печени применяются следующие методы визуализации:
1. УЗИ. Стеатоз может быть подтвержден при условии, что повышение количества жировых включений в ткани составляет не менее 30%. УЗИ имеет чувствительность 83% и специфичность 98%. Выявляют повышенную эхогенность печени и усиление дистального затухания звука. Возможна гепатомегалия . Также осуществляются выявление признаков портальной гипертензии, косвенная оценка степени стеатоза. Хорошие результаты получены при использовании аппарата Фиброскан, который позволяет дополнительно выявлять фиброз и оценивать его степень.
2. Компьютерная томография. Основные КТ-признаки:
- снижение рентгенологической плотности печени на 3-5 HU (норма 50-75 HU);
- рентгенологическая плотность печени меньше рентгенологической плотности селезенки;
- более высокая плотность внутрипеченочных сосудов, воротной и нижней полой вен по сравнению с плотностью печеночной ткани.
3. Магнитно-резонансная томография. Может полуколичественно оценить содержание жира в печени . Превосходит по диагностическим способностям УЗИ и КТ. Очаги снижения интенсивности сигнала на Т1-взвешенных изображениях могут свидетельствовать о локальном накоплении жира в печени.
5. Гистологическое исследование пунктата печени (золотой стандарт диагностики):
- крупнокапельная жировая дистрофия;
- балонная дистрофия или дегенерация гепатоцитов (при наличии/отсутствии воспаления, гиалиновых телец Маллори, фиброза или цирроза).
Степень стеатоза оценивается по бальной системе.
Оценка стеатоза печени у больных НАЖБП (система D.E.Kleiner CRN, 2005)
| Баллы | Степень выраженности стеатоза | Содержание жировой ткани в гепатоците |
| 0 | Отсутствие стеатоза | |
| 1 | Минимальная | ≤ 5-33% |
| 2 | Умеренная | 33-66% |
| 3 | Выраженная | > 66% |
Лабораторная диагностика
2. У 30-60% больных выявляют повышение активности щелочной фосфатазы (как правило, не более чем двукратное) и гамма-глутамилтранспептидазы (может быть изолированным, не связанным с повышением ЩФ). Уровень ГГТП > 96,5 Ед/л увеличивает риск наличия фиброза.
3. В 12-17% случаев встречается гипербилирубинемия в пределах 150-200% от нормы.
4. Признаки снижения белково-синтетической функции печени развиваются только при формировании цирроза печени. Наличие гипоальбуминемии без перехода в цирроз возможно у больных с диабетической нефропатией Нефропатия - общее название некоторых видов поражений почек.
.
5. У 10-25% больных выявляют незначительную гипергаммаглобулинемию.
6. У 98% пациентов наблюдается инсулинорезистентность. Ее выявление - важнейший неинвазивный метод диагностики.
В клинической практике инсулинорезистентность оценивают по соотношению уровней иммунореактивного инсулина и глюкозы в крови. Следует помнить, что это расчетный показатель, который вычисляется различными методиками. На показатель влияют уровень триглицеридов в крови и расовая принадлежность.
Исследование уровня инсулина рекомендуется проводить натощак.
7. У 20-80% пациентов с НАСГ наблюдается гипертриглицеридемия.
Многие пациенты будут иметь низкий уровень ЛПВП в рамках метаболического синдрома.
При прогрессировании заболевания нередко снижается уровень холестерина.
8. Серология: наличие любых серологических маркеров иных процессов (вирусных, аутоиммунных, паразитарных) исключает диагноз НАСГ.
Следует иметь в виду, что низкий уровень положительного титра антинуклеарных антител - не редкость при НАСГ, а также менее 5% пациентов могут иметь положительный низкий титр антител к гладкой мускулатуре.
10. Определение уровня фрагментов цитокератина 18 (TPS-test) - перспективный метод исследования активности процесса. Метод позволяет отличить наличие апоптоза гепатоцитов (гепатита) от жировой инфильтрации печени без использования биопсии.
К сожалению, данный показатель не специфичен; в случае его повышения необходимо исключать ряд онкологических заболеваний (мочевого пузыря, молочной железы и др.).
11. Комплексные биохимические тесты (BioPredictive, Франция):
- Стеато-тест - позволяет выявить наличие и степень стеатоза печени;
- Нэш-тест - позволяет выявить НАСГ у пациентов с избыточной массой тела, резистентностью к инсулину, гиперлипидемией, а также пациентов, больных сахарным диабетом).
Возможно использование других тестов при подозрении на неалкогольный фиброз или гепатит - Фибро-тест и Акти-тест.
Дифференциальный диагноз
Неалкогольная жировая болезнь печени дифференцируется со следующими заболеваниями:
- гепатиты различной установленной этиологии, в первую очередь - хронические гепатиты В, С, D, E, аутоиммунный гепатит и другие;
- алкогольная болезнь печени;
- вторичная жировая болезнь печени (лекарственный гепатит, метаболические нарушения, например, при болезни Вильсона , гемохроматозе или дефиците альфа-1-антитрипсина);
- идиопатические фиброз, склероз, цирроз печени;
- первичный склерозирующий холангит;
- первичный билиарный цирроз;
- гипотиреоз и гипертиреоз;
- отравление витамином А.
Практически вся дифференциальная диагностика построена на лабораторных тестах, специфичных для перечисленных выше заболеваний, и исследованиях биопсии.
Осложнения
Лечение
Общие положения
Нет никаких лекарственных препаратов, эффективность которых при лечении идиопатической неалкогольной жировой дистрофии доказана. Основной упор делается на модификацию образа жизни.
Изменение образа жизни должно быть основой для первой линии терапии. Другие патогенетические подходы могут быть применены при доказанных значимых этиологических причинах.
Цели лечения:
- нормализация биохимических параметров;
- уменьшение инсулинорезистентности;
- улучшение гистологической картины печени.
Контроль веса
Потеря избыточного веса пациента приводит к снижению резистентности к инсулину и улучшению мышечной чувствительности к инсулину. Исследования показали нормализацию ферментов и улучшение гистологической картины при снижении индекса массы тела (ИМТ).
Потеря веса должна быть постепенной: примерно от 0,5 до 1,0 кг в неделю. Рекомендуются:
- диета (ограничение углеводов, насыщенных жиров и калоража на 500-1000 ккал/сут.);
- регулярные аэробные упражнения (30 минут, 3-5 раз в неделю, затем до часа в день );
- в отдельных случаях допустимо применение орлистата; сибутрамин исключен из списков фармакологических средств, применяемых с целью снижения веса.
Медикаментозная терапия
1. Лечение инсулинорезистентности проводится по общим правилам для сахарного диабета и включает:
- метформин;
- розиглитазон;
- пиоглитазон.
2. Гиполипидемическая терапия.
Следует придерживаться рекомендаций по лечению конкретных дислипидемий. Наиболее часто применяемые препараты:
- аторвастатин (10 мг/сут. курсом до 2 лет);
- гемфиброзил;
- пробукол (эффект сомнителен).
3. Гепатопротективная терапия (эффективность препаратов при неалкогольной жировой болезни печени, кроме витамина Е, не изучались рандомизированных контролируемых исследованиях):
- антиоксиданты - витамин Е (300 МЕ, 2-10 месяцев), липоевая кислота 600 мг/сутки - 4 месяца;
- блокаторы ФНО-альфа - пентоксифиллин 400 мг, 2 раза в сутки, до 1 года;
- усиление выведения триглицеридов из гепатоцита - бетаин 20 мг в сутки (1 год), S-аденозилметионин 400 мг/сут., не менее трех месяцев.
4. Коррекция кишечной микрофлоры при вторичной форме (метронидазол 750 мг/сут., 7-10 дней).
В условиях прогрессирования печеночной недостаточности может возникнуть необходимость проведения трансплантации печени.
Прогноз
Ожидаемая продолжительность жизни при неалкогольной жировой болезни печени не ниже, чем у здоровых лиц.
У половины больных развивается прогрессирующий фиброз, а у 1/6 - цирроз печени.
При отсутствии адекватного лечения у пациентов с установленным диагнозом "неалкогольный стеатогепатит" в 20-37% случаев наблюдается прогрессирование воспаления и фиброза. Цирроз печени развивается у 10-20% больных.
При неалкогольном стеатогепатите 5-летняя выживаемость составляет 67%, 10-летняя - 59%. Следует учитывать, что данные показатели летальности могут быть обусловлены другими проявлениями метаболического синдрома.
Смертность, ассоциированная с циррозом в исходе неалкогольного стеатогепатита, составляет от 5% до 25%.
Госпитализация
- печеночная недостаточность;
- впервые выявленные и прогрессирующие другие проявления метаболического синдрома.
Профилактика
1. Нормализация массы тела.
2. Пациенты должны быть обследованы на вирусы гепатита. В случае отсутствия заболевания вирусным гепатитом, им должна быть предложена вакцинация от гепатитов В и А.
Читайте также:

