Трансплантация поджелудочной железы реферат
Обновлено: 04.07.2024
Более 90% трансплантаций поджелудочной железы включают трансплантацию почки.
Во многих центрах критериями выбора этого метода лечения также являются повторный отказ от контроля гликемии с применением стандартного лечения и случаи необъяснимой гипогликемии.
Относительными противопоказаниями являются возраст > 55 лет, серьезные сердечно-сосудистые атеросклеротические заболевания, предварительный инфаркт миокарда, хирургический шунт-трансплантат коронарной артерии, чрескожные коронарные вмешательства или положительный стресс-тест; эти факторы существенно повышают периоперационный риск.
Варианты трансплантации включают:
Одновременную трансплантацию поджелудочной железы, почек (ОПЖП)
Трансплантацию поджелудочной железы после почки (ПЖП)
Трансплантацию только поджелудочной железы
Преимуществами сочетанной трансплантации поджелудочной железы и почки являются одновременное воздействие иммуносупрессантов на оба органа сразу, потенциальная защита пересаженной почки от неблагоприятного воздействия гипергликемии и возможность контролировать отторжение почки, кроме этого почки более склонны к отторжению, нежели поджелудочная железа, чье отторжение трудно отследить.
Преимуществом трансплантации поджелудочной железы после почки является возможность оптимизировать подбор по главному комплексу гистосовместимости человека (HLA) и время выполнения трансплантации почек при использовании органа живого донора.
Трансплантация только поджелудочной железы используется главным образом для пациентов, не имеющих терминальной стадии заболеваний почек, но с тяжелой формой осложненного диабета, включая недостаточный контроль уровня глюкозы крови.
Доноры поджелудочной железы
Донорами являются недавно умершие пациенты в возрасте 10–55 лет, не имеющие в анамнезе непереносимости глюкозы и не злоупотреблявшие алкоголем.
Проводится небольшое количество (менее 1%) сегментарных трансплантаций от живых доноров, но такая процедура несет существенный риск для донора (например, инфаркт селезенки, абсцесс, панкреатит, подтекание панкреатического сока и псевдокиста, вторичный диабет), что ограничивает ее широкое применение.
Процедура трансплантации поджелудочной железы
Донору проводится антикоагуляция, и через чревную артерию вводится холодный консервирующий раствор. Поджелудочная железа охлаждается in situ ледяным солевым раствором, удаляется сразу вместе с печенью (для трансплантации разным реципиентам) и 2-ой частью двенадцатиперстной кишки, содержащей фатеров сосок. Подвздошная артерия также удаляется.
Донорская поджелудочная железа размещается интраперитонеально и латерально в нижней части брюшной полости.
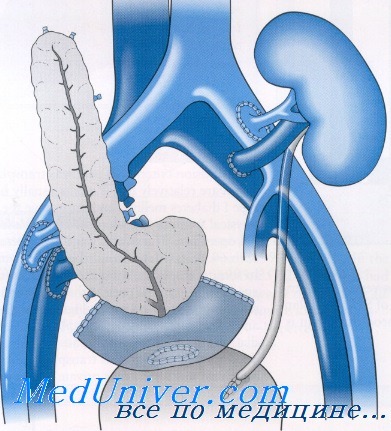
В случае сочетанной трансплантации поджелудочной железы и почки поджелудочную железу располагают в правой средней зоне брюшной полости, а почку – в левом нижнем квадранте. Собственная поджелудочная железа остается на месте. Донорская подвздошная артерия используется для реконструкции в операционной, чтобы восстановить селезеночную артерию и верхнюю брыжеечную артерию поджелудочной железы трансплантата. Этот метод приводит к использованию одной артерии для подключения к кровеносным сосудам реципиента. Окончательные анастомозы формируются между донорской подвздошной артерией и подвздошной артерией реципиента и между донорской портальной веной и подвздошной веной реципиента. Таким образом, эндокринные секреты систематически поступают в кровоток, приводя к гиперинсулинемии; иногда формируют анастомозы между донорской панкреатической венозной системой и портальной веной, дополнительно для восстановления нормального физиологического состояния, хотя эта процедура более травматичная, и ее преимущества не вполне ясны. Двенадцатиперстная кишка подшивается к верхушке желчного пузыря или к тощей кишке для дренажа экзокринного секрета.
Осложнения при трансплантации поджелудочной железы
Отторжение
При проведении сочетанной трансплантации почки и поджелудочной железы и трансплантации поджелудочной железы после трансплантации почки, отторжение поджелудочной железы лучше всего обнаруживается увеличением креатинина сыворотки, потому что отторжение поджелудочной железы почти всегда сопровождается отторжением почек. После проведения трансплантации только поджелудочной железы устойчивая концентрация амилазы в моче у пациентов с нормальным оттоком мочи исключает отторжение; ее уменьшение предполагает некоторые формы дисфункции трансплантата, но не является специфическим для реакции отторжения. Поэтому ранняя диагностика затруднена.
Диагноз ставится на основании данных цистоскопической трансдуоденальной биопсии, выполняемой под контролем ультразвука.
Лечение проводится антитимоцитарным глобулином.
Другие осложнения
Ранние осложнения отмечаются у 10–15% пациентов и включают раневую инфекцию и расхождение швов, значительную гематурию, интраабдоминальное подтекание мочи, рефлюксный панкреатит, рецидивирующие инфекции мочевых путей, обструкцию тонкого кишечника, абдоминальный абсцесс и тромбоз трансплантата.
Поздние осложнения связаны с потерей с мочой панкреатического бикарбоната натрия (NaHCO3–), что приводит к уменьшению объема циркулирующей крови и метаболическому ацидозу без анионного провала. Гиперинсулинемия, по-видимому, не оказывает отрицательного влияния на метаболизм глюкозы или липидов.
Прогноз при трансплантации поджелудочной железы
В целом, показатели выживаемости в течение первого года составляют
Неизвестно, выше ли показатель выживания у пациентов после трансплантации по сравнению с пациентами, которым трансплантация не выполнялась; однако основными преимуществами этой процедуры является устранение необходимости в применении инсулиновой терапии и стабилизация или некоторое улучшение многих осложнений диабета (например, нефропатия, нейропатия).
Скорость иммунологической потери трансплантата при трансплантации поджелудочной железы после почки и трансплантации только поджелудочной железы выше, возможно, потому что при трансплантации только поджелудочной железы нет надежного способа контролировать отторжение; в отличие от этого, отторжение после одновременной трансплантации поджелудочной железы и почки можно контролировать с использованием установленных показателей отторжения трансплантированной почки.
История клинической трансплантации поджелудочной железы развивалась на фоне постоянного совершенствования техники оперативного вмешательства.
Первая попытка лечения СД трансплантационными методами была выполнена задолго до того, как De Mayer в 1909 г. дал название теоретически обоснованной эндокринной субстанции поджелудочной железы — инсулин, a F.G. Banting и С.Н. Best в 1921 г. выделили ее и таким образом открыли новую эпоху в лечении диабета. В декабре 1983 г., через 3 года после того, как J. von Mering и О. Minkowski экспериментально показали, что панкреатэктомия приводит к развитию сахарного диабета у собак, P. Williams в Бристоле пересадил 3 фрагмента овечьей поджелудочной железы в подкожную клетчатку 15-летнему пациенту, спустя 5 месяцев от клинической манифестации заболевания. Больной умер через 3 суток на фоне прогрессирующего кетоацидоза. Тем не менее этот эксперимент послужил мощным толчком к пониманию патогенеза заболевания и роли поджелудочной железы в углеводном обмене.
Вторую пересадку поджелудочной железы осуществила та же бригада хирургов. 31 декабря 1966 г. они выполнили аллогенную трансплантацию панкреатодуоденального комплекса (АТПДК) и почки 32-летнему пациенту, с наложением анастомоза между дистальной частью донорской duodenum и начальным отделом тощей кишки реципиента. В послеоперационном периоде дважды развивалась реакция отторжения трансплантата. Через 4,5 месяца на фоне септического состояния пациент скончался. К этому моменту инсулинотерапия проводилась в первоначальном объеме.
В 1978 г. J. Dubernard предложил оригинальную методику сегментарной трансплантации поджелудочной железы с окклюзией панкреатических протоков синтетическим отвердевающим полимером неопреном. По этой методике 3—10 мл неопрена инъецировались непосредственно в выводящие протоки сегмента поджелудочной железы, с последующим лигированием протоков для предотвращения экстравазации. Артериальное кровоснабжение хвоста и тела поджелудочной железы осуществлялось по селезеночной артерии, а венозный отток — через селезеночную вену, анастомозированным с наружными подвздошными сосудами реципиента.
Преимущество методики в том, что операция, по существу, сводится к наложению сосудистых анастомозов.
Окклюзия протоковой системы поджелудочной железы производится в ходе ее изъятия у донора, либо непосредственно перед наложением сосудистых анастомозов, либо через 10—14 дней после операции. В последнем случае в просвет главного панкреатического протока вводился полиэтиленовый катетер для наружного отведения экзокринного секрета и промывания протоковой системы железы с целью снижения явлений послеоперационного панкреатита.
Главный же недостаток трансплантации поджелудочной железы с окклюзией протоков — невозможность контроля уровня амилазы в экзогенном секрете. Между тем именно этот показатель зачастую служит главным маркером реакции отторжения поджелудочной железы.
Кроме того, введение неопрена вызывает прогрессирующий фиброз трансплантата и увеличивает частоту реакций отторжения.
В результате эндокринная функция большинства трансплантатов утрачивалась в среднем через 1 год после успешной пересадки, поэтому с появлением новых способов интерес к данной методике снизился. Тем не менее в некоторых европейских трансплантационных центрах метод по-прежнему используется.
Еще в 1971 г. M.L. Gliedman предложил оригинальную методику трансплантации сегмента поджелудочной железы с выведением экзокринного секрета в мочеточник (после предварительной нефрэктомии) у пациентов, находящихся в терминальной стадии диабетической нефропатии. К 1973 г. Gliedman сообщил о результатах четырех подобных трансплантаций сегментов поджелудочной железы.
На основе принципа отведения панкреатического сока в мочевы водящие пути (bladder drainage — BD) в дальнейшем было разработано множество способов трансплантации поджелудочной железы. В 1983 г. Н. Sollinger предложил отводить секрет в мочевой пузырь не посредством дуктоуретероанастомоза с нативным мочеточником реципиента, а с помощью панкреатикоцистостомии.
Но полное признание и повсеместное распространение пересадка поджелудочной железы по типу BD получила только с 1987 г., когда D.D. Nghiem и R.J. Сопу предложили использовать для анастомоза с мочевым пузырем нисходящую часть 12-перстной кишки донора с сохраненным дуоденальным сосочком и неповрежденным Вирсунговым протоком.
В настоящее время за редким исключением трансплантация поджелудочной железы по типу BD выполняется следующим образом: после МОЗ на отдельном столе проводится разделение блока печень — поджелудочная железа и/или проводится предоперационная подготовка изолированного трансплантата поджелудочной железы.
Селезенку отделяют, а селезеночные сосуды надежно перевязывают лигатурами, клипируют или прошивают степлером. Длина нисходящего участка 12-перстной кишки с головкой поджелудочной железы и большим дуоденальным сосочком рекомендуется в пределах 6—10 см; после орошения просвета кишки раствором антисептиков и противогрибковых препаратов обе культи кишки прошиваются степлером и погружаются кишечным швом по Lembert.
Селезеночную и верхнюю брыжеечную артерии трансплантата анастомозируют с общими подвздошными артериями V-образного сосудистого трансплантата, полученного от того же донора.
Производят срединную лапаротомию: этот доступ снижает риск раневой инфекции в послеоперационном периоде и позволяет выполнить одновременную пересадку поджелудочной железы и почки из одного разреза. Нередко используется и параректальный доступ.
Лапаротомная рана ушивается послойно наглухо без дренирования брюшной полости. При необходимости дренирования дренажная трубка располагается непосредственно у сосудистых анастомозов и выводится наружу через контрапертуру.
Некоторые хирурги предпочитают экстраперитонеальную трансплантацию поджелудочной железы в одну из подвздошных ямок; оперативный доступ в этом случае будет аналогичен доступу, используемому для пересадки почки.
АТПЖ по типу BD обладает рядом неоспоримых преимуществ. Выведение экзокринного секрета в мочевой пузырь позволяет отслеживать уровень вырабатываемой трансплантатом амилазы и наличие воспалительных клеток с помощью анализа мочи и выявлять реакцию отторжения на ранних сроках. Отсутствие контакта с кишечным содержимым позволяет уменьшить опасность инфицирования протоков трансплантата поджелудочной железы, а мочевой катетер помогает контролировать состояние дуоденоцистоанастомоза.
Выживаемость трансплантата поджелудочной железы после изолированной пересадки по этому способу и по настоящее время существенно выше в сравнении с остальными. Однако наряду с достоинствами эта методика имеет и существенные недостатки: высокая частота инфекции мочевыводящих путей, гематурия, камнеобразование, мочевые затеки, панкреатит трансплантата поджелудочной железы, цистит, а также метаболический ацидоз и дегидратация за счет хронической потери жидкости и бикарбонатов с панкреатическим секретом. Поэтому с 1998 г. в мировой практике чаще используют отведение экзокринного секрета трансплантата поджелудочной железы в просвет кишечника реципиента.
Задача создания естественного, наиболее физиологичного дренирования панкреатического сока во внутрикишечное пространство стояла перед хирургами с самого начала освоения проблемы пересадки поджелудочной железы.
Трансплантации ПДК с наложением дуоденоеюноанастомоза были пионерскими операциями пересадки поджелудочной железы. Даже при сегментарных трансплантациях предпринимались попытки наложения инвагинационно-го панкреатикоеюноанастомоза. Однако частые осложнения в виде некрозов 12-перстной кишки и формирования фистул, связанные с ишемическим повреждением, скомпрометировали этот принцип. С совершенствованием методов консервации органов и прогрессом в области иммуносупрессии, приведшим к снижению риска ишемического или иммунологического повреждения двенадцатиперстной кишки, с начала 1990-х гг. интерес к возможности интестинального дренирования внешнего секрета трансплантированной поджелудочной железы (enteric drainage — ED) возродился.
На сегодняшний день пересадка поджелудочной железы по типу ED служит операцией выбора при SKPT и РАК.
По данным международного регистра, выживаемость пациентов после SKPT и РАК по типу ED значительно выше, чем по BD-методике, при том, что выживаемость трансплантатов различается незначительно. От 10 до 28% больных, ранее оперированных по BD-методике, в последующем подвергаются релапаротомии и реконструктивной операции по ED-типу в связи с развитием урологических осложнений.
Операционную рану закрывают послойно наглухо, при необходимости дренируют брюшную полость через отдельный прокол.
ED-вариант трансплантации поджелудочной железы имеет несколько модификаций. Некоторые хирурги использует для кишечного дренирования трансплантата Roux-петлю, сформированную из тощей или даже подвздошной кишки, при этом головка поджелудочной железы может быть направлена краниально, каудально или латерально. При анализе результатов как достоверных преимуществ, так и недостатков использования Roux-en-V петли не выявлено.
Заслуживает внимания способ дренирования Вирсунгова протока ПВХ-катетером, последовательно выведенным наружу через дуоденоеюноанастомоз и сформированную энтеростому. Метод позволяет контролировать функцию трансплантата по составу и динамике выделения панкреатического сока, на ранних сроках диагностировать реакцию отторжения, проводить профилактику ишемического панкреатита. Однако в связи с высоким риском инфекционных осложнений на фоне иммуносупрессивной терапии модификация не получила широкого распространения.
Обоснованием этого считают отмеченные в ряде исследований случаи гиперинсулинемии за счет попадания секретируемого трансплантатом инсулина непосредственно в системный кровоток, минуя печеночный этап регуляции углеводного обмена. Однако практически незначительные преимущества портального дренирования связаны с немалыми техническими трудностями, и большинство хирургов выбирает системное отведение крови от ПДК, тем более что факт послеоперационной гиперинсулинемии в этом случае признают далеко не все исследователи.
Недостатки АТПДК с отведением панкреатического сока в просвет кишечника: во-первых, высокий риск хирургических послеоперационных осложнений (кишечная непроходимость и несостоятельность межкишечного анастомоза); во-вторых, невозможность использовать показатели внешней секреции железы в качестве маркера воспалительных или иммунологических осложнений.
Таким образом, в настоящее время используются три основных метода трансплантации поджелудочной железы. При выполнении АТПДК одновременно или после пересадки почки предпочтительнее использовать различные варианты интестинального дренирования экзокринного секрета трансплантата. АТПЖ с отведением панкреатического сока в мочевыводящие пути преимущественно используется при изолированных пересадках поджелудочной железы в случаях гиперлабильного диабета и предуремической диабетической нефро-патии. Сегментарная АТПЖ с окклюзией панкреатических протоков может быть рекомендована одновременно с пересадкой почки ослабленным больным, а также при длительных сроках консервации или значительном ишемическом повреждении трансплантата поджелудочной железы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

