Современные представления о природе стволовых клеток реферат
Обновлено: 04.07.2024
Биология стволовых клеток , с одной стороны, оказывает огромное влияние на здоровье и качество жизни людей, а с другой - объединяет широкий круг фундаментальных и прикладных исследований в области молекулярной и клеточной биологии. Изучение стволовых клеток приближает нас к пониманию глубинных основ жизни. В то же время проблема стволовых клеток имеет огромный общественный резонанс, она обсуждается с точки зрения политики, религии, этики и экономики. Интерес общественности связан, в первую очередь, с потенциальной возможностью использования стволовых клеток для лечения таких болезней, как диабет, болезни Паркинсона, Альцгеймера, врожденные болезни сердца и др., а также озабоченностью этическими проблемами связанными с использованием стволовых клеток.
Классические представления о стволовых клетках сегодня сильно меняются. Согласно установившимся взглядам, взрослые стволовые клетки могут производить только клетки тех тканей , в которых они находятся . В отличие от них эмбриональные стволовые клетки, которые научились выращивать в культуре, могут давать начало любым типам клеток организма.
Однако последние исследования приносят все новые и новые сведения, согласно которым стволовые клетки обладают значительной пластичностью, когда стволовые клетки одного типа могут дифференцироваться в клетки других тканей и органов. Например, клетки крови - в клетки мозга , клетки крови - в клетки печени , клетки мозга - в клетки сердца и др. Если будет доказана пластичность стволовых клеток и возможность индуцировать плюрипотентные стволовые клетки в культуре, то перед врачами откроются неограниченные возможности. Появится возможность получать стволовые клетки из таких органов, откуда их легко выделить в больших количествах и после трансдифференциации использовать для восстановления пораженных органов и тканей. Очень интересна проблема клонирования путем переноса ядер (репродуктивное клонирование), когда в неоплодотворенное яйцо (из которого удален собственный генетический материал) переносится ядро соматической клетки и затем стимулируется развитие организма. Этот метод используется для выделения сельскохозяйственных животных, в том числе овец и коров.
* Данная работа не является научным трудом, не является выпускной квалификационной работой и представляет собой результат обработки, структурирования и форматирования собранной информации, предназначенной для использования в качестве источника материала при самостоятельной подготовки учебных работ.
Глава1 Описание, свойства и типы стволовых клеток………………. 5
Глава 2 История открытия стволовых клеток…………………………. 9
Глава 3 Применение клеточных технологий в клинике………………11
Список использованной литературы……………………………. ……16
Все живые существа (как животные, так и растения) состоят из клеток, образующих такни различных органов и их систем. Клетка представляет собой элементарную живую систему, основу строения и жизнедеятельности всех животных и растений. Она может существовать как самостоятельный организм (простейшие бактерии), так и в составе многоклеточных организмов. Размеры клеток варьируются в пределах от 0,1 – 0,25 мкм (некоторые бактерии) до 155 мм (яйцо страуса в скорлупе). Число клеток в организмах зависит от их вида и возраста. Например, организм взрослого человека состоит из 10 15 клеток, а число различных видов клеток в нем более 200.
Подобно любому живому существу, клетка способна питаться, расти и размножаться, вследствие чего её можно считать живым организмом. Отдельные её элементы лишены жизненных функций. Клетки, выделенные из различных тканей живых организмов и помещенные в специальную питательную среду, могут расти и размножаться, что широко используется в исследовательских прикладных целях.
Несмотря на большое разнообразие и существенные различия во внешнем виде и функциях, все клетки имеют общее строение: они состоят из трёх основных частей – плазматической мембраны, контролирующей переход вещества из окружающей среды в клетку и обратно, цитоплазмы с разнообразной структурой (органеллы – маленькие органы, окруженные своими мембранами, митохондрии – мешковидные образования с дыхательными ферментами, рибосомы – небольшие тельца, принимающие учасите в биосинтезе белка) и клеточного ядра с носителем генетической информации. Все животные и некоторые растительные клетки содержат центриоли – цилиндрические структуры, образующие клеточные центры.
Не все клетки организма многоклеточного животного или растения одинаковы. Видоизменение клеток происходит постепенно в процессе развития организма. Каждый организм животного развивается из одной клетки – яйца, которое начинает делиться, в конечном результате образуется множество отличающихся друг от друга клеток – мышечные, нервные, кровяные и др. Различие клеток определяется прежде всего набором белков, синтезируемых данной клеткой. Во всех растений или организмов животных хранится полная генетическая информация для построения всех белков определённого вида организма, а в клетке каждого типа синтезируются лишь белки, которые ей нужны.
Принято считать, что главная причина старения организма – утеря генетической информации. Молекулы ДНК постепенно подвергаются мутациям, что приводит к гибели клеток и всего организма. Повреждённые участки молекулы ДНК способны восстанавливаться благодаря репаративным ферментам. Хотя их возможности ограничены, но они играют важную роль в продлении жизни организма.
Ежедневно мы встречаем множество разных людей, но даже не задумываемся, что каждый из нас произошел из одной единственной оплодотворенной яйцеклетки. Она содержит не только информацию об организме, но и схему его последовательного будущего развития. В течение первых пяти дней после зачатия в результате деления этой самой клетки образуется шарик из совершенно одинаковых неспециализированных клеток. Примерно через шесть — семь дней он образует бластоцисту, которая делясь, формирует за считанные недели все органы и ткани человека. А недавно стало известно, что стволовые клетки могут продлить жизнь.
Актуальность вышеизложенных проблем и определила выбор темы.
Целью написания работы является изучение механизма получения стволовых клеток, проблемы и перспективы использования их в медицине
Содержание работы
Содержимое работы - 1 файл
Стволовые клетки Цыбина Алена.doc
1. История открытия стволовых клеток…………… …………………………..4
4. Происхождение стволовых клеток…………………………………………18
5. Функции и механизм функционирования стволовых клеток…………….19
6. Применение стволовых клеток……………………………………………..20
Список использованной литературы…………………………………………26
В течение многих лет исследователи пытаются понять, каким образом живой организм поддерживает гомеостаз, как восстанавливается после повреждения и какие механизмы участвуют в замене поврежденных клеток здоровыми. Стволовые клетки занимают центральное место в клеточном гомеостазе организма, прежде всего потому, что их основной функцией является восполнение естественной потери клеток, выполняющих специализированные функции.
Когда стало ясно, что стволовые клетки могут быть внесены в организм искусственно, начался настоящий бум. Ведь замена ленивых, ветхих или больных клеток организма на абсолютно здоровые позволит решить многие проблемы. Казалось бы, что может быть лучше? Однако оздоровление организма таким передовым способом дело малоизученное и, следовательно, таящее в себе реальные опасности.
Цель: Изучить биологические особенности стволовых клеток.
Объект: Стволовые клетки
Предмет: Функциональные и физиологические особенности стволовых клеток.
Гипотеза: Осмысление и анализ научной информации позволит сформировать целостное представление о стволовых клетках и их роли в жизнедеятельности организма.
1. ИСТОРИЯ ОТКРЫТИЯ СТВОЛОВЫХ КЛЕТОК
В настоящее время стволовыми принято считать только те клетки, которые одновременно обладают двумя специфическими свойствами, а именно: способностью к самовоспроизведению и способностью к дифференцировке.
Процесс самовоспроизведения стволовых клеток заключается в симметричном или асимметричном митотическом делении материнской клетки, в ходе которого хотя бы одна дочерняя клетка сохраняет статус стволовой и полностью идентична по цитохимическим, молекулярным и другим характеристикам материнской клетке.
Вторым важным свойством стволовых клеток, как уже было сказано выше, является их способность к дифференцировке. Дифференцировка – это процесс постепенного увеличения фенотипической обособленности типов клеток, связанный с их созреванием. Основа дифференцировки – синтез цито- и тканеспецифичных белков, что обусловлено развертыванием транскрипции различных генов.
Дифференцировка потомков стволовых клеток реализуется в промежутках между последующими митотическими делениями дочерних элементов и сопровождается постепенным ограничением их пролиферативного потенциала и широты сектора дифференциации.
- тотипотентность – способность давать начало росту всего организма, в том числе и тканям внезародышевых оболочек;
- плюрипотентность – способность воспроизводить любую ткань взрослого организма;
- мультипотентность – способность давать начало более чем одному типу дифференцированных клеток;
- унипотентность – способность воспроизводить однородный однотипный пул дифференцированных клеток.
Тотипотентными стволовыми клетками принято считать зиготу и бластомеры на стадии морулы. К плюрипотентным стволовым клеткам относятся эмбриональные стволовые клетки, стволовые клетки эмбриональной карциномы и эмбриональные зародышевые стволовые клетки. К мультипотентным стволовым клеткам относятся региональные стволовые клетки взрослого организма и плода, например, гемопоэтические стволовые клетки, мезенхимальные стволовые клетки, нейрональные стволовые клетки и др.
Практически во всех тканях взрослого организма человека содержится пул резидентных, т.е. характерных именно для этой ткани, мультипотентных стволовых клеток. Наличие в тканях взрослого организма монопотентных стволовых клеток остается под вопросом. Скорее всего, монопотентными стволовыми клетками являются прогениторные клетки на поздних стадиях созревания.
Прогениторными, или клетками-предшественницами, принято считать клетки, которые являются потомками мультипотентных стволовых клеток, но, несмотря на то, что обладают достаточно высоким пролиферативным потенциалом, утратили способность к асимметричному делению и вступили на путь дифференцировки.
3. ТИПЫ СТВОЛОВЫХ КЛЕТОК
Различают несколько типов стволовых клеток:
Современное развитие исследований стволовых клеток указывает на огромный потенциал их, как источника тканей для регенеративных терапий. Успех этих приложений будет зависеть от точных свойств и потенциалов стволовых клеток, изолированных либо из эмбриональных, либо из взрослых тканей. ЭСК, выделенные из внутренней массы ранних мышиных эмбрионов, характеризуются почти неограниченной пролиферацией и способностью дифференцироваться в дериваты по существу всех линий. Недавние изоляции и культивирование человеческих ЭСК представило новые возможности для реконструктивной медицины. Последние исследования показали также неожиданно высокий потенциал развития взрослых тканеспецифичных стволовых клеток.
Имея в виду все время увеличивающуюся потребность в человеческих стволовых клетках для трансплантации, было проведено исследование in vitro и in vivo человеческих эмбриональных клеток из костного мозга/ прогениторных клеток, полученных в результате прерывания беременности 16-20 недель. При использовании приматов, как модели, было показано, что эмбриональные ткани имеют определенные свойства, которые являются оптимальными для трансплантации. Было проведено тестирование и сравнение фенотипических и функциональных характеристики эмбрионального костного мозга, взрослого костного мозга, пуповинной крови и периферической крови – источников наиболее примитивных стволовых клеток/прогениторных клеток. Проделанные наблюдения указывают, что каждый источник гематопоэтических стволовых клеток имеет различные внутренние свойства, тесно коррелирующие с онтогенетическим возрастом, который является ведущий детерминантой для фенотипических характеристик, определения линии дифференцировки, иммуногенности, как и пролиферативного потенциала. Эти данные ясно показывают, что ЭМК являются лучшим источником стволовых клеток для трансплантации и терапевтической реконституции из-за очень высокой пролиферативной способности, низкой иммуногенности и наиболее высокого числа примитивных стволовых клеток/прогениторных клеток.
Эмбриональные ткани являются богатейшим источником изначальных стволовых клеток и имеют несколько свойств, которые делают их особенно полезными при пересадке. Они являются превосходящими взрослые (зрелые) ткани в определенных отношениях. Первое, эмбриональные клетки способны пролиферировать быстрее и более часто, чем зрелые, полностью дифференцированные клетки. Это означает, что эти донорские клетки способны быстро восстанавливать потерянную функцию хозяина. Дополнительно, эти эмбриональные клетки могут дифференцироваться в ответ на сигналы окружающей их среды. Из-за их локализации они могут расти, удлиняться, мигрировать и устанавливать функциональные связи с другими клетками вокруг них в организме хозяина. Было обнаружено, что эти эмбриональные ткани не так легко отторгаются реципиентом из-за низкого уровня антигенов гистосовместимости в эмбриональных тканях. В то же время в них имеются ангиогенные и трофические факторы в высоких концентрациях, что увеличивает их способность расти при трансплантации. Поскольку в ранних эмбриональных гематопоэтических тканях отсутствуют лимфоциты, реакции трансплантант против хозяина минимизированы. Эмбриональные клетки имеют тенденции переживать иссечение, рассечение и пересадку лучше, поскольку у них обычно нет длинных удлинений или прочных межклеточных соединений. В заключение, эмбриональные ткани могут выживать при более низком содержании кислорода, чем зрелые клетки. Это делает их более устойчивыми к ишемическим условиям, имеющим место при трансплантации или в ситуациях in vitro. Исследования на эмбриональных клетках/тканях были вдохновляющими. Эмбриональные ткани могут быть использованы по различным показаниям, например, транслантанты эмбриональной печени быть использованы для борьбы с апластической анемией, кровь пуповины может служить альтернативой трасфузии цельной крови взрослых, эмбриональный трансплантант надпочечников был испытан для борьбы с хронической болью при артритах, эмбриональный трансплантант тимуса использовался для лечения различных иммунодефицитных состояний. Трансплантант из мозговой эмбриональной ткани был пересажен в гетеротопное положение, и наблюдалась пролиферация ткани. Нейротрансплантация эмбриональных тканей при паркинсонизме показала позитивные результаты в нескольких глобальных исследованиях. Существуют потенциальные возможности использования эмбриональных тканей в биоинженерии.
Если у вас возникли сложности с курсовой, контрольной, дипломной, рефератом, отчетом по практике, научно-исследовательской и любой другой работой - мы готовы помочь.


1. Стволовые клетки
1.1 Эмбриональные стволовые клетки
1.2 Соматические стволовые клетки
1.3 Регенерация и стволовые клетки
2. Кровь жизни
Заключение
Литература
1.2 Соматические стволовые клетки
Соматические стволовые клетки – стволовые клетки взрослого организма. Недавно обнаружено, что некоторые клетки взрослого организма, по-видимому, хотя бы отчасти обладают способностью порождать стволовые клетки, характерные для эмбриона. Если такое действительно возможно, удастся устранить одно из этических препятствий на пути к использованию эмбриональных стволовых клеток — не придется разрушать эмбрион человека, чтобы получить эти клетки.
Во взрослом организме стволовые клетки находятся, в основном, в костном мозге[5] и, в очень небольших количествах, во всех органах и тканях: в коже, мышцах, жире, кишечнике, нервной ткани и даже сетчатке глаза.
Запас стволовых клеток взрослого организма очень невелик. Поэтому случается так, что обновить утраченные клетки организм самостоятельно уже не в состоянии: или очаг поражения слишком велик, или организм ослаблен, или возраст уже не тот. Можно ли помочь больному излечиться от цирроза, инсульта, паралича, диабета, ряда заболеваний нервной системы?
1.3 Регенерация и стволовые клетки
Некоторые животные способны восстанавливать утраченные части тела. А может ли человек восстанавливать утраченные ткани, и какую роль могут играть в этом стволовые клетки.
Оказывается, стволовые клетки обеспечивают восстановление поврежденных участков органов и тканей. Стволовые клетки, получив от регулирующих систем сигналы о какой-либо "неполадке", по кровяному руслу устремляются к пораженному органу. Они могут восстановить практически любое повреждение, превращаясь на месте в необходимые организму клетки (костные, гладкомышечные, печеночные, сердечной мышцы или даже нервные) и стимулируя внутренние резервы организма к регенерации (восстановлению) органа или ткани.
Уже сегодня ученые научились управлять стволовыми клетками. Достижения в этой области клеточной медицины делают возможности использования стволовых клеток практически безграничными.
2. Кровь жизни
Оказывается, при помощи стволовых клеток, взятых из крови плаценты возможно лечение лейкемии. Этот новый метод позволяет спасти детей, которым невозможно подобрать донора для пересадки костного мозга.
Этот парень родился со смертельным заболеванием крови. В 5 лет ему провели курс лечения. Метод лечения стволовыми клетками, взятыми из крови плаценты, был применен впервые на нем. Ребенок остался жить.
Северная Каролина. Госпиталь. Здесь находятся дети, которым районные врачи не в силах помочь. Болезнь заставила их приехать сюда со всего света. Здесь могут помочь некоторым из этих детей. Однако, некоторые из этих детей умрут.
Мальчика зовут Макс. Ему было 5 лет, когда у него на теле появились страшные синяки. До этого он был здоровым ребенком. Сделали анализ крови. Это был гром среди ясного неба. Шансов на то, что лечение, которое ему проводят, поможет всего лишь 10 из 100. У него очень агрессивная форма лейкемии. Максу очень плохо.
В мире тысячи детей страдает от болезней крови. Единственный способ их спасти удалить всю больную кровь и ввести новую, создать новую кровь.
Плацентарная кровь полна стволовых клеток, а это – ключ к жизни. Стволовые клетки продуцируют всю систему крови. Эти клетки работают всю нашу жизнь. Но когда кровеносная система больна стволовые клетки заменяют на здоровые.
Стволовые клетки находятся и в костном мозге, который также используется для лечения заболеваний крови. Это проверенный метод лечения. Но для большинства детей не могут найти донора костного мозга. Если произойдет отторжение, то это – смерть. Идеальный подбор – среди близких родственников. Но даже костный мозг близких родственников может не подойти!
Во всемирном списке доноров насчитывается 7 млн. имен. В 1/3 случаев подбор не помог. Поиски продолжаются, а ребенок может умереть каждую минуту.
Шансов найти доноров для этого мальчика (его зовут Лайдел) практически нет. Он родился в результате смешения рас. Потому он не сможет получить подходящего ему донора.
Ученые ищут альтернативу костному мозгу. Долгое время кровь из плаценты выбрасывалась. В момент родов стволовые клетки младенца продвигаются в костный мозг. Но пуповина содержит очень мало крови. Считалось, что количество стволовых клеток в крови из пуповины не достаточно для лечения заболеваний крови.
Однако, в середине 80-х годов прошлого века группа ученых решила опровергнуть это мнение. Они считали, что кровь из пуповины – новый источник стволовых клеток. Требуется не меньше 1 л костного мозга, а из пуповины набирается полчашки крови. Почти никто не верил, что что-то получится. Стали считать клетки. Результат был неожиданным. Оказалось, что в единице объема плацентарной крови больше стволовых клеток, чем в таком же объеме костного мозга. Для взрослого этого количества не достаточно, но ребенку, скорее всего, хватит.
Очень долго искали ребенка для опробования этого метода лечения. Родители не соглашались использовать своего малыша, в качестве подопытного.
У этого мальчика (Мэтью) была очень редкая болезнь, анемия Фанкони [6]). Она может перейти в лейкемию. Мэтью заболел, когда ему было 2 года. Врачи знали, что он проживет не более 5 лет. Искали донора. Мэтью старались побаловать, зная, что он скоро умрет.
Врачи сказали родителям мальчика, что если у них родится ребенок, то, скорее всего, он сможет быть идеальным донором для их сына. Мать Мютью забеременела. Однако, для того, чтобы взять у маленького ребенка (эта была девочка) костный мозг требовалось, чтобы она подросла, и ей исполнился хотя бы год. Но Мэтью мог и не дожить до этого времени! Врачи решили провести лечение раньше, чем его сестра подрастет. Спросили разрешение у Мутью, и он согласился.
25 февраля 1988 года родилась сестра Мэтью. Из пуповины извлекли кровь и заморозили. Мэтью решили отвезти в клинику Парижа, в которой лучше всего лечили анемию Фанкони. Родители взяли с собой видеокамеру и сняли на видео все, что происходило во время лечения их сына.
Сначала химическими препаратами уничтожили все стволовые клетки Мэтью, и только после этого была введена кровь сестры. Теперь оставалось только ждать (в стерильном боксе). Число белых кровяных клеток должно расти. Эти клетки защищают от инфекций. Через 18 дней после введения плацентарная кровь заработала. Через 6 месяцев Мэтью Фарроу отпустили домой. Он больше не болел. Кровь из пуповины его сестры спасла его от смерти. Теперь у мальчика сформировалась кровь, как у сестры. Так была найдена альтернатива костному мозгу.
Ребенок в утробе матери защищен. Его иммунитет не развит, потому не агрессивен. А значит меньше шансов, что произойдет отторжение крови. Таким образом, донора можно не искать, не надо генетического соответствия. Однако, не смотря на успех этой операции, многие врачи не торопятся лечить стволовыми клетками.
Конечно, нашлись и сторонники лечения стволовыми клетками. Многие госпитали по всему миру стали собирать плацентарную кровь. 7 банков такой крови создано в США, есть такой банк во Франции и Англии[7].
Макс получит стволовые клетки плацентарной крови (маленький пакетик крови). Макс очень болен. Есть неуверенность, что это ему поможет, ведь донора костного мозга так и не нашли. Выхода нет. Надо решаться.
Лайдел тоже получил курс лечения плацентарной кровью (ее получили при родах девочки). Кровь должна прижиться, это длиться около 10 недель. Кровь создается заново. Мальчик будет находится в стерильном боксе, так как подвержен инфекциям в течение этого периода.
Не точно подобранный костный мозг, хуже, чем плацентарная кровь. Но не все врачи с этим согласны. Однако, из крупных костей можно получить больше стволовых клеток.
Женщине 32 года (Хайди). У нее лейкемия. 4,5 млн. образцов костного мозга в базе, но нет ни одного подходящего для нее. Плацентарная кровь не подходит, так как такого количества слишком мало. Смешивание от нескольких детей, не поможет, потому, что в таком случае происходит отторжение.
Путь один – искусственное выращивание стволовых клеток. Вводят факторы роста в плацентарную кровь. И вот ей ввели экспериментальную кровь (выращенные стволовые клетки). Это единственный шанс на удачу.
Принятие новых клеток – начало новой жизни. После введения трансплантата, врачи следили за процессом создания новой крови. Но, прошло несколько недель, и Хайди умерла. У нее был чрезвычайно ослабленный иммунитет. Только два пациента из группы, которым вводили такую кровь, выжили.
От костного мозга врачи не откажутся. А плацентарная кровь – дополнение к костному мозгу.
Лайдела плацентарная кровь спасла. Через 21 день он покинул больницу. Но многие дети все равно умирают. Макс умер, его иммунная система не выдержала.
Как можно больше доноров костного мозга – это способ борьбы с лейкемией. Лечение плацентарной кровью еще не очень распространено. Но тысячи детей, которые выжили, получали такое лечение. В Англии 19 случаев применения плацентарной крови, половина из этих случаев – успешны.
Эта фирма специализируется на хранении пуповин новорожденных детей. Это источник стволовых клеток. Здесь к пуповине относятся, как к сокровищу. Сохранившиеся стволовые клетки обладают мощным потенциалом. Возможно, клетки из пуповины помогут излечить в будущем этого ребенка от болезней. Лейкемия, анемия. 3000 клиентов в этом банке пуповин. Нет гарантии, что пуповина окажется полезной, но все- таки это шанс на спасение в случае болезни.
Заключение
Cтволовые клетки — это основной "строительный материал" для всех видов тканей живого организма. При определённых условиях эти клетки могут преобразовываться в любой вид ткани. Это касается, в первую очередь, эмбриональных клеток, хотя и взрослые стволовые клетки могут иметь те же или подобные свойства.
Уже сегодня ученые умеют направлять стволовые клетки "по нужному пути". Достижения в этой области клеточной медицины делают возможности терапевтического использования стволовых клеток практически безграничными.
Исследования продолжаются. Стволовые клетки находятся в центре внимания ученых и не только[8]. Сотни млн. долларов тратятся на их изучение. Грядет революция в медицине!
1. Костный мозг Материалы предоставлены проектом Рубрикон.
2. Стволовые клетки Источник http://elementy.ru/index.html
3. Что такое стволовые клетки? Источник http://www.stvolkletki.ru/whatis/
4. Лицензированные Росздравнадзором организации
Источник http://stem-cells.ru/index.html
5. Стволовые клетки Материалы предоставлены проектом Рубрикон.
6. Плоды просвещения. "Кровь жизни" Документальный фильм (Великобритания, 2001).
7. Плоды просвещения. "Регенерация"Документальный фильм (Франция, 2003). Режиссер Жан-Мари Корнуэль.
8. Обнаружен ген, заставляющий стволовую клетку расти вечно 30.05.2003 Источник: University of Edinburgh
[1] Одной из наиболее сложных задач в развитиии методов направленной дифференцировки эмбриональных стволовых клеток (ЭСК) считается индукция их развития по энтодермальному пути. Вместе с тем, решение этой проблемы позволит вплотную подойти к получению клеток поджелудочной железы и печени для их последующей трансплантации больным людям. Об актуальности такой работы говорит хотя бы тот факт, что число страдающих сахарным диабетом 1 типа приближается во всем мире к 60 млн. Недавно группа калифорнийских исследователей из компании CyThera Inc. заявила, что получила обнадеживающие результаты в этом направлении. Альтернативный метод клеточного трансплантационного лечения сахарного диабета 1 типа – пересадка клеток костного мозга, пока не имеет вразумительного теоретического объяснения. Так, по данным различных исследователей трансдифференцировка клеток костного мозга в инсулин-продуцирующие клетки остается весьма спорна. Несмотря на это, в отечественной практике данное направление уже используется клиницистами. Разработка способов индукции направленной энтодермальной дифференцировки ЭСК животных и человека может привести к созданию не только методов коррекции различных патологий, но и одним из существенных аргументов в пользу продолжения исследований с этим материалом.
[3] Обнаружен ген, заставляющий, стволовую клетку расти вечно. Одновременно две группы исследователей – института исследований стволовых клеток при эдинбургском университете и японского института Нара – заявили об открытии давно искомого гена, ответственного за поддержание клеток в недифференцированном, "вечно молодом" состоянии. Открытие британских и японских учёных, возможно, со временем позволит произвольно манипулировать активностью обнаруженного гена, тем самым, позволяя превращать специализированные клетки взрослого организма в недифференцированные, потенциально способные замещать клетки других тканей. Это открывает широкие перспективы, поскольку может сделать возможной регенерацию повреждённых или больных органов за счёт собственных клеток организма. Новооткрытый ген был назван Nanog в честь мифического кельтского селения Tir nan Og, жители которого якобы были вечно молоды. В естественных условиях ген Nanog проявляет активность на ранних стадиях эмбрионального развития, поддерживая клетки зародыша в состоянии способности давать начало клеткам любого типа ткани. При определённых условиях клетки раннего эмбриона можно культивировать в культуре на протяжении большого числа поколений, однако они всё равно сохраняют способность дифференцироваться в клетки мышц, печени, костей, мозга или других тканей. Судя по всему, Nanog является исходным звеном в цепочке регуляции процесса дифференциации клеток. Его эффект делает их бессмертными. Судя по всему, он действует не "в одиночку". Таким образом, он способен включать или выключать активность целых блоков наследственной информации, тем самым, определяя момент дифференциации клетки. В эмбрионе человека активность Nanog, вероятно, играет особенно важную роль приблизительно на 4-5 сутки развития, когда "всё возможно, но ничего ещё не решено", то есть на стадии, после которой последующие поколения клеток уже специализированы. В одном из ключевых экспериментов, подтверждающих значение Nanog в организме, человеческий вариант гена был введен в стволовые клетки мыши, после чего последние помещались в условия, которые стимулируют их дифференциацию. Тем не менее, они не переходили в зрелое состояние, что подтверждает блокирующее значение Nanog в процессе приобретения клеткой специфических характеристик. Полученный результат также указывает на схожесть механизмов регуляции развития у человека и мыши и на достаточную консервативность эволюции гена Nanog. Так что, если удастся понять механизмы его работы, учёные смогут выращивать именно ту ткань, которая нужна в данный момент, в любых количествах.
[4] Клон (от греч. Klon – ветвь, отпрыск), ряд следующих друг за другом поколений наследственно однородных потомков одной исходной особи (растения, животного, микроорганизма) , образующихся в результате бесполого размножения. Клонирование клеток применяют в онкологии, генетике соматических клеток и др. Клон, или группа клеток, образуется делением первой клетки. Каждая соматическая клетка человека несет один и тот же набор ген, всю наследственную информацию. Если она начнет делиться, то вырастет новый организм, т.е. с таким же генотипом.
[5] Костный мозг - ткань, заполняющая полости костей у позвоночных животных и человека. Различают красный костный мозг, с преобладанием кроветворной миелоидной ткани и жёлтый с преобладанием жировой ткани. Красный костный мозг сохраняется в течение всей жизни в плоских костях (ребрах, грудине, костях черепа, таза), а также в позвонках и эпифазах трубчатых костей. У человека он составляет около 1,5% массы тела. С возрастом кроветворная ткань в полостях трубчатых костей замещается жировой и костный мозг в них становится жёлтым. Красный костный мозг - основной кроветворный орган у взрослых млекопитающих и человека. В нём происходит развитие эритроцитов, зернистых лейкоцитов (нейтрофилов, эозинофилов, базофилов), кровяных пластинок (тромбоцитов), а также костномозговых лимфоцитов. В состав костного мозга (около 0,1% всех его клеток) входят особые, так называемые стволовые, кроветворные клетки. Стволовые клетки, благодаря их способности к многократному делению и развитию в направлении всех форм кроветворных и лимфоидных клеток, поддерживают кроветворение в костном мозге и обеспечивают возмещение постоянно происходящей в организме убыли лейкоцитов и эритроцитов. Главную массу костного мозга составляют созревающие клетки разных ростков кроветворения (эритроидных, миелоидных, лимфоцитов, мегакариоцитов). Все они - потомки стволовых кроветворных клеток и пополняются за их счёт; часть из них способна к нескольким делениям. Относительное содержание в костном мозге созревающих клеток отдельных ростков кроветворения и более или менее зрелых клеточных форм каждого из ростков служит важной характеристикой процесса кроветворения. По мере созревания клетки из костного мозга поступают в кровяное русло. Кроме зрелых клеток, из костного мозга выходит и некоторое количество стволовых кроветворных клеток, способных переселяться в др. кроветворные органы. Основу красного костного мозга составляет ретикулярная ткань, образующая клеточный синцитий, на котором располагаются кроветворные клетки. Их размножение и созревание во многом зависят от взаимодействия с ретикулярной тканью, обладающей, кроме того, способностью к костеобразованию, что проявляется при заживлении переломов костей. Интенсивность кроветворения в костном мозге может резко увеличиваться. Благодаря этому значительный убыль клеток крови (например, при кровопотерях) или разрушение значительной части клеток костного мозга обычно быстро восполняются. Однако к некоторым воздействиям (например, ионизирующим излучениям) костный мозг и, в частности, его стволовые клетки высоко чувствительны.
[7] Список лицензированных Росздравнадзором на работу со стволовыми клетками организаций был опубликован в декабрьском номере (2005 г) научного журнала "Клеточная трансплантология и тканевая инженерия".Лицензии Росздравнадзора на осуществление забора и хранения клеточного материала ("Банк стволовых клеток") имеют 10 учреждений (8 в Москве, 1 – Самара,1 -:Санкт –Петербург).
[8] Не секрет, что некоторые журналисты в погоне за сенсацией часто не вникают в суть вопроса и не раздумывают, "истина или ложь" утверждение собеседника. И при публикациях своих материалов и не уточняют очень важных и значимых деталей. Наверное, именно поэтому в последнее время на все, что касается стволовых клеток и людей, которые ими занимаются, в СМИ выливают столько грязи.

2. Пинаев Г.П., Блинова М.И, Николаенко Н.С. Клеточная биотехнология: учебное пособие. – СПб.: Изд-во Политехн. ун-та, 2011. – С. 202-206.
3. Семенов М.Г., Степанова Ю.В. Перспективы применения стволовых клеток в реконструктивно-восстановительной хирургии челюстно-лицевой области // Ортопедия, травмотология и восстановительная хирургия детского возраста. – 2016. – Том 4, выпуск. – С. 85-89.
4. Шаповалова Е.Ю., Харченко С.В., Купша Е.И., Барановский Ю.Г. Актуальные вопросы гистологии. Регенеративные возможности тканей и органов : учебное пособие. – Симферополь, 2017. – С. 129.
5. Guangdong Zhou, Haiyue Jiang, Zongqi Yin. In Vitro Regeneration of Patient-specific Ear-shaped Cartilage and Its First Clinical Application for Auricular Reconstruction. // Journal EBioMedicine. – 2018 February. Volume 28. – P. 287-288.
6. Ben Mead, Ann Logan, Martin Berry, Wendy Leadbeater, Ben Scheven. Dental pulp stem cells: a novel cell therapy for retinal and central nervous system repair.// Journal Stem Cells. – 7 Jun 2016. – P. 133-141.
7. Penelope M. Tsimbouri, Peter G. Childs, Gabriel D. Pemberton. Stimulation of 3D osteogenesis by MSC using a nanovibration bioreactor. // Journal Nature Biomedical Engineering. – 2017. Volume 1. – P. 758–770.
8. Huang G.T., Gronthos S., Shi S. Mesenchymal stem cells derived from dental tissues vs. those from other sources: their biology and role in regenerative medicine.// Journal Dent Res. – 2009. Volum 88. – P.792-806
В настоящее время врачами побеждены многие болезни, и если раньше они были приговором, то сейчас существуют методы избавления от них. Но от этого в наш бурный 21 век не уменьшились случаи травм, ожогов, разрушения тканей и органов. В связи с этим невероятно быстрыми темпами развиваются клеточная и тканевая инженерия, а вместе с ними и регенеративная медицина.
Ознакомиться с перспективами применения стволовых клеток в стоматологии и всей регенеративной медицине в целом.
Материалы и методы
Современная научная литература, работа с ней, анализ последних научных исследований мира в области регенеративной медицины.
Результаты исследования и их обсуждения
Успехи и достижения клеточной восстановительной медицины показывают огромный потенциал регенеративной терапии, и хотя многие исследования и эксперименты пока не подтверждены клинической практикой, они открывают неограниченные возможности нашего организма и перспективы его лечения.
Регенеративная медицина сложна и многообразна, она дает множество возможностей, позволяющих восстанавливать нарушенные функции органов или целого организма, стимулируя его на самообновление. Во всем мире ведутся исследования в этом направлении. Специалистом Медицинского центра Columbia University Medical Center Д.Мао и его сотрудниками произведен эксперимент, в ходе которого удалось восстановить суставные хрящи кролика. Имеются и другие примеры восстановления тканей на клеточном уровне.
Клеточными биотехнологиями заняты ученые во всем мире. В конце 20 века зафиксировано большое количество экспериментов в данной области, но ещё больше открытий сделано в настоящее время – время, когда для восстановления структурной целостности и функций поврежденных органов и тканей используется культивирование стволовых клеток, синтез биополимеров и трехмерных скаффолдов, стимулирующих внутренние восстановительные процессы.
Длительные работы ученых привели к настоящему прорыву в медицине : тяжелые травмы, не поддающиеся традиционным методам лечения, дефекты , которые раньше отнимали у человека здоровье и жизнь, сейчас вполне исправимы . Врачи благодаря достижениям в области регенеративной медицины могут возвратить человеку его красоту, а значит свободу и счастье.
Мне бы хотелось подробнее остановиться на вопросах регенеративной медицины в области челюстно-лицевой хирургии и стоматологии.
Ушная раковина – важная отличительная черта человеческого тела, ее деформация оказывает глубокое воздействие на физическое и психическое состояние пациента. Ученые Гуандун Чжоу и Хайюэ Цзяниз из Китая (National Tissue Engineering Center of China, Shanghai) сделали настоящее открытие: они восстановили ушную раковину детей, родившихся с пороком ее развития(микротией), вырастив хрящ ушной раковины из собственных хондроцитов пациентов[5]. В этом исследовании компьютерная томография и 3D-печать были использованы для прямого изготовления биосовместимого скаффолда, который повторял точную аурикулярную структуру симметричного здорового уха пациента и обладал хорошими механическими свойствами. После выделения аутологичных хондроцитов из хряща патологического уха, их высевали на скаффолд, in vitro культивировали в течение 3 месяцев, создавали хрящевые структуры конкретного пациента, а затем имплантировали реконструированную ушную раковину пациенту. Так китайские врачи вылечили 5 детей, страдавших микротией. Эта операция – настоящий прорыв, ведь хрящевая ткань отлично прижилась. Успешное восстановление человеческой ушной раковины с использованием тканевого инженерного метода демонстрирует перспективы регенеративной медицины.
Последние исследования ученых всего мира доказывают мультипотентность МСК (мезенхимальных стволовых клеток), и ,таким образом, они могут быть использованы в восстановительной медицине самых разных областей, в том числе челюстно-лицевой хирургии и стоматологии.
ММСК(мультипотентные МСК) наряду с ЭСК (эмбриональными стволовыми клетками) имеют высокий уровень пролиферации, дифференцировки ( в разные клеточные линии – остеобласты, хондроциты, адипоциты..), но главные преимущества ММСК :
-их использование не вызывает этических противоречий по сравнению с ЭСК[1] ;
-ММСК могут быть получены из собственных клеток пациента;
-также ММСК секретируют множество биологически-активных веществ, которые способствуют заселению места дефекта ткани аутологичными стволовыми клетками, таким образом усиливая тканевую регенерацию;
-ученые культивируют ММСК in vitro в виде трехмерных структур на биосовместимых с организмом скаффолдах. Это позволяет производить индивидуальные имплантаты, которые с большей точностью устраняют дефекты КТ, максимально подходя по структурным, биомеханическим и иммунологическим особенностям пациента, что очень важно в практике челюстно-лицевого хирурга, которому каждый день необходимо возвращать пациентам их уникальные природные черты лица. Так недавно учеными была выращена 3-х мерная костная ткань:
Но в регенеративной медицине до си пор остается открытым вопрос, какие стволовые клетки все-таки использовать? По данным литературы [4], ответ может быть такой:
- аутологичные – при плановых, пластических операциях(если пациент не имеет каких-либо хронических,онкологических заболеваний);
-аллогенные-от тщательно подобранных иммунологичных доноров- при травмах КМ(костного мозга);
-дермальные эквиваленты с аллогенными фибробластами – в стоматологии;
Последние исследования ученых доказали, что мультипотентные СК находятся в пульпе молочных и постоянных зубов[4;8] ,а также имеют незубные интраоральные источники, такие как слизистая оболочка щек, десен и надкостница. Это несомненно расширяет границы терапевтических возможностей для регенеративной медицины, ведь DPSC (dental pulp stem cells) по своим характеристикам не уступают МСК и ЭСК а ,наоборот, имеют ряд преимуществ :легкодоступность,мультипотентность(дифференцировка в адипогенном, остеогенном, нейрогенном направлениях), способность к экспрессии мРНК генов факторов транскрипции, пролиферации (особенно в области корня 3 –го моляра), способность к сохранению своих свойств (даже у людей с пульпитом)[3], отсутствие этических противоречий(как с ЭСК), более мощная нейрогенетика в зубных СК (вероятно, благодаря происхождению из нервного гребня); процедура их выделения гораздо более выгодна экономически и малоинвазивна для пациента.
Зоны локализации DPSC:
-недифферецированные мезенхимные клетки (преодонтобласты)- субодонтобластический слой пульпы;
-популяция периваскулярно расположенных клеток (перициты, глиоциты);
-центральная зона пульпы;
Зуб наиболее часто подвергается сильным внешним и внутренним воздействиям, и все чаще у людей в связи с самыми разными причинами (современным образом жизни, генетикой, некачественной пищей, неблагоприятной экологией) ткань зуба быстро разрушается, но все же она способна и к регенерации. Наличие пульпарных стволовых клеток имеет большое значение в создании третичного дентина в ответ на внешние раздражители и жизнеобеспечения пульпы. При тяжелой травме зуба (например, глубоком кариесе) могут разрушиться дентинобласты, но DPSC , пролифирируя и дифференцируясь в них, приводят к синтезу третичного дентина и обеспечивают защиту пульпы.
В ходе многочисленных исследований учеными найдены 8 уникальных популяций стволовых клеток зуба(рис.1)[4;8] :
1) Постнатальные СК пульпы (DPSCs)- развиваются в дентиноподобную структуру,выстланную клетками (подобными одонтобластам человека), а также в адипоциты, хондробласты, миоциты, неврогенные клетки;
2) стволовые клетки молочных зубов(SHED);
3) СК периодонтальной связки(PDLSCs) могут дифференцироваться в цементобласты, адипоциты,фибробласты соединительной ткани, которая богата коллагеном I типа in vitro и in vivo;
4) клетки-предшественники зубных альвеол (DFPCs), дифференцирующиеся в компоненты периодонта, цемента,надкостницу альвеолярной кости;
5) MSCs-предшественники альвеолярной кости(ABMSCs);
6) СК апикального сосочка(SCAP,) дифференцирующиеся в одонтобласты и адипоциты, (при совместной трансплантации с PDLSCs в зубные альвеолы животных формировались дентин и периодонтальная связка). Таким образом, SCAP можно использовать для создания биологического корня зуба, вместо металлических имплантантов;
7) клетки-предшественники зубного зачатка (TGPCs);
8) клетки-предшественники десны(GMSCs)могут трансформироваться в адипоциты, нервные клетки, остеобласты, хондроциты, миоциты, кардиомиоциты, меланоциты и гепацитоподобные клетки in vitro[8].
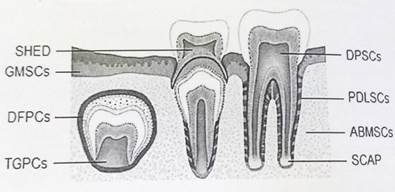
Рис.1 Популяции СК зуба (составлено авторами источника [4])
Несмотря на большие клинические достижения, перед врачами остаются открытыми вопросы: как контролировать рост, необходимую правильную диффиренцировку СК, как достичь нужной формы эмали, зуба в целом? Во всем мире ведутся многочисленные исследования в этой области. Например, итальянским ученым из University of Udine удалось получить зубной зачаток in vitro из популяции мезенхимальных стволовых клеток без скаффолда. [4]
Таким образом, современные технологии тканевой инженерии(трехмерные скаффолды для насаждения СК, биопринтинг, мультипотентные СК) имеют огромное значение и потенциал для развития стоматологии и челюстно-лицевой хирургии. МСК зуба и периодонтальных связок могут быть использованы для восстановления зубных тканей и формирования зубного зачатка, для восстановления костной, мышечной ткани лица, коррекции лицевого отдела черепа.Стоит отметить, что DPSC находят применение и для лечения лейкозов,заболеваний крови и иммунной системы, для восстановления гемопоэза после химиотерапии.
Также учеными из University Birmirgham установлено, что пульпарные стволовые клетки в будущем помогут и в лечении заболеваний, таких как травмы сетчатки глаза, глазного нерва ,глаукомы (как уточняют сами ученые, это связано с происхождением DPSC из нервного гребня, экспрессией нейрональных маркеров и трофических факторов NTF, обеспечивающих регенерацию аксонов ,восстановление их функционирования, консервацию)[6].
Будущее медицины – это клеточная восстановительная медицина. И мы видим уже сейчас, какое огромное количество экспериментов проведено по всему миру! Это очень важно, ведь теперь стоматологи и челюстно-лицевые хирурги имеют больше возможностей вылечить человека от микротии, врожденного порока развития десны, губы, разрушения костной ткани челюсти различной этиологии - одним словом, от любого порока развития или травмы лица.. Ведь что главное для челюстно-лицевого хирурга,стоматолога да и для любого врача? Благодарная улыбка его пациента. С помощью инноваций в регенеративной медицине достичь этого намного проще – подарить наконец человеку долгожданную свободу, красоту и счастье !
Читайте также:

