Реферат на тему высокомолекулярные соединения
Обновлено: 05.07.2024
1. Опишите основные закономерности процесса анионной полимеризации: механизм, катализаторы
Полимеризация по ионному механизму происходит на анионных активных центрах, когда концевой атом растущей полимеризационной цепи обладает отрицательным зарядом, т.е. представляет собой карбанион (с положительным противоионом).
Анионные системы очень чувствительны даже к небольшим количествам примесей веществ, способных разрушить активные анионные центры (вода, спирты и др.).
Поэтому использование анионной полимеризации в промышленности затруднено. Несмотря на это по ионному механизму ведут процессы получения синтетических каучуков, полимеризации капролактама, формальдегида. Возникающие трудности перекрываются высокой производительностью анионных процессов и возможностью получать полимеры с некоторыми специфическими свойствами. Вследствие большой концентрации активных центров скорость анионной полимеризации в 10 4 – 10 7 раз выше скорости радикальной полимеризации. /5, c. 426/
Анионными инициаторами являются доноры электронов. Инициирование можно осуществлять двумя путями:
1. Прямой атакой инициатора на молекулу мономера с образованием карбаниона (нуклеофильное инициирование);
2. Передачей (переносом) электрона от молекулы донора на двойную связь мономера с образованием анион-радикала.
Нуклеофильное инициирование осуществляется при взаимодействии полярного соединения основного характера с непредельной связью мономера с образованием активного центра в виде ионной пары (реже, свободного карбаниона):

В качестве инициаторов этого типа можно использовать металлалкилы, алкоксиды (алкоголяты) и амиды металлов (Me):

Реакционная способность анионного инициатора связана с ионностъю его активной связи (например, R—Ме).
Однако относительная активность в реакции инициирования зависит не только от ионности связи RMe, но и от реакционной способности карбаниона. Так, в алкоксидах металлов ROMe связь кислород — металл более ионная, чем связь углерод — металл в металлалкилах RMe, но реакционная способность ROMe по отношению к ненасыщенным мономерам значительно ниже (например, они совсем не полимеризуют диеновые углеводороды), чем у RMe. В некоторых случаях, например у широко применяемых литийорганических соединений, в неполярных средах соединения RLi (R — неполярный заместитель) представляют собой ассоциаты типа (RLi)n с коэффициентом п = 2—6, образующие равновесную си-хтему из различных .диссоциированных форм. /5, c. 423/.
Алкоксиды ROMe также образуют подобные ассоциаты (с я = = 9), которые устойчивы и в полярных растворителях при повышенной температуре. Естественно, что ассоциированные формы менее реакционноспособны, чем мономерные.
Если анионную полимеризацию ненасыщенных углеводородов проводить в условиях, исключающих обрыв цепи, то ее рост может продолжаться практически до полного израсходования всего мономера, причем на конце полимерных цепей будет сохраняться активный анионный центр, способный к дальнейшей реакции полимеризации (например, при добавлении в реакционную смесь новых порций мономера). Такие устойчивые макроанионы поэтому называют живущими полимерами. Они образуются в растворителях, не способных к реакциям передачи цепи (тетрагидрофуран, диоксан, 1,2-диметоксиэтан).
Кинетика образования живущих полимеров зависит в простейшем случае от соотношения констант скоростей реакций инициирования и роста (kp) цепи. При условии kи >>kp скорость реакции в системах без обрыва цепи будет соответствовать скорости роста:

где [M-] — общая концентрация живущих анионных центров, которая гари полном отсутствии в системе агентов передачи цепи соответствует исходной концентрации инициатора (катализатора) [С]о.
При kи >>kp возможно образование живущих полимеров с очень узким молекулярно-массовым распределением (например, распределение Пуассона), т. е. с очень однородным полимергомологическим составом. В случае kи
Высокомолекулярные соединения могут быть природными или синтетическими. К числу природных относятся белки, полисахариды, природные смолы, натуральный каучук и, а к числу синтетических – полиэтилен, полистирол, полиамиды, фенольные смолы. Высокомолекулярные соединения состоят из больших молекул, молекулярная масса которых превышает несколько тысяч, а иногда может достигать многих миллионов. Молекулы таких соединений состоят из комбинации малых молекул одинакового или разного химического строения. Соединяясь между собой силами главных валентностей (химическими связями), малые молекулы образуют высокомолекулярное вещество.
Прикрепленные файлы: 1 файл
курсовая.docx
Введение
Высокомолекулярные соединения могут быть природными или синтетическими. К числу природных относятся белки, полисахариды, природные смолы, натуральный каучук и, а к числу синтетических – полиэтилен, полистирол, полиамиды, фенольные смолы. Высокомолекулярные соединения состоят из больших молекул, молекулярная масса которых превышает несколько тысяч, а иногда может достигать многих миллионов. Молекулы таких соединений состоят из комбинации малых молекул одинакового или разного химического строения. Соединяясь между собой силами главных валентностей (химическими связями), малые молекулы образуют высокомолекулярное вещество.
В большинстве случаев высокомолекулярные соединения являются полимерами – веществами, молекулы которых состоят из многократно повторяющихся структурных единиц. В одну молекулу полимера может входить одна, две, а иногда три и более повторяющиеся структурные единицы. Широкий интерес к полимерам, многочисленные научные труды, посвященные им, большой объем промышленного производства синтетических полимеров обусловлены в первую очередь уникальным комплексом их физико-механических свойств. Наиболее важные физические свойства полимеров определяются их химическим строением. На первый взгляд кажется, что многие свойства, особенно свойства кристаллических полимеров, в основном определяются их структурой. Однако на самом деле тот или иной вид надмолекулярной организации (при всем ее разнообразии) в конечном счете зависит от химического строения полимерной цепи. Целью данной курсовой работы является изучение основных понятий, особенности строения, классификации полимеров.
1. Основные понятия и номенклатура полимеров
Полимерами называются соединения, в которых более или менее регулярно чередуется большое число одинаковых или неодинаковых атомных группировок, соединенных химическими связями в длинные линейные цепи или цепи, имеющие боковые ответвления, а также в пространственные сети. В зависимости от состава различают органические, неорганические и элементоорганические полимеры. Наиболее полно изучены органические соединения этого класса и поэтому именно на их примере целесообразно рассмотреть основные закономерности строения полимеров.[5,c.354]
Простейшим органическим полимером является полиэтилен – продукт полимеризации этилена. Этилен – ненасыщенный углеводород, легко вступающий в реакции присоединения . Две молекулы этилена, соединяясь, образуют молекулу бутилена:CH2=CH2+CH2=CH2CH®3- CH2-CH=CH2 Исходное вещество – этилен - называется мономером, образующийся бутилен – димером. При соединении трех молекул этилена образуется тример, четырех – тетрамер и т.д. Если соединяются n молекул мономера, образуется полимер (от слова “поли” - много):
Многократно повторяющиеся группировки, которые являются остатками мономеров, называются звеньями, или мономерными звеньями; большая молекула, составленная из звеньев, называется макромолекулой или полимерной цепью. Число звеньев в цепи называется степенью полимеризации и обозначается буквами n или Р. Произведение степени полимеризации n на молекулярный вес звена Мзв равно молекулярному весу полимера: Мпол=nМзв. Величина степени полимеризации может варьировать в широких пределах: от n, равного нескольким единицам, до n, равного 5000-10000 и даже больше. Полимеры с высокой степенью полимеризации называются высокополимерами, полимеры с низкой степенью полимеризации называются – олигомерами. Макромолекула может быть построена из одинаковых по химическому строению мономеров или из мономеров разного строения. Полимеры, построенные из одинаковых мономеров, называются гомополимерами. Полимерные соединения, цепи которых содержат несколько типов мономерных звеньев, называются сополимерами или смешанными полимерами. Остатки мономеров могут соединяться в макромолекуле друг с другом с образованием полимеров линейного, разветвленного или сетчатого (пространственного) строения.
Линейными полимерами называются полимеры, макромолекулы которых представляют собой длинные цепи с очень высокой степенью асимметрии. Если в общем виде остаток мономера обозначить буквой А, то формулу линейного полимера можно схематически записать следующим образом:
Разветвленный полимер представляет собой длинную цепь (называемую обычно главной, или основной) с боковыми ответвлениями (боковые цепи), причем число этих ответвлений и их длина могут варьировать в очень широких пределах. На практике очень широко используются сополимеры, блок-сополимеры и привитые сополимеры (последние иногда называют графт-сополимерами), совмещающие свойства различных полимеров. У обычных сополимеров это совмещение достигается тем, что при самом синтезе высокомолекулярного соединения применяются вместо одного вида мономера: два, три и т.д. Полученная таким образом макромолекула состоит из элементарных звеньев нескольких видов. В большинстве случаев не удается добиться правильного чередования элементарных звеньев в таких сополимерах, и поэтому они, как правило, имеют нерегулярное строение. Подобные сополимеры, у которых взаимное расположение мономерных остатков А и В носит случайный характер и эти остатки размещены вдоль макромолекулярной цепи беспорядочно, согласно законам статистики, называются статистическими. При определенных условиях можно получить правильно чередующиеся-альтернатные сополимеры со строгим чередованием элементарных звеньев. В то время как макромолекулярная цепь блок-сополимеров составлена из отдельных “блоков” различных полимеров, цепь привитых сополимеров состоит из одинаковых элементарных звеньев, но к ней “привиты” в виде боковых ответвлений цепи другого полимера. “Ствол” макромолекулы привитого сополимера построен из мономерных остатков одного полимера, а “ветки” из остатков.
Содержание
Введение……………………………………………………..……..….. 3 стр.
Историческая справка и раскрытие вопроса в литературных источниках……………………………………………………. ……. 5 стр.
Характеристика свойств растворов высокомолекулярных соединений……………………………………………………. …….. 8 стр.
Общие сведения о растворах высокомолекулярных соединений………………………………………………….….……. 8 стр.
Особенности растворов высокомолекулярных соединений……………………………………………………….…. 12 стр.
Классификация высокомолекулярных соединений (пепсин, желатин, крахмал)……………………………………………………….…….. 14 стр.
Технологические процессы свойственные растворам высокомолекулярных соединений ( набухание, растворение, высаливание)…………………………..……………………….……24 стр.
Технологические стадии изготовления и контроль качества данных растворов………………………………………………………..…… 34 стр.
Практическая часть………………………………………………… 35 стр.
Вывод по курсовой работе………………………………..……..
Список литературы……………………………………….……..
Вложенные файлы: 1 файл
Высокомолекулярными соединениями.docx
- Введение…………………………………………………….. ……..….. 3 стр.
- Историческая справка и раскрытие вопроса в литературных источниках…………………………………………………… . ……. 5 стр.
- Характеристика свойств растворов высокомолекулярных соединений…………………………………………………… . …….. 8 стр.
- Общие сведения о растворах высокомолекулярных соединений…………………………………………………. ….……. 8 стр.
- Особенности растворов высокомолекулярных соединений…………………………………………………… ….…. 12 стр.
Классификация высокомолекулярных соединений (пепсин, желатин, крахмал)………………………………………………………. …….. 14 стр.
- Технологические процессы свойственные растворам высокомолекулярных соединений ( набухание, растворение, высаливание)…………………………..……………… ……….……24 стр.
- Технологические стадии изготовления и контроль качества данных растворов……………………………………………………… ..…… 34 стр.
- Практическая часть………………………………………………… 35 стр.
- Вывод по курсовой работе………………………………..……..
- Список литературы……………………………………….……..
Стремительное развитие химии высокомолекулярных соединений
(ВМС) в последнее время способствует их широкому использованию в
различных отраслях промышленности. Особый интерес представляет
применение ВМС в фармации.
В фармацевтической практике ВМС применяются в качестве
лекарственных (белки, гормоны, ферменты, полисахариды, растительные
слизи и т.д.), и вспомогательных веществ, таро-укупорочных материалов.
Вспомогательные вещества широко используются в качестве
стабилизаторов, эмульгаторов, формообразователей, стабилизаторов
для создания более стойких дисперсных систем при производстве
различных лекарственных форм: суспензий, эмульсий, мазей, аэрозолей и
т.д. Введение в технологию новых ВМС позволило создать новые
лекарственные формы: многослойные таблетки длительного действия,
спансулы (гранулы, пропитанные раствором ВМС) микрокапсулы;
глазные лекарственные пленки; детские лекарственные формыи т.д.
Растворы ВМС – устойчивые системы, однако, при определенных
условиях возможно нарушение устойчивости, что приводит к
высаливанию, коацервации, застудневанию. Поэтому для технолога очень
важны знания об интенсивности взаимодействия между частицами
дисперсной фазы и дисперсионной среды, так как это существенно влияет
на выбор способа приготовления лекарственного препарата.
В современной фармацевтической практике находят применение
лекарственные вещества, представляющие собой защищенные коллоиды,
которые состоят из коллоидного компонента и высокомолекулярного
вещества. Все эти вопросы очень актуальны сейчас, именно поэтому мы рассмотрим данную тему в нашей курсовой работе.
В ходе данной работы мы подробно остановимся на решении следующих задач:
изучение высокомолекулярных растворов, их описание, мы так же попытаемся дать определение, установить взаимосвязи данных соединений с другими веществами используемыми в фармацевтической практике, исследуем методы образования и разложения ВМС, рассмотрим различные точки зрения по данной теме в разных источниках литературы, опишем физико - химические свойства ВМС, проведем анализ полученных теоретических данных, на основе теоретического материала проведем практическую работу, сделаем выводы и обобщения.
Объектом нашей работы будут являться растворы ВМС, а предметом их физико-химические особенности, строение, технология приготовления, получения, способы разложения, их полезные и отрицательные свойства.
Историческая справка и раскрытие вопроса в литературных источниках.
Термин "полимерия" введен в науку Й.Берцелиусом в 1833 для обозначения особого вида изомерии, при которой вещества одинакового состава имеют различную молекулярную массу, например этилен и бутилен, кислород и озон (таким образом, содержание термина не соответствовало современным представлениям о полимерах).
Ряд высокомолекулярных соединений был получен, по-видимому, еще в 1-й половине 19 в. Однако в то время их рассматривали как нежелательные побочные продукты "осмоления". Первые упоминания о синтетических высокомолекулярных соединениях относятся к 1838 (поливинилхлорид) и 1839 (полистирол).
До конца 20-х гг. 20 в. наука о высокомолекулярных соединениях развивалась главным образом в русле интенсивного поиска способов синтеза каучука (Г.Бушарда, У.Тилден, И.Л.Кондаков, С.В.Лебедев. и др.). В 30-х гг. было доказано существование свободнорадикального (Г.Штаудингер и др.) и ионного (Ф.Уитмор и др.) механизмов полимеризации. Большую роль в развитии представлений о поликонденсации сыграли работы У.Карозерса, который ввел в химию высокомолекулярных соединений понятия функциональности мономера, линейной и трехмерной поликонденсации. Он же в 1931 синтезировал совместно с Дж.А.Ньюландом хлоропреновый каучук (неопрен) и в 1937 разработал метод получения полиамида для формования волокна типа найлон.
Автором принципиально новых представлений о высокомолекулярных соединениях как о веществах, построенных из макромолекул, был Штаудингер. Победа его идей (к нач. 40-х гг. 20 в.) привела к тому, что высокомолекулярные соединения стали рассматривать как качественно новый объект исследования химии и физики. В 40-60-х гг. значительный вклад в исследование закономерностей поликонденсации, теорию растворов высокомолекулярных соединений и статистическую механику макромолекул внес П.Флори.
Развитие химии и физики высокомолекулярных соединений в СССР связано с именами: С.С.Медведева, который в 30-х гг. впервые установил свободнорадикальную природу активных центров роста цепи при инициированииполимеризации пер оксидами и сформулировал понятие передачи цепи; А.П.Александрова, впервые развившего в 30-х гг. представления о релаксационной природе деформации полимерных тел; В.А.Каргина, установившего в конце 30-х гг. факт термодинамической обратимости растворов полимеров и сформулировавшего систему представлений о трех физических состояниях аморфных высокомолекулярных соединений; К.А.Андрианова, впервые синтезировавшего в 1937 полиорганосилоксаны, и др.
Характеристика свойств растворов высокомолекулярных соединений.
Общие сведения о растворах высокомолекулярных соединений.
Высокомолекулярными соединениями (ВМС) называются вещества с молекулярной массой от нескольких тысяч до миллиона и более. Молекулы этих соединений - гигантские образования, состоящие из сотен и даже тысяч отдельных атомов, связанных друг с другом силами главных валентностей. Молекулы ВМС обычно имеют линейное, нитевидное строение, т. е. резко анизодиаметричны. Например, длина молекулы целлюлозы может достигать 400-500 нм, в то время как в поперечнике она всего 0,3-0,5 нм. Поскольку поперечник молекул указанных соединений значительно меньше 1 нм, они, будучи приведены в соприкосновение с соответствующим растворителем, образуют истинные (молекулярные) растворы.
Из-за больших размеров молекул этих соединений диффузия в их растворах, естественно, протекает медленно. По этой же причине они неспособны проникать через полупроницаемые мембраны. Эти особенности растворов ВМС сближают их с коллоидными растворами, но не дают оснований ставить между ними знак равенства.
Огромные размеры молекул являются причиной значительного своеобразия свойств и поведения растворов указанных соединений. Несмотря на то что макромолекулы не обнаруживаются в ультрамикроскопе, эти растворы обладают способностью светорассеяния, приводящей к опалесценции или некоторой мутности раствора. Растворы ВМС не подчиняются закону Вант-Гоффа и характеризуются небольшим по абсолютной величине, но аномально высоким осмотическим давлением. Такие растворы отличаются высокой вязкостью и способностью к тиксо-тропин. Последнее свойство говорит о том, что они должны быть отнесены к структурированным системам.
После того как будут разрушены связи между макромолекулами, т. е. когда нити их будут достаточно отодвинуты друг от друга, макромолекулы, получив способность к тепловому движению, начинают медленно диффундировать в фазу растворителя. Набухание переходит в растворение.
Процесс набухания указанных соединений нужно рассматривать как протекающий в две стадии. Первая стадия (сольватация - гидратация) сопровождается выделением тепла, т. е. убылью свободной энергии, и объемным сжатием (объем набухшего соединения оказывается меньше, чем суммарный объем его и поглощенного растворителя). Во второй стадии набухания жидкость поглощается без выделения тепла. Растворитель просто диффузно всасывается в петли сетки, образуемой спутанными нитями макромолекул. В этой стадии происходит поглощение большого количества растворителя, а в связи с этим и весьма значительное (в 10-15 раз) увеличение объема набухающего ВМС.
Набухание такого соединения не всегда заканчивается его растворением. Набухание может быть неограниченным и ограниченным. Неограниченное набухание заканчивается растворением: соединение сначала поглощает растворитель, а затем при той же температуре переходит в раствор. При ограниченном набухании высокомолекулярное соединение поглощает растворитель, а само в ней не растворяется, сколько бы времени оно ни находилось в контакте. Ограниченное набухание такого соединения всегда заканчивается образованием эластического геля (студня).
Набухание высокомолекулярных соединений носит избирательный характер. Они набухают лишь в жидкостях, которые близки им по химическому строению. Так, указанные соединения, имеющие полярные группы, набухают в полярных растворителях, а углеводородные - только в неполярных жидкостях (бензин, бензол и т. п.).
В аптечной практике растворы подобных соединений встречаются повседневно. Большей частью это растворы природных ВМС (животные и растительные белки, крахмал, пектины, камеди, растительные слизи и т. д.). Эти соединения в разнообразных сочетаниях содержатся в экстракционных галеновых препаратах (настойки, экстракты), которые вводятся в разнообразные микстуры.
Особенности строения высокомолекулярных соединений.
Отметим две особенности.
1. Существование двух типов связи:
• химические связи, соединяющие атомы в полимерной цепи (энергия связи порядка десятков и сотен кДж/моль);
• межмолекулярные силы Ван-дер-Ваальса, связывающие между собой макромолекулярные цепи и звенья, водородные связи (энергия связи порядка единиц и десятков кДж/моль).
2. Гибкость цепей, обусловленная внутренним вращением звеньев. Благодаря этому макромолекула может принимать различные конформации.
Конформациями называют пространственные энергетически неравноценные формы макромолекул, возникающие в результате вращения звеньев вокруг химических связей (без их разрыва).
В результате конформационных изменений макромолекулы могут принимать различную форму: линейную, клубка, глобул.
Глобула - это частица, образованная из скрученной макромолекулы, в которой осуществляется связь между сходными звеньями. Конформации и различные состояния макромолекул объясняются стремлением к самопроизвольному уменьшению энергии Гиббса, которое происходит при условии: ТДS >ДН.
Таким образом, конформация представляет собой пространственную форму макромолекул, соответствующую максимуму энтропии.
Особенности растворов высокомолекулярных соединений
По некоторым признакам растворы ВМС сходны с золями. Размер частиц в растворах ВМС соответствует коллоидной степени дисперсности (10-6-10-7 см). Частицы этих растворов, как и золей, задерживаются полупроницаемыми перегородками при диализе, обладают сравнительно небольшой скоростью диффузии, способны под влиянием внешних факторов коагулировать. Все это послужило основанием причислять такие растворы к золям. Однако исследованиями В. А. Каргина и С. М. Липатова было показано, что растворы ВМС представляют собой гомогенные истинные растворы, содержащие отдельные макромолекулы или макроионы растворенных веществ. Отличительной особенностью растворов ВМС (по сравнению с золями) является способность частиц взаимодействовать с молекулами растворителя, что выражается термином лиофильность. Вследствие этого такие растворы образуются самопроизвольно путем неограниченного набухания, переходящего в обычное растворение.
Высокомолекулярные соединения занимают особое место в группе органических веществ. Они обладают значительной массой, для их описания используются такие понятия, как макромолекула, мономер, степень полимеризации и другие. Характерны наличием множества повторяющихся звеньев в различных химических реакциях.
Классификация соединений
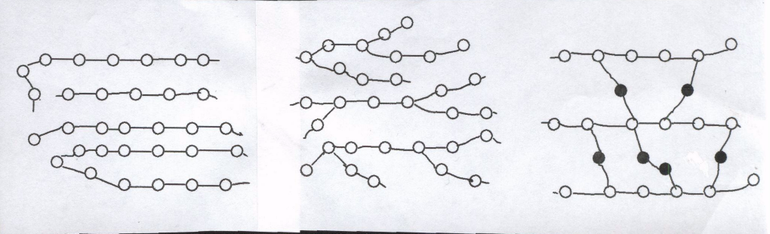
Высокомолекулярные соединения делятся на природные и синтетические. К первым относятся различные каучуки, полисахариды, нуклеиновые кислоты. Искусственно создаются полиэтилен, полипропилен, смолы на основе фенола и альдегидов. Атомы вещества в виде макромолекулы классифицируются следующим образом:
- Однотяжные цепи или последовательность циклов, которая применяется в спирополимерах.
- Разветвленные соединения, которыми обладают крахмал и дендримеры.
- Трехмерная сетка, которая состоит из отрезков структурной цепи.
- Соединения из множества повторяющихся звеньев в низкомолекулярных и высокомолекулярных разновидностях.
Полимеры в химии — это соединения, которые называются таковыми из-за большой массы и прочных химических связей и формул вдоль цепи вида C6H5CH.
Они могут быть стереополимерами, сополимерами и общими блок-сополимерами, которые делятся на стереорегулярные и нестереорегулярные в зависимости от периодичности чередования звеньев. Это зависит от степени расположения цепей, периодичности чередования и особенности строения.
Свойства и характеристики
Высокомолекулярные реакции обладают рядом химических свойств. Некоторые из них присущи исключительно ВМС (аббревиатура для обозначения таких соединений). Самыми важными характеристиками, которые лежат в основе классификации, можно назвать:
- Образование соответствующими методами высокоориентированных волокон и пленок.
- Способность к значительным обратимым деформациям с низкой упругостью по происхождению.
- Могут набухать, образуя упругие тела с веществами типа гелия.
- Очень высокая вязкость при получении раствора в разбавленном виде.
Указанные свойства обусловлены массой, строением цепей и способностью макромолекул изменять форму от внешних воздействий. Переход от линейных цепей к разветвленным и трехмерным делает такие характеристики менее выраженными.
В химии реакция полимеризации это процесс сшивания множества молекул мономера в макромолекулы. В нее вступают непредельные соединяющие элементы. Существует гомополимеризация и сополимеризация. В первом варианте идет слияние молекул одного мономера, а во втором воссоединяются два и более веществ. Она идет по радикальному или ионному механизму.
В случае радикальной полимеризации процесс инициируется свободными радикалами. К примеру, реакция поливинилхлорида идет по следующим стадиям:
- Зарождение цепи C6H5COO=2C2H5COO.
- После этого идет рост цепи с участием радикала R+CH2=CHCl=RCH2-CHCl.
- В конце происходит разветвление или обрыв цепи.
В ионной полимеризации роль активных центров играют катионы и анионы. Это позволяет разделить ее на катионную и анионную вариацию в зависимости от доноров и акцепторов. По ней протекает реакция полимеризации полиизобутилена, бутадиена, синтетического каучука и прочих неорганических реакций.
Применение полимеров

Полимеры благодаря высокой механической прочности и вязкости используются во многих отраслях промышленности. Среди них автомобилестроение, электротехника, сельское хозяйство, медицина. Основными примерами являются пластмассы, резины, лаки, краски и эмали, а также капрон и прочие элементарные полимерные соединения.
Высокомолекулярные соединения и вещества встречаются в химии часто и занимают особое место. Под расшифровкой ВМС понимают такие реакции полимеризации и поликонденсации, в которых выделяются аминокислоты, полиэтилены и остальные соединения.
Читайте также:

