Реферат на тему мышиная лихорадка
Обновлено: 05.07.2024
Пути заражения
Современная медицина определяет ГЛПС как опасное вирусное заболевание, которое передаётся в абсолютном большинстве случаев воздушно-пылевым путем. Переносят инфекцию в основном грызуны: разные виды мышей-полевок, а также домовые мыши и крысы. Некоторые исследователи не исключают латентного носительства инфекции другими представителями млекопитающих или птиц. Животные-носители вируса передают его друг другу чаще всего через дыхательные пути, а выделяют его в окружающую среду со слюной, калом, мочой.
Заражение человека в подавляющем большинстве случаев случается при вдыхании высохших испражнений животных (воздушно-пылевой путь) во время полевых, садово-огородных работ, при посещении леса, уборке частного дома и разборе дворовых сооружений и так далее. Вирус в состоянии аэрозольной пыли попадает прямиком в лёгкие человека, где для его размножения и жизни условия самые благоприятные. Допускается также проникновение вируса при непосредственном соприкосновении участков кожи, имеющих повреждения, с самими грызунами или с зараженными ими объектами (контактный путь). Иногда выявляются случаи инфицирования человека в процессе употребления не подвергшихся термической обработке продуктов, побывавших в контакте с зараженными мышами или их испражнениями (алиментарный путь).
Особой зависимости от возраста, пола и состояния здоровья человека не выявлено – восприимчивость к вирусу одинакова для всех, хотя в силу внешних обстоятельств дети заболевают реже, а взрослые, часто в силу профессии или особенностей проживания контактирующие с потенциально опасной внешней средой – работники сельского хозяйства и промышленности, водители, трактористы, рабочие и так далее – чаще. Хотя, повторю, что от заражения – на даче, в квартире, в турпоходах, при сборе грибов или даже в общепите при несоблюдении норм дератизации – не застрахован никто.
В силу природной обусловленности, пик заболеваемости приходится на летне-осенний период. Между людьми передача вируса не происходит, однако эпидемиологическая опасность в местности с большой концентрацией грызунов всегда повышена. У однажды переболевшего ГЛПС человека на всю жизнь вырабатывается специфический иммунитет, но заболевание еще нужно успешно вылечить, так как оно относится к категории особо опасных и чреватых тяжёлыми поражениями почек, кровеносных сосудов, головного мозга, печени, лёгких.
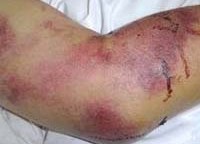
![Мышиная лихорадка – геморрагическая лихорадка с почечным синдромом]()
Клиническая картина
Самостоятельно распознать и определить у себя ГЛПС человек не в состоянии, так как первичная симптоматика может быть похожей на клинические проявления других заболеваний. С какими же симптомами нужно не раздумывая вызывать скорую помощь, чтобы не допустить развития ГЛПС до крайней степени тяжести?
Чаще всего геморрагическая лихорадка с почечным синдромом после инкубационного периода (около 2-3 недель) начинается остро: озноб, резкое повышение температуры, сильные головные боли, болевой синдром в области живота или поясницы, явления общего токсикоза: слабость, сухость во рту, тошнота, рвота, нарушения обмена веществ. Позднее развивается геморрагический синдром - специфическая сыпь на коже, мелкие кровоизлияния в глазное яблоко, гиперемия ротоглотки.
При отсутствии лечения в разгар болезни нарастают явления нарушения кровообращения и, соответственно, гипоксия различных органов. В первую очередь страдают почки, нарушается фильтрация, нарастает острая почечная недостаточность. Появляются отеки, дистрофические изменения внутренних органов. В дальнейшем лихорадочный период проходит, температура может спасть, однако нарастают геморрагические проявления: от гематом до носовых и кишечных кровотечений, кровохаркания. Болевой синдром в области поясницы и брюшной полости нарастает, возникают нарушения зрения, увеличивается печень, может вздуться живот. Быстро нарастают нарушения со стороны центральной нервной и сердечно-сосудистой системы, но особенно страдают почки и мочевыделительная система.
Осложнения
При наличии осложненного анамнеза, отсутствии правильной диагностики и лечения могут развиться различные осложнения ГЛПС. Наиболее опасным из них является инфекционно-токсический шок, который развивается к окончанию первой недели болезни и является наиболее частой причиной летальных исходов. В числе тяжелых последствий, замедляющих и крайне затрудняющих выздоровление – уремия (задержка мочи и нарушение выделительной функции почек), надрыв или разрыв капсулы почек, отеки внутренних органов, кровоизлияния и внутренние кровотечения, пневмонии, абсцессы, сепсис и т.д.
Диагностика и лечение
Для правильной диагностики ГЛПС важно не только собрать клинический, но и эпидемиологический анамнез заболевания, при малейших подозрениях выяснить возможность и степени контакта с предполагаемыми источниками заражения на природе, в жилище, при выполнении профессиональных обязанностей и так далее. Врач также проводит клинический осмотр и назначает ряд специальных лабораторных исследований крови, мочи и кала. Для исключения поражения внутренних органов проводятся также инструментальная диагностика: рентгенография, ФГДС, УЗИ, КТ и др.
Геморрагическая лихорадка с почечным синдромом лечится только в условиях стационара, обычно в инфекционном отделении, укомплектованном штатом специализированных врачей, обязательно оборудованных реанимационными палатами и хорошей биохимической лабораторией. При постановке диагноза ГЛПС требуется щадящий постельный режим во избежание нарастания болей, опасности надрывов и разрывов коркового вещества почки и нарушения кровообращения. Любая транспортировка больных в периоды острого течения болезни должна быть максимально бережной и осуществляться только по жизненно важным показаниям: для гемодиализа или операционного лечения. Постельный режим в зависимости от степени тяжести заболевания может длиться от семи до тридцати дней.
В основе медикаментозной терапии заболевания – противовирусные препараты, иногда комплексное применение нескольких по особой ступенчатой системе. Когда лечения требует уже не только наличие вируса, но и патологии некоторых органов, проводится терапия, направленная на уменьшение интоксикации, снижение полиорганной недостаточности, профилактику отеков, восстановление водно-солевого обмена, прочности стенок кровеносных сосудов и так далее. Лечение проводится под строгим лабораторным контролем и соблюдении принципа достаточности для исключения перегрузок на почки и другие внутренние органы.
Необходимым компонентом при лечении и реабилитации организма от ГЛПС является диетическое питание и недопускание голодания. Еда должна легко усваиваться, содержать достаточное количество питательных веществ и витаминов, в том числе некоторое количество поваренной соли. В начальный период заболевания показано обильное питье, однако, в объёме не большем, чем количество выведенной жидкости. Пищевой состав может меняться в зависимости от стадии развития болезни: при задержке мочевыделительной функции необходимо ограничивать количество белка и калийсодержащих продуктов. На стадии полиурии чернослив, картофель, изюм наоборот, рекомендуются в пищу.
Специфической вакцины от заболевания нет, однако предотвратить заражение тяжёлой инфекцией смогут банальные меры предосторожности: своевременная дератизация, соблюдение правил гигиены и санитарии, увлажненная марлевая повязка и перчатки при работе на дачном участке или в саду, термическая обработка овощей, хранившихся при возможном контакте с грызунами. Информированная осторожность, бдительность и аккуратность помогут избежать ГЛПС.
Геморрагическая лихорадка с почечным синдромом (ГЛПС) — вирус-индуцированное заболевание почек, характеризующееся нарастающей почечной недостаточностью, гематурией и возможными системными геморрагическими проявлениями, такими, как кожная пурпура, носовые, желудочно-кишечные, маточные кровотечения, ДВС-синдром.
1. ЭПИДЕМИОЛОГИЯ
На территории Российской Федерации ГЛПС длительно оставалась природно-очаговым заболеванием, особенно часто встречавшимся в Омской, Оренбургской областях, Хабаровском крае, Башкирии, а также в Поволжье и некоторых южных областях (Белгородской, Курской, Орловской). Однако в настоящее время в нашей стране четко прослеживается общемировая тенденция к утрате ГЛПС эндемичности. Изменение климата и влажности в 1990-х годах привели к массовым миграциям грызунов-носителей, в связи, с чем вспышки и спорадические случаи этого заболевания в настоящее время наблюдают почти повсеместно в европейской части Российской Федерации, в том числе в Тульской, Калужской и Московской областях.
В связи с нередкими сегодня абортивными вариантами течения ГЛПС, отличающимися отсутствием или минимальной выраженностью системного геморрагического синдрома, умеренным ухудшением функции почек, не сопровождающимся изменением диуреза, а также возможностью спонтанного излечения, многие ее случаи, особенно единичные, остаются нераспознанными, что затрудняет достоверную эпидемиологическую характеристику этой болезни.
Одна из первых вспышек ГЛПС была отмечена во время американо-корейской войны в 1951 году в бассейне реки НаNааn (именно поэтому возбудитель ГЛПС получил потом название хантавирусов): более чем у 3000 американских военнослужащих развились фебрильная лихорадка, острая почечная недостаточность, у части — геморрагический шок, 7% заболевших погибли. В настоящее время в мире регистрируют более 200 000 случаев хантавирусной ГЛПС ежегодно. В эндемических очагах заболеваемость достигает 200 случаев на 100 000 человек, а серопозитивными оказываются до 40% проживающих в них людей. Типичны два пика заболеваемости ГЛПС - весенний и осенний.
Путь заражения ГЛПС — фекально-оральный, и в связи с этим увеличение заболеваемости отмечают во время массовых миграций населения, в том числе во время локальных военных конфликтов, когда не соблюдаются общепринятые гигиенические нормы. Так, в Боснии и Герцеговине с 1994 по 1995 год число заболевших ГЛПС возросло почти в 50 раз.
Наибольшему риску заражения ГЛПС подвержены лица, работающие в сельской местности (сельскохозяйственные рабочие, охотники, особенно на пушных зверей и крупных грызунов, солдаты, задействованные на сезонной уборке урожая). Спорадические случаи ГЛПС нередко возникают и у городских жителей, выезжающих за город и во время пребывания в сельских домах и подсобных строениях контактирующих с грызунами-переносчиками (рыжей полевкой) и/или употребляющих пищевые продукты или воду, контаминированную их экскрементами. Существуют несколько возможных эпидемических источников ГЛПС:
· дикие животные (например, красная береговая полевка — резервуар вируса Риита1а в Центральной Европе), контакт с которыми человека относительно редок и всегда происходит в естественной среде их обитания;
· животные, обитающие в сельской местности, в том числе в населенных пунктах (например, желтошейная мышь Ароdетusflavicollis — разносчик вируса Dobrava, распространенного на Балканах и в южной Европе);
· животные, обитающие в непосредственном контакте с человеком, в том числе в городах, и распространяющие вирус через контаминированные мочу и фекалии (например, крыса Rattusnorvegicus, распространяющая вирус Sеои1, особенно часто встречающийся в Азии).
2. ЭТИОЛОГИЯ
Хантавирусы относятся к РНК-содержащему семейству Bunyaviridae, но, в отличие от других его представителей, не передаются от человека к человеку. Хантавирусы реплицируются в цитоплазме клетки-хозяина. Вирусная частица состоит из сферической липидной оболочки, 4 вирусных белков и 3 одноцепочечных ДНК-сегментов, кодирующих белок нуклеокапсида, поверхностные гликопротеиды G1 и G2, а также РНК-зависимую РНК-полимеразу.
Хантавирусы условно подразделяют на вирусы Старого и Нового Света. В зависимости от вида конкретного вируса клиническая картина заболевания может различаться, но в целом она представлена тремя основными вариантами — геморрагической лихорадкой с почечным синдромом, относительно доброкачественной по течению эпидемической нефропатией (ЭН) и хантавирусным легочным синдромом (ХЛС).
Группа хантавирусов Старого Света представлена вирусами Напtаап, Sеои1, Атиr, Ти1а и Dobravа, вызывающими преимущественно ГЛПС, а также одним из наиболее распространенных в Европе вирусом Риита1а, обусловливающим развитие ЭН. С начала 1990-х годов, вслед за первым идентифицированным вирусом SinNотbrе, было открыто несколько хантавирусов Нового Света, большинство из которых вызывают ХЛС.
Различные хантавирусы имеют разные ареалы распространения и переносятся разными видами животных.
3. ПАТОГЕНЕЗ
Имеются указания на то, что к ГЛПС, ЭН и ХЛС, индуцированным хантавирусами, имеется наследственная предрасположенность, маркерами которой могут служить носительство НLА-В8, DRB 1*0301 и НLА-DQ2 аллелей главного комплекса гистосовместимости. Показано также, что наличие аллеля НLА-В35 обусловливает более тяжелое течение ГЛПС. Тем не менее, генетические детерминанты, очевидно, не играют решающей роли в развитии органного поражения при хантавирусной инфекции, клинические проявления которой часто формируются и у тех, у кого соответствующие маркеры отсутствуют.
Хантавирусы проникают преимущественно в макрофаги и эндотелиоциты преимущественно почечных и легочных сосудов. Проникновение хантавируса в клетку-мишень осуществляется путем взаимодействия с расположенным на клеточной мембране интегрином αv β3 с последующим эндоцитозом. В цитоплазме активация вирусной РНК-зависимой РНК-полимеразы обусловливает транскрипцию фрагментов вирусной РНК. Белки вирусного нуклеокапсида и м-РНК РНК-полимеразы транслируются на свободных рибосомах, а м-РНК гликопротеидов — в эндоплазматических ретикулумах. Окончательная подготовка гликопротеидов G1 и G2 завершается их гликозилированием в аппарате Гольджи. В цитоплазме формируются крупные тельца-включения, состоящие из нуклеокапсида, а сборка вирусных частиц происходит на мембранах аппарата Гольджи. Цитопатическим действием на клетки-мишени (эндотелиоциты, макрофаги) хантавирусы не обладают. Тем не менее, установлена возможность индукции ими клеточного апоптоза (в том числе апоптоза эмбриональных почечных клеток), играющего, по-видимому, не последнюю роль в дальнейшем тканевом повреждении.
Макрофаги, инфицированные хантавирусами, начинают увеличивать продукцию интерферонов, однако темпы роста их секреции меньше, чем у интактных клеток макрофагального ряда. В ткани, где присутствуют хантавирусы, также быстро мигрируют МК-клетки (естественные киллеры). Кроме того, хантавирусная инфекция всегда приводит к тканевой активации мембранатакующего комплекса комплемента (С5Б-С9).
Инфицирование хантавирусами всегда сопровождается продукцией специфических IgА, IgМ и IgG; титры последних нарастают в дальнейшем в фазу реконвалесценции. Наряду с этим уже в начале острой фазы хантавирусной инфекции увеличивается продукция специфических IgЕ, приводящая к увеличению экспрессии и секреции интерлейкина-1β и трансформирующего фактора роста-β, обусловливающих неконтролируемый рост проницаемости эндотелиоцитов.
Острая фаза хантавирусной инфекции сопровождается гиперпродукцией ряда тканьдеструктивных цитокинов и хемокинов, в том числе α-фактора некроза опухолей, концентрация которого коррелирует с тяжестью клинических проявлений. Некоторые воспалительные цитокины могут определяться в моче. Воспалительные цитокины, хемокины, а также маркеры острофазового ответа, очевидно, играют центральную роль в развитии эндотелиальной дисфункции, следствием которой является формирование органного повреждения, реализуемого при резком увеличении объема внутриклеточной жидкости за счет проникновения в нее жидкой части плазмы, а также нарастающих расстройств системного и тканевого гемостаза.
Таким образом, формирование и прогрессирование органных поражений определяется в первую очередь нарастающей дисфункцией эндотелиоцитов с резким увеличением проницаемости эндотелия и расстройством систем гемостаза, нередко достигающим степени ДВС-синдрома. Пропотевание жидкой части плазмы в ткани-мишени и расстройство органной гемодинамики с образованием тромбов в микроциркуляторном русле и одновременным формированием очагов кровоизлияний определяют формирование недостаточности функций соответствующих органов — почек и легких.
4 . МОРФОЛОГИЯ
При ГЛПС почки увеличены, под капсулой и в корковом веществе обнаруживают кровоизлияния. Легкие отечны, в них также обнаруживаются очаги кровоизлияний. Из-за отечной жидкости масса легких может в два раза превышать нормальные значения. При развитии ДВС-синдрома кровоизлияния могут также быть обнаружены в коже и подкожно-жировой клетчатке, надпочечниках, головном мозге.
При микроскопическом исследовании ткани почек выявляют признаки тубуло-интерстициального нефрита — инфильтраты из иммунокомпетентных клеток, очаги кровоизлияний в интерстиций. Канальцевые эпителиоциты и эндотелиоциты капилляров отечны, многие интерстициальные капилляры спавшиеся, в их просвете могут обнаруживаться тромбы. Изменения клубочков носят вторичный характер.
5. КЛИНИЧЕСКАЯ КАРТИНА
В зависимости от типа хантавируса заболевание может развиваться по трем клиническим вариантам. ЭН нередко своевременно не распознают; ГЛПС и ХЛС нередко становятся неотложным состоянием и могут быстро приводить к смерти.
При ГЛПС инкубационный период составляет от 7 до 36 часов. В клиническом течении выделяют 5 фаз, в каждой из которых ведущее значение приобретают разные симптомы:
· фебрильная (3-4-й дни болезни);
· гипотензивная (на 3—6-й день с момента начала лихорадки);
· фаза восстановления диуреза (начиная с 11-го дня болезни);
· фаза реконвалесценции (3—6 месяцев с момента начала заболевания).
ЭН начинается внезапно, однако нередко может быть практически бессимптомной, характеризуясь преимущественно лабораторными проявлениями. Полиурию нередко отмечают уже на 3-й день болезни.
При ХЛС в течение 2—14 суток развиваются артериальная гипотензия и некардиогенный отек легких. У выживших регресс органных поражений с восстановлением функции происходит на 5—7-й день.
6. ДИАГНОСТИКА
В большинстве случаев лечение ГЛПС ограничивается только симптоматическими и патогенетическими методами.
При развитии ДВС-синдрома используют свежезамороженную плазму: при выраженной тромбоцитопении возможна трансфузия тромбоцитарной массы. При развитии артериальной гипотензии целесообразна инфузия физиологического раствора, инфузия коллоидных и кристаллоидных растворов — для коррекции гиповолемии, электролитных нарушений и артериальной гипотензии.
При ГЛПС риск геморрагических осложнений и острой сердечной недостаточности, сопряженный с проведением острого гемодиализа, очень велик. Кроме того, гемодиализ малоэффективен для устранения проявлений энцефалопатии и некардиогенного отека легких, в патогенезе которых ведущее значение имеет практически неустранимое с помощью аферезных и диализных методов лечения расстройство органного кровообращения, связанное, в том числе с интенсивным тромбогенезом в микроциркуляторном русле. При выраженной острой почечной недостаточности с установленной гипергидратацией и кардиогенным отеком легкого возможно проведение артериовенозной ультрафильтрации.
При хантавирусных инфекциях уточняют показания и режимы применения противовирусных препаратов. Накоплен определенный опыт клинического применения рибавирина, назначение которого оправдано, по-видимому, только в острую фазу заболевания, характеризующуюся активной репликацией вируса. Эффективность влияния рибавирина на основные клинические проявления почечного поражения удалось подтвердить не во всех клинических исследованиях. К тому же следует иметь в виду, что применение рибавирина может приводить к мутациям хантавируса, в результате которых эффективность этого препарата может быть утрачена, а вирус может приобрести способность ускользать от иммунного ответа хозяина.
Интерфероны при хантавирусной инфекции не эффективны. Эффективными могут оказаться некоторые биологические препараты, в частности рекомбинантный интерлейкин-2, позволяющий добиться достоверно более выраженного регресса креатининемии, чем это наблюдается у пациентов, не получающих данного препарата.
Таким образом, при ГЛПС, ЭН и ХЛС общие принципы лечения должны быть аналогичны используемым при других вирусных инфекциях, для которых противовирусные препараты отсутствуют или малоэффективны. Более обоснованными можно считать только симптоматические меры, направленные на коррекцию метаболических и электролитных нарушений, гемодинамических расстройств, а также ДВС-синдрома.
8. ПРОГНОЗ И ПЕРСПЕКТИВЫ
При ЭН острая почечная недостаточность и летальный исход наблюдаются не более чем у 1% пациентов. ХЛС приводит к смерти более чем у 50% больных. Смертность при ГЛПС, как правило, не превышает 15%.
Опыт длительного наблюдения за реконвалесцентами ГЛПС позволяет утверждать, что у части этих пациентов формируются признаки хронической болезни почек. Результаты сравнения переболевших с пациентами контрольной группы показало, что у лиц, перенесших ГЛПС, обнаруживают более высокие значения альбуминурии и систолического АД, СКФ у них чаще оказывается выше или ниже нормального диапазона, и почти у 15% переболевших выявляют признаки канальцевой дисфункции. Следовательно, ГЛПС может играть роль одной из эпидемически значимых причин формирования хронической болезни почек в первую очередь в очагах хантавируснои инфекции.
Перспективы в лечении хантавируснои инфекции определяются разработкой вакцин, в том числе получаемых из трансгенных животных и растений - продуцентов соответствующих антител. Так, в настоящее время в Южной Корее доступна инактивированная формалином вакцина против вируса Напtaап — коммерческое название Наntavах. Наряду с новыми противовирусными препаратами для лечения хантавируснои инфекции могут быть использованы и рекомбинантные нейтрализующие антитела. Кроме того, для ГЛПС и ХЛС прогноз может быть улучшен в случае внедрения новых патогенетических препаратов, разработанных для лечения ДВС-синдрома и респираторного дистресс-синдрома (например, рекомбинантного легочного сурфактанта). Необходимо также совершенствование противоэпидемических мероприятий, в частности своевременной дератизации.
9. НЕОТЛОЖНЫЕ МЕРОПРИЯТИЯ
1. Оценивать в динамике креатининемию, СКФ, калиемию и натриемию.
2. Периодически выполнять общий анализ мочи и количественную оценку гематурии.
3. Периодически выполнять общий анализ крови с подсчетом количества тромбоцитов.
4. Проводить мониторинг АД, ЧСС и ЭКГ.
5. Определить показатели коагулограммы и вести их мониторинг; исследовать плазменную концентрацию В-димера.
6. Проводить ультразвуковое исследование почек с целью обнаружения их спонтанного разрыва.
7. Проводить инфузию физиологического раствора, кристаллоидных и коллоидных растворов с целью коррекции гиповолемии.
8. При появлении признаков ДВС-синдрома — осуществлять трансфузии свежезамороженной плазмы.
1. Нефрология: неотложные состояния/ Под.ред. Н.А. Мухина. – М.: ЭКСМО, 2010 г.
Существует такая инфекция, которую переносят грызуны. Эта инфекция очень опасна для человека, попав в организм, она вызывает лихорадку, последствия которой для человеческого организма весьма плачевны. Речь идет о мышиной лихорадке. Но оградиться от нее можно, приняв своевременные меры профилактики.
На языке врачей мышиная лихорадка называется геморрагической лихорадкой с почечным синдромом. Ее относят к одному из самых тяжелых, смертельно опасных инфекционных заболеваний. Вирус, попав в организм человека, поражает мелкие кровеносные сосуды, почки, легкие и другие органы человека.
Как человек может заразиться этим вирусом? Вообще, в окружающую среду вирус мышиной лихорадки попадает с выделениям инфицированных грызунов. Заражение человека может происходить различными путями, но чаще всего оно происходит при непосредственном контакте человека со зверьками, а также употреблении продуктов питания, вдыхания пыли, содержащей выделения грызунов.
Инфекцию можно подцепить в течение всего года, однако наибольшее число заболеваний отмечается в весенне-летний сезон, когда люди выезжают на дачу, в лес, на природу.

Отметим также, на широкое распространение заболевания влияет количество грызунов - носителей вируса. Заразиться мышиной лихорадкой можно и в городе, однако наибольшая вероятность подцепить ее при выезде на природу. Непосредственными источниками этого инфекционного заболевания являются грызуны (чаще всего мыши-полевки, забирающиеся в дачные домики), а также суслики, кроты и другие.
Но, как показывает практика, люди уже в майские праздники начинают выезжать загород, на дачи, где проводят уборку домиков, в которых могут быть выделения грызунов. Тоже самое относится и к летнему периоду.
В чем заключается профилактика мышиной лихорадки? В первую очередь, она сводится к предупреждению контакта с грызунами и их выделениями. Помните о том, что в период долгого отсутствия в дачных домиках в любом случае заселяются грызуны.

Поэтому, приехав летом на дачу, первым делом надо проверить помещение в отсутствие людей. Второй шаг: защитив органы дыхания (подойдет респиратор или ватно-марлевая повязка), надев на руки резиновые перчатки, провести тщательную влажную уборку, провести дезинфекцию. Все постельные принадлежности необходимо выбить, перед этим просушив их на солнце не менее 4 часов.
Все меры по профилактике мышиной лихорадки направленные на предупреждение контактов с грызунами и их выделениями. Запасы продуктов питания и воды надо хранить в плотно закрытой таре. В случае их порчи их лучше уничтожить либо провести термическую обработку.
Помните о том, что любое скопление мусора или отходов привлекает грызунов, создает благоприятные условия для их размножения, тем самым снижает эффективность мероприятий, направленных на профилактику заболевания. Если хотите использовать специальные препараты для уничтожения грызунов, надо выбирать те, у которых есть сертификат соответствия. Помните о том, что против мышиной лихорадки нет вакцины или иммуноглобулина.
С момента заражения до проявления первых признаков лихорадки проходит от 7 до 10 дней. Заболевание на начальной стадии походе на обыкновенное острое респираторное заболевание: повышается температура тела, болит голова, появляется боль в мышцах, общая слабость, потеря аппетита. Иногда симптомами могут быть тошнота и рвота.
У некоторых людей появляется заложенность носа, сухой кашель, туман в глазах. Позже к этим симптомам добавляется боли в пояснице и животе, иногда появляется сыпь. Происходит нарушение функций почек, постоянно мучает жажда, сухость во рту, икота. Могут возникнуть кровотечения - почечные, желудочные, носовые и прочие.
Будьте внимательными, при любых проявлениях заболевания обратитесь сразу к врачу. Лечение может назначить только врач, самолечением заниматься ни в коем случае нельзя.
- Вернуться в оглавление раздела "Микробиология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Геморрагические лихорадки – вирусные инфекции с природно-очаговым распространением, протекающие с геморрагическим и острым лихорадочным синдромом. Симптоматика геморрагических лихорадок включает выраженную интоксикацию, высокую температуру тела, геморрагическую сыпь, кровотечения различной локализации, полиорганные нарушения. Форма геморрагической лихорадки определяется с учетом клинико-эпидемиологических и лабораторных данных (ПЦР, ИФА, РИФ). При геморрагических лихорадках проводится дезинтоксикационная, противовирусная, гемостатическая терапия, введение специфических иммуноглобулинов, борьба с осложнениями.
Общие сведения
Геморрагические лихорадки – группа инфекционных заболеваний вирусной природы, вызывающих токсическое поражение сосудистых стенок, способствуя развитию геморрагического синдрома. Протекают на фоне общей интоксикации, провоцируют полиорганные патологии. Геморрагические лихорадки распространены в определенных регионах планеты, в ареалах обитания переносчиков заболевания. Вызывают геморрагические лихорадки вирусы следующих семейств: Togaviridae, Bunyaviridae, Arenaviridae и Filoviridae. Характерной особенностью, объединяющей эти вирусы, является сродство к клеткам эндотелия сосудов человека.
Резервуаром и источником этих вирусов является человек и животные (различные виды грызунов, обезьяны, белки, летучие мыши и др.), переносчиком – комары и клещи. Некоторые геморрагические лихорадки могут передаваться контактно-бытовым, пищевым, водным и другими путями. По способу заражения эти инфекции подразделяются на группы: клещевые инфекции (Омская, Крымская-Конго и лихорадка Кьясанурского леса), комариные (желтая, лихорадка денге, Чукунгунья, долины Рифт) и контагиозные (лихорадки Лаоса, Аргентинская, Боливийская, Эбола, Марбург и др.).
Восприимчивость к геморрагическим лихорадкам у человека довольно высока, заболевают преимущественно лица, чья профессиональная деятельность связана с дикой природой. Заболеваемость в городах чаще отмечается у граждан, не имеющих постоянного места жительства и сотрудников бытовых служб, контактирующих с грызунами.

Симптомы геморрагической лихорадки
Геморрагические лихорадки в большинстве случаев объединяет характерное течение с последовательной сменой периодов: инкубации (как правило, 1-3 недели), начальный (2-7 дней), разгара (1-2 недели) и реконвалесценции (несколько недель). Начальный период проявляется общеинтоксикационной симптоматикой, обычно весьма интенсивной. Лихорадка при тяжелом течении может достигать критических цифр, интоксикация – способствовать расстройству сознания, бреду, галлюцинациям.
Перед наступлением периода разгара нередко отмечается кратковременная нормализация температуры и улучшение общего состояния, после чего токсикоз нарастает, интенсивность общей клиники увеличивается, развиваются полиорганные патологии, нарушения гемодинамики. В период реконвалесценции происходит постепенный регресс клинических проявлений и восстановление функционального состояния органов и систем.
Геморрагический дальневосточный нефрозонефрит нередко называют геморрагической лихорадкой с почечным синдромом, поскольку для этого заболевания характерно преимущественное поражение сосудов почек. Инкубация геморрагического дальневосточного нефрозонефрита составляет 2 недели, но может сокращаться до 11 и удлиняться до 23 дней. Впервые дни заболевания возможны продромальные явления (слабость, недомогание). Затем развивается тяжелая интоксикация, температура тела поднимается до 39,5 и более градусов и сохраняется на протяжении 2-6 дней. Спустя 2-4 дня от начала лихорадки появляется геморрагическая симптоматика на фоне прогрессирующей интоксикации. Иногда могут отмечаться менингеальные симптомы (Кернига, Брудзинского, ригидность затылочных мышц). Ввиду токсического поражения головного мозга, сознание нередко спутано, появляются галлюцинации, бред.
Крымская геморрагическая лихорадка характеризуется острым началом: отмечается рвота, боль в животе натощак, озноб. Температура тела резко повышается. Внешний вид больных характерный для геморрагических лихорадок: гиперемированное отечное лицо и инъецированные конъюнктивы, веки, склеры. Геморрагическая симптоматика выражена: петехиальные высыпания, кровоточивость десен, кровотечения из носа, примесь крови в кале и рвотных массах, маточные кровотечения у женщин. Селезенка чаще остается нормального размера, у некоторых больных может отмечаться ее увеличение. Тяжелое течение заболевания проявляется интенсивной болью в животе, частой рвотой, меленой. Пульс лабильный, артериальное давление снижено, сердечные тоны – глухие.
Омская геморрагическая лихорадка протекает более легко и доброкачественно, геморрагический синдром выражен слабее (хотя летальность имеет место и при этой инфекции). В первые дни лихорадка достигает 39 с небольшим градусов, в половине случаев лихорадочный период протекает волнообразно, с периодами повышения и нормализации температуры тела. Продолжительность лихорадки – 3-10 дней.
Геморрагическая лихорадка денге характеризуется инкубационным периодом от 5 до 15 дней, доброкачественным течением, симптоматикой общей интоксикации, усиливающейся к 3-4 дню и пятнисто-папулезной сыпью геморрагического происхождения, проходящей через 2-3 дня после появления (обычно возникает в разгар заболевания) и не оставляющей после себя пигментаций или шелушения. Температурная кривая может быть двухволновой: лихорадка прерывается 2-3-дневным периодом нормальной температуры, после чего возникает вторая волна. Такая форма характерна для европейцев, у жителей Юго-Восточной Азии лихорадка Денге развивается по геморрагическому варианту и имеет более тяжелое течение.
Геморрагические лихорадки могут способствовать развитию тяжелых, угрожающих жизни состояний: инфекционно-токсического шока, острой почечной недостаточности, комы.
Диагностика геморрагических лихорадок
Диагностику геморрагических лихорадок производят на основании клинической картины и данных эпидемиологического анамнеза, подтверждая предварительный диагноз лабораторно. Специфическая диагностика производится с помощью серологических исследования (РСК, РНИФ и др.), иммуноферментного анализа (ИФА), выявления вирусных антигенов (ПЦР), вирусологического метода.
Геморрагические лихорадки обычно характеризуются тромбоцитопенией в общем анализе крови, выявлением эритроцитов в моче и кале. При выраженной геморрагии появляются симптомы анемии. Положительный анализ кала на скрытую кровь говорит о кровотечении по ходу желудочно-кишечного тракта.
Лихорадка с почечным синдромом также проявляется при лабораторной диагностике в виде лейкопении, анэозинофилии, увеличением количества палочкоядерных нейтрофилов. Значительны патологические изменения в общем анализе мочи – удельный вес снижен, отмечается белок, (нередко повышение достигает 20-40%), цилиндры. В крови повышен остаточный азот. Крымская лихорадка отличается лимфоцитозом на фоне общего нормоцитоза, сдвигом лейкоформулы влево и нормальной СОЭ.
Лечение геморрагической лихорадки
Больные с любой геморрагической лихорадкой подлежат госпитализации. Прописан постельный режим, полужидкая калорийная легкоусвояемая диета, максимально насыщенная витаминами (в особенности С и В) – овощные отвары, фруктовые и ягодные соки, настой шиповника, морсы). Кроме того, назначают витаминотерапию: витамины С, Р. Ежедневно в течение четырех дней принимается викасол (витамин К).
Внутривенно капельно назначают раствор глюкозы, в период лихорадки могут производиться переливания крови небольшими порциями, а также введение препаратов железа, препаратов на основе водного экстракта из печени крупного рогатого скота. В комплексную терапию включают противогистаминные средства. Выписка из стационара производится после полного клинического выздоровления. По выписке больные некоторое время наблюдаются амбулаторно.
Прогноз и профилактика геморрагической лихорадки
Прогноз зависит от тяжести течения заболевания. Геморрагические лихорадки могут варьироваться по течению в весьма широких пределах, в некоторых случаях вызывая развитие терминальных состояний и заканчиваясь летально, однако в большинстве случаев при своевременной медицинской помощи прогноз благоприятен – инфекция заканчивается выздоровлением.
Профилактика геморрагических лихорадок в первую очередь подразумевает меры, направленные на уничтожение переносчиков инфекции и предупреждение укусов. В ареале распространения инфекции производят тщательную очистку мест, подготовленных под поселение, от кровососущих насекомых (комары, клещи), в эпидемически опасных регионах рекомендовано в лесных массивах носить плотную одежду, сапоги, перчатки, специальные противокомариные комбинезоны и маски, использовать репелленты. Для омской геморрагической лихорадки существует методика специфической профилактики, плановая вакцинация населения с помощью убитой вакцины вируса.
Читайте также:


