Новые технологии в пародонтологии реферат
Обновлено: 04.07.2024
В статье приведен обзор отечественной и зарубежной литературы о современных подходах к вопросам комплексного лечения воспалительных заболеваний пародонта. Отражены основные направления работы исследователей в области пародонтологии, проанализированы результаты проведенных авторами исследований, приведены рекомендации для практического здравоохранения. Представлены различные алгоритмы лечения заболеваний пародонта с использованием новых лекарственных средств и методов физиотерапии. Продемонстрирована важность комплексного подхода к решению поставленной проблемы, направленного на корректное сочетание местного и общего лечения, а также рациональное решение вопроса поддерживающей терапии. Проведенный анализ литературы свидетельствует о неудовлетворенности стоматологов существующими методами лечения пародонтита, обширном поиске новых, более эффективных способов лечения данной патологии, позволяющих получить наиболее эффективное, патогенетически обоснованное лечебное воздействие на ткани пародонта.

1. Аджи Ю.А. Особенности лечебного действия электроактивированных водных растворов при хроническом генерализованном пародонтите средней степени / Ю.А. Аджи // Материалы III Всерос. конф. молодых ученых, организованная ВГМА и Курским гос. мед. ун-том. – Воронеж, 2009. – Т. 2. – С. 158.
3. Булкина Н.В., Башкова Л.В. Иммуногистохимические критерии эффективности комплексного лечения больных быстропрогрессирующим пародонтитом с применением комбинированных физиотерапевтических методов // Дентал Юг. – 2009. – № 9 (69). – С. 15-17.
7. Грудянов А.И. Диагностика в пародонтологии / А.И. Грудянов, A.C. Григорьян, О.А. Фролова. – М.: Медицинское информационное агентство, 2004. – 104с.
8. Грудянов А.И., Масленикова Г.В., Загнат В.Ф. Сравнительное изу¬чение эффективности воздействия ряда местных антимикробных препаратов на видовой и количественный состав микробной флоры пародонтальных карманов // Стоматология. – 1992. – Т.71. – № 1. – С. 25-26.
9. Зубаирова Г.Ш. Изменение содержания секреторных иммуноглобулинов в полости рта больных хроническим генерализованным пародонтитом при лечении с локальным использованием пробиотика и иммуномодулятора / Г.Ш. Зубаирова, А.И. Булгакова, Ю.А. Медведев, И.В. Валеев, А.К. Юнусова // Вестник Российской военно-медицинской академии. – Санкт-Петербург, 2009. – №1 (21). – С. 73–75.
11. Иванов, П. В. Новые регенеративные методы лечения генерализованного пародонтита: моногр. / П. В. Иванов, Н. В. Булкина, А. П. Ведяева. – Пенза, 2013. – 230 с.
13. Маланьин И.В. Современные методы лечения и профилактики заболеваний пародонта. Учебно-методическое пособие // Кубанская научная школа стоматологии. – 2012. – 144 с.
15. Мардахаева В.Н. Оценка функционального состояния пародонта по показателям микроциркуляции при гигиенической чистке зубов: автореф. дис. … канд. мед. наук. – М., 2010. – 28 с.
16. Митин Н.Е., Дармограй В.Н., Курякина Н.В., Дармограй С.В. Новые подходы к лечению заболеваний пародонта растительными средствами // Информационный листок рязанского центра научно-технической информации. – Рязань, 1999. – С.1–3.
17. Непомнящая, Н.В. Особенности лечения хронического пародонтита в зависимости от групповой принадлежности крови у пациентов с зубочелюстными аномалиями / Н.В. Непомнящая, М.А. Постников // Ортодонтия. – 2008. – №4 (44). – С. 11-12.
19. Панин A.M. Новое поколение биокомпозиционных остеопластических материалов (разработка, лабораторно клиническое обоснование, клиническое внедрение): автореф. дис. … д-ра мед. наук. – М., 2004.
21. Ракова Т.В. Состояние местного иммунитета полости рта у больных хроническим катаральным гингивитом / Т.В. Ракова, А.И. Лазарев, А.В. Беседин, А.Л. Локтионов // Университетская наука: теория, практика, инновации: Сборник трудов 74-й научной конференции КГМУ, сессии Центрально-Черноземного научного центра РАМН и отделения РАЕН. – Курск: КГМУ, 2009. – Т. 1. – С. 139-141.
23. Сарапульцева М.В., Шляхтова И.А. Современные методы снятия зубных отложений (обзор литературы) // Пародонтология. – 2009. – № 4. – С.26-31.
25. Стоматов А.В., Ефимов Ю.В., Мухаев Х.Х., Ефимова Е.Ю., Ярыгина Е.Н., Иванов П.В. Влияние аутогенного тромбоцитарного геля в сочетании с внутрикостнымиинфузиями 0,03% раствора натрия гипохлорита на уровень базального кровотока десны при хирургическом лечении больных хроническим пародонтитом // Фундаментальные исследования. – 2011. – № 6. – С. 61–63.
26. Хохрина Т.Г. Профессиональная гигиена полости рта неотъемлемая часть профилактики стоматологических заболеваний / Т.Г. Хохрина // Клиническая стоматология. – 2000. – № 3. – С. 14-17.
27. Царев В. Н., Николаева Е.Н., Носик А.С., Щербо С.Н. Современные методы микробиологической диагностики заболеваний тканей пародонта // Медицинский алфавит. Стоматология. – 2005. – № 2. – С. 26-29.
28. Цимбалистов A.B., Шторина Г.Б., Михайлова Е.С. Профессиональная гигиена полости рта. Учебное пособие. – Санкт-Петербург, 2002. – 48 с.
29. Чернышова С.Б. Использование современных антибактериальных препаратов группы фторхинолонов в комплексном лечении болезней пародонта: автореф. дис. . канд. мед. наук/ С.Б. Чернышова. – М., 1999. – 28 с.
30. Шашкина И.В. Опыт лечения хронических заболеваний пародонта антибиотиком вильпрафен (джозамицин) / И.В. Шашкина, И.Б. Новикова, H.H. Клюева // Стоматология. 2001. – № 1. – С. 64-65.
31. Янушевич О.О. Стоматологическая заболеваемость населения России / О.О. Янушевич. – М.: МГМСУ, 2009. – 228 с.
32. Bjork A. Variations in the growth pattern of the human mandible: longitudinal radiographic study by the implant method. Journal of Dental Research, Suppl. 1999, 42: 400-411.
33. Garrett S. The effect of locally delivered controlled-release doxycycline or scaling and root planning on periodontal maintenance patients over 9 months / S. Garrett, D.F. Adams, G. Bogle et al. // J. Periodontol. – 2000. – Vol. 71. – P. 22-30.
34. Unsal E., Akkava M., Walsh T.F. Influence of a single applications of subgingival chlorhexidine gel or tetracycline paste on the clinical parameters of adult periodontitis patients //J. Clin. Periodontol. – May 1998. – P.351-5.
36. Gao, T. Composites of bone morphogenetic protein and type 4 collagen, coral-derived coral hydroxyapatite, and tricalcium phosphate ceramic / T. Gao, T.S. Lindholm, A. Marttinen, M.R. Urist // Int. orthop. 1996. – Vol. 20. – № 5. – P. 321-325.
На современном этапе развития стоматологии при лечении воспалительных заболеваний пародонта предусмотрен комплексных подход, цель которого - ликвидация воспалительных процессов в пародонте, восстановление структурных и функциональных свойств элементов пародонтального комплекса, повышение местных и общих факторов защиты, что достигается сочетанием этиотропной, патогенетической и симптоматической терапии [3,7,10,1,16,24,25,31].
Общее лечение предусматривает использование нестероидных препаратов: салицилатов, препараты пиразолона, производных ряда органических кислот: индолуксусной (индометацин, сулиндак), фенилуксусной (вольтарен), пропионовой (мефенаминовая кислота, понстан, опири, клотам), которые оказывают сочетанное противовоспалительное, болеутоляющее и жаропонижающее действие [2].
В общем лечении воспалительных заболеваний пародонта для подавления стойких субгингивальных патогенов применяют антибиотики [27,29,30,33]. Эти препараты применяют по строгим показаниям: гноетечение из пародонтальных карманов, абсцедирование, свищи, прогрессирующая деструкция костной ткани альвеолярного отростка, интоксикация, состояние до и после хирургического вмешательства. Доказано, что назначение антибактериальных препаратов изменяет микрофлору над- и поддесневой зубной бляшки, меняет клиническую картину пародонтита в сторону стабилизации процесса, замедляет воспалительную резорбцию костной ткани, однако приводит к формированию устойчивых к ним форм микрофлоры полости рта [13].
Антибиотики и другие противовоспалительные средства оказывают бактерицидное и бактериостатическое действие на микробное население пародонтальных карманов и полости рта. При этом происходит массовое недифференцированное и бесконтрольное уничтожение микрофлоры всего биотопа полости рта и, в первую очередь, сапрофитной микрофлоры. Кроме того, антибиотикотерапия приводит к селекции множественно устойчивых вариантов возбудителей, способствующих генерализации воспалительного процесса. Длительное назначение этих препаратов может привести к развитию дисбактериоза из-за подавления нормальной микрофлоры пациента. В связи с этим наиболее часто при пародонтите для подавления патогенных микроорганизмов субгингивальной бляшки применяют антибактериальные препараты местного действия - антисептики [8].
Широко известна высокая эффективность местного применения в качестве антисептика раствора хлоргексидина [34]. Хлоргексидин, будучи катионом, вступает во взаимодействие с бактериями, притягивая отрицательно заряженные мембранные компоненты. К отрицательным свойствам хлоргексидина относят раздражающее и аллергезирующее действие, окрашивание зубов, пломб и языка, неприятный вкус, расстройство вкусовой чувствительности, десквамацию эпителия полости рта [13].
В комплексной терапии больных хроническим пародонтитом существенное значение отводится хирургическим методам. Главная цель пародонтальной хирургии заключается в создании оптимальных функциональных условий для тканей пародонта: ликвидация пародонтальных карманов на фоне оптимизации условий для регенерации тканей пародонта [4,6].
Для оптимизации условий остеорепарации в настоящее время используются различные остеопластические материалы: на основе биологически активного стекла, гидроксиапатита, сульфата кальция, трикальций фосфата, костного коллагена и сульфатированных гликозаминогликанов [19,32,35]. Каждый из перечисленных препаратов достаточно эффективен, но вероятность его отторжения все же высока [36].
К основным хирургическим вмешательствам при заболеваниях пародонта относят кюретаж, гингивотомия, гингивэктомия, лоскутные операции и пластика десен. Вспомогательные хирургические вмешательства предполагают проведение по показаниям пластики уздечек губ, языка, вестибулопластики, рассечение мощных соединительнотканных тяжей [6,11].
В настоящее время общепринятыми методами местного лечения заболеваний пародонта являются профессиональная гигиена полости рта, лечение кариеса и его осложнений, удаление зубов, не подлежащих лечению, восстановление контактных пунктов, полировка пломб, удаление нерациональных ортопедических конструкций, индивидуальное пришлифовывание, хирургические методы лечения.
На сегодняшний день не вызывает сомнений взаимосвязь между распространенностью воспалительных заболеваний пародонта, тяжестью их течения и уровнем гигиены полости рта [26,23,28]. Из большого количества профилактических методов наиболее перспективными являются ультразвуковая обработка и чистка зубов методом пескоструйной обработки. М.В. Рыжкова (2008) разработала критерии оценки снижения активности воспалительного процесса на уровне зубодесневого соединения с использованием результатов исследования цитологического состава и уровня цитокинов (ИЛ-8 и ИЛ-1В) десневой жидкости, позволяющих судить о качестве и эффективности проводимых гигиенических мероприятий. Проведение повторных курсов профессиональной гигиены полости рта автор рекомендует проводить пациентам с катаральным гингивитом не позднее чем через 6 месяцев после проведения профилактических мероприятий, а пациентам без признаков патологии пародонта и с пародонтитом легкой степени тяжести - не позднее чем через год [22].
Мардахаева В.Н. (2009) на основании показателей микроциркуляции установила характер и степень гемодинамических изменений при гигиенической чистке зубов, что позволило автору определить продолжительность проведения процедуры в зависимости от состояния пародонта и вида зубной щетки с целью повышения эффективности профилактики и лечения начальных воспалительных заболеваний пародонта.
В литературе отмечена эффективность электроактивированных водных растворов. Исследователями разработана методика использования анолита и католита, заключающаяся в ирригации полости рта раствором анолита и затем католита (по 5 минут) с помощью ирригатора AQUAJETLD-A7 на протяжении семи визитов и прием католита внутрь два раза в день, что позволило получить быстрый противовоспалительный эффект, контролируемый клиническими и лабораторными методами исследования [14,15].
Сравнительный анализ эффективности стандартной терапии, комбинированного применения стандартной терапии и электроактивированных водных растворов и самостоятельного применения электроактивированных водных растворов, по разработанной авторами методике при хроническом генерализованном пародонтите легкой и средней степени выявил не только высокую эффективность электроактивированных водных растворов, как в отношении микробной флоры полости рта, так и процессов восстановления поврежденных тканей пародонта, но и преимущества перед традиционной терапией [12,1].
Одним из препаратов, которые нормализуют тканевой газообмен и метаболизм тканей пародонта, признан гепарин. Под влиянием гепарина происходит нормализация кислородного баланса тканей, улучшается микроциркуляция и транспорт веществ между тканью и кровью. Гепарин устраняет спазмы, ликвидирует микротромбы, повышает проницаемость сосудов, тканей и толерантность тканей к гипоксии, обладает антиаллергическим действием. Оказывая антикоагулирующее и противогипоксическое действие, Гепарин способствует реабилитации повреждённой ткани. Кроме того, Гепарин нормализует ток лимфы в очаге поражения. Нижник В.Г. (2000) доказала, что включение препарата Гепарин в комплексное лечение больных с воспалительными заболеваниями пародонта повышает терапевтический эффект: приводит к сокращению сроков лечения, увеличивает длительность ремиссии, способствует более быстрой ликвидации, наибольшая эффективность достигается при введении Гепарина в ткани пародонта с подогревом до 40 0 С, при помощи приспособления для введения медикаментов в ткани пародонта [18].
Зубаирова Г.Ш. (2009) разработала метод диагностики и комплексного лечения хронического генерализованного пародонтита с использованием нового лекарственного средства, содержащего комбинацию иммуномодулятора (лейкоцитарный интерферон) и пробиотика (бактисубтил). Для улучшения результатов лечения больных хроническим генерализованным пародонтитом автор рекомендует применение лечебного геля с антибактериальными и иммуномодулирующими свойствами, содержащего в качестве основы натрий - карбоксиметилцеллюлозы в сочетании с лейкоцитарным интерфероном и бактисубтилом по схеме: при легкой степени - 5, при средней - 7, при тяжелой - 9 раз, в составе пародонтальной повязки. Для профилактики рецидивов хронического генерализованного пародонтита необходимо повторное лечение по представленной схеме через 6-12 месяцев [9].
Непомнящей Н.В. (2008) выявлены группоспецифические клинические особенности хронического генерализованного пародонтита. Автор показал, что у больных с В(III) группой крови чаще встречается тяжелая форма заболевания. У пациентов с А(II) группой крови отмечены наихудшие показатели гигиены полости рта, о чем свидетельствует максимальные индекс зубного камня, индекс Мюлеманна, гигиенический индекс и степень подвижности зубов, у них менее результативна традиционная терапия. Также автором отмечено, что терапия хронического генерализованного пародонтита с включением препарата метаболического действия силистронга по 1 чайной ложке 2 раза в день внутрь, благодаря многогранному действию препарата из плодов расторопши, включающему противовоспалительный и мембранопротекторный эффекты, показана пациентам с сопутствующей соматической патологией и при склонности к рецидивирующему течению заболеваний пародонта [17].
В комплексном лечении заболеваний пародонта большое значение придается физиотерапевтическим методам лечения. Общеизвестны устройства для введения лекарственных веществ постоянным электрическим током, широко применяется переменное магнитное поле, лазеротерапия гелийнеоновым лазером, вакуум-электрофорез, комбинированная КВЧ-лазерная терапия и др. [3].
Таким образом, анализ литературы свидетельствует о неудовлетворенности стоматологов существующими методами лечения пародонтита, обширном поиске новых, более эффективных способов лечения данной патологии, позволяющих получить наиболее эффективное, патогенетически обоснованное лечебное воздействие на ткани пародонта.
Рецензенты:
Максимальное сохранение собственных зубов является, по сути, манифестом для всех пародонтологов, и целью, за которой уже многие годы следуют все стоматологи. Технологические усовершенствования сделали данную цель уже более достигаемой, чем ранее, но даже несмотря на возможности пародонтальной регенерации и реконструкции периодонтальной связки, цемента, десен и альвеолярной кости, полностью решить проблему пародонтальных поражений так и не удалось.
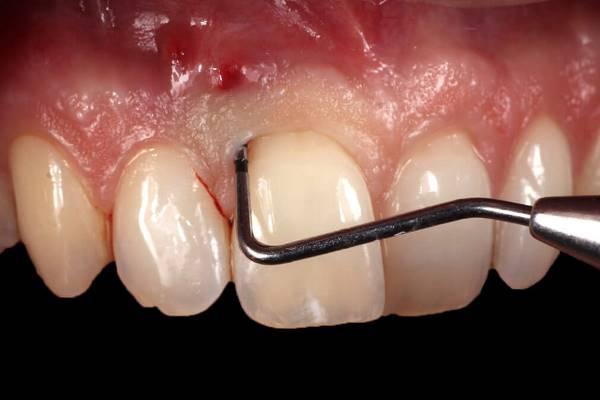
Растущее количество фактических данных указывает на наличие связи между патологией пародонта и системными заболеваниями организма: например, была обнаружена зависимость между пародонтитом умеренно-тяжелой степени сложности и повышенным риском возможности развития диабета. Эпидемиологические данные также свидетельствуют о том, что пародонтит повышает риск развития сердечно-сосудистых заболеваний. Хотя имеющихся данных пока что недостаточно, однако ученые уже отметили возможность существования патофизиологической связи между пародонтитом и хронической обструктивной болезнью легких, пневмонией, хронической болезнью почек, ревматоидным артритом, когнитивными нарушениями, ожирением, метаболическим синдромом и раком. Регенеративные методы коррекции пародонтальных нарушения нацелены не на замедление процесса прогрессирования заболевания, но на восстановление сформировавшихся дефектов мягких и твердых тканей, защиту еще интактных единиц зубного ряда и подготовку пораженных участков для дальнейшей реабилитации с использованием имплантатов. Однако воспаление, ассоциированное с пародонтитом, все же может быть уменьшено в процессе повторного физиологического восстановления тканей за счет естественных биологических механизмов.
Типы регенеративных техник пародонтальных вмешательств
Многие новые появляющиеся методы регенераторных пародонтальных вмешательств, в том числе и те, которые предполагают использование систем доставки определенных клеток, матричных остовов, костных анаболических агентов и мезенхимальных стволовых клеток, находятся на ранней доклинической стадии апробации и требуют дополнительного научного исследования для их дальнейшей имплементации в клиническую стоматологическую практику. Процедуры твердотканной аугментации позволяют восстановить костную ткань, периодонтальную связку и корневой цемент, которые в своем комплексе обеспечивают стабилизацию зуба. Процедуры мягкотканой аугментации позволяют стимулировать рост новых десен в области рецессии, улучшая эстетической вид слизистой. Наиболее распространенными в клинической практике являются следующие три типа пародонтальных ятрогенных вмешательств: костная аугментация, использование биологических агентов и направленная тканевая регенерация (НТР).
Костная пластика
Костная пластика является одной из наиболее долго используемых техник регенеративных ятрогенных вмешательств, в ходе реализации которой может быть использована собственная костная ткань пациента (аутотрансплантат), костная ткань другого пациента (аллотрансплантат), костная ткань разных видов животных (ксенотранслпантат), или же искусственно синтезированная костная ткань (аллопластный трансплантат). Со временем используемый аугментат замещается костью пациента.
Направленная тканевая регенерация
Процедура направленной регенерация тканей предусматривает применение барьерной мембраны для защиты и стабилизации кровяного сгустка в ходе процесса заживления области костной аугментации. Любые вмешательства в структуру кровяного сгустка во время заживления раны могут вызвать нарушения и формирование рубцовой ткани вместо новой кости и связки. Используемые мембраны могут быть резорбируемыми и нерезорбируемыми. Первые идеально подходят при вмешательствах непосредственно на пародонте, другие – лучше всего работают в ходе реконструкции альвеолярного гребня и его подготовки под будущую установку имплантатов. Резорбируемые мембраны исключают потребность проведения повторных хирургических вмешательств с целью их удаления, что очень удобно для пациента. Но при этом они также должны характеризовать соответствующими параметрами деградации, которые позволят удержать достаточный объем пространства для его выполнения костной тканью. В случаях, когда основная барьерная функция мембраны может быть компрометирована анатомическими особенностями в области вмешательства, врач должен прибегнуть к альтернативному методу лечения. Так, вместо мембраны можно использовать костный графт, который характеризуется достаточно быстрой резорбцией. Мембраны, которые резорбируются слишком медленно, могут препятствовать притоку крови к регенерированным структурам, и более часто подвергаются инфицированию. Как и в любом клиническом случае, врач должен использовать НТР только в клинических условиях, оптимально подходящих для такого вида вмешательства. Кроме того, для обеспечения успешности НТР врач должен провести прецизионную деконтаминацию корня зуба в области реализации основного хирургического вмешательства. Следует отметить, что надлежащая дезинфекция корня зуба также требует специальных технических навыков и соответствующего опыта.
Биопрепараты
Биологические агенты продемонстрировали значительный потенциал в процессе восстановления пародонтальных ран. Такие препараты включают факторы роста, производные эмалевого матрикса и костные анаболические агенты, которые стимулируют клетки к пролиферации, миграции, биосинтезу или дифференцированию матрикса. Как правило, большинство техник использования биопрепаратов являются на ранних стадиях апробации, однако некоторые из них уже довольно широко применяются в клинической практике. В будущем планируется проводить индивидуализированные пародонтальные вмешательства с учетом генетического фона пациента, использованием биомаркеров с целью прогноза, трехмерных технологий с целью планирования и клеточных остовов в качестве основных материалов для трансплантации.
Регенеративные процедуры при дефектах в области фуркации и внутрикостных дефектах
Результаты, полученные Huynh-Ba и коллегами, указывают на то, что НТР области фуркационных дефектов обеспечивает высокую выживаемость пролеченных зубов на уровне 83,3-100% в ходе 5-12 летнего мониторинга. Внутрикостные дефекты развиваются при внутреннем пародонтальном поражении альвеолярного гребня. Lang и коллеги рекомендуют оценить морфологию внутрикостного дефекта по количеству пораженных костных стенок.
Классификация Goldman и Cohen (1958) предполагает наличие четырех классов дефектов:
- с поражением трех или четырёх костных стенок;
- с поражением двух костных стенок;
- с поражением одной костной стенки;
- комбинированные дефекты (например, с поражением 3 и 2 стенок и т.д.).
Цель пародонтальной терапии любых типов дефектов состоит в непосредственной регенерации тканей пародонта, включая аппозицию нового цемента с проникновением в него волокон пародонтальной связки. Reynolds и коллеги установили, что регенеративное лечение внутрикостных пародонтальных дефектов повышает уровень клинического прикрепления, способствует редукции пародонтальных карманов и улучшает общее состояние пародонта. Алгоритм восстановления внутрикостных дефектов, как правило, предусматривает костную аугментацию посредством разных типов трансплантатов, однако с той же целью можно использовать методы направленной регенерации тканей и принципы применения биологически активных агентов.
От теории к практике
Материалы семинара AAP по регенерации были опубликованы в Journal of Periodontology, и включали в себя консенсусные отчеты и систематические обзоры по восстановлению мягкотканного покрытия поверхности корней, дефектов в области фуркаций и реконструкции пародонта. Сопровождающие практические рекомендации были опубликованы в журналах Clinical Advances in Periodontics и Journal of Periodontology, которые сформировали, собственно, переход от теории к практике.
Методы лечения дефектов рецессии десны представляют собой ключевую проблему в возможностях регенерации пародонта. Рецессия десны является довольно распространённым состоянием, и участники семинара сошлись на том, что оценка результатов его коррекции должна проводиться с учетом уменьшения глубины дефекта, улучшения уровня клинического прикрепления и прироста кератинизированных мягких тканей. С целью восстановления покрытия обнаженной поверхности зуба можно использовать техники субэпителиального соединительнотканевого лоскута, коронально смещенного лоскута, свободного десневого графта и его аналогов, по типу бесклеточного дермального матрикса, кетогенного коллагенового мактрикса и биоактивных агентов (рекомбинантного фактора роста, полученного из тромбоцитов или производных эмалевой матрицы).
Reynolds и коллеги резюмировали, что выбор наиболее эффективного метода лечения внутрикостных дефектов зависит от проведенной полноценной диагностики и учета пациент-ассоциированных факторов риска. При этом авторы также резюмировали, что терапевтические подходы, предусматривающие использование комбинированных техник лечения, также являются достаточно успешными. Так, например, бесклеточные трансплантаты для замещения дефектов, которые используются в протоколе направленной регенерации тканей, способствуют достижению надлежащей стабильности области аугментации, защите кровяного сгустка и формированию новой ткани. При этом данный подход, по сути, не предусматривает использование биологически-активных агентов. Выбор метода лечения внутрикостных дефектов должен предполагать анализ таких параметров, как количество резидуальных интактных стенок, потерю высоты ткани, близость дефекта к другим структурам, возможность достижения надлежащей васкуляризации в будущем.
Aichelmann-Reidy при лечении патологии в области фуркации рекомендуют учитывать системные пациент-ассоциированные факторы, локализированные анатомические возможности и характеристики самой области фуркации. Дефекты фуркации по II классу, как правило, подлежат прогнозированному лечению с применением методов регенераторного лечения, а дефекты по I классу можно восстановить посредством комбинации костной аугментации и изолирующих мембран. Lin и коллеги указывают на то, что современные технологии прогрессивно способствуют развитию новых пародонтально-регенеративных методов лечения, и публикующиеся клинические отчеты свидетельствуют о еще большей вариативности актуальных методов вмешательства на тканях пародонта. Однако, остается еще одна проблема – дефицит доказательной базы, но данный аспект зависит лишь от времени и результатов имплементации различных подходов.
Систематизированный консенсусный доклад Cochran и коллег о приоритетах будущих исследований в области новых пародонтальных технологий можно представить в виде последующих тезисов:
- Необходимо разработать неинвазивные методы оценки клинических результатов регенераторных вмешательств на пародонте. Такой подход должен также позволить оценить эффективность новых методов лечения.
- Необходимо провести валидацию тех методов лечения, которые используются не по прямому назначению, ведь некоторые пародонтальные техники вмешательства были оригинально разработаны для совсем других целей.
- Для персонализации лечения необходимо обеспечить анализ генетического и эпигенетического профилей пациента.
- Для выбора определенного метода лечения необходимо оценить влияние патогенеза, этиологии и потенциала к регенерации при разных формах поражений пародонта.
- Для более прогнозированного лечения и восстановления структуры и функции пародонта врач должен систематизировать все потенциальные факторы риска, связанные с ятрогенным вмешательством.
- Необходимо определить молекулярные и клеточные механизмы каждого из методов лечения с использованием моделей in vitro и in vivo.
- Необходимо определить пути развития пародонтальных поражений для оптимизации применения различных методов регенеративной терапии.
- Исследователи должны сосредоточиться на разработке минимально инвазивных технологий для минимизации постоперационных болевых ощущений и дискомфорта без ущерба для результатов реабилитации.
- Необходима разработка критериев, определяющих клинический успех вмешательств.
- Необходима оценка влияния выбранного метода регенераторной пародонтальной терапии на качество жизни пациента.
Заключение
Регенеративная терапия с использованием трансплантатов мягких и твердых тканей, биологических агентов или направленной тканевой регенерации имеет многообещающее будущее в отрасли пародонтологии. Ряд дополнительных регенеративных методов, включая новые системы доставки клеток, является весьма перспективным, но требует дальнейшего научного исследования для определения их эффективности. Результаты консенсусных семинаров по регенерации пародонта указывают на наличие сильной доказательной базы, подтверждающей эффективность реконструктивной терапии пародонтальных дефектов, позволяющей восстановить не только структуру мягких и твердых тканей, но и их полноценную функцию. Использование регенеративных вмешательств в области пародонта также способствует сохранению собственных зубов пациента, что является одной из наиболее важных целей в пародонтологии.
Авторы:
William V. Giannobile, DDS, DMSc
Pamela K. McClain, DDS
П ричиной воспаления десневого края является группа грамотрицательных бактерий, находящихся в биопленке и соединенных с поддесневой поверхностью корня зуба. Vector — это ультразвуковая стоматологическая система, предназначенная для минимально инвазивного лечения воспалительных заболеваний пародонта, микроинвазивного препарирования твердых тканей зуба и финишной обработки реставраций. Благодаря консервативному принципу работы и использованию не имеющих вибрационного момента минимально инвазивных инструментов достигается лояльность пациентов к лечению.
Среди актуальных проблем стоматологии одно из ведущих мест занимают заболевания пародонта. По данным ВОЗ выраженные деструктивные изменения в пародонте с вовлечением в процесс костной ткани наиболее часто выявляются у лиц от 35 до 44 лет – от 65 % до 98%, а в возрасте от 13 до 19 лет — от 55% до 95% [1].
Заболевания пародонта неблагоприятно действуют на функцию пищеварения психоэмоциональную сферу, снижают резистентность организма к действию инфекционных и других факторов, приводят к сенсибилизации больного. Средняя степень пародонтита не воспринимается больными как опасное заболевание. В основном их беспокоят такие проблемы, как воспаление, кровоточивость и, особенно, рецессия (снижение уровня) десны, приводящая к удлинению шеек зубов и соответствующим эстетическим нарушениям [2].
Пародонтит протекает в несколько стадий, и чем раньше начато лечение, тем больше шансов стабилизировать процесс и предотвратить потерю зубов. Одним из современных методов лечения пародонтита в настоящее время является применение стоматологической системы Vector.
Vector — это ультразвуковая стоматологическая система, предназначенная для минимально инвазивного лечения воспалительных заболеваний пародонта, микроинвазивного препарирования твердых тканей зуба и финишной обработки реставраций.
Показаниями для лечения с применением данной системы являются следующие заболевания: гингивит, хронический генерализованный и локализованный пародонтит различных степеней тяжести, быстропрогрессирующий пародонтит. ювенильный пародонтит, периимплантиты, обработка кариозных полостей, нависающих краев реставраций, полировка пломб [4].
Принцип работы Vector System сходен с ультразвуковыми очистительными ваннами и дроблением камней в почках. В процессе работы инструментом практически на всех участках соприкосновения с поверхностью зуба скорость движения насадки одинакова, и зон с ускорением или отсутствием движения не образуется. Продольные колебания насадки, полученные таким образом, практически исключают вибрацию инструмента и неконтролируемые боковые движения.
Вторым важным элементом системы Vector являются специальные суспензии — абразивная и полирующая, обеспечивающие непрямую передачу ультразвуковой энергии на операционное поле. Полирующая жидкость содержит частицы гидроксиапатита размером до 10 цт и предназначена для полирования поверхности зуба, обработки корня и удаления мягкого зубного налета. Мелкие частички гидроксиапатита не вызывают повреждения твердых структур зуба.
Абразивная жидкость содержит режущие частички карбида кремния размером около 40-50 цт. Эта жидкость применяется для удаления твердых зубных отложений, препарирования кариозных полостей, удаления нависающих краев реставраций [5].
Инструмент во время работы практически не нагревается, поэтому не требуется большого количества жидкости для его охлаждения. Строго заданная частота и амплитуда продольных колебаний насадки позволяет также удерживать жидкость на кончике инструмента независимо от его положения в полости рта, при этом разбрызгивание жидкости и образование аэрозоля не происходит. Работающий инструмент всегда окружен достаточной водяной пленкой. Пульсирующая подача жидкости обеспечивает хороший очищающий эффект [6].
Как правило, пациенты очень позитивно воспринимают терапию без использования ультразвуковых приборов, и методы, когда не используются приборы с эффектом вибрации, являются щадящими, сокращают время лечения различных видов пародонтит и во многих случаях позволяют обойтись без анестезии. Адгезивная поддесневая биопленка удаляется с помощью суспензии Vector с мелкозернистыми частицами (абразивная суспензия). Энергия прибора Vector опосредованно передается через содержащие жидкость пародонтальные карманы на соседние ткани. Благодаря предотвращению колебаний, направленных перпендикулярно поверхности корня, во время лечения наблюдаются лишь незначительные болевые ощущения [8].
Аналогично закрытому кюретажу с помощью ручных инструментов, система Vector имеет различные насадки для различных поверхностей передних и жевательных зубов. В то время как участки поверхности без наличия минерализованных отложений могут быть обработаны достаточно быстро, участки с отложениями зубного камня обрабатываются более продолжительно, до тех пор, пока тактильно или с помощью оптического контроля не наступит уверенность в их исчезновении. Возможные остатки отложений, которые не удается удалить при закрытом и даже при открытом кюретаже, обрабатываются дополнительно поверхностно и, таким образом деконтаминируются. Интенсивного сглаживания корня, возникающего при форсированной обработке острыми кюретами, следует избегать для сохранения важных для регенерации тканевых структур, особенно корневого цемента и мягких тканей пародонтальных карманов. Тем более, что при интенсивном сглаживании корня с удалением корневого цемента не ожидается лечебного эффекта, в отличие от осторожной и щадящей обработки. А отказ от обширного удаления корневого цемента или дентина, особенно у витальных зубов, обеспечивает минимизацию послеоперационной гиперчувствительности. Терапевтический успех противовоспалительного лечения связан не только лишь с механической обработкой, а зависит также от биологических реакций ткани на лечение [9].
Список использованной литературы
Пародонт ауруын емдеудің заманауи тәсілдері
Рысмендиева А.Д.
Түйін Тістің қызыл иегі шеттерінің қабынуына биоүлбір мен тістің түбіндегі қызыл еттің шетінде болатын грамтерістеуші бактериялар себеп болады. Vector — бұл тістің пародонтты қабынуын шағын инвазивті емдеуге лайықталған, ультрадыбыстық стоматологиялық жүйе,тістің қатты тінін микроинвазивті жолмен тесіп, фиништік жөндеу жасап өңдейді.
Жұмыстың консервативті принциптері мен вибрациялық сәттердің болмауына байланысты және инвазивті құралдардың аздығы себебінен пациент бұл емді дұрыс көреді.
Modern methods of treatment of periodontal disease
Rysmendieva A.
Abstract The cause of inflammation of the gingival margin is a group of Gram-negative bacteria in the biofilm and connected with the subgingival surface of the tooth root. Vector — a dental ultrasonic system for minimally invasive treatment of inflammatory periodontal disease, microinvasive preparation of dental hard tissues and finishing restorations. Due to the conservative principle of operation and use of non-vibratory torque is achieved by a minimally invasive instruments loyalty of patients to treatment.
Рысмендиева А.Д.
Отделение стоматологии
Центральная клиническая больница УДП РК
При пародонтите ткани вокруг зубов разрушаются – на фоне воспаления и инфекции убывают десны, оголяются корни, разрушаются периодонтальные связки, цемент зуба и альвеолярная кость. Вернуть их в норму очень важно не только для красоты улыбки. Эти ткани удерживают зубы в лунках. А стабильный зубной ряд – это основа правильного прикуса и жевания без боли.
Как восстановить здоровые ткани на месте утерянных? На помощь приходят биотехнологии – нано- и биоактивные препараты с факторами роста, ускоряющие естественное заживление. Грубо говоря, они запускают рост собственных клеток организма, что не только эффективно, но и очень безопасно.
Они не используются исключительно как самостоятельное средство лечения, но входят в комплексы Smile Recovery, где каждый этап продуман не просто для купирования воспаления, но и для восстановления до 80% разрушенных тканей.
Ускоренная реабилитация
Запуск процессов естественной регенерации клеток позволяет восстановить до 80% поврежденных тканей за первый год с последующим нарастанием эффекта
Исследованные материалы
Используем препараты ведущих брендов, которые подтвердили свою эффективность в многочисленных международных исследованиях на протяжении более 10 лет
Продолжительный эффект
Биопрепараты обладают длительным действием после однократного введения – эффект нарастает до нескольких лет
Стабильная ремиссия
Восстанавливается местный иммунитет и барьерные функции тканей пародонта, защищающие от повторного воспаления
Укрепляем зубы, восстанавливаем десны и дарим красивые улыбки! Используем передовые технологии и препараты с факторами роста.
В чем польза биопрепаратов при лечении пародонтита?
Инфекция при пародонтите как пожар. Даже если его потушить, остаются последствия – рецессии десен, внутрикостные дефекты, разрушенные связки, которые заживают очень медленно или вообще не могут восстановиться самостоятельно. Это места с ослабленным иммунитетом. Они могут стать отправной точкой для повторного воспаления.
При комплексном лечении важно восстановить разрушенные ткани быстро и в максимально возможном объеме – это еще одна гарантия, что пародонтит не вернется. Биопрепараты, обогащенные факторами роста, активируют в тканях местный иммунитет и дают толчок к правильному естественному заживлению.
Согласно исследованиям, биоматериалы последнего поколения способны за 1 год восстановить до 80% разрушенных мягких тканей: десневый карман закрывается здоровой тканью почти на 5 мм при легкой и средней стадиях пародонтита. 1 С помощью биопрепаратов успешно восстанавливают и кость.
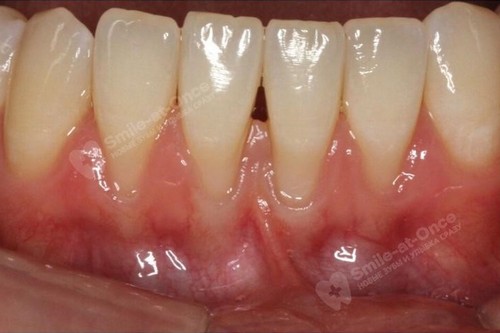
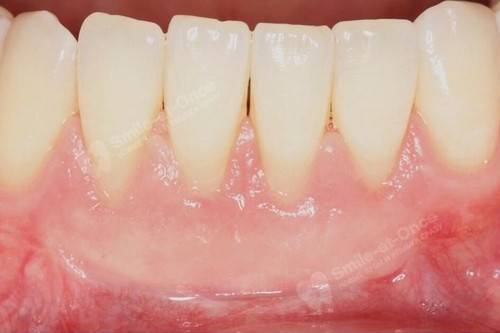
Каких результатов можно достичь?
Если проводить лечение в комплексе, то первые видимые результаты появятся уже через 2-3 месяца. А через год можно достигнуть практически полной ремиссии – после этого результат при проведении поддерживающей терапии будет только нарастать.
.jpg)
- восстановление мягких тканей,
- поддержание здоровья пародонта.
- устранение воспаления и восстановление тканей,
- достижение стойкой ремиссии.
- интенсивное восстановление мягких тканей и кости,
- сохранение зубов.
Какие препараты используются
Есть три направления, в которых используются препараты с факторами роста:
- для заживления мягких тканей и десен – биогели и препараты с факторами роста и биологическими агентами,
- для восстановления костных структур – подсадка биосовместимых костнозамещающих материалов в виде крошки, гранул или блоков,
- направленная регенерация тканей с применением барьерных коллагеновых мембран.
Специалисты центра Smile-at-Once уже много лет используют разработки передовых компаний в области регенеративных технологий. В частности, для лечения пародонтита мы активно применяем биоматериалы ведущих брендов Straumann, Geistlich и Nobel Biocare. Их эффективность подтверждена как многочисленными международными исследованиями, так и нашим многолетним практическим опытом.
В свободной продаже такие средства не найти, медицинские организации закупают их по договору у компании-поставщика. Препараты достаточно дорогие и могут использоваться только под контролем врача.
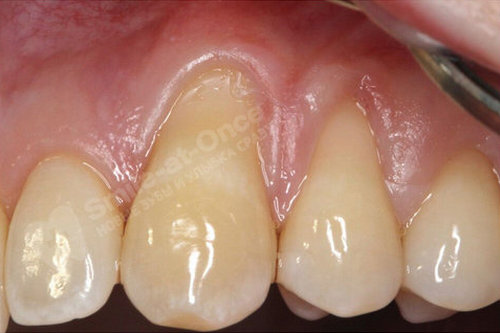
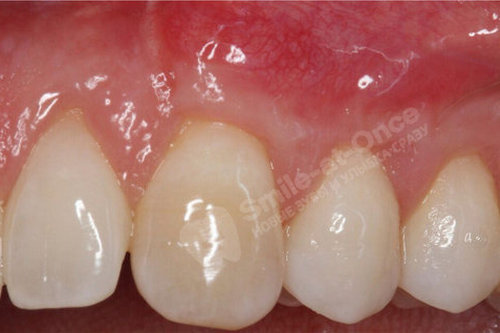
С помощью последних достижений медицины восстановить разрушенные пародонтитом десны и кость РЕАЛЬНО!
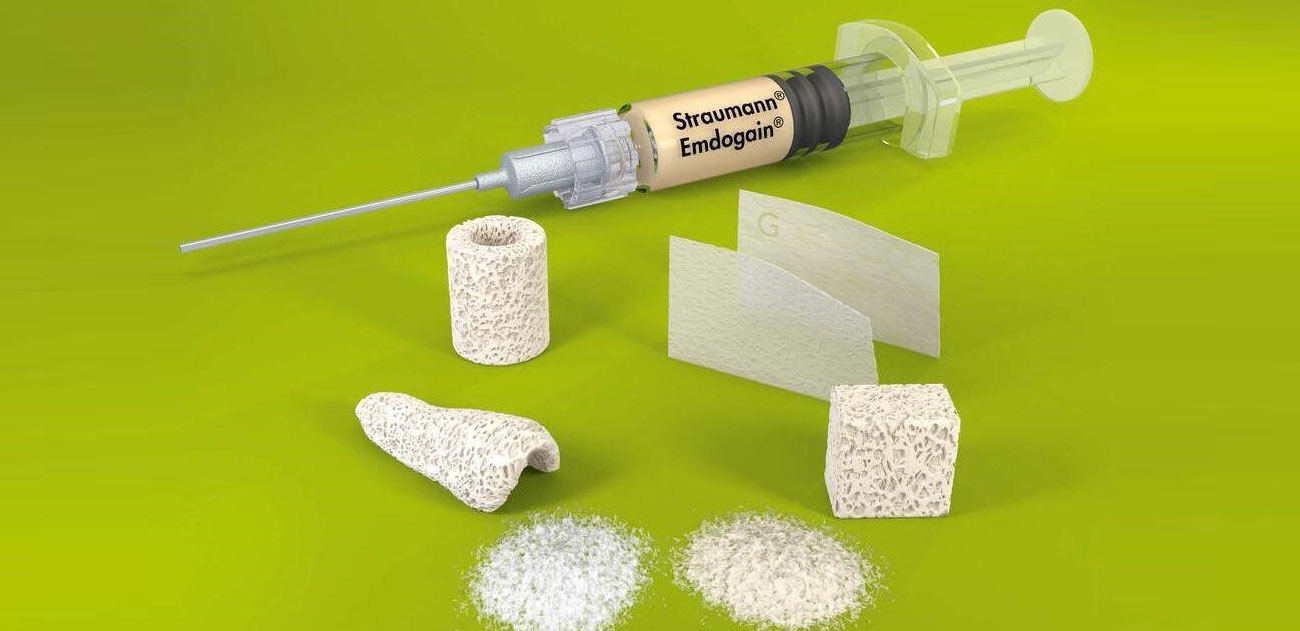
Биогель Emdogain® от Straumann для регенерации тканей пародонта
Это биоактивный гель на основе смеси эмалево-матричных протеинов, обогащенный факторами роста.
- цель применения: сократить рецессию десны, восстановить мягкие ткани, пародонтальную связку, корневой цемент и альвеолярную кость,
- форма выпуска: предварительно заполненный гелем одноразовый шприц в стерильном запечатанном блистере,
- как используют: однократно вводят под десны специальной насадкой или наносят на очищенные корни зубов во время открытого кюретажа,
- как работает: создает богатую протеиновую среду для активного роста и деления здоровых клеток, благодаря чему восстанавливаются костные структуры и мягкие ткани, а новая периодонтальная связка надежно прикрепляется к цементу зуба.
У Emdogain отличная биосовместимость, а также прогнозируемые результаты. Биогель используется порядка 20 лет, лечение успешно прошли более 2 миллионов пациентов. Количество послеоперационных осложнений на фоне использования Emdogain снижено почти до нуля – их менее 0,002%.
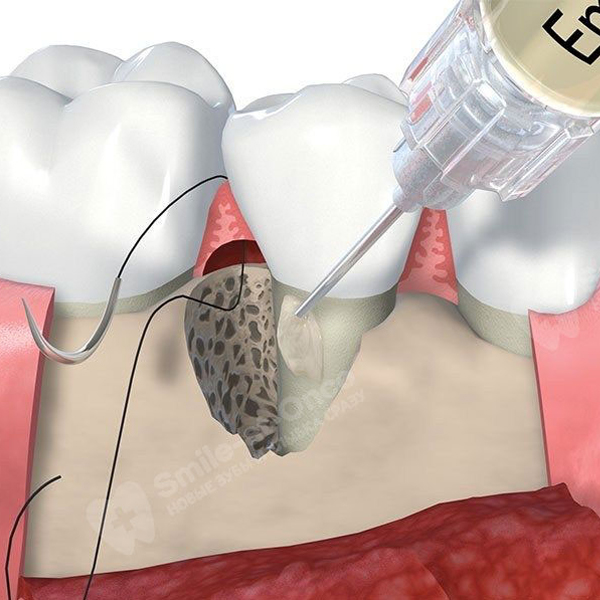
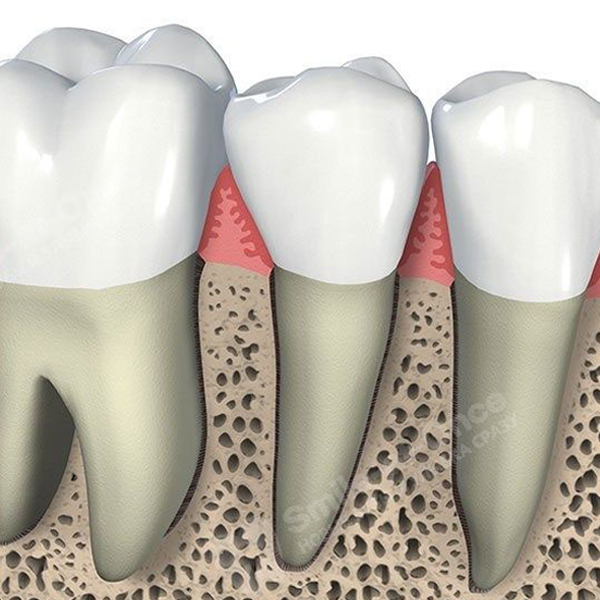
Эффективность препарата доказана более чем в 600 клинических исследований и 1000 международных научных трудов (их легко найти в открытых международных базах научных медицинских публикаций), а долгосрочные результаты изучались в течение 10-12 лет. 2
В частности, доказано, что после применения Straumann® Emdogain® глубина десневого кармана сокращается в среднем на 4.94 мм за 1 год, то есть дефект на 74% закрывается здоровыми мягкими тканями. И со временем эффект только нарастает.

- Революционные комплексы с применением биоматериалов нового поколения
- Купируем пародонтит и восстанавливаем здоровье десен
- Восстанавливаем до 80% поврежденных тканей в течение 1 года
Синтетическая костная крошка BoneCeramic® от Straumann для восстановления дефектов кости
Это один из самых изученных и эффективных искусственных костных заменителей, который применяется для восполнения объема различных костных дефектов, травм, трещин и атрофированных участков.

BoneCeramic® применялся более чем в 300 000 клинических случаях по всему миру параллельно с установкой имплантов и лечением пародонтита. Согласно одному из 55 исследований материала, опубликованному на портале PubMed, подсадка синтетической костной крошки при пародонтите позволила за 1 год значительно улучшить состояние кости, повысить выживаемость зубов и закрыть дефекты на 85%. 3
Костнозамещающий материал Bio-Oss от Geistlich
Это биосовместимые минеральные костные гранулы или блоки вещества кости, которые получают из высокоочищенного натурального материала. Так же, как и BoneCeramic®, Bio-Oss применяют для восстановления твердых тканей, утерянных при пародонтите.
- цель применения: сформировать начальный костный каркас и запустить регенерацию естественной кости,
- форма выпуска: в виде стерильно упакованных гранул или костных блоков,
- как используют: смешивают с физраствором или кровью пациента, а после вносят на участок с недостающей костью,
- как работает: принцип действия тот же, что и у BoneCeramic – Bio-Oss заполняет дефект, хорошо интегрируется с костью, создает новый костный каркас и, рассасываясь в течение нескольких лет, стимулирует рост собственной твердой ткани. Причем скорость рассасывания рассчитана так, что материал не проседает в месте подсадки, пока новая кость заполняет участок.
Geistlich Bio-Oss® используется больше 25 лет, а эффективность его применения исследована более чем в 900 научных трудах. Это один из лидирующих материалов в регенеративной стоматологии во всем мире. 4

Коллагеновая мембрана Creos xenoprotect® от Nobel Biocare
Это саморассасывающаяся прочная мембрана из переплетенных волокон коллагена и эластина – натуральных фибриллярных белков, входящих в основу соединительной ткани. Мембраны используют как барьер при направленной тканевой и костной регенерации совместно с костной крошкой, чтобы восстановить поврежденные участки кости и небольшие пародонтальные дефекты.

Мембраны наделяют противовоспалительными и противомикробными свойствами, а также обогащают биологическими веществами, усиливающими остеогенез, то есть образование новой костной ткани.
Creos xenoprotect® успешно применяется в имплантологии и пародонтологии, участвует в продолжительных исследованиях по всему миру. Мембрана способствует стабильному росту здоровой кости и снижает риск осложнений. 5
Используем лучшие средства для безболезненного и надежного восстановления тканей пародонта. Избавьтесь от болезни навсегда!
Есть ли недостатки у биотехнологий?
Регенерация тканей с помощью биоактивных препаратов и материалов – на данный момент одна из самых многообещающих концепций в комплексном лечении пародонтита. Недостатков у этих методов практически нет – технологии задействуют собственные силы организма, обладают высокой биологической совместимостью, почти не дают побочных аллергических реакций и осложнений. Показатель успешности технологий приближается к 90% – при благоприятных условиях десна, кость и связочный аппарат снова смогут удерживать зубы, что уберегает их от выпадения, позволяет спокойно жевать и улыбаться.
Единственный возможный минус – высокая стоимость такого лечения. Но, как показывает практика, достаточно 1-2 процедур, чтобы запустить процесс устойчивой регенерации тканей на годы вперед.
Стоимость процедур с использованием препаратов Straumann Emdogain®, BoneCeramic®, Bio-Oss® или Creos™ уже входит в наши комплексные программы Smile Recovery. Вам не нужно оплачивать их отдельно.
Также в лечении пародонтита очень важно отношение самого пациента к собственному здоровью – даже передовые биоразработки не дадут результата, если отступать от комплексного плана лечения, пропускать процедуры и контрольные осмотры у пародонтолога и небрежно относиться к гигиене полости рта.
Альтернативные методы
В долгосрочной перспективе биоматериалы дают самые стабильные результаты – они продолжают действовать вплоть до нескольких лет с момента применения. В этом плане другие методы, влияющие на регенерацию мягких тканей, существенно уступают.
Например, плазмолифтинг или инъекционная терапия больше направлены на снятие воспаления и восстановление микроциркуляции в тканях пародонта. Это поддерживающие методы лечения, которые создают благоприятные условия для дальнейшего заживления и действуют в короткой перспективе.
1 Tonetti MS, Lang NP, Cortellini P, Suvan JE, Adriaens P, Dubravec D, Fonzar A, Fourmousis I, Mayfield L, Rossi R, Silvestri M, Tiedemann C, Topoll H, Vangsted T, Wallkamm B. Enamel matrix proteins in the regenerative therapy of deep intrabony defects. J Clin Periodontol. 2002
2 Sculean A, et al. Ten-year results following treatment of intrabony defects with enamel matrix proteins and guided tissue regeneration. J Clin Periodontol. 2008
3 Queiroz LA, Santamaria MP, Casati MZ, Ruiz KS, Nociti F Jr, Sallum AW, Sallum EA. Enamel matrix protein derivative and/or synthetic bone substitute for the treatment of mandibular class II buccal furcation defects. A 12-month randomized clinical trial. Clin Oral Investig. 2016
4 iData Inc., European Dental Bone Graft Substitutes and other Biomaterials Market, 2015.
5 Wessing B, Urban I, Montero E, et al. A multicenter randomized controlled clinical trial using a new resorbable non-cross-linked collagen membrane for guided bone regeneration at dehisced single implant sites: interim results of a bone augmentation procedure. Clin Oral Implants Res. 2017
Читайте также:

