Нарушения в иммунной системе при спиде реферат
Обновлено: 01.07.2024
Что такое СПИД (синдром приобретённого иммунного дефицита) -
Синдром приобретённого иммунного дефицита (СПИД, синдром приобретенного иммунодефицита, англ. AIDS) - состояние, развивающееся на фоне ВИЧ-инфекции (англ. Human immunodeficiency virus, HIV) и характеризующееся падением числа CD4+ лимфоцитов, множественными оппортунистическими инфекциями и неинфекционными заболеваниями. По сути является терминальной стадией ВИЧ-инфекции.
Что провоцирует / Причины СПИДа (синдрома приобретённого иммунного дефицита):
СПИД вызывается вирусом иммунодефицита человека, относящимся к семейству ретровирусов, роду лентивирусов.
Как и все ретровирусы, ВИЧ имеет особенность репликации, называемую обратной транскрипцией, и свойство поражать клетки крови человека, имеющие на своей поверхности CD4-рецепторы (CD4+ Т-лимфоциты, макрофаги).
Оболочка вируса состоит из двуслойной липидной мембраны, на поверхности которой имеется ряд белков, таких как:
gp41 - трансмембранный гликопротеин, TM (англ. Transmembrane glycoprotein) и
gp120 - поверхностный гликопротеин SU (англ. Surface glycoprotein).
Патогенез (что происходит?) во время СПИДа (синдрома приобретённого иммунного дефицита):
С помощью gp120 (поверхностного гликопротеина) ВИЧ присоединяется к антиген-CD4 рецептору и ко-рецептору, находящихся на поверхностной мембране клеток. Для Т-лимфоцитов ко-рецептором является CXCR-4, а для макрофагов - CCR-5.
Клеточные мембраны клетки и вируса сливаются, вирус проникает внутрь клетки, где высвобождается вирусная РНК из капсида и начинается с помощью обратной транскриптазы, копирование двух нитей ДНК на вирусной РНК (обратная транскрипция).
Произведённая ДНК проникает внутрь ядра клетки-хозяина и интегрируется с помощью энзима интегразы в хромосому хозяина. С помощью РНК-полимеразы начинается синтез вирусного генома и информационной РНК вирусных белков (англ. RNA-messenger). С информационной РНК на рибосомах клетки считываются вирусные энзимы и структурные белки.
Синтезированные РНК выходят из ядра клетки в цитоплазму, где начинается образование нового вируса. Вирусный геном упорядочивает фермент - протеаза, а с помощью gp41 и gp120 формируется новая оболочка вируса. Новые вирусные частицы отпочковываются от поверхности клетка, захватывая часть её мембраны, и вирусы выходят в кровяное русло, а CD4+ лимфоцит хозяина погибает.
В период острой фазы ВИЧ-инфекции отсутствие специфического иммунного ответа позволяет вирусу активно реплицироваться и достигать высоких концентраций в крови. Вирус заселяет различные ткани, в первую очередь органы лимфатической системы, и разрушает CD4 лимфоциты.
В лимфоидной ткани ВИЧ размножается в течение всей ВИЧ-инфекции, поражая макрофаги, активированные и покоящиеся CD4 лимфоциты, фолликулярные дендритные клетки. Количество клеток, содержащих провирусную ДНК, в лимфоидной ткани в 5-10 раз выше, чем среди клеток крови, а репликация ВИЧ в лимфоидной ткани на 1-2 раза выше, чем в крови. Таким образом, основным резервуаром ВИЧ служат лимфатические узлы.
Кроме того в дендритных клетках лимфатических узлов вирус сохраняется длительное время после периода острой виремии и также является резервуаром инфекции.
Для активации лимфоцитов CD8 и образования антигенспецифических цитотоксических T-лимфоцитов необходимо представление пептидного антигена в комплексе с человеческим лейкоцитарным антигеном класса I (англ. en:Human leukocyte antigen). Дендритные клетки необходимы для начала первичных антигенспецифичных реакций. Они захватывают антигены, перерабатывают и переносят их на свою поверхность, где, в комплексе с дополнительными стимулирующими молекулами, они активируют T-лимфоциты. Зараженные клетки часто не выделяют дополнительных стимулирующих молекул и поэтому не способны вызвать образование достаточного числа клеток ответа (B- и T-лимфоцитов), функция которых зависит от дендритных клеток.
После завершения обратной транскрипции в CD4 лимфоците, вирусный геном представлен провирусной невстроенной ДНК. Для встраивания провирусной ДНК в геном клетки-хозяина, и для образования новых вирусов необходима активация T-лимфоцитов. Контакт лимфоцитов CD4 и антигенпредставляющих клеток в лимфоидной ткани, наличие вирусов на поверхности фолликулярных дендритных клеток и присутствие провоспалительных цитокинов (ИЛ-1, ИЛ-6 и ФНОα) способствует и поддерживает размножению ВИЧ в инфицированных клетках. Поэтому лимфоидная ткань служит самой благоприятной средой для репликации ВИЧ.
Генетические факторы
Некоторые генетические факторы могут предохранять от заражения ВИЧ. Так например: Люди имеющие мутации в CCR5 (корецептор М-тропных штаммов вируса) мало или совсем не восприимчивы к М-тропным штаммам ВИЧ-1, но заражаются Т-тропными штаммами.
Гомозиготность по HLA-Bw4 является предохраняющим фактором от прогрессирования болезни. У гетерозигот по локусам HLA класса I иммунодефицит развивается медленнее, чем у гомозигот.
Исследования показали, что у носителей HLA-B14, B27, B51, B57 и C8 инфекция прогрессирует медленнее, а у носителей HLA-A23, B37 и B49 иммунодефицит развивается быстро. У всех ВИЧ-инфицированных с HLA-B35 СПИД развивался не ранее, чем через 8 лет после заражения.
Исследования также показали: у половых партнеров, несовместимых по HLA класса I, риск заражения ВИЧ при гетеросексуальных контактах ниже.
Иммунитет при СПИДе
В острой фазе ВИЧ-инфекции, в стадии виремии, происходит резкое снижение CD4+ T-лимфоцитов за счёт прямого лизирующего действия вируса и нарастание числа копий вирусной РНК в крови.
После этого отмечается стабилизация процесса с некоторым увеличением числа CD4 клеток не достигающим, однако, нормальных величин.
Положительная динамика обусловлена увеличением числа цитотоксических CD8+ Т-лимфоцитов. Эти лимфоциты способны уничтожать ВИЧ-инфицированные клетки напрямую путем цитолиза без ограничения по человеческому лейкоцитарному антигену класса I (англ. Human leukocyte antigen-HLA).
Кроме того они секретируют подавляющие факторы (хемокины), такие как RANTES, MIP-1alpha, MIP-1beta, MDC, препятствующие размножению вируса путём блокировки корецепторов.
ВИЧ специфичные CD8+ лимфоциты играют главную роль в контроле острой фазы ВИЧ-инфекции, однако при хроническом течении инфекции не коррелируется с виремией, так как:
• Пролиферация и активация лимфоцитов CD8+ зависит от антиген-специфичных T-хелперов CD4.
• Лимфоциты CD8+ также могут заражаться ВИЧ, что может вести к снижению их числа.
Синдром приобретённого иммунодефицита является терминальной стадией ВИЧ-инфекции, развивается, у большинства больных, при падении числа CD4+ Т-лимфоцитов, крови ниже 200 клеток/мл (норма CD4+ T-лимфоцитов 1200 клеток/мл).
Депрессию CD4+ клеток при ВИЧ-инфекции объясняют следующими теориями:
• Гибель CD4+ T-лимфоцитов в результате прямого цитопатического действия ВИЧ
• ВИЧ поражает в первую очередь активированные лимфоциты CD4, а поскольку специфичные к ВИЧ лимфоциты входят в число первых клеток, активируемых в ходе ВИЧ-инфекции, они страдают одними из первых.
• Изменение вирусом клеточной мембраны CD4+ T-лимфоцитов, что ведёт их к слиянию между собой с образованием гигантских синцитиев, которое регулируется LFA-1 (англ. Lymphocyte function-associated antigen 1)
• Катастрофа CD4 клеток антителами, как результат антител-зависимого цитотоксического действия (англ. ADCC-antibody-dependent cellular cytotoxicity).
• Активация естественных клеток-киллеров[49][50].
• Аутоиммунная катастрофа
• Связывание белка вируса gp120 с CD4-рецептором (маскировка CD4-рецептора) и как результат - невозможность опознания антигена, невозможность взаимодействия CD4 с HLA класса II.
• Запрограммированной клеточной смертью.
• Анергия иммунного ответа (греч. Ανεργία - праздность, безделье, англ. Anergy).
B-лимфоциты при ВИЧ-инфекции подвергаются поликлональной активации и выделяют большое количество иммуноглобулинов, ФНОα, интерлейкин-6 и лектин DC-SIGN, который способствует проникновению ВИЧ в T-лимфоциты.
Кроме того наблюдается значительное снижение интерлейкина-2, вырабатываемого CD4-хелперами 1 типа и имеющего критическое значение в активации цитотоксических Т-лимфоцитов (CD8+, CTL) и подавление вирусом секреции макрофагами интерлейкина-12 - ключевого цитокина в образовании и активации T-хелперов 1 типа и NK-лимфоцитов (англ. Natural killer cells).
Антитела к ВИЧ
По одним данным, у 99 % инфицированных, антитела обнаруживаются в течение первых 12 недель (6 - 12 недели) после первичного контакта с вирусом. По другим данным: у 90-95 % в течение 3-х месяцев после заражения, у 5-9 % - через 6 месяцев, 0,5-1 % - в более поздние сроки).
Другая группа анти-gp120 антител, участвующая в антител-зависимом цитотоксическом действии (англ. ADCC) и уничтожении инфицированных ВИЧ CD4+ клеток, может уничтожать и неинфицированные клетки, рецепторы которых связаны свободным gp120, циркулирующим в крови - эффект названный: Innocent bystanders (Bystander killing).
Симптомы СПИДа (синдрома приобретённого иммунного дефицита):
Клинические стадии ВОЗ для взрослых и подростков ≥ 15 лет.
• Острая ВИЧ-инфекция
o Асимптоматическая
o Острый ретровирусный синдром
• Клиническая стадия 1
o Асимптоматическая
o Персистирующая генерализованная лимфаденопатия (ПГЛ)
• Клиническая стадия 2
o Себорейный дерматит
o Ангулярный хейлит
o Рецидивирующие язвы полости рта (два или более эпизода в течение 6 месяцев)
o Опоясывающий лишай (распространённый лишай)
o Рецидивирующие инфекции дыхательных путей - синусит, средний отит, фарингит, бронхит, трахеит, (два или более эпизода в течение 6 месяцев)
o Грибковые поражения ногтей
o Папулёзный зудящий дерматит
• Клиническая стадия 3
o Волосатая лейкоплакия полости рта
o Необъяснимая хроническая диарея продолжительностью более 1 месяца
o Рецидивирующий кандидоз полости рта (два или более эпизода в течение 6 месяцев)
o Тяжёлая бактериальная инфекция (пневмония, эмпиема, гнойный миозит, инфекции костей или суставов, менингит, бактеримия)
o Острый язвенно-некротический стоматит, гингивит или периодонтит
• Клиническая стадия 4 (*)
o Легочной туберкулёз
o Внелегочной туберкулёз (исключая лимфаденопатию)
o Необъяснимая потеря веса (более 10 % в течение 6 месяцев)
o ВИЧ истощающий синдром
o Пневмоцистная пневмония
o Тяжёлая или подтверждённая рентгенологически пневмония (два или более эпизода в течение 6 месяцев)
o Цитомегаловирусный ретинит (с или без колита)
o вирус простого герпеса (англ. HSV) (хронический или персистирующий более 1 месяца)
o Энцефалопатия
o Прогрессирующая мультифокальная лейкоэнцефалопатия
o Саркома Капоши и другие ВИЧ-обусловленные злокачественные новообразования
o Токсоплазмоз
o Диссеминированная грибковая инфекция (кандидоз, гистоплазмоз, кокцидиоидомикоз)
o Криптоспоридиоз
o Криптококковый менингит
o Инфекция вызванная нетуберкулёзными микобактериями, диссеминированная микобактеримия (англ. MOTT)
(*) Если подкрепляются достаточными доказательствами могут быть включены: карцинома заднепроходного отверстия и лимфома (Т-клеточная Ходжкинская лимфома)
Клиническая классификация ВИЧ-инфекции
1. Стадия инкубации
2. Стадия первичных проявлений Варианты течения:
• А. Бессимптомное
• Б. Острая инфекция без вторичных заболеваний
• В. Острая инфекция с вторичными заболеваниями
3. Субклиническая стадия
4. Стадия вторичных заболеваний
• 4А. Потеря массы тела менее 10 %, грибковые, вирусные, бактериальные поражения кожи и слизистых, повторные фарингиты, синуситы, опоясывающий лишай.
• Фазы: прогрессирование в отсутствие антиретровирусной терапии, на фоне антиретровирусной терапии; ремиссия (спонтанная, после антиретровирусной терапии, на фоне антиретровирусной терапии).
• 4Б. Потеря массы тела более 10 %, необъяснимая диарея или лихорадка более месяца, повторные стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних органов, локализованная саркома Капоши, повторный или диссеминированный опоясывающий лишай.
• Фазы: прогрессирование в отсутствие антиретровирусной терапии, на фоне антиретровирусной терапии; ремиссия (спонтанная, после антиретровирусной терапии, на фоне антиретровирусной терапии).
• 4В. Кахексия. Генерализованные вирусные, бактериальные, микобактериальные, грибковые, протозойные, паразитарные заболевания, в том числе: кандидоз пищевода, бронхов, трахеи, легких; пневмоцистная пневмония; злокачественные опухоли; поражения центральной нервной системы.
• Фазы: прогрессирование в отсутствие антиретровирусной терапии, на фоне антиретровирусной терапии; ремиссия (спонтанная, после антиретровирусной терапии, на фоне антиретровирусной терапии).
5. Терминальная стадия
Разрушение CD4+ лимфоцитов является главной причиной прогрессивного ослабления иммунной системы при ВИЧ инфекции, которая приводит, в конечном счёте, к синдрому приобретенного иммунодефицита, СПИД.
СПИД - это стадия ВИЧ-инфекции, при которой развиваются бактериальные, грибковые, вирусные, протозойные инфекции (оппортунистические инфекции) и неинфекционные заболевания, как проявление катастрофы иммунной системы в результате падения числа CD4+ лимфоцитов ниже определённого уровня. По классификации CDC диагноз СПИДа может выставляться при положительных тестах на ВИЧ и количестве CD4+ лимфоцитов ниже 200 клеток/мл. - категории А3, В3 и определённых патологических состояниях включённых в категорию С.
Критериями СПИДа, для взрослых и подростков, согласно протоколам ВОЗ 2006 г. и классификации CDC будут:
Бактериальные инфекции
• Легочной и внелегочной туберкулёз
• Тяжёлые бактериальные или рецидивирующие пневмонии (два или более эпизода в течение 6 месяцев)
• Инфекция вызванная атипичными микобактериями (Mycobacterium avium), диссеминированная микобактеримия
• Сальмонеллезная септицемия
Грибковые инфекции
• Кандидозный эзофагит
• Криптококкоз, внелегочной, криптококковый менингит
• Гистоплазмоз, внелегочной, диссеминированный
• Пневмоцистная пневмония вызываемая Pneumocystis jirovecii (Видовое название возбудителя Pneumocystis carinii было изменено на Pneumocystis jiroveci.)
• Кокцидиоидомикоз, внелегочной
Вирусные инфекции
• Инфекция вирусом простого герпеса (англ. Herpes simplex virus, HSV): хронический или персистирующий более 1 месяца, хронические язвы на коже и слизистых или бронхит, пневмонит, эзофагит
• Цитомегаловирусная инфекция, с поражением любого органа, кроме печени, селезенки и лимфоузлов. Цитомегаловирусный ретинит.
• Инфекция вирусом герпеса человека 8 типа (англ. Kaposhi Sarkoma Herpes Virus, KSHV)
• Инфекция папилломавирусом человека (англ. Human papillomavirus, HPV), в том числе рак шейки матки.
• Прогрессирующая мультифокальная лейкоэнцефалопатия
Протозойные инфекции
• Токсоплазмоз
• Криптоспоридиоз с диареей, продолжающейся более месяца
• Микроспоридиоз
• Изоспороз, с диареей более 1 мес
Другие заболевания
• Саркома Капоши
• Рак шейки матки, инвазивный
• Неходжкинская лимфома
• ВИЧ-энцефалопатия, ВИЧ-деменция
• ВИЧ истощающий синдром
• Вакуолярная миелопатия
Прогноз
Современные методы терапии обеспечивают высокий уровень выживаемости среди больных ВИЧ/СПИД. По данным на 2008 год выживаемость при современной терапии ВИЧ/СПИД составляет от 85,1 % до 99,3 %), в зависимости от того, насколько своевременно диагностировано заболевание и начато лечение.
На сегодняшний день говорить о времени развития СПИДа у ВИЧ-положительных пациентов, находящихся на современной терапии, некорректно. Поскольку современные схемы лечения разработаны в конце девяностых годов, и постоянно дополняются новыми разрабатываемыми классами препаратов. Считается, что ВИЧ-инфицированный находящийся на терапии, может прожить несколько десятилетий или всю жизнь. Однако большое влияние на качество и продолжительность жизни оказывают различные побочные эффекты от препаратов, применяемых при лечении ВИЧ. Прогрессирование ВИЧ зависит от многих факторов, в том числе: от количества CD4 лимфоцитов и числа копий вирусной РНК на момент начала лечения, возраста пациента, уровня доступной медицинской помощи, приверженности больного лечению и появления резистентных штаммов вируса.
Профилактика СПИДа (синдрома приобретённого иммунного дефицита):
Специфическая иммунопрофилактика ВИЧ-инфекции не разработана.
К медицинским профилактическим мероприятиям относятся:
1. Обследование доноров крови, лиц из групп риска.
2. Обследование на антитела к ВИЧ всех беременных.
3. Контроль деторождения у инфицированных женщин и отказ от грудного вскармливания их детей.
4. Пропаганда безопасного секса (то есть использования презервативов).
Профилактика инфицирования в медицинских учреждениях.
Наибольшую опасность распространения ВИЧ представляет кровь. Необходимо тщательно избегать случайных повреждений кожных покровов острыми инструментами. Все манипуляции с больными, а также работу с биологическими материалами от больного медицинские работники проводят в резиновых перчатках и масках. Кроме того, необходимо соблюдать все меры предосторожности, предусмотренные при работе с больными вирусным гепатитом В. Если все же произошёл контакт слизистой оболочки или поврежденной кожи медицинского работника с биологической жидкостью, потенциально содержащей ВИЧ, следует незамедлительно (желательно в первые три часа) начать курс постконтактной профилактики антиретровирусными препаратами, что позволит в несколько раз снизить вероятность инфицирования.
Обязательно тщательное мытье рук после снятия перчаток и индивидуальной одежды перед тем, как покинуть помещение, где проводится работа с потенциально инфицированным материалом.
Госпитализация больных СПИД и ВИЧ-инфицированных должна осуществляться так, чтобы предотвратить распространение инфекции, а также с учетом требований по содержанию больных с измененным поведением при поражении центральной нервной системы.
При лечении больных с ВИЧ-инфекцией необходимо применять инструментарий и шприцы только одноразового использования.
При загрязнении предметов обихода, постельных принадлежностей, окружающей среды выделениями больного необходимо проводить обработку дезинфицирующими средствами (0,2%-ный раствор гипохлорита натрия, этиловый спирт).
При соблюдении элементарных правил предосторожности общение с больными является полностью безопасным.
К каким докторам следует обращаться если у Вас СПИД (синдром приобретённого иммунного дефицита):
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о СПИДа (синдрома приобретённого иммунного дефицита), ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
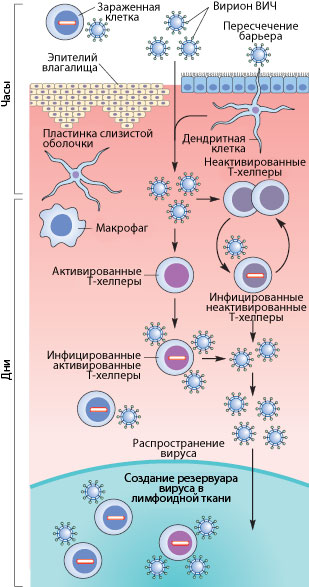
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
* Данная работа не является научным трудом, не является выпускной квалификационной работой и представляет собой результат обработки, структурирования и форматирования собранной информации, предназначенной для использования в качестве источника материала при самостоятельной подготовки учебных работ.
Работа допущена к защите
_______ июня 2008 г.
Иммунитет при СПИДе.
Клинические стадии, классификация ВИЧ/СПИДа.
Острая фаза ВИЧ-1 инфекции.
СПИД (виды инфекций).
Список используемой литературы.
Синдром приобретённого иммунного дефицита (СПИД) — состояние, развивающееся на фоне ВИЧ-инфекции (англ. Human immunodeficiency virus, HIV) и характеризующееся падением числа CD4+ лимфоцитов, множественными оппортунистическими инфекциями и неинфекционными заболеваниями. По сути является терминальной стадией ВИЧ-инфекции.
Данная серьёзная тема выбрана мной потому, что я считаю её весьма актуальной для всего человечества на данный момент. СПИД – это заболевание, против которого пока нет лекарств, поэтому единственное средство предотвращение СПИДА – это избежание новых заражений.
В данном реферате изложена историческая справка, в которой кратко описаны первые случаи заболевания СПИДом, научные исследования и собрания различных организаций по данному вопросу. Также включены глобальные данные распространения СПИДа по всему Земному шару, способы передачи ВИЧ, представлена схема проникновения вируса иммунного дефицита человека в клетку и его дальнейшие действия. Рассказывается о генетических факторах, предохраняющих от заражения ВИЧ, перечислены клинические стадии ВОЗ ВИЧ/СПИДа для взрослых и подростков старше 15 лет. В реферате содержится описание 5ти видов инфекций СПИДа. Уделено внимание диагнозу ВИЧ-инфекций и их лечению.
• 1985 г. — изучены основные пути передачи ВИЧ.
• 1985 г. — регистрация первого случая ВИЧ/СПИДа в СССР у иностранного гражданина.
• 1987 г. — появление первого препарата для лечения СПИДа.
• 1987 г. — регистрация первого случая ВИЧ-инфекции у гражданина СССР.
• 1988 г. — 1 декабря объявлен ООН Всемирным днем борьбы со СПИДом.
• 1995 г. — начало применения препаратов высокоактивной антиретровирусной терапии, позволяющий большинству больных ВИЧ/СПИДом сохранять жизнь.
• 1996 г. — создание объединенной программы ООН по СПИДу.
Распространенность ВИЧ среди взрослого населения по странам:
Источником инфекции является только больной человек.
Основными путями передачи инфекции являются:
Половой (у взрослых и подростков — гомосексуальный и гетеросексуальный), в том числе и работники секс-бизнеса;
Инъекционный и инструментальный — при использовании загрязненных вирусом шприцев, игл, катетеров и т. п. — особенно актуальный и проблематичный в среде лиц употребляющих инъекционные наркотики (наркомания).
Гемотрансфузионный (после переливания инфицированной крови или ее компонентов — плазмы, тромбоцитарной, лейкоцитарной или эритроцитарной массы, концентратов крови, факторов свертывания крови);
Перинатальный (антенатальный, трансплацентарный — от инфицированной матери; интранатальный — при прохождении ребенка по инфицированным родовым путям матери);
Трансплантационный (пересадка инфицированных органов, костного мозга, искусственная инсеминация инфицированной спермой);
Молочный (заражение ребенка инфицированным молоком матери);
Профессиональный и бытовой — заражение через поврежденные кожные покровы и слизистые оболочки людей, контактирующих с кровью или некоторыми секретами (слизью из влагалища, грудным молоком, отделяемым из ран, цереброспинальной жидкостью, содержимым трахеи, плевральной полости и др.) больных ВИЧ-инфекцией.
В то же время ВИЧ не передается при бытовых контактах через слюну, слёзную жидкость и воздушно-капельным путем, а также через воду или пищу. Слюна может представлять опасность только в том случае, если в ней видна кровь.
Болезнь вызывается вирусом иммунодефицита человека, относящимся к семейству ретровирусов, роду лентивирусов.
Как и все ретровирусы, ВИЧ имеет особенность репликации, называемую обратной транскрипцией и свойство поражать клетки крови человека имеющие на своей поверхности CD4-рецепторы (CD4+ Т-лимфоциты, макрофаги).
Оболочка вируса состоит из двухрядной липидной мембраны на поверхности которой имеется ряд протеинов, такие как:
gp41 — трансмембранный гликопротеин, TM (англ. Transmembrane glycoprotein) и
gp120 — поверхностный гликопротеин SU (англ. Surface glycoprotein).
обратная транскриптаза, RT (англ. Reverse transcriptase),
С помощью gp120 (поверхностного гликопротеина) вирус присоединяется к антиген-CD4 рецептору и Co-рецептору, находящихся на поверхностной мембране клеток. Для Т-лимфоцитов Co-рецептором является CXCR-4, а для макрофагов — CCR-5.
Клеточная мембрана растворяется, вирус проникает внутрь клетки, где высвобождается виральная РНК из капсида и начинается с помощью обратной транскриптазы, копирование двух нитей ДНК на виральной РНК (обратная транскрипция).
Синтезированные РНК выходят из ядра клетки в цитоплазму, где начинается образование нового вируса. Виральный геном упорядочивает фермент — протеаза, а с помощью gp41 и gp120 формируется новая оболочка вируса. Клеточная мембрана клетки разрывается, новый вирус выходит в кровяное русло, CD4+ лимфоцит хозяина погибает.
В период острой фазы ВИЧ-инфекции отсутствие специфического иммунного ответа позволяет вирусу активно реплицироваться и достигать высоких концентраций в крови. Вирус заселяет различные ткани, в первую очередь органы лимфатической системы и разрушает CD4 лимфоциты.
В лимфоидной ткани ВИЧ размножается в течение всей ВИЧ-инфекции, поражая макрофаги, активированные и покоящиеся CD4 лимфоциты, фолликулярные дендритные клетки. Количество клеток, содержащих провирусную ДНК, в лимфоидной ткани в 5-10 раз выше, чем среди клеток крови, а репликация ВИЧ в лимфоидной ткани на 1-2 раза выше, чем в крови. Таким образом, основным резервуаром ВИЧ служат лимфатические узлы.
Кроме того в дендритных клетках лимфатических узлов вирус сохраняется длительное время после периода острой виремии и также является резервуаром инфекции.
Для активации лимфоцитов CD8 и образования антигенспецифических цитотоксических T-лимфоцитов необходимо представление пептидного антигена в комплексе с человеческим лейкоцитарным антигеном класса I (англ. en:Human leukocyte antigen). Дендритные клетки необходимы для начала первичных антигенспецифичных реакций. Они захватывают антигены, перерабатывают и переносят их на свою поверхность, где, в комплексе с дополнительными стимулирующими молекулами, они активируют T-лимфоциты. Зараженные клетки часто не выделяют дополнительных стимулирующих молекул и поэтому не способны вызвать образование достаточного числа клеток ответа (B- и T-лимфоцитов), функция которых зависит от дендритных клеток.
После завершения обратной транскрипции в CD4 лимфоците, вирусный геном представлен провирусной невстроенной ДНК. Для встраивания провирусной ДНК в геном клетки-хозяина, и для образования новых вирусов необходима активация T-лимфоцитов. Контакт лимфоцитов CD4 и антигенпредставляющих клеток в лимфоидной ткани, наличие вирусов на поверхности фолликулярных дендритных клеток и присутствие провоспалительных цитокинов (ИЛ-1, ИЛ-6 и ФНО?) способствует и поддерживает размножению ВИЧ в инфицированных клетках. Поэтому лимфоидная ткань служит самой благоприятной средой для репликации ВИЧ.
Некоторые генетические факторы могут предохранять от заражения ВИЧ. Так например:
Люди имеющие мутации в CCR5 (корецептор М-тропных штаммов вируса) мало или совсем не восприимчивы к М-тропным штаммам ВИЧ-1, но заражаются Т-тропными штаммами.
Гомозиготность по HLA-Bw4 является предохраняющим фактором от прогрессирования болезни. У гетерозигот по локусам HLA класса I иммунодефицит развивается медленнее, чем у гомозигот.
Исследования показали, что у носителей HLA-B14, B27, B51, B57 и C8 инфекция прогрессирует медленнее, а у носителей HLA-A23, B37 и B49 иммунодефицит развивается быстро.
У всех ВИЧ-инфицированных с HLA-B35 СПИД развивался не ранее, чем через 8 лет после заражения.
Исследования также показали: у половых партнеров, несовместимых по HLA класса I, риск заражения ВИЧ при гетеросексуальных контактах ниже.
Иммунитет при СПИДе.
В острой фазе ВИЧ-инфекции, в стадии виремии, происходит резкое снижение CD4+ T-лимфоцитов за счёт прямого лизирующего действия вируса и нарастание числа копий вирусной РНК в крови.
После этого отмечается стабилизация процесса (см. график) с некоторым увеличением числа CD4 клеток не достигающим, однако, нормальных величин.
Положительная динамика обусловлена увеличением числа цитотоксических CD8+ Т-лимфоцитов. Эти лимфоциты способны уничтожать ВИЧ-инфицированные клетки напрямую путем цитолиза без ограничения по человеческому лейкоцитарному антигену класса I (англ. Human leukocyte antigen-HLA).
Кроме того они секретируют подавляющие факторы (хемокины), такие как RANTES, MIP-1alpha, MIP-1beta, MDC, препятствующие размножению вируса путём блокировки корецепторов.
ВИЧ специфичные CD8+ лимфоциты играют главную роль в контроле острой фазы ВИЧ-инфекции, однако при хроническом течении инфекции не коррелируется с виремией, так как:
Пролиферация и активация лимфоцитов CD8+ зависит от антиген-специфичных T-хелперов CD4.
Лимфоциты CD8+ также могут заражаться ВИЧ, что может вести к снижению их числа.
Синдром приобретённого иммунодефицита является терминальной стадией ВИЧ-инфекции, развивается, у большинства больных, при падении числа CD4+ Т-лимфоцитов, крови ниже 200 клеток/мл (норма CD4+ T-лимфоцитов 1200 клеток/мл).
Депрессию CD4+ клеток объясняют следующими теориями:
Гибель CD4+ T-лимфоцитов в результате прямого цитопатического действия ВИЧ.
ВИЧ поражает в первую очередь активированные лимфоциты CD4, а поскольку специфичные к ВИЧ лимфоциты входят в число первых клеток, активируемых в ходе ВИЧ-инфекции, они страдают одними из первых.
Изменение вирусом клеточной мембраны CD4+ T-лимфоцитов, что ведёт их к слиянию между собой с образованием гигантских синцитиев, которое регулируется LFA-1 (англ. Lymphocyte function-associated antigen 1).
Катастрофа CD4 клеток антителами, как результат антител-зависимого цитотоксического действия (англ. ADCC-antibody-dependent cellular cytotoxicity).
Активация естественных клеток-киллеров.
Связывание белка вируса gp120 с CD4-рецептором (маскировка CD4-рецептора) и как результат — невозможность опознания антигена, невозможность взаимодействия CD4 с HLA класса II.
Запрограммированной клеточной смертью.
Анергия иммунного ответа (греч. . — праздность, безделье, англ. Anergy).
B-лимфоциты при ВИЧ-инфекции подвергаются поликлональной активации и выделяют большое количество иммуноглобулинов, ФНО?, интерлейкин-6 и лектин DC-SIGN, который способствует проникновению ВИЧ в T-лимфоциты.
Кроме того наблюдается значительное снижение интерлейкина-2, вырабатываемого CD4-хелперами 1 типа и имеющего критическое значение в активации цитотоксических Т-лимфоцитов (CD8+, CTL). и подавление вирусом секреции макрофагами интерлейкина-12 — ключевого цитокина в образовании и активации T-хелперов 1 типа и NK-лимфоцитов (англ. Natural killer cells).
У 99 % инфицированных антитела обнаруживаются в течение первых 12 недель (6 — 12 недели) после первичного контакта с вирусом. В редких случаях антитела не выявляются в течение 6-9 месяцев (у 90-95 % в течение 3-х месяцев после заражения, у 5-9 % — через 6 месяцев, 0,5-1 % — в более поздние сроки).
Другая группа анти-gp120 антител, участвующая в антител-зависимом цитотоксическом действии (англ. ADCC) и уничтожении инфицированных ВИЧ CD4+ клеток, может уничтожать и неинфицированные клетки, рецепторы которых связаны свободным gp120, циркулирующим в крови — эффект названный: Innocent bystanders (Bystander killing).
Клинические стадии, классификация ВИЧ/СПИДа
Реферат на тему: Патофизиология ВИЧ-инфекции и СПИД
Выполнил: Нургалиев А. А.
Студент 2 курса, факультет ОМ, группа №242
Преподаватель: Байбакова М. К.
Содержание
Глава I. Общие понятия о ВИЧ-инфекции и СПИДе………………………. 4
- Определение ВИЧ/СПИД…….…………………………. ………..……4
- Этиология ……………………………………………. …………………4
- Эпидемиология…………………………………………………………. 5
2.1 Молекулярно-клеточные механизмы развития ВИЧ инфекции……. 11
2.2 Роль генетических факторов в патогенезе ВИЧ-инфекции…………..12
2.3 Роль лимфоидных органов в патогенезе ВИЧ-инфекции ..…………..12
2.4 Патогенетические этапы развития ВИЧ-инфекции…………………. 13
Список использованной литературы…………………………………………..16
Введение
ВИЧ продолжает охватывать территорию стран и наносить урон здоровью людей и экономике государств, несмотря на предпринимаемые меры по его устранению. Важность пандемии ВИЧ в современном мире, которая привела к серьезному социально-экономическому кризису во многих странах, сегодня ни у кого не вызывает сомнений. Многие международные лидеры, включая бывших президентов Билла Клинтона и Нельсона Манделу, постоянно призывают к консолидации международных усилий на борьбу с пандемией ВИЧ. (8).
По данным официальной статистики, основанной на регулярных исследованиях, количество ВИЧ-инфицированных в Республике Казахстан на 1 января 2015 года составило 20597 человек. (6).
Цель моей самостоятельной работы – рассмотрение вопросов этиологии и патогенеза, а также особенностей ВИЧ и СПИДа.
Глава I. Общие понятия о ВИЧ-инфекции и СПИДе
ВИЧ (вирус иммунодефицита человека) — это мельчайший вирус, вызывающий ВИЧ-инфекцию. Проникновение вируса (ВИЧ) в организм человека вызывает ослабление и разрушение иммунной системы, которая обеспечивает защиту организма человека от заболеваний, идентифицируя и уничтожая опухолевые клетки и патогены.
ВИЧ, попадая в организм человека, поражает клетки иммунной системы, в результате её работа угнетается и развивается СПИД — синдром приобретённого иммунного дефицита. Организм больного теряет возможность защищаться от инфекций и опухолей, возникают вторичные оппортунистические заболевания, которые не характерны для людей с нормальным иммунным статусом.
Вирус иммунодефицита человека относится к семейству ретровирусов. Вирусная частица представляет собой ядро, окружённое оболочкой. Ядро содержит РНК и ферменты – обратную транскриптазу (ревертазу), интегразу, протеазу. При попадании ВИЧ в клетку, РНК под воздействием ревертазы превращается в ДНК, которая встраивается в ДНК клетки-хозяина, продуцируя новые вирусные частицы – копии РНК вируса, оставаясь в клетке пожизненно. Ядро окружено оболочкой, в составе которой имеется белок – гликопротеид gp120, обуславливающий прикрепление вируса к клеткам организма человека, имеющий рецептор – белок CD4.
Известны 2 типа вируса иммунодефицита - человека, имеющие некоторые антигенные различия – ВИЧ-1 и ВИЧ-2. ВИЧ-2 встречается преимущественно в Западной Африке.
ВИЧ характеризуется высокой изменчивостью, в организме человека по мере прогрессирования инфекции происходит эволюция вируса от менее вирулентного к более вирулентному варианту.(8)
Имеются исследования, что движущей силой эпидемии ВИЧ-инфекции в Центральноазиатском регионе являются потребители инъекционных наркотиков, и эпидемия становится трудно управляемой, как это уже случилось в Российской Федерации, Беларуси, Украине, Молдове. Высокий уровень инфекций, передаваемых половым путем (ИППП) еще один потенциальный путь масштабного распространения ВИЧ-инфекции. По-прежнему более уязвимой и подверженной заражению ВИЧ-инфекцией и ИППП, остается категория молодых людей. (2)
Выявление отличительных свойств эпидемиологического процесса ВИЧ-инфекции в городе Астане является концептуально важным. Астана в сравнении с другими городами страны обладает рядом особенностей, которые влияют на многие социально-экономические показатели, в том числе и распространение ВИЧ-инфекции. Кроме того, информация требуется для определения стратегии противодействия эпидемии ВИЧ-инфекции и оценки эффективности профилактических вмешательств.
Население Астаны — одно из самых молодых в Казахстане, что девает столицу более уязвимой к распространению ВИЧ-инфекции. Средний возраст астанчан 30 лет. За последние 20 лет в структуре населения столицы произошли заметные изменения по полу и возрасту. Возросла доля мужчин, в общей численности населения наблюдается снижение доли детей в возрасте 0-14 лет и возрастного контингента 60 лет и старше (с 9,0% до 6,2%). Соответственно отмечается заметный I рост удельного веса населения в возрасте 15-59 лет (с 66,2% до 72,6%). Такая возрастная структура в столице сложилась, в основном, из-за миграционных процессов. Рост населения в трудоспособном возрасте (15-59 лет) произошел за счет граждан, прибывших в столицу с целью трудоустройства и получения образования.
Приведенные данные свидетельствуют, что столица имеет большой потенциал для дальнейшего развития естественного прироста населения, причинами которого являются ее экономические возможности — динамичный рынок труда и жилья, перспективы профессионального роста, высокая заработная плата. Соответственно с ростом численности населения возрастает вероятность дальнейшего распространения ВИЧ-инфекции. Более того, ежегодно до 10% заболеваемости обусловлено внутренними мигрантами.
Для характеристики частоты возникновения ВИЧ-инфекции и сопутствующих заболеваний и негативных последствий, с ними связанных, обычно используются такие основные эпидемиологические показатели, как заболеваемость, распространенность, пораженность, смертность и летальность. (4)
В течение эпидемии произошел значительный рост доли инфицированных при половых контактах, в 2007 году она почти достигла доли инфицировавшихся при парентеральных контактах (введение наркотических препаратов внутривенно) - 47,6% и 50,8% соответственно. Среди всех возможных способов передачи ВИЧ половой контакт остается на первом месте. Высокий риск заражения передачи ВИЧ при половом контакте обусловлен прямым контактом с выделениями (биологическими жидкостями), содержащими вирус. Наиболее высокие концентрации вирусных частиц обнаруживаются в крови и семенной жидкости. Таким образом, анализ причин заражения показал, что в последние 5 лет в городе отмечаются примерно равные относительные показатели основных путей инфицирования при значительном росте абсолютного числа инфицированных ВИЧ (как половым, так и парентеральным путями).
Изменение путей заражения отразилось, в первую очередь, на структуре ВИЧ-инфицированных по полу. Преобладавший в начале эпидемии парентеральный путь заражения поддерживался за счет мужчин — потребителей инъекционных наркотиков. Начиная с 2001 года, в эпидемию все больше стали вовлекаться женщины, нередко являющиеся половыми партнершами внутривенных наркопотребителей. С 2008 года доля женщин составляет до 40-48% от числа всех ВИЧ-инфицированных. (5).
Социальная контрастность населения столицы также накладывает свой отпечаток на заболеваемость. Так, в период с 2007-2014 годы доля неработающих варьировала с 41 до 54%, осужденные и следственно-арестованные лица в среднем составляли до 12% всех инфицированных.
Непрерывный миграционный поток как внутренних, так и внешних мигрантов является одним из факторов, влияющих на темпы распространения ВИЧ-инфекции. Ежегодно 10% всех случаев регистрируется среди иностранных граждан, 25- 27% случаев составляют жителем других регионов страны, прибывшие в поисках работы в столицу. (6)
Глава II. Патогенез
Отличительным признаком ВИЧ-инфекции является глубокий иммунодефицит в результате прогрессирующей количественной и качественной недостаточности Т-лимфоцитов. Снижение количества Т-лимфоцитов до определенного уровня ведет к развитию различных инфекционных и опухолевых процессов. Следует отметить, что некоторые проявления СПИДа невозможно объяснить лишь иммуносупрессивным эффектом ВИЧ. Патогенетические механизмы ВИЧ-инфекции являются многофакторными и многофазными, поэтому следует рассмотреть особенности течения ВИЧ-инфекции более подробно.(8)
2.1 Молекулярно-клеточные механизмы развития ВИЧ инфекции
- Роль клеточной активации в патогенезе ВИЧ-инфекции
Активация иммунной системы является важным компонентом адекватного иммунного ответа на внешний антиген. В физиологических условиях, после того как иммунная система прореагирует на антигенный стимул, она возвращается в состояние относительно спокойствия. Однако во время ВИЧ-инфекции иммунная система находится в состоянии постоянной активации в связи с наличием хронической инфекции. Такое состояние характеризуется гиперстимуляцией В-лимфоцитов, спонтанной пролиферацией лимфоцитов, экспрессией маркеров активации на поверхности CD4+ и CD8+ Т-лимфоцитов, гиперплазией лимфоузлов, усиленной секрецией провоспалительных цитокинов, повышенным уровнем неоптерина , β2-микроглобулина, кислотно-чувствительного интерферона, интерлейкина-2, а также аутоиммунными процессами.
- Роль апоптоза и суперантигенов в патогенезе ВИЧ-инфекции
Существует гипотеза, согласно которой апоптоз является одним из патогенетических механизмов ВИЧ-инфекции в связи с тем, что последовательные активационные стимулы способны уничтожать CD4+ Т-лимфоциты путем апоптоза. Степень апоптоза значительно увеличивается при ВИЧ-инфекции и представляет собой неспецифический механизм, отражающий ненормальный процесс постоянной иммунной активации.
Суперантигены способны связываться и активировать целые субпопуляции Т-лимфоцитов, и это ведет к массированной активации Т-клеток, которые, в результате, не способны реагировать на другие стимулирующие сигналы, и исключаются из процесса иммунного ответа.
Аутоиммунные процессы при ВИЧ-инфекции характеризуются наличием антител к лимфоцитам и нейтрофилам, играя роль в развитии тромброцитопении у больных с ВИЧ-инфекицией. (8).
2.2 Роль генетических факторов в патогенезе ВИЧ-инфекции
В ряде исследований была показана роль генов Главного Комплекса Гистосовместимости, а также ряда других генетических факторов в патогенезе ВИЧ-инфекции. В частности, предполагается определенная связь генетических факторов с клиническими проявлениями заболевания, а также с предрасположенностью к более длительному выживанию или, наоборот, - к более агрессивному течению. Эти генетически механизмы могут иметь отношение к экспрессии определенных эпитопов Т-лимфоцитов, обеспечивающих их более выраженные цитотоксические свойства и, следовательно, более эффективную иммунную защиту от ВИЧ-инфекции. Кроме того, возможна роль экспрессии генов, обеспечивающих более быстрое распознавание инфицированных клеток. (8)
2.3 Роль лимфоидных органов в патогенезе ВИЧ-инфекции
Лимфоузлы являются основными анатомическими органами, где происходит развитие ВИЧ-инфекции. Лимфаденопатия является отражением клеточной активации и иммунного ответа на вирус, который происходит в лимфоидной ткани и проявляется гиперплазией фолликул и зародышевых центров лимфоидной ткани.
По мере прогрессирования болезни структура зародышевых центров начинает разрушаться, а функция задержания вируса становится все более ограниченной. На этой стадии происходит усиление плазменной вирусемии, увеличение количества инфицированных лимфоцитов в периферической крови.
2.4 Патогенетические этапы развития ВИЧ-инфекции
Было установлено, что первыми клеточными мишенями ВИЧ являются клетки Лангенгарса и дентритные клетки, которые затем передают вирус лимфоцитам. После контакта вируса с CD4+ Т-лимфоцитами происходит интенсивная репликация вируса и развитие вирусемии, ведущей к распространению вируса по региональным лимфоузлам в головной мозг и другие ткани. После попадания ВИЧ в организм инфицированные клетки могут обнаруживаться в лимфоузлах в течение 2 дней, в плазме на 5 день.
Уникальность ВИЧ-инфекции заключается в том, что, несмотря на интенсивный клеточный и гуморальный иммунный ответ, вирус уничтожается не полностью, а продолжает ограниченную репликацию, которая может протекать в течение 10 лет до развития клинических симптомов СПИДа.
ВИЧ использует несколько механизмов, позволяющих избежать его уничтожения иммунной системой. В частности вирус обладает способностью мутировать. Другой важный механизм, связан с тем, что в период первичной инфекции ВИЧ и в процессе ее перехода в хроническую форму происходит парадоксальное разделение активированных цитолитических Т-лимфоцитов от их предшественников. Причем это происходит не в лимфоидной ткани, где происходит репликация вируса, а в периферической крови.
- Иммунопатологические процессы во время латентной инфекции
У ВИЧ-инфицированных происходит неуклонное снижение уровня CD4+ Т-лимфоцитов. В течение длительного периода времени прогрессирующее снижение концентрации CD4+ Т-лимфоцитов не сопровождается какими-либо симптомами. Понимание этого привело к выделению фазы болезни, которая характеризуется как клиническая латентность, которая, однако, не является эквивалентной понятию патогенетической латентности, поскольку инфекция продолжает прогрессировать, несмотря на отсутствие клинических симптомов.
После различных периодов времени, обычно исчисляемых годами, концентрация CD4+ Т-лимфоцитов в крови падает до критического уровня (менее 200 клеток на 1мл крови). В этот момент ВИЧ-инфицированные становятся высоко подверженными оппортунистическим инфекциям.
СПИД - финал инфекции ВИЧ - проявляется летальными осложнениями в виде тяжелого течения оппортунистических инфекций и различных новообразований. Основным проявлением терминальной стадии ВИЧ-инфекции является СПИД-кахексия. Однако основной причиной смерти больных в терминальной стадии ВИЧ-инфекции является не вирус, а присоединившиеся СПИД-ассоциируемые заболевания. (5).
Заключение
В силу влияния социально-экономических факторов, г. Астана является высоко восприимчивым городом к распространению ВИЧ-инфекции. Вместе с тем, наличие эффективной системы финансирования профилактических мероприятий способствовали результативному противодействию эпидемии в ее начальной стадии.
Больные с тяжестью воспринимают факт инфицирования – это непременно сказывается не только на их здоровье, но и на социально-бытовых условиях жизни, карьере и личной жизни, мироощущении. Отсутствие признания и невостребованность – все это оставляет след. В связи с этим, актуальность информирования населения о данном заболевании играет довольно весомую роль, ведь, как известно, при определенных условиях можно надолго продлить жизнь.
Исходя из изученной мною клинической и научно-популярной литературы, могу с уверенностью сказать, что СПИД, к большому сожалению, остается неизлечимой болезнью. Отсутствие эффективных методов лечения и борьбы с ВИЧ-инфекцией на сегодняшний день говорит мировому, и, конкретно научному сообществу, о большой необходимости продолжать исследования в этой области, что оно и делает. А значит, у человечества есть будущее.
Список использованной литературы доступен в полной версии работы
Читайте также:

