Маркеры повреждения миокарда реферат
Обновлено: 05.07.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Инфаркт миокарда: причины появления, симптомы, диагностика и способы лечения.
Определение
Инфаркт миокарда (ИМ) – это омертвление участка сердечной мышцы вследствие недостаточного ее кровоснабжения с развитием характерной клинической картины.
Причины появления инфаркта миокарда
Сердце – полый мышечный орган, имеющий форму конуса. Стенки сердца состоят из трех слоев. Внутренний слой – эндокард – выстилает полости сердца изнутри, и его выросты образуют клапаны сердца. Средний слой – миокард – состоит из сердечной мышечной ткани. Наружный слой – перикард. Сердце человека имеет четыре камеры: два предсердия и два желудочка. В правое предсердие поступает кровь из тканей самого сердца и всех частей тела (по верхней и нижней полым венам). В левое предсердие впадают четыре легочные вены, несущие артериальную кровь из легких. Из правого желудочка выходит легочный ствол, по которому венозная кровь поступает в легкие. Из левого желудочка выходит аорта, несущая артериальную кровь в сосуды большого круга кровообращения. Кислород к миокарду сердца доставляется по коронарным артериям.
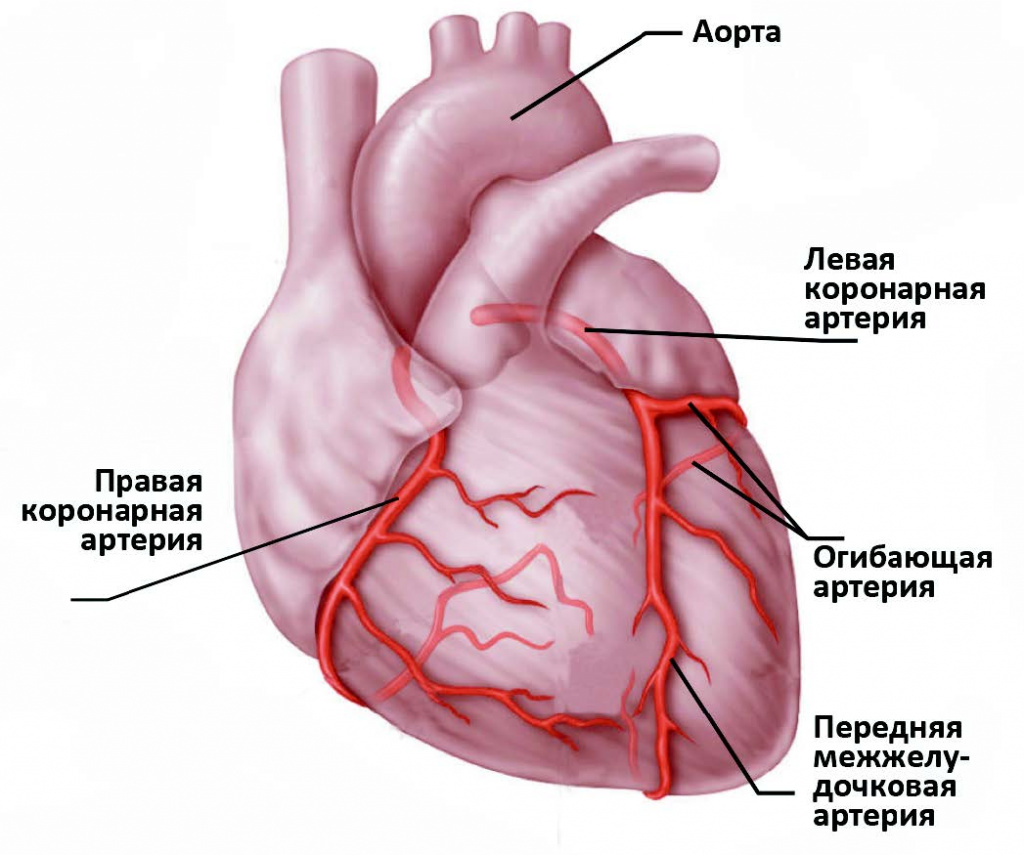
Сердце очень чувствительно к недостатку кровоснабжения (дефициту кислорода). В случае закупорки крупной коронарной артерии и при отсутствии эффективного альтернативного кровообращения по другим сосудам уже через 30 минут в пораженном участке начинается гибель кардиомиоцитов (мышечных клеток сердца).
Нарушение кровообращения вследствие атеросклеротического поражения коронарных артерий в 97-98% случаев имеет основное значение в возникновении инфаркта миокарда.
Атеросклерозом может поражаться как одна коронарная артерия, так и все три. Степень и протяженность сужения артерии могут быть различными. При повышении артериального давления склерозированный внутренний слой сосуда (эндотелий) легко повреждается, кровь проникает внутрь бляшки, активируется процесс свертывания крови и формируется тромб, который может частично или полностью закупорить сосуд.
Где может формироваться тромб:
- на месте разрыва уязвимой (нестабильной) атеросклеротической бляшки;
- на дефекте (эрозии) эндотелия коронарной артерии, не обязательно локализованном на поверхности атеросклеротической бляшки;
- в месте гемодинамически незначимого сужения коронарной артерии.
Развивающийся некроз миокарда может быть различных размеров, а некроз, проходящий через все слои сердца (трансмуральный) может стать причиной разрыва миокарда.
Образование очагов некроза в миокарде сопровождается изменением размера, формы и толщины стенки сердца, а сохранившийся миокард испытывает повышенную нагрузку и подвергается гипертрофии с увеличением объема и массы.
Такие сопутствующие состояния как: анемия, воспаление, инфекция, лихорадка, метаболические или эндокринные расстройства (в частности, гипертиреоз) могут спровоцировать или утяжелить ишемию миокарда.
К факторам риска развития инфаркта миокарда относятся:
- гиперлипидемия (нарушение нормального соотношения липидов крови);
- курение,
- сахарный диабет,
- артериальная гипертензия,
- абдоминальное ожирение,
- психосоциальные причины (стресс, депрессия и т.д.),
- низкая физическая активность,
- несбалансированное питание и потребление алкоголя.
Классификация инфаркта миокарда
I. Острый инфаркт миокарда.
- Острый трансмуральный инфаркт передней стенки миокарда.
- Острый трансмуральный инфаркт нижней стенки миокарда.
- Острый трансмуральный инфаркт миокарда других уточненных локализаций.
- Острый трансмуральный инфаркт миокарда неуточненной локализации.
- Острый инфаркт миокарда неуточненный.
- Повторный инфаркт передней стенки миокарда.
- Повторный инфаркт нижней стенки миокарда.
- Повторный инфаркт миокарда другой уточненной локализации.
- Повторный инфаркт миокарда неуточненной локализации.
- Гемоперикард.
- Дефект межпредсердной перегородки.
- Дефект межжелудочковой перегородки.
- Разрыв сердечной стенки без гемоперикарда.
- Разрыв сухожильной хорды.
- Разрыв сосочковой мышцы.
- Тромбоз предсердия, ушка предсердия и желудочка сердца.
- Другие текущие осложнения острого инфаркта миокарда.
- Коронарный тромбоз, не приводящий к инфаркту миокарда.
- Синдром Дресслера - постинфарктный склероз.
- Другие формы острой ишемической болезни сердца.
- Острая ишемическая болезнь сердца неуточненная.
Симптомы инфаркта миокарда
При инфаркте миокарда в результате нарушения кровообращения в пораженном участке сердца накапливаются продукты обмена, которые раздражают рецепторы миокарда и коронарных сосудов, что проявляется острой болью. Болевой приступ приводит к выбросу адреналина и норадреналина корой надпочечников.
Боль при типичном течении инфаркта миокарда является основным его признаком. Она возникает за грудиной, иногда может отдавать в левую руку, левое плечо, горло, нижнюю челюсть, в подложечную область.
По интенсивности и длительности такая боль в значительной степени превосходит обычный приступ стенокардии. Боль не снимается приемом нитроглицерина. Длительность болевого синдрома может быть различной - от 1 часа до нескольких суток. Иногда инфаркт миокарда сопровождается резкой слабостью, головокружением, головной болью, рвотой, потерей сознания. Больной выглядит бледным, губы синеют, наблюдается потливость.
В первые сутки развития инфаркта миокарда может регистрироваться тахикардия (учащенное сердцебиение), нарушение ритма, повышение температуры до 37-38℃.
Выделяют следующие клинические варианты:
- астматический - протекает как приступ бронхиальной астмы (присутствуют одышка, затрудненное дыхание, чувство нехватки воздуха);
- гастралгический – характеризуется болями в области желудка с распространением в загрудинное пространство, может быть отрыжка, икота, тошнота, многократная рвота, вздутие живота;
- аритмический – возникают нарушения ритма сердца, угрожающие жизни;
- церебральная – характеризуется нарушением мозгового кровообращения (наблюдаются тошнота, головокружение, нарушение сознания с развитием обморока);
- бессимптомный – инфаркт миокарда без типичного болевого приступа. В связи с несоблюдением постельного режима и отсутствием должного лечения протекает неблагоприятно.
Существуют четкие критерии диагностики инфаркта миокарда:
- клиническая картина инфаркта миокарда;
- картина инфаркта миокарда по данным ЭКГ;
- наличие новых участков миокарда со сниженным кровообращением или нарушение сократимости миокарда по данным инструментальных исследований;
- выявление тромбоза коронарных артерий по данным ангиографии.
-
определение уровня биохимических маркеров повреждения кардиомиоцитов в крови;
Высокочувствительное исследование тропонина-I применяется в современных алгоритмах диагностики острого инфаркта миокарда, а также повреждений миокарда в широком спектре иных клинических обстоятельств, таких как мониторинг состояния пациентов в критических состояниях, оценки периоперационного риска, прогноз кардиорисков у пациентов с сердечно-сосудистыми заболеваниями, контроль химиотерапии. Тест-системы вч TnI ARCHITECT (Abbott) одобрены также для оценки кардиорисков у условно-здоровых лиц при профилактическим скрининге
Лабораторные методы диагностики инфаркта миокарда. Ферменты инфаркта миокарда.
Помимо клинических данных и ЭКГ, в диагностике инфаркта миокарда существенное значение имеет резорбционно-некротический синдром — неспецифическая реакция миокарда, возникающая вследствие асептического некроза, всасывания продуктов некроза и эндогенной интоксикации. Его критерии: лихорадка, гиперферментемия (ферменты выходят из погибших миоцитов при разрушении их мембран) и изменения общего анализа крови. Верификация инфаркта миокарда базируется на существенном росте уровня кардиоспецифических ферментов в плазме. Весьма важны сроки определения уровня ферментов у больного ИМ.
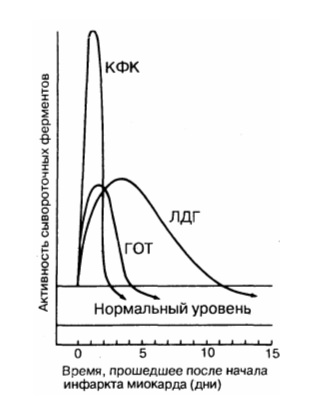
Динамика сывороточных ферментов после типичного инфаркта миокарда.
КФК - креатинфосфокиназа; ЛДГ - лактатдегидрогеназа; ГОТ - глутаматрксалоацетаттрансаминаза.
• изофермент МВ-КФК более специфичен (в высоких концентрациях отмечен только в сердце, но в небольших концентрациях содержится в скелетных мышцах). Уровень менее 10 мкг/л указывает на мелкоочаговый ИМ, а более 10 мкг/л — на крупноочаговый. Чтобы исключить ИМ, МВ-КФК регистрируют каждые 8 ч (нужны минимум 3 отрицательных результата). Оценка МВ-КФК весьма полезна, когда имеется сопутствующее поражение мышц или мозга (в них есть КФК, но нет МВ-КФК);
• суммарная КФК (норма - 20-80 усл. ед., или до 1,2 ммоль/л, в СИ) повышается через 4—6 ч (пик через 1—2 суток), а нормализуется на 4-й день. КФК содержится не только в сердце, но и в скелете, мышцах, мозге, потому рост ее может быть обусловлен травмами или болезнями мышц (полимиозит, миопатия); катетеризацией сердца; ИЭ и миокардитом (при которых интервал ST может повышаться во многих отведениях); ЭИТ; длительной иммобилизацией; шоком или алкогольной интоксикацией. Необходимо определять КФК в динамике (3-4 раза). Уровень КФК ее возрастает в ходе первых, суток, сохраняется стабильным в течение 3—4 суток и снижается к 6-7-м суткам. Пиковый уровень КФК (и МВ-КФК) на 2-е сутки после ИМ в большей мере, чем другие сывороточные маркеры, указывает на размер некроза.
В целом, исследование биохимических специфических маркеров некроза миокарда весьма важно (особенно, если данные ЭКГ позволяют сомневаться в диагнозе инфаркта миокарда). На основе их величин выделяют ОКС с некрозом (ИМ) и без некроза (НСт). Диагностика кардиоспецифических сывороточных ферментов (находившихся в миокардиоцитах и при их разрушении оказавшихся в кровяном русле) имеет большое значение для верификации ИМ без Q.
Biochemical Markers of Myocardial Necrosis. Part 1. General characterization of biomarkers. Their use for diagnosis of myocardial infarction: review of current guidelines
Лаборатория клинической кардиологии и Центр атеросклероза НИИ физико-химической медицины Минздрава Российской Федерации, Москва
119828 Москва, Малая Пироговская, la (Institute Physical-Chemical Medicine, Laboratory of Clinical Cardiology, Malaya Pirogovskaya, la, 119828 Moscow, Russia).
Ежедневно кардиологи и врачи приемного отделения оценивают состояние больных с болью в грудной клетке, выделяя среди них пациентов с острым коронарным синдромом (ОКС), причиной которого наиболее часто является остро возникший тромбоз в коронарных артериях. Диагностика базируется на выяснении жалоб, данных анамнеза и интерпретации ЭКГ покоя в 12 отведениях. Только 1/3 больных с ОКС описывают боль как типичную: локализованную за грудиной, имеющую характер жжения или сдавления [1, 2]. В остальных случаях больные сообщают о дискомфорте, тяжести в груди, сильной слабости, ноющей боли слева от грудины. Иногда у ряда пациентов с ОКС, особенно часто у больных сахарным диабетом, женщин, молодых пациентов (25—40 лет) и стариков (старше 75 лет), отсутствует ощущение боли или боль носит нетипичный характер [З]. Кроме того, согласно результатам крупных эпидемиологических исследований, около 50% пациентов с подозрением на ОКС в момент госпитализации не имеют диагностически значимых изменений ЭКГ [4]. Это больные со "старой" полной блокадой левой ножки пучка Гиса, с перенесенным ранее крупноочаговым инфарктом миокарда (ИМ), аневризмой левого желудочка (при отсутствии предшествующих ЭКГ для сравнения), больные с изменениями сегмента ST, не достигающими достаточной для постановки диагноза степени. В случаях, когда диагностика затруднена в связи с перечисленными выше обстоятельствами, существенную помощь оказывает определение ъ крови маркеров некроза миокарда [5, б].
Выявление повышенного уровня маркеров некроза миокарда помогает среди больных с ОКС без подъема сегмента 5Т выделить группу больных с максимальным риском неблагоприятных исходов (ИМ или смерть), максимально нуждающихся в современном антитромботическом лечении, реваскуляризации миокарда и тщательном наблюдении [3, 6—8].
II. Краткая характеристика биохимических маркеров некроза миокарда
1. Современные требования к маркеру некроза миокарда
Идеальный биохимический маркер должен обладать наивысшей специфичностью и чувствительностью в отношении некроза миокарда, в течение короткого времени после начала симптомов ИМ достигать в крови диагностически значимого уровня, этот уровень должен сохраняться в течение многих дней. В настоящее время маркера, полностью отвечающего всем этим требованиям, не существует [б], поэтому для диагностики ИМ рекомендуется параллельно использовать два маркера — "ранний" и "поздний". Содержание "раннего" маркера при ИМ диагностически значимо повышается в крови в первые часы заболевания, "поздний" —достигает диагностически значимого уровня только через 6—9 ч, но обладает высокой специфичностью в отношении некроза миокарда [6, 9]. Кривые, иллюстрирующие изменение содержания в крови больных ИМ большинства маркеров некроза миокарда, представлены на рисунке.
Время с момента начала симптомов ИМ, ч
Рисунок, Кривые "концентрация — время" для большинства известных биохимических маркеров некроза миокарда (F. Hartmann и соавт., 1998).
1. Ранние маркеры некроза миокарда
Миоглобин — дыхательный пигмент, широко представленный в мышечной ткани человека [11]. Молекулярная масса его составляет 18 кДа [10, 11]. Содержание миоглобина при ИМ повышается в сыворотке крови наиболее рано — в пределах 2 ч после возникновения симптомов. Он в неизмененном виде выводится мочой и к 24-му часу с момента начала симптомов исчезает из кровотока [11]. Существуют методики, позволяющие определить концентрацию миоглобина в крови в течение 10 мин [6]. Большое содержание миоглобина в скелетной мускулатуре и зависимость его концентрации от функции почек делают его неспецифичным в отношении некроза миокарда и ограничивают его применение для диагностики ИМ [6, 9, 12, 13]. Наиболее целесообразно применение миоглобина для суждения об успехе тромболитической терапии. У больных с успешной реканализацией артерии, кровоснабжающей зону ИМ, концентрация миоглобина в сыворотке крови нарастает уже через 60—90 мин после начала введения фибринолитика [6, 11].
МВ-КФК (сердечная форма креатинфосфокиназы — КФК)
КФК — фермент, широко представленный в мышечной ткани человека [14, 15]. Изолированное определение в крови общей КФК в .настоящее время большинством экспертов признано нецелесообразным для диагностики ИМ из-за высокого содержания этого фермента в скелетной мускулатуре и низкой специфичности в отношении некроза миокарда [15]. MB-изоформа КФК — это гетеродимер с молекулярной массой 86 кДа. Скелетные мышцы содержат мышечную форму КФК (ММ-КФК) и менее 3% сердечной формы (МВ-КФК) [16, 17]. МД-КФК при ИМ появляется в сыворотке крови через 3—4 ч после начала симптомов и достигает диагностически значимого уровня к 4—6-му часу. Повышенный ее уровень сохраняется 48—72 ч. Доля МВ-КФК среди общей КФК, превышающая 5—6%, является специфичным признаком некроза миокарда [17]. Однако хроническая почечная недостаточность, травматичные операции, гипотиреоз, некоторые онкологические заболевания, инсульты, миастении могут привести к повышенному уровню МВ-КФК в крови и гипердиагностике ИМ [13]. При использовании MB-КФК для диагностики ИМ необходимо повторно определять концентрацию этого маркера в крови [15]. Экспертами Европейского кардиологического общества (ЕКО) в настоящее время считается предпочтительным для диагностики ИМ определять массу МВ-КФК, а не активность этого фермента в крови [15].
Сердечная форма белка, связывающего жирные кислоты
В последние десятилетия внимание исследователей обращено на сердечную форму белка, связывающего жирные кислоты (сБСЖК). Впервые предложение использовать сБСЖК в качестве маркера ИМ было высказано J. Glatz и соавт. 10 лет назад [18].
сБСЖК по последовательности аминокислот идентичен БСЖК, содержащемуся в поперечнополосатой мышечной ткани скелетных мышц, однако представлен в скелетной мускулатуре в минимальном количестве [19—26]. Максимальное количество сБСЖК находится в ткани миокарда — 0,5 мг/г [26]. Единственная мышца, в которой имеется относительно большое количество сБСЖК, — это диафрагма (примерно 25% от содержания в ткани миокарда) [26]. Некоторое количество сБСЖК содержится в тканях аорты [26], и можно предположить, что содержание его повышается, в крови при расслаивающей аневризме аорты. Согласно данным Т. Borhers и соавт. [27], в цитоплазме содержится 3,18 мкг сБСЖК на 1 мг белка, в митохондриях — 0,18 мкг, а в ядре — 0,03 мкг. Так как сБСЖК в основном свободно расположен в цитоплазме клеток, в случае повреждения клеточной мембраны кардиомиоцита он быстро попадает в кровоток [28, 29]. В крови здоровых людей циркулирует небольшое количество сБСЖК. Было выявлено, что в крови у женщин уровень сБСЖК достоверно ниже, чем у мужчин (0,7 мкг/л против 1,2 мкг/л; p
Таблица 1. Биохимические маркеры некроза миокарда
- максимальная концентрация тропонина I или Т, превышающая установленный уровень (99-й персентиль эталонной контрольной группы) хотя бы в одном случае в течение 24 ч, следующих за клиническим событием;
- максимальное значение МВ-КФК (предпочтительно определение массы МB-КФК), превышающее 99-й персентиль эталонной контрольной группы при двух последовательных определениях, или однократное значение, превышающее верхнюю границу нормы в 2 раза в течение первых часов после начала клинического события. Уровень МВ-КФК. должен повышаться, а затем снижаться;уровень, остающийся без изменения, не связан с ИМ. При недоступности тропонина или МВ-КФК могут быть использованы общая КФК (в значении, в 2 раза превышающем контрольный уровень) или B-фракция КФК, но эти два последних биомаркера значительно менее пригодны, чем МД-КФК.
IV. Применение биохимических маркеров для диагностики и оценки состояния у больных с подозрением на ИМ в конкретных клинических ситуациях:
обобщение современных рекомендаций
Очевидно, что при длительной боли в грудной клетке в сочетании со стойкими диагностически значимыми подъемами сегмента SТ на ЭКГ нет необходимости ожидать результата определения маркеров некроза миокарда в крови [б]. В этом случае информации для принятия решения о лечебной тактике достаточно: скорее всего у больного имеется окклюзия крупной эпикардиальной коронарной артерии. Необходимо немедленно, если это возможно, предпринять попытку восстановления ее проходимости (тромболитическая терапия — ТЛТ или ангиопластика) [47]. Определение концентрации биохимических маркеров в этой ситуации не влияет на лечебную тактику, однако для подтверждения диагноза ИМ необходимо повторное определение маркеров некроза миокарда [6, 9].
При ОКС с подъемами сегмента ST использование биохимических маркеров является целесообразным также для суждения об успехе ТЛТ [6, 9, 48]. С этой целью рекомендуют взять кровь для оценки уровня маркера некроза до начала ТЛТ и через 90 мин после ее начала [9, 48]. Некоторые исследователи считают необходимым дополнительное взятие крови через 120 мин после начала ТЛТ
Если же по каким-либо причинам ТЛТ не проводится, для подтверждения диагноза целесообразно повторно определить содержание маркера некроза миокарда в крови через 8—12 ч после поступления больного [6, 9].
В "дотромболитическую эру" было выполнено большое количество работ, показывающих, что уровень биохимических маркеров при крупноочаговом ИМ характеризует размеры некроза и, следовательно, связан и с фракцией выброса левого желудочка и прогнозом заболевания [49, 50,52]. Так как лечение, направленное на коронарную реперфузию, в последние годы стало обычной практикой, использование биохимических маркеров для определения размера ИМ и оценки прогноза заболевания становится сложным из-за "феномена вымывания" в случае медикаментозной, механической или спонтанной реперфузии. Высокое содержание маркера некроза миокарда в крови в этих случаях скорее свидетельствует не о размерах очага некроза, а о быстро наступившей реканализации коронарной артерии [6, 9]. В настоящее время считается нецелесообразным использовать широко распространенные маркеры для определения размера ИМ [6, 9]. Наиболее перспективным для оценки объема некроза представляется определение в крови содержания легких цепей миозина, так как на их содержание в крови мало влияет наличие реперфузии миокарда [44,46]. Однако в настоящее время еще не разработан недорогой и удобный для применения в клинической практике диагностикум [6, 14, 44].
В случае неинформативной ЭКГ у больного с подозрением на ИМ рекомендуют определять маркеры некроза (как ранние, так и поздние) при поступлении, а также через 2-4, 6-9 и 12-24 ч [6, 9]. При следовании этой схеме эксперты Национальной академии клинической биохимии США рекомендуют ориентироваться на время поступления больного, а не на время начала болевого приступа [б]. Ориентироваться на результат определения поздних маркеров следует если взятие крови осуществлялось не ранее чем через 6 ч после начала болевого приступа [6, 9, 53]. Обнаружения диагностически значимого повышения маркеров в двух последовательных анализах достаточно для диагностики ИМ. При использовании сердечньк тропонинов для постановки диагноза ИМ достаточно однократного выявления их повышения [15]. В некоторых центрах США у таких больных взятие крови для исследования концентрации маркеров некроза миокарда осуществляется в 1-е сутки каждые 3—4 ч. Эта методика позволяет с большей точностью судить о возможном расширении зоны некроза в миокарде, выявить большее количество ИМ без зубца Q, однако стоимость ее высока [6, 9]. Национальная академия клинической биохимии США рекомендует для диагностики ИМ у больных с неинформативной ЭКГ придерживаться схемы определения маркеров некроза миокарда, представленной в табл.2.
Таблица 2. Рекомендуемая частота определения содержания биомаркеров в крови для выявления некроза миокарда у больных с неинформативной ЭКГ
| Рекомендации: для диагностики ИМ с помощью ферментных и белковых маркеров в случае отсутствия диагностических изменений ЭКГ рекомендуется следующая частота определения маркеров. | ||||
| Маркер | При поступлении | 2-4 ч | 6-9 ч | 12-24 ч |
| Ранний ( 6 ч) | X | X | X | (X) |
| Примечание. (X) — указаны дополнительные определения. Allan H.W. Wu, Fred S. Apple et al. Clinical Chemistry 1999;45:7:1104—1121. | ||||
Для диагностики ИМ у больных, перенесших оперативное вмешательство, нецелесообразно использовать ни КФК, ни МB-КФК, ни миоглобин, ни фракции ЛДГ из-за их низкой специфичности [6„ 9, 15]. С этой целью необходимо применять высокоспецифичные маркеры — сердечные тропонины [6, 9, 15]. Точная биохимическая диагностика ИМ у больных, перенесших операцию на сердце, связана с большими трудностями из-за повышенного содержания сердечных тропонинов в крови у этих больных вследствие повреждения миокарда в ходе вмешательства. При вьывлении в послеоперационном периоде уровня биохимического маркера, значительно превышающего обычный для такого вмешательства ожидаемый уровень, следует думать об ИМ [15].
Для ранней диагностики ИМ (менее 6 ч после начала боли) целесообразно использовать миоглобин из-за его высокой чувствительности (91% в 1-й час после поступления) [II]. Определение содержания миоглобина с высокой точностью исключает ИМ, однако низкая специфичность этого теста требует в дальнейшем определения у больных с повышенной концентрацией миоглобина содержания более специфичного маркера ИМ (MB-КФК или сердечного тропонина) для подтверждения наличия некроза миокарда [6, 9, 11, 15].
Для поздней диагностики ИМ много лет использовалось определение в крови концентрации изофермента ЛДГ-1 [38,39]. В настоящее время из-за низкой кардиоспецифичности определение этого маркера, как было отмечено вьпле, не рекомендовано для диагностики ИМ [6, 9, 15]. Более специфично в отношении некроза миокарда определение сердечных тропонинов. Поскольку значение сердечных тропонинов может оставаться повышенным после некроза миокарда в течение 7—10 дней и более, повышенное содержание сердечных тропонинов рекомендуют отнести к последнему (наиболее недавнему) клиническому событию [15].
Выявление рецидива ИМ может представлять специфические диагностические трудности, поскольку повышение уровня тропонинов может быть длительным и в том случае время начального повреждения миокарда сложно выяснить. При подозрении на рецидив ИМ следует определять ранние маркеры некроза миокарда (миоглобин и МД-КФК) [6, 9, 15, 54].
Повышение в крови больного уровня биохимических маркеров отражает наличие повреждения миокарда, но не указывает на его механизм [15, 54]. По этой причине повышенное содержание биохимического маркера в крови при отсутствии других данных о наличии ишемии миокарда побуждает к поиску другой причины повреждения сердца, такой как, например, миокардит [15].

Внедрение в широкую медицинскую практику новых диагностических тестов практически революционизировало многие медицинские дисциплины. Для многих людей лабораторные исследования остаются невидимой стороной медицины. Тем не менее, 60–70%, а по некоторым оценкам — и 80% всех медицинских решений принимают по результатам клинико-лабораторных исследований, от установления диагноза до выбора терапии и определения прогноза. Большой прогресс в этом направлении достигнут в кардиологии, благодаря разработке достаточно простых, но вместе с этим высокочувствительных и специфичных маркеров повреждения миокарда (1-3). К ним в первую очередь надо отнести кардиотропонины (cTnT и cTnI) мозговой натрийуретический пептид (BNP и NTproBNP), а так же маркеры риска неотложных состояний в кардиологии. К последним, наряду с показателями липопротеинового обмена, можно отнести целый ряд провоспалительных и других маркеров, характеризующих нестабильность сосудистой стенки в области атеросклеротической бляшки, а так же процессы ремоделирования в миокарде. Основные представления о биохимических маркерах в кардиологии сформулированы в ряде зарубежных обзоров и монографий. Они базируются на современной теории патогенеза сердечно-сосудистых заболеваний (рис.1).

Рис.1 Патогенетические представления о прогрессировании сердечно-сосудистой патологии
В соответствии с приведенной схемой можно предложить следующую классификацию биохимических маркеров при сердечно-сосудистой патологии. А именно:
Биомаркеры дислипидемии и модификации липопротеидов
Маркеры нестабильности и повреждения атеросклеротической бляшки
Маркеры ишемии и некроза сердечной мышцы
Маркеры дисфункции миокарда
Маркеры тромбообразования и фибринолиза
Очевидно, что для неотложной кардиологии наибольшее значение имеют маркеры 2, 3, 4, 5, 6 групп. Данные по ним обобщены в нескольких обзорах, опубликованных в последние годы (1,4). На Рис.2 приведен обобщенный перечень кардиальных маркеров при диагностике острого коронарного синдрома (ОКС). Практически каждый из указанных маркеров имеет ясное патогенетическое обоснование его применения с диагностической целью. Для определения большинства из них выпускаются специальные тест системы. Однако, с практической точки зрения наиболее важным для любого потенциального биомаркера являются сведения о его диагностической эффективности, полученные в исследованиях с высоким уровнем доказательности. Если рассмотреть кардиальные биомаркеры с этой позиции, то высокая диагностическая эффективность, подтвержденная в 3-5 популяционных исследованиях (уровень доказательности А), показана только для ограниченного числа показателей. Несомненно, к ним относятся сердечные тропонины, изоформа МВ креатинкиназы, миоглобин, NTproBNP и hsCRP. Последние два маркера не являются прямыми показателями некроза, однако, они характеризуют первый – функциональное состояние миокарда, а второй – высокочувствительный маркер воспаления, сопровождающего как дестабилизацию атеросклеротической бляшки, так и повреждения миокарда (3). Внедрение всех выше перечисленных маркеров в клиническую практику достаточно сильно повлияло на привычные определения таких нозологических единиц как инфаркт миокарда (ИМ) и нестабильная стенокардия (НС).
Наряду с этим многие из традиционно использовавшихся кардиомаркеров ИМ в силу своей низкой чувствительности и специфичности уходят (по крайней мере, должны уйти) в прошлое. Это касается активности креатинкиназы, изоформ лактатдегидрогеназы, аспартаттрансаминазы, определение которых для диагностики ИМ в настоящее время не рекомендуется. Целью настоящей работы явилось обсуждение роли тропонинов, СК-МВ и миоглобина в диагностике повреждений миокарда при ишемической болезни сердца.

2. Кардиотропонины

Диагностическая ценность биомаркёров ИМ определяется соотношением главным образом 2-х характеристик - чувствительности и специфичности. М. Plebani с соавт. ( 12) в сравнительном аспекте исследовали чувствительность и специфичность миоглобина, СК, СК-МВ, Т n Т и Т nI в диагностике ОИМ спустя 3, 6 и 12 часов от развития заболевания (Таблица 1). Как видно, показатели чувствительности у тропонинов через 3 часа были примерно одинаковыми (в среднем 51-54%) и выгодно отличались от соответствующего данных как у C К (31 %), так и в меньшей степени у C К-МВ mass (46%). Наиболее высокую чувствительность к 3-му часу имел миоглобин - 69%. Спустя 6 часов от начала ИМ чувствительность Т n Т составляла 78%, Т nI - 81%, к 12 часам - 100% в обоих случаях. В то же время показатель чувствительности C К к 12 часам не превышал 88%. Специфичность среди исследованных биомаркёров была наиболее высокой у тропонинов и наиболее низкой у миоглобина. Соотношение чувствительности и специфичности у тропонинов примерно соответствовало таковому C К-МВ.
Чувствительность и специфичность биомаркёров инфаркта миокарда
На основании вышеизложенного достаточно обоснованной можно считать следующую стратегию исследования биомаркеров при ОКС. Это так называемый двойной тест с обязательным определением динамики кардиомаркеров. Целесообразным представляется неоднократное исследование миоглобина после приступа как чувствительного раннего маркера и более длительное до конца 1 суток исследование тропонинов.
Несмотря на высокую специфичность, определяемые уровни тропонинов могут обнаруживаться при ряде других заболеваний: дилатационных кардиомиопатиях, заболеваниях мышечной и центральной нервной системы, хронической почечной недостаточности, сепсисе, заболеваниях лёгких и эндокринной системы, ВИЧ-инфекции. Сообщается о повышении тропонинов среди больных с тяжелыми функциональными классами хронической сердечной недостаточности. Следует отметить, что в указанных ситуациях повышение тропонинов, как правило, существенно ниже показателей, характерных для коронарогенных некрозов. Эти факты могут быть связаны с различными причинами. Прежде всего, при любой тяжелой соматической патологии не исключена возможность некоронарогенных некрозов в миокарде. У больных хронической почечной недостаточностью одна из возможных причин повышения тропонинов может быть связана с реэкспрессией генов, синтезирующих кардиальный Т n Т в поперечно-полосатой мускулатуре (13). При этом следует обратить внимание, что у больных хронической почечной недостаточностью с обнаруживаемыми концентрациями ТnT в крови отмечается и гораздо худший прогноз. Подобная реэкспрессия кардиальных изоформ Т n Т в скелетных мышцах может иметь место и при мышечной дистрофии Дюшенна, полимиозите ( 14).
До настоящего времени нет сведений о существовании какого-либо "безопасного уровня" повышения тропонинов; напротив, есть данные, что любое, даже незначительное их повышение несёт для больного дополнительный риск. В этой связи логичной является точка зрения экспертов Европейского общества кардиологов и Американской коллегии кардиологов (1) , заключающаяся в том, что любое повышение уровней тропонинов при обострениях ИБС или при проведении интракоронарных вмешательств должно быть обозначено как "ИМ".
Какой же уровень тропонинов следует считать повышенным? Считается, что "патологическим" является любой уровень, превышающий 99 перцентиль значений, полученных для контрольной группы (норма устанавливается в каждой лаборатории). При этом достаточна даже однократная регистрация повышенного уровня тропонинов при их динамическом исследовании в течение первых 24 часов развития события, заставляющего подозревать ИМ (1) .
3. Креатинкиназа МВ
При недоступности исследований сердечных тропонинов наилучшей альтернативой является количественное определение СК-МВ, - считают эксперты Европейского общества кардиологов и Американской коллегии кардиологов (1) . При этом диагноз ОИМ правомочен при регистрации повышенного (также выше 99 перцентили значений контрольной группы) уровня изофермента как минимум в 2-х последовательных измерениях, либо однократная регистрация уровня СК-МВ, в 2 раза превышающая нормальные значения. Динамический характер изменений уровня биомаркеров обязателен при диагностике ОИМ.
При отсутствии возможности определения СК-МВ диагностическим уровнем СК считаются значения, превышающие нормальные уровни не менее, чем в 2 раза. При необходимости раннего диагноза ОИМ могут исследоваться миоглобин, изоформы СК-МВ.
Достаточно велико значение определения биомаркеров при диагностике рецидивирующего инфаркта миокарда, а так же для выявления повреждения миокарда при интракоронарных манипуляциях. При анализе данных при подозрении на рецидив инфаркта следует помнить, что вариабельность определения современных биомаркеров меньше 10%, и следовательно, о повреждении можно говорить в том случае, когда при повторном измерении произошло увеличение показателя больше чем на 20%.
Развитие ОИМ как осложнения интракоронарных манипуляций происходит в 2-х ситуациях: 1) ИМ как следствие развития интракоронарного тромба, 2) ИМ как следствие эмболии фрагментов бляшки, пристеночного тромба при осуществлении интракоронарных вмешательств. В первом случае, как правило, развивается типичная клиническая и электрокардиографическая картина ОИМ, формируется обширный ИМ. Во втором - развивается микроинфаркт, наиболее надежным методом диагностики которого являются биомаркёры.
Эксперты (6) отмечают отсутствие единой точки зрения на диагностику ОИМ, как осложнения интракоронарных вмешательств, в случаях с умеренным повышением СК-МВ (значения индекса более 1, но менее 3-х).
Комитет Европейского общества кардиологов и Американской коллегии кардиологов) рекомендуют считать правомочным диагноз ОИМ при повышении сердечных тропонинов (определение рекомендуют проводить в период 6-8 часов и через 24 часа) после интракоронарных манипуляций в 3-5 раз. В то же время в рекомендациях американских экспертов по чрезкожным коронарным вмешательствам указывается на недостаточность научной информации для рекомендаций по диагностике ИМ, как осложнения интракоронарных вмешательств, основанных только на исследовании тропонинов.
Можно заключить, что современная диагностика инфаркта миокарда должна обязательно включать определение специфических маркеров повреждения миокарда, а именно кардиотропонинов, СК-МВ и миоглобина. Наиболее информативным является определение количества кардиотропонинов в период 6-24 часа после приступа стенокардии. Результаты исследования могут быть использованы для определения рисков летального исхода, выбора оптимальной тактики ведения больных ИБС, эффективности проводимой терапии. Особо важным представляется определение кардиотропонинов в диагностике ОКС, рецидивов инфаркта миокарда, повреждений миокарда при хирургических манипуляциях на коронарных сосудах. Повышение уровня тропонинов крови является решающим для постановки диагноз инфаркт миокарда без повышения ST сегмента на ЭКГ ( NSTEMI ). Однако,
не смотря на многочисленные исследования и рекомендации по интерпретации результатов определения кардиомаркеров изучение их будет продолжаться.
Читайте также:

