Достижения современной кардиологии отечественная зарубежная реферат
Обновлено: 05.07.2024
Содержание:
1. Понятие кардиологии …………………………………………………………………………… 3
2. История кардиологии …………………………………………………………………………… 3
3.1. Учение Галена ………………………………………………………………………………… 3
3.2. Описание артерии и вен А. Везалием ……………………………………………… 4
3.3. Деятельность Уильяма Гарвея ……………………………………………………….. 5
3.4. Возникновение представлений о круговом движениикрови ………… 6
3.5. Открытие ряда образований и методов обследования …………………. 8
3.6. Кардиология - самостоятельную отрасль медицины …………………… 8
3.7. Современный этап развития кардиологии …………………………………. 9
3. Заключение ……………………………………………………………………………………….… 10
4. Список литературы …………………………………………………………………………….. 11
Понятие кардиологии
Кардиология (отгреч. καρδία — сердце и λογος — изучение) — обширный раздел медицины, занимающийся изучением сердечно-сосудистой системы человека: строения и развития сердца и сосудов, их функций, а также заболеваний, включая изучение причин их возникновения, механизмов развития, клинических проявлений, вопросов диагностики, а также разработку эффективных методов их лечения и профилактики. Кроме того, в сфереведения кардиологии лежат проблемы медицинской реабилитации лиц с поражениями сердечно-сосудистой системы. Кардиология изучает такие патологические состояния, как ишемическая болезнь сердца (ИБС), гипертоническая болезнь, врождённые пороки сердца, приобретённые пороки сердца, цереброваскулярные заболевания и другие.
История кардиологии
История кардиологии, как и история медицины в целом, насчитываетне одну тысячу лет. С древности работа сердца и сосудов была загадкой, разгадывание которой происходило постепенно, на протяжении многих веков.
Понимание значимости работы сердца для организма можно найти еще в древнеегипетском папирусе Эберса (XVII век до н.э.) : "Начало тайн врача - знание хода сердца, от которого идут сосуды ко всем членам, ибо всякий врач, всякий жрец богини Сохмет, всякийзаклинатель, касаясь головы, затылка, рук, ладони, ног, везде касается сердца: от него направлены сосуды к каждому члену. ".
Спустя 12 веков (V в. до н.э.) житель греческого острова Кос Гиппократ впервые описывает строение сердца как мышечного органа. Уже тогда у него сформировалось представление о желудочках сердца и крупных сосудах.
Учение Галена
Римский врач Гален (II в. н.э.) создал новое,революционное для своего времени учение, которое на длительное время изменило представление людей о работе сердца и сосудов. К сожалению, в трудах Галена было много неточностей, оказались и грубые ошибки. Таково, например, его описание пути крови в теле.
Центром кровеносной системы Гален считал не сердце, а печень: образующаяся в печени кровь разносится по телу, питает его и целиком импоглощается, не возвращаясь обратно; в печени же образуется следующая партия крови для поглощения телом. Эта схема была общепризнанной вплоть до XVII в., когда ее ошибочность доказал Гарвей. Таким образом, не зная кровообращения, Гален представлял себе своеобразную систему кровоснабжения организма. Считая назначением левого сердца притягивание из легких пневмы вместе с воздухом, он рассматривал растяжение - диастолу,как активное движение сердца, систолу же - как пассивное спадение сердца, то есть понимал эти процессы совершенно превратно. Неудивительно, что Гален не мог объяснить происходящие в организме процессы и приписывал их нематериальным силам, которые изначально присущи человеку.
Описание артерии и вен А. Везалием
Серьезный прорыв в развитии представлении о работе сердечно-сосудистой системы произошелв эпоху Возрождения. Возможность препарирования трупов позволила Леонардо да Винчи создать множество анатомических иллюстраций, на которых среди прочего было достаточно точно отображена структура клапанов сердца. Многие ошибки Галена обнаружил и описал Андреас Везалий, создавший основные предпосылки для последующего открытия легочного кровообращения. Везалий тщательно.
Чтобы читать весь документ, зарегистрируйся.
Связанные рефераты
История болезни Кардиология
. терапии Зав.кафедрой профессор Карпов Р. С. ИСТОРИЯ БОЛЕЗНИ Куратор:студент.
34 Стр. 32 Просмотры
История болезни кардиология
. Учебная История болезни Обучающейся _______________________________.
7 Стр. 109 Просмотры
История болезни по кардиологии Ювенильный хронич
. Зав. кафедрой, профессор Преподаватель: ИСТОРИЯ БОЛЕЗНИ Ф.И.О. пациента.
История развития
. какую-либо сторону от средних показателей психического развития, т. е. не вписываются в.
история развития
Во всех учебниках по терапии написано, что характерным симптомом эмболии легочной артерии является обморок (синкопе). Однако именно этот вопрос вызывает жаркие дискуссии, по причине чего недавно был проведен анализ реестров пациентов из неотложных отделений США, Италии, Канады и Дании. Во всех центрах, принявших участие в исследовании, которое проводилось с 2000 по 2016 год, около 1,6 миллионов человек имели в анамнезе эпизод синкопального состояния, что и послужило причиной их обращения в больницу. По результатам исследования только лишь в 0,55 % случаев причиной синкопе пациента действительно являлась эмболия легочной артерии (95 % доверительный интервал (ДИ), 0,50–0,61 %).
В 2016 году в известном журнале NEJM было опубликовано исследование (PESIT), в котором также определялось количество случаев эмболии легочной артерии, симптомом которой являлось синкопальное состояние. Тогда оказалось, что по этой причине оказались госпитализированы 17 % пациентов из анализируемой группы. Авторы настоящего исследования предполагают, что такая разница может быть обусловлена различиями в методике проведения эксперимента. В рамках исследования PESIT ученые учитывали лишь госпитализированных в стационар пациентов с высоким риском развития эмболии.
По результатам исследования авторы сделали вывод, что в ходе дифференциальной диагностики заболевания, вызвавшего синкопе, в первую очередь необходимо исключить возможность неотложного состояния — эмболии легочной артерии, но при этом из-за ее низкой распространенности в данной группе пациентов ( Вирус гриппа провоцирует развитие инфаркта миокарда
Атеросклероз является воспалительным заболеванием артерий — это доказывают результаты многих клинических и экспериментальных исследований. Действительно, чаще всего отрыв атеросклеротических бляшек происходит именно после перенесенной инфекции. Ученые уже давно предполагали наличие связи между гриппозными инфекциями и возникновением острой ишемии миокарда, но лишь недавно было опубликовано соответствующее исследование — случай-контроль, в рамках которого были проанализированы данные 364 пациентов с инфарктом миокарда.
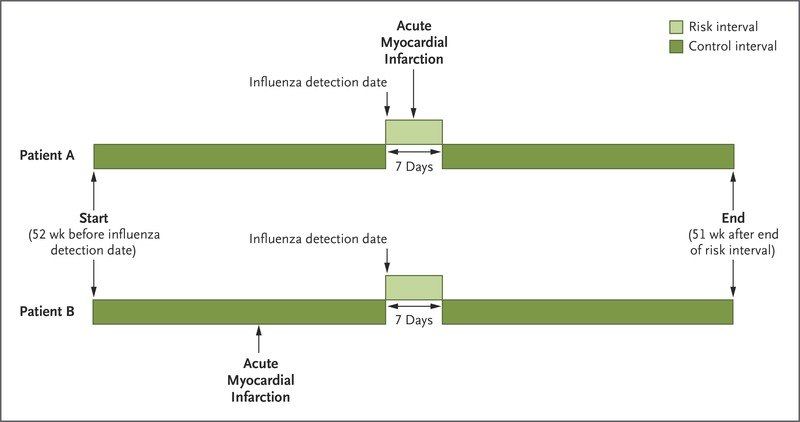
Ученых интересовало наличие лабораторно-химических маркеров присутствия вируса гриппа у этих пациентов. Все инфаркты при этом происходили в течение года после обнаружения маркеров вируса гриппа. В течение 7 дней после взятия пробы отделяемого дыхательных путей для скрининга инфекций происходило в 6 раз больше случаев инфаркта миокарда, чем в остальной период, особенно если возбудителем являлся вирус гриппа А (в 5,2 раза больше случаев инфаркта) и вирус гриппа В (в 10,1 раз больше случаев инфаркта). Это исследование особенно важно для группы пациентов, подверженных риску развития инфаркта миокарда, и еще раз подчеркивает важность вакцинации от вируса гриппа, а также необходимой госпитализации таких пациентов.
Дифференциальная диагностика острого аортального синдрома
Острый аортальный синдром (ОАС) включает в себя такие патологии, как диссекция аорты, интрамуральная гематома аорты, прободающая язва аорты и разрыв аорты. Все эти неотложные состояния чаще всего сопровождаются неспецифическими симптомами, что только усложняет их диагностику.
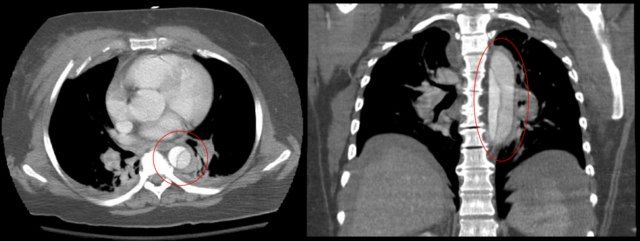
В рамках интернационального мультицентрического исследования ADvlSED ученые проанализировали данные 1850 неотложных пациентов с подозрением на острый аортальный синдром, симптомы которого были оценены по шкале ADD-RS (Aortic Dissection Detection Risk Score), включающей в себя определение D-димеров в плазме крови. В рамках этой оценки особое внимание уделялось трем ключевым признакам, каждый из которых оценивается в один балл. Таким образом, сумма баллов может быть от 0 до 3 (Rogers с соавт., Circulation, 2011 г.). Тест на наличие D-димеров считался отрицательным при их концентрации 1 и отрицательным тестом на D-димеры АОС развился у 5-ти человек. Для данной группы пациентов рекомендуется использование дополнительных методов диагностики для визуализации (КТ- или МРТ-ангиография и/или ЭхоКГ). При положительном тесте на D-димеры даже при ADD-RS ≤ 1 у 105 из таких 585 пациентов наблюдался АОС.
Таким образом ученым удалось сделать вывод о пригодности оценки по шкале ADD-RS ≤ 1 и отрицательным тестом на D-димеры в качестве диагностического инструмента для анализа состояния пациентов с низким риском развития ОАС.
Радиочастотная абляция в лечении мерцательной аритмии
Радиочастотная абляция (РЧА) оказывается эффективной в более 50 % случаев лечения мерцательной аритмии — к такому выводу пришла европейская ассоциация EHRA (European Heart Rhythm Association). В опубликованном анализе данных 3630 пациентов из Европы, Ближнего Востока и Северной Африки в 74 % случаев применение этого метода лечения не вызывало осложнений. При наблюдении за этой группой пациентов в течение от 3 до 12 месяцев после операции рецидива предсердной аритмии не происходило.
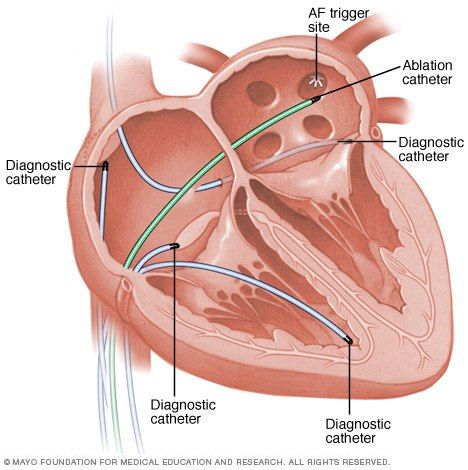
Обычно после проведения абляции пациентам, находящимся в группе риска развития ишемии головного мозга, назначают более двух антикоагулянтных препаратов. Однако в новом исследовании EHRA ученые заметили, что каждому четвертому пациенту из группы риска такая терапия не проводилась, а в трети всех случаев такая терапия проводилась, но это увеличивало риск развития кровотечений. Только в 60 % случаев пациенты после операции наблюдались у кардиолога, что обычно указано в рекомендациях. Также в течение нескольких суток после РЧА должна проводиться запись ЭКГ — это необходимо, чтобы убедиться в отсутствии рецидивов аритмии. Главный автор исследования, Dr. Elena Arbelo из испанского Национального Центра по исследованию сердечно-сосудистых заболеваний в Барселоне утверждает, что такое пренебрежение актуальными рекомендациями может приводить к серьезным последствиям (см. ниже).
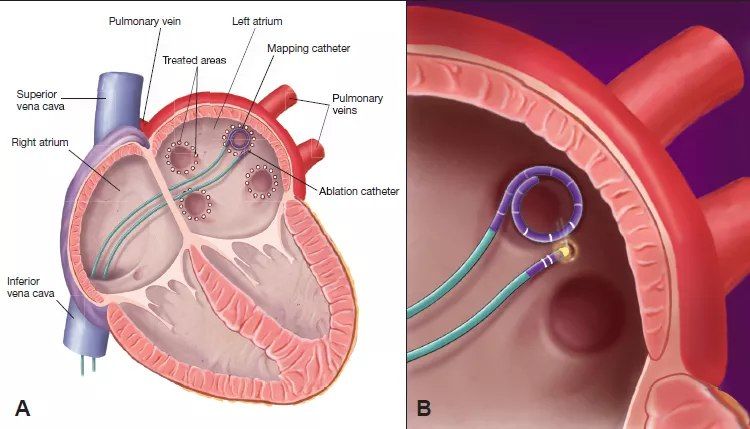
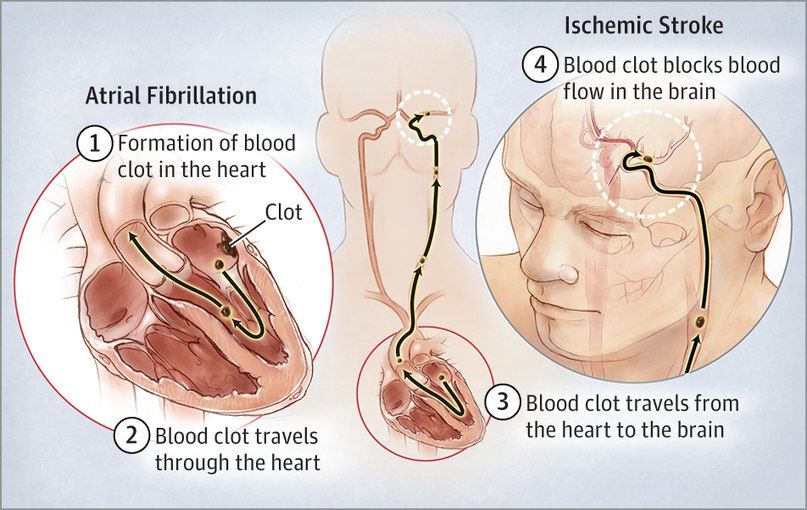
Другое исследование 2017 года, опубликованное в JAMA, напротив, показало, что в группе пациентов, подверженных риску развития инсульта, антикоагулянтные препараты назначаются все реже. В рамках данного исследования были проанализированы данные 94 474 пациентов с мерцательной аритмией, госпитализированных по причине острой ишемии головного мозга. 85 % пациентов на момент госпитализации не принимали антикоагулянтных препаратов, а в 30 % случаев им также не проводилась и антитромботическая профилактика. Только лишь 7,6 % пациентов регулярно принимали варфарин, а 8,8 % — НОАК. В 40 % случаев проводилась монотерапия ингибиторами агрегации тромбоцитов. Терапевтическая антикоагуляция была ассоциирована с меньшим риском развития инсульта средней и высокой степени тяжести и более низким уровнем смертности в результате инсульта. Наличие у пациента мерцательной аритмии повышает риск развития инсульта в 4–5 раз и является причиной 10–15 % всех ишемических инсультов.
Мерцательная аритмия, антикоагулянтная терапия и деменция
В терапии пациентов с мерцательной аритмией и высоким риском развития инсульта и системной эмболии часто применяют антикоагулянтные препараты. Самым распространенным осложнением их приема является развитие кровотечений. Проведенные в прошлом исследования показали, что у пациентов с мерцательной аритмией также высок риск развития деменции. До сих пор неясным оставался вопрос, приводит ли прием антикоагулянтов к нарушению когнитивных функций (из-за микрокровотечений в паренхиму мозговых тканей), или же, наоборот, предотвращает их (из-за снижения количества ишемических микроэмболизаций сосудов). Шведское исследование, в котором участвовало 444 106 пациентов с мерцательной аритмией, показало, что риск развития деменции снижался на 29 % при приеме антикоагулянтных препаратов с момента начала исследования, и на 48 % — при их продолжительном приеме. При этом ученым не удалось обнаружить разницу в приеме варфарина или НОАК. При этом стоит отметить, что использование варфарина оказалось ассоциировано с меньшим колебанием INR.
Ангиотензин II при шоке
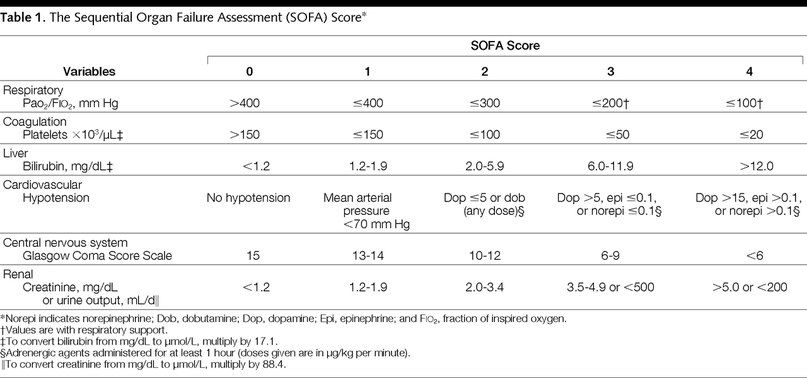
La Jolla Pharmaceutical Company в конце 2017 года анонсировала новый препарат для повышения давления при септическом и других видах шока. Согласно пресс-релизу FDA, его можно будет купить в США уже в марте 2018 года. Применяющиеся в настоящее время вазопрессорные препараты имеют множество недостатков и подвергаются постоянной критике, что дало ученым идею о необходимости разработки новых препаратов. В результате исследования ATHOS-3 была доказана эффективность ангиотензина II при шоковых состояниях. В 80,7 % случаев причиной шока являлся сепсис. В рамках данного исследования ученые провели анализ данных 321 пациента (медиана возраста — 64 года, 61 % — мужчины). Все пациенты на момент начала наблюдения находились в вазодилататорном шоке, а их состояние не улучшилось после введения классических сосудосуживающих препаратов в дозировке более чем 0,2 мкг/кг в минуту (норадреналин). В дополнение к стандартной терапии более чем половина пациентов (163 человека) получила дозу нового препарата. В первую очередь ученых интересовал уровень артериального давления спустя 3 часа после введения препарата. Повышением давления считался его подъем до 75 мм рт. ст. и выше или увеличение среднего АД на 10 мм рт. ст. Вторично ученые оценивали состояние внутренних органов по шкале SOFA (Sequential Organ Failure Assessment) в течение 48 часов после начала наблюдения.
Повышение давления в группе, получавшей ангиотензин II, наблюдалось в 69,9% случаев по сравнению с плацебо-группой, в которой давление повысилось только у 23,4% испытуемых (OШ = 7,95). Оценка по шкале SOFA также была более высокой в группе ангиотензина II (–1,75), чем в группе плацебо (–1,28).
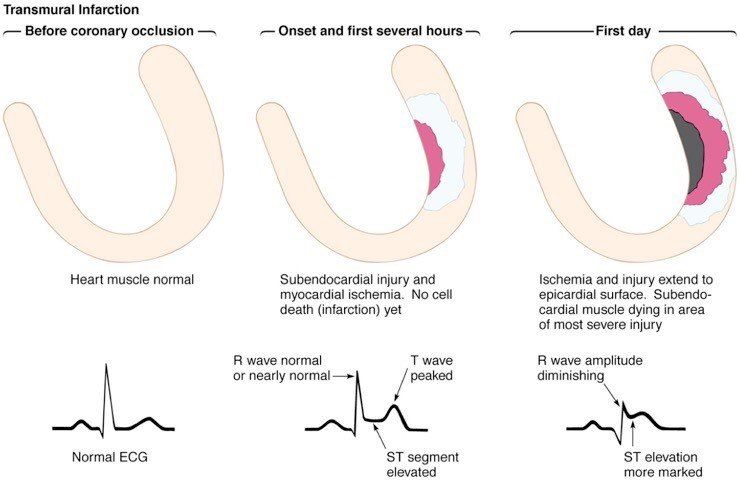
НОАК после инфаркта миокарда с подъемом сегмента ST (STEMI)
В рамках вторичной профилактики ОКС с целью предупреждения тромбоза чаще всего назначают антиагреганты и прямые оральные антикоагулянты. По результатам нового мета-анализа, эффект терапии прямыми оральными антикоагулянтами (НОАК) напрямую зависит от вида инфаркта.
Данный мета-анализ включает в себя шесть исследований препаратов апиксабан, ривароксабан и дабигатран. В общей сложности в них приняло участие почти 30 000 пациентов, поступивших в стационар с ОКС (14 580 c STEMI и 15 036 c NSTEMI), средний возраст которых составил 63 года. В целом прием двойной терапии снижал риск развития осложнений (ОШ: 0,85) по сравнению с группой, принимавшей только лишь антиагреганты. Однако такая терапия повышает риск развития кровотечений (ОШ: 3,17). Особенно этому оказались подвержены пациенты со STEMI (ОШ: 3,45), для сравнения — данные пациентов с NSTEMI (ОШ: 2,19). Однако при прогнозировании статистически значимая выгода отмечалась только для пациентов с STEMI (ОШ: 0,76), чего нельзя сказать о пациентах с NSTEMI (ОШ: 0,92; 95 % ДИ, 0,78–1,09; P = 0,36). Таким образом, данный мета-анализ заставляет задуматься о пересмотре рекомендаций по назначению терапии после инфаркта миокарда в зависимости от его типа. Двойная терапия улучшает прогноз после инфаркта миокарда с подъемом сегмента ST, но, хоть риск развития ишемических патологий и снижается, увеличивается вероятность развития кровотечений. У пациентов с NSTEMI дополнительный прием ДОАК чаще приводит к сильным кровотечениям, снижая риск развития ишемии лишь незначительно.
Послеоперационный инсульт при открытом овальном окне
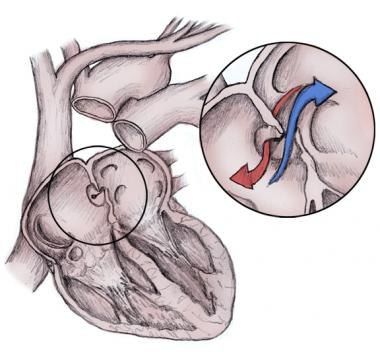
У 25 % всех людей наблюдается персистирующее овальное окно во время приема Вальсавы, через которое кровь из правого предсердия попадает в левое предсердие. Недавно опубликованное исследование показало, что перкутанное закрытие овального окна помогает избежать повторного послеоперационного инсульта вследствие эмболии. Обычно персистирующее овальное окно не приводит к гемодинамическим нарушениям. В настоящем исследовании приняли участие 150 000 пациентов, из которых у 1 % (1540 человек) наблюдалось открытое овальное окно. В этой группе риск развития инсульта в течение месяца после хирургического вмешательства был в 2,8 раза больше, чем у остальных. В этой группе пациентов наблюдалась также большая площадь инфаркта и более частое развитие неврологических дефицитов вследствие самого инсульта. Однако в исследовании ученые не учли, что только лишь часть пациентов была перед хирургическим вмешательством кардиологически обследована с помощью трансэзофагеальной ЭКГ. Возможно эта группа пациентов в целом была менее здоровой, что и привело к более тяжелому течению послеоперационного периода. Поэтому авторы рекомендуют проведение новых РКИ с целью выяснить прямую взаимосвязь между персистирующим овальным окном и риском развития пре- и послеоперационного инсульта. Эти данные могут в дальнейшем помочь в составлении рекомендаций касательно антикоагулянтной терапии в данной группе риска.
Спорт и сердечная недостаточность: никогда не поздно начать
Среди всех заболеваний ССС сердечная недостаточность (СН) занимает особое положение из-за постоянно увеличивающихся экономических затрат на ее лечение. Уже доказано, что регулярные занятия спортом снижают риск развития СН. До сих пор не было известно, имеет ли смысл начинать заниматься спортом представителям старшего поколения. В настоящем проспективном исследовании ARIC (Atherosclerosis Risk in Communities) приняло участие 11 351 пробандов без имеющихся сердечно-сосудистых заболеваний. Ученые рекомендовали участникам интенсивные занятия спортом более 75 минут в неделю или же тренировки с умеренной нагрузкой более 150 минут в неделю. С помощью регрессии Кокса ученые провели анализ активности пробандов с течением времени. Спустя 6 лет после старта эксперимента 42 % 60-летних участников все еще продолжали соблюдать врачебные рекомендации. В течение 19 лет наблюдений ученые в целом зафиксировали 1750 случаев возникновения осложнений со стороны ССС, из которых 1693 привели к госпитализации пациентов и 57 — к смерти по причине сердечной недостаточности. Среди тех, кто в течение 6 лет соблюдал рекомендации врача, риск развития сердечной недостаточности был минимален. Он также снизился и для тех, кто на момент начала эксперимента особо спортом не занимался, но все шесть лет соблюдал рекомендации. Бег в течение 30 минут 4 раза в неделю помог снизить риск развития сердечной недостаточности на 11 %. В случае усиленной нагрузки, такой как, например, езда на велосипеде в течение 30 минут 4 раза в неделю, риск снизился на 21 %. Несмотря на знание о том, что соблюдение полученных рекомендаций значительно снижает риск развития СН, лишь менее чем половина участников продолжала их придерживаться.

PCSK9-ингибиторы: новая надежда
Скоро на съезде американской коллегии кардиологов в Орландо будут представлены долгожданные результаты исследования ODYSSEY. Исходя из гипотезы о позитивном влиянии снижения ЛПНП-С в плазме крови, ученые протестировали препарат алирокумаб, являющийся моноклональным антителом к PCSK9.
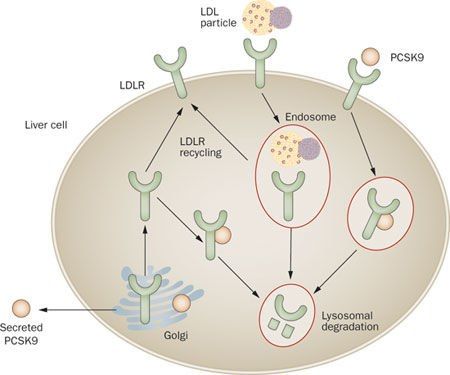
Его конкурентом в данной области считается эволокумаб, прошедший испытания в исследовании FOURIER. Результаты последнего вышли неоднозначными: количество осложнений, действительно, статистически значимо снизилось, но его применение оказалось экономически невыгодным. Оборот от продаж алирокумаба составил 195 млн. (из них 131 млн. долларов приходится на долю США), а эволокумаба — 319 млн. долларов (225 млн. долларов на долю США). В FOURIER приняли участие 27 564 пациента с различными заболеваниями ССС и концентрацией ЛПНП в плазме крови выше 70 мг/дл, уже принимающих статины. Концентрация ЛПНП-С в группе, принимавшей эволокумаб, снизилась на 60 % — с 92 до 30 мг/дл. Относительное снижение риска развития осложнений со стороны ССС по сравнению с плацебо-группой оказалось значительным и составило 15 % (абсолютное снижение — 1,5 %, с 11,3 до 9,8 %). При приеме эволокумаба ученые наблюдали снижение риска возникновения инфаркта (с 4,6 до 3,4 %) и инсульта (с 1,9 до 1,5 %). Однако ученые не смогли обнаружить разницу в смертности (общей и от сердечно-сосудистых заболеваний) между двумя группами. Кардиологическое сообщество тогда описало результаты данного исследования как сомнительные и незначительные, учитывая значительные затраты.
Методика проведения нового исследования ODYSSEY весьма похожа на FOURIER, но есть и отличия. Длительность FOURIER составила два года (количество участников — около 27 000 человек). Ученые предполагают, что такая длительность эксперимента не дала возможности сделать полноценные выводы о долгосрочном влиянии препарата. В рамках ODYSSEY ученые намерены обработать данные 18 000 пациентов, наблюдая их на протяжении уже трех лет, что дает этому исследованию преимущество. В отличие от FOURIER, в рамках ODYSSEY пациенты не принимали одинаковую дозу алирокумаба на протяжении всего времени наблюдения. Если концентрация ЛПНП-С в их крови так и не достигала отметки ниже 50 мг/дл, дозу увеличивали. Стоит отметить, что в исследовании ODYSSEY принимают участие только пациенты с высоким риском развития осложнений со стороны ССС, в то время как участники FOURIER уже проходили интенсивный курс терапии статинами.
Развитие современной кардиологии идет быстрыми темпами, постоянно появляются новые и совершенствуются уже имеющиеся способы лечения сердечно-сосудистых заболеваний. Одно из таких достижений — биоабсорбируемые внутрисосудистые эндопротезы (скаффолды), ставшие революционным решением в лечении ишемической болезни сердца. Они имеют много преимуществ по сравнению с обычными металлическими стентами.
К материалу для изготовления скаффолдов предъявляются особые требования: он должен быть механически прочным и обладать способностью к рассасыванию с образованием естественных метаболитов или инертных соединений. Оптимальными с этой точки зрения оказались полимолочная кислота и магний. Полимолочная кислота прошла много клинических испытаний на биосовместимость, ее уже давно используют в производстве протезных имплантатов и материалов для закрытия ран.
Биоабсорбируемые стенты обеспечивают временную поддержку изнутри и доставку лекарственного вещества в пораженный сосуд. Спустя 2 – 3 года после имплантации протез полностью рассасывается, а просвет артерии остается свободно проходимым. В случае необходимости повторное вмешательство на данном участке возможно уже спустя полгода после установки скаффолда. После его рассасывания сосуд восстанавливает способность реагировать на физиологические стимулы и лекарства сужением или расширением.
Преимущества биоабсорбируемых стентов:
- хорошая доставляемость к месту сужения;
- сохранная моторика сосуда;
- отсутствие явлений хронического воспаления вокруг стента;
- отсутствие рубцовых изменений в сосудистой стенке;
- контролируемое высвобождение антипролиферативного препарата;
- минимальная вероятность спадения в остром периоде и повторного стенозирования артерии в дальнейшем.
Применение скаффолдов позволило расширить спектр стентируемых сосудов до диаметра 2 мм. Так как биоабсорбируемые стенты имеют меньшую механическую прочность по сравнению с металлическими, перед их установкой необходима специальная подготовка сосуда серией предилятаций. Имплантация скаффолда также имеет особенности: ее выполняют, медленно повышая давление в системе доставки до полного раскрытия стента, затем давление поддерживают в течение 30 секунд и так же медленно снижают.
Одно из перспективных направлений в области стентирования — разработка имплантируемых чип-модулей (Smart-стенты) с возможностью дистанционного контроля скорости кровотока, давления и некоторых биохимических параметров (уровня глюкозы и некоторых пептидов). Smart-стент будет предупреждать возникновение осложнений во время его установки. Это изобретение позволит заменить участок поражения электронным чипом с возможностью считывания гемодинамических параметров на материнском устройстве по беспроводной сети.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Звук, ритм, частота, функции – эти и многие другие показатели работы сердца необходимо регулярно измерять, чтобы поддерживать его здоровье максимально долгое время. Технологическая и научная революция позволила добавить к традиционным профилактическим инструментам целый ряд цифровых решений, направленных на предотвращение сердечных приступов и снижение сердечно-сосудистых рисков. Будущее за этими решениями, а также за мелкими датчиками, цифровыми двойниками и искусственным интеллектом. Посмотрим, как может выглядеть будущее кардиологии.
Фитнес-трекеры, датчики здоровья и другие устройства способны не только измерять физическую активность, давать индивидуальные рекомендации по питанию, помогать в соблюдении режима приема лекарств или оптимизировать сон, но и контролировать различные параметры работы сердца. В течение следующих нескольких лет все это должно позволить кардиологии стать более ориентированной на прогнозирование и профилактику, чем на лечение уже случившихся заболеваний. Итак, что мы вправе ожидать в самом ближайшем будущем?
Как измерить тоны сердца?
Начнем с диагностики и самого распространенного обследования, проводимого каждым врачом общей практики: прослушивание тонов сердца с помощью стетоскопа. Его обновленная версия, так называемый цифровой стетоскоп, помогает этому заслуженному устройству соответствовать требованиям 21-го века.
Австралийская компания M3DICINE пошла еще дальше: вместе с учеными из Массачусетского технологического института (MIT), клиническими экспертами из Клиники Mэйо (Mayo Clinic), медсестрами, кардиологами и другими медицинскими работниками она разработала первую искусственную интеллектуальную стетоскоп-систему, которая может анализировать звуки сердца и легких, создавать уникальную личную биометрическую подпись, а также привязывать географическое местоположение и данные об окружающей среде к этой информации в режиме реального времени. Это дает совершенно новый взгляд на медицинские данные. В будущем врачи кардиологи могут также использовать искусственный интеллект в стетоскопах для прогнозирования потенциально опасных сердечных состояний. Кроме того, устройства могут использовать так называемые цифровые татуировки. Например, электронные татуировки, разработанные в университете штата Иллинойс в Урбана-Шампейн, регистрируют трудноуловимые звуки в теле человека, в том числе в сердце, мышцах и желудочно-кишечном тракте.
Ритм сердца и артериальное давление
В рамках второго тренда японская технологическая компания Omron представила на выставке CES 2018 умные часы Omron Heartguide. Гаджет может считывать показания, характерные для гипертонии, и оценивать риск развития инсульта во время сна. Этот функционал полностью заменяет традиционную практику измерения артериального давления, а значит может изменить и правила игры в кардиологии. Израильская компания Biobeat разрабатывает подобную систему: устройство мониторирует уровень артериального давления, вычисляет средний показатель давления, частоты пульса, насыщения крови кислородом и т.д. Судя по всему, в обозримом будущем манжеты для измерения артериального давления полностью исчезнут.
Измерение ЭКГ для мониторинга мерцательной аритмии во время мытья посуды дома?
Ваше сердце хочет выпрыгнуть из груди, словно птица, рвущаяся из клетки. Ваш пульс ускоряется, как космический корабль, желающий покинуть гравитационное поле Земли. Вы не знаете, что происходит, и боитесь того, что может случиться дальше. Все это типичные признаки мерцательной аритмии (МА). Это не только страшно, но и опасно: МА увеличивает риск инсульта, сердечной недостаточности и других сердечных осложнений.
Судя по всему, в будущем пациенты будут следить за состоянием своего сердца в любом месте, а гаджеты на основе искусственного интеллекта будут уведомлять пациентов и их врачей об отклонении от нормы. В случае выявления патологических отклонений кардиологи могут обследовать пациента – сделать 12-канальную ЭКГ в клинических условиях и провести другие диагностические тесты. Есть даже мнение, что наблюдать и лечить такие хронические заболевания, как МА или хроническая сердечная недостаточность, будут не кардиологи, а квалифицированные медсестры.
Искусственный интеллект и бляшки – как это работает вместе?
Искусственный интеллект необычайно важен для дальнейшего развития кардиологии. В течение нескольких лет все устройства для непрерывного мониторинга будут оснащены интеллектуальными алгоритмами – и новые данные для прогнозирования и лечения сердечно-сосудистых заболеваний могут прийти из совершенно неожиданных областей. Согласно исследованию, опубликованному в Nature Biomedical Engineering, сотрудники Google с помощью искусственного интеллекта предсказали факторы риска сердечно-сосудистых заболеваний, которые ранее не считались поддающимися количественной оценке, на… изображениях сетчатки глаза. Ученые смогли определить такие факторы риска, как возраст, пол, интенсивность курения, артериальное давление и серьезные неблагоприятные сердечные события – только глядя в глаза!
Гаджет Zebra на базе искусственного интеллекта включает алгоритм подсчета коронарного кальциевого индекса при выполнении КТ грудной клетки. Индекс может прогнозировать вероятность возникновения острого сердечного приступа в ближайшие 5 лет.
Искусственный интеллект и постоянный мониторинг могут не только помочь в профилактике развития, но и в диагностике сердечно-сосудистых заболеваний, выборе терапии. Например, Cardioexplorer – это первый научно обоснованный ИИ-тест, который обнаруживает атеросклеротические бляшки и жировые отложения в коронарных артериях с большей точностью, чем многие стандартные процедуры. Это чрезвычайно важно тогда, когда стенки сосудов становятся толстыми и жесткими, кровоток замедляется и это может привести к сердечному приступу.
Система Arterys с технологией AI Cardiac MR Suite позволяет кардиологам просматривать сердце пациента в четырехмерном режиме с помощью цветовой кодировки кровотока в режиме реального времени. Однако медицинские изображения, наиболее приближенные к реальности, связаны с концепцией цифрового двойника (близнеца). Речь идет о том, чтобы собрать как можно больше данных и смоделировать возможные риски и результаты терапии до фактического вмешательства. Например, Siemens Healthineers работает над алгоритмами, которые генерируют цифровые модели сердца на основе изображений МРТ и измерений ЭКГ. Французская компания ExactCure делает нечто похожее – цифровой двойник на смартфоне пациента имитирует индивидуальную реакцию на лекарства.
Источник: Medical Futurist. 02.04.2019
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Читайте также:

