Диуретики в терапии сердечно сосудистых заболеваний реферат
Обновлено: 06.07.2024
Петлевые диуретики. Клинические различия между торасемидом и фурасемидом. Сравнительная таблица
Петлевые диуретики — наиболее мощные по диуретическому эффекту среди всех диуретиков. Основные и всем известные их представители — фуросемид и торасемид. Оба лекарственных средства принадлежат к одной группе, поскольку их действие разворачивается толстом сегменте восходящей части петли Генле. Общий механизм действия обуславливает их общие показания и побочные эффекты. При этом фуросемид и торасемид имеют отличия в действии, которые играют роль при их назначении.
Общее для петлевых диуретиков
- Общий механизм действия
Петлевые диуретики относят к сильнодействующим салуретикам (выводящим соль). Их действие основано на выведении ионов натрия. Поскольку объем внеклеточной жидкости зависит в основном от NaCl, усиление экскреции Na + следом приводит к выведению внеклеточной жидкости. Петлевые диуретики ингибируют симпорт Na±2Cl- -K+в восходящем отделе петли Генле.
Мочегонный эффект петлевых диуретиков дозозависим. В максимальных дозах они способны выводить до 20-25% отфильтрованного в первичную мочу натрия — больше чем любые другие диуретики.
Ключевые отличия фуросемида и торасемида
Различия между препаратами имеют клиническое значение. Для удобства основные отличия помещены в таблицу.
-
Сила и продолжительность действия.
Фуросемид имеет быстрое, мощное и кратковременное действие.
Так, при однократном приеме внутрь первые два часа наблюдается усиленное, учащенное мочевыделение. В этот же период его максимального действия может возникать гипотония. Постепенно диуретический эффект сменяется задержкой натрия и воды.
Диуретическое действие торасемида развивается столь же быстро, но продолжается дольше и более плавно во времени. Благодаря тому, что пиковый эффект у торасемида менее выражен, а действие сохраняется до 18 часов, у пациентов отсутствует частое мочеиспускание первые часы после приема, практически не бывает снижения давления, реже возникает синдром рикошета (более выражен для доз 10 и 20 мг/сут).
Распространенность сердечной недостаточности в европейской популяции составляет от 0,4 до 2%. Частота ее быстро увеличивается с возрастом. В отличие от других распространенных сердечно-сосудистых заболеваний, смертность от сердечной недостаточности, скорректированная по возрасту, также повышается. Если не удается установить причину сердечной недостаточности, то прогноз неблагоприятный. Около половины больных с этим диагнозом умирают в течение 4 лет, а среди пациентов с тяжелой сердечной недостаточностью летальность в течение 1 года превышает 50% [1]. К числу основных достижений в изучении сердечной недостаточности можно отнести установление патогенетической роли нейрогуморальных систем, которое позволило коренным образом пересмотреть подходы к лечению этого состояния. В настоящее время большое внимание уделяется не только купированию симптомов, но и профилактике прогрессирования сердечной недостаточности и смерти. С этой целью чаще всего используют ингибиторы ангиотензинпревращающего фермента (АПФ) и β-адреноблокаторы. Среди последних доказанной эффективностью у больных сердечной недостаточностью обладают карведилол, метопролол и бисопролол. Хотя блокаторы нейрогуморальных систем улучшают прогноз больных сердечной недостаточностью и задерживают ее прогрессирование, они обычно не оказывают непосредственного влияния на клинические проявления этого состояния. Более то-го, неосторожное применение β-адреноблокаторов при декомпенсации сердечной недостаточности может при-вести к нарастанию симптомов за счет отрицательного инотропного действия, в то время как ингибиторы АПФ нередко вызывают артериальную гипотонию. В связи с этим назначение блокаторов нейрогуморальных систем не отменяет необходимость в использовании стандартных средств, прежде всего диуретиков. Важность адекватной диуретической терапии демонстрирует следующее наблюдение.
Больной В., 48 лет, инженер, обратился в клинику в феврале 2006 года с жалобами на одышку при ходьбе по ровному месту, приступы удушья, возникающие в положении лежа, сердцебиения, выраженные отеки ног, периодически тупые ноющие боли в области сердца, не снимающиеся нитроглицерином, тяжесть в правом подреберье. Одышка появилась около 2 лет назад. Первоначально она возникала только при подъеме по лестнице, однако постепенно нарастала. Иногда беспокоили боли в области сердца, не связанные с физической нагрузкой. При обследовании по месту жительства АД 125/80 мм рт. ст. Уровень общего холестерина сыворотки 152 мг/дл. На ЭКГ блокада левой ножки пучка Гиса. При эхокардиографии выявлена умеренная дилатация левого желудочка и снижение фракции выброса до 43%. Диагностированы ИБС, стенокардия II функционального класса, атеросклероз с поражением коронарных артерий. Проводилась терапия изосорбида динитратом в дозе 20 мг два раза в день и эналаприлом в дозе 5 мг/сут без особого эффекта. Ухудшение состояния с лета прошлого года: усилилась одышка, появились приступы сердечной астмы, утомляемость, отеки ног, увеличение живота, уменьшилось количество выделяемой мочи. Кардиолог в поликлинике расценил развитие сердечной недостаточности как следствие ИБС. От госпитализации больной отказался. К терапии были добавлены дигоксин в дозе 0,25 мг/сут, фуросемид по 40 мг через день, доза эналаприла увеличена до 10 мг/сут. В результате лечения самочувствие улучшилось: уменьшились одышка и отеки, улучшился сон, увеличился диурез.
Спустя 2-3 месяца вновь отмечено ухудшение состояния. Беспокоила одышка при небольшой физической нагрузке, определялись распространенные отеки, асцит. Больной ежедневно принимал фуросемид по 80 мг, однако добиться существенного увеличения диуреза не удавалось. На фоне активной диуретической терапии наблюдалось снижение уровня калия до 3,2 ммоль/л. Доза эналаприла была увеличена до 20 мг/сут, но затем ее пришлось снизить из-за артериальной гипотонии (90/55 мм рт. ст.). После присоединения спиронолактона в дозе 100 мг/сут отеки несколько уменьшились, однако выраженная одышка, приступы сердечной астмы и склонность к гипокалиемии сохранялись.
При поступлении в клинику состояние средней тяжести. Ортопноэ. Цианоз лица. Выраженные отеки ног. В легких выслушиваются незвонкие мелкопузырчатые хрипы в нижних отделах легких. Частота сердечных сокращений 92 в минуту. АД 110/70 мм рт. ст. Тоны сердца глухие, систолический шум на верхушке сердца. Живот увеличен в объеме за счет свободной жидкости. Размер печени по Курлову 10/4-10-8 см. Селезенка не увеличена. На ЭКГ блокада левой ножки пучка Гиса. При рентгенографии выявлено увеличение сердца в размерах, усиление легочного рисунка за счет застоя жидкости. При эхокардиографии обнаружены дилатация всех камер сердца (диастолический размер левого желудочка 7,3 см) и снижение фракции выброса левого желудочка до 23% (рис. 1). Уровень калия крови — 3,3 ммоль/л, общего холестерина сыворотки — 128 мг/дл, холестерина липопротеидов низкой плотности 82 мг/дл.
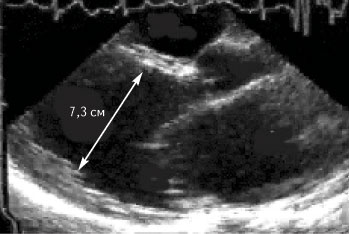
Рис. 1. Выраженная дилатация левых камер сердца на эхокардиограмме
Таким образом, у больного была выявлена картина дилатационного поражения сердца, которое характеризовалось значительным ухудшением насосной функции левого желудочка и тяжелой сердечной недостаточностью, рефрактерной к проводимой терапии. При отсутствии артериальной гипертонии и порока сердца в таких случаях в первую очередь следует исключать ИБС и алкогольную кардиомиопатию. Диагноз атеросклероза коронарных артерий представлялся маловероятным, учитывая отсутствие стенокардии и инфаркта миокарда в анамнезе, а также основных факторов риска, хотя исключить этот диагноз можно только с помощью коронарной ангиографии. По словам больного и его родственников, алкоголь практически не употребляет. Возможными причинами дилатационного поражения сердца являются также миокардит, эндокринные (гипотиреоз, акромегалия), системные (саркоидоз, наследственный гемохроматоз, системная склеродермия), нейромышечные заболевания, лучевая терапия, прием антрациклинов. Данных в пользу указанных заболеваний получено не было. Следует отметить, что исключить миокардит на основании клинической картины сложно, однако выполнение биопсии миокарда не представлялось возможным. Диагностирована дилатационная кардиомиопатия, хроническая сердечная недостаточность III функционального класса.
В клинике проводилось внутривенное введение дигоксина и фуросемида, увеличены дозы эналаприла до 20 мг/сут и спиронолактона до 150 мг/сут. В последующем фуросемид был заменен на торасемид (Диувер) в дозе 20 мг/сут. В результате лечения значительно уменьшились одышка и размеры печени, прекратились приступы сердечной астмы, практически полностью прошли отеки. Уровень калия повысился до 4 ммоль/л. После выписки продолжал прием дигоксина в дозе 0,25 мг/сут, торасемида в дозе 20 мг 2-3 раза в неделю, эналаприла в дозе 20 мг/сут. Спиронолактон был постепенно отменен. При этом уровень калия оставался нормальным. При применении торасемида отсутствовала проблема срочного диуреза, развивавшегося в первые 2 ч после приема фуросемида. Начата терапия карведилолом в дозе 3,125 мг два раза в сутки, которую постепенно увеличили до 25 мг два раза в сутки. При амбулаторном обследовании через 2 месяца состояние остается стабильным. Беспокоит умеренно выраженная одышка, однако отеки отсутствуют. При эхокардиографии выявлено уменьшение диастолического размера левого желудочка до 6,5 см и увеличение фракции выброса до 32%.
Дилатационная кардиомиопатия - это тяжелое заболевание сердечной мышцы, которое обычно характеризуется прогрессирующим течением. Этиология его остается неизвестной, поэтому лечение предполагает применение патогенетических средств, позволяющих уменьшить проявления сердечной недостаточности и задержать ее прогрессирование. В терминальной стадии показана трансплантация сердца. Всем больным следует назначать ингибиторы АПФ и β-адреноблокаторы, однако при нарастании застойной сердечной недостаточности ключевое значение имеет адекватная диуретическая терапия. В руководстве Европейского общества кардиологов по диагностике и лечению сердечной недостаточности содержатся следующие рекомендации по применению диуретиков [1]:
При наличии задержки жидкости, сопровождающейся застоем крови в легких или периферическими отеками, диуретики являются необходимым компонентом симптоматического лечения сердечной недостаточности. Их применение приводит к быстрому уменьшению одышки и увеличению толерантности к физической нагрузке (класс рекомендации I, уровень доказанности А),
В контролируемых рандомизированных исследованиях влияние диуретиков на симптомы и выживаемость больных не изучалось. Диуретики следует всегда назначать в комбинации с ингибиторами АПФ и β-адреноблокаторами (класс рекомендации I, уровень доказанности С).
Таким образом, эксперты рекомендуют назначать диуретики всем больным сердечной недостаточностью II-IV функционального класса. Влияние мочегонных средств на выживаемость таких пациентов не изучалось в длительных контролируемых исследованиях, однако их проведение нецелесообразно и неэтично, учитывая явный симптоматический эффект препаратов этой группы. Кроме того, протоколы всех исследований ингибиторов АПФ и β-адреноблокаторов у больных застойной сердечной недостаточностью предполагали обязательное применение стандартных средств, прежде всего диуретиков. В связи с этим монотерапия ингибитором АПФ или β-адреноблокатором обоснована только у больных с бессимптомной дисфункцией левого желудочка, например, после инфаркта миокарда.
При легкой сердечной недостаточности могут быть назначены тиазидные диуретики, однако по мере прогрессирования нарушений кровообращения обычно требуется применение петлевого диуретика. В эквивалентных дозах все петлевые диуретики вызывают сопоставимое увеличение диуреза. Снижение их эффективности может быть связано с ухудшением функции почек или нарушением всасывания фуросемида в желудочно-кишечном тракте. Возможные подходы к преодолению резистентности к петлевым диуретикам включают в себя увеличение их дозы, внутривенное введение (в том числе путем непрерывной инфузии), присоединение тиазида или спиронолактона (особенно при наличии гипокалиемии несмотря на прием ингибитора АПФ). В рекомендациях Европейского общества кардиологов (2005 г.) указано, что при снижении эффективности фуросемида его можно заменить на торасемид, так как биодоступность последнего не снижается у больных сердечной недостаточностью. Приведенное наблюдение подтверждает, что применение торасемида позволяет улучшить результаты лечения тяжелой сердечной недостаточности.
Главным преимуществом торасемида (Диувера) является высокая биодоступность, которая в разных исследованиях составляла 79-91% и превосходила таковую фуросемида (53%) [2]. Высокая и предсказуемая биодоступность определяет "надежность" диуретического действия торасемида. Торасемид обладает достаточно длительным периодом полувыведения (3-5 ч), в то время как длительность периода полувыведения фуросемида, буметанида и пиретанида составляет около 1 ч [2]. Благодаря этому торасемид действует длительнее фуросемида. Торасемид биотрансформируется в печени с образованием нескольких метаболитов. Только 25% дозы выводится с мочой в неизмененном виде (против 60-65% при приеме фуросемида и буметанида). В связи с этим фармакокинетика торасемида существенно не зависит от функции почек, в то время как период полувыведения фуросемида увеличивается у больных почечной недостаточностью. Этот факт имеет важное значение, так как при наличии выраженного застоя крови по большому кругу кровообращения функция почек обычно ухудшается. Действие торасемида, как и других петлевых диуретиков, начинается быстро. При внутривенном введении оно достигает пика в течение 15 мин. Доза торасемида 10-20 мг эквивалента 40 мг фуросемида. При увеличении дозы (до 200 мг) наблюдалось линейное повышение диуретической активности.
Для цитирования: Шилов А.М., Чубаров М.В., Князева С.А., Мельник М.В. Диуретики в лечении сердечно-сосудистой патологии. РМЖ. 2002;10:437.
ММА имени И.М. Сеченова
В настоящее время диуретики занимают ведущее место в лечении сердечной недостаточности и артериальной гипертензии различной этиологии.
Использование диуретических препаратов в лечении сердечно–сосудистых заболеваний началось в середине прошлого столетия, когда в 1956 году был синтезирован и впервые применен в клинической практике хлортиазид. В 1958 г. был создан более мощный тиазидный диуретик – гидрохлортиазид, в 1959 г. появился тиазидоподобный диуретик хлорталидон. 60–е годы характеризовались интенсивным применением тиазидных диуретиков в кардиологической практике, однако накопленный клинический опыт и экспериментальные исследования показали на фоне благоприятного эффекта ряд побочных реакций, которые снижали ожидаемый терапевтический успех, что побудило исследователей к поиску новых диуретических препаратов [1,2].
Диурез – мочеотделение, регулируемое почечными и внепочечными механизмами. К внепочечным механизмам относятся:1) состояние насосной функции сердца, 2) натрийдиуретический гормон предсердий, 3) антидиуретический гормон гипофиза, 4) альдостерон – гормон коры надпочечников. Внутрипочечный механизм регуляции диуреза осуществляется через увеличение или снижение фильтрации и реабсорбции солей из первичной мочи (в частности, ионов натрия) и облигатно к ним Н2О эпителием почечных канальцев.
Диуретики – лекарственные препараты, снижающие реабсорбцию натрия и воды, что ведет к увеличению диуреза, по своему механизму действия делятся на осмотические, солевые, водные (рис. 1).
Рис. 1. Схема действия диуретиков
Осмотические (маннитол, глюкоза, органические кислоты) и водные (демоклоциклин, препараты лития) диуретики применяются пpи лечении сердечной недостаточности. Солевые диуретики – при лечении артериальной гипертензии, острой и хронической сердечной недостаточности [3].
Согласно современным представлениям о строении нефрона – функциональной единицы почки и функции его различных отделов, солевые диуретики делятся на тиазидные, петлевые и калийсберегающие.
На рисунке 2 представлена схема строения и функции нефрона. Мочевыделительная функция регулируется двумя основными процессами в нефроне: фильтрацией в гломерулярном аппарате и реабсорбцией в различных отделах нефрона. Транспортная функция различных отделов нефрона представлена на рисунке 2. Реабсорбция жидкости через проксимальные отделы извитых тубул осуществляется изоосмотическим механизмом вслед за реабсорбцией приблизительно двух третей фильтрованного натрия. NаНСО3 реабсорбируется неэлектрогенным механизмом через секрецию ионов водорода. Подобный активный транспорт солей создает трансэпителиальный градиент осмотического давления, который позволяет осуществлять пассивный выход воды из нефрона в перитубулярные капилляры. Подъем концентрации Cl – в тубулярной жидкости соответствует снижению концентрации НCО3 – и становится определяющей силой движения ионов Cl – вниз по концентрационному градиенту. Прямая часть проксимального канальца осуществляет активный электрогенный транспорт Nа + . Оставшаяся одна треть гломерулярного фильтрата поступает в нисходящее колено петли Генле. Тонкая часть нисходящего колена петли Генле проницаема для Н2О и непроницаема для Nа + , удерживая NaCl в жидкости нефрона. В восходящий отдел петли Генле жидкость поступает с высокой концентрацией NaCl, который в начальной части пассивно выходит в перитубулярное пространство, создавая делюцию тубулярной жидкости. В толстом отделе восходящего колена петли Генле имеет место активная реабсорбция Cl – и пассивное выведение Nа + . В дистальном отделе извитых канальцев нефрона на активную реабсорбцию Nа + имеет место секреция в просвет нефрона К + и Н + . Собирательные канальца почки непроницаемы для воды в отсутствие антидиуретического гормона. В этом отделе альдостерон активизирует реабсорбцию Nа + и секрецию в мочу ионов водорода и калия.
Рис. 2. Схема строения нефрона и точки приложения диуретиков
Тиазидные диуретики в основном действуют на уровне проксимальных и дистальных канальцев нефрона через блокирование противотранспорта натрия и хлора, что ведет к осмотической задержке воды в нефроне и уменьшению объема циркулирующей плазмы в сосудистом русле.
Петлевые диуретики (фуросемид, этакриновая кислота и их производные) блокируют реабсорбцию хлора, что приводит к задержке натрия и облигатной задержке воды в нефроне.
Помимо диуретического эффекта, данный класс препаратов может оказывать ряд побочных отрицательных эффектов (нарушение водно–электролитно–щелочного баланса, повреждение форменных элементов крови), приводя к анемии, агранулоцитозу, тромбоцитопении, системным повреждениям в виде кожного васкулита, что в конечном итоге может вызвать сложные нарушения гемодинамики, вплоть до внезапной кардиогенной смерти или развитию печеночной комы. Возможные побочные эффекты диуретиков представлены в таблице 1.
Участие почки в регуляции насосной функции сердца и уровня артериального давления представлено на рисунке 3.
Рис. 3. Гипотетическая схема регуляции насосной деятельности сердца и артериального давления
Минутный объем сердца (МО) – интегральный показатель насосной деятельности сердца является производной величиной сократительного состояния миокарда (ударный объем) и частоты сердечных сокращений:
Одновременно МО контролируется объемом притекаемой крови к сердцу, т.е. объемом циркулирующей крови (ОЦК). ОЦК регулируется почкой через ренин–ангиотензин–альдостероновую систему. Включение ренин–ангиотензиновой системы осуществляется юкстагломерулярным аппаратом почек в результате снижения почечного кровотока в корковом слое, что ведет к выбросу ренина, который, в свою очередь, превращает ангиотензиноген в ангиотензин–1. Ангиотензин–1 под воздействием ангиотензинпревращающего фермента (АПФ) переходит в ангиотензин–2, являющийся мощным вазоконстриктором, стимулирующим рецепторы АТ сосудистой стенки. Воздействуя на кору надпочечников, ангиотензин–2 стимулирует синтез альдостерона, который снижает секрецию натрия в мочу в дистальных отделах собирательных почечных канальцев, приводя тем самым к задержке жидкости в сосудистом русле, т.е. увеличению ОЦК. В свою очередь, увеличение ОЦК ведет к увеличению МО. Одновременно увеличение концентрации натрия в крови способствует отеку сосудистой стенки, делает ее более чувствительной к прессорным агентам и способствует увеличению общего периферического сосудистого сопротивления (ОППС).
Уровень АД определяется произведением МО, как показателя насосной деятельности сердца, и ОПСС:
АД = МО x ОПСС, т.е.
АД = УО x ЧСС x ОПСС
ЧСС и сократительное состояние миокарда контролируется симпато–адреналовой системой через стимуляцию b –адренорецепторов, что приводит к учащению сердечного ритма и усилению сокращения миокарда, в конечном итоге – к увеличению УО.
Регуляция ОПСС осуществляется симпато–адреналовой системой (путем стимуляции a – и b –адренорецепторов) и ренин–ангиотензин–альдостероновой системой.
Распределение адренорецепторов в сердечно–сосудистой системе гетерогенно. В сердце преимущественно расположены b 1–адренорецепторы, в сосудистой стенке артерий и вен – a – и b 2–адренорецепторы. Стимуляция a – и b 2–адренорецепторов в венах вызывает повышение их тонуса, уменьшение емкости венозного русла, увеличение притока крови к сердцу и МО. Стимуляция b –адренорецепторов в артериях вызывает их сужение и повышение ОПСС. Стимуляция b 2–адренорецепторов в артериях вызывает вазодилатирующий эффект и снижает ОПСС.
ОППС зависит не только от тонуса артериального русла, но и от реологических свойств крови согласно упрощенной формуле Пуазейля:
ОПСС =( L x h ) / S , где
L – длина сосудов h – реологические свойства крови S – диаметр сосудов.
Реологические свойства крови определяются гематокритом (полицитемия), вязкостью крови (гиперлипидемия, гиперфибриногенемия, гипергликемия), подвижностью эритроцитов, агрегационным состоянием тромбоцитов и т.д.
Таким образом, имеют место 5 основных областей приложения терапевтических воздействий при лечении СН и АГ:
1) симпато–адреналовая система – блокада a – и b –адренорецепторов;
2) почки – диуретики;
3) ренин–ангиотензин–альдостероновая система – ингибиторы АПФ и блокаторы АТ1–рецепторов сосудов;
4) сосудистая система – периферические вазодилататоры, в частности, антикальциевые препараты;
5) реология крови – антиагреганты, гиполипидемические, сахароснижающие и т.п.
Современную кардиологию невозможно представить без b –адреноблокаторов, которых известно более 20 наименований, ингибиторов АПФ [5]. Однако в настоящее время диуретики занимают приоритетное место в лечении дилатационной кардиопатии и АГ.
При лечении АГ выделяют три основные цели: непосредственную, промежуточную и конечную [1,6,7].
Сравнительные исследования показали, что нет существенной разницы в антигипертензивной активности низких ( 25 мг) тиазидных диуретиков. По сводным данным 31 исследования, высокие дозы тиазидных диуретиков снижают уровни АД в среднем на 18/11 мм рт.ст., а низкие дозы – на 13/9 мм рт.ст. В то же время низкие дозы диуретиков гораздо лучше переносятся пациентами и не сопровождаются существенными электролитными и метаболическими нарушениями [11].
В отличие от b –адреноблокаторов, диуретики одинаково эффективно предотвращают сердечно–сосудистые осложнения у больных АГ как среднего, так и пожилого возрастов. В 18 рандомизированных исследованиях, в которых диуретики и b –адреноблокаторы применялись при лечении АГ у больных старше 60 лет, было обнаружено, что диуретики эффективно предотвращают развитие первичных и повторных нарушений мозгового кровообращения [12]. Однако в отличие от b –адреноблокаторов диуретики более эффективны в профилактике риска развития ИБС и летальных исходов, что делает их препаратами первого ряда при начальной терапии АГ.
Таким образом, тиазидные диуретики назначаются в небольших дозах (не более 25 мг в сутки), обладают достаточно высокой антигипертензивной активностью и хорошей переносимостью. Это единственный класс антигипертензивных препаратов, о которых известно, что они способны улучшить отдаленный прогноз у больных АГ.
Тиазидные и тиазидоподобные диуретики можно условно разделить на два поколения. Первое поколение – производные бензотиадиазона (гидрохлортиазид и др.) и фтелимидина (хлорталидон и др.); второе поколение – производные хлорбензамида (индапамид и др.), которые по химической структуре представляют собой производное хлорбензамида, содержащее метилиндолиновую группу.
Гемодинамический эффект индапамидоподобных диуретиков обусловлен их фармакологическим действием. В частности, индапамид - умеренный салуретический диуретик, связанный с ингибированием реабсорбции Na + , Cl – , H + и в меньшей степени К + и Мg2 + в проксимальных и дистальных канальцах короткого сегмента нефрона. Одновременно индапамид устраняет избыточное содержание ионов натрия в сосудистой стенке (вследствие его высокой липофильности), повышает синтез простагландина Е2 и простациклина I2, угнетает приток ионов Са в гладкомышечные клетки сосудов, что вызывает их дилатацию и снижает их чувствительность к прессорным агентам (катехоламинам, тромбоксану). Суммарный гемодинамический эффект индапамидов проявляется в виде:
- вазодилатирующего действия
- уменьшения ОПСС
- снижения системного артериального давления
- изменения вязкостных свойств крови за счет ингибирования агрегационной активности тромбоцитов.
Воздействие индапамидов на АД без существенного влияния на диурез проявляется в суточной дозе 2,5 мг, при увеличении которой диуретический эффект становится доминирующим.
По своей гипотензивной активности индапамид превосходит в 30 раз действие спиронолактонов, в 100 раз – фуросемида и в 300 раз – хлорталидона при применении в сопоставимых дозах [13]. Одним из идентифицированных антигипертензивных эффектов индапамида является воздействие на почечную продукцию и высвобождение простагландинов, ингибирование образования сосудистого вазоконстриктора – тромбоксана. Под действием индапамида у больных эсенциальной артериальной гипертензией увеличивалось выделение простагландина Е2, обладающего вазодилатирующей активностью. In vitro был верифицирован эффект ингибирования индапамидом синтеза тромбоксана А2 в тромбоцитах человека и стимулирования выделения вазодилатирующего простациклина I2 [14].
Терапевтическая эффективность индапамидовых диуретиков продемонстрирована в ряде крупных рандомизированных исследований. Отмечена их способность профилактировать развитие ИБС за счет снижения массы миокарда при АГ. Это свойство, нетипичное для других классов диуретиков, делает индапамид уникальным препаратом с кардиопротективным действием, выраженность которого не уступает b –адреноблокаторам и ингибиторам АПФ.
Таким образом, индапамид, сочетая в себе все положительные фармакодинамические, фармакокинетические и экономические достоинства, при отсутствии побочных эффектов других диуретиков, является препаратом, перспективным в плане терапевтической тактики у больных АГ и хронической сердечной недостаточностью.
ХСН довольно часто является следствием синдрома артериальной гипертензии и остается одной из главных причин в структуре причин инвалидизации и летальности от сердечно–сосудистой патологии. В настоящее время средствами выбора в лечении ХСН с систолической дисфункцией ЛЖ являются ингибиторы АПФ, а при диастолической дисфункции – диуретики. В основе ХСН у большинства больных АГ имеет место нарушение диастолической и систолической функции ЛЖ, поэтому наиболее перспективным является комбинированное лечение ингибиторами АПФ и диуретиками. С учетом вышеизложенного для лечения ХСН предпочтение должно отдаваться тиазидоподобным диуретикам – индапамидам с умеренным по силе и длительным по продолжительности действием [16]. Индапамид, снижая уровень внутриклеточного кальция, сохраняя содержание магния, уменьшает ригидность сосудистой стенки и способствует более эффективной релаксации кардиомиоцита в диастолу. При этом увеличивается синтез простациклинов, уменьшается агрегация тромбоцитов и выброс тромбоксана А2, что суммарно оказывает положительный гемодинамический эффект за счет уменьшения постнагрузки для ЛЖ.
Индапамид, улучшая микроциркуляцию в почке, устраняет микроальбуминурию, являющуюся маркером генерализованного поражения сосудов и предиктором сердечно–сосудистых и почечных осложнений.
Таким образом, использование диуретиков, в частности, индапамидоподобных, является актуальным и перспективным в профилактике и лечении АГ и ХСН.
1. Преображенский Д.В, Сидоренко Б.А. Дифференциальная медикаментозная терапия при артериальной гипертензии. Сonsilium Medicum. 2001. Т 3, 10, стр. 83
2. Преображенский Д.В., Сидоренко Б.А., Шатунова И. М., Марьенич А.В. Место диуретиков в лечении АГ. Индап. Москва, 2000.
3. Smith T.W., Brannwald E. The management of heart failure // Heart Disease. 1984. 587.
4. Grantham J.J., Chonko A.M. The physiological basis and clinical use of diuretics. Sodium and Water Homeostasis. New York, 1978, 179.
5. Шилов А.М., Князева С.А., Ушакова М.В. Бета–блокаторы в лечении АГ. Российские медицинские вести. 2001, VI, 4, стр. 31.
6. Joint National Committee on Prevention, Detection, Evaluation and Treatment of High Blood Pressure. // Arch. Intern. Med. 1997, V 157, 213.
7. Евсиков Е.М. Индапамид – современный гипотензивный препарат с сочетанием механизмов действия. Индап. Москва. 2000. 26.
8. Stimpel M. Arterial hypertension. Berlin – New York, 1996, 8.
9. Kaplan N.M. Clinical hypertension. 7 edition. Baltimore, 1998.
10. Opie L.H. Drugs for the heart. 4–edition. Philadelphia, 1995.
11. Ames R.P. A comparison of blood lipid and blood pressure responses during the treatment of systemic hypertension with indapamide and with thriazides. // Amer. J. Cardiol. 1996, 77, 128 – 168.
12. Psaty B., Smith N.L., Siscovick D.S. and all. Health outcomes associated with antihypertensive therapies used as first–line agents. A systematic review and meta–analysis. JAMA, 1997, 277, 739.
13. Ogilvie R.I. Diuretic treatment in essential hypertension. // Current Medical Research and Opinion. 1983, N8, 53.
14. Gbeassor F.M., Grose J.H., Le Bel M. Influence of diuretics on prostaglandin and thromboxane synthesis. // Clin. and Invest. Med., 1982, N5. 26.
15. Passeron J., Panly N., Despart J. International multicentre study of indapamide in the treatment of essential arterial hypertension. Postgrad. // Med. J., 1981, V 57, 53.
16. Куимов А.Д., Ложкина Н.Е., Казина Н.П. Лечение больных ХСН с синдромом АГ индапамидом в капсулированной форме и эналаприлом. Индап. Москва. 2000. 77.
При лечении пациента с хронической застойной сердечной недостаточностью необходимо попытаться прежде всего воздействовать на любую возможно обратимую причину данного синдрома. Коррекция гипертензии уменьшит избыточную нагрузку на сердце.
У больных с ишемической кардиомиопатией в плохо сокращающемся, но жизнеспособном миокарде, который снабжается кровью пораженными сосудами, возможно улучшение систолической функции после выполнения чрескожной внутрисосудистой коронарной ангиопластики (ЧВКА) или после операции шунтирования.
Таким образом, хотя больных со сниженной функцией ЛЖ и относят, как правило, к группе высокого операционного риска при проведении реваскуляризационных вмешательств, существенные преимущества таких вмешательств преобладают над риском. Клапанозамещающие или клапаносохраняющие операции у пациентов с застойной сердечной недостаточностью, развившейся вследствие патологии клапанов, также могут остановить прогрессирование желудочковой дисфункции.
Нужно упомянуть, что в соответствии с последними данными иммуносупрессивная терапия, направленная на лечение миокардитов вирусной или другой воспалительной этиологии, неэффективна.
После исчерпания этих возможностей нужно перейти к долгосрочным терапевтическим мероприятиям с целью стабилизации процесса. Крайне важны программы просвещения больных. Все пациенты с застойной сердечной недостаточностью должны получить подробные инструкции в отношении ограничений в диете (2 г в натрия день, низкое содержание жиров (холестерина) по показаниям), регулярного выполнения физических упражнений и правильного приема и возможных побочных эффектов лекарственных препаратов.

Как больные, так и члены их семей должны быть проинформированы об опасных жалобах и симптомах, появление которых требует госпитализации; члены семьи могут принять участие в программах обучения методам доврачебной реанимации.
Медикаментозная терапия застойной сердечной недостаточности достигла значительных успехов в течение последнего десятилетия. В настоящее время действие большинства эффективных препаратов направлено на прерывание порочного круга несостоятельной периферической адаптации и прогрессирующей нейрогуморальной активации.
Препараты другого типа действия все еще применяются как часть симптоматической терапии, хотя они и не приводят к увеличению продолжительности жизни. Ниже представлен обзор наиболее важных групп лекарственных препаратов.

Физическая подготовка при сердечной недостаточности. Все больше данных свидетельствует о пользе применения программ физической подготовки в терапии пациентов с сердечной недостаточностью. Выполнение в течение 12 недель стандартных тренировочных упражнений в объеме 70-80 % от пиковой аэробной мощности повышает способность пациентов с сердечной недостаточностью переносить физическую нагрузку. Недавние исследования показали, что регулярные физические упражнения меньшей интенсивности (
Мочегонные средства при хронической систослической сердечной недостаточности
Отеки голеней и (или) легочный застой часто служат ранними проявлениями сердечной недостаточности. Диуретики уменьшают симптомы застоя, развивающиеся в результате задержки жидкости и воды, и снижают повышенное внутрисердечное давление.
У больных со слабо и умеренно выраженными проявлениями заболевания начальная терапия тиазидным диуретиком (гидрохлоротиазид 25-50 мг ежедневно) будет способствовать уменьшению симптоматики. Лечение пациентов с более выраженными клиническими проявлениями обычно включает в себя применение петлевых диуретиков (например, фуросемид — Lasix, лазикс; 40-300 мг в день, общая доза и кратность введения зависят от клинического статуса и функции почек).
Если достигнутый диурез неадекватен, эффективность может быть повышена с помощью параллельного приема тиазидного диуретика или метолазона (Zaroxolyn, Diulo, Metenix; зароксолин, диуло, метеникс; 5-20 мг в день). Использование ингибитора альдостерона спиронолактона (Аldactone, альдактон; 25-200 мг в 1-2 приема ежедневно) также может усилить эффект через более длительный период времени. Внутривенные формы препаратов следует использовать у пациентов в состоянии декомпенсации, когда нарушено всасывание лекарств, принимаемых внутрь.
Применение мочегонных препаратов — часть стандартной терапии больных с застойной сердечной недостаточностью, однако оценка их эффективности должна сочетаться с учетом возможных побочных реакций. Избыточный диурез может привести к снижению сердечного выброса, что обусловит возникновение симптомов низкого кровотока и усугубит нарушение функции почек, проявляющееся возрастанием концентрации креатинина в сыворотке крови.
Кроме того, длительный прием диуретиков может вызвать электролитные нарушения, такие как гипокалиемия, которая способна провоцировать или усиливать летальные нарушения ритма, особенно у больных с риском смерти от аритмии или принимающих сердечные гликозиды. Терапия диуретиками должна выполняться под постоянным контролем концентрации калия и магния. Как только избыток жидкости выведен из организма, дозу мочегонных препаратов можно уменьшить или использовать лекарство периодически, чтобы избежать гиповолемии, гипокалиемии и гипомагниемии.
Видео этиология, патогенез сердечной недостаточности систолической, диастолической, лево- и правожелудочковой
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Диуретики в аптеке: классификация, применение, и что надо знать фармацевту
Диуретики – небольшая, но сложная фармакологическая группа лекарственных препаратов: не более десятка действующих веществ. При этом в клинической практике диуретические средства применяются широко и часто их покупают в аптеке. Когда назначаются препараты данной группы, чем они различаются, и можно ли их использовать для похудения читайте в нашей статье.
Для чего нужны диуретические средства
Общее свойство диуретиков усиливать выведение из организма ионов Na, а следовательно и воды с мочой, используется при лечении отеков различного генеза, но не только.
Разнообразные фармакологические эффекты диуретиков:
- Антигипертензивный: диуретики снижают объем циркулирующей крови и могут влиять на сосудистый тонус. Поэтому основная сфера применения диуретиков – сердечно-сосудистые заболевания: гипертония и сердечная недостаточность, сопровождающаяся отечным синдромом .
- Противоотечный: мочегонные активно применяются при острой и хронической почечной недостаточности, асците на фоне цирроза печени.
- Детоксикационный. Диуретики, особенно петлевые и осмотические, применяются для ускорения выведения водорастворимых ксенобиотиков при отравлениях.
- Специфические эффекты ацетазоламида. Известны эффекты ацетазоламида при глаукоме, внутричерепном давлении, горной болезни, некоторых видах эпилепсии.
- Прочие нетривиальные эффекты. В числе непривычных показаний: лечение обструкции легких для петлевых диуретиков, применение ацетазоламида при мозжечковой атаксии, синдроме ночного апноэ, психозах. Отмечается высокая противовоспалительная активность фуросемида и гидрохлортиазида, последний могут применять в терапии несахарного диабета.
Классификация диуретиков. Таблица
Лекарственные средства диуретического действия разнородны по своему химическому строению, силе, скорости и продолжительности основного мочегонного действия, которые во многом зависят от точки приложения. В таблице приводится классификация в зависимости от локуса действия и наблюдаемый диуретический эффект.
Краткая характеристика представителей групп
Ацетазоламид имеет ограниченное применение в связи со слабым и нестойким диуретическим действием, интенсивным выведением калия и бикарбонатов и быстро возникающей толерантностью. Применяется для снижения внутриглазного и внутричерепного давления, при некоторых формах малых приступов эпилепсии, для профилактики высотной болезни. Ингибирует карбоангидразу ресничного тела, вследствие чего снижается продукция водянистой влаги в передней камере глаза; снижает продукцию спинномозговой жидкости.
Осмотические диуретики маннит и мочевина вводятся внутривенно капельно в условиях стационара. Основное показание: снятие отёка мозга.
Тиазидные диуретики гидрохлортиазид и хлорталидон обладают умеренным мочегонным действием и высокой способностью понижать АД. Продолжительное действие позволяет широко использовать их в лечении гипертензии и отечного синдрома. Предпочтение данным препаратам отдается у больных с остеопорозом, поскольку они задерживают выведение кальция . Для данных диуретиков характерен потолок доз , выше которого не происходит усиление диуретического эффекта, поэтому для снятия выраженных отеков они не подходят. Кроме того, тиазиды сильнее всех выводят калий . Результат терапии данными препаратами зависит от состояния почек: при снижении их функции клинический эффект ослабевает.
Тиазидовые препараты непосредственно влияют на островковый аппарат поджелудочной железы, нарушая выделение инсулина. Имеется определенная патогенетическая связь между гипергликемией и гипокалиемией, так как ионы калия стимулируют секрецию инсулина. Таким образом, тиазидовые мочегонные не следует назначать пациентам с сахарным диабетом, а препараты калия могут применяться для коррекции этого побочного эффекта.
Тиазидоподобный индапамид обладает чересчур мягким мочегонным эффектом, поэтому в качестве противоотечного средства не применяется. Его действие основано на его способности вызывать дилатацию периферических сосудов , поэтому основное показание к применению индапамида – коррекция повышенного АД. Терапевтические дозировки, назначаемые при гипертензии не приводят к увеличению диуреза. Прием препарата не сопровождается электролитными нарушениями и функция почек на его эффективность не влияет.
Петлевые диуретики восходящей петли Генле представлены двумя препаратами, отличающимися в первую очередь по скорости действия.
Фуросемид – короткодействующий, мощный петлевой диуретик с дозозависимым эффектом . Чем выше дозировка препарата тем сильнее выведение мочи. Основное показание – снятие выраженных отеков, острая сердечная недостаточность, снятие гипертонического криза. При применении фуросемида, особенно в больших дозах, ежедневно, возможно развитие толерантности и феномена рикошета (резкое снижение диуреза после отмены при использовании больших доз). Фуросемид имеет побочное действие в виде электролитных сдвигов и ототоксичности .
Торасемид – длительно действующий диуретик, по силе сравним с фуросемидом. Преимущественным отличием от фуросемида, кроме длительного действия будут также отсутствие электролитных сдвигов и ототоксичности. Применяется при отечном синдроме различного генеза и артериальной гипертензии.
Петлевые диуретики могут эффективно применяться при недостаточной функции почек. Выводят кальций из организма, что неблагоприятно при остеопорозе. Препараты этой группы также задерживают секрецию мочевой кислоты, вызывая тем самым явления гиперурикемии. Это особенно важно учитывать у больных, страдающих подагрой.
Клопамид – петлевой диуретик, имеющий другую точку приложения в петле Генле. Средний по силе, с длительно развивающимся, стойким гипотензивным эффектом. Применяется только в препарате Норматенс, показания: для снижения давления в комбинации с резерпином и дигидроэргокристином.
Калийсберегающие диуретики чаще всего применяются в комбинациях с петлевыми и тиазидными для усиления диуретического эффекта и снижения потерь K. Например, спиронолактон + фуросемид, спиронолактон+ гидрохлортиазид, а триамтерен выпускается в уже готовой комбинации с гидрохлортиазидом в препарате Триампур композитум . Применяются они для лечения отеков и гипертонии. Комбинация спиронолактона и сердечных гликозидов позволяет усилить действие сердечных гликозидов, снизить их дозу и одновременно предупредить гипокалиемию на фоне их применения.
Блокаторы альдостерона спиронолактон и его производное эплеренон нашли особое применение у групп пациентов с хронической сердечной недостаточностью и постинфарктной систолической дисфункцией левого желудочка. Это связано с тем, что у больных с ХСН повышена секреция альдостерона, негативно влияющего на ССС. Спиронолактон и более селективно действующий эплеренон позволяют увеличить выживаемость в данной группе больных.
Блокаторы альдостерона, как имеющие стероидную структуру, могут вызывать гормональные сдвиги: у мужчин может возникнуть гинекомастия; у женщин — маскулинизация и нарушения менструального цикла.
При лечении калийсберегающими диуретиками критически важно контролировать уровень калия у лиц с тяжелой ХСН, поскольку гиперкалиемия может приводить к летальному исходу. Опасны комбинации с препаратами, вызывающими гиперкалиемию (препараты калия, другие калийсберегающие диуретики, ингибиторы АПФ, антагонисты рецепторов ангиотензина II, гепарин).
Почему диуретики должен назначать только врач, и почему их нельзя использовать самостоятельно
Патологии, при которых нужны диуретики, серьезные, и назначить терапию может только врач с учетом всех особенностей фармакологии и состояния больного. Врач назначает их при отсутствии противопоказаний, особенно при ХСН в тех случаях, когда у пациента имеется положительный баланс натрия (то есть количество натрия, принятого с пищей, превышает его выведение). И препарат, и дозу подбирает врач индивидуально для каждого конкретного случая.
Поэтому, диуретики должны продаваться только по показаниям и в соответствии с назначением!
Важнейшие наиболее частые побочные эффекты
Проявление
Каким диуретикам присущи
Ортостатическая гипотензия, тахикардия (особенно ночью и по утрам), аритмии, диспепсические расстройства
(тошнота, рвота), головная боль, дезориентациея, общая заторможенность.
Петлевые диуретики при высоких дозах
Мышечная слабость, мышечные подергивания,
сердцебиение, вздутие живота, запоры, анорексия. Могут наблюдаться судороги икроножных
мышц, полиурия. Характерны изменения на ЭКГ . Повышение риска ишемического инсульта.
Наиболее выражена при приеме тиазидных диуретиков, менее выражена при приеме петлевых диуретиков и ацетазоламида
Дискомфорт в эпигастрии, металический вкус во рту, мышечная
слабость, регидность и парестезии в pyкax и ногах. На ЭКГ регистрируются уширение интервала
РQ, высокие "гигантские" зубцы Т, уширение комплекса QRS, возможна внезапная остановка сердца.
При бесконтрольном применении калийсберегающих диуретиков
Нарушения сердечного ритма, повышение токсичности сердечных гликозидов.
Те же препараты, что и вызывающие гипокалиемию
Мышечная слабость, сонливость, недомогание, тошнота, психические нарушения, коматозное состояние, связанные также с вызванным гиповолемией повышением уровня АДГ, снижением способности почек к разведению и повышенной жаждой.
Наиболее часто наблюдается при использовании тиазидных диуретиков, реже — петлевых и калийсберегающих .
Парестезий, гиперрефлексии, судорог мышц рук и ног (преимущественно тонических, реже клонических, "руки акушера", "конской" стопы; ползание мурашек во рту и в пальцах), прогрессирования кариеса зубов и катаракты, а также поперечной исчерченности ногтей, сухости кожи и ломкости волос (трофические нарушения). На ЭКГ удлиняется интервал QT.
При применении больших доз петлевых диуретиков
Тошнота, жажда, боли в костях, адинамия, запоры, психическая заторможенность, язвенные поражения желудка, кальцификация мягких тканей. Кроме того, возможно поражение почечных канальцев с полиурией, дегидратацией организма, отложением фосфатных или оксалатных камней, развитием пиелонефрита. На ЭКГ укорачивается сегмент QT, зубец Т начинается у нисходящей части зубца R.
Иногда при применении тиазидных диуретиков
Снижение обоняния и вкусовой чувствительности
Нарушение сократимости миокарда и скелетных мышц, возможны парестезии, тремор, боли в костях, патологические переломы.
Приступы подагры (боли в суставах), риск ИБС
Петлевые, реже тиазидовые и ацетазоламид.
Риск атеросклеротического поражения сосудов с развитием ИБС, цереброваскулярные нарушения
Нарушение толерантности к углеводам и гипергликемия
Нарушение выделения инсулина поджелудочной железой, риск сахарного диабета
Тиазиды, особенно при длительном применении
Развитие остеопороза, в связи с этим противопоказан при дыхательной недостаточности и совместно с калийсберегающими диуретиками
Диакарб, редко калийсберегающие диуретики при длительном применении высоких доз
Клинически не выражен, однако требует коррекции в определенных случаях
Петлевые диуретики при длительном лечении высокими дозами, тиазиды
У мужчин может вызывать гинекомастию, гипертрофию предстательной железы, снижение либидо, эректильную дисфункцию, у женщин возможно нарушение менструального цикла.
Ннарушение выделительной функции почек
При длительной диуретической терапии главным образом мощными препаратами в высоких дозах.
Снижение слуха, вестибулярные нарушения
Применение диуретиков в качестве средства для похудения опасно. Диуретики у спортсменов могут отрицательно воздействовать на максимальную способность к физической нагрузке и продолжительность длительной субмаксимальной физической нагрузки. Дегидратация неблагоприятно сказывается на сердечно-сосудистой и терморегуляторной системах организма во время физической нагрузки. В ходе фармконсультирования, фармацевт должен не только выяснить кому и для чего приобретают препарат, но и провести об огромном потенциальном вреде самоназначения.
Противопоказания к применению диуретиков
Цирроз печени из-за риска печеночной энцефалопатии
Тяжелая печеночная и почечная недостаточность, первый триместр беременности
Выраженная сердечная и почечная недостаточность ввиду повышения ОЦК в начале действия. Мочевина абсолютно противопоказана при печеночной недостаточности
Гиповолемия, выраженная анемия. Осторожно назначают при печеночной недостаточности, выраженном поражении почек, тяжелой
сердечной недостаточности. Фуросемид не рекомендуется назначать при аллергии
Тяжелые формы подагры, выраженной гипокалиемии, осторожно - при сахарном диабете. Необходимо с особой осторожностью назначать при ХПН, тяжелой ХНК, тяжелой печеночной недостаточности
ХПН, гиперкалиемия, ацидоз, неполной в
атриовентрккулярной блокаде. При тяжелых заболеваниях печенирекомендуется коррекция доз. Недопустимо совместное применение нескольких
β-адреноблокаторы и ингибиторы АПФ увеличивают вероятность гиперкалиемии
Читайте также:

