Возбудитель чумы микробиология кратко
Обновлено: 02.07.2024
Чума (pestis) – острое инфекционное заболевание, протекающее по типу геморрагической септицемии. В прошлом чума была грозным бичом для человечества. Известны три пандемии чумы, которые унесли миллионы человеческих жизней.
Возбудитель чумы был открыт в 1894 г. французским ученым А. Иерсеном, в честь которого и получил название Yersinia pestis. Род Yersiniа относится к семейству Enterobacteriaceae и включает 11 видов, из них патогенными для человека являются три: Y. pestis, Y. pseudotuberculosis и Y. enterocolitica; патогенность остальных пока еще не ясна.
Резистентность. В мокроте палочка чумы может сохраняться до 10 дней; на белье и одежде, испачканных выделениями больного, сохраняется неделями (белок и слизь охраняют ее от губительного действия высыхания). В трупах людей и животных, погибших от чумы, выживает с начала осени до зимы; низкая температура, замораживание и оттаивание не убивают ее. Солнце, высыхание, высокая температура губительны для Y. pestis. Нагревание до 60 °C убивает через 1 ч, при температуре 100 °C погибает через несколько минут; 70° спирт, 5 % раствор фенола, 5 % раствор лизола и некоторые другие химические дезинфектанты убивают за 5 – 10 – 20 мин.
Антигенный состав. У Y. pestis, Y. pseudotuberculosis и Y. enterocolitica обнаружено до 18 сходных соматических антигенов. Для Y. pestis характерно наличие капсульного антигена (фракция I), антигенов T, V – W, белков плазмокоагулазы, фибринолизина, белков наружной мембраны и pH6-антигена. Однако в отличие от Y. pseudotuberculosis и Y. enterocolitica, Y. pestis в антигенном отношении более однородна;
серологической классификации этого вида нет.
1. Способность клеток сорбировать экзогенные красители и гемин. Она связана с функцией системы транспорта железа и обеспечивает Y. pestis возможность размножаться в тканях организма.
2. Зависимость роста при температуре 37 °C от наличия в среде ионов Ca 2+ .
5. Синтез капсулы (фракции I – FraI). Капсула угнетает активность макрофагов.
6. Синтез пестицина – видовой признак Y. pestis.
7. Синтез фибринолизина.
8. Синтез плазмокоагулазы. Оба эти белка локализованы в наружной мембране и обеспечивают высокие инвазивные свойства Y. pestis.
9. Синтез эндогенных пуринов.
10. Синтез термоиндуцибельных белков наружной мембраны – Yop-белков (англ. Yersinia outer proteins). Белки YopA, YopD, YopE, YopH, YopK, YopM, YopN подавляют активность фагоцитов.
11. Синтез нейраминидазы. Она способствует адгезии (высвобождает рецепторы для Y. pestis).
13. Синтез пилей адгезии. Они угнетают фагоцитоз и обеспечивают внедрение Y. pestis, как внутриклеточного паразита, в макрофаги.
14. Синтез аминопептидаз широкого спектра действия.
15. Эндотоксин (ЛПС) и другие компоненты клеточной стенки, обладающие токсическим и аллергенным действием.
16. pH6-антиген. Он синтезируется при температуре 37 °C и низкой рН, подавляет фагоцитоз и обладает цитотоксическим действием на макрофаги.
Значительная часть факторов патогенности Y. pestis контролируется генами, носителями которых являются следующие 3 класса плазмид, обнаруживаемых обычно вместе у всех патогенных штаммов:
1) рYP (9,5 т. п. н.) – плазмида патогенности. Несет 3 гена:
pst – кодирует синтез пестицина;
pim – определяет иммунитет к пестицину;
pla – определяет фибринолитическую (активатор плазминогена) и плазмокоагулазную активность.
3) pYV (110 т. п. н.) – плазмида вирулентности. Она определяет зависимость роста Y. pestis при 37 °C от присутствия в среде ионов Ca 2+ , поэтому имеет другое название – Lcr-плазмида (англ. low calcium response). Гены этой, особенно важной, плазмиды кодируют также синтез антигенов V и W и термоиндуцируемых белков Yop. Их синтез осуществляется под сложным генетическим контролем при температуре 37 °C и в отсутствие в среде Ca 2+ . Все типы Yop-белков, кроме YopM и YopN, гидролизуются за счет активности активатора плазминогена (ген pla плазмиды pYP). Белки Yop во многом определяют вирулентность Y. pestis. YopE-белок обладает антифагоцитарным и цитотоксическим действием. YopD обеспечивает проникновение YopE в клетку-мишень; YopH обладает антифагоцитарной и протеин-тирозин-фосфатазной активностью; белок YopN – свойствами кальциевого сенсора; YopM связывается с ?-тромбином крови человека.
Эпидемиология. Круг теплокровных носителей чумного микроба чрезвычайно обширен и включает более 200 видов 8 отрядов млекопитающих. Основным же источником чумы в природе являются грызуны и зайцеобразные. Естественная зараженность установлена у более чем 180 их видов, свыше 40 из них входят в состав фауны России и сопредельных территорий (в пределах бывшего СССР). Из 60 видов блох, для которых в экспериментальных условиях установлена возможность переноса возбудителя чумы, на этой территории обитают 36.
Основные (главные) носители Y. pestis на территории России и Средней Азии – суслики, песчанки и сурки, в некоторых очагах также пищухи и полевки. С ними связано существование следующих очагов чумы:
1) 5 очагов, в которых основным носителем чумного микроба выступает малый суслик (Северо-Западный Прикаспий; Терско-Сунженское междуречье; Приэльбрусский очаг; Волго-Уральский и Зауральский полупустынные очаги).
2) 5 очагов, в которых носители – суслики и сурки (на Алтае – пищухи): Забайкальский, Горно-Алтайский, Тувинский и высокогорные Тянь-Шанский и ПамироАлайский очаги.
3) Волго-Уральский, Закавказский и Среднеазиатский пустынные очаги, где основные носители – песчанки.
4) Высокогорные Закавказский и Гиссарский очаги с основными носителями – полевками.
Разные классификации Y. pestis основываются на разных группах признаков – биохимических особенностях (глицерин-позитивные и глицерин-негативные варианты), области распространения (океанические и континентальные варианты), видах основных носителей (крысиный и сусликовый варианты). По одной из наиболее распространенных классификаций, предложенной в 1951 г. французским исследователем чумы Р. Девинья (R. Devignat), в зависимости от географического распространения возбудителя и его биохимических свойств различают три внутривидовые формы (биовара) Y. pestis (табл. 28).
По классификации отечественных ученых (Саратов, 1985), вид Y. pestis разделен на 5 подвидов: Y. pestis subsp. pestis (основной подвид; он включает все три биовара классификации Р. Девинья), Y. pestis subsp. altaica (алтайский подвид), Y. pestis subsp. caucasica (кавказский подвид), Y. pestis subsp. hissarica (гиссарский подвид) и Y. pestis subsp. ulegеica (улэгейский подвид).
Заражение человека происходит через укус блох, при прямом контакте с заразным материалом, воздушно-капельным, редко алиментарным путем (например, при употреблении мяса верблюдов, больных чумой). В 1998 – 1999 гг. чумой в мире переболело 30 534 человека, из них 2 234 умерли.
Дифференциальные признаки биоваров Y. pestis
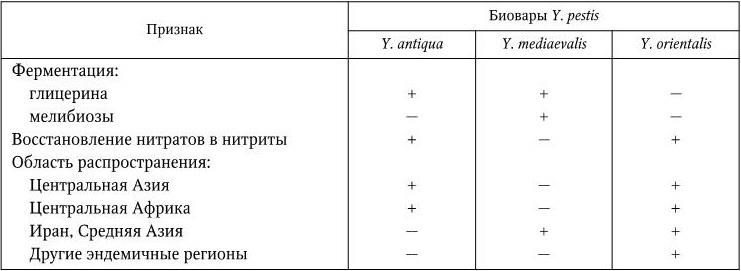
Примечание. (+) – признак положительный; ( – ) – признак отсутствует.
Постинфекционный иммунитет прочный, пожизненный. Повторные заболевания наблюдаются крайне редко. Природа иммунитета клеточная. Хотя антитела появляются и играют определенную роль в приобретенном иммунитете, он опосредуется главным образом Т-лимфоцитами и макрофагами. У лиц, переболевших чумой или вакцинированных, фагоцитоз имеет завершенный характер. Он и обусловливает приобретенный иммунитет.
Лабораторная диагностика. Используются бактериоскопический, бактериологический, серологический и биологический методы, а также аллергическая проба с пестином (для ретроспективной диагностики). Материалом для исследования служат: пунктат из бубона (или его отделяемое), мокрота, кровь, при кишечной форме – испражнения. Y. pestis идентифицируют на основании морфологии, культуральных, биохимических признаков, пробы с чумным фагом и с помощью биологической пробы. Простым и надежным методом определения антигенов чумной палочки в исследуемом материале является применение РПГА, особенно с использованием эритроцитарного диагностикума, сенсибилизированного моноклональными антителами к капсульному антигену, и ИФМ. Эти же реакции могут быть использованы для обнаружения антител в сыворотке больных.
Биологический метод диагностики заключается в заражении исследуемым материалом (когда он очень загрязнен сопутствующей микрофлорой) морской свинки накожно, подкожно или, реже, внутрибрюшинно.
При работе с материалом, содержащим возбудителя чумы, требуется соблюдение строгого режима, поэтому все исследования проводятся только хорошо обученным персоналом в специальных противочумных учреждениях.
Профилактика. Постоянный контроль за природными очагами чумы и организация мероприятий по предупреждению заболеваний людей в стране осуществляется специальной противочумной службой. Она включает в себя пять противочумных институтов и десятки противочумных станций и отделений.
Несмотря на наличие природных очагов, с 1930 г. на территории России в них не было ни одного случая заболевания людей чумой. Для специфической профилактики чумы используется живая ослабленная вакцина из штамма EV. Она вводится накожно, внутрикожно или подкожно. Кроме того, предложена сухая таблетированная вакцина для перорального применения. Поствакцинальный иммунитет формируется к 5 – 6-му дню после прививки и сохраняется в течение 11 – 12 мес. Для его оценки и ретроспективной диагностики чумы предложена внутрикожная аллергическая проба с пестином. Реакция считается положительной, если на месте введения пестина через 24 – 48 ч образуется уплотнение не менее 10 мм в диаметре и появляется краснота. Аллергическая проба положительна и у лиц, имеющих постинфекционный иммунитет.
Таксономия: Y.pestis вызывает чуму; отдел Gracilicutes, семейство Enterobacteriaceae, род Yersinia. Возбудитель – Yersinia pestis.
Морфологические свойства: грамотрицательные палочки, овоидной формы, окрашиваются биполярно. Подвижны, имеют капсулу, спор не образуют.
Факультативные анаэробы. Температурный оптимум +25С. Хорошо культивируются на простых питательных средах. Ферментируют большинство углеводов без образования газа. Психофилы - способны менять свой метаболизм в зависимости от температуры и размножаться при низких температурах. Вирулентные штаммы образуют шероховатые (R) колонии, переходные (RS) и сероватые слизистые гладкие авирулентные(S) формы.
Два типа колоний - молодые и зрелые. Молодые с неровными краями. Зрелые колонии крупные, с бурым зернистым центром и неровными краями. На скошенном агаре черед двое суток при +28 С образуют серовато - белый налет, врастающий в среду, на бульоне - нежную поверхностную пленку и хлопковидный осадок.
Биохимические свойства: фенментативная активнсть высокая: ферментация до кислоты ксилозу, синтез плазмокоагулазы, фибринолизина, гемолизина, лецитиназу, сероводород. Рамнозу, мочевину не ферментирует.
Группа белково - полисахаридных и липополисахаридных антигенов: термостабильный соматический О-антиген и термолабильный капсульный V,W антигены. С W-антигеном связывают вирулентность бактерий. Продуцирует факторы патогенности: фибринолизин, плазмокоагулазу, эндотоксин, экзотоксин, капсулу, V,W антигены.
Резистентность: чувствителен к антибиотикам (особенно стрептомицин), нестоек к окружающей среде при высокой температуре.
Обладает патогенным потенциалом, подавляет функции фагоцитарной системы, подавляет окислительный взрыв в фагоцитах и беспрепятственно в них размножается. Факторы патогенности контролируются плазмидами трех классов. В патогенезе выделяют три основных стадии - лимфогенного заноса, бактеремии, генерализованной септицемии. Имеют адгезины и инвазины, низкомолекулярные протеины (ингибируют бактерицидные факторы), энтеротоксин. Часть факторов контролируется плазмидами вирулентности.
Клинические особенности: Инкубационный период – несколько часов до 8 сут. Различают локальные – кожно-бубонная, бубонная; внешне-диссеминированные – первично-легочная, вторично-легочная и кишечная; генерализованная – первично-септическая, вторично-септическая формы чумы. Региональная лимфоаденопатия, энтероколиты, реактивные артриты, спондилит, лихорадка.
Эпидемиология: Чума - классический природноочаговый зооноз диких животных. Основные носители в природе - сурки, суслики, в городских условиях - крысы. В передаче возбудителя - блохи животных, способные заражать человека.
Иммунитет: клеточно-гуморальный, ограничен по длительности и напряженности.
Микробиологическая диагностика:
Бактериоскопическое исследование. Из исследуемого материала готовят мазки, окрашивают по Граму и водным раствором метиленового синего. Бактерии чумы представляют собой грамотрицательные палочки овоидной формы Бактериологическое исследование. Исследуемый материал засевают на чашки с питательным агаром. Посевы инкубируют при 25С. Первичное изучение посевов производят через 10ч. К этому сроку появляются колонии, которые образованы вирулентными R-формами. Мало- и авирулентные бактерии формируют S-формы колоний. Идентификацию чистой культуры проводят по морфологии бактериальных клеток, характеру роста, антигенным и биохимическим свойствам, чувствительности к специфическому фагу и биопробе.
На бульоне бактерии образуют пленку; ферментируют многие сахара до кислоты, индола не образуют, желатин не разжижают. Содержат групповой термостабильный соматический антиген и специфический термолабильный капсульный антиген.
Биопроба. Проводится для выделения чистой культуры из материала, загрязненного посторонней микрофлорой. Наиболее чувствительными лабораторными животными являются морские свинки, которым материал вводят подкожно. Внутрибрюшинно материал вводят в том случае, если он не загрязнен другими бактериями. После гибели животных отмечают патологические изменения органов и проводят бактериологическое исследование
Экспресс-методы лабораторной диагностики:
1.Иммунофлюоресцентный метод позволяет обнаружить присутствие возбудителя как в патологическом материале, так и в объектах окружающей среды (вода, воздух), а также в пищевых продуктах и эктопаразитах. С этой целью используют люминесцентную видоспецифическую противочумную сыворотку, люминесцентные противокапсульную и противосоматическую сыворотку.
2.РПГА - для обнаружения антигенов бактерий в материале с помощью стандартной противочумной сыворотки, антитела которой нагружены на эритроциты.
Лечение: антибиотики –стрептомицин, препараты тетрациклинового ряда.
Профилактика: специфическая профилактика - живая ослабленная чумная вакцина EV. Имеется сухая таблетированная вакцина для перорального применения. Для оценки иммунитета к чуме (естественного постинфекционного и вакцинального) может применяться внутрикожная аллергическая проба с пестином.

Обзор
Автор
Редактор

Один монах, странствуя по белому свету, встретил Чуму, которая направлялась в его город.
— Ты куда это направляешься, Чума? — спросил он ее.
— Иду в твой родной город, — ответила она. — Мне нужно забрать там тысячу жизней.
Через некоторое время монах снова встретил Чуму на своем пути.
— Почему ты меня обманула тогда? — спросил он ее с укором. — Ты говорила, что должна забрать тысячу жизней, а забрала пять тысяч.
— Я тогда сказала тебе правду, — ответила Чума. — Я действительно забрала тысячу жизней. Остальные умерли от страха.
Жертвы чумы исчислялись сотнями тысяч и даже миллионами человек, вымирали города, становились безлюдными целые области, и ужас пандемий чумы затмевал ужасы всех войн, какие знала история человечества. Целые тысячелетия люди не понимали, что является источником заболевания [2].
Библия — одно из древнейших дошедших до нас свидетельств эпидемий чумы (1 книга Царств, глава 5; 4 книга Царств, глава 19, стихи 35–36). В мировой истории отмечают три пандемии этой болезни:
Бубонная форма чумы является наиболее распространенной формой заболевания и при отсутствии лечения приводит к гибели 40–60% заболевших. Легочная форма возникает либо как осложнение бубонной или септической форм, либо при вдыхании воздуха, зараженного возбудителем чумы. Если лечение не начинают в первые 24 часа после появления симптомов, смерть наступает через 48 часов [8].
В природе чумной микроб встречается практически на всех континентах, исключая Австралию, Антарктиду, а также Арктику, что обусловливает ежегодно регистрируемые случаи этой болезни. Стремительная эволюция микроорганизмов приводит к появлению популяций бактерий (штаммов), устойчивых к антибиотикам [9], что в случае с возбудителем чумы особенно опасно. Кроме того, этих бактерий могут использовать в качестве агента биотерроризма. Все вышесказанное объясняет необходимость изучения чумного микроба.
Возбудитель чумы Yersinia pestis — самая опасная бактерия в мире [10]. Что делает ее столь смертоносной?
Факторы вирулентности, или вооружен и очень опасен
Со времен открытия возбудителя чумы в 1894 году французом Александром Йерсеном и японцем Китасато Сибасабуро ученые пытались выяснить, что определяет патогенность Y. рestis. В результате многолетней тяжелой и рискованной работы, которая продолжается и по сей день, выделили следующие факторы патогенности возбудителя:
- белки внешней мембраны (Yersinia outer proteins — называемые Yop-белками, эффекторными белками, или комплексом Yop-вирулона) [11];
- комплекс области пигментации [12];
- активатор плазминогена [13];
- капсульный антиген [14];
- пили адгезии или pH6-антиген [15].
Белки внешней мембраны, или зачем возбудителю чумы шприц?

Рисунок 1. Схема действия системы секреции III типа.
Комплекс области пигментации, или может ли стать потребность в чем-либо фактором патогенности?
Активатор плазминогена, или двуликий Янус
При вдыхании чумных микробов (и развитии легочной чумы) этот белок обеспечивает быстрое размножение бактерий в тканях легких и приводит к развитию молниеносной пневмонии и отеку легких, тогда как в отсутствии Pla инфекция не развивается в смертельную пневмонию. Установлено, что активатор плазминогена нарушает постоянство внутренней среды организма хозяина и блокирует иммунные реакции, направленные на уничтожение патогена [27].
Капсульный антиген, или скользкий тип этот возбудитель чумы
Бактерии окружены капсулой из слизистого вещества (фракция I, Fra1), которая препятствует поглощению и обезвреживанию Y. pestis иммунными клетками организма-хозяина в процессе фагоцитоза. На выявлении этого вещества-антигена основаны многие современные методы лабораторной диагностики чумы, оно входит в состав многих экспериментальных химических вакцин против чумы. Однако позднее обнаружили популяции бактерий, лишенные капсулы [28]. Кроме того, слизистая капсула есть у многих других микроорганизмов, например, возбудителя сибирской язвы, туляремии. Капсульное вещество иерсинии образуют при температуре 37 °С.
Антигены, схожие с рН6, были обнаружены у ряда возбудителей, вызывающих менее опасные болезни — кишечные инфекции (Y. pseudotuberculosis [31], Y. enterocolitica [32], Escherichia coli [8]).
Температурный фактор, или то, что действительно имеет значение
Необходимо заострить внимание на особой роли температуры в физиологии чумного микроба. Именно при температуре 37 °С у него повышаются питательные потребности [33] и синтезируются практически все известные детерминанты вирулентности (рис. 2) [34]. У других бактерий подобная зависимость выражена в меньшей степени, что позволяет говорить о ведущей роли температурного фактора в вирулентности возбудителя чумы [8].
Геном или все важное внутри
Помимо хромосомы у чумного микроба есть плазмиды — внехромосомные участки ДНК [38]. Большинство белковых факторов вирулентности закодированы на плазмидах: эффекторные белки на плазмиде pCad; капсула — pFra; активатор плазминогена — рPla (pPst, pPCP). Плазмиды pFra и рPla обнаружены только у Y. pestis (видоспецифические), pCad является общей с возбудителем псевдотуберкулеза (родоспецифическая) [20].
Заключение
В настоящее время продолжается работа по выявлению новых, еще не изученных маркеров вирулентности [39]. С использованием 2D-электрофореза, масс-спектрометрии, полногеномного секвенирования проводят сравнительный анализ отличающихся по вирулентности популяций чумного микроба для выявления различий в их белковых спектрах и геномных последовательностях. Ранее не известные белки и участки генома становятся объектом пристального внимания и изучения как потенциальные детерминанты вирулентности.
Таким образом, патогенность возбудителя чумы — это множественный (полидетерминантный) признак. Соединение многих факторов в единое целое создает страшную угрозу чумных эпидемий, с противостоянием которым, однако, прогрессивное человечество успешно справляется.
К 120-летию открытия А. Йерсеном и Ш. Китазато микроба чумы Yersinia pestis
Об авторе
Виктор Васильевич Сунцов — доктор биологических наук, ведущий научный сотрудник Института проблем экологии и эволюции им. А. Н. Северцова РАН. Занимается изучением происхождения и эволюции возбудителей природноочаговых инфекций, в частности чумы.
Диаграмма публикаций по проблеме чумы, фиксирующая скачок их числа с 2003 г.
Немного истории
Карта распространения чумы в Европе. Пандемия, начавшаяся в центральных районах Азии, достигла берегов Черного моря в 1347 г.
Когда появился микроб чумы?
Доказанное в 1980 г. молекулярными методами непосредственное родство псевдотуберкулезного (Y. pseudotuberculosis) и чумного (Y. pestis) микробов привело к выводу об их недавней дивергенции, правда, без указания времени и места, когда именно и где это случилось [5]. Высокое сходство их геномов позволяло некоторым авторам даже объединить их в один вид в качестве отдельных подвидов, хотя вызывают они совершенно разные болезни. И псевдотуберкулезного, и чумного микробов относят к семейству Enterobacteriaceae — возбудителям кишечных инфекций, но последний, будучи паразитом крови, не имеет к ним никакого отношения. У него иная адаптивная среда, и в принципе его нужно отнести к другому семейству [3].
Микрофотография чумной палочки. Увел. ×200. Фото с сайта cdc.gov
Идея недавнего отделения чумного микроба от псевдотуберкулезного была неожиданной, но отнюдь не новой. В 1950–1970-х годах такие мысли высказывали В. Н. Беклемишев, В. А. Бибикова, А. И. Дятлов, Л. Н. Классовский, В. С. Петров, Н. М. Хрусцелевская. Но тогда подобные интуитивные ощущения эволюционной молодости возбудителя чумы выглядели теоретически чуждыми, паранаучными и деструктивными, поэтому они не нашли поддержки у ортодоксов.
Головокружение от успехов
В современных исторических реконструкциях в биологии доминирует новая филогенетика (молекулярная филогенетика, генофилетика). Отчасти это лидерство оправдано широкими возможностями, которые предоставляют молекулярные структуры и компьютерные технологии филогенетических построений, позволяющие сравнивать и обрабатывать миллионы признаков, — таких, как последовательности нуклеотидов. Все составляющие новой филогенетики полезны, они необходимы для создания естественных филогенетических схем, но недостаточны, особенно в отношении прокариот. Молекулярная генетика — молодая наука, и закономерности молекулярной эволюции пока не вполне ясны. Филогении можно выстраивать только по гомологичным признакам, а их выявление, в том числе и на молекулярном уровне, представляет немалую проблему. Выводы на основе применения разных молекулярно-генетических методов далеко не однозначны, порой не согласуются между собой и с данными других наук: экологии, биогеографии, микробиологии и др. Такая обескураживающая разноголосица свойственна и заключениям в отношении микроба чумы.
Происхождение Yersinia pestis: взгляд натуралиста
Знание экологии монгольского сурка и его блох позволяет понять селективные (адаптационные) процессы, проходившие в микробных популяциях в природе, и причинно-следственные связи в эволюционных филумах. Появление возбудителя чумы в Центральной Азии предопределили два природных фактора: аридность горно-степных ландшафтов, постепенно увеличивающаяся с олигоцена-миоцена, и максимальное похолодание в сартанское время последнего оледенения. Проще говоря, индуктором видообразования микроба чумы был сухой и холодный климат Центральной Азии в конце ледниковой эпохи. Кроме того, в возникновении чумного микроба важную роль играет физиология, точнее поведение монгольского сурка, связанное с устройством зимовочной пробки, а также особенности сурочьей блохи O. silantiewi.
В Центральной Азии, в горно-степных поселениях сурка тарбагана влажность почвы очень низкая, всего 2–7% [3], а грунт в зимовочной норе зверька сухой и щебнистый. Изготовить из него земляную пробку внутри норы, в вертикальном лазе диаметром 15–20 см, все равно, что замазать сухим песком отверстие в потолке размером с футбольный мяч. Из-за дефицита почвенной влаги у монгольского сурка выработалось специфичное поведение. При залегании в спячку он устраивает зимовочную пробку из специально подготавливаемой смеси мелкозема, щебня и влажных каловых масс, которые летом собираются в отнорках (уборных). Для перетаскивания камней, обвалянных в фекалиях, сурки используют зубы, при этом частицы фекалий, а с ними и возбудитель псевдотуберкулеза, попадают в ротовую полость. Итак, во рту спящих тарбаганов — экскременты, а в них — кишечный паразит, микроб псевдотуберкулеза!
Монгольский сурок тарбаган и его зимовочная (постоянная) нора. Вверху: зимовочная пробка, состоящая из смеси мелкозема, щебня и цементирующих их экскрементов (1); гнездовая камера (2); отнорки-уборные, в которых в летние месяцы сурки накапливают строительную смесь (3). Внизу: слой мелкозема и щебня (а); и коренные породы (б), приведены температуры грунта и спящих сурков во время раскопки (февраль 1979 г.)
Сурки — типичные семейно-колониальные животные. Группировки из 2–22 разновозрастных и разнополых зверьков совместно зимуют в одной постоянной, или зимовочной, норе. У каждого зверька в течение зимней спячки более длительные периоды глубокого сна (торпора) чередуются с короткими периодами бодрствования (эутермии). В торпорной фазе температура тела снижается до 2–5°C, в эутермной может достигать нормальной, у активных сурков — около 37°С. За осенне-зимне-весеннее время сурки не вполне синхронно просыпаются до 15 раз, примерно дважды в месяц. Таким образом, каждый зверек в течение периода подземной жизни имеет два гомеостатических состояния, между которыми лежит промежуток физиологической гетеротермии. Отсюда следствие: блохи в холодное время года питаются на сурках, температура тела которых лежит в диапазоне 5–37°C. Обратим внимание на непрерывность температур!
В 1970-х годах в тувинском очаге чумы, расположенном в Центральной Азии, мы изучали зимнюю спячку тарбагана. В феврале-марте, во время максимального зимнего промерзания грунта (до глубины более 2 м), раскопали три зимовочных норы. Из них изъяли восемь глубоко спящих и девять проснувшихся активных зверьков, среди которых были молодые, полувзрослые и взрослые особи. Из их шерсти собрали 230 личинок O. silantiewi, 60 живых и 452 пустых коконов, а из ротовой полости торпидных зверьков — дополнительно 20 личинок. Пустые коконы (от 4 до 87) обнаружили также на 22 зверьках, отловленных в первые две недели после весеннего пробуждения.
Тувинский природный очаг чумы, Монгун-Тайгинский мезоочаг. Снеговое покрытие в зимне-весенние месяцы не превышает 30–40%, грунт промерзает на глубину более 2 м к началу января, а оттаивает в июле
Отметим распределение коконов на шерсти: большая часть прикреплена на голове, у основания хвоста и на наружной стороне задних ног. Все личинки, извлеченные из ротовой полости, оказались с кровью и увеличенными в размерах за счет развития жирового тела, что свидетельствовало о полноценности пищи и об их готовности к окукливанию. У спящих зверьков поврежденная личинками слизистая ротовой полости и язык обильно кровоточили, изо рта заметно выступала кровяная пена, а рот, зубы, лапы были обильно испачканы экскрементами (следами устройства зимовочной пробки осенью). Незарубцевавшиеся раны в ротовой полости мы наблюдали у всех сурков, отловленных после выхода из нор в конце марта и начале апреля, что говорит о массовости описываемого явления, его общепопуляционном характере.
Отсюда понятна причина концентрации пустых коконов на голове, хвосте и наружной стороне задних ног у спящих и недавно пробудившихся сурков тарбаганов. Зимой грунт промерзает глубже гнездовых камер, и личинки переходят из гнездовой выстилки на более теплые тела спящих зверьков. При этом некоторые личинки, произвольно перемещаясь в шерсти, попадают в ротовую полость сурка, где, питаясь на слизистой, травмируют ее. Перед окукливанием личинки покидают ротовую полость и прикрепляются к шерсти близ рта. Зная позу свернувшегося в шар спящего сурка, у которого нос уткнулся в анус, а задние ноги прижаты к щекам, легко предсказать места прикрепления коконов.
На основе новых эколого-географических, палеоклиматических и генетических данных можно сформулировать основные постулаты теории происхождения и мировой экспансии микроба чумы.
Происхождение, естественное распространение в Евразии и антропогенная мировая экспансия микроба Y. pestis во время первой (I), второй (II) и третьей (III) пандемий. 1 — южная граница зоны многолетнемерзлых грунтов; 2 — граница доминантного распространения в природе микроба Y. pseudotuberculosis O:1b; 3 — ареал сурка-тарбагана, район происхождения микроба чумы; 4 — первичные природные очаги; 5 — вторичные природные очаги; gly + (gly − ) — способность (неспособность) штаммов ферментировать глицерин
Предковая форма возбудителя чумы — микроб псевдотуберкулеза 1-го серотипа (Y. pseudotuberculosis O:1b), который доминирует в северо-центрально-азиатских и дальневосточных районах с суровым климатом.
Метаморфоза микроба псевдотуберкулеза в чумную бактерию произошла в конце позднего плейстоцена. За весь четвертичный период глубокое промерзание грунта (2 м и более) в Центральной Азии отмечено только в сартанское время позднего плейстоцена и в голоцене, т. е. не ранее 22 тыс. лет назад [10].
В ультраконтинентальном районе зимнего антициклона в Центральной Азии личинки блох, паразитирующие на монгольском сурке тарбагане, зимой переходят к факультативной гематофагии, что приводит к устойчивому контакту крови сурков с псевдотуберкулезным микробом [3].
Теперь уже можно легко представить, как сапрозоонозный кишечный псевдотуберкулезный микроб постепенно эволюционировал в облигатный паразит крови незимоспящих грызунов: экскременты тарбагана → спящий сурок → активный сурок → незимоспящий грызун.
Знание молекулярно-генетических, популяционных и биоценотических факторов, а также их многообразных связей позволяет выделить в эволюционной истории возбудителя чумы основные вехи.
IV. Во время третьей пандемии с корабельными крысами микроб уже другого подвида (orientalis) из Азии вновь проник в Африку и впервые на быстроходных морских судах добрался до Нового Света, где закрепился в виде вторичных природных очагов в популяциях земляных белок, луговых собачек, полевок, морских свинок.
В поисках согласия
Экологический сценарий происхождения, эволюции и мировой экспансии возбудителя чумы весьма заметно расходится с гипотезами, построенными на основе генетических данных. Где же истина? Какой из них достоин большего одобрения?
В пользу экологического сценария говорит следующее:
Такие аргументы делают этот экологический сценарий наиболее правдоподобным в сравнении с другими, позволяют принять его за исходную гипотезу и наполнять его генетическими признаками. Биологическое содержание сценария, понятное широкому кругу исследователей, дает существенные гносеологические преимущества перед слишком редуцированными историческими реконструкциями. К примеру, некоторые авторы из-за сходства отдельных генетических признаков у кавказского подвида Y. pestis caucasica и псевдотуберкулезного микроба считают Кавказ родиной чумы и выстраивают соответствующую филограмму [11, 12]. Но на Кавказе, в относительно теплом климатическом регионе, нет псевдотуберкулезного микроба 1-го серотипа или он встречается крайне редко! Истоки чумы следует искать в холодных, суровых краях — как в предложенном сценарии.
Несмотря на разительное несходство экологической и генетической филогений, между ними нет непреодолимой пропасти, более того, есть безусловные точки соприкосновения. Экологический сценарий для молекулярных и генетических признаков очерчивает диапазон генетической изменчивости микробной популяции, вступившей на путь видообразования, выделяет рамки экологической достоверности генетических фактов, привлекаемых для филогенетических выводов [3, 13].
Читайте также:

