Синтез коллагеновых волокон кратко
Обновлено: 02.07.2024
Свидетельство и скидка на обучение каждому участнику
Зарегистрироваться 15–17 марта 2022 г.
Министерство образования и науки Российской Федерации
федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
Институт Естествознания и Экономики
ПО ДИСЦИПЛИНЕ
БИОЛОГИЧЕСКАЯ ХИМИЯ
Коллаген – главный белок соединительной ткани
Направление подготовки: 050100 Педагогическое образование
Профиль подготовки: Биология
Форма обучения: очная
Доцент кафедры химия
Коллаге́н — фибриллярный белок, составляющий основу соединительной ткани организма (сухожилие, кость, хрящ, дерма и т. п.) и обеспечивающий её прочность и эластичность. Коллаген обнаружен у многоклеточных животных; отсутствует у растений, бактерий, вирусов, простейших и грибов. Коллаген - основной компонент соединительной ткани и самый распространённый белок у млекопитающих, составляющий от 25 % до 35 % белков во всём теле, т.е. 6% массы тела. Название "коллаген" объединяет семейство близкородственных фибриллярных белков, которые являются основным белковым элементом кожи, костей, сухожилий, хряща, кровеносных сосудов, зубов. В разных тканях преобладают разные типы коллагена, а это, в свою очередь, определяется той ролью, которую коллаген играет в конкретном органе или ткани.
Молекула коллагена (тропоколлагена) построена из трех пептидных цепей, каждая из которых содержит около 1000 аминокислотных остатков. Необычен аминокислотный состав коллагена: каждая третья аминокислота – это глицин, 20 % составляют остатки пролина и гидроксипролина, 10 % - аланина, остальные 40 % представлены всеми другими аминокислотами. Коллаген – единственный белок, в котором содержится гидроксипролин. Эта аминокислота получается путем гидроксилирования части остатков пролина уже после образования пептидных цепей.
Коллаген – сложный белок, гликопротеин: содержит моносахаридные (галактозильные) и дисахаридные (галактозилглюкозильные) остатки, соединенные с гидроксильными группами некоторых остатков оксилизина.
Учёные десятилетиями не могли понять молекулярное строение коллагена. Первое доказательство того, что коллаген имеет постоянную структуру на молекулярном уровне, было представлено в середине 30-х годов прошлого века. С того времени много выдающихся учёных, включая Нобелевских лауреатов, таких как Фрэнсис Крик, Лайнус Полинг, Александр Рич, Ада Йонат, Хелен Берман, Вилеайнур Рамачандран работали над строением мономера коллагена.
Коллаген синтезируют и поставляют в межклеточный матрикс почти все клетки (фибробласты, хондробласты, остеобласты, одонтобласты, цементобласты, кератобласты и др.). Синтез и созревание коллагена является сложным многоэтапным процессом, который начинается в клетке и заканчивается в межклеточном матриксе. Нарушения синтеза коллагена, обусловленные мутацией в генах, а также в процессе трансляции и пост- трансляционной модификации сопровождаются появлением дефектных коллагенов. Поскольку около 50% всех коллагеновых белков содержатся в тканях скелета, а остальные 40% в дерме и 10% в строме внутренних органов, то нарушения синтеза коллагена сопровождаются патологией как костно-суставной системы, так и внутренних органов.
Синтез коллагена включает два этапа. На внутриклеточном этапе происходит трансляция и посттрансляционная модификация полипептидных цепей, и на внеклеточном - модификации белка, завершающаяся образованием коллагеновых волокон (рис.1).
Внутриклеточный этап синтеза коллагена. Пептидные α-цепи коллагена синтезируются на полирибосомах, связанных с мембранами эндоплазматической сети. Её синтезированные пептидные цепи в цистернах подвергаются посттрансляционной модификации, которая включает:
• удаление сигнального пептида проколлагеновой цепи при участии специфической протеиназы;
• гидроксилирование остатков пролина и лизина, которое начинается в период трансляции полипептидной цепи вплоть до её отделения от рибосом.
Реакции гидроксилирования катализируют оксигеназы. В реакции гидроксилирования используются О2 и 2-оксоглутарат, а в качестве кофактора участвует аскорбиновая кислота. Гидроксилазы пролина и лизина в активном центре содержат Fе2+, а аскорбиновая кислота, которая легко окисляется в дегидроаскорбиновую кислоту, необходима для сохранения атома железа в ферроформе (рис.2). В реакциях гидроксилирования один атом кислорода присоединяется к четвёртому атому углерода в остатке пролина, а второй атом кислорода включается в янтарную кислоту, которая образуется при декарбоксилировании 2-оксоглутарата (рис.3).
Наряду с гидроксилированием пролина происходит гидроксилирование остатков лизина с образованием 5-гидроксилизина. В дальнейшем гидроксилированные остатки лизина подвергаются гликозилированию(рис.4).
При участии гликозилтрансфераз образуются ковалентные О-гликозидные связи между 5-ОН группой гидроксилизина и остатком галактозы или дисахаридом галактозилглюкозой. К амидной группе аспарагина присоединяются молекулы N-ацетилглюкозамина или маннозы. Одновременно с гидроксилированием пролина формируется стабильная трёхспиральная структура коллагена. Из эндоплазматической сети молекулы проколлагена перемещаются в аппарат Гольджи, где они включаются в секреторные пузырьки и в их составе секретируются во внеклеточное пространство (рис.5).
Внеклеточный этап - модификация молекул проколлагена. В межклеточном пространстве при участии протеолитических ферментов от молекулы проколлагена отщепляются N- и С-концевые пептиды и освобождается тройная спираль коллагена (тропоколлагена). Далее происходит процесс самосборки коллагеновых фибрилл, фиксированных межмолекулярными ковалентными связями (сшивками). В формировании этих связей участвуют остатки лизина и 5-гидроксилизина и их альдегидные производные, которые образуются вследствие окислительного дезаминирования. Окислительное дезаминирование лизина и 5-гидроксилизина происходит с участием лизилоксидазы. Особенностью этого фермента является присутствие Cu2+ в активном центре. Молекулы лизилоксидазы синтезируются в клетке в виде проферментов и после связывания с ионами Cu2+ упаковываются в везикулы, которые покидают клетку. На клеточной поверхности молекула пролизилоксидазы подвергается ограниченному протеолизу и в сфор- мировавшемся активном центре при участии ионов Cu2+ происходит окисление остатка тирозина до тирозинхинона. Образовавшаяся в активном центре хиноидная структура связывает остатки лизина в молекуле проколлагена с образованием фермент-субстратного комплекса (рис.6).
На следующем этапе аллизин и 5-гидроксиаллизин конденсируются вместе с лизиловыми и гидроксилизиловыми остатками; формируются внутри- и межмолекулярные поперечные связи. В реакции конденсации аллизина с остатком лизина другой цепи образуется основание Шиффа. В случае альдольной конденсации двух остатков аллизина образуются альдольные межмолекулярные связи (лизиннорлейцин) (рис.7).
Альдольная конденсация характерна для коллагена костной ткани и дентина, а основания Шиффа наиболее часто встречаются в коллагенах сухожилий.
Около 25% молекул тропоколлагена распадается, не образуя фибрилл. Получившиеся фрагменты выполняют сигнальные функции и стимулируют коллагеногенез. Пространственная организация фибрилл завершается при участии фибронектина, протеогликанов и коллагенов, ассоциированных с фибриллами.
Коллаген - ярко выраженный полиморфный белок. В настоящее время известно 19 типов коллагена, которые отличаются друг от друга по первичной структуре пептидных цепей, функциям и локализации в организме. Вариантов α-цепей, образующих тройную спираль, гораздо больше 19 (около 30). Для обозначения каждого вида коллагена пользуются определённой формулой, в которой тип коллагена записывается римской цифрой в скобках, а для обозначения α-цепей используют арабские цифры: например коллагены II и III типа образованы идентичными α-цепями, их формулы, соответственно [α1(II)]3 и [α1(III)]3; коллагены I и IV типов являются гетеротримерами и образуются обычно двумя разными типами α-цепей, их формулы, соответственно [α1(I)]2α2(I) и [α1(IV)]2α2(IV). Индекс за скобкой обозначает количество идентичных α-цепей (табл. 1).
Гены коллагена называются соответственно типам коллагена и записываются арабскими цифрами, например COL1 - ген коллагена I типа, COL2 - ген коллагена II типа, COL7 - ген коллагена VII типа и т.д. К этому символу приписываются буква А (обозначает α-цепь) и арабская цифра (обозначает вид a-цепи). Например, COL1A1 и COL1A2 кодируют, соответственно, α1 и α2-цепи коллагена I типа.
Молекула коллагена представляет собой правозакрученную спираль из трёх α-цепей. Такое образование известно под названием тропоколлаген. Один виток спирали α-цепи содержит три аминокислотных остатка. Молекулярная масса коллагена около 300 кДа, длина 300 нм, толщина 1,5 нм.
Коллаген относится к тем немногим белкам животного происхождения, которые содержат остатки нестандартных аминокислот: около 21 % от общего числа остатков приходится на 3-гидроксипролин, 4-гидроксипролин и 5-гидроксилизин. Каждая из α-цепей состоит из триад аминокислот. В триадах третья аминокислота всегда глицин, вторая — пролин или лизин, первая — любая другая аминокислота, кроме трёх перечисленных.
Выделяют 19 типов коллагена, которые подразделяют на несколько классов в зависимости от того, какие структуры они могут образовывать.
95% всего коллагена в организме человека составляют коллагены I, II и III типов, которые образуют очень прочные фибриллы. Значительное содержание именно этих типов коллагена объясняется тем, что они являются основными структурными компонентами органов и тканей, которые испытывают постоянную или периодическую механическую нагрузку (кости, сухожилия, хрящи, межпозвоночные диски, кровеносные сосуды), а также участвуют в образовании стромы паренхиматозных органов. Поэтому коллагены I, II и III типов часто называют интерстициальными. К классу фибриллообразующих относят также минорные коллагены V и XI типов (рис.8).
Этот класс объединяет коллагены, которые выполняют очень важную функцию: они ограничивают размер фибрилл, образуемых интерстициальными коллагенами (прежде всего, I и II типов), и участвуют в организации межклеточного матрикса в костях, коже, хрящах, сухожилиях. К этим коллагенам относят коллагены IX, XII, XIV и XVI типов. Коллагены этого класса сами фибрилл не формируют, но непосредственно связаны с фибриллами, которые образуют интерстициальные коллагены.
К этому классу относят коллагены IV, VIII, X типов. Особенности строения и функционирования таких белков можно рассмотреть на примере наиболее изученных к настоящему времени коллагенов IV и VIII типов.
Коллаген IV типа является ключевым структурным компонентом базальных мембран, которые представляют собой особую форму межклеточного матрикса. Его секретируют различные типы клеток: эпителиальные, эндотелиальные, мышечные, нервные, жировые. Особенностью коллагена IV типа является то, что повторяющиеся спирализованные участки с последовательностью (Гли-х-у)nчасто прерываются короткими неспиральными сегментами. Это, вероятно, увеличивает гибкость коллагена IV типа и способствует образованию на его основе сетчатых структур (рис.9).
К этому классу относят коллаген VI типа, который является короткоцепочечным белком. Он образует микрофибриллы, которые располагаются между крупными фибриллами интерстициальных коллагенов. Этот коллаген широко представлен в хрящевом матриксе, но больше всего его содержится в межпозвоночных дисках: в nucleus pulposus он составляет -20% общего коллагена. Две молекулы этого коллагена соединяются антипараллельно с образованием димера. Из димеров образуются тетрамеры, которые секретируются из клетки, и вне клетки связываются "конец в конец" с образованием микрофибрилл.
Функции коллагена VI типа пока полностью не ясны, хотя известно, что его микрофибриллы могут связываться со многими компонентами межклеточного матрикса: фибриллами интерстициальных коллагенов, гиалуроновой кислотой, протеогликанами. Молекула этого коллагена содержит многочисленные последовательности Арг-Гли-Асп (RGD), поэтому возможно его участие в клеточной адгезии через присоединение к мембранным адгезивным молекулам, например интегринам α1β1 и α2β1 (рис.10).
К этому классу относят коллагены VII и XVII типов, которые называют также коллагенами, связанными с эпителием, так как они обычно находятся в местах соединения эпителия с субэпителиальными слоями.
Коллаген VII типа - основной структурный компонент "заякоренных" фибрилл. Каждая молекула этого белка содержит два неколлагеновых домена (НК1 - у С-конца, НК2 - у N-конца) и один коллагеновый домен между ними. Из мономеров образуются димеры, при этом молекулы соединяются в области НК2-доменов антипараллельно по отношению друг к другу. Затем НК2домены отщепляются, и димеры соединяются между собой "бок о бок" с образованием фибрилл (рис.11).
Эти фибриллы играют важную роль в присоединении эпидермиса к дерме, так как одним концом они могут присоединяться к lamina densa, на которой лежит кожный эпителий, а другой их конец проникает в более глубокие субэпидермальные слои кожи и связывается там со структурами, называемыми "якорные диски".
Коллаген XVII типа представляет собой трансмембранный белок и обычно находится в гемидесмосомах эпидермиса. Предполагают, что этот коллаген взаимодействует с другими молекулами гемидесмосом и таким образом участвует в процессе присоединения эпидермиса к дерме.
Как и любой белок, коллаген функционирует в организме определённое время. Его относят к медленно обменивающимся белкам; Т1/2 составляет недели или месяцы. Разрушение коллагеновых волокон осуществляется активными формами кислорода и/или ферментативно (гидролитически).
Нативный коллаген не гидролизуется обычными пептидгидролазами. Основной фермент его катаболизма - коллагеназа, которая расщепляет пептидные связи в определённых участках спирализованных областей коллагена. Известны 2 типа коллагеназ:
1.Тканевая коллагеназа присутствует у человека в различных органах и тканях. В норме она синтезируется клетками соединительной ткани, прежде всего, фибробластами и макрофагами. Тканевая коллагеназа - металлозависимый фермент, который содержит Zn2+ в активном центре. В настоящее время известно 4 изоформы этого фермента. Активность коллагеназы зависит от соотношения в межклеточном матриксе её активаторов и ингибиторов. Среди активаторов особую роль играют плазмин, калликреин и катепсин В. Тканевая коллагеназа обладает высокой специфичностью, она перерезает тройную спираль коллагена в определённом месте, примерно на 1/4 расстояния от С-конца, между остатками глицина и лейцина (или изолейцина) (рис.12).
Образующиеся фрагменты коллагена растворимы в воде, при температуре тела они спонтанно денатурируются и становятся доступными для действия других протеолитических ферментов. Нарушение катаболизма коллагена ведёт к фиброзу органов и тканей (в основном печени и лёгких). А усиление распада коллагена происходит при аутоиммунных заболеваниях (ревматоидном артрите и системной красной волчанке) в результате избыточного синтеза коллагеназы при иммунном ответе.
2.Бактериальная коллагеназа синтезируется некоторыми микроорганизмами. Например,Clostridium histolyticum (возбудитель газовой гангрены) выделяет коллагеназу, расщепляющую пептидную цепь коллагена более чем в 200 местах. Этот фермент гидролизует следующую связь -X-Гли-Про-У- между звеньями X и Гли.
Таким образом разрушаются соединительнотканные барьеры в организме человека, что обеспечивает проникновение (или инвазию) этого микроорганизма и способствует возникновению и развитию газовой гангрены. Сам возбудитель не содержит коллагена и поэтому не подвержен действию коллагеназы.
У молодых людей обмен коллагена протекает интенсивно, с возрастом (и особенно в старости) заметно снижается, так как у пожилых и старых людей увеличивается количество поперечных сшивок, что затрудняет доступность коллагена для действия коллагеназы. Поэтому, если у молодых людей в возрасте 10-20 лет содержание гидроксипролина в моче может достигать 200 мг/сут, то с возрастом экскреция гидроксипролина снижается до 15-20 мг/сут.
В некоторых ситуациях синтез коллагена заметно увеличивается. Например, фибробласты мигрируют в заживающую рану и начинают активно синтезировать в этой области основные компоненты межклеточного матрикса. Результат этих процессов - образование на месте раны соединительнотканного рубца, содержащего большое количество хаотично расположенных фибрилл коллагена. Сходным образом происходит замещение погибающих клеток соединительной тканью в печени при циррозе, в стенках артерий при атеросклерозе, в мышцах при их дистрофии.
Коллаген является основным белком соединительной ткани млекопитающих и составляет около 30% от общей массы белков организма. Существование разновидностей волокнистой соединительной ткани: рыхлой и плотной (оформленной и неоформленной) во многом объясняется наличием всевозможных комбинаций различных типов коллагена, молекулы которых кодируются почти 20 генами.
Коллаген входит в состав косметических средств, используемых для:
1)образования воздухопроницаемого, влагоудерживающего слоя на поверхности кожи, обладающего пластифицирующими (разглаживающими) свойствами, со свойствами влажного компресса;
2)пролонгирования действия экстрактов, масел и др. в составе косметических композиций;
3)придания блеска волосам, создания коллагенового (защитного) слоя на поверхности волос.
1. Бурджанадзе Т.В. Термодинамическое обоснование водно-мостиковой структуры коллагена Биофизика, 1992;37(2):231-237.
2. Вавилова Т.П. Биохимия тканей и жидкостей полостей рта: учебное пособие / - 2-е изд., испр. и доп. - 2008. - 208 с. : ил.
3. Михайлов А.Н. Коллаген кожного покрова и основы его переработки. М., 1971;527.
4.Николаев А.Я. Биологическая химия.- 3-е изд., перераб. и доп.-М.: Медицинское информационное агенство.-2004.-566 с.: ил.
5. Павлова В.Н, Копьева Т.П, Слуцкий Л.И, Павлов Г.Г. Хрящ. М., 1988:325.
6. Степанов B.M. Молекулярная биология. М., 1996; 334.
7. Церетели Г.И. Тепловая денатурация коллагена в растворе и фибриллах. Биофизика 1982;27(5):780-784.
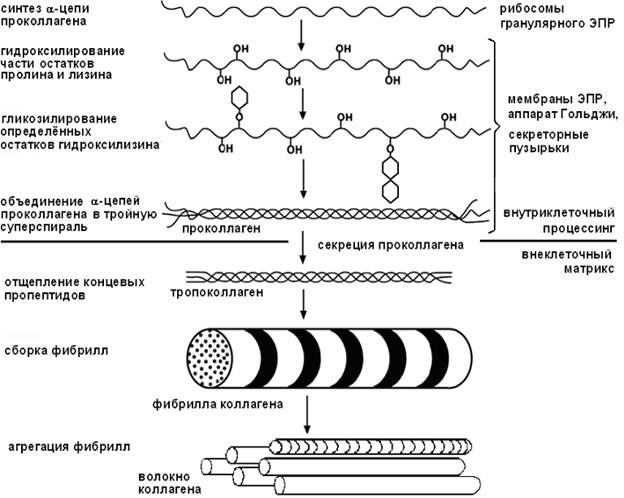
Коллаген синтезируется в фибробластах в виде высокомолекулярного предшественника – проколлагена.
На этапах синтеза коллагена после включения пролина и лизина в полипептидную цепь происходит их гидроксилирование (специфично для молекулы коллагена). Образование гидроксипролила и гидроксилизила катализируют железосодержащие ферменты — пролилгидроксилаза и лизилгидроксилаза, их кофактор — аскорбиновая кислота. Гидроксилирование аминокислот является диоксигеназной реакцией, т.е. молекула кислорода одновременно окисляет два субстрата (аминокислоту и a-кетоглутарат):
В результате реакции образуются оксипролин и сукцинат (в молекулу которого включён второй атом кислорода из молекулы О2) и выделяется СО2. Реакция высокоспецифична – остатки пролина и лизина подвергаются гидроксилированию, если они расположены со стороны аминогруппы глицинового остатка. Аскорбиновая кислота работает как восстановительный агент, благодаря которому железо в активном центре фермента сохраняется в форме Fe 2+ . При недостатке витамина С синтез коллагена нарушается, возникает непрочность коллагеновых волокон, кровоточивость десен, расшатывание зубов (проявления цинги). Расшатывание зубов обусловлено, главным образом, недогидроксилированием вновь синтезированного коллагена периодонтальной связки. Такой коллаген плохо агрегирует.
К остаткам гидроксилизина под действием сначала галактозилтрансферазы, затем глюкозилтрансферазы присоединяются углеводные единицы (сначала – одна галактоза, затем некоторые галактозы достраиваются до дисахарида – галактоза-глюкоза).
Гидроксилирование и трансферазная реакция происходят во вновь синтезированном коллагене, ещё не претерпевшем спирализации в просвете эндоплазматического ретикулюма. Затем каждая про-a-цепь с помощью водородных связей объединяется с двумя другими в молекулу проколлагена, которая секретируется в межклеточный матрикс.
• Проколлаген имеет более длинные цепи, чем тропоколлаген. Дополнительные концевые фрагменты не образуют обычную трехцепочечную спираль, а объединяются друг с другом в глобулярные домены, структура которых совершенно не похожа на уникальную линейную структуру зрелого коллагена (например, есть дисульфидные мостики). Это препятствует агрегации и образованию фибрилл внутриклеточно, что было бы фатальным для клетки. Вне клетки протеолитические ферменты последовательно удаляют оба домена – N-концевой и С-концевой (маркёры синтеза коллагена).
Ниже Более подробная схема синтеза коллагена
После того как во внеклеточном пространстве сформировались коллагеновые фибрилы, их прочность существенно увеличивается, так как образуются ковалентные сшивки между остатками лизина внутри и между молекулами тропоколлагена, укрепляя четвертичную структуру.
Сшивки создаются в несколько этапов.
I этап. Вначале некоторые остатки лизина и гидроксилизина дезаминируются лизилоксидазой с образованием альдегидных групп, обладающих высокой реакционной способностью. Затем эти группы самопроизвольно реагируют с образованием ковалентных связей друг с другом или с другими остатками лизина или гидроксилизина.
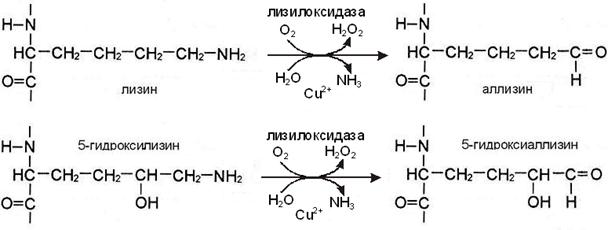
II этап. Альдегидные группы самопроизвольно взаимодействуют друг с другом, образуя альдольные поперечные связи коллагена, или реагируют с аминогруппой остатков лизина или 5-гидроксилизина (рис. А), обеспечивая образование бифункциональных ковалентных сшивок между соседними молекулами тропоколлагена.
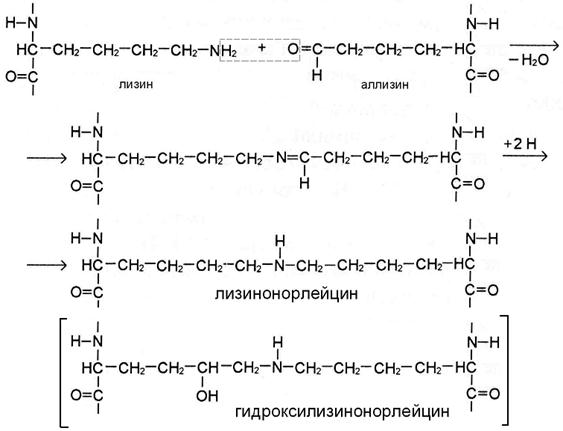
РИС А
Если в реакции участвует аллизин, то она протекает по механизму альдиминной конденсации. При этом по иминной связи промежуточного соединения присоединяются 2 атома Н. В результате образуются сшивки с группировкой -NH- в середине – лизиннорлейцин или гидроксилизиннорлейцин (рис. А).
Присутствие гидроксильной группы в 5 положении гидроксиаллизина предопределяет течение реакции по механизму кетоиминной конденсации (рис Б). В этом случае в цепи получившейся поперечной сшивки лизино-5-кетонорлейцина или гидроксилизино-5-кетонорлейцина вместе с группировкой -NH- присутствует кето-группа.

Цепочки таких перемычек достаточно длинные, чтобы иметь некоторую гибкость, а ковалентное соединение атомов придаёт им высокую прочность и закрепляет регулярную структуру микрофибрилл коллагена.
Поперечные бифункциональные сшивки имеют свой вариант упорядоченности: каждый концевой телопептид тропоколлагена соединён перемычкой с расположенным на том же уровне участком смежной молекулы (рис. 9). Подобная локализация и прочность сшивок позволяет обнаружить их в составе N- и C-телопептидов, отщепляемых при распаде коллагена (для идентификации таких специфичных фрагментов разработаны методы, основанные на иммуноферментном анализе).
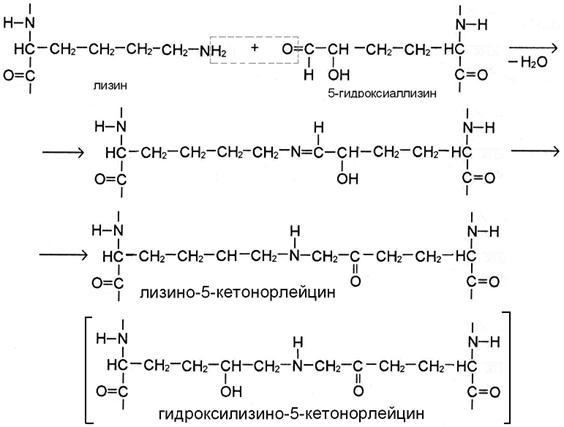
РИС Б
Бифункциональные связки наиболее присущи фибриллообразующим коллагенам типа I, II и III, причём в зависимости от вида ткани преобладает какой-либо определённый вид сшивки.
III этап. По мере созревания ткани возникают перемычки и между микрофибриллами. В бифункциональных сшивках сохраняются реакционноспособные атомы, которые постепенно вступают в реакции дополнительной конденсации с образованием трифункциональных сшивок, имеющих в центре гетероцикл – пиридиниевое или пиррольное кольцо (рис. В, Г). Эти процессы протекают также неферментативно путём спонтанного взаимодействия кетоиминной двойной сшивки одной микрофибриллы с альдегидным радикалом, расположенным в телопептидной части другой микрофибриллы.
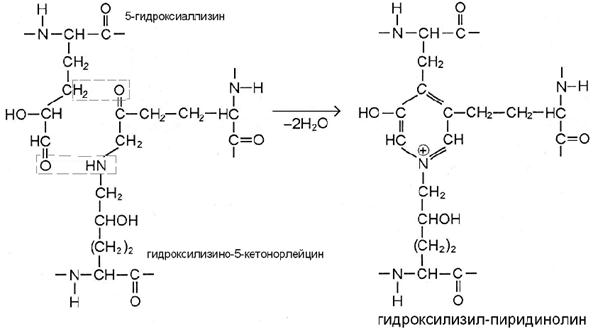
Если в реакции участвуют 5-гидроксиаллизин и уже сформированная сшивка гидроксилизино-5-кетонорлейцина, то продукт – гидроксилизил-пиридинолин (рис. В).
В большинстве тканей это главная трифункциональная сшивка коллагенов.
В минерализуемых тканях (кость, ткани зуба) число пиридиниевых сшивок в 5-10 раз меньше, чем в хряще и сухожилиях, причём чаще всего здесь встречается лизил-пиридинолин – вариант с негидроксилированной цепочкой в перемычке, образованной с участием лизино-5-кетонорлейцина. Более того, для минерализованных тканей характерны сшивки пиррольного типа, которые образует негидроксилированный аллизин, соединяясь с бифункциональной сшивкой гидроксилизино-5-кетонорлейцином (рис. Г). Из всех трифункциональных перемычек для минерализуемых тканей специфичен именно гидроксилизилпиррол. Дополнительные перемычки циклического характера нужны для повышения механической прочности волокон коллагена.
В
На примере коллагена -I: характерен для кости, является основным белком дентина. (закрепляем материал по пост трансляционному процессингу белка и ферментам микросомального окисления)

Коллаген синтезируется в фибробластах в виде высокомолекулярного предшественника – проколлагена.
На этапах синтеза коллагена после включения пролина и лизина в полипептидную цепь происходит их гидроксилирование (специфично для молекулы коллагена). Образование гидроксипролила и гидроксилизила катализируют железосодержащие ферменты — пролилгидроксилаза и лизилгидроксилаза, их кофактор — аскорбиновая кислота. Гидроксилирование аминокислот является диоксигеназной реакцией, т.е. молекула кислорода одновременно окисляет два субстрата (аминокислоту и a-кетоглутарат):
В результате реакции образуются оксипролин и сукцинат (в молекулу которого включён второй атом кислорода из молекулы О2) и выделяется СО2. Реакция высокоспецифична – остатки пролина и лизина подвергаются гидроксилированию, если они расположены со стороны аминогруппы глицинового остатка. Аскорбиновая кислота работает как восстановительный агент, благодаря которому железо в активном центре фермента сохраняется в форме Fe 2+ . При недостатке витамина С синтез коллагена нарушается, возникает непрочность коллагеновых волокон, кровоточивость десен, расшатывание зубов (проявления цинги). Расшатывание зубов обусловлено, главным образом, недогидроксилированием вновь синтезированного коллагена периодонтальной связки. Такой коллаген плохо агрегирует.
К остаткам гидроксилизина под действием сначала галактозилтрансферазы, затем глюкозилтрансферазы присоединяются углеводные единицы (сначала – одна галактоза, затем некоторые галактозы достраиваются до дисахарида – галактоза-глюкоза).
Гидроксилирование и трансферазная реакция происходят во вновь синтезированном коллагене, ещё не претерпевшем спирализации в просвете эндоплазматического ретикулюма. Затем каждая про-a-цепь с помощью водородных связей объединяется с двумя другими в молекулу проколлагена, которая секретируется в межклеточный матрикс.
• Проколлаген имеет более длинные цепи, чем тропоколлаген. Дополнительные концевые фрагменты не образуют обычную трехцепочечную спираль, а объединяются друг с другом в глобулярные домены, структура которых совершенно не похожа на уникальную линейную структуру зрелого коллагена (например, есть дисульфидные мостики). Это препятствует агрегации и образованию фибрилл внутриклеточно, что было бы фатальным для клетки. Вне клетки протеолитические ферменты последовательно удаляют оба домена – N-концевой и С-концевой (маркёры синтеза коллагена).
Ниже Более подробная схема синтеза коллагена
После того как во внеклеточном пространстве сформировались коллагеновые фибрилы, их прочность существенно увеличивается, так как образуются ковалентные сшивки между остатками лизина внутри и между молекулами тропоколлагена, укрепляя четвертичную структуру.
Сшивки создаются в несколько этапов.
I этап. Вначале некоторые остатки лизина и гидроксилизина дезаминируются лизилоксидазой с образованием альдегидных групп, обладающих высокой реакционной способностью. Затем эти группы самопроизвольно реагируют с образованием ковалентных связей друг с другом или с другими остатками лизина или гидроксилизина.

II этап. Альдегидные группы самопроизвольно взаимодействуют друг с другом, образуя альдольные поперечные связи коллагена, или реагируют с аминогруппой остатков лизина или 5-гидроксилизина (рис. А), обеспечивая образование бифункциональных ковалентных сшивок между соседними молекулами тропоколлагена.

РИС А
Если в реакции участвует аллизин, то она протекает по механизму альдиминной конденсации. При этом по иминной связи промежуточного соединения присоединяются 2 атома Н. В результате образуются сшивки с группировкой -NH- в середине – лизиннорлейцин или гидроксилизиннорлейцин (рис. А).
Присутствие гидроксильной группы в 5 положении гидроксиаллизина предопределяет течение реакции по механизму кетоиминной конденсации (рис Б). В этом случае в цепи получившейся поперечной сшивки лизино-5-кетонорлейцина или гидроксилизино-5-кетонорлейцина вместе с группировкой -NH- присутствует кето-группа.
Цепочки таких перемычек достаточно длинные, чтобы иметь некоторую гибкость, а ковалентное соединение атомов придаёт им высокую прочность и закрепляет регулярную структуру микрофибрилл коллагена.
Поперечные бифункциональные сшивки имеют свой вариант упорядоченности: каждый концевой телопептид тропоколлагена соединён перемычкой с расположенным на том же уровне участком смежной молекулы (рис. 9). Подобная локализация и прочность сшивок позволяет обнаружить их в составе N- и C-телопептидов, отщепляемых при распаде коллагена (для идентификации таких специфичных фрагментов разработаны методы, основанные на иммуноферментном анализе).

РИС Б
Бифункциональные связки наиболее присущи фибриллообразующим коллагенам типа I, II и III, причём в зависимости от вида ткани преобладает какой-либо определённый вид сшивки.
III этап. По мере созревания ткани возникают перемычки и между микрофибриллами. В бифункциональных сшивках сохраняются реакционноспособные атомы, которые постепенно вступают в реакции дополнительной конденсации с образованием трифункциональных сшивок, имеющих в центре гетероцикл – пиридиниевое или пиррольное кольцо (рис. В, Г). Эти процессы протекают также неферментативно путём спонтанного взаимодействия кетоиминной двойной сшивки одной микрофибриллы с альдегидным радикалом, расположенным в телопептидной части другой микрофибриллы.
Если в реакции участвуют 5-гидроксиаллизин и уже сформированная сшивка гидроксилизино-5-кетонорлейцина, то продукт – гидроксилизил-пиридинолин (рис. В).
В большинстве тканей это главная трифункциональная сшивка коллагенов.
В минерализуемых тканях (кость, ткани зуба) число пиридиниевых сшивок в 5-10 раз меньше, чем в хряще и сухожилиях, причём чаще всего здесь встречается лизил-пиридинолин – вариант с негидроксилированной цепочкой в перемычке, образованной с участием лизино-5-кетонорлейцина. Более того, для минерализованных тканей характерны сшивки пиррольного типа, которые образует негидроксилированный аллизин, соединяясь с бифункциональной сшивкой гидроксилизино-5-кетонорлейцином (рис. Г). Из всех трифункциональных перемычек для минерализуемых тканей специфичен именно гидроксилизилпиррол. Дополнительные перемычки циклического характера нужны для повышения механической прочности волокон коллагена.

В
Синтез коллагена протекает в два этапа:
1. внутриклеточный этап синтеза начинается в цитоплазме фибробласта.
2. внеклеточный этап биосинтеза коллагенового волокна завершается в межклеточном веществе.
Внутриклеточный этап:
Далее проколлаген поступает из гЭПС в КГ, где идет его гликозилирование, а затем он выделяется из клетки и наступает уже внеклеточный этап биосинтеза коллагена – сборка фибрилл.
Внеклеточный этап:
Этот процесс начинается с отщепления концевых фрагментов, в результате проколлаген превращается в нерастворимый белок, который способен к самосборке. Соединяясь между собой конец в конец, молекулы этого белка формируюттропоколлагендиаметром 1 – 4 нм. Образование тропоколлагена является надмолекулярным уровнем организации коллагенового волокна. Полимеризация (утолщение) тропоколлагена приводит к образованию протофибрилл, толщина которых составляет до 5 нм. 5 – 6 протофиблилл соединяясь между собой, формируют микрофибриллы толщиной до 20 нм. Микрофибриллы, в свою очередь, соединяются между собой при помощи глюкозаминогликанов (ГАГ), и в результате образуется коллагеновая фибрилла толщиной 20 – 120 нм. Ее образование завершает фибриллярный уровень организации коллагенового волокна. Особое соединение тропоколлагена между собой в конечном итоге придает коллагеновой фибрилле исчерченность и, кроме этого, обеспечивает прочность волокну. Фибриллы объединяясь между собой в пучки, формируют волокна толщиной до 20 мкм. Это четвертый уровень организации – волоконный.
Эластические волокна
Эластические волокна тоньше, чем коллагеновые (диаметр 0,2 – 10 мкм), менее прочные, однако обладают способностью к растяжению, ветвятся, и анастомозируют друг с другом, формируя сети и придавая РВНСТ растяжимость и эластичность.
Эластические волокна состоят из центрального светлого компонента, который образован белком эластином, и периферического компонента, который образован белком фибриллином. По степени зрелости можно выделить три разновидности эластических волокон: окситалановое, элауниновое и эластическое волокно. Первоначально фибробласты синтезируют микрофибриллы, состоящие из белка фибриллина, которые затем связываются между собой и формируют окситалановое волокно. Позднее в центральной части этого волокна накапливается белок эластин и волокно уже становится элауниновым. Постепенно количество эластина в волокне нарастает, он накапливается в центре волокна, а фибриллина уменьшается, он смещается на периферию и волокно становится зрелым эластическим волокном.
Ретикулярные волокна
Ретикулярные волокна самые тонкие, их диаметр составляет от 0, 1 до 2 мкм. Они формируют трехмерные сети, образованные коллагеном III типа. Синтезируются такие волокна преимущественно фибробластами и ретикулярными клетками. Основная функция данных волокон – опорная.
Основное аморфное вещество
Основное аморфное вещество - это среда, в которую погружены клетки и волокна. Состоит из воды, протеогликанов, которые связывают эту воду и структурных гликопротеидов. Также аморфное вещество содержит белки плазмы крови, ионы и т.д.
Структурные гликопротеидыэто нефибриллярные белки, которые опосредуют взаимосвязь между клетками и межклеточным веществом. К ним относится:
1. Фибронектин – синтезируется фибробластами, обеспечивает липкость, подвижность, рост и специализацию клеток
2. Ламинин– входит в состав базальных мембран
3. Фибриллин - формирует микрофибриллы
4. Нидоген – формирует базальные мембраны
Понятие об иммунитете
Иммунитет – специфическая защитная реакция организма на внедрение чужеродного по антигенам объекта. Выделяют двавида иммунитета:
2. Гуморальный иммунитет направлен преимущественно против вирусов. Протекает он примерно также, однако эффекторной (рабочей) клеткой в данном случае будет являться плазмоцит– конечный этап развития В-лимфоцита. Плазмоцит живет не долго, но за все непродолжительное время своего существования он активно продуцирует иммуноглобулины (антитела) различных классов: A, M, G, E, D. Эти белки способны активировать систему комплемента, нейтрофилы, макрофаги, опсонируя на них со связанным антигеном, тем самым косвенно способствуют гибели чужеродных агентов.
Статья содержит данные относительно состава волокон коллагенового каркаса кожи, стадий биосинтеза коллагена, а также факторов, которые регулируют данные процессы в фибробластах.
Со временем кожа истончается, а ее барьерная функция и естественная защита от ультрафиолета постепенно снижаются.
Коллагеновая масса и гибкость также начинают ослабевать (примерно на 1% в год), а коллаген является одним из самых главных структурных белков нашей кожи.
Структура коллагена и его роль в омоложении кожи лица
Коллаген − основной структурный белок кожи, который содержится, главным образом, в дерме (составляет более 70% сухой кожи и 25% всех белков).
Коллаген − это фибриллярный белок, который отличается от других рядом особенностей своего состава и структуры.
Первичная структура . Пептидная цепь, входящая в состав коллагена содержит примерно 1000 аминокислотных остатков, из которых 33% составляет глицин, около 21% − пролин и оксипролин, 11% − аланин и только примерно 35% − все остальные аминокислоты.
Новая эра в решении проблем потери объема: коррекция филлерами без восстановительного периода
В сосочковом слое дермы содержатся различные типы коллагенов :
Якорные волокна стабилизируют структуру кожи, укрепляя связь эпидермиса с подлежащей соединительной тканью, что естественно играет большую роль в омоложении кожи лица и обеспечении ровного рельефа без риска образования морщин и заломов.
Биосинтез коллагена в коже
Процесс синтеза коллагена можно разделить на внутри - и внеклеточную стадии:
• Основная функция коллагена состоит в обеспечении структурной опоры тканей
• Коллагены представляют собой семейство, состоящее более чем из 20 различных белков внеклеточного матрикса. Эти белки — наиболее распространенные в царстве животных
• Коллагеновые субъединицы выходят из клеток и затем, во внеклеточном пространстве, собираются в более крупные фибриллы и волокна
• Мутации в коллагеновых генах вызывают множество патологических состояний, начиная от появления морщин до развития хрупкости костей и таких тяжелых заболеваний, как образование кожных волдырей
Семейство коллагенов включает более 20 белков, которые относятся к наиболее распространенным белкам клеток животных. У многоклеточных организмов коллагены существуют по крайней мере 500 млн лет. Почти все клетки животных синтезируют и секретируют по меньшей мере одну из форм коллагена.
Коллагены обеспечивают тканям структурную поддержку и существуют во множественных формах, организованных в различные структуры. Все белки семейства коллагенов характеризуются одним общим свойством: они собраны в тонкие (примерно 1,5 нм диаметром) тройные спиральные суперспирализованные структуры, состоящие из трех субъединиц коллагеновых белков, которые удерживаются вместе ковалентными и нековалентными связями.
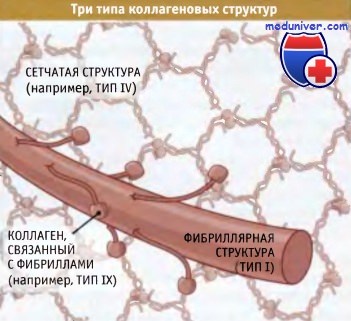
Коллагеновые субъединицы собираются в тройные спиральные структуры, которые организуются в фибриллы или в сеть,
где они связаны между собой другими белками внеклеточного матрикса, включая коллагены, связанные с фибриллами.
Суперспирализованные структуры бывают трех типов — фибриллярные, слоистые и связанные с фибринами:
• Слоистые коллагены представляют собой сеть, состоящую из суперспирализованных спиральных структур. Они в меньшей степени устойчивы к мышечным усилиям, но гораздо лучше противостоят растяжению в нескольких направлениях. Сеть таких структур, например, характерна для кожи.
Независимо от организации, коллагены образуют основную каркасную структуру внеклеточного матрикса. Такие входящие во внеклеточный матрикс белки, как фибронектин и витронектин, связываются с коллагенами и вплетены в структуры, образованные коллагеновым каркасом. Один из представителей семейства коллагенов представляет собой трансмембранный белок, который участвует в формировании межклеточных контактов.
Существует примерно 20 различных типов коллагена, большая часть которых может быть сгруппирована в четыре класса. Каждая из тройных спиралеобразных структур обозначается римской цифрой (I, II, III и т. д.). Каждая коллагеновая субъединица имеет обозначение как субъединица а, а ее типу присвоен номер (а1, а2, а3 и т. д.), после которого римской цифрой обозначен тип, в котором она находится. Например, основной фибриллярный коллаген хвоста (и других тканей) крыс относится к типу I и состоит из двух копий субъединиц а1(1) и одной копии субъединицы а2 (I).
На рисунке ниже представлена структура коллагеновых волокон. Три полипептидные субъединицы параллельно обернуты вокруг друг друга и образуют суперспирализованную спиральную структуру длиной 300 нм. Для коллагенов характерна повторяющаяся последовательность аминокислот, содержащая элемент глицин-X-Y, где X и Y могут представлять собой любую аминокислоту, но обычно это пролин и гидроксипролин соответственно.
Такая последовательность способствует плотной упаковке трех субъединиц и облегчает образование суперспиральной структуры. Субъединицы длиной 300 нм скрепляются вместе посредством ковалентных связей, которые образуются между N-концевым участком одной субъединицы и С-концевым участком примыкающей к ней. Суперспирализованные спиральные структуры располагаются параллельно, образуя между собой небольшие зазоры (64-67 нм). Эти зазоры обеспечивают характерный вид (исчерченность) фибрилл, видимый в электронном микроскопе.

Коллагеновые белки подразделяются на четыре основные группы, которые отличаются по молекулярной формуле,
характеру полимерных форм и по распределению в тканях. Некоторые группы включают коллагены нескольких типов.
Полностью собранные коллагеновые структуры (фибриллярные или сетчатые) по размерам оказываются гораздо больше, чем сами клетки; некоторые фибриллы могут достигать нескольких миллиметров длины. Таким образом, субъединицы коллагена синтезируются и секретируются в виде суперспирализованных спиральных структур, и окончательные этапы их сборки происходят вне клетки. Как показано на рисунке ниже, синтез коллагена и дальнейший его процессинг происходят на протяжении всего секреторного пути. При синтезе коллагеновые белки направляются в гранулярный эндоплазматический ретикулум (ЭПР) при участии частиц, распознающих сигнал и связанного с ними белкового аппарата.
После того как проколлагены попали в просвет ЭР, по мере транспорта из ЭР через аппарат Гольджи и в секреторные везикулы, они претерпевают серию модификаций. В процессе транспорта проколлагена через ЭР и аппарат Гольджи, к боковым цепям пролина и лизина, находящимся в средней части молекул проколлагена, добавляются гидроксильные группы (-ОН). При этом образуются гидроксипролин и гидроксилизин.
Эти модификации обеспечивают правильное образование водородных связей, которые скрепляют вместе три субъединицы в суперспирализованной спиральной структуре. Между амино- и карбоксиконцевыми частями пропептидов образуются дисульфидные связи, которые затем обеспечивают правильное расположение трех проколлагеновых субъединиц с образованием тройной спиральной суперспирализованной структуры. Затем спираль образуется спонтанно, в направлении от С-конца к N-концу.
Пропептиды препятствуют взаимодействию суперспирализованных спиралей друг с другом, тем самым предотвращая полимеризацию коллагена в клетке. Когда произошла секреция тройных спиралей проколлагена, ферменты, которые называются протеазы проколлагена, отщепляют пропептиды. Остающийся белок, известный под названием тропоколлагена, почти весь организован в тройную спираль и представляет собой основную структурную единицу коллагеновой фибриллы.
Фибриллы собираются просто: боковые цепи лизина в тропоколлагене модифицируются при действии фермента лизилоксидазы, образуя аллизины. Эти модифицированные лизины образуют ковалентные сшивки, которые обеспечивают полимеризацию тропоколлагенов. Лизилоксидаза представляет собой внеклеточный фермент, и эта стадия сборки фибрилл происходит только после выхода проколлагена из клетки. После сборки фибриллы могут объединяться, образуя большие пучки или волокна, характерные для фибриллярного коллагена.
Мутации в коллагеновом гене типа IV приводят к нарушению сборки базальной ламины в большинстве эпителиальных тканей и к развитию такого кожного заболевания, как буллезный эпидермоз.
Клетки связываются с коллагеном посредством специфических рецепторов, называемых интегринами. Эти рецепторы обеспечивают возможность обратимого связывания клеток с коллагенами по мере их движения по внеклеточному матриксу. Интегриновые рецепторы также активируют пути передачи сигналов, так что связывание с коллагенами (и с другими белками внеклеточного матрикса) изменяет активность в клетке биохимических процессов и, таким образом, способствует контролю над ростом и дифференцировкой клеток.
Схематическое строение тройной спиральной структуры коллагена (наверху),
организация витой структуры в фибрилле (в середине) и фибрилл в коллагеновом волокне (внизу).
Наличие 67-нм зазора между соседними спиральными структурами обусловливает видимую в электронном микроскопе исчерченность фибрилл, составляющих волокно. Посттрансляционная модификация и сборка субъединиц проколлагена в тройные спиральные структуры происходит при внутриклеточном перемещении по секреторному пути.
Однако сборка фибрилл происходит во внеклеточном пространстве после секреции тройных спиралей, обладающих витой структурой.
Для упрощения в тройных структурах не показаны гидроксильные группы и сахарные остатки. Лизилоксидаза катализирует ковалентное связывание двух боковых цепей лизина с образованием аллизинов (альдегидных производных лизина),
которые затем образуют между собой альдольную связь.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

