Расскажите о строении и свойствах железоуглеродистых сплавов кратко
Обновлено: 05.07.2024
В практике строительства наибольшее применение нашли железоуглеродистые сплавы, которые называют черными металлами.С целью придания специфических свойств в их состав вводят легирующие добавки. В зависимости от содержания углерода черные металлы подразделяют на хрупкий чугун (2 – 4 % С) и относительно пластичную сталь (до 2 % С). В металлургии из железных руд вначале получают чугун, а затем путем окисления и удаления избыточного углерода, марганца, фосфора, кремния – сталь.
Сырьемдля получения чугуна служат руды, содержащие железо в виде окислов: красный железняк (гематит), бурый железняк, магнитный железняк (магнетит).В зависимости от содержания железа руды подразделяют на богатые (от 15 до 70 %) и бедные. Первые после дробления и сортировки направляют в доменную печь для плавки, а бедные подвергают обогащению за счет отделения пустой породы. Топливом в доменном процессе служит кокс, полученный путем сжигания без доступа воздуха каменного угля. Для понижения температуры плавления пустой породы и облегчения перевода ее и золы топлива в шлак в состав шихты вводят специальные добавки – флюсы, ими могут быть известняки, доломиты и песчаники.
Современная доменная печь поглощает большое количество материалов и воздуха. Так для производства каждых 100 т чугуна необходимо в среднем подать в печь 190 т железной руды, 95 т кокса, 50 т известняка и около 350 т воздуха. В результате кроме 100 т чугуна получается около 80 т шлака и 500 т доменного газа. Это энергоемкий процесс.
В состав чугунов, кроме железа и углерода, обычно входят примеси кремния, марганца, фосфора, а также легирующие добавки – никель, хром, магний, которые придают ему высокие механические свойства и обеспечивают износо-, жаро- и коррозионную стойкость. В зависимости от химического состава и микроструктуры выпускают белый, серый, высокопрочный и ковкий чугуны. Большую часть выплавленного чугуна используют для переработки (передела) в сталь – белый передельный чугун.Для изготовления фасонного литья применяют серый литейный чугун.
Белый чугун(передельный) тверд, хрупок, плохо обрабатывается резанием. Высокая твердость белого чугуна обеспечивает высокую износостойкость, его применяют для получения ковкого чугуна и стали.
Серый чугун– один из наиболее распространенных литейных сплавов. Это самый дешевый металлический материал. Он имеет высокие литейные свойства, хорошую обрабатываемость резанием.
С целью значительного повышения пластичности чугун или чугун в сочетании с металлоломом (скрапом) и рудой переплавляют. При плавке вводят флюсы и раскислители, в случае необходимости – легирующие добавки. При этом из железоуглеродистого сплава путем окисления и перевода в шлак удаляют избыток углерода, марганца, кремния, фосфора. Наиболее высокопроизводительные способы выплавки стали – кислородно-конверторный, мартеновский и электродуговой.
Кислородно-конверторным способомполучают сталь из жидкого чугуна с добавлением скрапа и руды. Конвертором называют стальную реторту, состоящую из цилиндрической части, днища и конусообразной горловины, футерованную внутри огнеупорным кирпичом (рис. 3.3). Технологический цикл выплавки стали составляет 50 – 60 мин. К недостаткам этого способа относится большое пылеобразование, требующее применения сложных пылеочистительных установок.
Мартеновским способомвыплавляют в зависимости от используемого сырья кислую и основную мартеновскую сталь. Современная мартеновская печь (см. рис. 3.3) представляет собой ванну сферической формы, футерованную огнеупорным кирпичом. В качестве топлива используют природный газ или мазут. Мартеновские печи могут работать как на твердой шихте, состоящей из смеси стального лома и твердого чушкового чугуна, так и на смешанной шихте. Последняя представляет собой скрап, богатую железную руду и жидкий чугун. Продолжительность получения стали в мартеновской печи составляет несколько часов. Фактор времени и значительный расход топлива являются недостатками мартеновского способа выплавки стали. К достоинствам можно отнести возможность использования различной шихты и разнообразного топлива, а также широкий ассортимент выпускаемого продукта (углеродистые и легированные стали).
Для выплавки высококачественных легированных сталей используют электропечи(см. рис. 3.3). Плавка шихты происходит за счет тепла трех электрических дуг (по числу фаз переменного тока), образующихся между электродами и металлом при температуре 1200 °С. К достоинствам способа можно отнести быстрый разогрев металлов, точное регулирование температуры, пониженное содержание в стали вредных примесей.
 |
Рис. 3.3. Печи для выплавки стали:
1 – мартеновская; 2 – конверторная; 3 – электродуговая
Основной недостаток всех перечисленных сталеплавильных агрегатов – периодичность действия. Для увеличения производительности печей, снижения эксплуатационных затрат, повышения качества стали, уменьшения технологических отходов и лучшего использования сырья разрабатываются сталеплавильные агрегаты непрерывного действия.
Стальклассифицируют по способу производства, химическому составу, назначению. По способу производстваразличают мартеновскую, кислородно-конверторную и электросталь; химическому составу – углеродистую и легированную; назначению– конструкционную (строительную и машиностроительную), инструментальную и специального назначения.
Углеродистая стальв свою очередь бывает обыкновенного качества, качественная конструкционная(для машиностроения и наиболее ответственных конструкций) и высококачественная инструментальная(для изготовления режущих инструментов, штампов, матриц). Основное применение в строительстве находит углеродистая сталь обыкновенного качества. В ней присутствуют кроме углерода (0,06 – 0,62 %) примеси кремния, марганца. Наиболее нежелательно присутствие фосфора, который придает стали свойство хрупкости при низких температурах (хладноломкость), и серы, вызывающей аналогичное действие при высоких температурах. В зависимости от назначения и гарантируемых механических характеристик сталь углеродистую обыкновенного качества делят на две группы (А, Б) и подгруппу (В) (ГОСТ 14637-79). Для строительных целейиспользуют в основном сталь группы А, которую изготовляют следующих марок: СтО, Ст1, Ст2, . Ст6. По мере увеличения номера стали повышаются пластичность и ударная вязкость.
Наиболее широкое применение нашла сталь Ст3, так как по сочетанию важнейших свойств – прочности и свариваемости она занимает промежуточное положение в ряду. Для получения арматуры используют Ст5, малонагруженных деталей – Ст0, Ст1. Существуют углеродистые стали обыкновенного качества специального назначения, например, для строительства мостов Ст3м. Этот вид сталей имеет существенные недостатки: хладноломкость, исключающую их применение при низких температурах, и относительно невысокую прочность, приводящую к перерасходу металла и увеличению массы металлоконструкций.
Качественные конструкционные углеродистые сталиподразделяют в зависимости от содержания углерода (в сотых долях %) на малоуглеродистые(10 – 25), которые хорошо свариваются, пластичны, применяют их для сварных и клепаных конструкций; среднеуглеродистые
(30 –50), хуже свариваются, более прочные и хрупкие, используют для деталей, подвергающихся большим нагрузкам; высокоуглеродистые(55 – 70) применяют для изготовления пружин, рессор и зубчатых колес.
Углеродистые стали не могут по прочности удовлетворять высоким требованиям, предъявляемым к современным конструкционным материалам. Этот вид стали имеет склонность к старению, повышению хрупкости при пониженных температурах, малую стойкость против коррозии. С целью повышения качества в сталь вводят легирующие элементы с условным обозначением Сr (X), Мn (Г), Ni (Н), Мо (М), Со (К), Si (С).
Преимущества легированных сталей выявляются в большинстве случаев только после дополнительной термообработки. Легированные стали классифицируют по химическому составу и назначению.Похимическому составу–низколегированнаяс общим содержанием легирующих элементов до 2,5 %, среднелегированная (от 2,5 до 10 %) и высоколегированная (более 10 %). По назначению–конструкционная,применяемая при обычных и повышенных температурах, инструментальная,которую применяют для режущего, штампованного и измерительного инструмента, и сталь с особымифизическими, химическими и механическими свойствами.
Цветные металлы и сплавы
Основным сырьем для производства алюминия служат бокситы, содержащие до 75 % оксида алюминия.По распространенности в земной коре алюминий занимает первое место среди металлов. По объему производства и масштабам применения он уступает только черным металлам. Широкое использование обусловлено важнейшими свойствами алюминия – малой плотностью (2700 кг/м 3 ), высокой электро- и теплопроводностью. Алюминий – серебристо-белый металл, устойчивый против коррозии вследствие образования на его поверхности плотной оксидной пленки. Благодаря высокой пластичности алюминий хорошо обрабатывается давлением как в холодном, так и в горячем состоянии. Этот металл хорошо сваривается газовой и контактной сваркой, но имеет низкие литейные свойства и плохо обрабатывается резанием. Из отрицательных свойств алюминия как конструкционного материала следует подчеркнуть его недостаточную жесткость, модуль его упругости в 3 раза меньше, чем у стали. На свойства алюминия большое влияние оказывают примеси железа, кремния и др., которые понижают его электро- и теплопроводность, коррозионную стойкость и пластичность, повышая его прочность и твердость.
В строительстве алюминий используют главным образом в виде сплавов, которые обладают малой плотностью (2550 – 2710 кг/м 3 ) и достаточной прочностью.
Алюминиевые сплавы классифицируют по технологии изготовленияизделий налитейные, порошковыеидеформируемые.
Литейные и порошковые сплавыпредназначены для изготовления фасонных отливок в машиностроении.
Деформируемые сплавыпредназначены для изготовления листов, профилей, проволоки, труб методами холодной или горячей деформации. В строительстве наиболее широкое применение нашли сплавы алюминия и магния (магналии), алюминия с медью и магнием (дуралюмины), алюминия, магния и кремния (авиаль).
Конструкции из алюминиевых сплавов используют в случае необходимости значительного снижения массы ограждающих и несущих конструкций, повышения их архитектурной выразительности, коррозионной стойкости, а также при предъявлении специальных требований: отсутствие искрообразования, магнитных свойств и надежность работы при отрицательных температурах. В связи с этим основными определяемыми показателями для алюминиевых сплавов являются модуль сдвига и упругости, коэффициенты поперечной деформации и линейного расширения, которые определяют в интервале температур от – 70 до + 100 о С.
Важнейшим сырьем при получении медиявляются сернистые руды, в частности, медный колчедан. Медь – металл красновато-розового цвета, который обладает высокой электро- и теплопроводностью, пластичностью и коррозионной стойкостью, хорошей обрабатываемостью давлением в холодном и горячем состоянии. Для устранения существенных недостатков (низкие литейные свойства, плохая обрабатываемость резанием, относительно невысокие прочностные характеристики) ее легируют различными элементами. В строительстве нашли применение в основном два вида сплавов меди: латунь– сплав меди с цинком, бронза– сплавы меди с оловом или с алюминием, железом и марганцем. Латунь используют в виде листов, прутьев, проволоки, труб, а также архитектурных изделий для отделки интерьеров зданий; бронзу – для внутренней отделки зданий. Чистую медь в виде тонких листов применяют в качестве долговечного кровельного материала.
Цинк– металл синевато-белого цвета. Он обладает высокой коррозионной стойкостью, поэтому служит для оцинкования различных стальных изделий (кровельной стали, закладных деталей, болтов и т.д.).
Нанесение защитных покрытий может производиться следующими способами:
- цинкованием в расплаве цинка – горячее цинкование;
- металлизацией – напыление сжатым воздухом частиц расплавленного цинка;
- термодиффузионным цинкованием – химико-термическая обработка изделий в цинковых порошках при температуре от 380 до 500 о С;
- нанесением на предварительно очищенную поверхность красок с предельным содержанием цинка и последующей сушкой в естественных условиях – метод холодного цинкования.
Долговечная, надежная защита поверхности обеспечивается за счет самого химически стойкого металла и труднорастворимых продуктов его взаимодействия с окружающей средой.
Свинец– тяжелый металл серовато-синего цвета, химически стоек, обладает высокими защитными свойствами по отношению к действию рентгеновских лучей. В строительстве свинец используют при изготовлении специальных труб, защитных покрытий и экранов.
Железоуглеродистые сплавы - сплавы железа (Fe) с углеродом (C) на основе железа. Варьируя состав и структуру, получают железоуглеродистые сплавы с разнообразными свойствами, что делает их универсальными материалами. Различают чистые железоуглеродистые сплавы для исследовательских целей (со следами примесей) и технические железоуглеродистые сплавы - стали и чугуны.
В металловедении различают три типа сплавов: твердый раствор, механическую смесь, химическое соединение. Если атомы входящих в состав сплава элементов незначительно отличаются размером и строением электронной оболочки, то они могут образовывать общую кристаллическую решетку. Сплав с таким строением называют твердым раствором. Если элементы сплава не образуют твердого раствора, а каждый из них кристаллизуется самостоятельно, то такой сплав называют механической смесью. Если элементы сплава вступают в химическое взаимодействие, образуя новое вещество, такой сплав называется химическим соединением. Практически сплавы могут сочетать все три типа строения.
Способность железа растворять углерод и другие элементы служит основой для получения разнообразных сплавов.
Углерод, растворяясь в железе, образует твердые растворы. В низкотемпературной модификации железа растворяется мало углерода (до 0,02 %), такой раствор называется феррит. Феррит обладает низкой твердостью и высокой пластичностью. Чем больше содержится в сплаве феррита, тем он мягче и пластичнее. Высокотемпературная модификация железа лучше растворяет углерод (до 2 %), образуя твердый раствор аустенит, также характеризующийся высокой пластичностью.
Химическое соединение железа с углеродом — карбид железа, в котором содержится 6,67 % углерода, называется цементитом. Цементит хрупок и имеет высокую твердость. Чем больше цементита в сплаве, тем он более твердый и хрупкий. В некоторых случаях (например, в присутствии больших количеств кремния) цементит не образуется, а углерод выделяется в виде графита, как это имеет место в сером чугуне.
В сталях и чугунах феррит, аустенит и цементит существуют в виде механических смесей. Иными словами, сталь и чугун — поликристаллические материалы, свойства которых зависят как от химического состава (количества железа, углерода и других примесей), так и от структуры (типа и размера кристаллов). Например, при нагревании до температуры выше 723 °С твердая и прочная углеродистая сталь, состоящая из смеси феррита и цементита, становится мягкой и прочность ее падает, так как смесь феррита и цементита переходит в аустенит. На этом основана горячая обработка углеродистых сталей. Этим же объясняется резкое падение прочности стальных конструкций при нагреве во время пожара.
Железоуглеродистые сплавы - сплавы железа (Fe) с углеродом (C) на основе железа. Варьируя состав и структуру, получают железоуглеродистые сплавы с разнообразными свойствами, что делает их универсальными материалами. Различают чистые железоуглеродистые сплавы для исследовательских целей (со следами примесей) и технические железоуглеродистые сплавы - стали и чугуны.
В металловедении различают три типа сплавов: твердый раствор, механическую смесь, химическое соединение. Если атомы входящих в состав сплава элементов незначительно отличаются размером и строением электронной оболочки, то они могут образовывать общую кристаллическую решетку. Сплав с таким строением называют твердым раствором. Если элементы сплава не образуют твердого раствора, а каждый из них кристаллизуется самостоятельно, то такой сплав называют механической смесью. Если элементы сплава вступают в химическое взаимодействие, образуя новое вещество, такой сплав называется химическим соединением. Практически сплавы могут сочетать все три типа строения.
Способность железа растворять углерод и другие элементы служит основой для получения разнообразных сплавов.
Углерод, растворяясь в железе, образует твердые растворы. В низкотемпературной модификации железа растворяется мало углерода (до 0,02 %), такой раствор называется феррит. Феррит обладает низкой твердостью и высокой пластичностью. Чем больше содержится в сплаве феррита, тем он мягче и пластичнее. Высокотемпературная модификация железа лучше растворяет углерод (до 2 %), образуя твердый раствор аустенит, также характеризующийся высокой пластичностью.

Химическое соединение железа с углеродом — карбид железа, в котором содержится 6,67 % углерода, называется цементитом. Цементит хрупок и имеет высокую твердость. Чем больше цементита в сплаве, тем он более твердый и хрупкий. В некоторых случаях (например, в присутствии больших количеств кремния) цементит не образуется, а углерод выделяется в виде графита, как это имеет место в сером чугуне.
В сталях и чугунах феррит, аустенит и цементит существуют в виде механических смесей. Иными словами, сталь и чугун — поликристаллические материалы, свойства которых зависят как от химического состава (количества железа, углерода и других примесей), так и от структуры (типа и размера кристаллов). Например, при нагревании до температуры выше 723 °С твердая и прочная углеродистая сталь, состоящая из смеси феррита и цементита, становится мягкой и прочность ее падает, так как смесь феррита и цементита переходит в аустенит. На этом основана горячая обработка углеродистых сталей. Этим же объясняется резкое падение прочности стальных конструкций при нагреве во время пожара.
Металлы, как и другие вещества, могут существовать в различных кристаллических формах (модификациях). Это явление называется полиморфизм.
Полиморфные превращения в металлах происходят при изменении температуры. Так, при температуре свыше 723 °С железо переходит из а-модификации в б-модификацию, при этом изменяются физико-механические свойства металла. При резком охлаждении металла высокотемпературные модификации могут и не переходить в низкотемпературные. На этом, например, основана термообработка металлов (закалка, отпуск, нормализация).
Химически чистые металлы на практике используют редко. Это связано с трудностью получения чистых веществ, а также с возможностью получать металлы с определенными требуемыми свойствами путем создания различных сплавов.
В металловедении различают три типа сплавов: твердый раствор, механическую смесь, химическое соединение. Если атомы входящих в состав сплава элементов незначительно отличаются размером и строением электронной оболочки, то они могут образовывать общую кристаллическую решетку. Сплав с таким строением называют твердым раствором. Если элементы сплава не образуют твердого раствора, а каждый из них кристаллизуется самостоятельно, то такой сплав называют механической смесью. Если элементы сплава вступают в химическое взаимодействие, образуя новое вещество, такой сплав называется химическим соединением. Практически сплавы могут сочетать все три типа строения.
Рассмотрим зависимость свойств сплава от его состава и строения на примере железоуглеродистых сплавов (сталей и чугунов).
Чистое железо — серебристо-белый мягкий пластичный металл, почти не окисляющийся на воздухе. Прочность его значительно ниже прочности стали и чугуна. При производстве в черные металлы в виде примесей к железу попадают углерод, кремний и некоторые другие вещества. Наибольшее влияние на их свойства оказывает углерод, содержащийся в количестве 0,5…5 %.
Способность железа растворять углерод и другие элементы служит основой для получения разнообразных сплавов.
Углерод, растворяясь в железе, образует твердые растворы. В низкотемпературной модификации железа (а-же-лезе) растворяется мало углерода (до 0,02 %), такой раствор называется феррит. Феррит обладает низкой твердостью и высокой пластичностью. Чем больше содержится в сплаве феррита, тем он мягче и пластичнее. Высокотемпературная модификация железа (у-железо) лучше растворяет углерод (до 2 %), образуя твердый раствор аусте-нит, также характеризующийся высокой пластичностью.
Химическое соединение железа с углеродом — карбид железа, в котором содержится 6,67 % углерода, называется цементитом. Цементит хрупок и имеет высокую твердость. Чем больше цементита в сплаве, тем он более твердый и хрупкий. В некоторых случаях (например, в присутствии больших количеств кремния) цементит не образуется, а углерод выделяется в виде графита, как это имеет место в сером чугуне.
В сталях и чугунах феррит, аустенит и цементит существуют в виде механических смесей. Иными словами, сталь и чугун — поликристаллические материалы, свойства которых зависят как от химического состава (количества железа, углерода и других примесей), так и от структуры (типа и размера кристаллов). Например, при нагревании до температуры выше 723 °С твердая и прочная углеродистая сталь, состоящая из смеси феррита и цементита, становится мягкой и прочность ее падает, так как смесь феррита и цементита переходит в аустенит. На этом основана горячая обработка (прокат, ковка) углеродистых сталей. Этим же объясняется резкое падение прочности стальных конструкций при нагреве во время пожара.
Различные комбинации этих элементов приводят к получению большого количества сплавов, которые можно разделить на три большие группы:
- Техническое железо.
- Стали.
- Чугуны.

К техническому железу относят материалы, в которых содержится менее 0,02% углерода. К сталям относят, материалы, в которых углерод находится в пределах от 0,02 до 2,14%. И в группу чугунов входят материалы, количество углерода в которых превышает 2,14%.





Сферы применения

Несмотря на некоторое понижение прочностных свойств, обусловленное принадлежностью металла к классу ферритовых сталей, этот материал распространен в разных областях. Например, в машиностроении применяются детали, выполненные из доэвтектоидных сталей. Другое дело, что используются высокие марки сплавов, в изготовлении которых применялись передовые технологии обжига и нормализации. Также структура доэвтектоидной стали с пониженным содержанием феррита вполне позволяет использовать металл в производстве строительных конструкций. Более того, доступная стоимость некоторых марок стали такого типа позволяет рассчитывать на существенную экономию. Иногда в изготовлении стройматериалов и стальных модулей вовсе не требуется повышенная прочность, но необходима износостойкость и упругость. В таких случаях как раз и оправдано применение доэвтектоидных сплавов.
Компоненты в системе железо углерод
Аустенит
Атомы размещается в гранецентрированной ячейке. Твердость аустенита имеет твердость 200 … 250 единиц по Бринеллю. Кроме того у него хорошая пластичность и он отличается парамагнитностью.
Железо
Железо – это материал, относящийся к металлам. Его натуральный цвет – серебристо-серый. В чистом виде он очень пластичен. Его удельный вес составляет 7,86 г/куб. см. Температура плавления составляет 1539 °C. На практике чаще всего применяют техническое железо, в составе которого присутствуют следующие примеси – марганец, кремний и многие другие. Массовая доля примесей не превышает 0,1%.

У железа есть такое свойство как полиформизм. То есть, при одном и том же химическом составе, это вещество может иметь разную структуру кристаллической решетки и соответственно разные свойства. Модификации железа называют соответственно – Б, Г, Д. Все эти модификации существуют при разных условиях. Например, тип Б, может существовать только при температуре 911 °С. Тип Г может существовать в диапазоне от 911 до 1392 °С. Тип Д существует в диапазоне от 1392 до 1539 °С.
Каждый из типов обладает своей формой кристаллической решеткой, например, у типа Б решетка представляет собой куб, решетка типа Г имеет гранецентрированную кубическую форму. Решетка типа Д, имеет форму объемно центрированного куба.
Еще одно свойство состоит в том, что при температуре ниже 768 железо ферримагнитно, а при ее повышении это свойство теряется.
Точки полиморфной и магнитной трансформации называют критическими. На таблице они обозначены следующим образом – А2, А3, А4. Цифровые индексы показывают тип трансформации. Для более полного различия превращения железа из одного вида в другой к обозначению добавляют индексы с и r. Первый говорит о нагреве, второй об охлаждении.

Полиморфные модификации железа
При высоких параметрах пластичности, железо не обладает высокой твердостью, по шкале Бринелля она равна 80 единиц.
Железо имеет возможность образовывать твердые растворы. Их можно разделить на две группы – раствор замещения и внедрения. Первые состоят их железа и других металлов, вторые из железа и углерода, водорода и азота.
Углерод
Другой компонент системы – углерод. Это – неметалл и он обладает тремя модификациями в виде алмаза, графита и угля. Он плавится при 3500 °С.

Аллотропные модификации углерода
В сплаве железа, этот элемент находится в виде твердого раствора, его называют цементит или в виде графита. В таком виде он присутствует в сером чугуне. Графит, не отличается ни пластичностью, ни прочностью.
Цементит
Доля углерода составляет 6,67%. Он обладает высокой твердостью – 800 НВ, но при этом у него отсутствует пластичность. Полиморфными свойствами не обладает.
Он обладает следующим свойством – при формировании раствора замещения, углерод может быть заменен на атомы других веществ, например, на хром или никель. Такой раствор получил название легированного раствора.

Он не обладает устойчивостью, при наличии некоторых условий он может разлагаться, при этом происходит трансформация углерода в графит. Это свойство нашло применение при образовании чугунов.
Кстати, в жидком состоянии, железо может растворять в себе примеси, при этом образуя, однородная масса.
Феррит
Так называют твердый раствор, при котором происходит внедрение углерода в железо.
Он растворяется с определенной переменностью, при нормальной (комнатной) температуре объем углерода лежит в пределах 0,006%, при 727 °С, то концентрация углерода составит 0,02%. По достижении 1392 °С образуется феррит.

Содержание углерода составит 0,1%. Его атомы размещаются в дефектных узлах решетки.
Феррит по своим параметрам близок к железу.
Промышленное получение
Железоуглеродистые сплавы производятся металлургическими заводами из разных компонентов. Основа — железо с углеродом. Этапы производственного процесса:
- Подготовка расходного сырья (руды). Ее сортируют по размерам кусков, химическому составу. Бедные руды обогащаются требуемыми компонентами. Пустые породы удаляются.
- Подготовка топлива. Коксовый уголь проходит процедуру грохочения. Она нужна, чтобы удалить из топлива посторонние примеси, которые могут привести к тепловым потерям при плавке руды.
- Подготовка флюса. Вещества, которые будет применяться для производства чугуна измельчают. При этом отсеивается мелочь, удаляются сторонние примеси.
- Загрузка расходных материалов, руды в доменную печь. Сначала она заполняется коксом, сверху выкладывается руда, поверх нее засыпается еще один слой кокса. Внутрь вдувается разогретый воздух для поддержания температуры плавления металла. При сгорании кокса выделяется большое количество углекислого газа, который проходит через остатки кокса, образуя соединение СО. В процессе восстановления железо набирается твердости. Постепенно углерод начинает растворяться. Жидкий чугун подается к специальным ковшам, из которых разливается по формам.
Для производства чугуна применяются большие доменные печи. Их высота может достигать 30 м, а внутренний диаметр — 12 м.

Доменная печь (Фото: Instagram / viktormacha)
Аустенит в сталях
Наличие аустенита в стальных сплавах придает им определенные свойства. Детали и узлы, произведенные из подобных сталей, предназначаются для работы в средах, содержащие агрессивные компоненты, например, на предприятиях, перерабатывающих разные кислоты.
Стали этого класса отличаются высоким уровнем легирования, во время кристаллизации формируется гранецентрированная решетка. Такая структура не подвержена изменению даже под воздействием глубокого холода.
Стали этого типа можно разделить на два типа отличающиеся друг от друга составом. В первых, содержатся такие вещества как железо, никель, хром. При этом общее количество добавок не может превышать 55%. Ко второй группе относят никелевые и железоникелевые композиции. В никелевых композициях, его содержание превышает 55%. В железоникелевых составах соотношение никеля и железа составляет 1:5, а количество никеля начинается от 65%.
Такое количество никеля обеспечивает повышенную пластичность, а хром, в свою очередь обеспечивает высокую коррозионную стойкость и жаропрочность. Применение других легирующих материалов позволяет выплавлять сплавы с уникальными эксплуатационными свойствами. Металлурги, составляя рецептуру сплавов, руководствуются будущим назначением сталей.
Для получения легированный сталей применяют ферритизаторы, которые придают постоянство аустенитам, к таким веществам относят ниобий, кремний и некоторые другие. Кроме них применяют углерод, марганец – их называют аустенизаторами.
Отжиг стали
Практикуется использование нескольких методов отжига. Принципиально различаются техники полного и неполного отжига. В первом случае происходит интенсивный нагрев аустенита до критической температуры, после чего осуществляется нормализация посредством охлаждения. Тут же происходит распад аустенита. Как правило, полный отжиг сталей производится в режиме 700-800 °С. Термическая обработка на таком уровне как раз активизирует процессы распада элементов феррита. Скорость охлаждения тоже поддается регулировке, например, обслуживающий печь персонал может управлять дверцей камеры, закрывая или открывая ее. Новейшие модели изотермических печей в автоматическом режиме могут осуществлять замедленное охлаждение в соответствии с заданной программой.

Что касается неполного отжига, то он производится при нагреве с температурой выше 800 °С. Однако имеют место серьезные ограничения по времени удержания критического температурного воздействия. По этой причине происходит неполный отжиг, в результате которого феррит не исчезает. Следовательно, не устраняется и множество недостатков структуры будущего материала. Зачем же нужен такой отжиг сталей, если он не улучшает физические качества? На самом деле именно неполная термическая обработка позволяет сохранить мягкую структуру. Конечный материал, возможно, потребуется не в каждой сфере применения, характерной для углеродистых сталей как таковых, но зато позволит с легкостью произвести механическую обработку. Мягкий доэвтектоидный сплав без особых затруднений поддается резке и дешевле обходится в процессе изготовления.
Цементит: формы существования
Так называют соединение углерода и железа. Это компонент чугуна и некоторых сталей. В него входит 6,67% углерода.
В его кристалл входит несколько октаэдров, они расположены друг по отношению к другу с некоторым углом. Внутри каждого из них расположен атом углерода. В результате такого построения получается следующая картина – один атом вступает в связь с несколькими атомами железа, а железо в свою очередь связано с тремя атомами этого элемента.

Кристаллическая решетка цементита
У этого вещества имеются все свойства, которые присущи металлам – электропроводность, своеобразным блеском, высокая теплопроводность. То есть, смесь железа и углерода, ведет себя как металл. Этот материал обладает определенной хрупкостью. Большая часть его свойств определена сложным строением кристаллической решетки.
Этот материал плавится при 1600 градусах Цельсия. Но на этот счет существует несколько мнений, одни исследователи считают, что его температура плавления лежит в диапазоне от 1200 до 1450, другие определяют, что верхний уровень равен 1300 °С.
Первичный цементит
Металлурги разделяют три типа этого вещества – первичный, вторичный, третичный.

Первичный, получается из жидкости при закалке сплавов, которые содержат в себе 5,5% углерода. Первичный имеет форму в виде крупных пластин.
Вторичный
Этот элемент получается из аустенита при охлаждении последнего. На диаграмме этот процесс этот процесс можно видеть по диаграмме Fe – C. Цементит представлен в виде сетки, размещенной по границам зерен.
Третичный
Этот тип, является производным от феррита. Он имеет форму иголок.
В металлургии существуют и другие формы цементита, например, цементит Стеда и пр.
Другие структурные составляющие в системе железо углерод
Перлит
Перлит – это механическая смесь, которая состоит из феррита и цементита. Ледебурит представляет собой переменный раствор.

При температуре от 1130 и до 723 °С в его состав входят аустенит и цементит. При более низких температурах он состоит из аустенит заменяет феррит.
Свойства
Характеристики железоуглеродистых сплавов:
- Плотность — до 7,9 г/см3.
- Температура плавления — до 1520 °C.
- Удельная теплоемкость — 462 Дж/(кг·°C) при температуре окружающей среды не более 20 °C.
- Удельная теплота плавления — 84 кДж/кг.
- Коэффициент теплопроводности — 30 Вт/(м·К) при температуре 100 °С.
- Коэффициент линейного теплового расширения — 11,5·10-6 1/°C.
Железоуглеродистые сплавы производятся промышленными предприятиями. К ним относятся разные виды стали, чугуна. Они применяются в разных сферах промышленности.
Узловые критические точки диаграммы состояния системы железо углерод
На диаграмме железо углерод отмечено некоторое количество точек, называемых критичными. Каждая точка несет в себе информацию о температуре, долевом содержании углерода и описанием того, что именно происходит в этом месте.
Всего существует 14 этих критичных точек.
Например, А, говорит о том, что при температуре 1539 °С и при нулевом содержании углерода происходит плавление чистого железа. D говорит о том, что при температуре 1260 возможно плавление Fe3c.
сплавы железа с углеродом на основе железа. Варьируя состав и структуру, получают Ж. с. с разнообразными свойствами, что делает их универсальными материалами. Различают чистые Ж. с. (со следами примесей), получаемые в небольших количествах для исследовательских целей, и технические Ж. с. — стали (См. Сталь) (до 2%С) и Чугуны (св. 2% С), мировое производство которых измеряется сотнями млн. т. Технические Ж. с. содержат примеси. Их делят на обычные (фосфор Р, сера S, марганец Mn, кремний Si, водород Н, азот N, кислород О), легирующие (хром Cr, никель Ni, молибден Mo, вольфрам W, ванадий V, титан Ti, кобальт Со, медь Cu и др.) и модифицирующие (магний Mg, церий Ce, кальций Ca и др.). В большинстве случаев основой, определяющей строение и свойства сталей и чугунов, является система Fe — С. Начало научному изучению этой системы положили русские металлурги П. П. Аносов (1831) и Д. К. Чернов (1868). Аносов впервые применил микроскоп при исследовании Ж. с., а Чернов установил их кристаллическую природу, обнаружил дендритную кристаллизацию и открыл в них превращения в твёрдом состоянии. Из зарубежных учёных, способствовавших созданию диаграммы состояния Fe — С сплавов, следует отметить Ф. Осмонда (Франция), У. Ч. Робертса-Остена (Англия), Б. Розебома (Голландия) и П. Геренса (Германия).
Фазовые состояния Ж. с. при разных составах и температурах описываются диаграммами стабильного (рис. 1, а) и метастабильного (рис. 1, б) равновесий. В стабильном состоянии в Ж. с. встречаются жидкий раствор углерода в железе (Ж), три твёрдых раствора углерода в полиморфных модификациях железа (табл. 1)
α-раствор (α-феррит), γ-раствор (аустенит) и δ-раствор (δ-феррит), и графит (Г). В метастабильном состоянии в Ж. с. встречаются Ж, α-, γ-, δ-растворы и карбид железа Fe3C — цементит (Ц). Области устойчивости Ж. с. в однофазных и двухфазных состояниях указаны на диаграммах. При некоторых условиях в Ж. с. могут существовать в равновесии и три фазы. При температурах НВ возможно перитектич. равновесие δ + γ + Ж, E’C’F’ — эвтектическое стабильное равновесие γ + Ж + Г; при ECF — эвтектическое метастабильное равновесие γ + Ж + Ц; при P'S'K' — эвтектоидное стабильное равновесие α + γ + Г', при PSK — эвтектоидное метастабильное равновесие α + γ + Ц. Диаграммы а и б вычерчиваю и в одной координатной системе (рис. 1, в). Такая сдвоенная диаграмма наглядно характеризует относительное смещение однотипных линий равновесия и облегчает анализ Ж. с., содержащих стабильные и метастабильные фазы одновременно.
Основной причиной появления в Ж. с. высокоуглеродистой метастабильной фазы в виде цементита являются трудности формирования графита. Образование графита в жидком растворе Ж и твёрдых растворах α и γ связано с практически полным удалением атомов железа из участков сплава, где зарождается и растет графит. Оно требует значительных атомных передвижений. Если Ж. с. охлаждаются медленно или длительно выдерживаются при повышенных температурах, атомы железа успевают удалиться из мест, где формируется графит, и тогда возникают стабильные состояния. При ускоренном охлаждении и недостаточных выдержках удаление малоподвижных атомов железа задерживается, почти все они остаются на месте, и тогда в жидких и твёрдых растворах зарождается и растет цементит. Необходимая для этого диффузия легкоподвижных при повышенных температурах атомов углерода, не требующая больших выдержек, успевает происходить и при ускоренном охлаждении. Помимо основных фаз, указанных на диаграммах, в технических Ж. с. встречаются небольшие количества и др. фаз, появление которых обусловлено наличием примесей. Часто встречаются сульфиды (FeS, MnS), фосфиды (Fe3P), окислы железа и примесей (FeO, MnO, Al2O3, Cr2O3, TiO2 и др.), нитриды (FeN, AlN) и др. неметаллические фазы. Точечными линиями на диаграммах отмечены точки Кюри, наблюдающиеся в Ж. с. в связи с магнитными превращениями феррита (768°С) и цементита (210°С).
Строение Ж. с. определяется составом, условиями затвердевания и структурными изменениями в твёрдом состоянии. В зависимости от содержания углерода Ж. с. делят на стали и чугуны. Стали с концентрацией углерода, меньшей чем эвтектоидная S' и S (табл. 2), называют доэвтектоидными, а более высокоуглеродистые — заэвтектоидными. Чугуны с концентрацией углерода, меньшей чем эвтектическая C 1 и С, называют доэвтектическими, а более высокоуглеродистые — заэвтектическими.
Строение затвердевших Ж. с. существенно изменяется при дальнейшем охлаждении. Эти изменения обусловлены полиморфными превращениями железа, уменьшением растворимости в нём углерода, графитизацией цементита. Структура может изменяться в твёрдом состоянии в результате процессов рекристаллизации твёрдых растворов, сфероидизации кристаллов (из неравноосных становятся равноосными), коалесценции (одни кристаллы цементита укрупняются за счёт других) высокоуглеродистых фаз.
Полиморфные превращения Ж. с. связаны с перестройками гранецентрированной кубической (ГЦК) решётки γ-Fe и объёмноцентрированной решётки (ОЦК) α- и δ-Fe
В зависимости от условий охлаждения и нагревания полиморфные превращения твёрдых растворов происходят разными путями. При небольших переохлаждениях (и перегревах) имеет место т. н. нормальная перестройка решёток железа, осуществляющаяся в результате неупорядоченных индивидуальных переходов атомов от исходной фазы к образующейся; она сопровождается диффузионным перераспределением углерода между фазами. При больших скоростях охлаждения или нагревания полиморфные превращения твёрдых растворов происходят бездиффузионным (мартенситным) путём. Решётка железа перестраивается быстрым сдвиговым механизмом в результате упорядоченных коллективных смещений атомов без диффузионного перераспределения углерода между фазами. Например, при закалке Ж. с. в воде γ- раствор переходит в α- раствор того же состава. Этот пересыщенный углеродом α- раствор называют мартенситом (рис. 2, е). Превращения при промежуточных условиях могут совмещать в себе сдвиговую перестройку решётки железа с диффузионным перераспределением углерода (бейнитное превращение). Формирующиеся при этом структуры существенно различны. В первом случае образуются равноосные с малым числом дефектов кристаллы твёрдого раствора (рис. 2, а). Во втором и третьем — игольчатые и пластинчатые кристаллы (рис. 2, е) с многочисленными двойниками и линиями скольжения. Структура Ж. с. изменяется также и в связи с изменением растворимости углерода в α- и γ-железе при охлаждении и нагревании. При охлаждении растворы пересыщаются углеродом и выделяются кристаллы высокоуглеродистых фаз (цементита и графита). При нагревании имеющиеся высокоуглеродистые фазы растворяются в α- и γ-фазах.
Зарождение и рост кристаллов цементита в пересыщенных растворах происходит обычно с большей скоростью, чем образование графита, и поэтому Ж. с. часто метастабильны. В зависимости от переохлаждения цементит, выделяющийся из твёрдого раствора, может иметь вид равноосных кристаллов, пограничной сетки, пластин и игл (рис. 2, г, д). При высокотемпературных выдержках кристаллы цементита сфероидизируются; может происходить и процесс коалесценции. Если Ж. с., содержащие цементит, длительно выдерживать при повышенных температурах, происходит графитизация — зарождается и растет графит, а цементит растворяется, Этот процесс используется при производстве изделий из графитизированной стали и ковкого чугуна (рис. 2, м). Важную роль при формировании структуры Ж. с. в твёрдом состоянии играет эвтектоидный распад т-раствора на α-раствор и высокоуглеродистую фазу. При очень малых переохлаждениях образуются феррит и графит (рис. 2, м), при небольшом увеличении переохлаждения — феррит и сфероидизированный цементит (рис. 2, г), затем (рис. 2, в) смесь феррита и цементита приобретает пластинчатое строение перлита, тем более тонкое, чем больше переохлаждение. При персохлаждениях, измеряемых сотнями градусов, эвтектоидный распад подавляется, и γ- раствор превращается в мартенсит (рис. 2, е). Строение Ж. с. можно изменять в широких пределах. Основными методами управления структурой Ж. с. являются изменения химического состава, условий затвердевания, пластической деформации, термической и термомеханической обработок. Меняя фазовый состав, величину, форму, распределение и дефектность кристаллов, можно широко варьировать и свойства Ж. с. Например, важнейшие при эксплуатации Ж. с. механические свойства изменяются в следующих пределах: твёрдость от 60 до 800 HB; предел прочности 2·10 4 —3,5·10 6 н/см 2 (2·10 3 —3,5·10 5 кгс/см 2 ); относительное удлинение от 0 до 70%.
Лит.: Д. К. Чернов и наука о металлах, под ред. Н. Т. Гудцова, Л.—М., 1950; Бочвар А. А., Металловедение, 5 изд., М., 1956; Лившиц Б. Г., Металлография, М., 1963; Тыркель Е., История развития диаграммы железо — углерод, пер. с польск., М., 1968; Бунин К. П., Баранов А. А., Металлография, М., 1970.

Рис. 2м. Типичные структуры железоуглеродистых сплавов. Ковкий чугун (включения графита в ферритной основе). Увеличено в 150 раз.
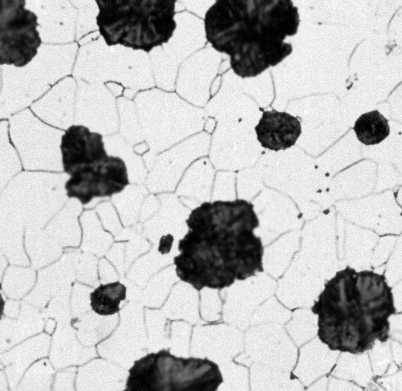
Рис. 2з.Типичные структуры железоуглеродистых сплавов. Серый чугун с шаровидным графитом на ферритной основе.
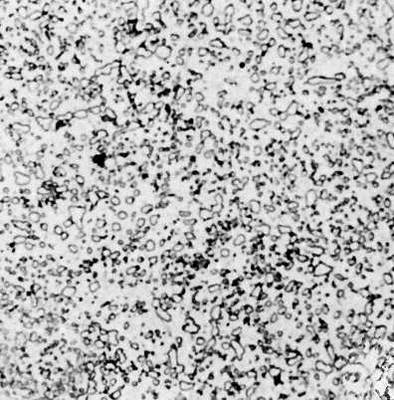
Рис. 2г. Типичные структуры железоуглеродистых сплавов. Сталь с 0,91% С (сфероидизированный цементит в феррите). Увеличено в 500 раз.
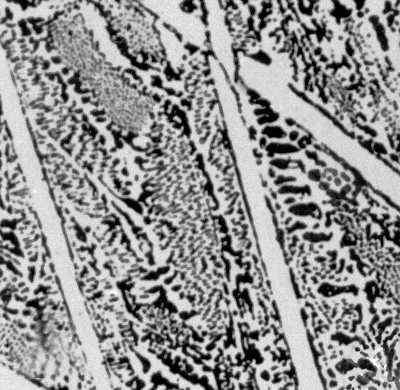
Рис. 2л. Типичные структуры железоуглеродистых сплавов. Белый заэвтектический чугун (пластины первичного цементита и ледебурит). Увеличено в 150 раз.

Рис. 2ж. Типичные структуры железоуглеродистых сплавов. Серый чугун: разветвленные пластины графита (тёмные) и зёрна феррита.

Рис. 2в. Типичные структуры железоуглеродистых сплавов. Сталь с 0,8% С (пластинчатый перлит). Увеличено в 500 раз.
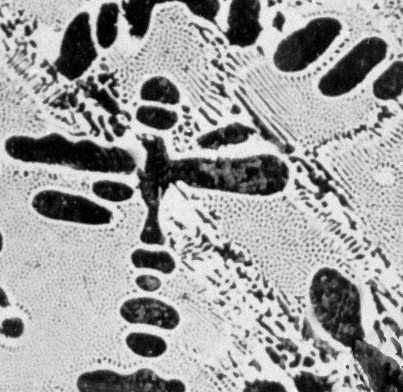
Рис. 2к. Типичные структуры железоуглеродистых сплавов. Белый доэвтектический чугун: дендриты первичного аустенита (и ледебурит). Увеличено в 150 раз.

Рис. 2е. Типичные структуры железоуглеродистых сплавов. Сталь с 0,85% С (пластины мартенсита и остаточный аустенит). Увеличено в 500 раз.
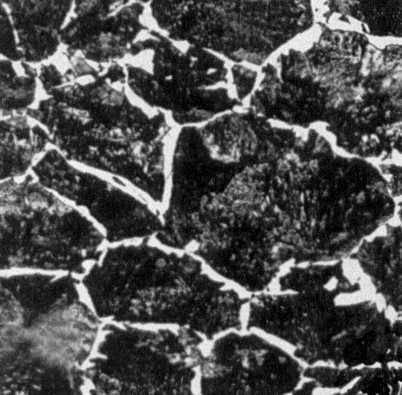
Рис. 2б. Типичные структуры железоуглеродистых сплавов. Сталь с 0,65% С (сетка феррита и перлит). Увеличено в 150 раз.
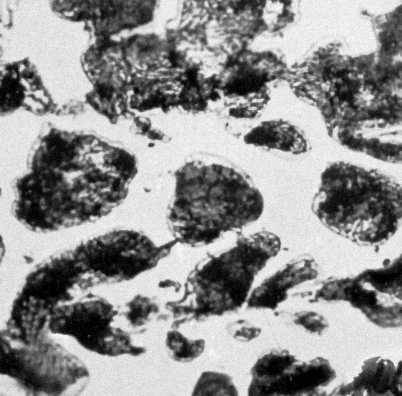
Рис. 2и. Типичные структуры железоуглеродистых сплавов. Белый доэвтектический чугун (эвтектический монолитный цементит и перлит). Увеличено в 500 раз.
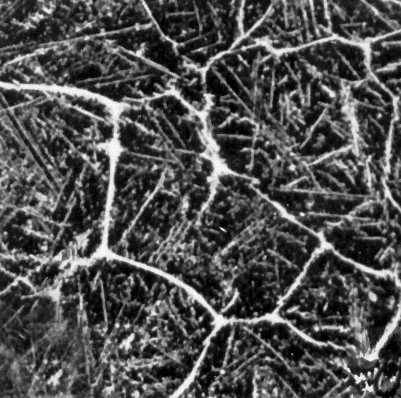
Рис. 2д. Типичные структуры железоуглеродистых сплавов. Сталь с 1,18% С: сетка и пластины цементита (светлые) в перлите. Увеличено в 150 раз.

Рис. 2а. Типичные структуры железоуглеродистых сплавов. Сталь с 0,15% С: зёрна феррита (светлые) и участки перлита (тёмные). Увеличено в 150 раз.
Большая советская энциклопедия. — М.: Советская энциклопедия . 1969—1978 .
Полезное
Смотреть что такое "Железоуглеродистые сплавы" в других словарях:
ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ — сплавы Fe с С на основе Fe. Варьируя состав и структуру, получают железоуглеродистые сплавы с разнообразными свойствами, что делает их универсальными материалами. Различают чистые железоуглеродистые сплавы для исследовательских целей (со следами… … Металлургический словарь
ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ — сплавы Fe (основа) с С. Различают чистые железоуглеродистые стали (со следами примесей), получаемые в небольших количествах для исследовательских целей, и технические железоуглеродистые стали стали (до 2% С) и чугуны (св. 2% С), содержащие… … Большой Энциклопедический словарь
железоуглеродистые сплавы — сплавы Fe (основа) с C. Различают чистые железоуглеродистые сплавы (со следами примесей), получаемые в небольших количествах для исследовательских целей, технические железоуглеродистые сплавы стали (до 2% C) и чугуны (свыше 2% C), содержащие… … Энциклопедический словарь
Чёрные металлы, чёрные сплавы — Чёрными металлами условно называют железо и его сплавы чугуны, стали, иногда и ферросплавы. Остальные металлы и сплавы, в отличие от чёрных металлов и сплавов, называют цветными. А П. Гуляев подразделяет чёрные металлы следующим образом: Железные … Металлургический словарь
Железные сплавы — металлические системы, одним из компонентов которых (как правило, преобладающим) служит железо. Ж. с. содержат обычно примеси (марганец, кремний, серу, фосфор и др.), а также Легирующие элементы. Важнейшими Ж. с., наиболее часто… … Большая советская энциклопедия
ЖЕЛЕЗНЫЕ СПЛАВЫ — металлич. системы, одним из компонентов к рых (как правило, преобладающим) служит железо. Ж. с. содержат обычно примеси (марганец, кремний, серу, фосфор и др.), а также легирующие элементы (см. Легирование, Легированная сталь). Важнейшими Ж. с.,… … Большой энциклопедический политехнический словарь
Металловедение — наука, изучающая связи состава, строения и свойств металлов и сплавов, а также закономерности их изменения при тепловых, механических, физико химических и др. видах воздействия. М. научная основа изысканий состава, способов изготовления и … Большая советская энциклопедия
ЧУГУН — (тюркское) сплав железа с углеродом (С обычно более 2%, массовая доля), содержащий также постоянные примеси (Si, M, P и S), а иногда и легирующие элементы. Чугун важнейший первичный продукт черной металлургии (смотри Доменное производство),… … Металлургический словарь
Закалка — термическая обработка материалов, заключающаяся в их нагреве и последующем быстром охлаждении с целью фиксации высокотемпературного состояния материала или предотвращения (подавления) нежелательных процессов, происходящих при его… … Большая советская энциклопедия
СТАЛЬ — (от немецкого Stahl) деформируемый (ковкий) сплав железа с углеродом (до 2%) и другими элементами. Сталь получают главным образом из смеси чугуна, выплавляемого в доменных печах, со стальным ломом. Основные агрегаты для производства стали… … Металлургический словарь
Читайте также:

