Прямой обратимый цикл карно кратко
Обновлено: 05.07.2024
Цикл Карно - обратимый круговой процесс, в котором совершается наиболее полное превращение теплоты в работу (или работы в теплоту). Термический КПД и холодильный коэффициент цикла Карно не зависят от физических свойств рабочего тела. Прямой (обратный) цикл Карно имеет максимально возможный термический КПД (холодильный коэффициент) в заданном интервале температур.
Т.к. t цикла Карно всегда больше 1, не зависит от рода рабочего тела и имеет наибольшее значение по сравнению с t любых других циклов, ограниченных тем же интервалом температур, то:
а) никакими новыми конструкциями тепловых двигателей или применением новых рабочих тел нельзя всю подведенную в цикле теплоту превратить в полезную работу;
б) для увеличения t нужно стремиться к таким процессам, образующим цикл, в которых средняя температура подвода теплоты была бы как можно больше, а средняя температура отвода теплоты - как можно меньше.
Прямой цикл Карно


Рис. 6.2. Прямой цикл Карно: а- в vP-диаграмме; б- в sT-диаграмме
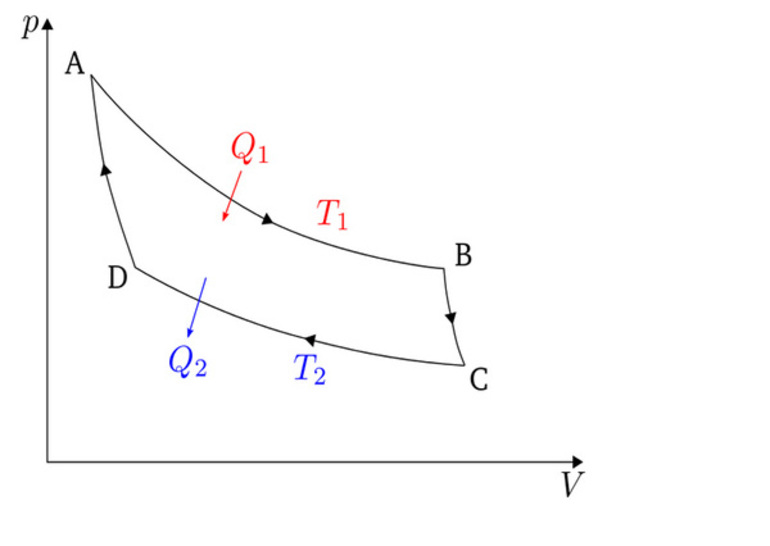
Два процесса 1-2 и 3-4 (рис. 6.2) протекают при постоянных температурах, причем Т1- температура горячего источника (нагревателя), Т2 – температура холодного источника (холодильника, т.е. Т1Т2. Процессы 2-3 и 4-1 - адиабатные. В соответствии с первым законом термодинамики

Внутренняя энергия при Т = const не меняется, а изменение внутренней энергии в адиабатных процессах, протекающих в одном и том же интервале температур, одно и то же, поэтому работа цикла:

и термический КПД

Согласно sT-диаграмме:

, тогда

. (6.4)
Таким образом, КПД цикла Карно определяется обращением температур горячего и холодного источников теплоты. Его значение возрастает при увеличении Т1 или уменьшении Т2. В случае отсутствия перепада температур t = 0. Цикл Карно состоит из обратимых процессов и поэтому является обратимым.
Обратный цикл Карно


Рис. 6.2. Обратный Карно: а- в vP-диаграмме; б- в sT-диаграмме

Обратный цикл Карно характеризуется затрачиваемой извне работой . При этом теплота от холодного источника передается горячему. Это цикл холодильной машины. Ее холодильный коэффициент всегда больше 1:

(6.5)
Аналитическое выражение iIзакона термодинамики.
Для обратимого цикла Карно имеем:

,
тогда или.
Если учесть в этом соотношении, что q1 0 (теплота подводится к рабочему телу) и q20 (теплота отводится от рабочего тела), то
или (6.6)
Отношение подводимой или отводимой теплоты к соответствующей абсолютной температуре называется приведенной теплотой. Выражение (6.6) показывает, что алгебраическая сумма приведенных теплот для обратимого цикла Карно равна нулю, т.е.

. (6.7)
Отношениесчитаютполным дифференциалом функции состояния , называемой энтропией. Т.к.dq = Tds, то

(6.8)
Таким образом, алгебраическая сумма приведенных теплот для любого обратимого цикла равна нулю. Энтропия рабочего тела в результате совершения произвольного обратимого цикла не изменяется.
Уравнение (6.8), выведенное Клаузиусом в 1854 году, представляет собой аналитическое выражение II закона термодинамики для произвольного обратимого цикла и называется первым интегралом Клаузиуса.
В цикле с необратимыми процессами при прочих равных условиях работа, совершаемая рабочим телом меньше, чем в цикле с обратимым процессом, и при одинаковх температурах источника теплоты и холодильника
Поэтому при наличии в цикле необратимых процессов:

0 (6.9)
или после интегрирования по контуру

0 (6.10)
Это неравенство представляет собой аналитическое выражение II закона термодинамики для произвольного необратимого цикла и называется вторым интегралом Клаузиуса.
Объединяя (6.7) и (6.10), можно записать одно уравнение II закона термодинамики для обратимых (=) и необратимых () циклов:

0 (6.11)
Энтропия есть функция состояния рабочего тела, поэтому изменение энтропии как для обратимого, так и необратимого процессов будет одним и тем же.
Для элементарного необратимого процесса
(6.12)
В общем виде для любого процесса изменение энтропии удовлетворяет соотношению

, (6.13)
где dq - количество теплоты, полученное телом от источника теплоты; Т- абсолютная температура источника теплоты. Знак равенства относится к обратимым, знак неравенства - к необратимым процессам.
Следует различать понятия энтропия тела и энтропия системы.
Энтропия не является функцией состояния системы, состоящей из нескольких тел (рабочее тело, холодильники и источники теплоты), каждое из которых характеризуется своими параметрами. Поэтому на изменение энтропии системы влияет характер процесса теплообмена между рабочим телом и источником теплоты. При протекании обратимых процессов энтропия системы остается постоянной; при необратимых процессах энтропия системы возрастает.
Если в адиабатной изолированной системе протекают только обратимые процессы, то
ds = dq/T,
для адиабатной системы это уравнение принимает вид: dq = Tds = 0
Так как Т 0, то для всей системы ds = 0 и s = const.
Таким образом, если в изолированной адиабатной системе протекают только обратимые процессы, то энтропия всей системы остается величиной постоянной.
Для адиабатной системы при наличии в ней необратимых процессов:
.
Т.к. dq = 0, то для адиабатной изолированной системы ds 0, т.е. происходит увеличение энтропии.
В термодинамике большое значение имеет понятие работы, которую совершает система при изменении своего состояния и условий, при которых получается максимальная работа.
Получение работы возможно только от такой системы, которая не находится в равновесном состоянии с окружающей средой. По мере совершения работы система будет приближаться к равновесному состоянию со средой. Тепловая энергия, переданная в окружающую среду, становится полностью неработоспособной, т.к. при этом происходит выравнивание температур источника и приемника. Очевидно, наибольшая работа в системе может быть совершена при достижении в ней равновесного состояния путем обратимых процессов.
Максимальная работоспособность системы, получаемая в обратимом цикле Карно в температурном интервале от до, называетсяэксергией (ex).

. (6.14)
Работа необратимого цикла Карно, в котором теплота передается рабочему телу при температурениже температуры нагревателя:

. (6.15)

. (6.17)

Эксергия является обобщенной качественной и количественной характеристикой для потока теплоты и потока вещества, зависящей одновременно от параметров системы и окружающей среды. В отличии от энергии в реальных процессах, эксергия количественно не сохраняется. Всякая необратимость в системе приводит к уменьшению работоспособности, т.е. к потерям энергии. Уменьшение работы ведет к увеличению энтропии :

. (6.18)
В 1824 г. С. Карно предложил цикл, которому было присвоено его имя. Прямой обратимый (т.е. состоящий только из равновесных, обратимых процессов) цикл Карно является идеальным циклом тепловых двигателей и осуществляется при наличии горячего источника постоянной температуры , и холодного источника постоянной температуры .
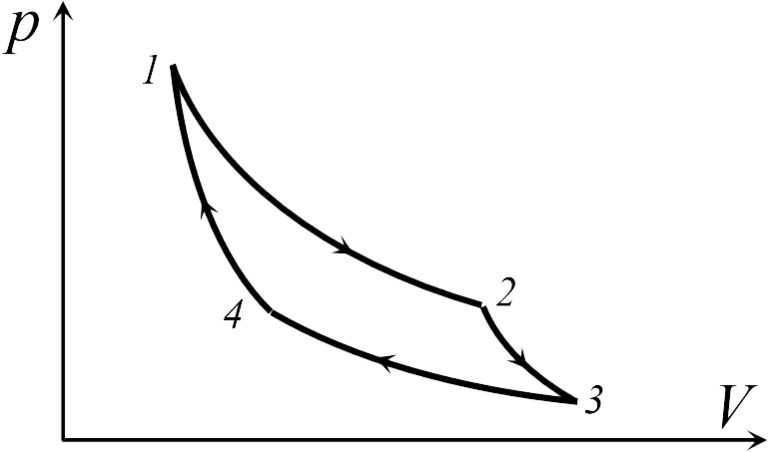
Цикл состоит из двух изотермических и двух адиабатных процессов. Его графическое изображение в pv-диаграмме и Ts-диаграмме приведено на рис. 1.14 и 1.15. В качестве рабочего тела в цикле Карно используется 1 кг идеального газа. Из начального состояния 1 газ расширяется по изотерме 1-2 при температуре , получая от горячего источника теплоту , которая полностью переходит в работу расширения (1.76);

В точке 2 рабочее тело отключается от горячего источника и расширяется по адиабате 2 - 3, совершая работу за счет внутренней энергии. В связи с этим температура газа понижается от , в точке 2 до в точке 3.


По уравнению (1.86) эта работа равна

В точке 3 газ сообщается с холодным источником и сжимается по изотерме
3 - 4, отдавая теплоту (1.76), равную работе, затраченной на сжатие, при постоянной температуре :

В точке 4 рабочее тело отключается от холодного источника, и газ адиабатным сжатием по 4 — 1 возвращается в начальное состояние, при этом температура газа повышается от до :

Из уравнений (1.100) и (1.102) следует, что в цикле Карно работа адиабатных процессов расширения и сжатия равна по абсолютной величине и обратна по знаку. Поэтому величины работ расширения и сжатия на результирующую работу цикла влияния не оказывают.
Для определения значения термического к.п.д. цикла Карно воспользуемся формулой (1.97) и изображением цикла Карно (см. рис. 1.15) в Ts-диаграмме:

Из Ts-диаграммы цикла Карно имеем:

Но для адиабатных процессов 2-3 и 4-1 получаем, что = :


(1.107)
Полученное уравнение позволяет сделать следующие выводы:
1. Термический к.п.д. цикла Карно зависит только от абсолютных температур горячего источника и холодного источника .
2. Термический к.п.д. тем выше, чем выше температура горячего источника и чем ниже температура холодного источника.
3. Так как температура холодного источника всегда положительна, то к.п.д. цикла Карно всегда меньше единицы. Значит, что теплоту , подводимую к рабочему телу, невозможно полностью превратить в работу — часть ее в количестве передается холодному источнику.
4. В уравнении (1.107) видно, что термический к.п.д. цикла Карно не зависит от природы рабочего тела (газа).
При помощи Ts-диаграммы несложно доказать еще одно важное свойство цикла Карно: в заданном интервале температур , и ; термический к.п.д. цикла Карно имеет наибольшее значение по сравнению с любым другим произвольным циклом, и это позволяет считать его эталоном.
На рис. 1.15 показаны произвольный цикл (а, Ь, с, d) и цикл Карно (/, 2, 3, 4), протекающие в интервале температур , и . Оба цикла прямые и обратимые.
Из общего уравнения термического к.п.д.. следует, что термический к.п.д. будет тем больше, чем меньше отношение .

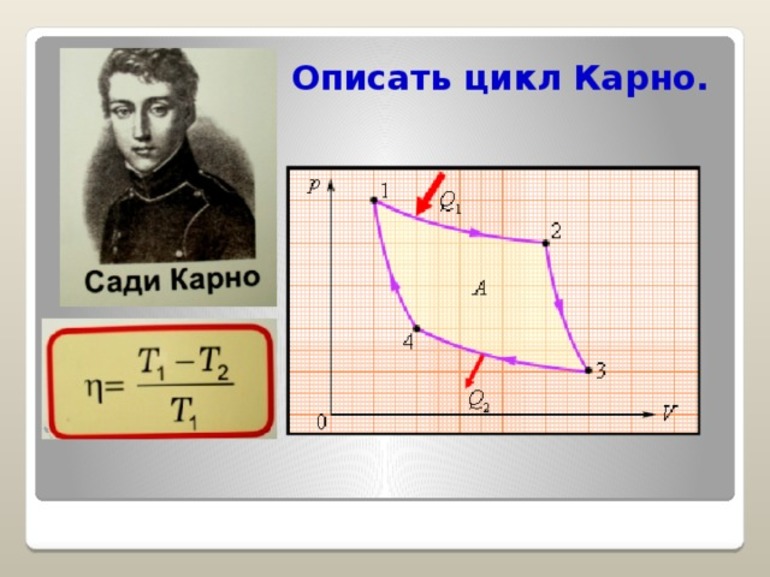
Краткая биография
Николя Леонард Сади Карно, сын высокопоставленного военачальника Лазаря Николая Маргарита Карно, родился в Париже в 1796 году. Его отец ушёл из армии в 1807 году, чтобы обучить Николаса и его брата Ипполита — оба получили широкое домашнее образование, включающее:
- науку;
- искусство;
- иностранные языки;
- музыку.
В 1812 году 16-летний Николас Карно был принят в Высшую политехническую школу в Париже. Его учителями были Джозеф Луи Гей-Люссак, Симеон Дени Пуассон и Андре-Мари Ампер, а сокурсниками — будущие учёные Клод-Луи Навье и Гаспар-Гюстав Кориолис. Во время учёбы в школе Карно проявил особый интерес к теории газов и решению задач промышленной инженерии. После окончания университета он поступил во французскую армию в качестве военного инженера и прослужил до 1814 года.
Освободившись от ограничений военной жизни, Карно начал широкий спектр исследований, которые продолжались, несмотря на многочисленные перерывы, до само́й смерти. В дополнение к частным занятиям он посещал курсы:
- в Сорбонне;
- Коллеж де Франс.
- в Школе шахт;
- в Консерватории искусств.
В последней он стал другом Николаса Клемента, который преподавал курс прикладной химии, а затем занимался важными исследованиями паровых двигателей и теории газов.
Одним из особых интересов Карно было промышленное развитие, которое он изучал во всех его аспектах. Он часто посещал фабрики и мастерские, читал новейшие теории политической экономии и оставлял в своих заметках подробные предложения по таким актуальным проблемам, как налоговая реформа. Помимо этого, его деятельность и способности охватили математику и изобразительное искусство.
После публикации Карно продолжил исследования, выводы из которых сохранились в его рукописных заметках. Однако реорганизация корпуса Генерального штаба вынудила Карно вернуться на службу в 1827 году в звании капитана. После менее чем годовой работы в качестве военного инженера Карно ушёл в отставку навсегда и вернулся в Париж. Он снова сосредоточил своё внимание на проблемах конструкции двигателя и теории тепла.
Работы учёного
- изотермическое расширение при подаче пара в цилиндр;
- адиабатическое расширение;
- изотермическое сжатие в конденсаторе.
Эссе как по методам, так и по целям похоже на многие статьи, опубликованные между 1818 и 1824 годами такими учёными, как Хашетт, Навье, Пети и Комбес. Работа Карно, однако, отличается своим тщательным, чётким анализом используемых единиц и концепций и тем, что он использует как адиабатическую рабочую стадию, так и изотермическую стадию. Отточенный характер, в отличие от его грубых заметок, делало её предназначенной для публикации, хотя она оставалась неизвестной в рукописи до 1966 года.
- Существует ли установленный предел для движущей силы тепла и, следовательно, для улучшения паровых двигателей?
- Есть ли агенты предпочтительнее пара в производстве этой движущей силы?
Обе проблемы были своевременными и, хотя французские инженеры исследовали их в течение десятилетия, не было принято общепринятых решений. В отсутствии чёткой концепции эффективности предлагаемые конструкции паровых двигателей оценивались в основном по практичности, безопасности и экономии топлива.
Некоторые инженеры считали воздух, углекислоту и спирт лучшим рабочим веществом, чем пар. Обычным подходом к этим проблемам было либо эмпирическое исследование расхода топлива и выходной мощности отдельных двигателей, либо применение математической теории газов к абстрактным операциям конкретного типа двигателя. В своём выборе проблем Карно был твёрд в этой инженерской традиции, однако его метод был радикально новым и являлся сутью его вклада в науку о тепле.
Предыдущая работа над паровыми машинами, как видел Карно, провалилась из-за отсутствия достаточно общей теории, применимой ко всем тепловым двигателям и основанной на установленных принципах. В качестве основы своего исследования Карно тщательно изложил три предпосылки. Первой была невозможность вечного движения — принцип, который долгое время предполагался в механике. В своей второй предпосылке Карно использовал калорийную теорию тепла, которая, несмотря на некоторую оппозицию, была принятой и самой развитой, доступной теорией тепла.
Принципы работы цикла Карно
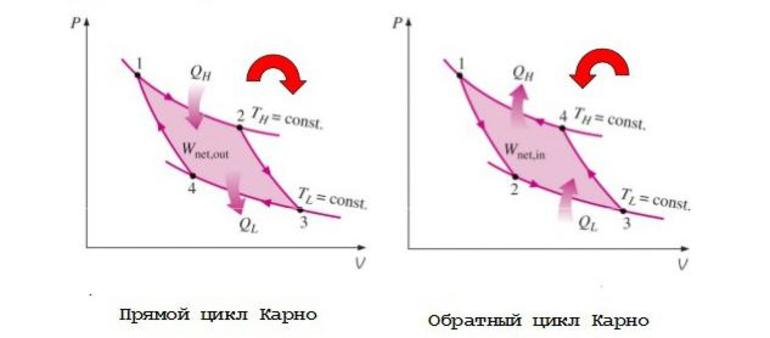
Этот теоретический идеальный круговой термодинамический цикл был предложен французским физиком Сади Карно в 1824 году. Он обеспечивал максимально возможный предел эффективности для любого классического термодинамического двигателя во время преобразования тепла в работу или, наоборот, эффективность системы охлаждения при создании разницы температур при приложении работы к системе. Фактический термодинамический цикл является теоретической конструкцией.
Каждая термодинамическая система существует в определённом состоянии. Когда система проходит через ряд различных явлений и, наконец, возвращается в исходное состояние, говорят, что произошёл термодинамический цикл. В процессе прохождения этого цикла система может выполнять работу, например, перемещая поршень, тем самым действуя, как тепловой двигатель.
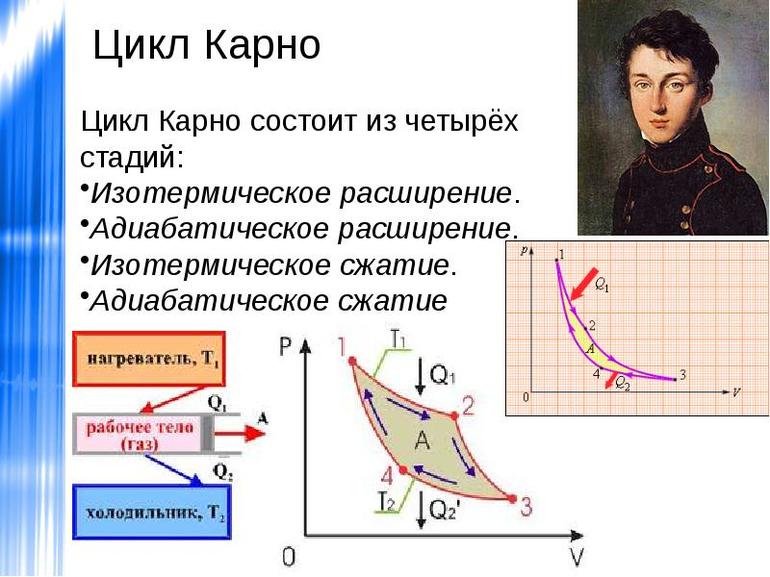
Из каких процессов состоит Цикл Карно при работе в качестве теплового двигателя:
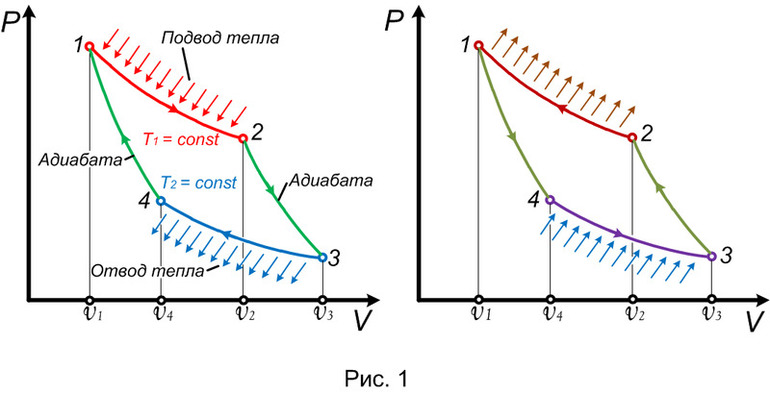
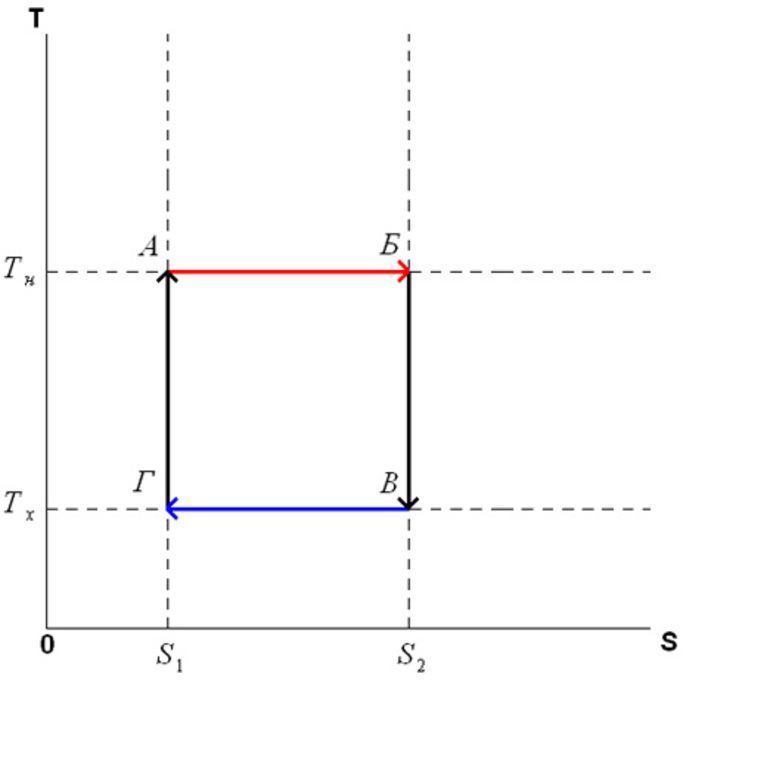
Во время цикла произвольное количество энтропии S извлекается из горячего резервуара (нагревателя) и осаждается в холодном резервуаре. Поскольку в обоих резервуарах изменения объёма не происходит, они не работают, и в течение цикла количество энергии T h ΔS извлекается из горячего резервуара, а меньшее количество энергии T c ΔS откладывается в холодном резервуаре. Разница в двух энергиях (T h -T c) ΔS равна работе, проделанной двигателем.
Поведение двигателя или холодильника Карно лучше всего понять с помощью диаграммы, в которой координатами являются температура и энтропия. Термодинамическое состояние определяется точкой на графике с энтропией (S) в качестве горизонтальной оси и температуры (T) в качестве вертикальной оси. Для простой замкнутой системы любая точка на графике будет представлять конкретное состояние системы. Термодинамический процесс будет состоять из кривой, соединяющей начальное состояние (A) и конечное состояние (B), и представляющей собой количество тепловой энергии, передаваемой в процессе.
Если процесс движется к большей энтропии, площадь под кривой будет количеством тепла, поглощённого системой. Когда процесс движется к меньшей энтропии, это будет количество отводимого тепла. Для любого циклического процесса есть верхняя часть цикла и нижняя часть. Для цикла по часовой стрелке область под верхней частью будет тепловой энергией, поглощённой в течение цикла, тогда как область под нижней частью будет тепловой энергией, удалённой во время цикла.
Площадь внутри цикла будет тогда разницей между ними, но поскольку внутренняя энергия системы должна вернуться к своему первоначальному значению, эта разница должна быть объёмом работы, которую должна совершать системой за цикл.
Перевёрнутый цикл
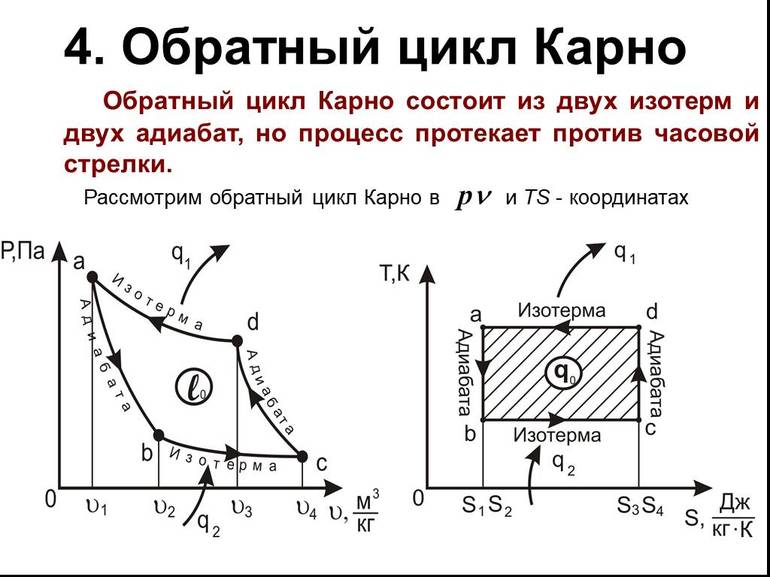
Описанный цикл теплового двигателя является полностью обратным циклом Карно. То есть все процессы, из которых он состоит, могут быть обращены вспять, и в этом случае цикл становится холодильным циклом Карно.
На этот раз цикл остаётся точно таким же, за исключением того, что направления любых тепловых и рабочих взаимодействий меняются местами. Тепло поглощается из низкотемпературного резервуара, отбрасывается в высокотемпературный резервуар, и для этого требуется работа. Диаграмма P-V обращённого цикла такая же, как и для цикла Карно, за исключением того, что направления процессов меняются местами.
Если же в цикле возникает передача теплоты при наличии разности температур, а такими являются все технические реализации термодинамических циклов, то цикл становится необратимым. КПД такого цикла будет всегда меньше, чем КПД цикла Карно.
Теорема Карно

Эта теорема является формальным утверждением этого факта: ни один двигатель, работающий между двумя тепловыми резервуарами, не может быть более эффективным, чем двигатель Карно, работающий между этими же резервуарами.
Следствие из теоремы Карно гласит: все реверсивные двигатели, работающие между одними и теми же тепловыми резервуарами, одинаково эффективны. Теоретический максимальный КПД теплового двигателя равён разнице в температуре между горячим и холодным резервуаром, делённой на абсолютную температуру горячего резервуара.
Исходя из этого, становится очевидным интересный факт: понижение температуры холодного резервуара будет иметь большее влияние на потолочную эффективность теплового двигателя, чем повышение температуры горячего резервуара на ту же величину. В реальном мире это труднодостижимо, так как холодный резервуар часто имеет существующую температуру окружающей среды.
Другими словами, максимальная эффективность достигается тогда, когда в цикле не создаётся новая энтропия, что было бы в случае, если, например, трение привело к рассеиванию работы в тепло. В противном случае, поскольку энтропия является функцией состояния, требуемый сброс тепла в окружающую среду для удаления избыточной энтропии приводит к (минимальному) снижению эффективности.
В мезоскопических тепловых двигателях работа за цикл обычно колеблется из-за теплового шума. Если цикл выполняется квазистатически, флуктуации исчезают даже на мезомасштабах. Но если цикл выполняется быстрее, чем время релаксации рабочего тела, колебания работы неизбежны. Тем не менее когда учтены рабочие и тепловые колебания, существует точное равенство, которое связывает экспоненциальное среднее значение работы, выполненной любым тепловым двигателем, и теплопередачу от горячей тепловой ёмкости.
Карно понимал, что в действительности невозможно создать термодинамический обратимый двигатель, поэтому реальные тепловые двигатели менее эффективны. Кроме того, реальные двигатели, работающие в этом цикле, встречаются редко. Но хотя прямой цикл французского учёного является идеализацией, его выражение эффективности всё ещё полезно для дальнейших исследований.
Примером обратимого цикла также является идеальный цикл Стирлинга. Существует и другие идеальные циклы, в которых коэффициент полезного действия определяется по той же формуле, что и для циклов Карно и Стирлинга, например, цикл Эрикссона.
Цикл Карно - обратимый круговой процесс, в котором совершается наиболее полное превращение теплоты в работу (или работы в теплоту). Термический КПД и холодильный коэффициент цикла Карно не зависят от физических свойств рабочего тела. Прямой (обратный) цикл Карно имеет максимально возможный термический КПД (холодильный коэффициент) в заданном интервале температур.
Т.к. t цикла Карно всегда больше 1, не зависит от рода рабочего тела и имеет наибольшее значение по сравнению с t любых других циклов, ограниченных тем же интервалом температур, то:
а) никакими новыми конструкциями тепловых двигателей или применением новых рабочих тел нельзя всю подведенную в цикле теплоту превратить в полезную работу;
б) для увеличения t нужно стремиться к таким процессам, образующим цикл, в которых средняя температура подвода теплоты была бы как можно больше, а средняя температура отвода теплоты - как можно меньше.
Прямой цикл Карно


Рис. 6.2. Прямой цикл Карно: а- в vP-диаграмме; б- в sT-диаграмме
Два процесса 1-2 и 3-4 (рис. 6.2) протекают при постоянных температурах, причем Т1- температура горячего источника (нагревателя), Т2 – температура холодного источника (холодильника, т.е. Т1Т2. Процессы 2-3 и 4-1 - адиабатные. В соответствии с первым законом термодинамики

Внутренняя энергия при Т = const не меняется, а изменение внутренней энергии в адиабатных процессах, протекающих в одном и том же интервале температур, одно и то же, поэтому работа цикла:

и термический КПД

Согласно sT-диаграмме:

, тогда

. (6.4)
Таким образом, КПД цикла Карно определяется обращением температур горячего и холодного источников теплоты. Его значение возрастает при увеличении Т1 или уменьшении Т2. В случае отсутствия перепада температур t = 0. Цикл Карно состоит из обратимых процессов и поэтому является обратимым.
Обратный цикл Карно


Рис. 6.2. Обратный Карно: а- в vP-диаграмме; б- в sT-диаграмме

Обратный цикл Карно характеризуется затрачиваемой извне работой . При этом теплота от холодного источника передается горячему. Это цикл холодильной машины. Ее холодильный коэффициент всегда больше 1:

(6.5)
Аналитическое выражение iIзакона термодинамики.
Для обратимого цикла Карно имеем:

,
тогда или.
Если учесть в этом соотношении, что q1 0 (теплота подводится к рабочему телу) и q20 (теплота отводится от рабочего тела), то
или (6.6)
Отношение подводимой или отводимой теплоты к соответствующей абсолютной температуре называется приведенной теплотой. Выражение (6.6) показывает, что алгебраическая сумма приведенных теплот для обратимого цикла Карно равна нулю, т.е.

. (6.7)
Отношениесчитаютполным дифференциалом функции состояния , называемой энтропией. Т.к.dq = Tds, то

(6.8)
Таким образом, алгебраическая сумма приведенных теплот для любого обратимого цикла равна нулю. Энтропия рабочего тела в результате совершения произвольного обратимого цикла не изменяется.
Уравнение (6.8), выведенное Клаузиусом в 1854 году, представляет собой аналитическое выражение II закона термодинамики для произвольного обратимого цикла и называется первым интегралом Клаузиуса.
В цикле с необратимыми процессами при прочих равных условиях работа, совершаемая рабочим телом меньше, чем в цикле с обратимым процессом, и при одинаковх температурах источника теплоты и холодильника
Поэтому при наличии в цикле необратимых процессов:

0 (6.9)
или после интегрирования по контуру

0 (6.10)
Это неравенство представляет собой аналитическое выражение II закона термодинамики для произвольного необратимого цикла и называется вторым интегралом Клаузиуса.
Объединяя (6.7) и (6.10), можно записать одно уравнение II закона термодинамики для обратимых (=) и необратимых () циклов:

0 (6.11)
Энтропия есть функция состояния рабочего тела, поэтому изменение энтропии как для обратимого, так и необратимого процессов будет одним и тем же.
Для элементарного необратимого процесса
(6.12)
В общем виде для любого процесса изменение энтропии удовлетворяет соотношению

, (6.13)
где dq - количество теплоты, полученное телом от источника теплоты; Т- абсолютная температура источника теплоты. Знак равенства относится к обратимым, знак неравенства - к необратимым процессам.
Следует различать понятия энтропия тела и энтропия системы.
Энтропия не является функцией состояния системы, состоящей из нескольких тел (рабочее тело, холодильники и источники теплоты), каждое из которых характеризуется своими параметрами. Поэтому на изменение энтропии системы влияет характер процесса теплообмена между рабочим телом и источником теплоты. При протекании обратимых процессов энтропия системы остается постоянной; при необратимых процессах энтропия системы возрастает.
Если в адиабатной изолированной системе протекают только обратимые процессы, то
ds = dq/T,
для адиабатной системы это уравнение принимает вид: dq = Tds = 0
Так как Т 0, то для всей системы ds = 0 и s = const.
Таким образом, если в изолированной адиабатной системе протекают только обратимые процессы, то энтропия всей системы остается величиной постоянной.
Для адиабатной системы при наличии в ней необратимых процессов:
.
Т.к. dq = 0, то для адиабатной изолированной системы ds 0, т.е. происходит увеличение энтропии.
В термодинамике большое значение имеет понятие работы, которую совершает система при изменении своего состояния и условий, при которых получается максимальная работа.
Получение работы возможно только от такой системы, которая не находится в равновесном состоянии с окружающей средой. По мере совершения работы система будет приближаться к равновесному состоянию со средой. Тепловая энергия, переданная в окружающую среду, становится полностью неработоспособной, т.к. при этом происходит выравнивание температур источника и приемника. Очевидно, наибольшая работа в системе может быть совершена при достижении в ней равновесного состояния путем обратимых процессов.
Максимальная работоспособность системы, получаемая в обратимом цикле Карно в температурном интервале от до, называетсяэксергией (ex).

. (6.14)
Работа необратимого цикла Карно, в котором теплота передается рабочему телу при температурениже температуры нагревателя:

. (6.15)

. (6.17)

Эксергия является обобщенной качественной и количественной характеристикой для потока теплоты и потока вещества, зависящей одновременно от параметров системы и окружающей среды. В отличии от энергии в реальных процессах, эксергия количественно не сохраняется. Всякая необратимость в системе приводит к уменьшению работоспособности, т.е. к потерям энергии. Уменьшение работы ведет к увеличению энтропии :

. (6.18)
Читайте также:

