Препараты гормонов поджелудочной железы фармакология кратко
Обновлено: 03.07.2024
Несмотря на то, что инсулин вызывает множество эффектов в различных тканях человеческого тела, его основным эффектом является стимулирование перехода глюкозы из крови внутрь клеток, что приводит к снижению концентрации глюкозы в крови.
Другими эффектами инсулина являются стимулирование синтеза в печены и мышцах гликогена из глюкозы, увеличение создания жиров и белков, подавление активности ферментов, разрушающих жиры и белки. Таким образом, инсулин обладает анаболическим действием, поскольку усиливает образование жиров и белков, одновременно замедляя их распад.
Основной эффект инсулина заключается в усилении переноса глюкозы через клеточную мембрану внутрь клетки. Других гормонов, снижающих уровень глюкозы крови, в организме человека не существует. Основные эффекты инсулина проявляются в мышцах и жировой ткани, поэтому эти ткани называют инсулинозависимыми. Уровень глюкозы крови снижается при воздействии инсулина и повышается при воздействии т.н. гипергликемических гормонов (глюкагона, соматотропного гормона, глюкокортикоидов).
Дополнительными эффектами инсулина являются увеличение интенсивности образования гликогена, уменьшение образования глюкозы в печени, усиление поглощения клетками аминокислот, необходимых для синтеза белка. Одновременно инсулин уменьшает разрушение белков и жиров. Таким образом, общий эффект инсулина является анаболическим – направленным на формирование жировой и мышечной ткани.
Строение инсулина
Инсулин является полипептидным гормоном, состоящим из двух аминокислотных цепей: А- и В-цепи. Полипептидные цепи соединяются дисульфидными мостиками. Человеческий инсулин по структуре близок к свиному и бычьему, хотя и отличается от них одним и тремя аминокислотными остатками соответственно.
Открытие инсулина
Островки поджелудочной железы были открыты в 1869 году Паулем Лангергансом при микроскопическом исследовании структуры поджелудочной железы. В 1889 году Оскар Малиновски в Германии при удалении поджелудочной железы у собаки вызвал у нее симптомы сахарного диабета. В 1921 году Ф. Бантинг и Ч. Бест выделили из клеток островков поджелудочной железы инсулин, а Д. Коллип разработал методику его очистки.
В 1922 году инсулин впервые был введен пациенту, страдающему сахарным диабетом. Его лечебное действие показало, что такой вид терапии является наиболее эффективным. В последующие годы основные усилия ученых были направлены на организацию производства в больших количествах. В 1923 году была вручена Нобелевская премия за открытие и выделение инсулина. В последующем аминокислотная структура инсулина была полностью расшифрована Ф. Сенгером.
Синтез инсулина
В островковых клетках поджелудочной железы инсулин синтезируется в несколько этапов. На первом этапе происходит синтез молекулы предшественника инсулина – препроинсулина. На втором этапе от молекулы препроинсулина отделяется сигнальный пептид, после чего образуется проинсулин. После созревания происходит образование окончательной молекулы инсулина. На этапе созревания от молекулы проинсулина отделяется С-пептид, который не оказывает биологического действия. После отделения С-пептида формируется активная форма инсулина.
Выделение инсулина в кровь происходит при повышении уровня глюкозы в крови. Дополнительно регуляция выработки инсулина производится автономной нервной системы. Разрушение инсулина происходит в печени и почках при воздействии фермента инсулиназы.
Препараты инсулина
В настоящее время фармацевтическая промышленность производит значительное число препаратов инсулина, имеющих различные биологические эффекты. Выделяют человеческий, свиной инсулины, инсулин крупного рогатого скота. По степени очистки различают традиционные, монопиковые, монокомпонентные инсулины. По времени действия выделяют инсулины короткого и пролонгированного действия. Последние делятся на инсулины среднего, длительного и сверхдлительного срока действия. Есть также инсулины ультракороткого и депо-инсулины, выделяющиеся медленно из подкожной клетчатки.
Подбор схемы инсулинотерапии – сложное и очень ответственное мероприятие. От правильности выбора формы инсулина и схемы его дозирования зависит успешность достижения компенсации сахарного диабета и, как следствие, качество жизни пациента.
Типы сахарного диабета
В настоящее время выделяется два основных типа сахарного диабета, различающиеся по причине и механизму появления, а также по принципам лечения
Сахарный диабет 1 типа
Сахарный диабет 1 типа - заболевание эндокринной системы, для которого характерным признаком является повышенная концентрация глюкозы в крови, которое развивается из-за деструктивных процессов в специфических клетках поджелудочной железы, секретирующих гормон - инсулин, вследствие чего наблюдается абсолютный недостаток инсулина в организме
Сахарный диабет 2 типа
Сахарный диабет 2 типа - одна из разновидностей сахарного диабета - заболевания обмена веществ, возникающего в результате пониженной чувствительности клеток к инсулину, а также относительной недостачи инсулина в организме
Гестационный сахарный диабет при беременности
Гестационный сахарный диабет может развиваться при беременности (примерно в 4% случаев). В его основе лежит снижение способности по усвоению глюкозы
Гипогликемия
Гипогликемией называют патологическое состояние, характеризующееся снижением концентрации глюкозы в плазме крови ниже уровня 2,8 ммоль/л, протекающее с определенной клинической симптоматикой, либо менее 2,2 ммоль/л независимо от наличия или отсутствия клинических признаков
Кома при сахарном диабете
Информация о наиболее опасном осложнении сахарного диабета, требующем экстренной медицинской помощи,- коме. Описываются виды ком при сахарном диабете, их специфические признаки, тактика лечения
Синдром диабетической стопы
Синдром диабетической стопы - одно из осложнений сахарного диабета, наряду с диабетической офтальмопатией, нефропатией и др., представляющее собой патологическое состояние, возникшее вследствие поражения периферической нервной системы, артериального и микроциркуляторного русла, проявляющееся гнойно-некротическими, язвенными процессами и повреждением костей и суставов стопы
О диабете
Сахарный диабет — термин, объединяющий эндокринные заболеваний, характерной чертой которых является недостаточность действия гормона инсулина. Главным симптомом сахарного диабета является развитие гипергликемии – увеличения концентрации глюкозы в крови, имеющее стойкий характер
Симптомы диабета
Эффективность лечения сахарного диабета напрямую зависит от времени выявления этого заболевания. При сахарном диабете 2 типа заболевание может длительное время вызывать лишь незначительно выраженные жалобы, на которые пациент может не обращать внимания. Симптомы диабета могут быть стертыми, что затрудняет диагностику. Чем раньше поставлен правильный диагноз и начато лечение, тем меньше риск развития осложнений сахарного диабета
Анализы в СПб
Одним из важнейших этапов диагностического процесса является выполнение лабораторных анализов. Чаще всего пациентам приходится выполнять анализ крови и анализ мочи, однако нередко объектом лабораторного исследования являются и другие биологические материалы.
Консультация эндокринолога
Специалисты Северо-Западного центра эндокринологии проводят диагностику и лечение заболеваний органов эндокринной системы. Эндокринологи центра в своей работе базируются на рекомендациях Европейской ассоциации эндокринологов и Американской ассоциации клинических эндокринологов. Современные диагностические и лечебные технологии обеспечивают оптимальный результат лечения.
Анализ на гликогемоглобин
Гликогемоглобин (гликированный гемоглобин, гликозилированный гемоглобин, гемоглобин А1с) – соединение гемоглобина с глюкозой, образующееся в эритроцитах
Диагностика и лечение гинекологических заболеваний, консультирование семейных пар по вопросам лечения бесплодия ЭндокринологДиагностика и лечение сахарного диабета, ожирения, остеопороза Хирург-эндокринологДиагностика и лечение заболеваний щитовидной железы, околощитовидных желез, надпочечников Диетолог-эндокринологЛечение ожирения, диагностика эндокринных причин ожирения, комплексные программы снижения веса Андролог Помощь в решении мужских проблем: бесплодия, нарушения потенции, воспалительных заболеваний Детский эндокринологДиагностика и лечение эндокринных заболеваний у детей до 18 лет МаммологДиагностика и лечение заболеваний молочных желез
Отзывы
Истории пациентов
Видеоотзывы: опыт обращения в Северо-Западный центр эндокринологии
Услуги
Экспертное УЗИ щитовидной железы
УЗИ щитовидной железы выполняется хирургами-эндокринологами с использованием аппаратов экспертного класса
Денситометрия: ультразвуковая
Денситометрия (определение плотности костной ткани) - без облучения, выполняется эндокринологом
Гормоны щитовидной железы
Всё о сдаче анализа на гормоны щитовидной железы: какие гормоны существуют, как сдавать гормоны, где сдавать анализ на гормоны
Удаление щитовидной железы
Информация об удалении щитовидной железы в Северо-Западном центре эндокринологии
Сотрудничество с центром
Возможности сотрудничества
Варианты и обсуждение вопросов сотрудничества с Северо-Западным центром эндокринологии
Специалисты Центра эндокринологии регулярно участвуют в международных конгрессах, стажировках, обучающих семинарах. За 3 года специалистами центра получено 15 патентов РФ на изобретения
Поджелудочная железа выделяет два гормона: инсулин и глюкагон, оказывающих разнонаправленное действие на уровень глюкозы в крови. Инсулин понижает содержание глюкозы в крови, обеспечивая ее транспорт через клеточные мембраны и утилизацию в тканях, стимулирует образование глюкозо-6-фосфата, активирует процессы энергообразования, стимулирует синтез белков и жирных кислот. Недостаточной продукцией инсулина обусловлен сахарный диабет - тяжелое заболевание, проявляющееся повышением уровня сахара в крови и появлением его в моче, нарушением окислительных процессов (с накоплением кетоновых тел), нарушением липидного обмена и развитием сосудистой патологии (диабетические ангиопатии). Углеводный голод клеток (инсулинзависимых тканей), нарушение электролитного баланса и кетоацидоз вызывает развитие тяжелого проявления сахарного диабета - диабетической комы.
Инсулин - белок, состоящий из двух полипептидных цепей, соединенных дисульфидными мостиками. В настоящее время осуществлен синтез инсулина человека и животных, усовершенствован биотехнологический способ его получения (генно-инженерный инсулин). Инсулин используют при инсулинзависимом сахарном диабете со склонностью к кетоацидозу. Введение инсулина больным сахарным диабетом приводит к падению уровня сахара в крови и накоплению в тканях гликогена. Уменьшается глюкозурия и обусловленные ею полиурия и полидипсия. Нормализуется белковый и липидный обмен, что обусловливает снижение содержания азотистых оснований в моче. В крови и моче перестают определяться кетоновые тела.
В медицинской практике применяют препараты инсулина с различной продолжительностью действия (короткого, среднего, длительного). Дозу рассчитывают индивидуально, учитывая тяжесть процесса. С целью уменьшения количества инъекций, после достижения компенсации, больных переводят на инсулин пролонгированного действия: суспензия цинк-инсулина кристаллического, суспензия инсулина-ультралонг, протамин-цинк - инсулин. Часто для лечения используют комбинации различных (по длительности действия) видов инсулина. Препараты инсулина не лишены недостатков. Инсулин инактивируется в печени инсулиназой, что обусловливает недостаточную продолжительность его действия (4-6 ч). Инъекции инсулина весьма болезненны, на месте введения возможно возникновение инфильтратов. Инсулин и его пролонгированные формы могут вызывать аллергические реакции. При передозировке инсулина возможно развитие гипогликемической комы. При легкой степени гипогликемии ее можно компенсировать приемом сахара или пищи, богатой углеводами; при коме необходимо парентерально вводить глюкозу.
Кроме инсулина, в качестве сахаропонижающих средств используют синтетические гипогликемические средства. К ним относят производные сульфонилмочевины: толбутамид (бутамид), хлорпропамид, бигуаниды: буформин (глибутид, метформин (глюкофаг, глиформин). Производные сульфонилмочевины назначают при средней тяжести диабета в дополнение к диетотерапии. Бигуаниды целесообразно использовать при инсулиннезависимом сахарном диабете средней тяжести. Они сочетаются также с инсулином и сульфонамидами. Предполагаемый механизм действия пероральных противодиабетических средств связан с повышением секреции инсулина и чувствительности к нему клеток-мишеней. Механизм действия производных бигуанидов обусловлен стимуляцией поглощения глюкозы мышцами и угнетением процессов всасывания глюкозы.
Сахарный диабет (СД) – это группа заболеваний, развивающихся вследствие недостаточности гормона инсулина, проявляющиеся увеличением количества сахара (глюкозы) в крови, в результате чего повреждаются мелкие кровеносные сосуды, особенно глаз, стоп ног, почек, сердце, нервы, что в свою очередь может стать причиной слепоты, нарушения функции почек, инфаркта миокарда и ампутации нижних конечностей.
Инсулин – гормон, выделяемый ?-клетками поджелудочной железы, биологическая роль которого заключается в снижении уровня сахара в крови. С помощью инсулина клетки организма, преимущественно печени и мышц, распознают глюкозу, потребляют ее и вырабатывают энергию, необходимую для нормальной работы организма.
Эффекты инулина и его терапевтическое действие
Инсулин увеличивает проницаемость плазматических мембран для глюкозы, активирует ключевые ферменты гликолиза (процесс окисления глюкозы, при котором из одной молекулы глюкозы образуются две молекулы пировиноградной кислоты и 2 молекулы энергии, АТФ), стимулирует образование в печени и мышцах из глюкозы гликогена (полисахарид, образованный остатками глюкозы, который является основной формой хранения глюкозы в клетках), усиливает синтез жиров и белков, подавляет активность ферментов, расщепляющих гликоген и жиры.
Механизм действия инсулина
Молекула инсулина стимулирует специфические рецепторы, которые имеются на мембране почти всех клеток организма (печени, мышц, жировой ткани, крови, головного мозга, половых желез), что запускает каскад биохимических реакций, в результате которых происходит активация внутриклеточных белков и развитие соответствующих эффектов. Инсулин способен также регулировать транскрипцию соответствующих генов, однако, механизм, по которому протекают данные реакции, до конца не изучен.
Регуляция выделения инсулина
Выделение инсулина регулируется многими факторами, например, другими гормонами, аминокислотами, приемом пищи и автономной нервной системой (табл. 1).
Таблица 1. Регуляция выделения инсулина

Выделяют два основных типа сахарного диабета, которые отличаются причиной и лечением: сахарный диабет I типа и сахарный диабет II типа (табл. 2).
Таблица 2. Отличительные особенности сахарного диабета I и II типа

Сахарный диабет I типа
При сахарном диабете I типа, частота развития которого составляет 5-10 % всех случаев сахарного диабета, поджелудочная железа не выделяет инсулин из-за разрушения ?-клеток поджелудочной железы, вследствие чего другие клетки организма не могут распознать и потребить глюкозу, поэтому уровень сахара в крови остается стабильно высоким. Причиной разрушения ?-клеток, как правило, являются аутоиммунные процессы в организме, характеризующиеся выработкой организмом антител к собственным клеткам. Другими причинами возникновения СД I типа являются: вирусные инфекции (врожденная краснуха, энтеровирус, ротавирус, цитомегаловирус и др.), дефицит витамина D, воздействие загрязняющих факторов внешней среды на плод во время беременности и др.
Лечение сахарного диабета I типа
Для лечения этого типа заболевания используются препараты синтетического инсулина, которые вводятся с помощью специальных устройств – шприц-ручек, инсулиновых помп (насосов) или инсулиновых шприцов под кожу.
Классификация препаратов синтетического инсулина
В зависимости от длительности действия данные препараты подразделяются на:
1. Инсулины ультракороткого действия (инсулин лизпро, инсулин аспарт, инсулин глулизин).
2. Инсулины короткого действия (инсулин растворимый [человеческий генно-инженерный]; инсулин растворимый [человеческий полусинтетический]).
3. Инсулины средней длительности действия (инсулин изофан).
4. Инсулины длительного действия (инсулин гларгин, инсулин детемир).
5. Препараты инсулина комбинированного действия (бифазные препараты).
Противопоказания к применению препаратов синтетического инсулина
Нельзя разводить или смешивать препараты синтетических инсулинов с другими ЛС в одном шприце, а также использовать их у пациентов с аллергией на них.
Нежелательные реакции
При передозировке инсулина или его одновременного применения с препаратами, снижающими уровень сахара в крови из других фармакологических групп, значительно повышается риск резкого падения уровня сахара в крови (гипогликемия), которое может сопровождаться потерей сознания (кома), бледностью и влажностью кожных покровов, сердцебиением (тахикардией) и другими симптомами. Характерно, что плотность глазных яблок не изменена.
В случае развития гипогликемической комы в первую очередь необходимо срочно обратиться за медицинской помощью к врачу. При наличии лиц, обладающих необходимыми знаниями и навыками, необходимо начать купирование гипогликемической комы внутривенным введением 40 % раствора глюкозы до выхода пациента из комы. В тяжёлых случаях возможно использовать препараты адреналина, глюкокортикоидов или глюкагона.
При отсутствии адекватной терапии сахарного диабета I типа, неправильном использовании препаратов инсулина или избыточного поступления глюкозы с пищей у пациентов может развиться гипергликемическая кома, которая, как правило, развивается медленно и сопровождается сухостью во рту, выраженной жаждой, недомоганием, головной болью, тошнотой и другими симптомами. Характерным симптомом этого типа комы является мягкость глазных яблок на ощупь. В случае гипергликемической комы необходимо незамедлительно вызвать врача, а при наличии людей, обладающих необходимой квалификацией, начать введение инсулина короткого действия, инфузионной и симптоматической терапии.
Другими возможными осложнениями лекарственной терапии препаратами синтетического инсулина являются: покраснение или сыпь на месте введения и аллергические реакции.
Сахарный диабет II типа
По данным эпидемиологических исследований, сахарный диабет II типа является наиболее распространенным и составляет около 90–95 % всех случаев постановки диагноза сахарный диабет. При данном заболевании поджелудочная железа вырабатывает недостаточное количество инсулина, которое осложняется сопутствующим снижением чувствительности тканей организма к действию данного гормона – инсулинорезистентностью, вследствие которой ?-клетки поджелудочной железы не могут обеспечить повышенную потребность организма в инсулине, транспорт глюкозы нарушается и концентрация сахара в крови повышается.
Лечение сахарного диабета II типа
Для лечения сахарного диабета II типа применяются синтетические ЛС, снижающие уровень сахара в крови (синтетические гипогликемические средства), которые по механизму действия можно разделить на:
1. ЛС, усиливающие выделение инсулина клетками поджелудочной железы.
1.1. Производные сульфонилмочевины (глибенкламид, глимепирид, глипизид и др.).
1.2. ЛС, механизм действия которых обусловлен инкретиновыми эффектами (более выраженное выделение инсулина поджелудочной железой в ответ на поступление глюкозы при приеме внутрь, в сравнении с ее внутривенным введением, которое вызвано стимулирующим влиянием гормонов-инкретинов, таких как глюкозозависимый инсулинотропный пептид, ГИП иглюкагоноподобный пептид-1, ГПП-1).
1.2.1. Агонисты ГПП-1: эксенатид, лираглутид.
1.2.2. Ингибиторы ДПП-4: ситаглиптин, вилдаглиптин, саксаглиптин, линаглиптин.
1.3. Секретагоги (меглитиниды): репаглинид, натеглинид.
2. ЛС, усиливающие захват и потребеление глюкозы клетками печени и мышц.
2.1. Бигуаниды: метформин.
2.2. Тиазолидиндионы: росиглитазон, пиоглитазон.
3. Ингибиторы всасывания глюкозы (ингибиторы альфа-глюкозидаз): акарбоза, миглитол.
4. ЛС, усиливающие выведение сахара с мочой: ингибиторы натрий-глюкозного котранспортера 2 типа (SGLT2), глифлозины: эмпаглифлозин, канаглифлозин, дапаглифлозин.

Рис. 3. Механизм действия синтетических гипогликемических средств.
Производные сульфонилмочевины: глибенкламид, глимепирид, глипизид и др.
Механизм действия производных сульфонилмочевины связан со стимуляцией ?-клеток поджелудочной железы и усилением выброса инсулина. Соответственно, основной предпосылкой для проявления их эффекта является наличие в поджелудочной железе функционально активных ?-клеток. Длительное применение препаратов из данной группы может привести к снижению их эффективности, что предположительно связано с уменьшением количества рецепторов. Фармакологические эффекты со стороны других органов и систем, такие как увеличение чувствительности клеток к инсулину и снижение образования глюкозы в печени, не играют значительной роли в снижении уровня глюкозы.
Противопоказания
Препараты противопоказаны пациентам, имеющим гиперчувствительность, кетоацидоз, обширные ожоги, хирургические вмешательства и травмы, состояния, гипо– или гипертиреоз, нарушение функции печени и почек, лейкопения, сахарный диабет типа 1, а также находящимся в прекоматозном или коматозном состоянии.
Нежелательные реакции
Прием препаратов сульфонилмочевины может вызывать значительное снижение уровня глюкозы (гипогликемию) вплоть до гипогликемической комы, депрессию, спутанность сознания, брадикардию.
Секретагоги (меглитиниды): репаглинид, натеглинид.
Механизм действия
Секретагоги усиливают выделение инсулина поджелудочной железой, за счет блокады АТФ-зависимых калиевые каналов в мембранах функционально активных ?-клеток поджелудочной железы.
Противопоказания
Препараты противопоказаны при гиперчувствительности, сахарном диабете I типа и диабетическом кетоацидозе и др.
Нежелательные реакции
Гипогликемия, повышение уровня мочевой кислоты и риска развития подагры, диспепсические явления, временное нарушение зрения и др.
Лекарственные средства, механизм действия которых обусловлен инкретиновыми эффектами
1. Агонисты ГПП-1: эксенатид, лираглутид.
2. Ингибиторы ДПП-4: ситаглиптин, вилдаглиптин, саксаглиптин, линаглиптин.
Механизм действия
Усиление секреции инсулина поджелудочной железой за счет действия, сходного с действием инкритинов (ГИП, ГПП-1) – гормонов, являющихся частью внутренней физиологической системы регуляции уровня глюкозы, и секретирующихся в кишечнике в течение суток. При нормальной или повышенной концентрации глюкозы в крови гормоны семейства инкретинов способствуют увеличению синтеза инсулина, а также его секреции ?-клетками поджелудочной железы. Дипептидилпептидаза-4 (ДПП-4) – фермент, функция которого заключается в быстрой инактивации ГПП-1 и ГИП. Ингибирование данного фермента приводит к повышению концентрации ГПП-1 и ГИП. Отличительной особенностью данных препаратов является то, что они, относительно редко вызывают гипогликемию.
Противопоказания
Гиперчувствительность, сахарный диабет I типа, диабетический кетоацидоз, панкреатит в анамнезе, почечная недостаточность тяжелой степени, тяжелые нарушения ЖКТ и др.
Нежелательные реакции
Боли в животе, тошнота, рвота, гипогликемия и др.
Бигуаниды (метформин)
Механизм действия
Угнетают глюконеогенез в печени и повышают захват глюкозы периферическими тканями за счет повышения их чувствительности к инсулину (преимущественно поперечно-полосатой мускулатуры, а в меньшей степени – жировой ткани). Снижение уровня сахара в крови при приеме бигуанидов возможно только в присутствии инсулина, так как эти препараты сами по себе не влияют на секрецию данного гормона.
Противопоказания
Гиперчувствительность, тяжелые заболевания почек или ренальная недостаточность, выраженные нарушения функции печени, дегидратация, состояния, сопровождающиеся гипоксией и др.
Нежелательные реакции
Тошнота, рвота, боли в животе, нарушение функции печени, при длительном применении возможны снижение концентрации витамина B12, фолиевой кислоты, лактоацидоз (повышение уровня молочной кислоты в крови) и др.
Важные лекарственные взаимодействия
Бигуаниды обладают синергизмом с ЛС, усиливающими выделение инсулина клетками поджелудочной железы (производные сульфонилмочевины, секретагоги (меглитиниды), агонисты ГПП-1, ингибиторы ДПП-4), что может быть эффективно использовано при тяжелых формах сахарного диабета, однако повышает риск развития тяжелой гипогликемии и комы.
Тиазолидиндионы (росиглитазон, пиоглитазон)
Механизм действия
Тиазолидиндионы регулируют работу генов, вовлеченных в контроль за продукцией, транспортом и утилизацией глюкозы, а также участвующих в метаболизме жирных кислот. Повышая чувствительность тканей-мишеней (мышцы, жировая ткань, печень) к инсулину, ЛС этой группы способствуют снижению уровня глюкозы, инсулина и свободных жирных кислот в крови.
Противопоказания
Гиперчувствительность, сердечная недостаточность III и IV класса по NYHA, сахарный диабет I типа, тяжелые нарушения функции печени и др.
Нежелательные реакции
Нарушения деятельности сердечно-сосудистой системы, например, сердечная недостаточность; переломы костей, отеки, увеличение массы тела и др.
Важные лекарственные взаимодействия
Тиазолидиндионы обладают синергизмом с ЛС, усиливающими выделение инсулина клетками поджелудочной железы (производные сульфонилмочевины, секретагоги (меглитиниды), агонисты ГПП-1, ингибиторы ДПП-4), что может быть эффективно использовано при тяжелых формах сахарного диабета, однако повышает риск развития тяжелой гипогликемии и комы.
Ингибиторы альфа-глюкозидаз (акарбоза, миглитол)
Механизм действия
Препараты из группы ингибиторов альфа-глюкозидаз инактивируют альфа-глюкозидазы – ферменты, расщепляющие невсасывающиеся в кишечнике полисахариды (крахмал, гликоген и др.) до моносахаридов (глюкозы), которые способны достигать системного кровотока, способствуют незначительному снижению их концентрации в крови.
Противопоказания
Гиперчувствительность, диабетический кетоацидоз, цирроз печени; острые и хронические воспалительные заболевания кишечника, осложненные нарушениями пищеварения и всасывания (например, неспецифический язвенный колит) и др.
Нежелательные реакции
Метеоризм, диарея, боли в животе, непроходимость кишечника, нарушение функции печени и др.
Глифлозины (эмпаглифлозин, канаглифлозин, дапаглифлозин)
Механизм действия
Глифлозины снижают уровень сахара в крови за счет стимуляции выведения глюкозы с мочой путем инактивации SGLT2-белка, ответственного за ее обратное всасывание (реабсорбцию) в почках.
Противопоказания
Гиперчувствительность, сахарный диабет I типа, диабетический кетоацидоз, тяжелая почечная недостаточность, тяжелая печеночная недостаточность и др.
Нежелательные реакции
Кетоацидоз, инфекции мочеполовой системы, гипогликемия и др.
Действия в случае обнаружения нежелательных реакций
В случае развития нежелательных реакций или иных осложнений у пациента, получающего синтетические гипогликемические средства из любой группы, необходимо прекратить прием препаратов и немедленно обратиться за помощью к врачу.
Гормоны поджелудочной железы. Островки Лангерганса. Соматостатин. Амилин. Регуляторные функции гормонов поджелудочной железы.
Эндокринную функцию в поджелудочной железе выполняют скопления клеток эпителиального происхождения, получившие название островков Лангерганса и составляющие всего 1 —2 % массы поджелудочной железы — экзокринного органа, образующего панкреатический пищеварительный сок. Количество островков в железе взрослого человека очень велико и составляет от 200 тысяч до полутора миллионов.
В островках различают несколько типов клеток, продуцирующих гормоны: альфа-клетки образуют глюкагон, бета-клетки — инсулин, дельта-клетки — соматостатин, джи-клетки — гастрин и РР- или F-клетки — панкреатический полипептид. Помимо инсулина в бета-клетках синтезируется гормон амилин, обладающий противоположными инсулину эффектами. Кровоснабжение островков более интенсивно, чем основной паренхимы железы. Иннервация осуществляется постганлионарными симпатическими и парасимпатическими нервами, причем среди клеток островков расположены нервные клетки, образующие нейроинсулярные комплексы.
Инсулин синтезируется в эндоплазматическом ретикулуме бета-клеток вначале в виде пре-проинсулина, затем от него отщепляется 23-аминокис-лотная цепь и остающаяся молекула носит название проинсулина. В комплексе Гольджи проинсулин упаковывается в гранулы, в них осуществляется расщепление проинсулина на инсулин и соединительный пептид (С-пептид). В гранулах инсулин депонируется в виде полимера и частично в комплексе с цинком. Количество депонированного в гранулах инсулина почти в 10 раз превышает суточную потребность в гормоне. Секреция инсулина происходит путем экзоцитоза гранул, при этом в кровь поступает эквимолярное количество инсулина и С-пептида. Определение содержания последнего в крови является важным диагностическим тестом оценки секреторной способности (3-клеток.
Секреция инсулина является кальцийзависимым процессом. Под влиянием стимула — повышенного уровня глюкозы в крови — мембрана бета-клеток деполяризуется, ионы кальция входят в клетки, что запускает процесс сокращения внутриклеточной микротубулярной системы и перемещение гранул к плазматической мембране с последующим их экзоцитозом.
Стимулированная секреция инсулина представляет собой ответ бета-клеток островков на повышенный уровень D-глюкозы в притекающей к бета-клеткам крови. Под влиянием глюкозы активируется энергетический рецептор бета-клеток, что увеличивает транспорт в клетку ионов кальция, активирует аденилатциклазу и пул (фонд) цАМФ. Через эти посредники глюкоза стимулирует выброс инсулина в кровь из специфических секреторных гранул. Усиливает ответ бета-клеток на действие глюкозы гормон двенадцатиперстной кишки — желудочный ингибиторный пептид (ЖИП). В регуляции секреции инсулина определенную роль играет и вегетативная нервная система. Блуждающий нерв и ацетилхолин стимулируют секрецию инсулина, а симпатические нервы и норадреналин через альфа-адренорецепторы подавляют секрецию инсулина и стимулируют выброс глюкагона.
Поджелудочная железа сочетает функции как эндокринной, так и экзокринной железы. Экзокринная функция заключается в выработке пищеварительного сока, который выделяется в двенадцатиперстную кишку и содержит сумму ферментов, необходимых для переваривания белков (трипсин, химотрипсин, коллагеназа, элластаза и др.), жиров (фосфолипаза, триглицеридлипаза, холестеролэстераза), углеводов (-амилаза, сахараза, мальтаза, галактаза) и нуклеиновых кислот (эндонуклеазы, ДНК-азы, РНК-азы).
Эндокринную функцию поджелудочной железы выполняют особые скопления эндокринных клеток – островки Лангерганса. В ткани железы располагается около 1 млн. островков. Островки содержат клетки 4 типов, которые вырабатывают по крайней мере 5 видов гормонов (см. таблицу 1).
Таблица 1. Гормоны, продуцируемые поджелудочной железой и их функция.
Усиление гликогенолиза и липолиза.
Усиление гликолиза, синтеза гликогена, белка, липидов; торможение гликогенолиза и липолиза.
Торможение захвата глюкозы -клетками, секреции инсулина, конверсия проинсулина в инсулин
Торможение секреции инсулина, глюкагона, СТГ, гастрина, соляной кислоты
Торможение секреции инсулина, пепсина, соляной кислоты.
Недостаточность эндокринной функции поджелудочной железы. Наиболее важной патологией с клинической точки зрения является сахарный диабет.
Сахарный диабет – эндокринное заболевание, обусловленное абсолютной или относительной недостаточностью инсулина, которая приводит к нарушению всех видов обмена веществ, поражению сосудов (ангиопатии) и нервов (нейропатии). Под абсолютной инсулиновой недостаточностью понимают снижение секреции инсулина -клетками поджелудочной железы, тогда как под относительной – понижение чувствительности к инсулину периферических тканей на фоне нормальной или даже повышеннной секреции инсулина.
Согласно современной клинической классификации различают 2 основных типа заболевания:
Инсулинзависимый сахарный диабет (ИЗСД или диабет I типа);
Инсулиннезависимый сахарный диабет (ИНСД или диабет II типа).
Особенности каждого из этих типов диабета представлены в таблице 2.
Таблица 2. Сравнительная характеристика типов сахарного диабета.
Семейный характер заболевания
Связь с генами HLA
Другие аутоиммунные заболевания
нормальный или понижен
Потребность лечения инсулином
обязательна у всех
у отдельных лиц
Распространенность в популяции
Классификация противодиабетических средств:
Средства заместительной терапии:
Модифицированные инсулины: лизпроинсулин, инсулин аспарт, гларгининсулин.
Средства, стимулирующие секрецию инсулина из -клеток поджелудочной железы (секретагоги):
I поколения: карбутамид, толбутамид;
II поколения: глибенкламид, гликвидон, глипизид;
III поколения: глимепирид.
Производные бензойной кислоты: репаглинид, натеглинид
Средства, повышающие чувствительность периферических тканей к инсулину (периферические сенситайзеры):
Производные бигуанида: метформин.
Производные тиазолидиндиона: пиоглитазон, розиглитазон.
Средства, снижающие абсорбцию углеводов в кишечнике:
Ингибиторы -глюкозидаз: акарбоза, воглибоза;
Производные смол: гуарем.
Инсулин (Insuline). Инсулин человека – небольшой белок с Mr=5.808 Да, состоящий из 51 аминокислоты. Инсулин образуется в -клетках поджелудочной железы в виде препроинсулина, который содержит 110 аминокислот. После выхода из эндоплазматической сети от молекулы отщепляется N-концевой сигнальный пептид из 24 аминокислот и образуется проинсулин. В комплексе Гольджи путем протеолиза из середины молекулы проинсулина удаляются 4 основные аминокислоты и С-пептид из 31 аминокислоты. В итоге, образуется 2 цепи инсулина – А-цепь из 21 аминокислоты (содержит дисульфидную связь) и В-цепь из 30 аминокислот. Между собой А и В цепи соединяются 2 дисульфидными связями. В дальнейшем в секреторных гранулах -клеток инсулин депонируется в виде кристаллов, состоящих из 2 атомов цинка и 6 молекул инсулина. В целом поджелудочная железа человека содержит до 8 мг инсулина, что примерно соответствует 200 ЕД инсулина.

Схема 1. Образование инсулина. В процессе протеолиза от проинсулина отщепляется видоспецифичный С-пептид и 4 оснóвные аминокислоты (показаны красным).
Секреция инсулина. -клетки поджелудочной железы содержат в своей мембране большое количество К + -каналов, которые находятся в открытом состоянии и обеспечивают постоянный выход ионов калия из клетки и гиперполяризацию ее мембраны.
Основным стимулятором секреции инсулина является глюкоза (см. рис. 2). При повышении концентрации глюкозы более 5 ммоль/л она при помощи переносчика GLUT-2 поступает внутрь -клеток и подвергается фосфорилированию ферментом глюкокиназой. Глюкокиназа – особый фермент, который содержится только в клетках печени и поджелудочной железы, он имеет относительно низкое сродство к глюкозе (Km10-20 мМ), поэтому фосфорилирует глюкозу только в том случае, если ее концентрация достаточно высока. В остальных клетках нашего организма фосфорилирование глюкозы осуществляется гексокиназой – ферментом, который имеет высокое сродство к глюкозе (Km1-2 мМ) и активируется даже небольшим количеством глюкозы.

Схема 2. Регуляция секреции инсулина. Г – глюкоза, GLUT-2 – глюкозный транспортер, Г-киназа – глюкокиназа, обеспечивающая фосфорилирование глюкозы до глюкозо-6-фосфата (Г-6-Ф), который включается в ЦТК с образованием в итоге АТФ. Молекулы АТФ блокируют калиевые канала мембраны -клеток и гиперполяризующий ток калия прекращается, а мембранный потенциал понижается. Уменьшение мембранного потенциала способствует открытию кальциевых каналов, поступлению ионов кальция в клетку и секреции инсулина (Ins).
После фосфорилирования глюкозы в -клетках она включается в ЦТК и обеспечивает синтез молекул АТФ, которые соединяются со специальными рецепторами внутренней поверхности калиевого канала и закрывают его. В итоге, ток ионов калия из клетки прекращается и развивается небольшая деполяризация мембраны, которая приводит к открытию Са 2+ -каналов. Ионы кальция поступают в клетку и выполняют роль стимулятора секреции приводя к выбросу инсулина в кровь.
После того, как под влиянием инсулина уровень глюкозы понизится, активность переносчика GLUT-2 падает и транспорт глюкозы в -клетки прекращается, уровень глюкозы в цитоплазме клетки также понижается. Глюкокиназа не может провести фосфорилирование глюкозы и синтез АТФ в -клетках ослабевает, калиевые каналы освобождаются от молекул АТФ и вновь открываются, что приводит к возобновлению тока ионов калия из клетки и гиперполяризации ее мембраны. Секреция инсулина падает.
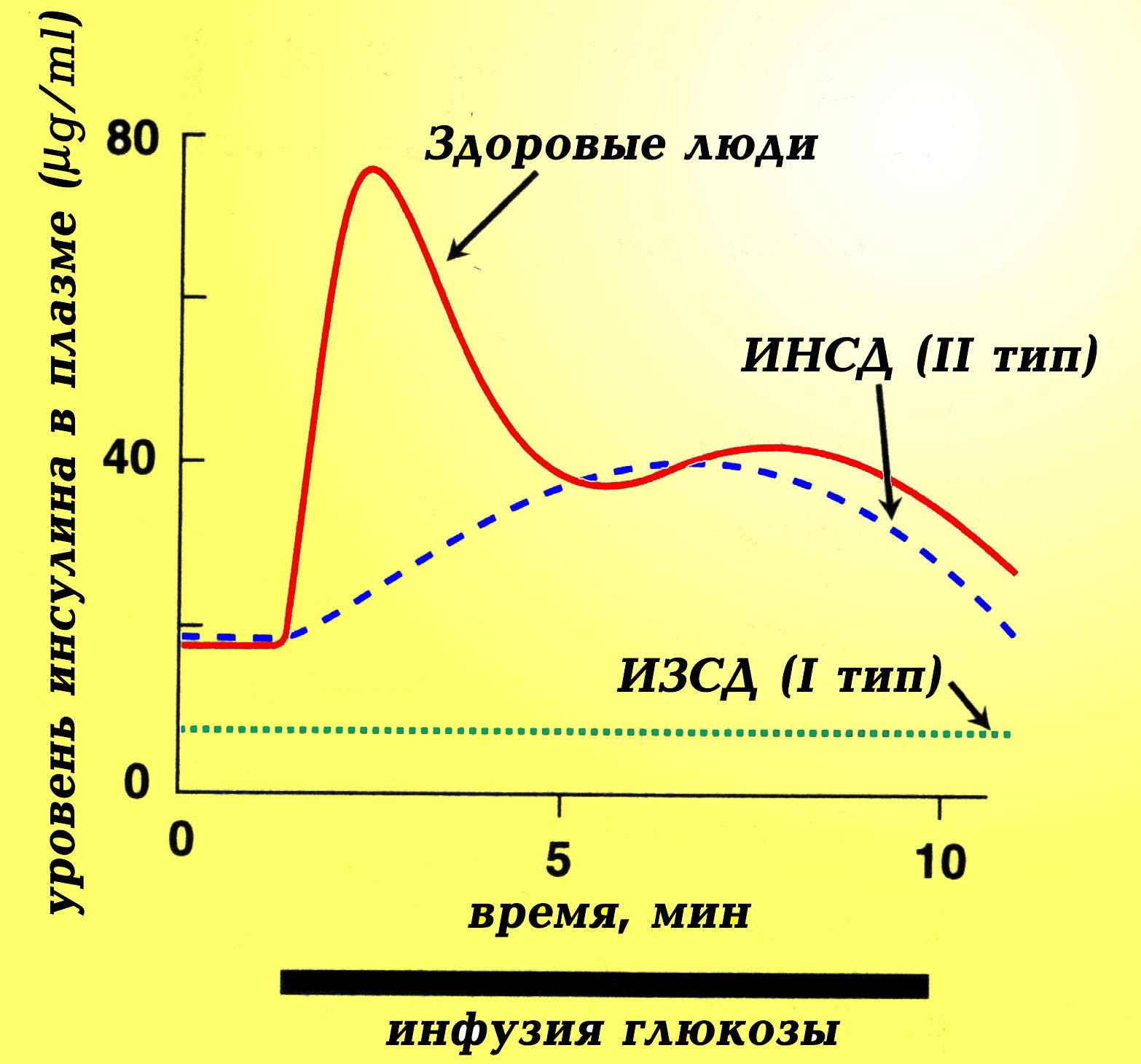
Схема 3. Постпрандиальная секреция инсулина у человека. У здорового человека в секреции инсулина имеется ранняя фаза и поздняя фаза. У лиц, которые страдают ИНСД сохраняется только поздняя фаза, а у пациентов с ИЗСД выпадают обе фазы.
Метаболизм и деградация инсулина. Период полуэлиминации инсулина после его выделения в кровь составляет всего 5-6 минут. Основными органами, где происходит разрушение инсулина являются печень, почки и скелетные мышцы. Деградация инсулина происходит под влиянием инсулиназы (расщепляет дисульфидные связи) и дигидропептидазы II типа (ангиотензинпревращающий фермент, который расщепляет В-цепь инсулина).
Поскольку кровь от поджелудочной железы по системе воротной вены поступает в печень, то 50-60% инсулина так и не достигают органов-мишеней и подвергаются разрушению при первом прохождении через гепатоциты, оставшиеся 35-40% инсулина элиминируются почками. У пациентов с диабетом, которые получают подкожные инъекции инсулина его элиминация носит нефизиологический характер: более 50-60% инсулина элиминируется почками и только 35-40% печенью.
Механизм действия инсулина. Инсулин действует на трансмембранные инсулиновые рецепторы, расположенные на поверхности тканей мишеней (скелетные мышцы, печень, жировая ткань) и активирует эти рецепторы.
Инсулиновый рецептор содержит 2 субъединицы: -субъединицу, которая расположена с внешней стороны мембраны и -субъединицу, которая прошивает мембрану насквозь. При связывании инсулина с рецепторами происходит их активация, при этом молекулы рецепторов объединяются попарно и приобретают тирозинкиназную активность (т.е. способность фосфорилировать остатки тирозина в молекулах ряда белков). Активированный рецептор подвергается аутофосфорилированию и в результате его тирозинкиназная активность усиливается в десятки раз. В дальнейшем сигнал с рецептора передается двумя путями:
Немедленный ответ (развивается через несколько минут). Связан с фосфорилированием остатков тирозина в белке IRS-2, который активирует фосфатидилинозитол-3-киназу (PI-3 киназа). Под влиянием этой киназы молекулы фосфатидилинозитол бифосфата (PIP2) фосфорилируются до фосфатидилинозитол трифосфата (PIP3). PIP3 активирует ряд протеинкиназ, которые влияют на:
активность трансмембранных транспортеров питательных веществ;
активность внутриклеточных ферментов метаболизма углеводов и жиров;
транскрипцию в ядре клетки ряда генов.
Замедленный ответ (развивается через несколько часов). Обусловлен фосфорилированием остатков тирозина в молекуле IRS-1, которая стимулирует митоген-активируемые протеинкиназы (МАРК) и запускает процесс роста клеток и синтеза ДНК.
Физиологические эффекты инсулина. Основным эффектом инсулина является его влияние на транспорт глюкозы в клетки. Через мембрану клеток глюкоза проникает путем облегченного транспорта за счет специальных переносчиков – транспортеров глюкозы GLUT. Различают 5 видов этих транспортеров, которые могут быть объединены в 3 семейства:
GLUT-1,3,5 – транспортеры глюкозы в инсулиннезависимые ткани. Для работы этих транспортеров не требуется инсулин. Они имеют крайне высокое сродство к глюкозе (Km1-2 мМ) и обеспечивают транспорт глюкозы в эритроциты, нейроны мозга, эпителий кишечника и почек, плаценту.
GLUT-2 – транспортер глюкозы в инсулинрегулирующие ткани. Он также не требует для своей работы инсулина и активируется только при высоких концентрациях глюкозы, так как имеет к ней крайне низкое сродство (Km15-20 мМ). Обеспечивает транспорт глюкозы в клетки поджелудочной железы и печени (т.е. в те ткани, где идет синтез и деградация инсулина). Он принимает участие в регуляции секреции инсулина при повышении уровня глюкозы.
GLUT-4 – транспортер глюкозы в инсулинзависимые ткани. Этот транспортер имеет промежуточное сродство к глюкозе (Km5 мМ), но в присутствии инсулина его сродство к глюкозе резко повышается и он обеспечивает захват глюкозы клетками мышц, адипоцитами, печенью.
Под влиянием инсулина происходит перемещение молекул GLUT-4 из цитоплазмы клетки в ее мембрану (увеличивается количество молекул переносчика в мембране), повышается сродство переносчика к глюкозе и она поступает внутрь клетки. В итоге, концентрация глюкозы в крови понижается, а в клетке возрастает.
В таблице 3 представлено влияние инсулина на обмен веществ в инсулинзависимых тканях (печени, скелетных мышцах, жировой ткани).
Таблица 3. Влияние инсулина на обмен веществ в органах мишенях.
Мембранный эффект
Внутриклеточный эффект
транспорта глюкозы в клетку
гликогенолиза (угнетает гликогенфосфорилазу);
синтеза гликогена (активирует глюкокиназу и гликогенсинтетазу);
глюконеогенез из аминокилот и глицерина (угнетает фосфоенолпируват карбоксикиназу)
гликолиз (активирует гексокиназу, которая фосфорилирует глюкозу и способствует ее удержанию в клетке, повышает активность фосфофруктокиназы и пируваткиназы).
превращение жирных кислот в кетокислоты и синтез кетоновых тел (ацетоуксусной и -оксимасляной кислот, ацетона).
синтез триглицеридов и ЛПОНП (транспортная форма липидов).
захват K + и PO4 3-
транспорта глюкозы в клетку
гликогенолиза (угнетает гликогенфосфорилазу);
синтеза гликогена (активирует глюкокиназу и гликогенсинтетазу).
транспорта аминокислот в клетку
рибосомальный синтез белков;
синтез ДНК и РНК.
Жировая ткань
транспорта глюкозы в клетку
гликолиз с образованием диоксиацетонфосфата, необходимого для синтеза глицерина
транспорта жирных кислот в клетку
липогенез и синтез триглицеридов из глицеролфосфата и жирных кислот (активирует ацетил-КоА- карбоксилазу);
активность липопротеидлипазы (высвобождение триглицеридов из липопротеинов).
В целом для инсулина характерно анаболическое действие на процессы обмена белков, жиров и углеводов (т.е. усиление синтетических реакций) и антикатаболические эффекты (торможение распада гликогена и липидов).
Терапевтические эффекты инсулина при сахарном диабете связаны с тем, что инсулин нормализует транспорт глюкозы в клетку и устраняет все проявления диабета (таблица 4).
Таблица 4. Терапевтические эффекты инсулина.
Проявления диабета
Действие инсулина
Гипергликемия – обусловлена нарушением транспорта глюкозы в клетку и ее накоплением в крови.
Нормализует транспорт глюкозы в клетку и ее внутриклеточное фосфорилирование, что способствует удержанию глюкозы в клетке. Уровень гликемии понижается.
Полиурия. Во время фильтрации в почках глюкоза выделяется в мочу и если ее уровень превышает возможность переносчиков в канальцах нефрона реабсорбировать глюкозу, ее излишек начинает выделяться с мочой. Повышается осмотическое давление мочи и это замедляет реабсорбцию воды – количество мочи резко увеличивается.
Инсулин нормализует уровень глюкозы в крови, выделение глюкозы в мочу снижается и переносчики полностью удаляют глюкозу из мочи. Осмотичность мочи падает и реабсорбция воды возвращается к норме. Диурез снижается.
Полидипсия. Потеря воды с мочой и увеличение уровня глюкозы в крови повышают осмотичность крови и активируют осморецепторы гипоталамуса, что проявляется возникновением жажды.
Нормализация диуреза обеспечивает сохранение жидкости в организме и осмотическое давление крови падает. Осморецепторы центра жажды в гипоталамусе не активны и потребление жидкости понижается.
Инсулин восстанавливает поступление глюкозы в клетку, синтез АТФ и нормализует аппетит.
Похудание. Недостаток субстратов для синтеза АТФ компенсаторно усиливает липолиз и -окисление жирных кислот, как альтернативный источник энергии.
Инсулин восстанавливает поступление глюкозы в клетку и синтез АТФ гликолитическим путем, уменьшает липолиз и активирует липогенез.
Кетонемия. Для обеспечения клеток организма субстратами для синтеза АТФ печень начинает синтезировать кетоновые тела из ацетилКоА, который высвободился в ходе -окисления жирных кислот.
Инсулин восстанавливает транспорт глюкозы в клетку и синтез АТФ гликолитическим путем, потребность в кетоновых телах устраняется и их синтез прекращается.
Полинейропатии и полиангиопатии. Избыток глюкозы в крови приводит к активации инсулиннезависимых путей ее метаболизма – глюкоза конвертируется в сорбитол (сорбитоловый шунт) и затем во фруктозу. Избыток сорбитола откладывается в тканях сосудов, нервов и хрусталика глаза.
Инсулином восстанавливается инсулинзависимый метаболизм глюкозы и активность сорбитолового шунта падает.
Пиодермия. Избыток глюкозы в крови приводит к гликозилированию белков клеток иммунной системы (иммуноглобулинов, интерферона и лизоцима). Это нарушает нормальное протекание иммунных реакций
Инсулин нормализует уровень глюкозы и прекращает гликозилирование белков, которые участвуют в иммунном ответе.
Характеристика препаратов инсулина. В медицинской практике применяют 3 вида инсулинов – говяжий, свиной, человеческий. Инсулин быка отличается от инсулина человека всего 3 аминокислотами, тогда как инсулин свиньи – только одной аминокислотой. В связи с этим инсулин свиньи более гомологичен инсулину человека и менее антигенен, чем инсулин быка. В настоящее время во всех развитых странах не рекомендовано применять для лечения лиц больных диабетом говяжьи инсулины.
Читайте также:

