Окислительно восстановительные свойства серы и ее соединений кратко
Обновлено: 05.07.2024
Сера на наружном энергетическом уровне содержит 6 электронов, из которых два непарные. Так же как и кислород располагается в VI группе главной подгруппе периодической системы химических элементов. Впрочем, по сравнению с атомами кислорода атомы серы имеют больший радиус, меньшее значение электроотрицательности. В связи с этим может проявлять восстановительные и окислительные свойства. В качестве восстановителя формирует соединения со степенями окисления +2, +4, +6. По отношению к водороду и металлам сера показывает окислительные свойства со степенью окисления –2.

I. Окислительные свойства
-
Взаимодействует с металлами
При обычных условиях реагирует со щелочными, щелочноземельными металлами, медью, ртутью, серебром.
Mg + S → MgS
Hg + S → HgS
Соединения серы с металлами называют сульфидами.
II. Восстановительные свойства
-
При взаимодействии со сложными веществами, с выраженными окислительными свойствами, сера проявляет себя восстановителем.
По механизму реакции диспропорционирования сера реагирует со щелочами:
При внесении горящей серы в кислород сгорание ее ускоряется, и пламя становиться ярко-синим.
Сера - элемент VIa группы 3 периода периодической таблицы Д.И. Менделеева. Относится к группе халькогенов - элементов VIa группы.
Сера - S - простое вещество имеет светло-желтый цвет. Использовалась еще до нашей эры в составе священных курений при религиозных обрядах.

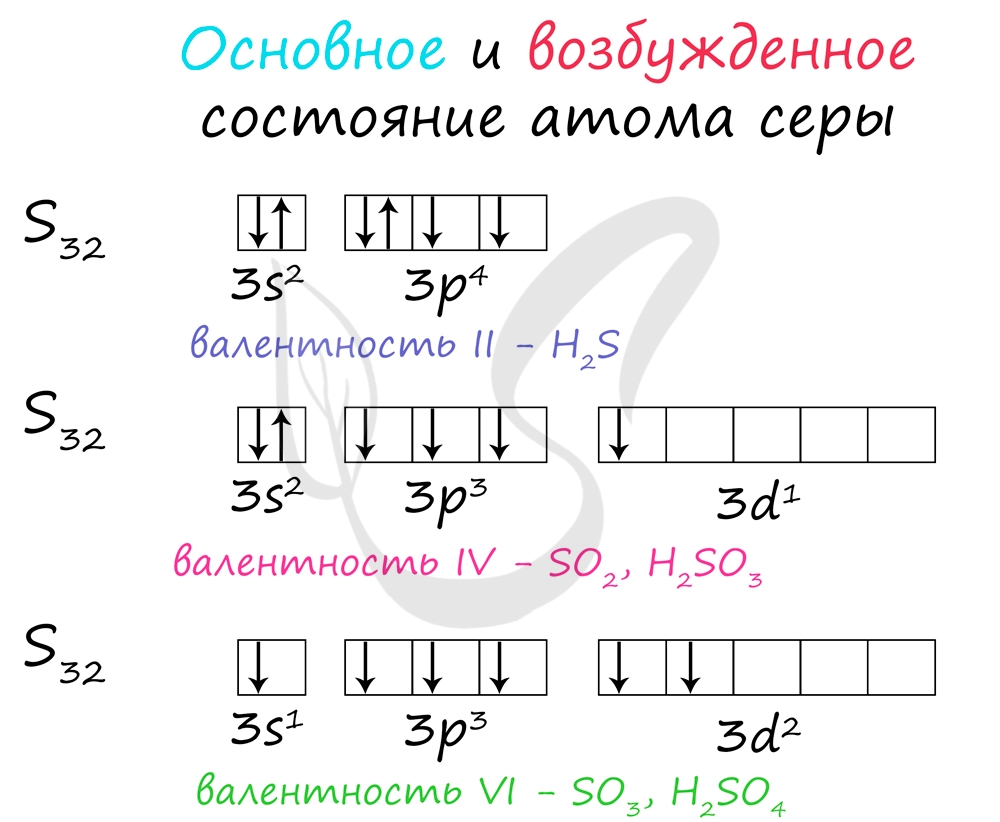
Основное и возбужденное состояние атома серы
Электроны s- и p-подуровня способны распариваться и переходить на d-подуровень. Как и всегда, количество валентных электронов отражает количество возможных связей у атома.
В разных электронных конфигурациях сера способна принимать валентности: II, IV и VI.
Природные соединения
- FeS2 - пирит, колчедан
- ZnS - цинковая обманка
- PbS - свинцовый блеск (галенит), Sb2S3 - сурьмяный блеск, Bi2S3 - висмутовый блеск
- HgS - киноварь
- CuFeS2 - халькопирит
- Cu2S - халькозин
- CuS - ковеллин
- BaSO4 - барит, тяжелый шпат
- CaSO4 - гипс
В местах вулканической активности встречаются залежи самородной серы.

В промышленности серу получают из природного газа, который содержит газообразные соединения серы: H2S, SO2.
Серу можно получить разложением пирита
В лабораторных условиях серу можно получить слив растворы двух кислот: серной и сероводородной.
-
Реакции с неметаллами
На воздухе сера окисляется, образуя сернистый газ - SO2. Реагирует со многими неметаллами, без нагревания - только со фтором.

При нагревании сера бурно взаимодействует со многими металлами с образованием сульфидов.
При взаимодействии с концентрированными кислотами (при длительном нагревании) сера окисляется до сернистого газа или серной кислоты.
Сера вступает в реакции диспропорционирования с щелочами.
Сера вступает в реакции с солями. Например, в кипящем водном растворе сера может реагировать с сульфитами с образованием тиосульфатов.
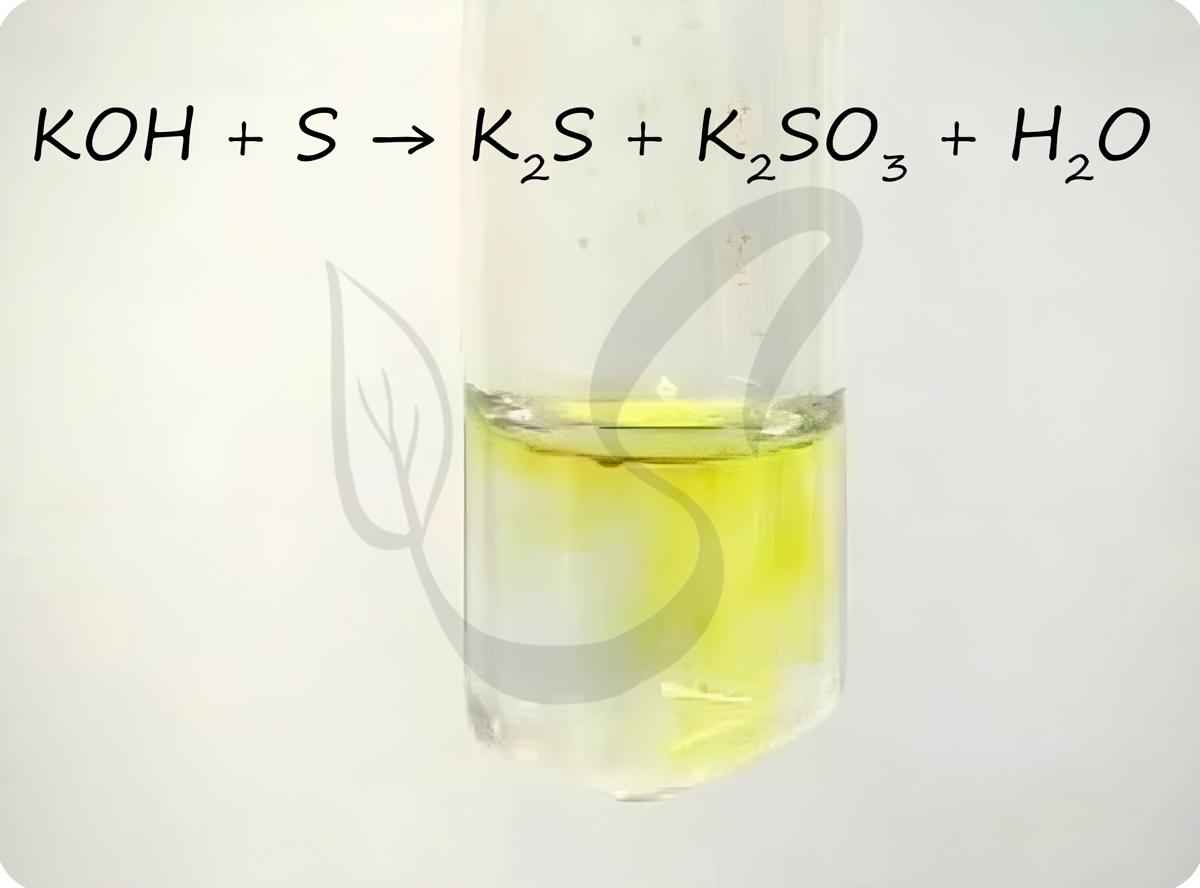
Сероводород - H2S
Бесцветный газ с характерным запахом тухлых яиц. Огнеопасен. Используется в химической промышленности и в лечебных целях (сероводородные ванны).

Сероводород получают в результате реакции сульфида алюминия с водой, а также взаимодействия разбавленных кислот с сульфидами.

Сероводород плохо диссоциирует в воде, является слабой кислотой. Реагирует с основными оксидами, основаниями с образованием средних и кислых солей (зависит от соотношения основания и кислоты).
KOH + H2S = KHS + H2O (гидросульфид калия, избыток кислоты)
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из кислоты.
Сероводород - сильный восстановитель (сера в минимальной степени окисления S 2- ). Горит в кислороде синим пламенем, реагирует с кислотами.

Качественной реакцией на сероводород является реакция с солями свинца, при котором образуется сульфид свинца.
Оксид серы - SO2
Сернистый газ - SO2 - при нормальных условиях бесцветный газ с характерным резким запахом (запах загорающейся спички).

В промышленных условиях сернистый газ получают обжигом пирита.
В лаборатории SO2 получают реакцией сильных кислот на сульфиты. В ходе подобных реакций образуется сернистая кислота, распадающаяся на сернистый газ и воду.
Сернистый газ получается также в ходе реакций малоактивных металлов с серной кислотой.
С основными оксидами, основаниями образует соли сернистой кислоты - сульфиты.

Химически сернистый газ очень активен. Его восстановительные свойства продемонстрированы в реакциях ниже.
В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства (понижать степень окисления).
Сернистая кислота
Слабая, нестойкая двухосновная кислота. Существует лишь в разбавленных растворах.
Диссоциирует в водном растворе ступенчато.
В реакциях с основными оксидами, основаниями образует соли - сульфиты и гидросульфиты.
H2SO3 + KOH = H2O + KHSO3 (соотношение кислота - основание, 1:1)
С сильными восстановителями сернистая кислота принимает роль окислителя.
Как и сернистый газ, сернистая кислота и ее соли обладают выраженными восстановительными свойствами.

Оксид серы VI - SO3
Является высшим оксидом серы. Бесцветная летучая жидкость с удушающим запахом. Ядовит.
В промышленности данный оксид получают, окисляя SO2 кислородом при нагревании и присутствии катализатора (оксид ванадия - Pr, V2O5).
В лабораторных условиях разложением солей серной кислоты - сульфатов.
Является кислотным оксидом, соответствует серной кислоте. При реакции с основными оксидами и основаниями образует ее соли - сульфаты и гидросульфаты. Реагирует с водой с образованием серной кислоты.
SO3 + 2KOH = K2SO4 + 2H2O (основание в избытке - средняя соль)
SO3 + KOH = KHSO4 + H2O (кислотный оксид в избытке - кислая соль)

SO3 - сильный окислитель. Чаще всего восстанавливается до SO2.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Сера — химический элемент № \(16\). Она расположена в VI А группе третьем периоде Периодической системы.
На внешнем слое атома серы содержатся шесть валентных электронов. До завершения внешнего слоя не хватает двух электронов. Поэтому в соединениях с металлами и водородом сера проявляет степень окисления \(–2\). При взаимодействии с более электроотрицательными элементами (кислородом, галогенами) сера образует соединения, в которых её степень окисления положительная (\(+4\) или \(+6\)).
В земной коре сера встречается в самородном виде или в виде минералов и горных пород: (пирит — Fe S 2 , цинковая обманка — ZnS , свинцовый блеск — PbS , гипс — CaS O 4 ⋅ 2 H 2 O , глауберова соль — Na 2 S O 4 ⋅ 10H 2 O ).


Сера образует несколько аллотропных модификаций. Обычно мы имеем дело с кристаллической серой, которая состоит из восьмиатомных циклических молекул.
Молекулы образуют кристаллы разного строения, и поэтому существуют аллотропные видоизменения: ромбическая и моноклинная сера. Обе модификации представляют собой жёлтые легкоплавкие вещества. Температуры плавления их несколько различаются (\(+112,8\) °С и \(+119,3\) °С).

При нагревании сера плавится, превращается в лёгкую жидкость, а затем начинает темнеть и становится вязкой. Образуется пластическая сера, состоящая из длинных линейных молекул.
В воде сера не растворяется и ею не смачивается . Поэтому порошок серы не тонет в воде, несмотря на более высокую плотность (\(2,07\) г/см³). Такое явление называется флотацией .
Подожжённая сера реагирует с кислородом , и образуется сернистый газ. Сера в этой реакции — восстановитель .
При нагревании сера вступает в реакцию с большинством металлов — железом, алюминием, цинком и другими, кроме золота и платины.
Ключевые слова конспекта: соединения серы, серная кислота, участие в кислотно-основных и окислительно-восстановительных взаимодействиях, получение и применение серной кислоты.

Серная кислота H2SO4 – вещество молекулярного строения. Её графическая формула:
В серной кислоте сера находится в высшей степени окисления +6.
Серная кислота представляет собой бесцветную маслянистую жидкость, хорошо растворимую в воде. Смешивается с водой в неограниченном количестве и очень гигроскопична. При растворении верной кислоты в воде выделяется значительное количество теплоты.
Химические свойства серной кислоты можно рассмотреть с точки зрения кислотно-основных и окислительно-восстановительных взаимодействий.
Участие в кислотно-основных взаимодействиях
- Серная кислота – сильный электролит, в водных растворах диссоциирует практически полностью:

Изменяет окраску индикатора (например, лакмуса с фиолетовой на красную).
Более корректно электролитическая диссоциация H2SO4 описывается уравнениями:

- Серная кислота реагирует с основными и амфотерными оксидами:
H2SO4 + CuO = CuSO4 + H2O
2Н + + CuO = Cu 2+ + H2O
- Серная кислoта реагирует с основаниями и амфотерными гидроксидами:
H2SO4 + Cu(OH)2 = CuSO4 + 2H20
2Н + + Cu(OH)2 = Cu 2+ + 2H20
- Сернaя кислота вытесняет более слабые кислоты из их солей:

- Сeрная кислота вытесняет и сильные, но летучие кислоты из их солей:

Участие в окислительно-восстановительных взаимодействиях

Разбавленные растворы H2SO4 реагируют с металлами, расположенными в электрохимическом ряду напряжений металлов до H2, с образованием сульфатов и выделением водорода:
Чистая H2SO4 и H2SO4 в концентрированных растворах проявляют сильные окислительные свойства за счёт S +6 .
Концентрированная H2SO4 взаимодействует с металлами (в том числе с Cu, Ag, Hg), стоящими после H2 в ряду напряжений металлов, с образованием сульфатов, воды и продуктов восстановления S +6 : H2S, S, SO2. Концентрированная серная кислота не реагирует с благородными металлами вследствие их малой активности, а также с Al, Cr, Fe из-за пассивации. На поверхности этих металлов образуется защитная оксидная плёнка, защищающая их от дальнейшего окисления.

Глубина восстановления зависит от восстановительных свойств металлов.
Активные металлы восстанавливают H2SO4 до H2S:

Металлы с меньшей активностью восстанавливают H2SO4 до SO2:

Концентрированная сeрная кислoта окисляет и некоторые неметаллы. Например:

Важной химической особенностью серной кислоты является её способность выступать в качестве дегидратирующего реагента. Концентрированная серная кислота вступает в реакции дегидратации со многими органическими веществами, отщепляя от них молекулы воды. Например:
Получение и применение серной кислоты
Промышленное получение серной кислоты включает несколько стадий. Сырьём является сера S и сульфидные руды (в основном пирит FeS2).
В ходе получения серной кислоты из пирита осуществляются три химические реакции:
- Обжиг пирита (проводится при температуре около 800 °С):

Эта реакция – обратимая, экзотермическая, каталитическая (её проводят в присутствии катализатора V2O5 при температуре около 450 °С).
Оксид серы (VI) (серный ангидрид) SO3 при обычных условиях – летучая жидкость (t°кип. = 44,8 °С), неограниченно растворяется в воде. Оксид серы (VI) SO3 – кислотный оксид, ему соответствует сильная серная кислота.
В промышленности для этой реакции используют концентрированную H2SO4, образуется олеум H2SO4 • SO3, при разбавлении которого получают концентрированную H2SO4.
Серная кислота – один из важнейших продуктов химической промышленности. Важнейшие области её применения: производство минеральных удобрений, других кислот и солей, красителей, пластмасс, волокон, лекарственных веществ, очистка нефтепродуктов, металлургия.
Читайте также:

