Механизм регуляции синтеза белка у эукариот кратко
Обновлено: 04.07.2024
Регуляция синтеза белков в клетках эукариот сложнее: не характерна прямая субстратная регуляция, так как опероны ( транскриптоны) имеют обширные регуляторные зоны; структурные гены разбросаны по геному; в ядрах дифференцированных клеток эукариот большинство генов находится в репрессированном состоянии; все структурные гены делят уэукариот на три группы - гены, функционирующие во всех клетках организма, в тканях одного типа, в специализированных клетках одного типа; пространственное разделение процессов - транскрипция в ядре, трансляция в рибосомах.
Регуляция биосинтеза белка уэукариот происходит на всех уровнях матричных биосинтезов.
1. На уровне генов:
ü Репрессия генов: Стойкая репрессия генов гетерохроматина обеспечивается пространственной укладкой ДНК, при которой гетерохроматин находится в высококонденсированном состояни связыванием с гистонами и образованием нуклеосом, которые также снижают транскрипционную активность ДНК.
ü Перестройка генов:Перемещения генов между хромосомами или внутри хромосомы, объединение генов с образованием изменённой хромосомы, которая после таких структурных изменений способна к репликации и транскрипции. Этот процесс получил название "генетическая рекомбинация". Напимер: при половом слиянии яйцеклетки и сперматозоида.
ü Изменение количества генов:Амплификация (или увеличение числа) генов используется организмом в том случае, когда возникает необходимость увеличить синтез определённого генного продукта. Умплификация (утрата генетического материала) - довольно редкий способ регуляции. Наиболее яркий пример потери всех генов за счёт разрушения ядра - процесс созревания эритроцитов.
2. Регуляция транскрипции:Изменение скорости транскрипции отдельных генов под влиянием регуляторных белков.Энхансеры - участки ДНК размером 10-20 пар оснований, присоединение к которым регуляторных белков увеличивает скорость транскрипции. Они не кодируют синтез белка, чрезвычайно эффективны, может наблюдаться 200-кратное усиление транскрипции. Если участки ДНК, связываясь с белками, обеспечивают замедление транскрипции, то их называют сайленсерами.
3. Посттранскрипционная регуляция на уровне процессинга мРНК.Дифференциальный процессинг включает альтернативный сплайсинг - сборка РНК из разных экзонов. Редактирование мРНК - замена одного из нуклеотидов с изменением генетической информации, приводящее к образованию изменённых белков.
4. На уровне стабильности и активности мРНК. мРНК в клетке образует комплекс с белками, который называется инфосома. В их составе мРНК не разрушается ферментами, сохранения в активном, стабильном состоянии. При необходимости она высвобождается из комплекса и транслируется. Процесс образования и распада инфосом регулируется гормонами. С одной молекулы РНК транслируется большое количество белков.
6. Регуляция на уровне трансляции:
ü Избирательная дискриминация. Определённые виды мРНК избирательно не транслируются. С них не синтезируется белок.
ü Трансляция с альтернативных стартовых участков.таким образом может происходить выбор исходной стартовой точки трансляции.
ü Тотальная регуляция может быть в виде тотальной репрессии или индукции за счёт изменения концентрации белковых факторов трансляции.
Механизмы регуляции биосинтеза белков у эукариот более разнообразны и осуществляются на разных уровнях. Так, стойкую репрессию генов вызывает компактная упаковка хроматина, включая взаимодействие с гистонами, образование нуклеосом и хроматиновых фибрилл. В гетерохроматине для транскрипции доступно менее 1% генов, в эухроматине, имеющем более рыхлую укладку, − значительно больше. В разных типах клеток в область эухроматина попадают неодинаковые гены, что обеспечивает стабильную репрессию одних генов и дерепрессию других на протяжении всей жизни клетки.
Большинство генов эукариот подвергается адаптивной регуляции, осуществляющейся на уровне транскрипции. Вследствие огромной протяженности и сложности эукариотической ДНК специфические регуляторные участки ДНК и взаимодействующие с ними белки-регуляторы весьма многочисленны. Выявлено более 100 различных белков, способных взаимодействовать с регуляторными последовательностями ДНК и тем самым влиять на сборку транскрипционного комплекса и скорость транскрипции. Эти белки содержат ДНК-связывающие домены, отвечавшие за узнавание специфических участков в молекуле ДНК, а также домены, активирующие транскрипцию. Последние связываются с транскрипционными факторами либо с РНК-полимеразой. Регуляторные белки могут иметь в своем составе антирепрессорные домены, которые взаимодействуют с гистонами нуклеосом, освобождая от них участки ДНК. Эти белки могут содержать в себе также домены, связывающие лиганды – индукторы транскрипции (стероидные гормоны, гормоны щитовидной железы, производные витаминов). После связывания лиганда конформация белка изменяется, и он образует участок, узнающий в регуляторной зоне ДНК специфическую последовательность и индуцирующий транскрипцию определенного гена.
Важную роль в регуляции активности генов играют участки ДНК, расположенные на значительном (1000 и более пар оснований) расстоянии от промотора.
Регуляция на уровне транскрипции наиболее экономична, но она осуществляется недостаточно быстро. Поэтому важное значение имеет регуляция на других этапах реализации генетической информации.
На многих эукариотических генах, имеющих полиэкзонное строение, после транскрипции и процессинга образуется несколько вариантов зрелой мРНК, когда зкзон одного варианта сплайсинга может оказаться интроном в другом. Это приводит к образованию разных мРНК и, соответственно, разных белков с одного первичного транскрипта. Так, в парафолликулярных клетках щитовидной железы в ходе транскрипции гена гормона кальцитонина образуется первичный транскрипт мРНК, который имеет в своем составе шесть экзонов. мРНК кальцитонина образуется путем сплайсинга первых четырех зкзонов. Этот же первичный транскрипт в клетках головного мозга в ходе альтернативного сплайсинга образует другую мРНК, кодирующую белок, не обладающий гормональной активностью.
На состав белков клетки оказывает влияние также неодинаковая стабильность мРНК. Время жизни эукариотических мРНК составляет от нескольких часов до нескольких дней. Расположенный на 3'-конце фрагмент поли-(А) увеличивает продолжительность жизни молекул мРНК и, соответственно, количество белка.
Регуляция синтеза белка осуществляется и на уровне трансляции. Разные мРНК имеют неодинаковое сродство к рибосомным субчастицам, поэтому полирибосома может содержать различное количество рибосом. Так определяется соотношение белков в клетке. Наконец, может происходить подавление инициации трансляции всех мРНК клетки (например, при действии теплового шока, стрессах, недостатке железа, вирусной инфекции и т. п.). Стрессовый фактор индуцирует фосфорилирование второго фактора инициации (IF-2), тем самым инактивирует его и, следовательно, трансляцию.

Механизмы регуляции биосинтеза белков у эукариот более разнообразны и осуществляются на разных уровнях. Так, стойкую репрессию генов вызывает компактная упаковка хроматина, включая взаимодействие с гистонами, образование нуклеосом и хроматиновых фибрилл. В гетерохроматине для транскрипции доступно менее 1% генов, в эухроматине, имеющем более рыхлую укладку, − значительно больше. В разных типах клеток в область эухроматина попадают неодинаковые гены, что обеспечивает стабильную репрессию одних генов и дерепрессию других на протяжении всей жизни клетки.
Большинство генов эукариот подвергается адаптивной регуляции, осуществляющейся на уровне транскрипции. Вследствие огромной протяженности и сложности эукариотической ДНК специфические регуляторные участки ДНК и взаимодействующие с ними белки-регуляторы весьма многочисленны. Выявлено более 100 различных белков, способных взаимодействовать с регуляторными последовательностями ДНК и тем самым влиять на сборку транскрипционного комплекса и скорость транскрипции. Эти белки содержат ДНК-связывающие домены, отвечавшие за узнавание специфических участков в молекуле ДНК, а также домены, активирующие транскрипцию. Последние связываются с транскрипционными факторами либо с РНК-полимеразой. Регуляторные белки могут иметь в своем составе антирепрессорные домены, которые взаимодействуют с гистонами нуклеосом, освобождая от них участки ДНК. Эти белки могут содержать в себе также домены, связывающие лиганды – индукторы транскрипции (стероидные гормоны, гормоны щитовидной железы, производные витаминов). После связывания лиганда конформация белка изменяется, и он образует участок, узнающий в регуляторной зоне ДНК специфическую последовательность и индуцирующий транскрипцию определенного гена.
Важную роль в регуляции активности генов играют участки ДНК, расположенные на значительном (1000 и более пар оснований) расстоянии от промотора.
Регуляция на уровне транскрипции наиболее экономична, но она осуществляется недостаточно быстро. Поэтому важное значение имеет регуляция на других этапах реализации генетической информации.
На многих эукариотических генах, имеющих полиэкзонное строение, после транскрипции и процессинга образуется несколько вариантов зрелой мРНК, когда зкзон одного варианта сплайсинга может оказаться интроном в другом. Это приводит к образованию разных мРНК и, соответственно, разных белков с одного первичного транскрипта. Так, в парафолликулярных клетках щитовидной железы в ходе транскрипции гена гормона кальцитонина образуется первичный транскрипт мРНК, который имеет в своем составе шесть экзонов. мРНК кальцитонина образуется путем сплайсинга первых четырех зкзонов. Этот же первичный транскрипт в клетках головного мозга в ходе альтернативного сплайсинга образует другую мРНК, кодирующую белок, не обладающий гормональной активностью.
На состав белков клетки оказывает влияние также неодинаковая стабильность мРНК. Время жизни эукариотических мРНК составляет от нескольких часов до нескольких дней. Расположенный на 3'-конце фрагмент поли-(А) увеличивает продолжительность жизни молекул мРНК и, соответственно, количество белка.
Регуляция синтеза белка осуществляется и на уровне трансляции. Разные мРНК имеют неодинаковое сродство к рибосомным субчастицам, поэтому полирибосома может содержать различное количество рибосом. Так определяется соотношение белков в клетке. Наконец, может происходить подавление инициации трансляции всех мРНК клетки (например, при действии теплового шока, стрессах, недостатке железа, вирусной инфекции и т. п.). Стрессовый фактор индуцирует фосфорилирование второго фактора инициации (IF-2), тем самым инактивирует его и, следовательно, трансляцию.
У прокариот, если какой-нибудь участок транскрибируется, то он автоматически транслируется, т. е. регуляция синтеза белка у прокариот осуществляется на уровне транскрипции.
У эукариот транскрипция и трансляция пространственно разделены (транскрипция в ядре, трансляция в цитоплазме) , и регуляция синтеза белка происходит в три этапа
транскрипция
экспорт из ядра
трансляция
Регуляция синтеза белка у эукариот осуществляется в основном на уровне трансляции, когда регуляторные вещества присоединяются к управляющим участкам 3’-НТО и 5’-НТО.
5'-НТО отвечает за частоту трансляции
3'-НТО отвечает за время жизни иРНК в цитоплазме.
Транскрипция у эукариот регулируется почти так же, как у прокариот. Разница: у эукариот транскрипция может не только подавляться репрессорами, присоединенными к операторам, но и стимулироваться активаторами, присоединенными к энхансерам опероны у эукариот пространственные, т. е. участок, к которому присоединен репрессор, может находиться не в том же участке хромосомы, где лежат промотор и структурные гены, и приближаться к ним за счет укладки ДНК в интерфазном ядре.

В статье автор рассматривает особенности регуляции биосинтеза белка у прокариот и эукариот, а также факторы, влияющие на него.
Ключевые слова: биосинтез белка, прокариоты, эукариоты, факторы, система оперон, белки, ферменты, белок-репрессор.
В нашем мире существует 2 вида организмов: прокариотические и эукариотические. Они отличаются строением и происходящими в них биологическими процессами, в том числе и биосинтезом белка — разновидностью пластического обмена, в ходе которого генетическая информация ДНК преобразуется в последовательность аминокислот будущего белка. На этот сложный процесс у про- и эукариот оказывают влияние разные факторы.
Регуляция биосинтеза у прокариот происходит на уровне транскрипции, поскольку он неразрывен с трансляцией. Он основан на регуляции активности генов, схема которой была открыта в 1961 Жакобом и Моно и названа опероном. Ученые проводили опыты на примере кишечной палочки и описали действие лактозного оперона. Они определили, что гены функционально неодинаковы: различают структурные гены, которые составляют структуру оперона, кодируют последовательность аминокислот в белке, и регуляторные гены, влияющие на работу структурных генов посредством белка-репрессора, который он кодирует. Любой оперон строится по определенному принципу: вначале стоит промотор, ответственный за связывание с РНК-полимеразой, за ним — оператор, включающий и выключающий структурные гены и определяющий работу гена-регулятора, далее следует последовательность генов, кодирующих определенную структуру белка, и заканчивается оперон геном-терминатором, сигнализирующем о прекращении синтеза РНК [4].
Рассмотреть действие оперона проще всего на лактозном опероне кишечной палочки (Рис. 1). При наличии глюкозы в цитоплазме бактерии, белок-репрессор находится на промоторе, тем самым препятствуя началу транскрипции. При попадании путем пассивного транспорта в клетку лактозы, последняя связывается с белком-репрессором, что приводит к отсоединению белка от промотора. На данном участке становится возможным транскрипция, в результате образуется и-РНК, кодирующая 3 белка. После трансляции и-РНК мы получаем фермент β-галактозидазу, пермиазу и β-галактозид трансацетилазу. Первый расщепляет лактозу на глюкозу и галактозу, второй является интегральным мембранным белком, обеспечивающим легкое и быстрое проникновение лактозы из окружающей среды в клетку. Когда лактоза заканчивается, она отщепляется от белка-рецептора и тот возвращается на промотор, препятствуя синтезу и-РНК. Таким образом, на примере работы оперона наиболее ярко видна регуляция биосинтеза белка в прокариотической клетке.
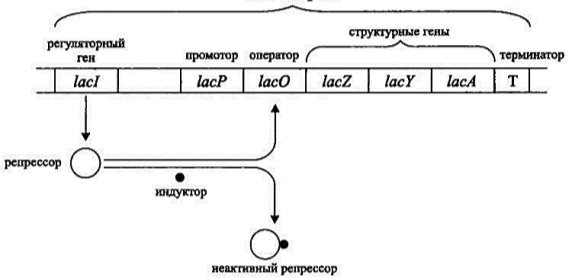
Рис. 1. Лактозный оперон
Другой пример — триптофанный оперон кишечной палочки. Он работает по другому принципу. До тех пор, пока триптофан расходуется, клетка его синтезирует. Но как только возникает избыток данной аминокислоты, она связывается с белком-репрессором. Данный белок присоединяется к промотору оперона, что приводит к прекращению синтеза триптофана. Со временем клетка расходует запасенную аминокислоту, начинает испытывать недостаток. Тогда триптофан отсоединяется от белка-репрессора, последний больше не может удерживаться на промоторе и освобождает. После этого начинается синтез и-РНК с матрицы оперона, после трансляции которой клетка получает необходимую ей кислоту триптофан. Цикл повторяется [2].

Рис. 2. Триптофанный оперон
Вообще, биосинтез микроорганизмов может осуществляться двумя путями: быстрым и более медленным. В первом случае речь идет о секундах или минутах, а механизм регуляции активности фермента зависит от изменений молекул, входящих в его состав. Во втором случае процесс может занимать часы, а количество фермента определяется интенсивностью процессов синтеза и распада оного. В обоих случаях работает принцип обратной связи — благодаря низкомолекулярным соединениям определяется количественное соотношение различных веществ в составе клетки, а структура и количество этого соединения определяется регуляторными механизмами биосинтеза [3].
В эукариотических клетках процессы транскрипции и трансляции разделены ядерной мембраной: транскрипция происходит в ядре, трансляция — в цитоплазме, поэтому в качестве одного из этапов биосинтеза выделяют экспорт из ядра. В пределах эукариотических клеток также можно рассматривать систему оперон, однако она будет иметь свои особенности.
Первая особенность состоит в пространственной организации оперона: если у эукариот гены оперона находятся последовательно друг за другом, то в эукариотической клетке репрессор может находится не в том же участке хромосомы, что промотор и структурные гены, а приближаться к ним только в интерфазу при высоком уровне компактизации хромосомы [1].
Такой способ регуляции считается достаточно экономичным, однако на него затрачивается большое количество времени, поэтому регуляция белка у клеток данного типа осуществляется на уровне трансляции посредством регуляторных веществ, присоединяющихся к 3’ и 5’ не транскрибируемым участкам. Здесь количественное соотношение белков регулируется благодаря разной продолжительности жизни м-РНК, определяемой полиадениловым фрагментом 3’ конца ДНК. Кроме того, структура и-РНК определяет сродство к рибосомальным субъединицам, что влияет на длину полисомы, а значит и на количество образующегося белка. Возможно также полное подавление трансляции при действии неблагоприятных и стрессовых факторов, которые негативно сказываются на факторах инициации.
Таким образом, у прокариот и эукариот механизмы регуляции биосинтеза белка различны. Для первого типа организмов характерна регуляция на уровне транскрипции, для второго — на уровне и транскрипции, и трансляции. В обоих случаях применима схема оперона, однако существуют определенные различия для этих видов клеток: важно учитывать трехмерную организацию оперона и наличие энхансеров и сайленсеров в эукариотической клетке. Количественное содержание белков в этом типе клеток находится под влиянием регуляторных веществ и определяется генами ДНК.
Основные термины (генерируются автоматически): кишечная палочка, клетка, оперон, белок, биосинтез белка, ген, последовательность аминокислот, последовательность генов, промотор, трансляция, уровень транскрипции, эукариот.
Читайте также:

