Кетоновые тела биохимия кратко
Обновлено: 02.07.2024
При состояниях, сопровождающихся снижением глюкозы крови, клетки органов и тканей испытывают энергетический голод. Так как окисление жирных кислот процесс "трудоемкий", а нервные клетки вообще неспособны окислять жирные кислоты, то печень облегчает использование этих кислот тканями, заранее окисляя их до уксусной кислоты и переводя последнюю в транспортную форму – кетоновые тела .
К кетоновым телам относят три соединения близкой структуры – ацетоацетат , 3-гидроксибутират и ацетон .
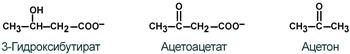
Строение кетоновых тел
Стимулом для образования кетоновых тел служит поступление большого количества жирных кислот в печень. Как уже указывалось, при состояниях, активирующих липолиз в жировой ткани, не менее 30% образованных жирных кислот задерживаются печенью. К таким состояниям относится голодание , сахарный диабет I типа , длительные физические нагрузки . Так как синтез ТАГ в этих условиях невозможен, то жирные кислоты из цитозоля попадают в митохондрии и окисляются с образованием кетоновых тел.
Для понимания причин развития кетонемии при различных ситуациях необходимо понимать роль оксалоацетата для регуляции цикла трикарбоновых кислот. При голодании соотношение инсулин/глюкагон низкое и поэтому в печени активно идет глюконеогенез, для которого используется оксалоацетат. Поэтому при голодании жирные кислоты, поступающие в большом количестве в печень, не сгорают в ЦТК, а уходят в синтез кетоновых тел. При длительной мышечной нагрузке резервы гликогена в печени истощаются, развивается тенденция к гипогликемии и секретируется глюкагон, который усиливает глюконеогенез, при этом количество оксалоацетата снижается, и жирные кислоты, попавшие в печень, будут окисляться с образованием кетоновых тел.
Кроме отмеченных ситуаций, количество кетоновых тел в крови возрастает при алкогольном отравлении и потреблении жирной пищи. При богатой жирами диете , особенно у детей, жирные кислоты не успевают включиться в состав ТАГ и ЛПОНП и частично переходят в митохондрии, что увеличивает синтез кетоновых тел. При алкогольном отравлении субстратом для синтеза кетонов является ацетил-SКоА, синтезируемый при обезвреживании этанола.
В обычных условиях синтез кетоновых тел также идет, хотя в гораздо меньшем количестве. Для этого используются как жирные кислоты, так и безазотистые остатки кетогенных и смешанных аминокислот.
Для детей раннего возраста характерна неустойчивость жирового обмена, связанная с недостаточностью регуляторного влияния ЦНС и эндокринной системы. Поэтому кетонемия и кетонурия у грудных детей наблюдается чаще, чем у взрослых.
Уровень ацетоацетата быстро нарастает между 12 и 24 часами жизни и сохраняется высоким первую неделю жизни, что свидетельствует об активной мобилизации жира из депо, высокой утилизации свободных жирных кислот в печени и малом использовании кетоновых тел в тканях.
У детей до 7 лет под влиянием различных стимулов (краткое голодание, инфекции, эмоциональное возбуждение) ускоряется синтез кетоновых тел и может легко возникать кетоацидоз, сопровождающийся неукротимой рвотой ("ацетонемическая рвота"). Причиной этого служит неустойчивость углеводного обмена и малые запасы гликогена у детей, что усиливает липолиз в адипоцитах, накопление жирных кислот в крови и, следовательно, кетогенез в печени.
Синтез кетоновых тел (кетогенез)
Синтез ацетоацетата происходит только в митохондриях печени, далее он либо восстанавливается до 3-гидроксибутирата, либо декарбоксилируется до ацетона. После синтеза все три соединения поступают в кровь и разносятся по тканям. Ацетон, как летучее вещество, легко удаляется с выдыхаемым воздухом и потом. Все кетоновые тела могут выделяться с мочой.
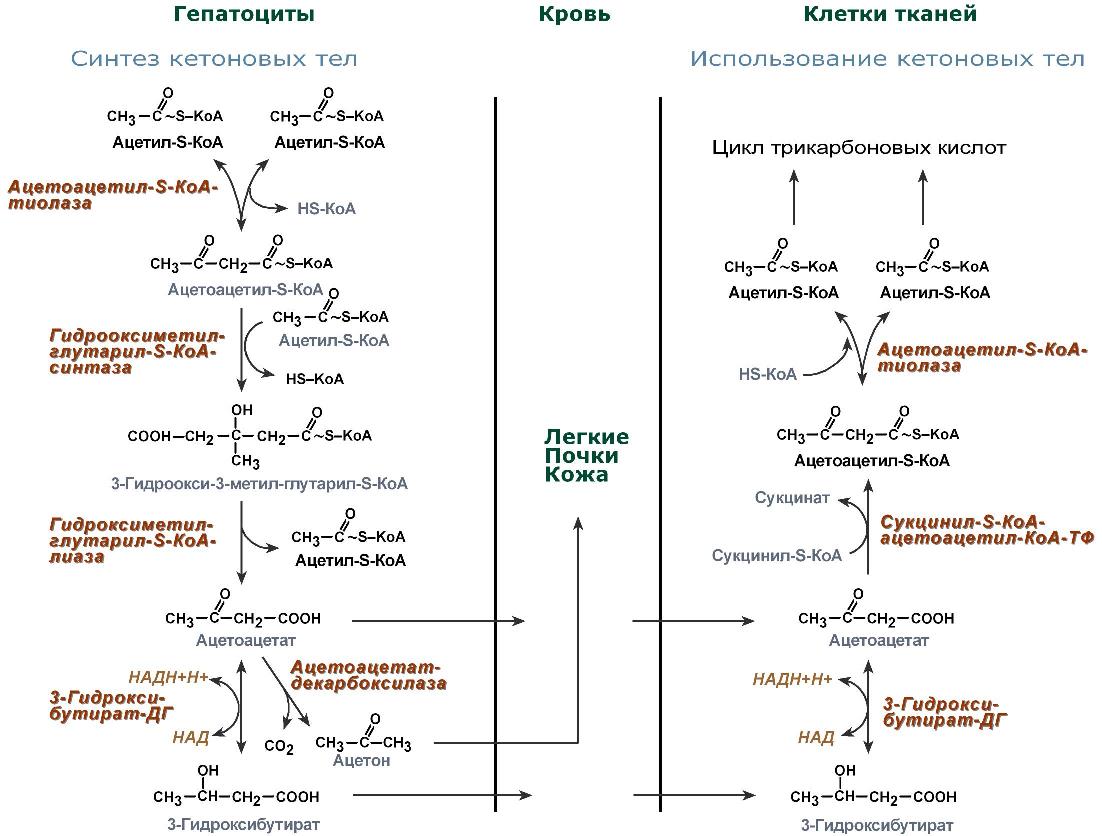
Реакции синтеза и утилизации кетоновых тел
Используются кетоновые тела клетками всех тканей, кроме печени и эритроцитов. Особенно активно, даже в норме, они потребляются миокардом и корковым слоем надпочечников.
В тканях реакции утилизации кетоновых тел в целом совпадают с обратным направлением реакций синтеза. В цитозоле клеток 3-гидроксибутират окисляется, образующийся ацетоацетат проникает в митохондрии, активируется за счет сукцинил-SКоА и превращается в ацетил-SКоА, который сгорает в ЦТК.
При голодании синтез кетоновых тел ускоряется в 60 раз (повышение в крови до 0,6 г/л при норме менее 0,01 г/л), при сахарном диабете I типа – в 400 (!) раз (до 4 г/л).
При сахарном диабете 1 типа (инсулинзависимом) в гепатоците глюкозы может быть много, т.к. глюкоза проникает в него через ГлюТ-2 без участия инсулина. Однако, точно также как при голодании, соотношение инсулин/глюкагон низкое, и оксалоацетат очень активно уходит на синтез глюкозы, что тормозит ЦТК и отправляет ацетил-SKoA на образование кетоновых тел.
При сахарном диабете 2 типа (инсулиннезависимом) инсулина достаточно и соотношение инсулин/глюкагон велико, поэтому глюконеогенез не активен и оксалоацетата хватает для поддержания ЦТК. Образуемый здесь ацетил-SKoA либо сгорает в ЦТК, либо используется для реакций синтеза холестерина и синтеза жирных кислот (которые стимулируются инсулином). К тому же при наличии инсулина попадающие в печень жирные кислоты будут не окисляться, а вовлекаться в синтез триацилглицеролов и ЛПОНП.
В здоровом организме ацетон в крови присутствует в крайне низких концентрациях, образуется в результате спонтанного декарбоксилирования ацетоацетата и, по-видимому, не имеет определенного физиологического значения.
Кетоновые тела образуются в печени. Прежние представления о том, что кетоновые тела являются промежуточными продуктами β-окисления жирных кислот, оказались ошибочными.
Во-первых, в обычных условиях промежуточными продуктами β-окис-ления жирных кислот являются КоА-эфиры этих кислот, например β-окси-бутирил-КоА, ацетоацетил-КоА.
Во-вторых, β-оксибутирил-КоА, образующийся в печени при β-окисле-нии жирных кислот, имеет L-конфигурацию, в то время как β-оксибутират, обнаруживаемый в крови, представляет собой D-изомер. Именно β-окси-бутират D-конфигурации образуется в ходе метаболического пути синтеза β-окси-β-метилглутарил-КоА (3-гидрокси-3-метилглутарил-КоА):
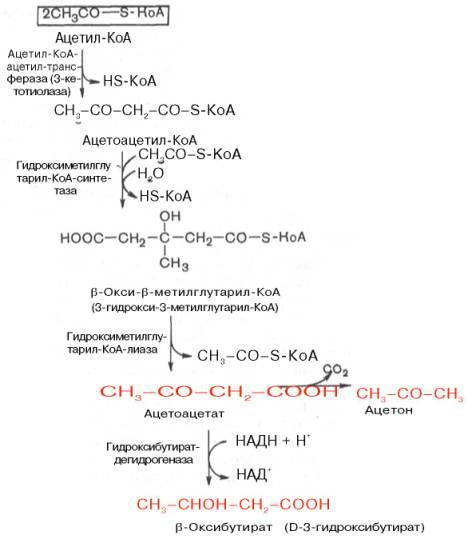
На первом этапе из 2 молекул ацетил-КоА образуется ацетоацетил-КоА. Реакция катализируется ферментом ацетил-КоА-ацетилтрансферазой (3-ке-тотиолазой). Затем ацетоацетил-КоА взаимодействует еще с одной молекулой ацетил-КоА. Реакция протекает под влиянием фермента гидро-ксиметилглутарил-КоА-синтетазы. Образовавшийся β-окси-β-метилглута-рил-КоА способен под действием гидроксиметилглутарил-КоА-лиазы расщепляться на ацетоацетат и ацетил-КоА.
Ацетоацетат восстанавливается при участии НАД-зависимой D-3-гид-роксибутиратдегидрогеназы, при этом образуется D-β-оксимасляная кислота (D-3-гидроксибутират). Следует подчеркнуть, что фермент специфичен по отношению к D-стереоизомеру и не действует на КоА-эфиры.
Существует второй путь синтеза кетоновых тел. Образовавшийся путем конденсации 2 молекул ацетил-КоА ацетоацетил-КоА способен отщеплять коэнзим А и превращаться в ацетоацетат. Этот процесс катализируется ферментом ацетоацетил-КоА-гидролазой (деацилазой):
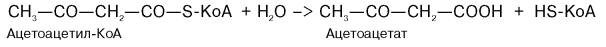
Однако второй путь образования ацетоуксусной кислоты (ацетоацетата) не имеет существенного значения, так как активность деацилазы в печени низкая.
В крови здорового человека кетоновые тела содержатся лишь в очень небольших концентрациях (в сыворотке крови 0,03–0,2 ммоль/л). При патологических состояниях (у лиц с тяжелой формой сахарного диабета, при голодании, а также у животных с экспериментальным острым стрептозотоциновым или аллоксановым диабетом) концентрация кетоновых тел в сыворотке крови увеличивается и может достигать 16–20 ммоль/л.
Как отмечалось, основным местом образования ацетоацетата и 3-гид-роксибутирата служит печень. Из митохондрий печени эти соединения диффундируют в кровь и переносятся к периферическим тканям.
Известно, что в периферических тканях 3-гидроксибутират (β-оксимас-ляная кислота) способен окисляться до ацетоацетата, а последний активируется с образованием соответствующего КоА-эфира (ацетоацетил-КоА). Ацетоацетат может быть активирован путем переноса КоА с сукцинил-КоА в реакции, катализируемой специфической КоА-трансферазой. Образовавшийся ацетоацетил-КоА далее расщепляется тиолазой с образованием 2 молекул ацетил-КоА, которые затем включаются в цикл Кребса:
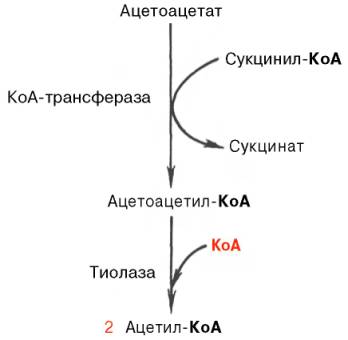
Не исключено, что существует и второй путь активации ацетоацетата – это использование АТФ и HS-KoA аналогично тому, как при активации жирных кислот:

Присутствие кетоновых тел в моче называется кетонурией. Это ненормальное явление, так как причиной присутствия кетонов в моче является, прежде всего, диабет типа 1. Другие причины включают голодание, чрезмерную физическую нагрузку, алкоголизм и крайне низкое потребление углеводов.
Достаточно высокая концентрация кетоновых тел в моче означает, что организм для получения энергии использует жиры, а не глюкозу.
Что такое кетоновые тела?
Это соединения, которые возникают в результате биохимических изменений в жирах. Кетоновые тела образуются в печени, откуда они попадают в кровь. У здорового человека норма кетоновых тел в крови не должна превышать 0,2 ммоль / л.

Механизм образования кетоновых тел
Глюкоза является основным энергетическим материалом для клеток, но при ее недостатке энергия поступает из жиров. В моче и крови человека присутствуют 3 кетоновых тела: B-гидрокси-масляная кислота, ацетоуксусная кислота, ацетон.
Кетоны в моче — обратите внимание
Состояние, при котором кетоновые тела присутствуют в моче, называется кетонурия. Если в моче обнаружены кетоновые тела, это означает, что организм использует жиры для получения энергии. Может быть много причин, вызывающих кетонурию, наряду с сопутствующими симптомами.
Симптомы возникают, когда организм не в состоянии утилизировать углеводы. что приводит к сжиганию жира у пациентов с диабетом. У пациентов без диабета причиной кетонурии может быть недостаток углеводов. Главное, определить причину кетонов в моче как можно скорее и начать соответствующее лечение. Значение имеет каждый день задержки.
Симптомы, которые могут сопровождать кетонурию
Если есть кетоны в моче или симптомы, которые могут быть связаны с наличием кетонов в моче, следует немедленно обратиться к эндокринологу. Симптомы появляются при уже прогрессирующей кетонурии.
Признаки, которые могут указывать на наличие кетоновых тел:
- характерный — фруктовый запах изо рта — за него отвечает ацетон, который присутствует в выдыхаемом воздухе (это наиболее характерный симптом кетонурии );
- высокий уровень глюкозы в крови, превышающий 300 мг / дл;
- изменился цвет кожи, покраснение или наоборот — бледный цвет;
- желудочно-кишечные симптомы — диарея, рвота, боль в животе;
- частые инфекции;
- хроническая усталость;
- сухость во рту и усиление жажды;
- полиурия.
Исследование мочевых кетоновых тел
Кетоновые тела могут быть обнаружены с помощью стрип-тестирования анализа мочи. Сдавать нужно утреннюю мочу среднего потока, когда первая порция мочи поступает в туалет, средняя часть — в специально подготовленный стерильный контейнер, а последняя — снова в туалет.

Тестирование анализа мочи
Прежде чем собирать мочу, нужно помыться. В течение периода, предшествующего общему анализу мочи, не меняйте свою диету и не выполняйте слишком много упражнений.
Нормальный результат теста тела мочи на кетоны отрицательный. Если в моче обнаруживаются кетоновые тела, лечение должно быть начато немедленно.
Причины кетоновых тел в моче
- Диабет, чаще всего диабет 1 типа . Тело диабетика не справляется с сжиганием углеводов. Причина этого — дефицит инсулина, связи с чем жировые запасы мобилизуются для получения энергии. В результате этих изменений образуются кетоновые тела. Избыток кетонов накапливается в крови, и это состояние называется кетонемией. Организм, страдающий диабетом, желая избавиться от лишних кетонов, выделяет их вместе с мочой, а также с выдыхаемым воздухом. Чаще всего кетоновые тела в моче сопровождаются гипергликемией , то есть высоким уровнем глюкозы в крови, а также наличием глюкозы в моче (глюкозурия). Избыток кетоновых тел в организме приводит к развитию кетоацидоза. Это опасное для жизни состояние. Факторы, предрасполагающие к кетоацидозу, включают: неправильное использование инсулина, внезапное прекращение инсулиновой терапии, хронические инфекции, опасные для жизни состояния: инсульт, инфаркт, панкреатит.
- Низкоуглеводная диета . При длительном голодании кетоновые тела образуются в процессе чрезмерного B-окисления жиров.
- Хронический алкоголизм.
- Другие причины — временно в случае сильной рвоты, хронической лихорадки, чрезмерных физических нагрузок.
Определив причину присутствия кетоновых тел в моче, врач начнет соответствующее лечение.
Кетоны в моче — норма ацетона в моче и интерпретация результата
Нормой кетонов в моче является отсутствие кетоновых тел. Любой положительный результат (кет в моче положительный) означает проблему в организме и требует дальнейшей диагностики. Следы кетонов в моче или их низкие уровни, например кетоны в моче 5 или кетоны в моче 15 мг / дл, могут указывать на:
- интенсивные физические усилия;
- недостаток калорий в рационе;
- рвоту;
- лихорадку;
- ожоги;
- потребление алкоголя.


Чаще всего умеренная кетонурия возникает без симптомов, которые могут указывать на диабет или кетоацидоз.
Слишком высокое содержание кетонов в моче, т. е. результат теста, указывающий на содержание кетонов в моче 50 мг/дл и более, может говорить о более серьезных нарушениях здоровья, таких как заболевания с тяжелым истощающим течением, заболевания щитовидной железы или почечная глюкозурия. Высокие кетоны в моче также сопровождают декомпенсированный или недиагностированный и нелеченный диабет.
Кетоны в моче ребенка — причины
Ацетон в моче у детей чаще всего сопровождается рвотой или лихорадкой. Иногда это признак недоедания или недостаточности надпочечников — тогда высокий уровень кетоновых тел у детей в моче сопровождается гипогликемией, то есть низким уровнем глюкозы в крови. Напротив, кетоны в моче при низком уровне глюкозы при увеличении печени могут указывать на наличие гликогеноза.
Кетоновые тела и глюкоза в моче ребенка могут указывать на диабет; В молодом возрасте наиболее распространен диабет типа 1. Для определения наличия кетонов у ребенка необходимо сначала определить уровень глюкозы в крови натощак. Дальнейшая диагностика зависит от результата глюкозы.
Кетоновые тела в моче во время беременности — что они показывают?
Кетоны в моче во время беременности не редкость. Женщины, которые страдают от частой рвоты в первом триместре беременности, показывают наличие кетонов очень часто. Кроме того, привести к увеличению кетоновых тел в крови и моче может отсутствие аппетита при беременности или пропуск вечернего приема пищи за день до анализов мочи.
Так как высокое содержание ацетона в моче беременной женщины может указывать на гестационный диабет, состояние всегда требует дальнейшей диагностики. Тогда помимо кетонов в моче беременной женщины также может наблюдаться глюкоза, кроме того, могут быть симптомы кетоацидоза.
Следы кетонов в моче — лечение
Кетонурия — это не болезнь, а симптом болезни, поэтому ее невозможно вылечить. Чтобы восстановить уровень кетонов в моче до нормы, необходимо устранить или вылечить основное заболевание. Необходимо компенсировать нарушения кислотно-основного и водно-электролитного обмена. Это особенно важно в случае диабета, осложнением которого может быть кетоновая кома.
Чтобы избавиться от кетонов в моче при диабете, необходимо нормализовать уровень глюкозы и инсулина в крови. В случае кетонурии, вызванной недоеданием, необходимо изменить рацион питания на высококалорийный и обеспечить адекватный калорийный баланс. Во время рвоты назначаются противорвотные препараты.
cetogénesis это процесс, с помощью которого получают ацетоацетат, β-гидроксибутират и ацетон, которые вместе называют кетоновыми телами. Этот сложный и тонко регулируемый механизм осуществляется в митохондриях, от катаболизма жирных кислот.
Получение кетоновых тел происходит, когда организм подвергается истощающим периодам голодания. Хотя эти метаболиты синтезируются в основном в клетках печени, они обнаруживаются в качестве важного источника энергии в различных тканях, таких как скелетные мышцы и ткани сердца и головного мозга..

Hydro-гидроксибутират и ацетоацетат являются метаболитами, используемыми в качестве субстратов в сердечной мышце и коре почек. В мозгу кетоновые тела становятся важными источниками энергии, когда организм исчерпал свой запас глюкозы.
- 1 Общая характеристика
- 2 Типы и свойства кетоновых тел
- 3 Синтез кетоновых тел
- 3.1 Условия для кетогенеза
- 3.2 Механизм
- 3.3 β-окисление и кетогенез связаны между собой
- 3.4 Регуляция β-окисления и его влияние на кетогенез
- 5.1 Сахарный диабет и накопление кетоновых тел
Общие характеристики
Кетогенез считается очень важной физиологической функцией или метаболическим путем. Как правило, этот механизм осуществляется в печени, хотя было показано, что он может осуществляться в других тканях, способных метаболизировать жирные кислоты..
Образование кетоновых тел является основным метаболическим производным ацетил-КоА. Этот метаболит получают из метаболического пути, известного как β-окисление, которое является разложением жирных кислот.
Наличие глюкозы в тканях, где происходит β-окисление, определяет метаболическую судьбу ацетил-КоА. В особых ситуациях окисленные жирные кислоты почти полностью направляются на синтез кетоновых тел..
Типы и свойства кетоновых тел
Основным кетоновым телом является ацетоацетат или ацетоуксусная кислота, которая синтезируется главным образом в клетках печени. Другие молекулы, которые составляют кетоновые тела, происходят из ацетоацетата.
Восстановление ацетоуксусной кислоты приводит к образованию D-β-гидроксибутирата, второго кетонового тела. Ацетон представляет собой соединение, которое трудно разлагать, и он образуется в результате спонтанной реакции декарбоксилирования ацетоацетата (поэтому он не требует вмешательства какого-либо фермента), когда он присутствует в высоких концентрациях в крови.
Обозначение кетоновых тел было принято условно, поскольку, строго говоря, β-гидроксибутират не имеет кетонной функции. Эти три молекулы растворимы в воде, что облегчает их транспорт в крови. Его основная функция заключается в обеспечении энергией определенных тканей, таких как скелетные и сердечные мышцы..
Ферменты, участвующие в образовании кетоновых тел, в основном находятся в клетках печени и почек, что объясняет, почему эти два места являются основными продуцентами этих метаболитов. Его синтез происходит только и исключительно в митохондриальном матриксе клеток..
Как только эти молекулы синтезируются, они попадают в кровоток и попадают в ткани, которые в них нуждаются, где они разлагаются до ацетил-КоА..
Синтез кетоновых тел
Условия для кетогенеза
Метаболическая судьба ацетил-КоА от β-окисления зависит от метаболических потребностей организма. Это окисляется до СО2 и H2Или через цикл лимонной кислоты или синтез жирных кислот, если метаболизм липидов и углеводов в организме стабилен.
Когда организму требуется образование углеводов, оксалоацетат используется для производства глюкозы (глюконеогенез) вместо запуска цикла лимонной кислоты. Это происходит, как уже упоминалось, когда организм имеет некоторую неспособность получить глюкозу в таких случаях, как длительное голодание или наличие диабета..
В связи с этим ацетил-КоА, полученный в результате окисления жирных кислот, используется для производства кетоновых тел..
механизм
Процесс кетогенеза начинается с продуктов β-окисления: ацетацетил-КоА или ацетил-КоА. Когда субстратом является ацетил-КоА, на первом этапе происходит конденсация двух молекул, реакция, катализируемая ацетил-КоА-трансферазой, с образованием ацетацетил-КоА.
Ацетацетил-КоА конденсируется с третьим ацетил-КоА под действием синтазы ГМГ-КоА с образованием ГМГ-КоА (β-гидрокси-β-метилглутарил-КоА). HMG-CoA разлагается до ацетоацетата и ацетил-КоА под действием лиазы HMG-CoA. Таким образом получается первое кетоновое тело..
Ацетоацетат восстанавливается до β-гидроксибутирата путем вмешательства β-гидроксибутиратдегидрогеназы. Эта реакция зависит от НАДН.
Основным ацетоацетатным кетоновым телом является β-кетокислота, которая подвергается неферментативному декарбоксилированию. Этот процесс прост и производит ацетон и СО2.
Таким образом, эта серия реакций приводит к образованию кетоновых тел. Они, будучи растворимыми в воде, могут легко транспортироваться через кровоток без необходимости прикрепления к структуре альбумина, как в случае жирных кислот, которые нерастворимы в водной среде..
Β-окисление и кетогенез связаны между собой
Метаболизм жирных кислот производит субстраты для кетогенеза, поэтому эти два пути функционально связаны.
Ацетоацетил-КоА является ингибитором метаболизма жирных кислот, поскольку он останавливает активность ацил-КоА-дегидрогеназы, которая является первым ферментом β-окисления. Кроме того, он также оказывает ингибирование на ацетил-КоА-трансферазу и синтазу HMG-КоА..
Фермент синтаза HMG-CoA, подчиненный СРТ-I (фермент, участвующий в производстве ацилкарнитина при β-окислении), представляет важную регуляторную роль в образовании жирных кислот.
Регуляция β-окисления и его влияние на кетогенез
Питание организмов регулирует сложный набор гормональных сигналов. Углеводы, аминокислоты и липиды, потребляемые в рационе, откладываются в форме триацилглицеринов в жировой ткани. Инсулин, анаболический гормон, участвует в синтезе липидов и образовании триацилглицеринов.
На уровне митохондрий β-окисление контролируется поступлением и участием некоторых субстратов в митохондриях. Фермент CPT I синтезирует ацилкарнитин из цитозольного ацил-КоА.
Когда организм питается, активируется ацетил-КоА-карбоксилаза, и цитрат повышает уровень СРТ I, а его фосфорилирование уменьшается (циклическая АМФ-зависимая реакция).
Это вызывает накопление малонил-КоА, который стимулирует синтез жирных кислот и блокирует их окисление, предотвращая образование бесполезного цикла..
В случае голодания активность карбоксилазы очень низка, так как уровни фермента СРТ I были снижены, и он был фосфорилирован, активируя и стимулируя окисление липидов, что впоследствии позволит образованию кетоновых тел через ацетил-КоА.
деградация
Кетоновые тела диффундируют из клеток, где они синтезируются и транспортируются кровью в периферические ткани. В этих тканях они могут окисляться через цикл трикарбоновых кислот.
В периферических тканях β-гидроксибутират окисляется до ацетоацетата. Впоследствии настоящий ацетоацетат активируется ферментом 3-кетоацил-КоА-трансферазой.
Сукцинил-КоА действует как донор КоА, становясь сукцинатом. Активация ацетоацетата происходит, чтобы предотвратить превращение сукцинил-КоА в сукцинат в цикле лимонной кислоты при сопряженном синтезе ГТФ под действием сукцинил-КоА-синтазы..
Полученный ацетоацетил-КоА подвергается тиолитическому расщеплению с образованием двух молекул ацетил-КоА, которые включаются в цикл трикарбоновых кислот, более известный как цикл Кребса..
В клетках печени отсутствует 3-кетоацил-КоА-трансфераза, предотвращающая активацию этого метаболита в этих клетках. Таким образом, гарантируется, что кетоновые тела не окисляются в клетках, где они были произведены, но что они могут переноситься в ткани, где требуется их активность..
Медицинская значимость кетоновых тел
В организме человека высокие концентрации кетоновых тел в крови могут вызывать особые состояния, называемые ацидозом и кетонемией..
Производство этих метаболитов соответствует катаболизму жирных кислот и углеводов. Одной из наиболее распространенных причин патологического состояния кетогенеза является высокая концентрация фрагментов дикарбоната уксусной кислоты, которые не разлагаются путем окисления трикарбоновых кислот..
Вследствие этого наблюдается повышение уровня кетоновых тел в крови выше 2-4 мг / 100 Н и их присутствие в моче. Это приводит к нарушению промежуточного метаболизма указанных метаболитов..
Определенные дефекты нейрогландулярных факторов гипофиза, которые регулируют деградацию и синтез кетоновых тел, наряду с нарушениями метаболизма углеводородов, являются причиной состояния гиперцетонемии..
Сахарный диабет и накопление кетоновых тел
Сахарный диабет (тип 1) является эндокринным заболеванием, вызывающим увеличение выработки кетоновых тел. Недостаточное производство инсулина препятствует транспорту глюкозы в мышцы, печень и жировую ткань, накапливаясь в крови.
Клетки в отсутствие глюкозы начинают процесс глюконеогенеза и распада жиров и белков для восстановления их метаболизма. Как следствие, концентрация оксалоацетата снижается, а окисление липидов увеличивается..
Затем происходит накопление ацетил-КоА, которое в отсутствие оксалоацетата не может следовать по пути лимонной кислоты, вызывая высокую выработку кетоновых тел, характерных для этого заболевания..
Накопление ацетона определяется его присутствием в моче и дыхании людей, которые имеют это состояние, и на самом деле является одним из симптомов, которые указывают на проявление этого заболевания.
Читайте также:

