Инвазивные процедуры это кратко
Обновлено: 02.07.2024
Каждый пациент на приёме у врача больше всего боится, что у него заподозрят или, что хуже, найдут новообразование. Однако мало кто знает о механизме развития опухоли и за счет чего конкретно данный диагноз является настолько страшным. В этой статье мы разберёмся, что именно делает онкологические заболевания такими опасными для жизни.
Строение тканей с точки зрения формирования опухолевого процесса
Чтобы разобраться в механизме образования и развития опухоли, необходимо иметь представление о принципе строения тканей в организме. Большинство тканей, независимо от места их расположения, имеют сходный план строения:
- Базальная мембрана — это неклеточная структура, отграничивающая ткани друг от друга;
- Ростковый слой — группа активно делящихся клеток, расположенных на базальной мембране, которые обеспечивают обновление ткани. Именно изменение генетического материала клеток росткового слоя влечёт за собой развития опухоли;
- Слой созревающих клеток — клетки ростового слоя, которые постепенно продвигаются в верхние слои в процессе дифференцировки (приобретения формы и свойств, характерных для данной ткани);
- Поверхностный слой — группа клеток, которая и обеспечивает выполнение тканью определённой функции.
Между ростковым и поверхностным могут располагаться дополнительные слои в зависимости от конкретного вида ткани. Но принцип строения всегда один и тот же: клетки, способные делиться, находятся на базальной мембране. В процессе созревания они перемещаются в верхние слои, утрачивая способность к делению и приобретая специфические свойства.
Доброкачественные и злокачественные опухоли: в чем разница?
Исходя из того, клетки какого слоя подверглись мутации, выделяют два типа неоплазий — доброкачественные и злокачественные. Их отличия заключаются в том, что первый тип формируется из высоко дифференцированных клеток созревающего слоя. При доброкачественных опухолях клетки не будут сильно отличаться от здоровых клеток данной ткани. Такая неоплазия считается неагрессивной и растет медленно, а также не даёт метастазы. Патогенное действие доброкачественного новообразования заключается главным образом в сдавлении окружающих её тканей. Иногда такие опухоли полностью или частично закрывают просвет какого-либо полого органа.
В процессе развития рака выделяют 4 стадии:

Что такое инвазия опухоли?
Инвазия обуславливает способность опухолей давать метастазы — вторичные очаги онкологического процесса вдали от материнской опухоли, возникшие из-за миграции раковых клеток. Обязательное условие метастазирования — наличие у опухоли собственной капиллярной сети. Она формируется, когда количество неопластических клеток достигает 103 (1-2 мм).
- Разрыв межклеточных связей, соединяющих раковые клетки между собой;
- Прикрепление клеток опухоли к базальной мембране;
- Разрушение базальной мембраны лизирующими (расщепляющими) ферментами;
- Миграция клеток в соседние ткани и органы.
Раковые клетки, находящиеся в процессе инвазии, более устойчивы к облучению и химеотерапии, чем стационарные. Во многом это связано с временной утратой мигрирующими клетками способности к делению. Также движущиеся опухолевые клетки проявляют повышенную активность антиапоптотических генов (гены, препятствующие запрограммированной смерти клетки — апоптозу). И, поскольку химиотерапевтические препараты направлены на стимуляцию апопоза, их устойчивость к лечению возрастает.
Факторы, определяющие степень инвазивности опухоли
Чтобы злокачественная опухоль проросла сквозь базальную мембрану, необходимо наличие следующих факторов:
- Быстрое деление и давление. Механическое воздействие опухолевой массы на базальную мембрану способствует её разрушению и, как следствие, инвазии раковых клеток;
- Подвижность клеток. Клетки новообразования способны к миграции, причем их движение не является хаотичным. Они движутся в направлении большей концентрации кислорода, питательных веществ, а также в сторону более нейтрального показателя кислотности (рН);
- Межклеточные связи. Чем прочнее эти контакты, тем меньше шансов, что опухоль начнет инвазивный рост. У злокачественных клеток связи слабые, поэтому клетки легко отрываются от новообразования и попадают в кровоток или в лимфатическую систему;
- Действие лизосомальных ферментов. Злокачественная опухоль вырабатывает вещества, способные разрушать здоровые клетки и межклеточное вещество, что будет способствовать инвазии;
- Иммунная система человека. В организме существует собственная противоопухолевая защита, которую обеспечивает наш иммунитет. Её активность у каждого человека индивидуальна. Она зависит от генетической предрасположенности и состояния всего организма в конкретный момент. Так, при заболеваниях, сопровождающихся угнетением иммунной системы (например, при ВИЧ), пациенты могут погибать от онкологических заболеваний, возникших из-за отсутствия противоопухолевой активности.
Инвазия раковых клеток в сосуды
Вслед за прорастанием в базальную мембрану наступает интравазальная (внутрисосудистая) инвазия опухоли. Чаще раковые клетки мигрируют в артерии. Это связано с тем, что стенки артерий более упругие и эластичные, в то время как у вен они тонкие и легко спадаются в опухолях. Однако раковые клетки могут быть занесены в вены из лимфатических сосудов.
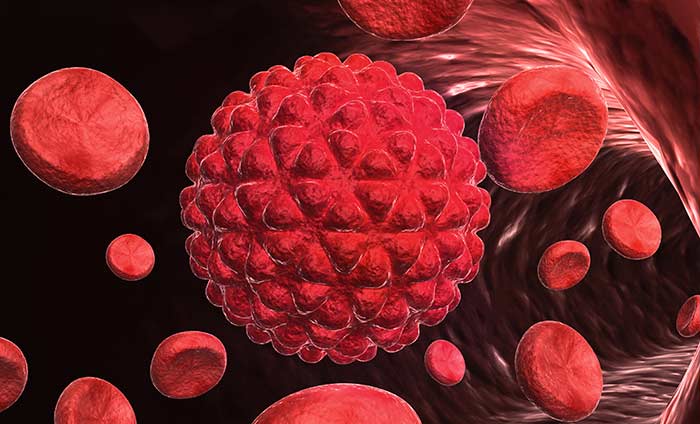
Циркуляция раковых клеток в системе кровотока и экстравазация
Экстарвазация представляет собой выход опухолевых клеток из сосудов для формирования метастатического очага. В этом процессе задействованы те же ферменты, что и в инвазии через базальную мембрану.

Пренатальная (дородовая) диагностика позволяет исключить большую часть врожденных и наследственных патологий плода на этапе внутриутробного развития.
К инвазивным методам относятся:
хорионбиопсия — получение клеток, формирующих плаценту (срок беременности — 10 – 14 недель);
плацентобиопсия — получение клеток плаценты (срок беременности — 14 – 20 недель);
амниоцентез — пункция околоплодного пузыря с забором небольшого количества околоплодных вод (срок беременности — 15 – 18 недель);
фетоскопия — введение зонда и осмотр плода (проводится на 18 – 19-й неделе беременности);
кордоцентез — забор крови из пуповины плода (срок беременности — с 20-й недели).
В редких случаях проводят биопсию тканей плода.
1) Хорионбиопсия — инвазивная процедура, заключающаяся в получении ворсин хориона для последующего исследования в целях диагностики врожденных и наследственных заболеваний плода. Осложнения — кровянистые выделения из половых путей после проведения трансцервикальной хорионбиопсии — встречаются у каждой третьей пациентки. Как правило, они прекращаются самостоятельно, не влияя на исход беременности. В 4 % случаев после биопсии может формироваться ретрохориальная гематома, которая обычно рассасывается до 16-й недели беременности. При трансабдоминальном доступе кровотечение из половых путей после операции встречается в единичных случаях.
Возможны и инфекционные осложнения.
2) Плацентоцентез — получение образца ткани плаценты путем пункции матки через переднюю брюшную стенку. Эта ткань в основном имеет ту же генетическую структуру, что и плод, поэтому пригодна для проведения генетической диагностики. По основным клиническим и техническим аспектам плацентоцентез схож с биопсией хориона.
3) Амниоцентез — это инвазивная процедура, заключающаяся в пункции амниотической оболочки с целью получения околоплодных вод для последующего лабораторного исследования. Амниоцентез можно выполнять в первом, втором и третьем триместрах беременности (оптимально — на 16 – 20-й неделе).
•преждевременное излитие околоплодных вод;
•возможно кратковременное подтекание небольшого количества ОВ на протяжении первых суток после операции (в 1 – 2 % случаев);
•отслойка плодных оболочек;
•инфицирование (наиболее неблагоприятен в этом отношении второй триместр беременности вследствие низкого уровня антибактериальной активности околоплодных вод).
4) Фетоскопия относительно опасна, так как может спровоцировать выкидыш. Поэтому она не имеет широкого применения и проводится только в крайних случаях.
5) Кордоцентез — это инвазивная процедура, в ходе которой производят пункцию сосудов пуповины с целью получения крови для лабораторных исследований.
Совокупный риск развития осложнений не превышает 5 %. Среди них:
•кровотечение из области пункции пуповины — наиболее частое осложнение кордоцентеза, возникает в 50 % случаев (при этом его риск увеличивается при пункции артерий), продолжается в среднем не более минуты. Для снижения частоты постпункционных кровотечений предпочтительно использовать иглы меньшего диаметра;
•нарушение функционального состояния плода — довольно частое осложнение;
•прерывание беременности — наблюдают в среднем в 1,4 % случаев;
•гематома пуповины, может формироваться в области пункции. Гематомы малых размеров (в среднем в 17 % случаев), как правило, не влияют на показатели функционального состояния плода. Большие встречаются редко, могут образовываться после пункции артерий, чаще на фоне нарушений коагуляции;
При условии соблюдения всех норм и правил проведения инвазивной диагностики основной риск перечисленных процедур — это угроза выкидыша. В количественном отношении он равен 2 – 3 %. Но эти показатели не выше, чем у остальных беременных. Между тем получаемый результат чрезвычайно важен для прогноза здоровья будущего ребенка, ведь эти методы диагностики являются наиболее точными.
Виды инвазивных методов в пренатальной диагностике пороков развития.
Инвазивные диагностические методы (ИДМ) — это пункции плаценты (хориона), пуповины или амниотической полости, которые проводятся с целью получения биологического материала для дальнейших исследований (цитогенетических, молекулярных, биохимических и т.д.).
Лечебные инвазивные методы - это операции с целью пренатальной коррекции некоторых пороков развития плода, а также вмешательства, направленные на лечение некоторых заболеваний плода (например, анемии). В этой главе мы не будем рассматривать вопросы, касающиеся лечения патологии в дородовом периоде. Пренатальная хирургия в настоящее время уже выделилась в самостоятельную область медицины, хотя до сих пор во всем мире является уделом лишь высоко специализированных клиник. Печально констатировать тот факт, что в России в настоящее время пренатальная хирургия практически отсутствует. Мизерный опыт отдельных диагностических центров еще не обобщен, поэтому разговор о лечебных инвазивных вмешательствах на страницах этой книги стал бы преждевременным.

Существует множество классификаций инвазивных диагностических методов:
1) по характеру доступа: трансабдоминальные, трансцервикальные;
2) по виду получаемого материала: ворсины хориона (плаценты), кровь плода, амниотическая жидкость;
3) по характеру контроля за процедурой: ультразвуковой, эндоскопический;
4) по технике проведения вмешательства: путем аспирации, путем биопсии;
5) по основной задаче исследования: получение материала для исследования, визуальная оценка структур плода.
Сегодня в практическом здравоохранении с диагностической целью наиболее часто применяются трансабдоминальная аспирация ворсин хориона, плацентоцентез, амниоцентез и кордоцентез. Все инвазивные вмешательства проводятся под ультразвуковым контролем. В зарубежных странах в учреждениях первого уровня используются, как правило, технически более простые методы (амниоцентез. реже, аспирация ворсин хориона), а полный спектр ИДМ применяется в крупных госпиталях и университетских клиниках, т. е. в диагностических центрах второго и третьего уровней.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

К искусственной вентиляции легких (ИВЛ) прибегают для оказания помощи пациентам с острой или хронической дыхательной недостаточностью, когда больной не может самостоятельно вдыхать необходимый для полноценного функционирования организма объем кислорода и выдыхать углекислый газ. Необходимость в ИВЛ возникает при отсутствии естественного дыхания или при его серьезных нарушениях, а также во время хирургических операций под общим наркозом.
Что такое ИВЛ?
Искусственная вентиляция в общем виде представляет собой вдувание газовой смеси в легкие пациента. Процедуру можно проводить вручную, обеспечивая пассивный вдох и выдох путем ритмичных сжиманий и разжиманий легких или с помощью реанимационного мешка типа Амбу. Более распространенной формой респираторной поддержки является аппаратная ИВЛ, при которой доставка кислорода в легкие осуществляется с помощью специального медицинского оборудования.
Показания к искусственной вентиляции легких
Искусственная вентиляция легких проводится при острой или хронической дыхательной недостаточности, вызванной следующими заболеваниями или состояниями:
- хроническая обструктивная болезнь легких (ХОБЛ);
- муковисцидоз;
- пневмония;
- кардиогенный отек легких;
- рестриктивные патологии легких;
- боковой амиотрофический синдром;
- синдром ожирения-гиповентиляции;
- кифосколиоз;
- травмы грудной клетки;
- дыхательная недостаточность в послеоперационный период;
- дыхательные расстройства во время сна и т. д.
Инвазивная вентиляция легких
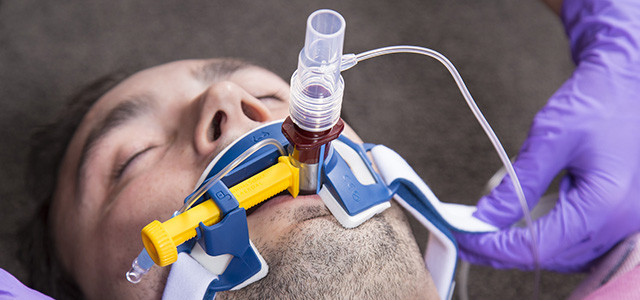
Эндотрахеальная трубка вводится в трахею через рот или через нос и подсоединяется к аппарату ИВЛ
При инвазивной респираторной поддержке аппарат ИВЛ обеспечивает принудительную прокачку легких кислородом и полностью берет на себя функцию дыхания. Газовая смесь подается через эндотрахеальную трубку, помещенную в трахею через рот или нос. В особо критических случаях проводится трахеостомия – хирургическая операция по рассечению передней стенки трахеи для введения трахеостомической трубки непосредственно в ее просвет.
Инвазивная вентиляция обладает высокой эффективностью, но применяется лишь случае невозможности помочь больному более щадящим способом, т.е. без инвазивного вмешательства.
Кому и когда необходима инвазивная ИВЛ?
Подключенный к аппарату ИВЛ человек не может ни говорить, ни принимать пищу. Интубация доставляет не только неудобства, но и болезненные ощущения. Ввиду этого пациента, как правило, вводят в медикаментозную кому. Процедура проводится только в условиях стационара под наблюдением специалистов.
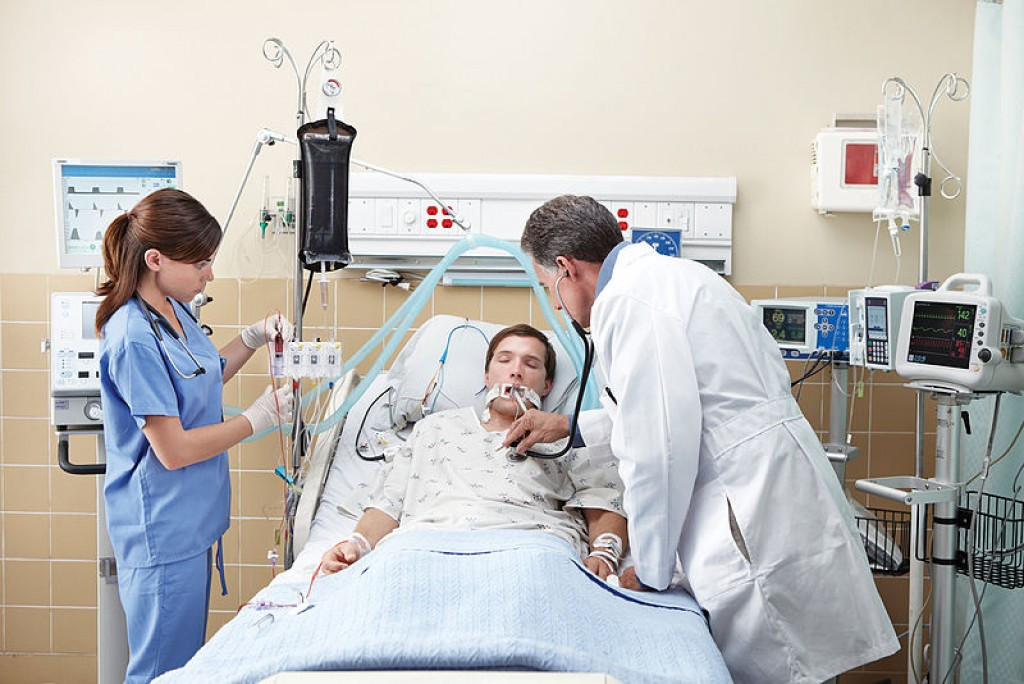
Инвазивная вентиляция легких отличается высокой эффективностью, однако интубация предполагает введение пациента в медикаментозную кому. Кроме того, процедура сопряжена с рисками.
Традиционно инвазивную респираторную поддержку применяют в следующих случаях:
- отсутствие эффекта или непереносимость НИВЛ у пациента;
- повышенное слюнотечение или образование чрезмерного количества мокроты;
- экстренная госпитализация и необходимость немедленной интубации;
- состояние комы или нарушение сознания;
- вероятность остановки дыхания;
- наличие травмы и/или ожогов лица.
Как работает аппарат инвазивной ИВЛ?
Принцип работы приборов для инвазивной ИВЛ можно описать следующим образом.
- Для краткосрочной ИВЛ эндотрахеальная трубка вводится в трахею больного через рот или нос. Для долгосрочной ИВЛ на шее пациента делается разрез, рассекается передняя стенка трахеи и непосредственно в ее просвет помещается трахеостомическая трубка.
- Через трубку в легкие подается дыхательная смесь. Риск утечки воздуха сведен к минимуму, поэтому больной гарантированно получает нужное количество кислорода.
- Состояние больного можно контролировать с помощью мониторов, на которых отображаются параметры дыхания, объем подаваемой воздушной смеси, сатурация, сердечная деятельность и др. данные.
Особенности оборудования для инвазивной вентиляции
Оборудование для инвазивной вентиляции легких имеет ряд характерных особенностей.
- Полностью берет на себя функцию дыхания, т.е. фактически дышит вместо пациента.
- Нуждается в регулярной проверке исправности всех клапанов, т.к. от работоспособности системы зависит жизнь больного.
- Процедура должна контролироваться врачом. Отлучение пациента от аппарата ИВЛ также предполагает участие специалиста.
- Используется с дополнительными аксессуарами – увлажнителями, откашливателями, запасными контурами, отсосами и т. д.
Неинвазивная вентиляция легких
За последние два десятилетия заметно возросло использование оборудования неинвазивной искусственной вентиляции легких. НИВЛ стала общепризнанным и широко распространенным инструментом терапии острой и хронической дыхательной недостаточности как в лечебном учреждении, так и в домашних условиях.
Одним из ведущих производителей медицинских респираторных устройств является австралийская компания ResMed
НИВЛ — что это?
Неинвазивная вентиляция легких относится к искусственной респираторной поддержке без инвазивного доступа (т.е. без эндотрахеальной или трахеостомической трубки) с использованием различных известных вспомогательных режимов вентиляции.
Оборудование подает воздух в интерфейс пациента через дыхательный контур. Для обеспечения НИВЛ используются различные интерфейсы – носовая или рото-носовая маска, шлем, мундштук. В отличие от инвазивного метода, человек продолжает дышать самостоятельно, но получает аппаратную поддержку на вдохе.
Когда применяется неинвазивная вентиляция легких?
Ключом к успешному использованию неинвазивной вентиляции легких является признание ее возможностей и ограничений, а также тщательный отбор пациентов (уточнение диагноза и оценка состояния больного). Показаниями для НИВЛ являются следующие критерии:
- одышка в состоянии покоя;
- частота дыхания ЧД>25, участие в респираторном процессе вспомогательной дыхательной мускулатуры;
- гиперкапния (PaC02>45 и его стремительное нарастание);
- уровень Ph
Читайте также:

