Иммуноглобулины история открытия кратко
Обновлено: 18.05.2024
Все началось в далеком 19 веке. В 1890 г. Э. Беринг и С. Китасато установили, что сыворотки кроликов, которым вводили дифтерийный токсин, приобретали способность нейтрализовать этот токсин и оказывать лечебное действие при дифтерийной инфекции. Так были открыты антитела.
Примерно в это же время, в конце 19 века, Пауль Эрлих установил, что антитела, отвечающие за иммунные реакции, имеют на своей поверхности специальные рецепторы, с помощью которых они прикрепляются к чужеродному объекту и связывают его. Он установил присутствие в плазме крови особых белков, способных нейтрализовать микробные тела (отсюда название – антитела, т.е. факторы против микробных тел). За обоснование гуморальной теории иммунитета П. Эрлих получил Нобелевскую премию в 1908 году.
В 1952 году О. Брутон впервые в мире описал клинический случай агаммаглобулинемии у людей (болезни отсутствия антител) и успешно апробировал заместительную терапию γ-глобулином, полученным из сыворотки крови здоровых доноров.
В дальнейшем Нельс Эрне, Цезарь Мильштейн и Георг Келлер обосновали теорию идиотипической цепи (идиотип – участок антитела, ответственный за специфическое взаимодействие с антигеном), а также разработали методику получения гибридом, что позволило синтезировать моноклональные антитела к разнообразным молекулам. С тех пор моноклональные иммуноглобулины с успехом используются для диагностики и лечения многих болезней человека. За эти открытия учёные получили Нобелевскую премию в 1984 году.
Исследователь Сусуми Тонегава открыл механизм формирования неограниченного разнообразия антител, который получил название реаранжировки генов иммуноглобулинов. Стало ясно, что человеческий организм приспосабливается к условиям окружающей среды не только фенотипически, но и на генотипическом уровне. Молекулярной основой такой адаптации является пожизненное формирование новых генов антигенс-вязывающих сайтов иммуноглобулинов путём запуска процессов рекомбинативной изменчивости. В 1987 году С. Тонегава удостоен Нобелевской премии по физиологии и медицине.
Не сложно заметить, что за работы в области изучения антител уже получены 4 Нобелевские премии. Данный случай - уникальный прецедент в работе Нобелевского комитета, поскольку такому количеству наград не удостаивались открытия ни по одной другой теме физиологии и медицины. Это указывает на чрезвычайную важную роль иммуноглобулинов в иммунных процесса.
Антитела (иммуноглобулины, ИГ, Ig) — белковые соединения плазмы крови, образующиеся в ответ на введение в организм человека или теплокровных животных бактерий, вирусов, белковых токсинов и других антигенов. Связываясь активными участками (центрами) с бактериями или вирусами, антитела препятствуют их размножению или нейтрализуют выделяемые ими токсические вещества.
Антитела являются особым классом гликопротеинов, имеющихся на поверхности B-лимфоцитов в виде мембраносвязанных рецепторов и в сыворотке крови. Антитела являются важнейшим фактором специфического гуморального иммунитета. Антитела используются иммунной системой для идентификации и нейтрализации чужеродных объектов — например, бактерий и вирусов.
Антитела выполняют две функции:
- антигенсвязывающую,
- эффекторную (вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента).
Антитела синтезируются плазматическими клетками, которыми становятся некоторые В-лимфоциты, в ответ на присутствие антигенов. Для каждого антигена формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела распознают антигены, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена.
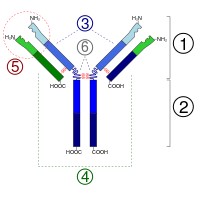
Общий план строения иммуноглобулинов: 1) Fab; 2) Fc; 3) тяжёлая цепь; 4) лёгкая цепь; 5) антиген-связывающийся участок; 6) шарнирный участок
Антитела являются относительно крупными (~150 кДа — IgG) гликопротеинами, имеющими сложное строение. Состоят:
- из двух идентичных тяжёлых цепей (H-цепи, в свою очередь состоящие из VH, CН1, шарнира, CH2- и CH3-доменов),
- из двух идентичных лёгких цепей (L-цепей, состоящих из VL- и CL- доменов).
К тяжёлым цепям ковалентно присоединены олигосахариды. При помощи протеазы папаина антитела можно расщепить на два Fab (англ. fragment antigen binding — антигенсвязывающий фрагмент) и один Fc (англ. fragment crystallizable — фрагмент, способный к кристаллизации). В зависимости от класса и исполняемых функций антитела могут существовать как в мономерной форме (IgG, IgD, IgE, сывороточный IgA), так и в олигомерной форме (димер-секреторный IgA, пентамер — IgM). Всего различают пять типов тяжёлых цепей (α-, γ-, δ-, ε- и μ-цепи) и два типа лёгких цепей (κ-цепь и λ-цепь).

зложена на разныеЧеловеческий иммунитет – это сложная многоступенчатая система защиты организма от вредоносного воздействия извне (вирусов, бактерий, аллергенов, грибков). Не существует одного органа, который бы отвечал за иммунную защиту. Эта функция возложена на разные органы иммунной системы: начиная с лимфатических узлов до кишечника и заканчивая белковыми веществами – иммуноглобулинами.
Общая характеристика иммуноглобулинов
Иммуноглобулины (Ig), или антитела, представляют собой гликопротеины, имеющие в своем составе центры специфического нековалентного связывания антигена, основанного на принципе комплементарности. Существуют растворимые формы иммуноглобулинов, которые и называют антителами, и мембранные формы иммуноглобулинов, составляющие основу В-клеточных рецепторов на поверхности В-лимфоцитов. Иммуноглобулины содержатся в крови и в некоторых секреторных жидкостях и вырабатываются как ответ на контакт с антигенами, например, бактериями или вирусами. Иногда иммуноглобулины продуцируются после контакта с собственными тканями организма, называемыми аутоантигенами.
Дефицит или избыток антител может быть признаком различных патологий, поэтому определение их количества в крови является важной частью при диагностике многих заболеваний. Кроме того, современные достижения в биомедицине позволяют использовать синтетические антитела в лечении некоторых заболеваний.
Структура антител
Иммуноглобулины – это симметричные Y-образные молекулы, состоящие из двух тяжелых длинных (Н) и двух коротких легких (L). цепей, которые соединены друг с другом либо дисульфидными (SS), либо водородными связями. Каждая молекула иммуноглобулина содержит не менее двух идентичных Н-цепей. Тяжелые цепи иммуноглобулинов разных классов состоят из четырех или пяти доменов и обозначаются буквами греческого алфавита соответственно латинской аббревиатуре класса. Принадлежность антитела к конкретному классу и подклассу называют изотипом, который обозначается по типу тяжелой цепи.
Легкие цепи построены из двух доменов. В их составе обязательно находится два вида доменов – вариабельный (V – variable) и константный (С-coпstaпt). Иммуноглобулины, продуцируемые разными клонами плазматических клеток, имеют разные по аминокислотной последовательности вариабельные домены. Константные домены сходны или очень близки для каждого изотипа иммуноглобулина. Вариабельные домены являются N-концевыми. В составе легкой цепи N-концевой домен является вариабельным (VL), С-концевой домен – константным (CL). Тяжелые цепи имеют один вариабельный (N-концевой) домен (Vн) и несколько константных доменов. Легкие и тяжелые цепи иммуноглобулинов гликозилированы.
Иными словами, каждое антитело подходит к антигену по принципу ключа и замка, а при соединении образуют иммунные комплексы. Но также антитела способны проявлять гибкость чужеродных агентов, благодаря чему с легкостью адаптироваться к различным антигенам. Однако эта способность иммуноглобулинов иногда провоцирует у человека перекрестные аллергические реакции – когда иммунитет человека с аллергией не может различать аллергены. Например, человек с аллергией на цветочную пыльцу вследствие “ошибки” иммуноглобулинов может также реагировать на сырые фрукты и овощи.
Разновидности иммуноглобулинов

В человеческом организме иммуноглобулины представлены в двух формах:
- растворимые (продуцируются плазматическими клетками);
- связанные с наружной мембраной B-лимфоцитов, они же – рецепторные антитела.
Кроме основных классов иммуноглобулинов существует несколько подклассов. Разница между ними основана на незначительных отличиях в типе тяжелых цепей каждого класса. В человеческом организме встречаются 4 подкласса антител. Нумерация соответствует порядку уменьшения их концентрации в сыворотке. Так, антитела IgG и IgA дополнительно группируют на подклассы IgG1, IgG2, IgG3, IgG4, а также IgA1 и IgA2.
Большинство антител (IgG, IgD, IgE) в организме представлены в форме мономера (одной молекулы). Исключение составляет антитела класса А, которые также встречается в форме димера, и IgМ, образующий форму снежинки (пентамер).
Характеристика разных классов иммуноглобулинов
Класс IgA
Около 15% антител, содержащихся в организме здорового человека, это иммуноглобулины класса IgA, которые разделяются на два подкласса IgA – IgA1 и IgA2. Они различаются молекулярной массой тяжелых цепей и концентрацией в сыворотке, где IgA представлен в основном как мономер, с молекулярной массой 160 кДа. В секреторных жидкостях иммуноглобулины присутствуют в виде димера, образованных двумя мономерами, их содержание составляет 10-15% от общего количества сывороточных иммуноглобулинов. Димерные иммуноглобулины присутствуют в большинстве секреторных жидкостей, включая слизистые оболочки дыхательных и мочеполовых путей, ЖКТ, а также слюну, слезы, молозиво и молоко у женщин. Поскольку IgA присутствует на слизистых оболочках пищеварительной системы, где он может подвергаться воздействию ферментов, в его составе есть специальный компонент, который защищает молекулу от преждевременного разрушения.
Основная функция иммуноглобулинов этого класса состоит не в разрушении антигенов, а в предотвращении проникновения инфекционных агентов в систему кровообращения. Сами по себе IgA не способны самостоятельно разрушать бактерии, поэтому они всегда работают вместе с лизоцимами – ферментами, которые также присутствуют в секреторных жидкостях и могут разрушать бактерии.
Нарушения концентрации иммуноглобулинов класса IgA в организме способствуют его восприимчивости к инфекционным заболеваниям дыхательных путей и мочеполовой системы, в том числе нефропатии. Лица, с недостаточностью IgA, более склонны к аутоиммунным расстройствам, таким как ревматоидный артрит, волчанка, аллергия и астма.
К снижению содержания IgA могут привести разные заболевания, среди которых – гонорея. Бактерии, вызывающие гонорею, продуцируют фермент, который расщепляет IgA на две части: Fc и Fab фрагменты. Что интересно, Fab все еще может находить опасные для организма бактерии, но без взаимодействия с Fc он не способен противостоять им.
Класс IgD

Иммуноглобулины класса D в организме человека представлены в очень маленьком количестве и составляют примерно 0,2% от всех антител. Известно, что IgD прикрепляется к поверхности некоторых В-лимфоцитов как рецептор В-клеток. Тем не менее его функции в человеческом организме на сегодня до конца еще не изучены. Предполагается, что именно IgD является причиной аллергии на пенициллин, а также он может участвовать в запуске аутоиммунных реакций.
Класс IgE
Иммуноглобулин IgE в норме составляет не более 0.1% от общего количества сывороточных иммуноглобулинов. Более 90% синтезируемого плазматическими клетками IgE секретируется в слизистых экзосекретах желудочно-кишечного тракта. Биологическая функция заключается в защите от внеклеточных паразитов, хотя она полностью не выяснена, и резкое увеличение количества IgE является патогенетическим признаком при аллергических реакциях.
Иммуноглобулины этой группы связываются с поверхностью базофилов и тучных клеток. Дальше к ним присоединяется антиген, что в свою очередь ведет к выбросу в кровоток вазоактивных аминов и развитию IgE-зависимой аллергической реакции по следующему механизму.
Различные антигены, такие как пыльца, ядовитые вещества, споры грибов, пылевые клещи или перхоть домашних животных связываются с IgE и запускают высвобождение гепарина, гистамина, протеолитических ферментов, лейкотриенов и цитокинов. Это ведет к расширению сосудов и повышению их проницаемости, что способствует проникновению чужеродных агентов в капилляры, а затем и в ближайшие ткани, вследствие чего развиваются характерные для аллергической реакции симптомы. Однако, большинство типичных аллергических реакций в виде чихания, кашля, слезотечения и повышенного выделения слизи способствует выведению из организма оставшихся аллергенов.
Исследования показали, что такие расстройства, как астма, ринит, экзема, крапивница и дерматит вызывают повышение уровня IgE. Антитела Е-типа также активно продуцируются в ответ на присутствие в организме гельминтов, персистирующих инфекций (герпесвирусы, атипичные микроорганизмы) и некоторых членистоногих (например, вшей). Кроме того, IgE играет косвенную роль в иммунном ответе, стимулируя другие иммунные компоненты. Также он может защищать поверхности слизистых оболочек, вызывая, в случае опасности, воспалительные реакции.
Патологически низкий уровень антител класса IgE может возникать на фоне редкого генетического заболевания, сопровождающегося нарушением координации мышц (атаксия телеангиэктазия).
Класс IgG

Иммуноглобулины класса G являются доминирующими в человеческом организме. На их долю приходится 75% всех антител. Частично это связано с длительным периодом полураспада: от 7 до 23 дней (зависимо от подкласса). Кроме того, они могут сохраняться в крови в течение нескольких десятков лет после контакта с антигеном.
Существуют 4 подкласса IgG:
IgG играет ключевую роль в гуморальном иммунном ответе. Это основной иммуноглобулин, содержащийся в крови, а также в лимфатической, спинномозговой и брюшной жидкостях. Способность оставаться в организме в течение длительного времени делает его наиболее полезным антителом для пассивной иммунизации. Это единственное антитело, способное проникать через плаценту матери и попадать в кровообращение плода, обеспечивая послеродовую защиту новорожденного в течение первых месяцев его жизни.
Главные функции IgG:
- усиление фагоцитоза в макрофагах и нейтрофилах;
- нейтрализация токсинов;
- инактивация вирусов;
- уничтожение бактерий.
Класс IgM
IgM – это самый важный представитель семейства человеческих иммуноглобулинов, хотя он и отличается весьма коротким периодом полураспада – около 5 дней.
Иммуноглобулины класса IgM в общей доле сывороточных антител в человеческом организме составляют примерно 10-13%. Они участвуют в первичных иммунных реакциях и обладает выраженной антибактериальной активностью, способностью связывать комплемент, не проникают через плацентарный барьер. Первыми синтезируются в ответ на антигенную стимуляцию организма. Наиболее ранние антитела относятся к иммуноглобулинам класса М, что нередко используется в диагностике инфекционных заболеваний. Они же первыми появляются в процессе онтогенеза и филогенеза.
Повышение уровня IgM можно расценивать как признак недавно перенесенной инфекции или присутствия в организме антигена. На мембране В-лимфоцитов присутствует мономерная форма IgM, выполняющая функцию основной составляющей В-клеточного рецептора.
Роль иммуноглобулинов в организме

Антитела являются частью гуморального иммунного ответа и действуют очень специфично, так как всегда направлены против определенного антигена.
Задача любого антитела в организме человека – участвовать в иммунных реакциях. Иммуноглобулины обладают способностью образовывать иммунные комплексы с молекулами антигена, активировать систему комплемента (комплекс белков, содержащихся в крови, необходимых для защиты организма от чужеродных агентов) и вызывать воспаления. Все эти действия направлены на нейтрализацию антигена и безопасное удаление его из организма.
Вследствие различных структурных свойств разные классы антител могут выполнять специализированные функции:
- нейтрализовать паразитов (IgE);
- нейтрализовать микроорганизмы (IgM, IgG);
- защищать от повторных заболеваний, таких как эпидемический паротит (IgG);
- защищать слизистые оболочки (IgA);
- участвовать в синтезе лимфоцитов (IgD);
- защищать плод (IgG) и новорожденного малыша (IgA).
Антитела и иммунологическая память
Иммунный ответ делится на первичный и вторичный. Первичный ответ проявляется во время первого контакта с антигеном, после чего организм сначала вырабатывает иммуноглобулины класса IgM, которые затем замещаются более специфическими и стабильными антителами IgG.
Вторичный иммунный ответ возникает при повторном контакте с тем же антигеном. Он интенсивнее первичного, концентрация антител достигает более высоких уровней, чем в первый раз.
Такой эффект обусловлен иммунологической памятью, которая опосредована В-имфоцитами. Это долгоживущие клетки которые вступают в контакт с антигеном, начинают очень интенсивно делиться и продуцировать специфические антитела.
Как определяется количество антител
Антитела составляют от 12% до 18% сывороточных белков. Количества отдельных белковых фракций, в лабораторных условиях определяется на основании протеинограмм.

Тест на антитела методом иммуноферментного анализа (ИФА), как правило, проводится с венозной кровью (позволяет определить количество иммуноглобулинов класса IgM, IgG, IgE, IgA). Кроме того, определить количество антитела класса IgA можно путем биохимического исследования слюны или кала человека – методом полимеразной цепной реакции (ПЦР). В отдельных ситуациях тест может быть проведен с использованием другого материала, например спинномозговой жидкости.
Если в крови пациента диагностировано критическое повышение некоторых иммуноглобулинов, говорят о гипергаммаглобулинемии. Как правило, у таких пациентов чрезмерно повышаются антитела класса IgM, при этом остальные остаются в дефиците.
На фоне патологического повышения некоторых антител могут развиваться разные заболевания, в том числе:
- острые и хронические воспаления;
- паразитарные, бактериальные, вирусные или грибковые заболевания;
- аутоиммунные болезни;
- цирроз печени;
- саркоидоз; .
Патологически низкое количество антител в сыворотке может возникать на фоне:
- врожденных генетически расстройств;
- приема некоторых противомалярийных, цитостатических, глюкокортикоидных препаратов;
- недоедания;
- инфекции, в том числе ВИЧ;
- онкологических заболеваний;
- нефротического синдрома;
- обширных ожогов;
- тяжелой диареи.
Иммуноглобулины и вакцинация
Антитела играют ключевую роль в развитии иммунитета после вакцинации. В результате контакта с антигеном, содержащимся в вакцине, иммунная система вырабатывает антитела. Сначала менее стойкий и специфический IgM, а затем более стойкий IgG. Например, во время вакцинации против вируса гепатита В, вакцину вводят трижды с определенным интервалом между прививками. Это позволяет создать стойкий иммунитет к болезни. Эффективность такой вакцинации определяется изменением в организме количества антител IgG.
Антитела в медицине
Благодаря развитию биохимии, молекулярной биологии и медицины, в наше время стало возможным синтезировать иммуноглобулины в лабораторных условиях (как правило, антитела класса IgG). Такие антитела называются моноклональными, так как они происходят из клона одной клетки и работают против определенного антигена.
Сегодня моноклональные иммуноглобулины используют для лечения разных заболеваний. Впервые эта методика была применена в 1981 году для лечения лимфомы. А уже в 1984 году изобретатели моноклональных антигенов – немецкий биолог Георг Келер и британский иммунолог Сезар Мильштейн – получили Нобелевскую премию.
В современной медицине моноклональные антитела применяют для:
- уничтожения раковых клеток;
- ингибирования отдельных клеток иммунной системы после трансплантации органов (позволяет предотвратить отторжение пересаженного органа);
- подавления иммунных реакций при аутоиммунных заболеваниях.
Иммунный ответ на каждый отдельный антиген включает продукцию множества молекул антител, синтезируемых разными плазматическими клетками, и имеющих разное строение активного центра и изотип. Вследствие различий в строении активных центров образующиеся антитела имеют различную специфичность и аффинность.
Специальность: врач педиатр, инфекционист, аллерголог-иммунолог .

Антитела (иммуноглобулины, ИГ, Ig) – это особый класс гликопротеинов (т.е. белков с присоединенных к ним углеводными остатками), присутствующих в сыворотке крови, тканевой жидкости или на клеточной мембране, которые распознают и связывают антигены. Иммуноглобулины синтезируются В-лимфоцитами (плазматическими клетками) в ответ на вещества определенной структуры – антигены. Антитела используются иммунной системой для идентификации и нейтрализации чужеродных и нежелательных эндогенных объектов – например, бактерий и вирусов, опухолевых клеток и др. Они являются важнейшим фактором специфического гуморального иммунитета. Антитела выполняют две функции: антиген-связывающую и эффекторную (вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента).
Антитела синтезируются плазматическими клетками, которыми становятся В-лимфоциты в ответ на присутствие антигенов. Для каждого антигена формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела распознают антигены, связываясь с определённым эпитопом – характерным фрагментом антигена.
Антитела являются относительно крупными (~150 кДа для IgG) гликопротеинами, имеющими сложное строение. Антитела состоят из двух идентичных тяжелых цепей и из двух идентичных лёгких цепей, т.е.
фрагментов с меньшим и большим молекулярным весом (рис. 3). К тяжелым цепям ковалентно присоединены олигосахариды. При помощи протеазы папаина антитела можно расщепить на два Fab (англ. fragment antigen binding – антиген-связывающий фрагмент) и один Fc (англ. fragment crystallizable – фрагмент, способный к кристаллизации). Fab фрагменты называются также вариабельной областью антител, т.к. именно их строение определяет связывающую функцию Ат и варьируется в зависимости от структуры антигена. Fc фрагмент называется константной областью Ат, т.к. у особей данного вида для всех молекул Ат этот фрагмент является идентичным.


Рис. 5. Структура антител
В зависимости от выполняемых функций антитела могут существовать как в различных формах (классы иммуноглобулинов): мономерной (IgG, IgD, IgE, сывороточный IgA) или в олигомерной форме (димер-секреторный IgA, пентамер – IgM). Схематичное строение
Иммуноглобулины класса G (IgG) – основной иммуноглобулин сыворотки здорового человека, составляет 70–75 % всей фракции иммуноглобулинов. IgG наиболее активны во вторичном иммунном ответе и антитоксическом иммунитете. Являются единственной фракцией иммуноглобулинов, способной к транспорту через плацентарный барьер и тем самым обеспечивают иммунитет плода и новорожденного. IgG являются самыми небольшими молекулами по сравнению с другими классами Ig (молекулярная масса М = 146 кДа).
Иммуноглобулины класса А (IgA) содержатся в сыворотке (15–20 %
всей фракции Ig), в секреторном компоненте: слюне, слезах, молозиве, молоке, отделяемом слизистой оболочки мочеполовой
и респираторной системы. IgA представлены в виде мономеров (80 % в сыворотке), димеров (в секрете), и тримеров. Средняя молекулярная масса IgA М = 500 кДа.
Иммуноглобулины класса М (IgM) являются пентамерами IgG и составляют до 10 % фракции иммуноглобулинов. Появляются IgM при первичном иммунном ответе B-лимфоцитами на неизвестный антиген. IgM встроены в плазматическую мембрану B-лимфоцитов и выполняют роль антиген распознающего рецептора. Средняя молекулярная масса IgМ М = 970 кДа.
Иммуноглобулины класса D (IgD) представлены в виде мономеров и содержатся в основном на мембране некоторых В-лимфоцитов, а также в небольшом количестве в плазме (
Начало применения препаратов из крови человека для профилактики и лечения инфекционных болезней относится к 1910 г., когда исследователи из Института Пастера во Франции M. Nicolle и E. Consei предложили для предупреждения тифа у детей использовать сыворотку крови реконвалесцентов [1], а в 1918 г. M. Nicolle и E. Consei, а также D.L. Richardson и H. Connor независимо друг от друга успешно применили сыворотку детей, выздоровевших после перенесенной кори, для профилактики этого заболевания [2]. В СССР это направление профилактики было начато в 1925 г. [3]. Гомологичные сыворотки обладали профилактической эффективностью в отношении ряда инфекционных заболеваний, однако было много проблем с их производством и применением. Себестоимость получаемой сыворотки была высокой, в то же время пациентам требовалось введение больших доз препарата. Так, например, для профилактики кори необходимо было вводить детям в возрасте до 2 лет от 15 до 40 мл сыворотки, процедура была болезненной и небезопасной из-за высокой вероятности развития абсцессов в месте введения [4]. Практическому здравоохранению требовались более дешевые, безопасные и эффективные иммунобиологические лекарственные препараты.
В СССР в 1948 г. исследователями Московского института эпидемиологии и бактериологии Н.В. Холчевым и Л.И. Колесниковой метод получения гамма-глобулина из сыворотки, разработанный Коном и сотрудниками, был доработан, вместо центрифугирования осадка предложен метод фильтрации [6]. Методика была принята к использованию для производства гамма-глобулина с целью профилактики кори [7]. Препарат, содержащий не менее 18% белка, для предупреждения кори вводился внутримышечно в объеме 3,0 мл (соответствовало 60 мл проти-вокоревой сыворотки) [8].
В 1952 г. военный врач O. Вruton (США) успешно использовал фракцию гамма-глобулина человека, полученную Коном и сотрудниками [9], в форме внутримышечной инъекции для профилактики хронических болезней легких и других бактериальных инфекций у детей с крайне низким содержанием иммуноглобулинов, выявленным методом электрофореза образцов крови [10]. В 1952–1953 гг. гамма-глобулин был внесен в медицинские стандарты США [11]. Таким образом, было положено начало широкого применения препаратов иммуноглобулина человека нормального (ИГЧН) в заместительной терапии первичных и некоторых вторичных иммунодефицитов (отсутствия или снижения уровня выработки антител), а также иммуномодулирующей терапии. В середине ХХ в. гамма-глобулин активно применяли для профилактики кори, краснухи, ветряной оспы, полиомиелита, эпидемического паротита и инфекционного гепатита [12–15].
Менее токсичное подкожное введение препаратов ИГЧН практиковалось реже, т.к. этот способ введения препарата был ограничен по объему (как правило, не более 5 мл за одну инъекцию), что не позволяло использовать его в качестве средства для иммунозаместительной терапии [19].
В отчете экспертного комитета по применению иммуноглобулина при ВОЗ [16] отмечено, что начиная с 1945 г., когда гамма-глобулин начали применять для профилактики кори и инфекционного гепатита, сфера его применения значительно расширилась и получила развитие в двух направлениях: профилактика некоторых вирусных болезней (корь, инфекционный гепатит и краснуха); лечение синдромов дефицита антител для предотвращения рекуррентных бактериальных инфекций. Тем не менее в отчете было указано, что нормативная база, регламентирующая применение гамма-глобулина, должна быть пересмотрена, т.к. развитие и широкое применение безопасных и эффективных вакцин снижает необходимость пассивной иммунизации и, соответственно, применения гамма-глобулина.
Авторы отчета на основании результатов многочисленных клинических данных (в т.ч. с участием воинских контингентов в различных странах) признали, что ИГЧН не эффективен для профилактики и лечения гриппа и других респираторных вирусных инфекций.
Согласно современным требованиям ВОЗ, опыту практического применения препаратов, внутримышечное введение ИГЧН ограничено коротким перечнем показаний: профилактика гепатита А, а также некоторых специфических инфекций (например, кори) [20, 21]. Показана эффективность таких препаратов для предупреждения бактериальных инфекций у детей с наследственной агаммаглобулинемией [22].
В инструкциях по применению отечественных препаратов указаны следующие показания: профилактика гепатита А, профилактика кори, профилактика и лечение гриппа, профилактика коклюша, профилактика менингококковой инфекции, профилактика полиомиелита, лечение гипо- и агаммаглобулинемии у детей, повышение резистентности организма в периоде реконвалесценции острых инфекционных заболеваний с затяжным течением и при хронических пневмониях. При этом перечень показаний в инструкциях по применению различных препаратов значительно различается и требует пересмотра. Результаты многочисленных клинических исследований подтвердили неэффективность применения иммуноглобулина для профилактики и лечения гриппа [24], а также внутримышечного введения препаратов для заместительной терапии и иммуномодуляции [21].
В тексте документа указано противопоказание к применению ИГЧН – дефицит IgA, т.к. терапия иммуноглобулином может вызывать индукцию антител против IgA и как следствие – нежелательную реакцию. Тем не менее применение иммуноглобулина может быть целесообразным под наблюдением специалиста в случае комбинированного дефицита IgA-IgG2, если препарат содержит низкий уровень IgA.
В последние годы выпускаются препараты ИГЧН для внутривенного введения с высокой чистотой, полной активностью Fc-фрагмента, высокой степенью вирусной безопасности, достигаемой многоступенчатым процессом производства. В то же время следует констатировать, что пока не разработаны технологические приемы, позволяющие гарантировать вирусную безопасность крови на 100%. Достигнута только максимальная степень вирусной безопасности [22, 29].
Терапевтическая эффективность иммуноглобулинов для внутривенного введения при отдельной патологии по мере накопления опыта их применения периодически переоценивается. Использование стандартных иммуноглобулинов для внутривенного введения, по данным многоцентрового исследования, не снижало смертности у кардиохирургических больных с тяжелой послеоперационной системной воспалительной реакцией, считавшейся показанием к их применению. Многолетняя клиническая практика показала, что только введение препаратов, обогащенных иммуноглобулинами классов M и A, повышает выживаемость пациентов при лечении сепсиса [22].
Современные технологии получения препаратов иммуноглобулина с высокой степенью очистки позволили за последнее десятилетие вернуться к практике их подкожного введения. Применение иммуноглобулина в виде подкожных инфузий было обсуждено в рекомендациях ВОЗ в 2007 г. [33]. Данный способ введения ИГЧН эксперты ВОЗ рекомендовали при лечении первичных иммунодефицитов. На основании многолетней практики применения подкожного введения ИГЧН практикующие врачи и международные органы контроля Европейского союза в нормативных документах [20, 34, 35] указывают, что подкожное введение предпочтительно, т.к. может проводиться в домашних условиях, позволяет поддерживать постоянный уровень IgG в сыворотке (в отличие от снижения концентрации IgG при внутривенном введении), уменьшает вероятность возникновения нежелательных реакций и переноса трансмиссивных инфекционных агентов. Такой способ введения значительно комфортнее для пациентов, зачастую подходит даже пациентам, у которых были ранее отмечены нежелательные реакции при внутривенном введении иммуноглобулинов, и позволяет врачам и пациентам проводить заместительную терапию без премедикации кортикостероидами или антигистаминными препаратами. Кроме того, подкожное применение иммуноглобулина комфортно как для детей и взрослых, так и для пожилых пациентов и, что немаловажно, значительно снижает стоимость лечения. Продолжительность инфузии при подкожном введении препаратов иммуноглобулина ограничивается одним часом или менее, в то время как внутривенные инфузии продолжаются в течение нескольких часов. В настоящее время ИГЧН для подкожного введения в основном используются для лечения пациентов с низким уровнем IgA, с положительными серологическими воспалительными маркерами, флебитами, заболеваниями почек и другой патологией, создающей условия для осложнения при внутривенном введении иммуноглобулинов [36]. Целью заместительной терапии служит снижение частоты и тяжести бактериальных инфекций, предотвращение развития необратимых и тяжелых осложнений, а также жизнеугрожающих инфекций, что возможно при достижении близких к нормальным претрансфузионных уровней IgG [37].
Спрос на препараты иммуноглобулина человека растет по мере появления новых показаний. Так, на Европейском конгрессе иммунологов (Германия, 2014 г) было отмечено, что 42% мирового потребления ИГЧН связано с неврологическими показаниями, 18% – с гематоонкологическими болезнями [38, 40]. В 33% случаев препараты ИГЧН применяются не по показаниям. В настоящее время проводятся многочисленные клинические исследования по применению ИГЧН для лечения дерматомиозитов/полимиозитов, хронического идиопатического и комплексного регионального болевого синдрома, тяжелой диабетической полинейропатии, глиобластомы, нейробластомы, аутоиммунной вегетативной ганглиопатии, аутоиммунных нейропсихиатрических нарушений у детей, ассоциированных со стрептококковой инфекцией, ВИЧ-ассоциированной миелопатии, анемии, вызванной парвовирусом B19 и/или кардиомиопатией, спинально-церебеллярной атаксии типа 3, острого ишемического инсульта, миастении гравис, синдромаЛамберта–Итона, токсического эпидермального некролиза, системной красной волчанки и волчаночного нефрита, идиопатической острой и рефрактерной солнечной крапивницы, при трансплантации органов, для предотвращения опосредованного антителами отторжения трансплантированного органа, септического шока, беременных женщин с первичной цитомегаловирусной инфекцией, привычных выкидышей, для удаления антигенов лейкоцитов человека [38].
Согласно действующим нормативным документам Минздрава России и Роспотребнадзора (приказы об утверждении стандартов оказания медицинской помощи различного уровня, санитарно-эпидемиологические правила и методические указания по профилактике отдельных инфекционных болезней), препараты ИГЧН без указания способа введения рекомендовано применять детям и взрослым для профилактики вирусных гепатитов В, дельта, ни А, ни В с парентеральным механизмом передачи возбудителя, профилактики и лечения гриппа и острых респираторных заболеваний, профилактики и лечения эпидемического паротита; детям – для лечения ветряной оспы, инфекционного мононуклеоза, цитомегаловирусной инфекции, геморрагической лихорадки с почечным синдромом, генерализованной формы менингококковой инфекции, шигеллеза, сальмонеллеза, острых кишечных инфекций и пищевых отравлений, псевдотуберкулеза, иерсиниоза, кампилобактериоза, хронических панкреатитов, гастроэнтеритов вирусной этиологии, хронического активного гепатита (аутоиммунного), цирроза печени, болезни Крона, язвенного (хронического) илеоколита (неспецифического язвенного колита), эпилепсии, тяжелой миастении, осложненной кризом, вирусного энцефалита, миелита, острого рассеянного энцефаломиелита, юношеского артрита с системным началом; взрослым – для лечения полиневропатии с системными поражениями соединительной ткани, узелкового полиартрита и родственных состояний, других некротизирующих васкулопатий и других системных поражений соединительной ткани, при системном склерозе, абсцессе, фурункуле, карбункуле кожи, при искусственном прерывании беременности, при гипертензии со значительной протеинурией, вызванной беременностью, больным с неуточненными эффектами излучения, острым промиелоцитарным лейкозом, наследственным дефицитом фактора VIII, наследственным дефицитом фактора IX, отдельными нарушениями, вовлекающими иммунный механизм.
Читайте также:

