Действие генов в эмбриогенезе кратко
Обновлено: 30.06.2024
В результате делений дробления создаются условия для возникновения различий между частями зародыша - дифференцировки. Клетки, образовавшиеся из разных участков яйца, получают неодинаковую цитоплазму (что определяет первичную дифференцировку) и становятся способными к передвижениям, обеспечивающим формирование органов будущего организма.
После действия ряда факторов они постепенно детерминируются, т. е. приобретают способность развиваться в одном, определённом направлении. По мере развития клетки всё более дифференцируются, специализируются их строение и функция. Так, напр., в части эктодермы, образующей зачаток нервной системы, обособляется головной мозг, часть его развивается в зачатки глаз, в к-рых выделяется сетчатка, а в ней дифференцируются палочковые и колбочковые зрительные клетки, имеющие характерные узкоспециализированные строение и функцию. 3. р. определяется наследственным аппаратом клетки, заключённым в ядре. Содержащиеся в ядре хромосомы состоят из мн. генов, каждый из к-рых несёт информацию о строении одного из белков. Признаки родительского организма, закодированные в генах, реализуются в ходе 3. р. Клетки при делениях получают полный набор генов, но в каждой ткани функционирует только часть генов, обеспечивая синтез белков, свойственных данной ткани.
Поэтому на генетич. уровне процесс 3. р. заключается во "включении" отдельных генов, в результате чего синтезируется соответств. рибонуклеиновая к-та (РНК), передающая наследств. информацию из ядра в цитоплазму, где синтезируется молекула специфич. белка, функция генов начинается ещё в предзародышевом развитии, когда в растущей яйцеклетке происходит активное накопление желтка и всех видов РНК, необходимых для обеспечения синтеза белков в раннем развитии. В ходе 3. р. в разных зачатках на тех или иных стадиях развития включаются разные гены, определяющие синтез белков, необходимых для каждого вида дифференцировок. Т. о., реализация наследственности в ходе 3. р. состоит в том, что факторы дифференцировки определяют включение специфич. генов, те вызывают синтез соответств. белков, а белки обеспечивают диффе-ренцировку клеток. Роль мн. белков в этом процессе уже известна - гемоглобин синтезируется при дифференцировке эритроцитов, миозин - при образовании мышц, ферменты и гормоны - при развитии желез и т. д. Однако ещё не изучены белки, определяющие изменения формы клеток, их движение и поведение в ходе 3. р. Неизвестны также механизмы, благодаря к-рым факторы дифференцировки приводят к включению специфич. генов.
Амплификация (amplification) - Процесс образования дополнительных копий участков хромосомной ДНК, как правило, содержащих определенные гены либо сегменты структурного гетерохроматина. Амплификация может быть ответом клеток на селективное воздействие (например, при действии метотрексата). Амплификация – один из механизмов активации онкогенов в процессе развития опухоли, например, онкогена N-myc при развитии нейробластомы (наиболее распространенная форма рака плотных тканей у детей). Также амплификация – накопление копий определенной нуклеотидной последовательности во время ПЦР – полимеразной цепной реакции.
В результате возникает хромосома дицентрик, что может привести к ассиметричному распределению ДНК в каждом клеточном делении. Другой механизм был предложен при амплификации KAD в клетках HT1080. В данном случае амплификация возможно начинается с рекомбинации через центромеры сестринских хроматид, обеспечивающей i(2)+i(2q). В каждом случае оба механизма зависят от неравнего распределения генов между дочерними клетками, сопровождающимся событиями рекомбинации. Таким образом, потеря хромосомного материала может быть связана с амплификацией генов, и оба этих явления объясняются одним механизмом.
Еще до оплодотворения, т.е в ооците, начинается экспрессия генов, продукты которых несколько позже принимают участие в формировании различий между передним и задним полюсом оплодотворенного яйца дрозофилы. Это так называемые "материнские" гены. К ним относятся, например, ген caudal (определяет полярность ооцита), ген bicoid (мутация по нему вызывает появление эмбрионов без головы и торакального ганглия), ген oskar (у мутантных эмбрионов нет брюшка).
Уже в самом эмбрионе проявляют свое действие гены других групп.
Больше всего информации получено по генам сегментации и по так называемым гомейозисным генам.
Гены сегментации. Мутации по ним нарушают метамерию, т.е. деление тела зародыша дрозофилы на сегменты, а также вызывают аномалии развития сегментов разных категорий. Могут происходить, например, потеря сегментов (ген gap), появление дефектных по структуре сегментов "через один" (ген pair rule), нарушение внутренней структуры полярности сегмента (engrailed). Совместное действие нормальных аллелей генов этих групп обеспечивает формирование сегментации тела. Мутации генов сегментации несовместимы с нормальным ходом эмбриогенеза и вызывают его остановку с последующей гибелью зародыша на разных стадиях.
Гомейозисные гены. Исторически первыми были описаны и изучены мутации по генам, которые вызывают заметные морфологические аномалии (уродства), но, тем не менее, совместимы с жизнью, т.е. не только не вызывают гибели зародыша, а даже не препятствуют метаморфозу и развитию имаго. Это так называемые гомейозисные мутации, выражающиеся в формировании сегментов с "неправильными" органами. Наиболее известны среди них — мутации aristapedia и antennaepedia, когда вместо аристы или антенны на голове мухи формируется конечность.
Гомеобокс. Молекулярно-биологические исследования гомейозисных мутаций выявили в соответствующих участках ДНК короткую консервативную последовательность оснований, которая была названа гомеодоменом, или гомеобоксом (Нох) (подробнее см.: Дондуа, 1997). Гомеодомен кодирует небольшого размера белковую молекулу, которая может связываться с ДНК. Эти данные позволили предположить, что гомеобокс кодирует регуляторный белок, способный включать и выключать экспрессию генов в определенные моменты развития. Структурные особенности ДНК Hох-доменов подтверждают предположение, что продукты этих генов могут связываться с ДНК и регулировать транскрипцию.
Итак, действие генов ряда групп проявляется либо в оплодотворенном яйце, либо позднее, на разных стадиях формирования самого эмбриона.
Эмбриогенез человека. Зародошевые и стволовые клетки
В ходе развития клетки делятся (размножаются), приобретают новые функции или структуры (дифференцируются), перемещаются в пределах эмбриона (мигрируют) и подвергаются программируемой гибели (часто через апоптоз).
Хотя рост может казаться слишком очевидным, чтобы его обсуждать, он тщательно регулируется в ходе развития, и нерегулируемый рост чреват катастрофическими последствиями. Простое удвоение (один дополнительный цикл деления клетки) количества клеток (гиперплазия) или увеличение их размера (гипертрофия), вероятно, будет фатальным для организма.
Неправильная регуляция роста сегментов тела может вызывать тяжелые уродства и дисфункции, как при гемигиперплазии и других сегментарных нарушениях избыточного роста. Кроме того, тонкое дифференциальное регулирование роста может изменять форму ткани или органа.
Эмбриогенез человека - это описание развития человека начинается с конца главы 2 — оплодотворения. После оплодотворения продукт зачатия подвергается серии клеточных делений без общего роста, называемых дроблениями. Оплодотворенная яйцеклетка подвергается четырем делениям, к 3 дню образуя 16-клеточную морулу.
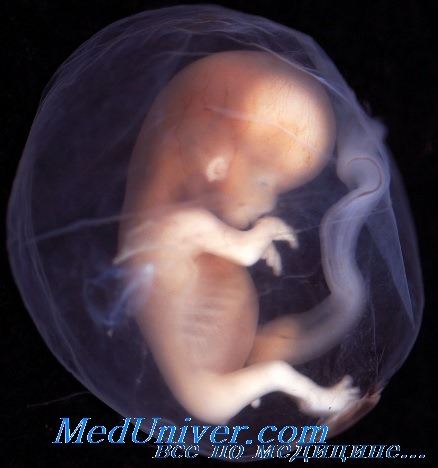
На 4-й день морула переходит в бластоцисту, клетки-предшественницы плаценты формируют стенки, внутри которых клетки, формирующие сам эмбрион, собираются с одной стороны, образуя внутреннюю клеточную массу. Это — та точка, когда продукт зачатия приобретает первое отчетливое проявление полярности, ось асимметрии, отделяющую внутреннюю клеточную массу (в основном формирующую готовый организм) от эмбриональных тканей, формирующих хорион и другие экстраэмбриональные образования (плаценту и т.д.).
Внутренняя клеточная масса затем подразделяется на эпибласт, формирующий собственно эмбрион, и гипобласт, создающий амниотическую мембрану.
Эмбрион имплантируется в эндометрий на 7-12-й день после оплодотворения. После имплантации происходит гаструляция, клетки перестраиваются в структуру, состоящую из трех групп клеток, названных первичными эмбриональными листками: эктодермы, мезодермы и эндодермы.
Три эмбриональных листка формируют разные структуры. Клетки эндодермального происхождения формируют центральную часть органов. Это клетки стенок кишечника, выстилка дыхательных путей и другие аналогичные структуры. Мезодермальное происхождение имеют почки, сердце, сосуды и структурные или опорные ткани организма. Почти исключительно мезодермального происхождения кости и мышцы выполняют две основных функции — структурную (физическая поддержка) и обеспечение необходимой опоры и нутритивной поддержки кроветворной системы. Из эктодермы формируются ЦНС, периферическая нервная система и кожа.
Следующие основные этапы развития — инициация нервной системы, создание основного плана строения тела, и затем органогенез, продолжающийся с 4 по 8 нед гестации. Положение и основные структуры всех органов к этому времени устанавливаются, а клеточные компоненты, необходимые для их полного развития, находятся на своих местах.
Обычно считают, что плодный период развития охватывает с 9 по 40 нед гестации, в это время в первую очередь происходят созревание и дальнейшая дифференцировка органов. Для некоторых систем органов развитие с рождением не прекращается. Например, мозг подвергается значительному развитию после родов, а конечности продолжают эпифизарный рост, заканчивающийся только после наступления половой зрелости.
Зародышевые (герминативные) клетки: передача генетической информации
Помимо роста и дифференцировки соматических тканей, организм также должен определить, какие клетки разовьются в гаметы взрослого организма. Этой цели служит образование половых (герминативных) клеток. Половые клетки коммитируются к последующему гаметогенезу и мейозу для того, чтобы индивидуум мог передавать свои генетические признаки, используя рекомбинацию и произвольное распределение хромосом.
Кроме того, при формировании половых клеток должен восстанавливаться полоспецифический эпигенетический импринтинг, требующийся для некоторых генов.
Стволовые клетки: поддержка регенеративных возможностей в тканях
Кроме программы определения дифференцировки, необходимой для развития, организм должен также установить тканеспецифические стволовые клетки, способные регенерировать различные клетки во взрослой жизни. Эти клетки наилучшим образом изучены в кроветворной системе.
Среди 10 11 -10 12 ядерных кроветворных клеток во взрослом организме — почти 10 4 -10 5 клеток, способных трансформироваться в любую из более специализированных кровяных клеток непрерывно в течение всей жизни. Стволовые кроветворные клетки можно пересадить другим людям и полностью переформировать их кроветворную систему.
Необходимый размер пула стволовых кроветворных клеток поддерживает система взаимодействующих продуктов генов. Эти регуляторы устанавливают баланс между использованием стволовых клеток в самовоспроизводстве и создании клеток-предшественниц, способных к дальнейшему развитию в различные зрелые клетки кроветворной системы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Теория дифференциальной активности генов – в основе развития организмов (при формировании индивида) лежат процессы экспрессии генов Томаса Моргана.
При этом, справедливо предположение о том, что при равнонаследственном делении клеток неэкспрессируемые гены сохраняются.
Дифференциальная активность генов достигается разнообразными путями активации и репрессии генов как прямыми путями – (с помощью транскрибционных факторов) так и опосредованными (путем изменения структуры ДНК и укладки хроматина, а также путем модификации структуры ДНК).
Процессы эмбриогенеза не исчерпываются генетическим уровнем контроля, хотя и основаны на дифференциальной активности генов.
Основы этой теории были сформулированы Томасом Морганом, в начале 1930 гг. Морган полагал, что в разных участках зародыша в ходе эмбрионального развития активизируются разные группы генов.
Далее, в бластомерах этот процесс продолжается, но с учетом того, что в разные бластомеры попадают разные участки зиготы (особенно после ооплазматической сегрегации). То есть в разных бластомерах активируются разные группы генов.
На третьем этапе – продукты деятельности активированных генов видоизменяют цитоплазму, что ведет в свою очередь к включению новых наборов генов и формированию новых свойств цитоплазмы.
В конечном итоге, такой каскад включений новых и новых групп генов приводит к формированию сложно устроенного организма.
В свое время концепция дифференциальной активности генов не сразу была принята современниками (некоторые вообще отвергали и хромосомную теорию наследственности Т.Моргана).
Причина: загадка сама природа гена (1930 гг.), а идея о взаимодействии между генами, о соподчинении и координации их работы вообще казалась нереальной.
Такое представление в эмбриологии было прямым детерминизмом – и опровергалось данными экспериментальной эмбриологии, так как не оставляло места процессам самоорганизации целостной системы развивающегося зародыша.
Достаточно вспомнить данные о существовании регуляционного пути развития и законе Дриша.
Новое рождение идеи дифференциальной активности генов Т.Моргана получили в в середине 20 столетия, когда стало ясно значение генов в жизни клетки и была выяснена функция ДНК.
Развитие молекулярной биологии и генной инженерии создали реальные предпосылки для плодотворного анализа раннего эмбриогенеза, когда происходит становление организменного уровня многоклеточного организма.
Исследования в этой области дали начало новому направлению биологии генетике развития.
Первые достижения молекулярной биологии показали, что в составе генома многих организмов многие тысячи генов.
Так в геноме нематоды Caenorhabdites elegans 19 000 генов, у дрозофилы около 13 000, а геноме человека около 30 000 (по другим данным около 60 000) генов.
Изучение функций генома в процессах размножения, дифференциации и морфогенеза, составляющих основу индивидуального развития организма, показало наличие сложных разветвленных сетей взаимодействующих генов, что показало ограниченность первоначально постулированного в теории дифференциальной активности генов каскадного типа взаимодействия генов.
В генетике представление о сложности взаимодействия между генами было показано давно, когда стали известны факты неоднозначного проявления генотипа.

Молекулярно-генетическое обеспечение плана строения организма
Общая биология.
Лекция
Теория дифференциальной активности генов – в основе развития организмов (при формировании индивида) лежат процессы экспрессии генов Томаса Моргана.
При этом, справедливо предположение о том, что при равнонаследственном делении клеток неэкспрессируемые гены сохраняются.
Дифференциальная активность генов достигается разнообразными путями активации и репрессии генов как прямыми путями – (с помощью транскрибционных факторов) так и опосредованными (путем изменения структуры ДНК и укладки хроматина, а также путем модификации структуры ДНК).
Процессы эмбриогенеза не исчерпываются генетическим уровнем контроля, хотя и основаны на дифференциальной активности генов.
Основы этой теории были сформулированы Томасом Морганом, в начале 1930 гг. Морган полагал, что в разных участках зародыша в ходе эмбрионального развития активизируются разные группы генов.
Далее, в бластомерах этот процесс продолжается, но с учетом того, что в разные бластомеры попадают разные участки зиготы (особенно после ооплазматической сегрегации). То есть в разных бластомерах активируются разные группы генов.
На третьем этапе – продукты деятельности активированных генов видоизменяют цитоплазму, что ведет в свою очередь к включению новых наборов генов и формированию новых свойств цитоплазмы.
В конечном итоге, такой каскад включений новых и новых групп генов приводит к формированию сложно устроенного организма.
В свое время концепция дифференциальной активности генов не сразу была принята современниками (некоторые вообще отвергали и хромосомную теорию наследственности Т.Моргана).
Причина: загадка сама природа гена (1930 гг.), а идея о взаимодействии между генами, о соподчинении и координации их работы вообще казалась нереальной.
Такое представление в эмбриологии было прямым детерминизмом – и опровергалось данными экспериментальной эмбриологии, так как не оставляло места процессам самоорганизации целостной системы развивающегося зародыша.
Достаточно вспомнить данные о существовании регуляционного пути развития и законе Дриша.
Новое рождение идеи дифференциальной активности генов Т.Моргана получили в в середине 20 столетия, когда стало ясно значение генов в жизни клетки и была выяснена функция ДНК.
Развитие молекулярной биологии и генной инженерии создали реальные предпосылки для плодотворного анализа раннего эмбриогенеза, когда происходит становление организменного уровня многоклеточного организма.
Исследования в этой области дали начало новому направлению биологии генетике развития.
Первые достижения молекулярной биологии показали, что в составе генома многих организмов многие тысячи генов.
Так в геноме нематоды Caenorhabdites elegans 19 000 генов, у дрозофилы около 13 000, а геноме человека около 30 000 (по другим данным около 60 000) генов.
Изучение функций генома в процессах размножения, дифференциации и морфогенеза, составляющих основу индивидуального развития организма, показало наличие сложных разветвленных сетей взаимодействующих генов, что показало ограниченность первоначально постулированного в теории дифференциальной активности генов каскадного типа взаимодействия генов.
В генетике представление о сложности взаимодействия между генами было показано давно, когда стали известны факты неоднозначного проявления генотипа.
Дифференцировка– возникновение различий между клетками, тканями, органами. До 7 дня зигота тотипотентна, т.е. из любой её клетки можно вырастить целый организм или орган. После 7 дня тотипотентность теряется из-за дифференцировки.
Все структурные клетки условно делят на 3 типа:
1) гены “домашнего” хозяйства – работающего во всех клетках организма;
2) гены, работающие в специализированных тканях;
3) гены, выполняющие 1-ну узкую функцию. Большинство генов многоклеточного организма работают только на определённых стадиях онтогенеза или в определённых тканях.
Примеры неравномерной работы генов:
1) инактивация “х” хромосомы у самок. Сначала на ранних стадиях эмбриогенеза из 2-х “х” хромосом по принципу случайности, выбирается одна, затем она инактивируется мителированием – её неактивное состояние стабилизируется, т.е. сохраняется в течение всей жизни данного организма. Любой женский организм мозаичный, т.е. 50% отцовских, 50% материнских “х” хромосом. Неравномерная активность отцовских и материнских генов называется геномным иниринтингом.
2) у эукариот зигота до стадии поздней бластулы развивается за счёт информации, содержащееся в информосомах. Гены ядра начинают работать со стадии гаструлы.
3) работа гигантских хромосом в слюнных железах личинок насекомых. На них находятся активные гены.
4) изменение состояния гемоглобина у человека и животных с возрастом.
Опыты экспериментальной эмбриологии. Эмбриональная индукция как процесс взаимодействия между частями развивающегося зародыша. Индукторы и индукционные взаимодействия в эмбриогенезе. Каскадная индукция. Примеры.
Экспериментальная эмбриология занимается изучением развития животных при искусственных условиях.
1) Опыт Вильгельма Ру:
2) Опыт Гертвига:
В 90-х гг. прошлого столетия О. Гертвиг и другие исследователи показали, что при полном разделении двух бластомеров амфибий из каждого развивается целый нормальный зародыш. Впоследствии многие ученые производили опыты по разделению бластомеров на разных этапах дробления у разных видов животных. Результаты оказались тоже разными. У многих беспозвоночных, например, у гребневиков, круглых червей, спирально дробящихся кольчатых червей и моллюсков, а также у ящериц, изолированные бластомеры дают такие же зачатки, какие получаются из них при нормальном развитии. Они как бы обладают способностью к самодифференцировке.
3) Опыты Шпемана:
Г. Шпеман также проводил свои опыты на зародышах амфибий. Один из опытов заключается в следующем: кусочек зародыша из области дорсальной губы бластопора на стадии гаструлы тритона одного вида(гребенчатого) пересаживают на боковую или вентральную сторону гаструлы тритона другого вида(полосатого). В месте пересадки происходит развитие неровной трубки, хорды и других органов. Развитие может достичь довольно продвинутых стадий с образованием дополнительного зародыша на боковой или вентральной стороне зародыша реципиента. Следовательно, участок, взятый из спинной губы бластопора способен индуцировать развитие зародыша как в обычном, так и в нетипичном месте.
Явление, при котором один участок зародыша влияет на развитие другого, назвали эмбриональной индукцией
В роли индукторов могут выступать разнообразные убитые ткани, вытяжки из самых различных тканей беспозвоночных и позвоночных животных, а также растений, несколько классов химических соединений (белки, нуклеопротеины, стероиды и даже неорганические вещества).
Явления индукции многочисленны и многообразны. Индукция может носить каскадный или переплетающийся (сетевой) характер.
Каскадные взаимодействия типичны для дифференцировки, т.к. индукция многих структур зависит от предшествующих индукционных событий.


На всех этих стадиях развития у многоклеточных животных геном обычно не функционирует. На снимках: развитие медузы Aequorea от первого деления зиготы до бластулы (фото с сайта raven.zoology.washington.edu)

Типичная гаструла многоклеточного животного. A — эктодерма (наружный зародышевый листок), B — бластоцель (первичная полость тела), C — первичная кишка, D — энтодерма (внутренний зародышевый листок), E — бластопор (первичный рот). Фото: Dr. Anna E. Ross, Christian Brothers University, TN (с сайта coris.noaa.gov)
Зародыш между тем претерпевает сложные превращения. Яйцеклетка начинает дробиться, число клеток эмбриона растет в геометрической прогрессии: 2, 4, 8, 16, 32. Наконец формируется однослойный шар из клеток (бластула). Клетки, находящиеся на одном из полюсов бластулы, мигрируют внутрь, давая начало второму зародышевому листку (энтодерме), из которой позже разовьется кишечник. На этой стадии двуслойный зародыш называется гаструлой. Только на этом этапе у многих животных начинают наконец включаться гены, унаследованные от папы с мамой. У других это происходит чуть раньше — на стадии бластулы. И только млекопитающие — группа уникальная во многих отношениях — включают свои гены еще раньше (например, мышь делает это на стадии двух клеток).
Ответ на первый вопрос более или менее ясен. Яйцеклетка содержит большое количество матричных РНК, унаследованных от материнского организма. Эти мРНК считываются с материнских генов заблаговременно, в процессе созревания яйцеклетки. Именно они обеспечивают синтез белков, необходимых для ранних стадий онтогенеза. В определенный момент материнские мРНК начинают уничтожаться. Это происходит как раз тогда, когда зародыш начинает сам производить мРНК, то есть включает свои гены. Этот довольно быстрый процесс замены зародышем материнских мРНК на свои собственные называется maternal-zygotic transition (MZT).
Впрочем, ни одна из этих теорий не объясняет всей совокупности имеющихся фактов. Например, они не в состоянии объяснить, почему эмбриональные гены включаются постепенно, в строго определенном порядке, а единичные гены могут быть включены уже на самых ранних стадиях дробления.
Источник: Alexander F. Schier. The Maternal-Zygotic Transition: Death and Birth of RNAs // Science. 2007. V. 316. P. 406–407.
Читайте также:

